Тактика ведения доношенных и недоношенных новорожденных детей с непрямой гипербилирубинемией
Также:
Неонатальная желтуха
Версия: Клинические рекомендации РФ 2013-2017 (Россия)
Категории МКБ:
Неонатальная желтуха вследствие других и неуточненных повреждений клеток печени (P59.2), Неонатальная желтуха неуточненная (P59.9), Неонатальная желтуха, обусловленная другими уточненными причинами (P59.8), Неонатальная желтуха, связанная с преждевременным родоразрешением (P59.0), Синдром сгущения желчи (P59.1)
Разделы медицины:
Неонатология, Педиатрия
Общая информация
Краткое описание
Российское общество неонатологов
Тактика ведения доношенных и недоношенных новорожденных детей с непрямой гипербилирубинемией
2016
Определения.
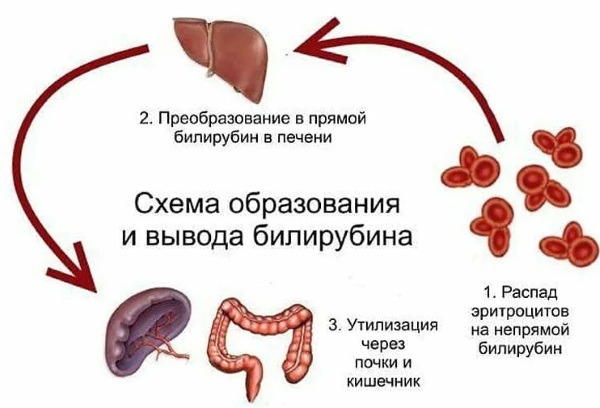
Гипербилирубинеми́я (греч. hyper- + Билирубин + греч. haima кровь). В клинической лабораторной практике под термином гипербилирубинемия понимают любое увеличение концентрации билирубина в сыворотке или плазме крови сверх нормативных значений.
Учитывая существенные отличия нормативных значений билирубина у детей периода новорожденности от других возрастных групп, а также необходимость профилактики и лечения гипербилирубинемии у детей различного гестационного возраста, в неонатологии термином гипербилирубинемия обозначают состояния, при которых у доношенных и поздних недоношенных ГВ 35-36 недель отмечается повышение концентрации общего билирубина в сыворотке крови более 256 мкмоль/л, а у детей, родившихся до 35 недели гестации — повышение концентрации общего билирубина более 171 мкмоль/л (Уровень доказательности – B) [1,2,3].
Международные исследования, проведенные в начале 2000-х годов показали, что 95% перцентиль концентрации общего билирубина в сыворотке крови у доношенных детей в возрасте 96 ± 6,5 часов находился в диапазоне от 265 до 299 мкмоль/л(Уровень доказательности – B) [4,5,6]. Более высокие показатели были характерны для детей, получавших исключительно грудное вскармливание [7]. Однако, с учетом того, что в многоцентровые лабораторные исследования были включены дети, потребовавшие госпитализации для проведения фототерапии, критерии гипербилирубинемии, традиционно принятые в неонатологии, остались неизменными.
Термин «непрямая гипербилирубинемия» используют в тех случаях, когда это повышение обусловлено преимущественно (более чем на 80%) непрямой фракцией билирубина (Уровень доказательности – D) [8].
Желтуха — визуальное проявление повышенного уровня билирубина в крови. У доношенных новорожденных появляется при уровне билирубина более 67 мкмоль/л; у недоношенных — более 120 мкмоль/л (Уровень доказательности – C) [9].
Повышение концентрации билирубина в крови у новорожденных детей и развитие желтухи может быть вызвано как физиологическими, так и патологическими причинами. К раннему появлению, прогрессирующему нарастанию и высокой интенсивности желтухи следует относится как к симптомам потенциально опасного заболевания (Уровень доказательности – D) [8, 10, 11, 12, 13, 14].
Коды по МКБ-10
Р 59 Неонатальная желтуха, обусловленная другими и неуточненными причинами
Р 59.0 Неонатальная желтуха, связанная с преждевременным родоразрешением
Р 59.1 Синдром сгущения желчи
Р 59.2 Неонатальная желтуха, вследствие других и неуточненных повреждений клеток печени
Р 59.8 Неонатальная желтуха, обусловленная другими уточненными причинами
Р 59.9 Неонатальная желтуха неуточненная
Этиология и патогенез
Физиологическая желтуха
Основными физиологическими причинами повышения концентрации билирубина в сыворотке крови у детей в первые дни жизни являются следующие (Уровень доказательности – D) [15, 16,17 ].
— более высокая скорость образования билирубина, обусловленная физиологической полицитемией и более короткой продолжительностью жизни эритроцитов, содержащих фетальный гемоглобин (70–90 дней, по сравнению со 110–120 днями у взрослых);
— функционирующий венозный проток и уменьшенная перфузия крови в пространства Диссе препятствует полноценному захвату билирубина гепатоцитами;
-сниженная активность фермента глюкуронилтрансферазы (ГТФ), обеспечивающей конъюгацию билирубина, и недостаточная концентрация У-протеина, обеспечивающего транспорт билирубина в гепатоцитах;
— исходно низкая экскреторная функция печени (1–2% от экскреторной способности печени взрослого);
— усиленная реабсорбция билирубина из тонкого кишечника вследствие высвобождения билирубина из химической связи с глюкуроновой кислотой под влиянием повышенной активности фермента бета-глюкоронидазы.
Желтуха на первой неделе жизни регистрируется у 60-80% здоровых доношенных новорожденных детей (Уровень доказательности – A) [9, 17, 18].
Для физиологической желтухи характерно:
— Удовлетворительное состояние ребенка
— Нормальные пальпаторные размеры печени и отсутствие признаков увеличения селезенки;
— Отсутствие клинико-лабораторных признаков анемии или полицитемии;
— Появление желтой окраски кожи в возрасте более 24 час жизни (при этом почасовой прирост билирубина в первые сутки составляет менее 3,4 мкмоль/л, суммарно за первые сутки — менее 85,5 мкмоль/л);
— Максимальная выраженность желтой окраски лица, туловища и конечностей на 3-4 сутки жизни; желтуха не распространяется на ладони и стопы;
— Не наблюдается патологических оттенков желтой окраски кожи (серого, зеленоватого, лимонного);
— Нормальная, соответственно возрасту, окраска стула;
— Максимальная концентрация общего билирубина не более 255 мкмоль/л; концентрация прямой фракции билирубина – не выше 34 мкмоль/л;
— Быстрое уменьшение интенсивности и распространенности желтухи после 4 суток жизни; угасание желтухи к 8-10 суткам жизни.
Примерно в половине случаев при физиологическом течении желтухи к 3-4 стукам возникает кратковременная непрямая гипербилирубинемия, которая не имеет негативных клинических последствий и не требует никаких медицинских вмешательств (Уровень доказательности – D) [16 , 19].
Понятие физиологическая желтуха применимо только по отношению к доношенным и «поздним» недоношенным (ГВ 35-36 нед) новорожденным (Уровень доказательности – D) [16].
Непрямая гипербилирубинемия, вызванная патологическими причинами
Несоответствие хотя бы по одному из типичных для физиологической желтухи клинических и лабораторных признаков с высокой вероятностью свидетельствует о том, что нарушение обмена билирубина вызвано патологическими причинами.
Факторы, предрасполагающие к развитию патологической гипербилирубинемии у доношенных новорожденных B:
Восточно-азиатское или средиземноморское происхождение (Уровень доказательности – B) [20, 21, 22]
Несовместимость по АВО- или резус-фактору матери и плода (Уровень доказательности – B) [23, 24, 25, 26, 27, 28]
Использование окситоцина в родах(Уровень доказательности – D) [29]
Желтуха, развившаяся в первые сутки (24 часа) жизни (Уровень доказательности – B) [30, 31, 32, 33]
Кефалогематома/экхимозы, крупные гемангиомы (Уровень доказательности – B) [20, 34, 35, 36]
Гипогалактия при исключительно грудном вскармливании (Уровень доказательности – C) [20, 37, 38, 39]
Нарушенное сосание/недостаточное питание (Уровень доказательности – C) [40]
Эксикоз (патологическая убыль массы тела) (Уровень доказательности – B) [37,41]
Полицитемия (Уровень доказательности – A) (40, 42, 43, 44, 45, 46, 47, 48, 49, 50)
Врожденные и перинатальные инфекции (Уровень доказательности – B) [51, 52, 53, 54]
Дефицит глюкозо-6-фосфат дегидрогеназы (Уровень доказательности – B) ]55 , 56, 57, 58, 59]
Практически всегда гипербилирубинемия у недоношенных детей, родившихся ранее 35 недели гестации, обусловлена нефизиологическими причинами.
В свою очередь, в большинстве случаев патологической гипербилирубинемии, возникающей на первой неделе жизни, отмечается преимущественное повышение в крови непрямой фракции билирубина (Уровень доказательности – C) [60].
По ведущим патогенетическим механизмам все случаи непрямой гипербилирубинемии у новорожденных можно разделить на четыре группы: 1) обусловленные увеличением скорости продукции билирубина, 2) обусловленные замедлением конъюгации билирубина в печени 3) обусловленные повышением реабсорбции билирубина из кишечника 4) обусловленные комбинированным действием вышеперечисленных факторов. Наиболее вероятные причины, приводящие к непрямой патологической гипербилирубинемии у новорожденных детей, с учетом ведущих патогенетических механизмов перечислены в таблице 3 (Уровень доказательности – C) [23, 24, 25, 26, 35, 42, 43, 44, 45, 47, 48, 49, 50, 51, 52, 56, 59, 61, 62, 63, 64, 65, 66, 67, 68] .
Таблица 3. Основные причины непрямой патологической гипербилирубинемии у новорожденных детей
Ведущие патогенетические механизмы развития гипербилирубинемии во многом определяют время возникновения и степень выраженности гипербилирубинемии. Раннее распознавание конкретной причины нарушений билирубинового обмена позволяет не только прогнозировать течение желтухи, но и эффективно предупреждать осложнения, ассоциированные с гипербилирубинемией (Уровень доказательности – C) [32, 37].
Во всех случаях развития непрямой (патологической) гипербилирубинемии, обусловленных гиперпродукцией билирубина, и в части случаев, обусловленных нарушением конъюгации и реабсорбции билирубина, существует риск развития метаболического поражения ЦНС за счет потенциальной нейротоксичности неконъюгированного билирубина (Уровень доказательности – C) [11, 12, 13, 16, 69]
Билирубиновая энцефалопатия (Код по МКБ-10 – Р57)
Нарушение структуры и функции головного мозга, обусловленное непрямой гипербилирубинемией, носит название билирубиновой энцефалопатии (БЭ) или ядерной желтухи. При использовании современных перинатальных технологий БЭ является предотвратимым состоянием (Уровень доказательности – D) [70].
Согласно литературным данным, накопленным в эру, предшествующую внедрению современных протоколов профилактики и лечения патологической гипербилирубинемии, билирубиновая энцефалопатия (БЭ) у доношенных новорожденных развивается в случаях превышения концентрации общего билирубина сыворотки крови порога в 342 мкмоль/л с выраженными индивидуальными различиями концентраций (от 342 до 684 мкмоль/л), при которых происходит метаболическое поражение головного мозга (Уровень доказательности – B) [71, 72, 73, 74].
В последние два деятилетия частота билирубиновой энцефалопатии в различных странах мира находится в диапазоне 0.4/100, 000 до 2.7/100,000 [75] B.
Вероятность развития билирубиновой энцефалопатии при патологической гипербилирубинемии повышается на фоне следующих факторов риска (B):
недоношенность или морфо-функциональная незрелость организма ребенка (Уровень доказательности – B) [ 41, 74, 75, 76, 77]
тяжелая врожденная и неонатальная инфекция (сепсис, менингит) (Уровень доказательности – B) [51, 52, 53, 54]
гемолитическая болезнь новорожденого (Уровень доказательности – B) [23, 24, 25, 25, 26,27 ]
дефицит Г-6-ФДГ (Уровень доказательности – C) [80]
гипоальбуминемия (концентрация сывороточного альбумина менее 25 г/л) (Уровень доказательности – C) [79].
выраженный метаболический ацидоз (pH артериальной крови менее 7,15 более 1 часа) (Уровень доказательности – C) [79]
тяжелая асфиксия новорожденного (оценка по Апгар менее 4 баллов), артериальная гипотензия, апноэ, потребность в ИВЛ (Уровень доказательности – C) [79]
гипотермия (ректальная температура менее 35 (С) (Уровень доказательности – C) [78]
обширная травма мягких тканей в родах, массивные кефалогематомы, перивентрикулярные, внутрижелудочковые и субарахноидальные кровоизлияния (Уровень доказательности – C) [20, 34, 35]
синдром полицитемии (Уровень доказательности – B) [42, 43, 44, 45, 46 , 47, 49, 50, 64]
задержка отхождения мекония (Уровень доказательности – C) [78]
мужской пол (Уровень доказательности – C) [32, 33]
Следует помнить, что ряд препаратов (в первую очередь антибиотиков), используемых в практике врача неонатолога могут вытеснять билирубин из связи с альбумином. Так, коэффициент вытеснения для цефазолина (антибитик, цефалоспорин 1-го поколения) составляет 1.17, для цефметазола (цефалоспорин 2-го поколения) – 2.0 , а для цефтриаксона (цефалоспорин 3-го поколения пролонгированного действия ) – 3.0 (Уровень доказательности – C) [8].
У недоношенных детей вероятность билирубинового поражения ЦНС развивается при более низких концентрациях билирубина, чем у доношенных новорожденных, и зависит от концентрации билирубина в крови и массы тела ребенка при рождении.
У детей, родившихся с очень низкой и экстремально низкой массой тела (ОНМТ и ЭНМТ), БЭ может возникнуть даже после умеренного повышения концентрации общего билирубина в сыворотке крови (в диапазоне 171-255 мкмоль/л) (Уровень доказательности – B) [76,82, 83, 84, 85, 86, 87].
Несмотря на попытки разработки и внедрения лабораторных методов, прогнозирования индивидуальной чувствительности мозга к билирубину, в повседневной неонатологической практике при определении риска развития БЭ ориентируются на минимальные пороговые концентрации билирубина в сыворотке крови, при которых в прошлом регистрировались случаи развития ядерной желтухи. [71 73 75, 76, 82, 83, 85]. В течении билирубиновой энцефалопатии можно условно выделить 4 фазы [85]:
I.Нарастание признаков билирубиновой интоксикации: угнетение безусловно-рефлекторной деятельности – апное, апатия, вялость, сонливость, плохо сосут, может быть монотонный крик, срыгивания, рвота, “блуждающий взгляд”. При неблагоприятном течении гемолитической болезни новорожденного эти признаки в большинстве случаев появлялись на 4 день жизни и, в случаях экстренного проведения ОЗПК, носили обратимый характер (Уровень доказательности – A) [13, 86].
II.Спастическая. При неэффективном лечении появляются классические признаки ядерной желтухи: спастичность, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, “негнущимися” конечностями и сжатыми в кулак кистями; периодическое возбуждение и резкий мозговой крик, выбухание большого родничка, подергивание мышц лица, крупноразмашистый тремор рук, исчезновение рефлекса Моро и видимой реакции на сильный звук, сосательного рефлекса; нистагм, апноэ, брадикардия, летаргия, иногда повышение температуры; судороги, симптом заходящего солнца. Эта фаза имеет продолжительность от нескольких дней до нескольких недель; поражение ЦНС носит необратимый характер.
III. Фаза ложного неврологического благополучия и полного или частичного исчезновения спастичности (2-3 месяц жизни);
IY.Период формирования клинической картины неврологических осложнений (после 3-5 месяца жизни): параличи, парезы, атетоз, хореоатетоз, глухота, ДЦП, задержка психического развития, дизартрия (Уровень доказательности – B) [32, 37, 41, 46, 88].
Первые две фазы заболевания являются признаком острого метаболического поражения ЦНС и обозначаются термином острая билирубиновая энцефалопатия (ОБМ). Отдаленные неврологические нарушения, вызванные нейротоксическим действием билирубина (4 фаза), обозначаются термином хроническая билирубиновая энцефалопатия (ХБЭ) [13, 89, 90].
Развитие классических признаков ОБЭ в случаях непрямой гипербилирубинемии характерно для доношенных и поздних недоношенных (ГВ 34-36 недель) новорожденных детей (Уровень доказательности – A) [13, 89, 91]. У глубоконедоношенных детей при надпороговых значениях гипербилирубинемии характерные клинические признаки ОБЭ могут отсутствовать или маскироваться симптомами других патологических состояний, но во втором полугодии жизни у них появляются типичные признаки ХБЭ (Уровень доказательности – D) [82, 92].
С целью раннего выявления, оценки динамики и определения тяжести билирубиновой энцефалопатии у новорожденных детей Jonson L.,Bhutani V.K., Karp K. et al. была предложена бальная шкала, позволяющая учитывать степень выраженности неврологических дисфункций, характеризующих ОБЭ (таблица 4) [93, 94].
Таблица 4. Бальная оценка тяжести клинических проявлений билирубиновой энцефалопатии у новорожденных детей в остром периоде
Интерпретация результатов:
1-3 балла – минимальная,
4-6 баллов – умеренная,
7-9 баллов – тяжелая
Диагностика
Клинико-анамнестический и клинико-лабораторный скрининг новорожденных детей на возможность развития или наличие патологической гипербилирубинемии
Клинико-анамнестические данные.
В группу высокого риска по развитию непрямой гипербилирубинемии сразу после рождения должны быть выделены:
новорожденные, с клиническими и/или лабораторными признаками гемолитической болезни
новорожденные с выраженными признаками морфофункциональной незрелости, в т.ч. глубоконедоношенные дети
новорожденные с множественными подкожными кровоизлияниями и обширными кефалогематомами
новорожденные, нуждающиеся в проведении реанимационной и интенсивной терапии в раннем неонатальном периоде, включая детей с врожденными инфекциями и неонатальным сепсисом
новорожденные с высоким риском раннего проявления болезней обмена или наследственных гемолитических анемий (отягощенный семейный анамнез или наличие соответствующих лабораторных признаков)
наличие в семье других детей с выраженной гипербилирубинемией, требующей лечения в неонатальном периоде
Визуальное наблюдение за временем появления и интенсивностью нарастания желтухи.
Исторически сложилось, что с целью раннего выявления гипербилирубинемии многие неонатологи ориентируются в первую очередь на изменение цвета кожных покровов [95, 96]. Безусловно, раннее появление желтухи (до 24 часов жизни), нарастание после 4 суток и сохранение более 2 недель свидетельствуют о наличии патологических причин для развития гипербилирубинемии. При этом практически всегда появление желтухи в первые 24 часа свидетельствует о гиперпродукции билирубина, вызванного патологическим гемолизом эритроцитов, а нарастание желтухи после 4 суток жизни с высокой вероятностью указывает на нарушение конъюгации билирубина в печени и его недостаточной экскреции (Уровень доказательности – B) [30, 97].
Дополнительную информацию о патологической природе желтухи может иметь появление на ее фоне лимонного (типично для ГБН), зеленоватого (типично для холестаза) или сероватого (типично для сепсиса) оттенка кожи.
Первоначально желтый цвет приобретает кожа лица и туловища ребенка. Дальнейшее нарастание концентрации билирубина, независимо от причины, приводит к распространению желтухи и окрашиванию кожи конечностей. Увеличение концентрации билирубина более 255-306 мкмоль/л сопровождается прокрашиванием ладоней и стоп (Уровень доказательности – C) [95, 98].
Основываясь на этой закономерности, Kramer L.I. в 1969 году предложил выделять 5 степеней выраженности желтухи новорожденных, каждой из которых соответствует свой диапазон концентрации билирубина в сыворотке крови (рис 1.) [98]. В настоящее время эксперты РОН считают, что клиническая оценка степени выраженности желтухи на основе шкалы Крамера остаточно субъективна и требует подтверждения наличия гипербилирубинемии инструментальными и лабораторными методами. Шкала Крамера может быть использована для определения необходимости забора крови на биохимический анализ билирубина у доношенных новорожденных в тех медицинских организациях, в которых отсутствуют аппараты для чрезкожного определения билирубина (Уровень доказательности – D).
Клиническая оценка распространенности желтухи у новорожденных по Крамеру (Kramer LI).
При использовании шкалы Крамера с целью определения показаний к биохимическому исследованию крови на билирубин у доношенных новорожденных следует помнить, что однократная оценка по Крамеру в большинстве случаев не позволяет дифференцировать физиологическую и патологическую гипербилирубинемию. С этой точки зрение описание во врачебных дневниках желтухи с указанием кожных зон, предложенных Крамером, помогает более точно определить показания для исследований крови. Желтое окрашивание 2 и 3 зон не позволяет исключить или подтвердить гипербилирубинемию, распространение желтухи на 4 и 5 кожные зоны практически всегда свидетельствует о наличии гипербилирубинемии, но не позволяет объективно оценивать вероятность развития БЭ. Таким образом, распространение желтухи на 4 и 5 зоны по Крамеру у доношенного новорожденного ребенка должно рассматриваться как показание к биохимическому исследованию крови. Вместе с тем, при ранней выписке новорожденных из акушерского стационара такой подход не позволяет прогнозировать нарастание желтухи после 3-х суток. Кроме того, шкалу Крамера нельзя применять у недоношенных и новорожденных с дефицитом массы тела. Шкала Крамера не может быть использована для оценки эффективности фототерапии (D).
Все вышеизложенное подчеркивает существенное ограничение возможностей использования визуальной оценки степени желтухи для скрининга детей, составляющих группу риска по развитию БЭ (Уровень доказательности – A) [99, 100].
Чрезкожное измерение уровня билирубина у новорожденных детей
Более объективным методом оценки скорости и степени накопления билирубина в коже ребенка, чем визуальная оценка, является чрескожное измерение отраженного от кожи и подкожных тканей света с помощью специальных приборов (Уровень доказательности – B) [101, 102].
В настоящее время для чрезкожного измерения уровня билирубина у новорожденных в Российской Федерации используются приборы как отечественного, так и зарубежного производства (Билитест, производство «Техномедика», Россия; JM-103, производство Dräger, Германия; BiliCheck, производство «Philips», Нидерланды и др.). Использование каждого из вышеперечисленных приборов имеет свои особенности, поэтому проведение чрезкожного измерения билирубина должно выполняться в строгом соответствии с инструкцией по эксплуатации [102].
Общим для всех приборов является то, что в диапазоне концентраций общего билирубина от 100 до 255 мкмоль/л отмечается прямая линейная зависимость между показателями содержания билирубина в коже и сыворотке крови у доношенных и недоношенных новорожденных ГВ более 35 недель. При определении чрезкожными анализаторами концентраций билирубина более 255 мкмоль/л линейная зависимость между содержанием билирубина в коже и сыворотке крови уменьшается, что требует перепроверки уровня билирубинемии стандартными лабораторными методами (Уровень доказательности – B) [33, 103, 104, 105].
Особенности и ограничения чрезкожного измерения уровня билирубина, независящие от конструкции прибора: [5, 105, 106, 107, 108, 109, 110]:
Исследование уровня билирубина чрезкожным методом показано всем доношенным новорожденным с желтухой, независимо от степени ее выраженности
Измерение уровня билирубина должно проводиться только в области лба и/или грудины. Для определения показаний к повторному измерению или срочному определению концентрации билирубина в крови стандартными лабораторными методами могут быть использованы процентильные кривые Bhutani VK
Следует помнить, данный метод измерения билирубина не может быть использован после начала фототерапии (Уровень доказательности – B) [111].
Процентильные кривые уровня билирубина крови, измеренного чрезкожным методом у доношенных и поздних недоношенных детей (ГВ 35-37 нед), предназначенные для определения степени риска развития патологической гипербилирубинемии, представлены на рисунке 2 [102].
Рис 2. Процентильные кривые уровня билирубина крови, измеренного чрезкожным методом у доношенных и поздних недоношенных детей (ГВ 35-37 нед) (Bhutani VK и соавт, 1999)
При ранней выписке новорожденного из акушерского стационара целесообразно воспользоваться алгоритмом, представленном на рис 3 (мнение экспертов РОН, уровень доказательности – D).
Рациональное использование приборов для чрезкожного измерения билирубина у новорожденных детей в условиях акушерского стационара позволяет: 1) уменьшить неоправданно широкое использование забора крови на билирубин у доношенных новорожденных; 2) более объективно выделять среди клинически здоровых новорожденных группу риска по развитию непрямой патологической гипербилирубинемии; 3) предотвращать раннюю выписку домой новорожденных, у которых имеется потенциальный риск отсроченного развития БЭ (Уровень доказательности – B)[14,18,97,99,101].
Рис 3. Алгоритм использования чрезкожного измерения билирубина при ранней выписке новорожденного из акушерского стационара
Таким образом, рациональное использование приборов для чрезкожного измерения билирубина у новорожденных детей в условиях акушерского стационара позволяет: 1) уменьшить неоправданно широкое использование забора крови на билирубин у доношенных новорожденных; 2) более объективно выделять среди клинически здоровых новорожденных группу риска по развитию непрямой патологической гипербилирубинемии; 3) предотвращать раннюю выписку домой новорожденных, у которых имеется потенциальный риск отсроченного развития БЭ.
Особенности использования приборов для чрезкожного измерения билирубина у недоношенных детей
Несмотря на то, что в последнее десятилетие опубликован ряд научно-исследовательских работ, продемонстрировавших перспективность использования метода у недоношенных детей ГВ 28-34 недели (C), к настоящему времени не накоплено достаточного количества клинических данных, позволяющих рекомендовать рутинное чрезкожное измерение билирубина у недоношенных детей, за исключением группы поздних недоношенных ГВ более 35 недель. При этом подходы к использованию метода практически ничем не отличаются от описанных выше для доношенных новорожденных (Уровень доказательности – A) [102, 104,106, 107, 112].
Лабораторные методы измерения концентрации билирубина в крови у новорожденных детей
Своевременное измерение концентрации билирубина в крови у новорожденных детей имеет ключевое значение для определения медицинской тактики ведения при подозрении на патологическую желтуху. Несмотря на то, что нейротоксическим эффектом обладает в основном непрямая фракция билирубина, лечебная стратегия на первой недели жизни, независимо от причины и характера развития желтухи, строится исходя из абсолютных значений общего билирубина в крови, а не его отдельных фракций.
Стандартное лабораторное исследование концентрации билирубина в крови показано (Уровень доказательности – A) [ 97, 100]:
— Всем недоношенным детям ГВ менее 35 недель с желтухой
— Всем новорожденным, у которых желтуха появилась в первые 24 часа
— Новорожденным с признаками ГБН или другими известными факторами риска развития патологический желтухи
— Доношенным и поздним недоношенным детям, если уровень билирубина, определенный транскутанным методом, составил:
более 140 мкмоль/л в возрасте 24-48 часов
более 200 мкмоль/л в возрасте 48-72 часов
более 250 мкмоль/л в возрасте старше 72 часов.
— Всем детям, получающим фототерапию (с интервалом 12-24 в сутки)
Особенности лабораторного определения билирубина в крови
В настоящее время для определения уровня общего билирубина в плазме или сыворотке крови применяются разнообразные лабораторные методы. В большинстве случаев измерение концентрации билирубина в крови выполняют либо биохимическими методами (в основном с диазокрасителями), либо методами прямого фотометрирования плазмы (с разведением или без разведения) [96, 112]
С целью уменьшения объема исследуемой крови внедрено измерение оптической плотности плазмы капиллярной крови (так называемый «микрометод»), забор крови производится в стеклянный капилляр без дозирования, внутренний объем которого составляет примерно 30 мкл [113]. Плазма для фотометрирования получается непосредственно в капилляре на любой гематокритной центрифуге. Недостатком метода является невозможность определить фракции билирубина, а также существенное снижение точности измерения при выраженном гемолизе. Данный метод может использоваться для скрининга детей группы риска в случаях, когда невозможно использовать приборы для чрезкожного определения, с целью снижение частоты забора большего объема крови на стандартное биохимическое исследование. Однако он не может заменять стандартный биохимический метод при выборе и обосновании методов интенсивной терапии непрямой (патологической) гипербилирубинемии. Его можно рассматривать в качестве вспомогательного метода лабораторного контроля за эффективностью фототерапии у детей (преимущественно недоношенных) с концентрацией билирубина в крови менее 280 мкмоль/л. Однако, в случаях, когда определяются более высокие концентрации и при любых формах гемолитической болезни новорожденного, лабораторный контроль за эффективностью лечения должен осуществляться стандартными биохимическими методами определения билирубина в сыворотке крови. (Уровень 4)
Сопоставление точности измерения общего билирубина плазмы капиллярной крови портативными анализаторами и автоматическими биохимическими анализаторами, в которых используется биохимический метод Йендрашика, свидетельствуют о сопоставимости результатов до достижения максимальной концентрации билирубина в крови 280 мкмоль/л. Для точного определения более высоких концентраций или проверки спорных результатов исследования (например, при явном несоответствии между клинической картиной и концентрации билирубина в крови, измеренной путем прямой фотометрии) должно проводится стандартное биохимические исследование с диазокрасителями (Уровень доказательности – D).
Клинико-лабораторные характеристики основных патологических причин непрямой гипербилирубинемии [23, 24, 25, 28, 51, 52, 55, 63,114, 115, 116, 117,].
Гипербилирубинемия, обусловленная избыточным гемолизом эритроцитов.
Повышенное образование билирубина вследствие гемолиза эритроцитов может быть обусловлено иммунным конфликтом между эритроцитами матери и плода, наследственными нарушениями структуры или функции эритроцитов, гемоглобинопатиями, ятрогенными факторами (лекарственный гемолиз — высокие дозы викасола), рядом инфекционных заболеваний (врожденные инфекции – цитомегалия, герпес, краснуха, токсоплазмоз, листериоз, сифилис; неонатальный сепсис)
Наиболее опасной, с точки зрения развития билирубиновой энцефалопатии, причиной гипербилирубинемии является гемолитическая болезнь новорожденных (ГБН).
Клинические формы ГБН подробно описаны в соответствующем протоколе.
Лабораторные критерии ГБН
• концентрация билирубина в пуповинной крови (в момент рождения) – при легких формах иммунологического конфликта по Rh и во всех случаях AB0- несовместимости ≤ 51 мкмоль/л; при тяжелых формах иммунологического конфликта по Rh и редким факторам – существенно выше 51 мкмоль/л;
• концентрация гемоглобина в пуповинной крови в легких случаях – на нижней границе нормы, в тяжелых – существенно снижена;
• почасовой прирост билирубина в первые сутки жизни больше 5,1 мкмоль/л/час;
• максимальная концентрация общего билирубина на 3–4 сутки в периферической или венозной крови у доношенных новорожденных; при отечной и желтушной формах она существенно выше 256 мкмоль/л;
• общий билирубин крови повышается преимущественно за счет непрямой фракции,
• относительная доля прямой фракции (при условии отсутствия холестатических осложнений) составляет менее 20%,
• снижение концентрации гемоглобина, уменьшение количества эритроцитов и повышение количества ретикулоцитов в периферической и венозной крови в течение 1 недели жизни.
Для наследственных гемолитических желтух (обусловленная дефицитом Г-6-Ф-ДГГ, серповидно-клеточная анемия, наследственный микросфероцитоз и др.) характерно отсроченное (после 24 ч жизни), появление признаков гемолиза, а также изменение формы и размеров эритроцитов при морфологическом исследовании мазка крови, нарушение их осмотической стойкости .
Несмотря на отличия в патогенезе, сходными клиническими и лабораторными признаками сопровождаются гипербилирубинемии, обусловленные полицетемией/повышенной вязкостью крови, а также повышенным экстравазальным образованием билирубина (при множественных и обширных экхимозах, больших кефалогематомах и др.).
Гипербилирубинемия, обусловленная нарушением конъюгации билирубина (конъюгационные желтухи).
Конъюгационные желтухи обусловлены преимущественным нарушением конъюгации билирубина в гепатоцитах. К ним относятся желтухи связанные с исключительно грудным вскармливанием (при гипогалактии) и особенностями состава грудного молока (семейной транзиторной гипербилирубинемии Ариаса– Люцея–Дрискола) (при нормальном уровне лактации); желтухи, обусловленные диабетической фетопатией и врожденным гипотиреозом. Выраженные нарушения конъюгации билирубина отмечаются при ряде наследственных заболеваний: синдроме Криглера–Найяра 1-го и 2-го типов, синдроме Жильбера и др.
Конъюгационные желтухи характеризуются следующими признаками:
Динамика желтухи:
появляется не ранее 24 часов после рождения;
продолжает нарастать или остается выраженной после 4 суток жизни;
сохраняется более 10 дней жизни.
Особенности клинической картины:
кожные покровы имеют оранжевый оттенок;
пальпаторные размеры печени и селезенки не увеличены;
кал и моча обычной окраски.
Лабораторные критерии:
концентрация билирубина в пуповинной крови (в момент рождения) – менее 51 мкмоль;
концентрация гемоглобина в пуповинной крови соответствует норме;
почасовой прирост билирубина в первые сутки жизни менее 6,8 мкмоль/л/час;
максимальная концентрация общего билирубина на 3–4 сутки в периферической или венозной крови у доношенных детей > 255 мкмоль/л;
общий билирубин крови повышается за счет непрямой фракции;
относительная доля прямой фракции составляет менее 20%;
Гипербилирубинемия, обусловленная повышением кишечной реабсорбции чаще всего наблюдается при высокой кишечной непроходимости.
Клиническая картина зависит от причины кишечной непроходимости (атрезия 12-ти перстной кишки, пилоростеноз, обструкция кишечника объемным образованием и т.п.), а также, нередко, сопутствующими симптомами обезвоживания и гипогликемии.
Лабораторные критерии сходны с критериями конъюгационной желтухи.
Непрямая гипербилирубинемия смешанного генеза чаще всего является ранним клиническим проявлением врожденной или перинатальной инфекции. Клиническая картина и лабораторные признаки являются составной частью симптомокомплекса TORCHES или сепсиса.
Стандартное обследование новорожденного с подозрением на патологическую желтуху:
Уточнение срока появления желтухи
Физикальный осмотр (степень распространенности желтухи, размеры печени и селезенки, цвет стула и мочи)
Группа крови и Rh-фактор, реакция Кумбса
Клинический анализ крови (Hb, ретикулоциты, особенности лейкоцитарной формулы крови и др.)
Биохимический анализ крови (билирубин и его фракции, другое – по показаниям)
УЗИ органов брюшной полости.
Лечение
Подготовка и проведение лечебных мероприятий, направленных на уменьшение концентрации непрямого билирубина в сыворотке крови.
Общие принципы. Важным условием для профилактики и лечения гипербилирубинемии у новорожденных является создание оптимальных условий для ранней неонатальной адаптации ребенка. При этом все здоровые и условно здоровые новорожденные дети нуждаются в проведении раннего (начиная с первого часа жизни) и регулярного грудного вскармливания (Уровень доказательности – B). [118, 119].
Необходимо рекомендовать матери кормить грудью* как минимум 8 — 12 раз в сутки без ночного перерыва в течение первых нескольких дней жизни. Увеличение частоты кормления грудью снижает вероятность последующей тяжелой гипербилирубинемии у новорожденных при грудном вскармливании (Уровень доказательности – D). [38, 39]. (*Отношение к грудному вскармливанию при ГБН изложено в соответствующих клинических рекомендациях).
Дополнительное введение воды либо растворов глюкозы новорожденным, находящимся на грудном вскармливании, при отсутствии признаков дегидратации, не показано. Дополнительное введение в рацион воды либо растворов глюкозы не предупреждает развитие гипербилирубинемии и не снижает уровень общего билирубина сыворотки.
В качестве крайней меры может рассматриваться временное (1-3 дня) прекращение грудного вскармливания и переход на кормление адаптированной смесью, что может способствовать снижению уровня билирубина и/или повышению эффективности фототерапии в случае желтухи обусловленной составом грудного молока (Уровень доказательности – D) [38]. В случаях медицинских противопоказаний к раннему прикладыванию к груди или избыточной убыли первоначальной массы тела к 3–4 дню жизни новорожденным необходимо организовать докорм адаптированной питательной смесью.
Во всех случаях заболевания новорожденного необходимо заботиться о поддержании оптимальной температуры тела, обеспечении его организма достаточным количеством жидкости и питательных веществ, профилактике таких метаболических нарушений, как гипогликемия, гипоксемия и ацидоз.
Фототерапия
Основным методом лечения непрямой гипербилирубинемии является фототерапия.
При неэффективности фототерапии и угрозе развития БЭ показано проведение обменного переливания крови (Уровень доказательности – A) [85, 120, 121, 122, 123] .
Виды фототерапии [ 124, 125].:
• Традиционная – проведение фототерапии с использованием одного источника света – люминесцентные лампы голубого света;
• LED фототерапия – фототерапия с использованием светодиодов, обеспечивает меньшие потери жидкости организмом;
• Фиброоптическая фототерапия – процедура с использованием одного источника света с волоконно-оптическим кабелем, через который световой луч проходит на гибкую светящуюся поверхность, на которую помещается ребенок или может быть обернута вокруг него (не требует защиты глаз). Может быть использована у недоношенных новорожденных;
• Комбинированная фототерапия – осуществляется с помощью двух и более источников света (две и более единицы или сочетание ламп обычной и фиброоптической фототерапии). Показана для лечения как доношенных, так и недоношенных новорожденных при наличии хотя бы одного признака:
— если почасовой прирост ОБС > 6,8 мкмоль/л/час;
— если через 72 часа уровень ОБС находится на уровне менее 50 мкмоль/л от порового значения для начала операции ЗПК;
— если после проведения фототерапии в течение 6 часов уровень ОБС повышается или не снижается.
Проведение фототерапии в непрерывном режиме (проводится в течение суток непрерывно, допустимы лишь перерывы на кормление и манипуляции (не более 30 минут) более предпочтительно (Уровень доказательности – A) [126].
Техника фототерапии при использовании установок с традиционными и LED-источниками света [120]:
Обнаженный ребенок помещается в кувез или в кроватку с термоматрасом (выбор режима зависит от гестационного возраста ребенка, особенностей терморегуляции, при этом температура тела ребенка должна быть в пределах 36,6 – 37,0 С) [127 ур 1+ ].
глаза ребенка и половые органы мальчиков должны быть защищены светонепроницаемым материалом.
источник фототерапии располагается над ребенком на высоте 50-55 см, если ребенок находится в кувезе, то расстояние от верхней стенки кувеза до лампы фототерапии должно быть 5,0 см.
фототерапия при помощи установок, не предназначенных для домашнего использования, должна проводится в палатах для новорожденных под контролем среднего медицинского персонала
каждые 1-2 часа фототерапии необходимо менять положение ребенка по отношению к источнику света, переворачивая его поочередно вверх животом или спиной [97 ур 1++]
каждые 2 часа необходимо измерять температуру тела ребенка,
при отсутствии противопоказаний необходимо сохранять кормление материнским молоком в полном объеме,
физиологическая потребность ребенка в жидкости увеличивается на 10-20%, при невозможности увеличения объема питания проводится инфузионная терапия [118 ур 1-, 119 ур 1+]
в процессе фототерапии нельзя ориентироваться на цвет кожных покровов, и показатели приборов для чрезкожного измерения билирубина
всем детям, получающим фототерапию, необходимо ежедневно проводить биохимический анализ крови на билирубин (при угрозе билирубиновой энцефалопатии – каждые 6-12 часов); только стандартный биохимический анализ крови может служить критерием эффективности фототерапии,
фототерапия может быть прекращена, если отсутствуют признаки патологического прироста билирубина, а концентрация общего билирубина в сыворотке крови стала ниже значений, послуживших основанием для начала фототерапии,
через 12 часов после окончания фототерапии необходимо контрольное исследование билирубина крови,
у некоторых детей в ответ на фототерапию может появиться аллергическая сыпь, участиться и измениться в цвете стул и появиться бронзовый оттенок кожи. Все три эффекта, как правило, бесследно исчезают после прекращения фототерапии.
Показания для фототерапии и операции ЗПК у доношенных и поздних недоношенных детей (боле 35 недель гестации) при непрямой гипербилирубинемии, не связанной с ГБН, в раннем неонатальном периоде основываются на определении пороговых значений общей концентрации билирубина сыворотки крови в зависимости от постнатального возраста в часах и наличия или отсутствия факторов риска. При быстром нарастании уровня билирубина и при критической гипербилирубинемии фототерапию необходимо проводить в непрерывном режиме (Уровень доказательности – C) [131]. Во всех случаях наличия у ребенка факторов риска, повышающих вероятность развития билирубиновой энцефалопатии, фототерапию необходимо начинать при минимальных значениях билирубина. Несмотря на то, что в отдельных Европейских странах в последнее десятилетие наметилась тенденция к пересмотру (повышению) пороговых значений концентрации билирубина в сыворотке крови [126], при которых рекомендовано начало фототерапии и проведение операции ЗПК новорожденным детям, по мнению экспертов РОН, в нашей стране на данном этапе развития перинатальных технологий наиболее целесообразно использовать показания, разработанные Американской Академией Педиатрии (AAP) в 2004 году, которые в графическом виде представлены на рис 4. (Уровень доказательности – D).
При снижении концентрации общего билирубина на фоне проводимой фототерапии лечение продолжается до момента, когда при плановом биохимическом исследовании билирубина его концентрация оказывается ниже значений (насколько ниже?), явившихся показанием к началу фототерапии. Через 12 часов после завершения фототерапии должно быть проведено контрольное исследование билирубина, чтобы убедиться что ребенок не нуждается в лечении гипербилирубинемии. Продолжение фототерапии при концентрациях билирубина ниже, указанных на рис 4, является необоснованным и потенциально опасным.
Рис 4. Показания к проведению фототерапии доношенных и поздних недоношенных детей (ГВ 35-37 нед) в раннем неонатальном периоде
После начала фототерапии, ее эффективность при непрямой гипербилирубинемии, не связанной с ГБН, должна оцениваться каждые 12 часов путем измерения концентрации общего билирубина в сывротке крови стандартными лабораторными методами. В случае неэффективности фототерапии – осуществляется подготовка и проведение операции ЗПК (Уровень доказательности – A) [14, 97, 85, 120, 122, 124]. Показания к проведению операции, разработанные Американской Академией Педиатрии (AAP) в 2004 году, представлены на рис 5. [128]
Рис 5. Показания к проведению операции обменного переливания крови у доношенных и поздних недоношенных детей (ГВ 35-37 нед) в раннем неонатальном периоде
Этапы подготовки и проведения операции [129]:
1. Обязательно получение от родителей информированного согласия на проведение ОЗПК.
2. Манипуляцию выполняют в палате/отделении реанимации и интенсивной терапии новорожденных (ПИТН/ОРИТН) (в акушерских отделениях медицинских организаций I уровня оказания перинатальной помощи — в процедурном кабинете).
3. До начала операции у новорожденных, которые находятся в тяжелом состоянии, стандартными методами интенсивной терапии должны быть устранены ацидоз, гипоксемия, гипогликемия, электролитные нарушения, гемодинамические расстройства, гипотермия и т.д.
4. ОЗПК проводит бригада, состоящая, как минимум, из двух человек: врача (неонатолога/анестезиолога-реаниматолога/педиатра) и детской медицинской сестры.
5. Обязательно в истории болезни заполняется протокол ОЗПК (прил. 1).
6. Обязательно строгое соблюдение правил асептики и антисептики.
7. Дети не должны получать энтеральное питание в течение последних 3 часов до предполагаемого начала операции.
8. В желудок перед операцией должен быть введен постоянный зонд, через который необходимо периодически удалять содержимое желудка.
9. Перед операцией необходимо сделать очистительную клизму.
10. В течение всего процесса подготовки к ОЗПК, выполнения операции и последующего ведения ребенка необходим постоянный мониторинг витальных функций (ЧСС, ЧД, сатурация, АД, температура тела).
11. Донорская кровь и (или) ее компоненты при ОЗПК переливаются из расчета 150-170 мл/кг массы тела для доношенного ребенка и 170-180 мл/кг для недоношенного (пример расчета объема замещения представлен в приложении 2).
12. Соотношение эритроцитарной массы/взвеси и свежезамороженной плазмы составляет 2 : 1.
13. Согласно Приказу Минздрава России от 2 апреля 2013 г. N 183н «Об утверждении правил клинического использования донорской крови и (или) ее компонентов» при трансфузии (переливании) донорской крови и (или) эритроцитсодержащих компонентов новорожденным:
— переливаются эритроцитсодержащие компоненты, обедненные лейкоцитами (эритроцитная взвесь, эритроцитная масса, отмытые эритроциты, размороженные и отмытые эритроциты);
— при подборе компонентов донорской крови для трансфузии (переливания) учитывается, что мать является нежелательным донором свежезамороженной плазмы для новорожденного, поскольку плазма матери может содержать аллоиммунные антитела против эритроцитов новорожденного, а отец является нежелательным донором эритроцитсодержащих компонентов, поскольку против антигенов отца в крови новорожденного могут быть антитела, проникшие из кровотока матери через плаценту;
— наиболее предпочтительной является трансфузия негативного по цитомегаловирусу эритроцитосодержащего компонента;
— не допускается переливание свежезамороженной плазмы вирус (патоген) инактивированной реципиентам детского возраста, находящимся на фототерапии.
Для заменного переливания крови используются эритроцитсодержащие компоненты со сроком хранения не более 5 дней с момента заготовки компонента.
Подбор компонентов донорской крови осуществляется в соответствие с группой крови и резус-фактором реципиента
Техника проведения ОЗПК:
уложить ребенка в заранее согретую открытую реанимационную систему с сервоконтролем;
зафиксировать конечности ребенка путем надежного пеленания, кожа живота остается открытой;
установить пупочный катетер с присоединенным к нему заранее тройником со строгим соблюдением правил асептики и антисептики и зафиксировать его;
при наличии противопоказаний для катетеризации пупочной вены ОЗПК проводят через любую другую центральную вену;
компоненты донорской крови предварительно необходимо согреть до температуры 36-370 С;
первую порцию выводимой крови необходимо отобрать для биохимического исследования на уровень билирубина;
далее последовательно проводят постепенное выведение крови ребенка и последующее восполнение выведенного объема;
объем одного замещения (однократного выведения крови) и одного восполнения (однократного введения компонентов крови) зависит от массы тела ребенка, ГВ и тяжести состояния ребенка (у доношенных — 10-20 мл/кг, у недоношенных – 5-10 мл/кг под обязательным контролем показателей гемодинамики, дыхания и функции почек);
скорость одного замещения – 3-4 мл/мин;
на 2 шприца эритроцитарной массы вводится 1 шприц свежезамороженной плазмы;
после каждых 100 мл замещающей среды (эритроцитарной массы и плазмы) ввести 1,0-2,0 мл 10% раствора глюконата кальция или 0,5 мл 10% раствора хлористого кальция, предварительно разведенных в 5,0 мл 5 % глюкозы (только между шприцами с эритроцитарной массой!);
перед окончанием операции осуществляется забор крови на билирубин;
в результате операции (с учетом крови, взятой на биохимическое исследование) суммарный объем вводимых компонентов донорской крови должен быть равен суммарному объему выведенной крови ребенка.
NB! О безусловной эффективности ОЗПК свидетельствует более чем 2-х кратное снижение билирубина к концу операции.
Ведение ребенка в послеоперационном периоде:
Продолжить мониторинг витальных функций;
Энтеральное питание начинать не ранее, чем через 3-4 часа после ОЗПК;
Продолжить фототерапию;
Продолжить поддерживающую и симптоматическую терапию;
Удаление пупочного катетера сразу после операции не рекомендуется в связи с вероятностью повторного проведения ОЗПК;
Контроль уровня билирубина выполняется через 12 часов после ОЗПК, далее по показаниям, но не реже 1 раза в 24 часа до 7 суток жизни;
Контроль гликемии через 1 час после ОЗПК, далее по показаниям;
Согласно Приказу МЗ РФ №183н после окончания трансфузии (переливания) донорской крови и (или) ее компонентов донорский контейнер с оставшейся донорской кровью и (или) ее компонентами (5 мл), а также пробирка с кровью реципиента, использованная для проведения проб на индивидуальную совместимость, подлежат обязательному сохранению в течение 48 часов при температуре 2-60 С в холодильном оборудовании.
В процессе операции ЗПК и в раннем постоперационном периоде возможно развитие следующих осложнений (Уровень доказательности – С) [130, 132, 133, 134].
1. Со стороны сердечно-сосудистой системы:
аритмия;
объемная перегрузка;
застойная сердечная недостаточность;
остановка кровообращения.
передозировка гепарина;
нейтропения;
тромбоцитопения;
реакция «трансплантант против хозяина».
бактериальные и вирусные инфекции.
ацидоз;
гипокальциемия;
гипогликемия;
гиперкалиемия;
гипернатриемия.
эмболии;
тромбозы;
некротизирующий энтероколит;
портальная гипертензия;
перфорация сосудов пуповины.
гипотермия.
Важно отметить, что показания к фототерапии и операции ЗПК, содержащиеся в рекомендациях AAP 2004 года, определяют тактику ведения только доношенных и поздних недоношенных детей ГВ более 35 недель, и ограничены ранним неонатальном периодом. В связи с недостаточностью объективных данных об условиях, при которых БЭ может возникнуть у новорожденных после окончания первой недели жизни, большинство экспертов РОН предлагает расширить действие этих рекомендаций до конца неонатального периода. Вместе с тем у доношенных детей с наследственными нарушениями обмена (например, с синдромом Криглера-Найара – см. ниже), нуждающихся в длительном проведении фототерапии, показания к операции ЗПК должны определяться консилиумом специалистов с учетом патогенеза заболевания и индивидуальной реакции ЦНС ребенка на хроническую непрямую гипербилирубинемию (Мнение экспертов РОН, уровень доказательности – D).
Показания к фототерапии и операции ЗПК у недоношенных детей
До 2007 года в нашей стране не было общепринятых показаний к лечению непрямой гипербилирубинемии у недоношенных и глубоконедоношенных детей. Национальное руководство по неонатологии (2007, 2013) предлагает для определения показаний к фототерапии и операции ЗПК ориентироваться на массу тела новорожденных. Вместе с тем, в прошедшее десятилетие были накоплены и обобщены клинические данные, позволившие составить рекомендации по лечению непрямой гипербилирубинемии недоношенных с учетом их ГВ (B) .
В настоящее время эксперты РОН для определения показаний к фототерапии и операции ЗПК у недоношенных, с учетом ГВ и дополнительных факторов риска рекомендует использовать модифицированные рекомендации AAP (Уровень доказательности – B) [126] Рис. 6,7.
Рис 6.Показания к проведению фототерапии в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
Рис 7. Показания к проведению операции обменного переливания крови в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
Вместе с тем, учитывая высокий риск осложнений операции ЗПК у глубоконедоношенных детей, окончательное решение проведнии операции у детей, родившихся ранее 32 недели гестации должен принимать консилиум врачей-специалистов (Мнение экспертов РОН, уровень доказательности – D).
Неэффективные и потенциально опасные методы лечения, которые следует исключить из клинической практики:
1) Инфузионная терапия имеет ограниченные показания при гипербилирубинемии.
Токсическим действием обладает непрямой жирорастворимый билирубин, и его уровень не может быть снижен введением дополнительных водных растворов. Дополнительная инфузия водного раствора 5-10% глюкозы новорожденным с гипербилирубинемией показана только при развитии эксикоза на фоне интенсивной фототерапии, парентеральное введение жидкости может определяется другими показаниями (рвота, патологическая потеря жидкости, др.) (Мнение экспертов РОН, уровень доказательности – D).
2) Включение в программу инфузионной терапии свежезамороженной донорской плазмы и альбумина при гипербилирубинемии не рекомендуется и не оправдано с позиции доказательной медицины. Данные препараты должны применятся по строгим показаниям; (Уровень доказательности – B) [136].
3) Назначение фенобарбитала. Значимая индукция ферментов печени происходит не ранее 3 дней от момента его назначения, чаще к концу первой недели жизни. Кроме того, при лечении желтухи фенобарбиталом возникают нежелательные эффекты в виде вялости, угнетения дыхания и снижения активности сосания. По этим причинам в течение последних 15-20 лет фенобарбитал для лечения гипербилирубинемии не применяется (Уровень доказательности – A) [139].
4) Нет убедительных научных доказательств, и патогенетического обоснования для лечения непрямой гипербилирубинемии гепатопротективными и желчегонными препаратами, такими как Эссенциале, ЛИВ-52, Хофитол. Препараты урсодезоксихолевой кислоты показаны только при развитии синдрома холестаза (Мнение экспертов РОН, уровень доказательности – D).
Условия выписки из стационара доношенных новорожденных с непрямой гипербилирубинемией
Условия выписки доношенных новорожденных, получавших фототерапию по поводу непрямой гипербилирубинемии, не связанной с ГБН:
— удовлетворительное общее состояние,
— снижение интенсивности желтухи в динамике,
— концентрация билирубина сыворотки крови менее той, которая требует лечения спустя 12 и более часов после окончания фототерапии,
-в случае ранней выписки необходимо ориентироваться на центильную кривую Bhutani VK (см. выше) и учитывать реальные возможности педиатрической службы региона обеспечить динамическое наблюдение за новорожденным ребенком после выписки из стационара.
При выписки ребенка из ОПННД следует помнить, что непрямая гипербилирубинемия редко является единственным патологическим состоянием, определяющим длительность стационарного лечения. Сроки выписки ребенка зависят от результатов лечения основного и сопутствующих заболеваний.
Особенности наблюдения на амбулаторном этапе за новорожденным с непрямой гипербилирубинемией.
Наиболее опасным периодом с точки зрения риска развития БЭ является первые 7 дней жизни (Уровень доказательности – B) [135]. В данном случае тактика наблюдения и лечения ребенка не отличается от таковой в условиях стационара (см. выше). У детей старше 7 дней жизни риск БЭ уменьшается, однако недосточно объективных данных для изменения показаний к лечению в позднем неонатальном периоде (Мнение экспертов РОН, уровень доказательности – D).
Во всех случаях патологической желтухи, генез которой не уточнен, необходимо проведение дополнительного обследования:
Анамнестические данные
— Наличие указаний на патологическую желтуху в неонатальном периоде в семье и/или синдрома Жильбер
Клинические данные:
— степень выраженности желтухи, размеры печени и селезенки, цвет стула и мочи
— вид вскарливания, динамика веса
— наличие срыгиваний и/или рвот, кратность стула
Клинический анализ крови
Биохимия крови, включающая билирубин и его фракции, печеночные тесты: АЛТ, АСТ, ГГТ
Гормоны крови: Т4 св, ТТГ
Таким образом, поводом для госпитализации ребенка в ОПННД перинатального центра или детской больницы является как необходимость дополнительного обследования, которое трудно организаовать в условиях детской поликлиники, так и необходимость лечения патологической гипербилирубинемии.
Наличие косвенных признаков гемолиза эритроцитов у ребенка (снижение концентрации гемоглобина и уменьшение количества эритроцитов, повышение числа ретикулоцитов на фоне, увеличения размеров селезенки и печени) свидетельствует о гемолитическом генезе желтухи (рис). Дополнительное диагностическое значение при этом имеют сроки появления желтухи. Для ГБН характерно раннее развитие желтухи — в течение первых 24 часов жизни, — тогда как при наследственных гемолитических анемиях желтуха появляется не ранее 2–3-х суток жизни, а может возникать и в более поздние сроки.
Клиническая характеристика наиболее частых причин патологической непрямой гипербилирубинемии, возникающей в позднем неонатальном периоде.
Коньюгационные желтухи
Желтуха, связанная с составом грудного молока наблюдается у 0,5–2,5% здоровых доношенных детей, находящихся на грудном вскармливании. Ее развитие связывают с повышенным содержанием метаболитов прогестерона (32-20-β-прегнандиола, 5-β-прегнан-3α, 20-β-диол) и неэстерифицированных длинноцепочечных жирных кислот, которые конкурентно ингибируют глюкуронилтрансферазу, наличием глюкуронидазы, высокой активностью фермента липопротеинлипазы в молозиве и грудном молоке. Часто этот вариант гипербилирубинемии ассоциирован с приемом гормональных препаратов и некоторых других лекарственных средств во время беременности, стимуляцией родовой деятельности [137]. Не исключено влияние длительного, в течение всей беременности, приема поливитаминов. В отличие от детей с физиологической желтухой, у новорожденных с желтухой, связанной с составом грудного молока, наблюдается более высокая концентрация НБ в крови к 4–6 дням жизни, которая продолжает нарастать, достигая пика к 10–15 дням жизни. Состояние ребенка при этом удовлетворительное, отмечается хорошая прибавка в весе. Если ребенок продолжает получать грудное молоко, желтуха держится 4–6 недель и затем начинает постепенно ослабевать. Уровень НБ в крови нормализуется к 16-й неделе жизни. Прекращение грудного вскармливания на 48-72 часа способствует быстрому снижению концентрации НБ, как правило, не менее чем на 40%. После возобновления кормления грудью матери НБ может повыситься, но он не достигает исходного уровня и в дальнейшем постепенно снижается. Таким образом, кратковременная отмена грудного вскармливания имеет диагностическое значение при данном варианте гипербилирубинемии. Вместе с тем, длительная отмена грудного молока с целью полной нормализации билирубина нецелесообразна, так как в большинстве случаев уровень билирубина не превышает 340 мкмоль/л.
Транзиторная семейная гипербилирубинемия новорожденных (синдром Люцея — Дрискола) является разновидностью желтухи, связанной с составом грудного молока, так как механизм ее развития связывают с наличием неидентифицированного фактора, ингибирующего ферментную систему трансферазы глюкуроновой кислоты в грудном молоке [137]. Желтуха появляется с первых дней жизни, имеет тенденцию к прогрессивному нарастанию и затяжному течению. Уровень НБ в крови может превышать 340 мкмоль/л, что обусловливает необходимость своевременной диагностики и лечения. Отмена грудного вскармливания на 2-3 дня способствует снижению уровня билирубина и, следовательно, имеет диагностическое значение. Исследование химического состава грудного молока может позволить дифференцировать данный вариант гипербилирубинемии с другими желтухами, связанными с составом грудного молока, что не является принципиальным с практической точки зрения.
В основе желтухи, обусловленной исключительно грудным вскармливанием, лежит первоначально недостаточный объем питания, что способствует усилению липолиза и, как следствие, повышению в крови неэстерифицированных жирных кислот, нарушающих процесс захвата билирубина гепатоцитом и подавляющих активность глюкуронилтрансферазы [138]. Вторым фактором, способствующим гипербилирубинемии, является замедление пассажа по кишечнику и, как следствие, повышение реабсорбции билирубина. Этот вариант желтухи отмечается у детей, находящихся на грудном вскармливании в период становления лактации и не получающих должный объем питания.
Как правило, первоначальная потеря веса составляет 8–10% и более; общее состояние ребенка не страдает. По мере увеличения объема кормления нормализуются обменные процессы, восстанавливается пассаж по кишечнику и купируется желтуха. Желтуха, обусловленная грудным вскармливанием, встречается примерно у 12% детей, получающих исключительно грудное молоко. Она появляется на 2–4-е сутки жизни, пик приходится на 3–6-й день, купируется к концу первого месяца жизни при условии нормализации веса. В случае большой потери веса у детей на исключительно грудном вскармливании – необходимо обеспечить докорм ребенка.
При отсутствии самостоятельного стула, рекомендации по его восстановлению (изменения характера вскармливания, газоотводные трубочки, свечи, клизьмы и т.д.)
Конъюгационная желтуха при гипотиреозе [140]. Гормоны щитовидной железы регулируют активность глюкуронилтрансферразы и, следовательно, их дефицит может стать причиной нарушения конъюгации билирубина. Подтверждением диагноза является низкий уровень Т3, Т4 и повышение ТТГ в крови.
Наследственные формы конъюгационных желтух
Синдром Жильбера [2] — наследственное заболевание, передающееся по аутосомно-доминантному типу (подобная аномалия есть у одного из родителей) и связанное с нарушением захвата билирубина синусоидальной мембраной гепатоцита. Одновременно отмечается и некоторое снижение активности глюкуронилтрансферазы печени — до 50% от нормы. Частота этого синдрома в популяции составляет от 2 до 6%. Желтуха обычно выражена умеренно, в пределах 80–120 мкмоль/л, случаев ядерной желтухи не описано, общее состояние детей не нарушается. Клинические проявления могут отмечаться со 2–3- х суток жизни, причем интенсивность желтухи может меняться каждые 3–5 недель. С диагностической целью может быть использован фенобарбитал в терапевтической дозе 5 мг/кг/сут коротким курсом в течение 3 дней: характерно снижение билирубина на 50–60%, что позволяет с высокой вероятностью предположить данный синдром. Дополнительное диагностическое значение имеет анализ родословной, свидетельствующий о синдроме Жильбера в семье. Подтверждение диагноза возможно на основании генетического тестирования.
Синдром Криглера—Найяра [67,68] — наследуемая негемолитическая желтуха с повышением уровня НБ вследствие врожденной недостаточности глюкуронилтрансферазы. Механизм желтухи при синдроме Криглера — Найяра сводится к полной или почти полной неспособности печени конъюгировать билирубин. Известны две генетически гетерогенные формы данного синдрома и в связи с этим выделяют 2 типа.
Синдромом Криглера — Найяра 1 типа передается по аутосомно-рецессивному типу. Характерна интенсивная желтуха с 15–50-кратным превышением нормального уровня НБ сыворотки крови, которая во случаях (без лечения) сопровождается прокрашиванием ядер мозга, т. е. развитием ядерной желтухи. При этой форме гипербилирубинемия, как правило, развивается в течение первых дней после рождения и сохраняется всю жизнь. Назначение фенобарбитала с целью стимуляции глюкуронилтрансферазы печени не приводит к уменьшению сывороточной концентрации билирубина. Диагноз устанавливается на основании прогрессивного нарастания уровня непрямого билирубина, не связанного с гемолизом эритроцитов, и отсутствия эффекта от приема фенобарбитала. Подтверждается молекулярно-генетическими методами. Использование фототерапии является наиболее эффективным методом консервативного лечения детей раннего возраста, позволяющим несколько снизить уровень билирубина и зафиксировать его на некоторое время. В течение первых 10 дней жизни оптимально постоянное проведение фототерапии с целью поддержания уровня билирубина ниже 340 мкмоль/л. В дальнейшем чувствительность гематоэнцефалического барьера снижается, в связи с чем уровень билирубина может подниматься выше 340 мкмоль/л, но, по-видимому, не более чем до 500 мкмоль/л, поэтому продолжительность фототерапии может быть уменьшена до 10–16 часов в сутки. К сожалению, у детей старше месячного возраста нет однозначного мнения об уровне билирубина, который является токсичным. Имеющиеся в литературе данные имеют широкий диапазон колебаний — от 500 до 800 мкмоль/л. Наш собственный опыт наблюдения ребенка с синдромом Криглера — Найяра I типа свидетельствует о повышении билирубина до 650 мкмоль/л без развития признаков билирубиновой энцефалопатии. Радикальным методом лечения служит трансплантация печени или гепатоцитов. В ургентных ситуациях, при высоком риcке развития билирубиновой энцефалопатии, показано проведение операции ОПК или плазмафереза.
Синдром Криглера — Найяра II типа передается по аутосомно-доминантному типу, является прогностически более благоприятным заболеванием и сопровождается более слабой желтухой с 5–20-кратным повышением НБ сыворотки крови. Отличительной особенностью этой формы служит уменьшение сывороточной концентрации билирубина на фоне 3-дневного применения фенобарбитала не менее чем на 50–60%. При синдроме Криглера — Найяра II типа дефицит глюкуронилтрансферазы менее выражен, уровень билирубина в сыворотке крови широко варьирует (от 91 до 640 мкмоль/л), но чаще всего не превышает 340 мкмоль/л. Развитие билирубиновой энцефалопатии отмечается редко и в основном происходит в раннем неонатальном периоде при участии других патологических факторов. Динамический контроль за показателями НБ в сыворотке крови и раннее назначение фенобарбитала, своевременное и адекватное проведение фототерапии позволяют эффективно снизить уровень билирубина и предупредить развитие энцефалопатии. С целью подтверждения диагноза возможно проведение молекулярно-генетического исследования.
. [141]
Следует помнить, что патологическая непрямая гипербилирубинемия может быть вторичной вследствие повышения реабсорбции билирубина в кишечнике может быть обусловлено обструкцией желудочно-кишечного тракта или кишечной непроходимостью при пилоростенозе, болезни Гиршпрунга, мекониальном илеусе, при парезах кишечника и др.. Исключение врожденных и приобретенных заболеваний желудочно-кишечного тракта должно входить в план дополнительного обследования ребенка с поздней или «затянувшейся» желтухой.
Профилактика
Принципы профилактики БЭ
В случаях выявления патологической гипербилирубинемии, первоочередные усилия медицинских работников должны быть направлены на предотвращение критических концентраций билирубина в крови, при которых вероятно развитие БЭ.
Медицинские мероприятия, направленные на профилактику БЭ, можно условно разделить на 4 этапа:
1. Клинико-анамнестический и клинико-лабораторный скрининг новорожденных детей на возможность развития или наличие патологической гипербилирубинемии (выявление группы риска).
2. Определение степени и выявление ведущего патогенетического механизма развития гипербилирубинемии.
3. Подготовка и проведение лечебных мероприятий, направленных на уменьшение концентрации непрямого билирубина в сыворотке крови:
— cоздание оптимальных условий медицинского ухода и, при необходимости, проведение интенсивной терапии основного и сопутствующих заболеваний;
— фототерапия (использование оптимальных режимов);
— в случаях недостаточной эффективности фототерапии, подготовка и проведение операции заменного переливания крови; при необходимости — создание дополнительных условий, повышающих эффективность ЗПК;
— клинико-лабораторный мониторинг безопасности и эффективности комплекса лечебных мероприятий (до момента полного их завершения)
4. Выявление или подтверждение конкретной причины развития непрямой гипербилирубинемии, потребовавшей медицинского вмешательства; при необходимости (в диагностически сложных случаях) — продолжение дифференциально-диагностических мероприятий и лечения основного и сопутствующего заболеваний.
Первые три этапа должны быть организованы в любой медицинской организации (МО) акушерско-гинекологического или педиатрического профиля, независимо от ее функционального уровня. Для организации 4 этапа может потребоваться перевод ребенка в учреждение 3 уровня (в Перинатальный центр или детскую многопрофильную или специализированную больницу).
Информация
Источники и литература
-
Клинические рекомендации Российского общества неонатологов
- 1. Brown AK, Kim MH, Wu PYK, et al. Efficacy of phototherapy in prevention and
management of neonatal hyperbilirubinemia. Pediatrics 1985;75:393.
2. Kaplan M, Hammerman C, Renbaum P, et al. Gilbert’s syndrome and
hyperbilirubinaemia in ABO-incompatible neonates. Lancet 2000;356:652.
3. Gomella TL, Cunningham MD Neonatology: Management, Procedures, On Call
Problems, Diseases, and Drugs. 7th Edition. 2013
4. Newman ТВ, Escobar GJ, Gonzales VM, et al. Frequency of neonatal bilirubin testing
and hyperbilirubinemia in a large health maintenance organization. Pediatrics 1999;
104:1198.
5. Bhutani VK, Johnson L, Sivieri EM. Predictive ability of a predischarge hour-specific
serum bilirubin for subsequent significant hyperbilirubinemia in healthy-term and nearterm
newborns. Pediatrics 1999; 103:6.
6. Maisels MJ, FanaroffAA Stevenson DK, et al. Serum bilirubin levels in an international,
multiracial newborn population. Pediatr Res 1999;45:167A.
7. Ryan AS, Wenjun MS, Acosta A Breastfeeding continues to increase into the new
millennium. Pediatrics 2002; 110:1103. 8. Cashore WJ, Gartner LM, Oh W, et al. Clinical application of neonatal bilirubin-binding
determinations: current status. J Pecfafr» 1978;83:827.
9. Keren R, Tremont K, Luan X, et al. Visual assessment of jaundice in term and late
preterm infants. Arch Dis Child Fetal Neonatal Ed 2009;94:F317.
10. Maisels MJ, Pathak A, Nelson NM, et al. Endogenous production of carbon monoxide in
normal and erythroblastotic newborn infants. J Clin Invest 1971 ;50:1.
11. Ahdab-Barmada M. The neuropathology of kernicterus: definitions and debate. In:
Maisels MJ, Watchko JF, eds. Neonatal jaundice. London, UK: Harwood Academic
Publishers, 2000:75.
12. Turkel SB. Autopsy findings associated with neonatal hyperbilirubinemia. Clin Perinatol
1990;17:381.
13. Volpe JJ. Bilirubin and brain injury. In: Volpe JJ. Neurology of the newborn. 5th ed.
Philadelphia, PA W.B. Saunders, 2008:619
14. Wennberg RP, Ahlfors CE, Bhutani V, et al. Toward understanding kernicterus: a
challenge to improve the management of jaundiced newborns. Pediatrics 2006; 117:474.
15. Bellarosa C, Muchova L, Vitek L, et al. Bilirubin metabolism and transport. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:55.
16. Hansen TWR, Bratlid D. Physiology of neonatal unconjugated hyperbilirubinemia. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:65
17. Kaplan M, Muraca M, Hammerman C, et al. Imbalance between production and
conjugation of bilirubin: a fundamental concept in the mechanism of neonatal jaundice.
Pediatrics 2002; 110(4).
18. Bhutani VK, Stark AR, Lazzeroni LC, et al. Predischarge screening for severe neonatal
hyperbilirubinemia identifies infants who need phototherapy. J.Pediatrics 1999;103:6–14.
19. Brodersen R. Binding of bilirubin to albumin. CRC Crit Rev Clin Lab Sci 1980; 11:305
20. Maisels MJ, Newman ТВ. The epidemiology of neonatal hyperbilirubinemia. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:97
21. Watchko JF, Lin Z. Genetics of neonatal jaundice. In: Stevenson DK, Maisels MJ,
Watchko JF, eds. Care ofthe jaundiced neonate. New York: McGraw Hill, 2012:1.
22. Engle WD, Jackson GL, Sendelbach D, et al. Assessment of a transcutaneous device in
the evaluation of neonatal hyperbilirubinemia in a primarily Hispanic population.
Pediatrics 2002; 110:61.
23. Bowman JM. The management of alloimmune fetal hemolytic disease. In: Maisels MJ,
Watchko JF, eds. Neonatal jaundice. London, UK: Harwood Academic Publishers,
2000:23.
24. Koenig JM. Evaluation and treatment of erythroblastosis fetalis in the neonate. In:
Christensen RD, ed. Hematologic problems ofthe neonate. Philadelphia, PA W.B.
Saunders Co., 2000:185.
25. Bowman JM. Immune hemolytic disease. In: Nathan DG, Orkin SH, eds. Hematology of
infancy and childhood, 5th ed. Philadelphia, PA: W.B. Saunders Company, 1998:54.
26. Bowman JM. RhD hemolytic disease of the newborn. N Engl J Med 1998;339:1775.
27. Rath MEA Smits-Wintjens VEHJ, Walther FJ, et al. Hematological morbidity and
management in neonates with hemolytic disease due to red cell alloimmunization. Early
Hum Dev 2011;87:583.
28. Ozolek J, Watchko J, Mimouni F. Prevalence and lack of clinical significance of blood
group incompatibility in mothers with blood type A or B. J Pediatry 994; 125:87. 29. Maisels MJ. Neonatal Jaundice. In: Sinclair JC, Bracken MB, eds. Effective care of the
newborn infant. Oxford, UK: Oxford University Press, 1992:507.
30. Newman ТВ, Liljestrand P, Escobar GJ. Jaundice noted in the first 24 hours after birth in
a managed care organization. Arch Pediatr Adolesc Med 2002; 156:1244.
31. Knudsen A. Prediction ofthe development of neonatal jaundice by increased umbilical
cord blood bilirubin. Acta Paediatr Scand 1989; 78:217.
32. Newman ТВ, Xiong B, Gonzales VM, et al. Prediction and prevention of extreme
neonatal hyperbilirubinemia in a mature health maintenance organization. Arch Pediatr
AdolescMed2000,IMA 140.
33. Maisels MJ, DeRidder JM, Kring EA, et al. Routine transcutaneous bilirubin
measurements combined with clinical risk factors improve the prediction of subsequent
hyperbilirubinemia. J Perinatol 2009; 29:612.
34. Yamauchi Y, Yamanouchi I. Difference in TcB readings between full term newborn
infants born vaginally and by cesarean section. Acta Paediatr Scand 1989;78:824.
35. Amato M, Fouchere JC, von Muralt G. Relationship between peri-intraventricular
hemorrhage and neonatal hyperbilirubinemia in very low birth weight infants. Am J
Perinatol 1987;4:275.
36. Silverman WA A difference in mortality rate and incidence of kernicterus among
premature infants allotted to two prophylactic antibacterial regimens. Pediatrics 1998;
102:225 (supplement).
37. Keren R, Luan X, Friedman S, et al. A comparison of alternative risk-assessment
strategies for predicting significant neonatal hyperbilirubinemia in term and near-term
infants. Pediatrics 2008; 121 :e170.
38. Bertini G, Dani C, Trochin M, etal. Is breastfeeding really favoring early neonatal
jaundice? Pediatrics 2001;107.
39. Yamauchi Y, Yamanouchi I. Breast-feeding frequency during the first 24 hours after
birth in full-term neonates. Pediatrics 1990;86:171.
40. Gartner U, Goeser T, Wolkoff AW. Effect of fasting on the uptake of bilirubin and
sulfobromophthalein by the isolated perfused rat liver. Gastroenterology 1997; 113:1707.
41. Maisels MJ, Kring EA. Length of stay, jaundice and hospital readmission. Pediatrics
1998; 101:995.
42. McDonald SJ, Middleton P. Effect of timing of umbilical cord clamping of term infants
on maternal and neonatal outcomes. Cochrane Database Syst Rev 2008;
16(2):CD004074.
43. Saigal S, O’Neill A, Surainder Y, et al. Placental transfusion and hyperbilirubinemia in
the premature. Pediatrics 1972;49:406.
44. Black VD, Lubchenco LO, Koops BL, et al. Neonatal hyperviscosity: randomized study
of effect of partial plasma exchange transfusion on longterm outcome. Pediatrics
1985;75:1048
45. Goldberg K, Wirth FH, Hathaway WE, et al. Neonatal hyperviscosity II. Effect of partial
plasma exchange transfusion. Pediatrics 1982;69:419.
46. Ultee CA, van der Deure J, Swart J, et al. Delayed cord clamping in preterm infants
delivered at 34-36 weeks’ gestation: a randomised controlled trial. Arch Dis Child Fetal
Neonatal Ed 2008;93(1 ):F20.
47. Frishberg Y, Zelicovic I, Merlob P, et al. Hyperbilirubinemia and influencing factors in
term infants. IsrJ Med Sci 1989;25:28.
48. Jahrig D, Jahrig K, Striet S, et al. Neonatal jaundice in infants of diabetic mothers. Acta
Paediatr Scand Suppl 1989;360:101. 49. Jahrig D, Jahrig K, Striet S, et al. Neonatal jaundice in infants of diabetic mothers. Acta
Paediatr Scand Suppl 1989;360:101.
50. Berk MA Mimouni F, Miodovnik M, et al. Macrosomia in infants of insulin-dependent
diabetic mothers. Pediatrics 1989;83:1029.
51. Chavalitdhamrong P-O, Escobedo MB, Barton LL, et al. Hyperbilirubinemia and
bacterial infection in the newborn. Arch Dis Child 1975;50:652.
52. Linder N, Yatsiv I, Tsur M, etal. Unexplained neonatal jaundice as an early diagnostic
sign ofsepticemia in the newborn. J Perinatol 1988;8:325.
53. Garcia FJ, Nager AL. Jaundice as an early diagnostic sign of urinary tract infection in
infancy. Pediatrics 2002; 109: 6.
54. Maisels MJ, Newman ТВ. Neonatal jaundice and urinary tract infections. Pediatrics
2003^ 12:1213.
55. Kaplan M, Hammerman C. Hemolytic disorders and their management. In: Stevenson
DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York: McGraw
Hill, 2012:145.
56. Kaplan M, Hammerman C. Glucose-6-phosphate dehydrogenase-deficient neonates: a
potential cause for concern in North America. Pediatrics 2000; 106:1478.
57. Kaplan M, Algur N, Hammerman C. Onset of jaundice in glucose-6-phosphate
dehydrogenase-deficient neonates. Pediatrics 2001; 108:956.
58. Kaplan M, Beutler E, Vreman HJ, et al. Neonatal hyperbilirubinemia in glucose-6-
phosphate dehydrogenase deficient heterozygotes. Pediatrics 1999; 104:68.
59. Kaplan M, Hammerman C, Renbaum P, et al. Differing pathogenesis of perinatal
bilirubinemia in glucose-6-phosphate dehydrogenase-deficient versus normal neonates.
Pediatr Res 2001;50:532.
60. Bender GJ, Cashore WJ, Oh W. Ontogeny of bilirubin-binding capacity and the effect of
clinical status in premature infants born at less than 1300 grams. Pediatrics
2007;’120:1067.
61. Ross ME, Waldron PE, Cashore WJ, et al. Hemolytic disease of the fetus and newborn.
In: de Alarcon PA, Werner EJ, Christensen RD, eds. Neonatal hematology, pathogenesis,
diagnosis, and management of hematologic problems, 2nd ed. Cambridge UK:
Cambridge University Press, 2013:65.
62. Gallagher PG. Disorders of erythrocyte metabolism and shape. In: Christensen RD, ed.
Hematologic problems of the neonate. Philadelphia, PA W.B. Saunders Co, 2000:209.
63. Christensen RD, Henry E. Hereditary spherocytosis in neonates with hyperbilirubinemia.
Pediatrics 2010; 125:120.
64. Black VD, Lubchenco LO, Luckey DW, et al. Developmental and neurologic sequelae in
the neonatal hyperviscosity syndrome. Pediatrics 1982;69:426.
65. Watchko JF, Daood MJ, Biniwale M. Understanding neonatal hyperbilirubinaemia in the
era of genomics. Semin Neonatol 2002;7:143.
66. Kaplan M, Hammerman C, Maisels MJ. Bilirubin genetics for the nongeneticist:
hereditary defects of neonatal bilirubin conjugation. Pediatrics 2003; 111:886.
67. Job H, Hart G, Lealman G. Improvements in long term phototherapy for patients with
Crigler-Najjar syndrome type I. Phys Med Biol 1996;41 (11 ):2549.
68. Fox IJ, Roy-Chowdhury J, Kaufman SS, et al. Treatment of the Crigler-Najjar syndrome
type I with hepatocyte transplantation. N Engl J Med 1998;338:1422.
69. Vaz AR, Delgado-Esteban M, Brito MA, et al. Bilirubin selectively inhibits cytochrome с
oxidase activity and induces apoptosis in immature cortical neurons: assessment of the
protective effects of glycoursodeoxycholic acid. J Neurochem 2010; 112:56.
70. Wennberg RP. Cellular basis of bilirubin toxicity. NY State J Med 1991 ;91:493
- 1. Brown AK, Kim MH, Wu PYK, et al. Efficacy of phototherapy in prevention and
Информация
Коллектив авторов
Список сокращений
БЭ -билирубиновая энцефалопатия
Г-6-ФДГ — глюкозо-6-фосфат дегигдрогеназа
ГБН — гемолитическая болезнь новорожденных
КОС — кислотно-основное состояние
МКБ-10 — международная классификация болезней -10
ОБ — общий билирубин
ОБС — общий билирубин сыворотки
ОЗПК — операция заменного переливания крови
ОРИТН — отделение реанимации и интенсивной терапии новорожденных
ФТ — фототерапия
TcBr — билирубин, измеренный чрезкожно (транскутанно)
Методология
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кохрановскую библиотеку, базы данных MEDLINE и EMBASE по состоянию на 1 сентября 2016 г.
Глубина поиска составляла 60 лет.
Методы, использованные для оценки качества и силы доказательств:
Консенсус экспертов;
Оценка значимости в соответствии с рейтинговой схемой (схема прилагается)
Рейтинговая схема для оценки силы рекомендаций представлена в таблице 1.
Таблица 1 — Уровни доказательности
Методы, использованные для формулирования рекомендаций:
консенсус экспертов.
Рейтинговая схема оценки силы рекомендаций представлена в таблице 2.
Таблица 2 – Рейтинговая схема оценки силы рекомендаций
Индикаторы доброкачественной практики (GoodPracticePoints – GPPs):
рекомендуемая доброкачественная практика базируется на клиническом опыте рабочей группы по разработке рекомендаций.
анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Методы валидизации рекомендаций:
Внешняя экспертная оценка;
Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами.
Получены комментарии со стороны врачей неонатологов из нескольких регионов первого и второго этапов выхаживания новорожденных детей (гг. Москва, Екатеринбург, Калужская область, Республика Карелия, Хабаровский край и др.) в отношении доступности, доходчивости и возможности применения рекомендаций в повседневной практике.
Все комментарии, полученные от экспертов, анализировались председателем и членами рабочей группы, вносились изменения с учетом рекомендаций.
Консультация и экспертная оценка
Предварительная версия была размещена для обсуждения на сайте http://neonatologynmo.geotar.ru, для того, чтобы широкий круг лиц имел возможность принять участие в обсуждении и совершенствовании рекомендаций.
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Силы рекомендаций (A-D), уровни доказательств (1++, 1+, 1-, 2++, 2+, 2-, 3, 4) и индикаторы доброкачественной практики — goodpracticepoints (GPPs) приводятся в ходе изложения текста рекомендаций.
Заключение.
Непрямая гипербилирубинемия является одним из наиболее частых транзиторных и патологических состояний, требующих повышенного внимание врачей- неонатолов и педиатров. Подробное описание этиологии и патогенеза желтух новорожденных, а также принципов дифференциальной диагностики и лечения, представлено в медицинских учебниках и врачебных руководствах наших великих учителей и наставников – В.А.Таболина, Г.М.Савельевой, Н.П.Шабалова, Н.Н.Володина, Сидельниковой В.М. А.Г.Антонова, Г.В.Яцык [142-147].
Представленные клинические рекомендации, основанные на последних достижениях перинатальной медицины, направлены в первую очередь на достижение двух основных целей: 1) повышение эффективности предупреждения билирубиновой энцефвалопатии у доношенных и недоношенных новорожденных детей; 2) уменьшение числа инвазивных и потенциально опасных медицинских вмешательств у новорожденных детей, сокращение необоснованных госпитализаций новорожденных.
Члены рабочей группы будут признательны за любые конструктивные замечания и предложения, направленные на совершенствование подходов к профилактике и лечению патологических непрямых гипербилирубинемий у новорожденных.
Электронная версия данного документа доступна на сайте Российского общества неонатологов (РОН) – www. neonatology.pro
Прикреплённые файлы
Мобильное приложение «MedElement»
Версия: Клинические рекомендации РФ 2013-2017 (Россия)
Категории МКБ:
Неонатальная желтуха вследствие других и неуточненных повреждений клеток печени (P59.2), Неонатальная желтуха неуточненная (P59.9), Неонатальная желтуха, обусловленная другими уточненными причинами (P59.8), Неонатальная желтуха, связанная с преждевременным родоразрешением (P59.0), Синдром сгущения желчи (P59.1)
Разделы медицины:
Неонатология, Педиатрия
Общая информация
Краткое описание
Российское общество неонатологов
Тактика ведения доношенных и недоношенных новорожденных детей с непрямой гипербилирубинемией
2016
Определения.
Гипербилирубинеми́я (греч. hyper- + Билирубин + греч. haima кровь). В клинической лабораторной практике под термином гипербилирубинемия понимают любое увеличение концентрации билирубина в сыворотке или плазме крови сверх нормативных значений.
Учитывая существенные отличия нормативных значений билирубина у детей периода новорожденности от других возрастных групп, а также необходимость профилактики и лечения гипербилирубинемии у детей различного гестационного возраста, в неонатологии термином гипербилирубинемия обозначают состояния, при которых у доношенных и поздних недоношенных ГВ 35-36 недель отмечается повышение концентрации общего билирубина в сыворотке крови более 256 мкмоль/л, а у детей, родившихся до 35 недели гестации — повышение концентрации общего билирубина более 171 мкмоль/л (Уровень доказательности – B) [1,2,3].
Международные исследования, проведенные в начале 2000-х годов показали, что 95% перцентиль концентрации общего билирубина в сыворотке крови у доношенных детей в возрасте 96 ± 6,5 часов находился в диапазоне от 265 до 299 мкмоль/л(Уровень доказательности – B) [4,5,6]. Более высокие показатели были характерны для детей, получавших исключительно грудное вскармливание [7]. Однако, с учетом того, что в многоцентровые лабораторные исследования были включены дети, потребовавшие госпитализации для проведения фототерапии, критерии гипербилирубинемии, традиционно принятые в неонатологии, остались неизменными.
Термин «непрямая гипербилирубинемия» используют в тех случаях, когда это повышение обусловлено преимущественно (более чем на 80%) непрямой фракцией билирубина (Уровень доказательности – D) [8].
Желтуха — визуальное проявление повышенного уровня билирубина в крови. У доношенных новорожденных появляется при уровне билирубина более 67 мкмоль/л; у недоношенных — более 120 мкмоль/л (Уровень доказательности – C) [9].
Повышение концентрации билирубина в крови у новорожденных детей и развитие желтухи может быть вызвано как физиологическими, так и патологическими причинами. К раннему появлению, прогрессирующему нарастанию и высокой интенсивности желтухи следует относится как к симптомам потенциально опасного заболевания (Уровень доказательности – D) [8, 10, 11, 12, 13, 14].
Коды по МКБ-10
Р 59 Неонатальная желтуха, обусловленная другими и неуточненными причинами
Р 59.0 Неонатальная желтуха, связанная с преждевременным родоразрешением
Р 59.1 Синдром сгущения желчи
Р 59.2 Неонатальная желтуха, вследствие других и неуточненных повреждений клеток печени
Р 59.8 Неонатальная желтуха, обусловленная другими уточненными причинами
Р 59.9 Неонатальная желтуха неуточненная
Этиология и патогенез
Физиологическая желтуха
Основными физиологическими причинами повышения концентрации билирубина в сыворотке крови у детей в первые дни жизни являются следующие (Уровень доказательности – D) [15, 16,17 ].
— более высокая скорость образования билирубина, обусловленная физиологической полицитемией и более короткой продолжительностью жизни эритроцитов, содержащих фетальный гемоглобин (70–90 дней, по сравнению со 110–120 днями у взрослых);
— функционирующий венозный проток и уменьшенная перфузия крови в пространства Диссе препятствует полноценному захвату билирубина гепатоцитами;
-сниженная активность фермента глюкуронилтрансферазы (ГТФ), обеспечивающей конъюгацию билирубина, и недостаточная концентрация У-протеина, обеспечивающего транспорт билирубина в гепатоцитах;
— исходно низкая экскреторная функция печени (1–2% от экскреторной способности печени взрослого);
— усиленная реабсорбция билирубина из тонкого кишечника вследствие высвобождения билирубина из химической связи с глюкуроновой кислотой под влиянием повышенной активности фермента бета-глюкоронидазы.
Желтуха на первой неделе жизни регистрируется у 60-80% здоровых доношенных новорожденных детей (Уровень доказательности – A) [9, 17, 18].
Для физиологической желтухи характерно:
— Удовлетворительное состояние ребенка
— Нормальные пальпаторные размеры печени и отсутствие признаков увеличения селезенки;
— Отсутствие клинико-лабораторных признаков анемии или полицитемии;
— Появление желтой окраски кожи в возрасте более 24 час жизни (при этом почасовой прирост билирубина в первые сутки составляет менее 3,4 мкмоль/л, суммарно за первые сутки — менее 85,5 мкмоль/л);
— Максимальная выраженность желтой окраски лица, туловища и конечностей на 3-4 сутки жизни; желтуха не распространяется на ладони и стопы;
— Не наблюдается патологических оттенков желтой окраски кожи (серого, зеленоватого, лимонного);
— Нормальная, соответственно возрасту, окраска стула;
— Максимальная концентрация общего билирубина не более 255 мкмоль/л; концентрация прямой фракции билирубина – не выше 34 мкмоль/л;
— Быстрое уменьшение интенсивности и распространенности желтухи после 4 суток жизни; угасание желтухи к 8-10 суткам жизни.
Примерно в половине случаев при физиологическом течении желтухи к 3-4 стукам возникает кратковременная непрямая гипербилирубинемия, которая не имеет негативных клинических последствий и не требует никаких медицинских вмешательств (Уровень доказательности – D) [16 , 19].
Понятие физиологическая желтуха применимо только по отношению к доношенным и «поздним» недоношенным (ГВ 35-36 нед) новорожденным (Уровень доказательности – D) [16].
Непрямая гипербилирубинемия, вызванная патологическими причинами
Несоответствие хотя бы по одному из типичных для физиологической желтухи клинических и лабораторных признаков с высокой вероятностью свидетельствует о том, что нарушение обмена билирубина вызвано патологическими причинами.
Факторы, предрасполагающие к развитию патологической гипербилирубинемии у доношенных новорожденных B:
Восточно-азиатское или средиземноморское происхождение (Уровень доказательности – B) [20, 21, 22]
Несовместимость по АВО- или резус-фактору матери и плода (Уровень доказательности – B) [23, 24, 25, 26, 27, 28]
Использование окситоцина в родах(Уровень доказательности – D) [29]
Желтуха, развившаяся в первые сутки (24 часа) жизни (Уровень доказательности – B) [30, 31, 32, 33]
Кефалогематома/экхимозы, крупные гемангиомы (Уровень доказательности – B) [20, 34, 35, 36]
Гипогалактия при исключительно грудном вскармливании (Уровень доказательности – C) [20, 37, 38, 39]
Нарушенное сосание/недостаточное питание (Уровень доказательности – C) [40]
Эксикоз (патологическая убыль массы тела) (Уровень доказательности – B) [37,41]
Полицитемия (Уровень доказательности – A) (40, 42, 43, 44, 45, 46, 47, 48, 49, 50)
Врожденные и перинатальные инфекции (Уровень доказательности – B) [51, 52, 53, 54]
Дефицит глюкозо-6-фосфат дегидрогеназы (Уровень доказательности – B) ]55 , 56, 57, 58, 59]
Практически всегда гипербилирубинемия у недоношенных детей, родившихся ранее 35 недели гестации, обусловлена нефизиологическими причинами.
В свою очередь, в большинстве случаев патологической гипербилирубинемии, возникающей на первой неделе жизни, отмечается преимущественное повышение в крови непрямой фракции билирубина (Уровень доказательности – C) [60].
По ведущим патогенетическим механизмам все случаи непрямой гипербилирубинемии у новорожденных можно разделить на четыре группы: 1) обусловленные увеличением скорости продукции билирубина, 2) обусловленные замедлением конъюгации билирубина в печени 3) обусловленные повышением реабсорбции билирубина из кишечника 4) обусловленные комбинированным действием вышеперечисленных факторов. Наиболее вероятные причины, приводящие к непрямой патологической гипербилирубинемии у новорожденных детей, с учетом ведущих патогенетических механизмов перечислены в таблице 3 (Уровень доказательности – C) [23, 24, 25, 26, 35, 42, 43, 44, 45, 47, 48, 49, 50, 51, 52, 56, 59, 61, 62, 63, 64, 65, 66, 67, 68] .
Таблица 3. Основные причины непрямой патологической гипербилирубинемии у новорожденных детей
Ведущие патогенетические механизмы развития гипербилирубинемии во многом определяют время возникновения и степень выраженности гипербилирубинемии. Раннее распознавание конкретной причины нарушений билирубинового обмена позволяет не только прогнозировать течение желтухи, но и эффективно предупреждать осложнения, ассоциированные с гипербилирубинемией (Уровень доказательности – C) [32, 37].
Во всех случаях развития непрямой (патологической) гипербилирубинемии, обусловленных гиперпродукцией билирубина, и в части случаев, обусловленных нарушением конъюгации и реабсорбции билирубина, существует риск развития метаболического поражения ЦНС за счет потенциальной нейротоксичности неконъюгированного билирубина (Уровень доказательности – C) [11, 12, 13, 16, 69]
Билирубиновая энцефалопатия (Код по МКБ-10 – Р57)
Нарушение структуры и функции головного мозга, обусловленное непрямой гипербилирубинемией, носит название билирубиновой энцефалопатии (БЭ) или ядерной желтухи. При использовании современных перинатальных технологий БЭ является предотвратимым состоянием (Уровень доказательности – D) [70].
Согласно литературным данным, накопленным в эру, предшествующую внедрению современных протоколов профилактики и лечения патологической гипербилирубинемии, билирубиновая энцефалопатия (БЭ) у доношенных новорожденных развивается в случаях превышения концентрации общего билирубина сыворотки крови порога в 342 мкмоль/л с выраженными индивидуальными различиями концентраций (от 342 до 684 мкмоль/л), при которых происходит метаболическое поражение головного мозга (Уровень доказательности – B) [71, 72, 73, 74].
В последние два деятилетия частота билирубиновой энцефалопатии в различных странах мира находится в диапазоне 0.4/100, 000 до 2.7/100,000 [75] B.
Вероятность развития билирубиновой энцефалопатии при патологической гипербилирубинемии повышается на фоне следующих факторов риска (B):
недоношенность или морфо-функциональная незрелость организма ребенка (Уровень доказательности – B) [ 41, 74, 75, 76, 77]
тяжелая врожденная и неонатальная инфекция (сепсис, менингит) (Уровень доказательности – B) [51, 52, 53, 54]
гемолитическая болезнь новорожденого (Уровень доказательности – B) [23, 24, 25, 25, 26,27 ]
дефицит Г-6-ФДГ (Уровень доказательности – C) [80]
гипоальбуминемия (концентрация сывороточного альбумина менее 25 г/л) (Уровень доказательности – C) [79].
выраженный метаболический ацидоз (pH артериальной крови менее 7,15 более 1 часа) (Уровень доказательности – C) [79]
тяжелая асфиксия новорожденного (оценка по Апгар менее 4 баллов), артериальная гипотензия, апноэ, потребность в ИВЛ (Уровень доказательности – C) [79]
гипотермия (ректальная температура менее 35 (С) (Уровень доказательности – C) [78]
обширная травма мягких тканей в родах, массивные кефалогематомы, перивентрикулярные, внутрижелудочковые и субарахноидальные кровоизлияния (Уровень доказательности – C) [20, 34, 35]
синдром полицитемии (Уровень доказательности – B) [42, 43, 44, 45, 46 , 47, 49, 50, 64]
задержка отхождения мекония (Уровень доказательности – C) [78]
мужской пол (Уровень доказательности – C) [32, 33]
Следует помнить, что ряд препаратов (в первую очередь антибиотиков), используемых в практике врача неонатолога могут вытеснять билирубин из связи с альбумином. Так, коэффициент вытеснения для цефазолина (антибитик, цефалоспорин 1-го поколения) составляет 1.17, для цефметазола (цефалоспорин 2-го поколения) – 2.0 , а для цефтриаксона (цефалоспорин 3-го поколения пролонгированного действия ) – 3.0 (Уровень доказательности – C) [8].
У недоношенных детей вероятность билирубинового поражения ЦНС развивается при более низких концентрациях билирубина, чем у доношенных новорожденных, и зависит от концентрации билирубина в крови и массы тела ребенка при рождении.
У детей, родившихся с очень низкой и экстремально низкой массой тела (ОНМТ и ЭНМТ), БЭ может возникнуть даже после умеренного повышения концентрации общего билирубина в сыворотке крови (в диапазоне 171-255 мкмоль/л) (Уровень доказательности – B) [76,82, 83, 84, 85, 86, 87].
Несмотря на попытки разработки и внедрения лабораторных методов, прогнозирования индивидуальной чувствительности мозга к билирубину, в повседневной неонатологической практике при определении риска развития БЭ ориентируются на минимальные пороговые концентрации билирубина в сыворотке крови, при которых в прошлом регистрировались случаи развития ядерной желтухи. [71 73 75, 76, 82, 83, 85]. В течении билирубиновой энцефалопатии можно условно выделить 4 фазы [85]:
I.Нарастание признаков билирубиновой интоксикации: угнетение безусловно-рефлекторной деятельности – апное, апатия, вялость, сонливость, плохо сосут, может быть монотонный крик, срыгивания, рвота, “блуждающий взгляд”. При неблагоприятном течении гемолитической болезни новорожденного эти признаки в большинстве случаев появлялись на 4 день жизни и, в случаях экстренного проведения ОЗПК, носили обратимый характер (Уровень доказательности – A) [13, 86].
II.Спастическая. При неэффективном лечении появляются классические признаки ядерной желтухи: спастичность, ригидность затылочных мышц, вынужденное положение тела с опистотонусом, “негнущимися” конечностями и сжатыми в кулак кистями; периодическое возбуждение и резкий мозговой крик, выбухание большого родничка, подергивание мышц лица, крупноразмашистый тремор рук, исчезновение рефлекса Моро и видимой реакции на сильный звук, сосательного рефлекса; нистагм, апноэ, брадикардия, летаргия, иногда повышение температуры; судороги, симптом заходящего солнца. Эта фаза имеет продолжительность от нескольких дней до нескольких недель; поражение ЦНС носит необратимый характер.
III. Фаза ложного неврологического благополучия и полного или частичного исчезновения спастичности (2-3 месяц жизни);
IY.Период формирования клинической картины неврологических осложнений (после 3-5 месяца жизни): параличи, парезы, атетоз, хореоатетоз, глухота, ДЦП, задержка психического развития, дизартрия (Уровень доказательности – B) [32, 37, 41, 46, 88].
Первые две фазы заболевания являются признаком острого метаболического поражения ЦНС и обозначаются термином острая билирубиновая энцефалопатия (ОБМ). Отдаленные неврологические нарушения, вызванные нейротоксическим действием билирубина (4 фаза), обозначаются термином хроническая билирубиновая энцефалопатия (ХБЭ) [13, 89, 90].
Развитие классических признаков ОБЭ в случаях непрямой гипербилирубинемии характерно для доношенных и поздних недоношенных (ГВ 34-36 недель) новорожденных детей (Уровень доказательности – A) [13, 89, 91]. У глубоконедоношенных детей при надпороговых значениях гипербилирубинемии характерные клинические признаки ОБЭ могут отсутствовать или маскироваться симптомами других патологических состояний, но во втором полугодии жизни у них появляются типичные признаки ХБЭ (Уровень доказательности – D) [82, 92].
С целью раннего выявления, оценки динамики и определения тяжести билирубиновой энцефалопатии у новорожденных детей Jonson L.,Bhutani V.K., Karp K. et al. была предложена бальная шкала, позволяющая учитывать степень выраженности неврологических дисфункций, характеризующих ОБЭ (таблица 4) [93, 94].
Таблица 4. Бальная оценка тяжести клинических проявлений билирубиновой энцефалопатии у новорожденных детей в остром периоде
Интерпретация результатов:
1-3 балла – минимальная,
4-6 баллов – умеренная,
7-9 баллов – тяжелая
Диагностика
Клинико-анамнестический и клинико-лабораторный скрининг новорожденных детей на возможность развития или наличие патологической гипербилирубинемии
Клинико-анамнестические данные.
В группу высокого риска по развитию непрямой гипербилирубинемии сразу после рождения должны быть выделены:
новорожденные, с клиническими и/или лабораторными признаками гемолитической болезни
новорожденные с выраженными признаками морфофункциональной незрелости, в т.ч. глубоконедоношенные дети
новорожденные с множественными подкожными кровоизлияниями и обширными кефалогематомами
новорожденные, нуждающиеся в проведении реанимационной и интенсивной терапии в раннем неонатальном периоде, включая детей с врожденными инфекциями и неонатальным сепсисом
новорожденные с высоким риском раннего проявления болезней обмена или наследственных гемолитических анемий (отягощенный семейный анамнез или наличие соответствующих лабораторных признаков)
наличие в семье других детей с выраженной гипербилирубинемией, требующей лечения в неонатальном периоде
Визуальное наблюдение за временем появления и интенсивностью нарастания желтухи.
Исторически сложилось, что с целью раннего выявления гипербилирубинемии многие неонатологи ориентируются в первую очередь на изменение цвета кожных покровов [95, 96]. Безусловно, раннее появление желтухи (до 24 часов жизни), нарастание после 4 суток и сохранение более 2 недель свидетельствуют о наличии патологических причин для развития гипербилирубинемии. При этом практически всегда появление желтухи в первые 24 часа свидетельствует о гиперпродукции билирубина, вызванного патологическим гемолизом эритроцитов, а нарастание желтухи после 4 суток жизни с высокой вероятностью указывает на нарушение конъюгации билирубина в печени и его недостаточной экскреции (Уровень доказательности – B) [30, 97].
Дополнительную информацию о патологической природе желтухи может иметь появление на ее фоне лимонного (типично для ГБН), зеленоватого (типично для холестаза) или сероватого (типично для сепсиса) оттенка кожи.
Первоначально желтый цвет приобретает кожа лица и туловища ребенка. Дальнейшее нарастание концентрации билирубина, независимо от причины, приводит к распространению желтухи и окрашиванию кожи конечностей. Увеличение концентрации билирубина более 255-306 мкмоль/л сопровождается прокрашиванием ладоней и стоп (Уровень доказательности – C) [95, 98].
Основываясь на этой закономерности, Kramer L.I. в 1969 году предложил выделять 5 степеней выраженности желтухи новорожденных, каждой из которых соответствует свой диапазон концентрации билирубина в сыворотке крови (рис 1.) [98]. В настоящее время эксперты РОН считают, что клиническая оценка степени выраженности желтухи на основе шкалы Крамера остаточно субъективна и требует подтверждения наличия гипербилирубинемии инструментальными и лабораторными методами. Шкала Крамера может быть использована для определения необходимости забора крови на биохимический анализ билирубина у доношенных новорожденных в тех медицинских организациях, в которых отсутствуют аппараты для чрезкожного определения билирубина (Уровень доказательности – D).
Клиническая оценка распространенности желтухи у новорожденных по Крамеру (Kramer LI).
При использовании шкалы Крамера с целью определения показаний к биохимическому исследованию крови на билирубин у доношенных новорожденных следует помнить, что однократная оценка по Крамеру в большинстве случаев не позволяет дифференцировать физиологическую и патологическую гипербилирубинемию. С этой точки зрение описание во врачебных дневниках желтухи с указанием кожных зон, предложенных Крамером, помогает более точно определить показания для исследований крови. Желтое окрашивание 2 и 3 зон не позволяет исключить или подтвердить гипербилирубинемию, распространение желтухи на 4 и 5 кожные зоны практически всегда свидетельствует о наличии гипербилирубинемии, но не позволяет объективно оценивать вероятность развития БЭ. Таким образом, распространение желтухи на 4 и 5 зоны по Крамеру у доношенного новорожденного ребенка должно рассматриваться как показание к биохимическому исследованию крови. Вместе с тем, при ранней выписке новорожденных из акушерского стационара такой подход не позволяет прогнозировать нарастание желтухи после 3-х суток. Кроме того, шкалу Крамера нельзя применять у недоношенных и новорожденных с дефицитом массы тела. Шкала Крамера не может быть использована для оценки эффективности фототерапии (D).
Все вышеизложенное подчеркивает существенное ограничение возможностей использования визуальной оценки степени желтухи для скрининга детей, составляющих группу риска по развитию БЭ (Уровень доказательности – A) [99, 100].
Чрезкожное измерение уровня билирубина у новорожденных детей
Более объективным методом оценки скорости и степени накопления билирубина в коже ребенка, чем визуальная оценка, является чрескожное измерение отраженного от кожи и подкожных тканей света с помощью специальных приборов (Уровень доказательности – B) [101, 102].
В настоящее время для чрезкожного измерения уровня билирубина у новорожденных в Российской Федерации используются приборы как отечественного, так и зарубежного производства (Билитест, производство «Техномедика», Россия; JM-103, производство Dräger, Германия; BiliCheck, производство «Philips», Нидерланды и др.). Использование каждого из вышеперечисленных приборов имеет свои особенности, поэтому проведение чрезкожного измерения билирубина должно выполняться в строгом соответствии с инструкцией по эксплуатации [102].
Общим для всех приборов является то, что в диапазоне концентраций общего билирубина от 100 до 255 мкмоль/л отмечается прямая линейная зависимость между показателями содержания билирубина в коже и сыворотке крови у доношенных и недоношенных новорожденных ГВ более 35 недель. При определении чрезкожными анализаторами концентраций билирубина более 255 мкмоль/л линейная зависимость между содержанием билирубина в коже и сыворотке крови уменьшается, что требует перепроверки уровня билирубинемии стандартными лабораторными методами (Уровень доказательности – B) [33, 103, 104, 105].
Особенности и ограничения чрезкожного измерения уровня билирубина, независящие от конструкции прибора: [5, 105, 106, 107, 108, 109, 110]:
Исследование уровня билирубина чрезкожным методом показано всем доношенным новорожденным с желтухой, независимо от степени ее выраженности
Измерение уровня билирубина должно проводиться только в области лба и/или грудины. Для определения показаний к повторному измерению или срочному определению концентрации билирубина в крови стандартными лабораторными методами могут быть использованы процентильные кривые Bhutani VK
Следует помнить, данный метод измерения билирубина не может быть использован после начала фототерапии (Уровень доказательности – B) [111].
Процентильные кривые уровня билирубина крови, измеренного чрезкожным методом у доношенных и поздних недоношенных детей (ГВ 35-37 нед), предназначенные для определения степени риска развития патологической гипербилирубинемии, представлены на рисунке 2 [102].
Рис 2. Процентильные кривые уровня билирубина крови, измеренного чрезкожным методом у доношенных и поздних недоношенных детей (ГВ 35-37 нед) (Bhutani VK и соавт, 1999)
При ранней выписке новорожденного из акушерского стационара целесообразно воспользоваться алгоритмом, представленном на рис 3 (мнение экспертов РОН, уровень доказательности – D).
Рациональное использование приборов для чрезкожного измерения билирубина у новорожденных детей в условиях акушерского стационара позволяет: 1) уменьшить неоправданно широкое использование забора крови на билирубин у доношенных новорожденных; 2) более объективно выделять среди клинически здоровых новорожденных группу риска по развитию непрямой патологической гипербилирубинемии; 3) предотвращать раннюю выписку домой новорожденных, у которых имеется потенциальный риск отсроченного развития БЭ (Уровень доказательности – B)[14,18,97,99,101].
Рис 3. Алгоритм использования чрезкожного измерения билирубина при ранней выписке новорожденного из акушерского стационара
Таким образом, рациональное использование приборов для чрезкожного измерения билирубина у новорожденных детей в условиях акушерского стационара позволяет: 1) уменьшить неоправданно широкое использование забора крови на билирубин у доношенных новорожденных; 2) более объективно выделять среди клинически здоровых новорожденных группу риска по развитию непрямой патологической гипербилирубинемии; 3) предотвращать раннюю выписку домой новорожденных, у которых имеется потенциальный риск отсроченного развития БЭ.
Особенности использования приборов для чрезкожного измерения билирубина у недоношенных детей
Несмотря на то, что в последнее десятилетие опубликован ряд научно-исследовательских работ, продемонстрировавших перспективность использования метода у недоношенных детей ГВ 28-34 недели (C), к настоящему времени не накоплено достаточного количества клинических данных, позволяющих рекомендовать рутинное чрезкожное измерение билирубина у недоношенных детей, за исключением группы поздних недоношенных ГВ более 35 недель. При этом подходы к использованию метода практически ничем не отличаются от описанных выше для доношенных новорожденных (Уровень доказательности – A) [102, 104,106, 107, 112].
Лабораторные методы измерения концентрации билирубина в крови у новорожденных детей
Своевременное измерение концентрации билирубина в крови у новорожденных детей имеет ключевое значение для определения медицинской тактики ведения при подозрении на патологическую желтуху. Несмотря на то, что нейротоксическим эффектом обладает в основном непрямая фракция билирубина, лечебная стратегия на первой недели жизни, независимо от причины и характера развития желтухи, строится исходя из абсолютных значений общего билирубина в крови, а не его отдельных фракций.
Стандартное лабораторное исследование концентрации билирубина в крови показано (Уровень доказательности – A) [ 97, 100]:
— Всем недоношенным детям ГВ менее 35 недель с желтухой
— Всем новорожденным, у которых желтуха появилась в первые 24 часа
— Новорожденным с признаками ГБН или другими известными факторами риска развития патологический желтухи
— Доношенным и поздним недоношенным детям, если уровень билирубина, определенный транскутанным методом, составил:
более 140 мкмоль/л в возрасте 24-48 часов
более 200 мкмоль/л в возрасте 48-72 часов
более 250 мкмоль/л в возрасте старше 72 часов.
— Всем детям, получающим фототерапию (с интервалом 12-24 в сутки)
Особенности лабораторного определения билирубина в крови
В настоящее время для определения уровня общего билирубина в плазме или сыворотке крови применяются разнообразные лабораторные методы. В большинстве случаев измерение концентрации билирубина в крови выполняют либо биохимическими методами (в основном с диазокрасителями), либо методами прямого фотометрирования плазмы (с разведением или без разведения) [96, 112]
С целью уменьшения объема исследуемой крови внедрено измерение оптической плотности плазмы капиллярной крови (так называемый «микрометод»), забор крови производится в стеклянный капилляр без дозирования, внутренний объем которого составляет примерно 30 мкл [113]. Плазма для фотометрирования получается непосредственно в капилляре на любой гематокритной центрифуге. Недостатком метода является невозможность определить фракции билирубина, а также существенное снижение точности измерения при выраженном гемолизе. Данный метод может использоваться для скрининга детей группы риска в случаях, когда невозможно использовать приборы для чрезкожного определения, с целью снижение частоты забора большего объема крови на стандартное биохимическое исследование. Однако он не может заменять стандартный биохимический метод при выборе и обосновании методов интенсивной терапии непрямой (патологической) гипербилирубинемии. Его можно рассматривать в качестве вспомогательного метода лабораторного контроля за эффективностью фототерапии у детей (преимущественно недоношенных) с концентрацией билирубина в крови менее 280 мкмоль/л. Однако, в случаях, когда определяются более высокие концентрации и при любых формах гемолитической болезни новорожденного, лабораторный контроль за эффективностью лечения должен осуществляться стандартными биохимическими методами определения билирубина в сыворотке крови. (Уровень 4)
Сопоставление точности измерения общего билирубина плазмы капиллярной крови портативными анализаторами и автоматическими биохимическими анализаторами, в которых используется биохимический метод Йендрашика, свидетельствуют о сопоставимости результатов до достижения максимальной концентрации билирубина в крови 280 мкмоль/л. Для точного определения более высоких концентраций или проверки спорных результатов исследования (например, при явном несоответствии между клинической картиной и концентрации билирубина в крови, измеренной путем прямой фотометрии) должно проводится стандартное биохимические исследование с диазокрасителями (Уровень доказательности – D).
Клинико-лабораторные характеристики основных патологических причин непрямой гипербилирубинемии [23, 24, 25, 28, 51, 52, 55, 63,114, 115, 116, 117,].
Гипербилирубинемия, обусловленная избыточным гемолизом эритроцитов.
Повышенное образование билирубина вследствие гемолиза эритроцитов может быть обусловлено иммунным конфликтом между эритроцитами матери и плода, наследственными нарушениями структуры или функции эритроцитов, гемоглобинопатиями, ятрогенными факторами (лекарственный гемолиз — высокие дозы викасола), рядом инфекционных заболеваний (врожденные инфекции – цитомегалия, герпес, краснуха, токсоплазмоз, листериоз, сифилис; неонатальный сепсис)
Наиболее опасной, с точки зрения развития билирубиновой энцефалопатии, причиной гипербилирубинемии является гемолитическая болезнь новорожденных (ГБН).
Клинические формы ГБН подробно описаны в соответствующем протоколе.
Лабораторные критерии ГБН
• концентрация билирубина в пуповинной крови (в момент рождения) – при легких формах иммунологического конфликта по Rh и во всех случаях AB0- несовместимости ≤ 51 мкмоль/л; при тяжелых формах иммунологического конфликта по Rh и редким факторам – существенно выше 51 мкмоль/л;
• концентрация гемоглобина в пуповинной крови в легких случаях – на нижней границе нормы, в тяжелых – существенно снижена;
• почасовой прирост билирубина в первые сутки жизни больше 5,1 мкмоль/л/час;
• максимальная концентрация общего билирубина на 3–4 сутки в периферической или венозной крови у доношенных новорожденных; при отечной и желтушной формах она существенно выше 256 мкмоль/л;
• общий билирубин крови повышается преимущественно за счет непрямой фракции,
• относительная доля прямой фракции (при условии отсутствия холестатических осложнений) составляет менее 20%,
• снижение концентрации гемоглобина, уменьшение количества эритроцитов и повышение количества ретикулоцитов в периферической и венозной крови в течение 1 недели жизни.
Для наследственных гемолитических желтух (обусловленная дефицитом Г-6-Ф-ДГГ, серповидно-клеточная анемия, наследственный микросфероцитоз и др.) характерно отсроченное (после 24 ч жизни), появление признаков гемолиза, а также изменение формы и размеров эритроцитов при морфологическом исследовании мазка крови, нарушение их осмотической стойкости .
Несмотря на отличия в патогенезе, сходными клиническими и лабораторными признаками сопровождаются гипербилирубинемии, обусловленные полицетемией/повышенной вязкостью крови, а также повышенным экстравазальным образованием билирубина (при множественных и обширных экхимозах, больших кефалогематомах и др.).
Гипербилирубинемия, обусловленная нарушением конъюгации билирубина (конъюгационные желтухи).
Конъюгационные желтухи обусловлены преимущественным нарушением конъюгации билирубина в гепатоцитах. К ним относятся желтухи связанные с исключительно грудным вскармливанием (при гипогалактии) и особенностями состава грудного молока (семейной транзиторной гипербилирубинемии Ариаса– Люцея–Дрискола) (при нормальном уровне лактации); желтухи, обусловленные диабетической фетопатией и врожденным гипотиреозом. Выраженные нарушения конъюгации билирубина отмечаются при ряде наследственных заболеваний: синдроме Криглера–Найяра 1-го и 2-го типов, синдроме Жильбера и др.
Конъюгационные желтухи характеризуются следующими признаками:
Динамика желтухи:
появляется не ранее 24 часов после рождения;
продолжает нарастать или остается выраженной после 4 суток жизни;
сохраняется более 10 дней жизни.
Особенности клинической картины:
кожные покровы имеют оранжевый оттенок;
пальпаторные размеры печени и селезенки не увеличены;
кал и моча обычной окраски.
Лабораторные критерии:
концентрация билирубина в пуповинной крови (в момент рождения) – менее 51 мкмоль;
концентрация гемоглобина в пуповинной крови соответствует норме;
почасовой прирост билирубина в первые сутки жизни менее 6,8 мкмоль/л/час;
максимальная концентрация общего билирубина на 3–4 сутки в периферической или венозной крови у доношенных детей > 255 мкмоль/л;
общий билирубин крови повышается за счет непрямой фракции;
относительная доля прямой фракции составляет менее 20%;
Гипербилирубинемия, обусловленная повышением кишечной реабсорбции чаще всего наблюдается при высокой кишечной непроходимости.
Клиническая картина зависит от причины кишечной непроходимости (атрезия 12-ти перстной кишки, пилоростеноз, обструкция кишечника объемным образованием и т.п.), а также, нередко, сопутствующими симптомами обезвоживания и гипогликемии.
Лабораторные критерии сходны с критериями конъюгационной желтухи.
Непрямая гипербилирубинемия смешанного генеза чаще всего является ранним клиническим проявлением врожденной или перинатальной инфекции. Клиническая картина и лабораторные признаки являются составной частью симптомокомплекса TORCHES или сепсиса.
Стандартное обследование новорожденного с подозрением на патологическую желтуху:
Уточнение срока появления желтухи
Физикальный осмотр (степень распространенности желтухи, размеры печени и селезенки, цвет стула и мочи)
Группа крови и Rh-фактор, реакция Кумбса
Клинический анализ крови (Hb, ретикулоциты, особенности лейкоцитарной формулы крови и др.)
Биохимический анализ крови (билирубин и его фракции, другое – по показаниям)
УЗИ органов брюшной полости.
Лечение
Подготовка и проведение лечебных мероприятий, направленных на уменьшение концентрации непрямого билирубина в сыворотке крови.
Общие принципы. Важным условием для профилактики и лечения гипербилирубинемии у новорожденных является создание оптимальных условий для ранней неонатальной адаптации ребенка. При этом все здоровые и условно здоровые новорожденные дети нуждаются в проведении раннего (начиная с первого часа жизни) и регулярного грудного вскармливания (Уровень доказательности – B). [118, 119].
Необходимо рекомендовать матери кормить грудью* как минимум 8 — 12 раз в сутки без ночного перерыва в течение первых нескольких дней жизни. Увеличение частоты кормления грудью снижает вероятность последующей тяжелой гипербилирубинемии у новорожденных при грудном вскармливании (Уровень доказательности – D). [38, 39]. (*Отношение к грудному вскармливанию при ГБН изложено в соответствующих клинических рекомендациях).
Дополнительное введение воды либо растворов глюкозы новорожденным, находящимся на грудном вскармливании, при отсутствии признаков дегидратации, не показано. Дополнительное введение в рацион воды либо растворов глюкозы не предупреждает развитие гипербилирубинемии и не снижает уровень общего билирубина сыворотки.
В качестве крайней меры может рассматриваться временное (1-3 дня) прекращение грудного вскармливания и переход на кормление адаптированной смесью, что может способствовать снижению уровня билирубина и/или повышению эффективности фототерапии в случае желтухи обусловленной составом грудного молока (Уровень доказательности – D) [38]. В случаях медицинских противопоказаний к раннему прикладыванию к груди или избыточной убыли первоначальной массы тела к 3–4 дню жизни новорожденным необходимо организовать докорм адаптированной питательной смесью.
Во всех случаях заболевания новорожденного необходимо заботиться о поддержании оптимальной температуры тела, обеспечении его организма достаточным количеством жидкости и питательных веществ, профилактике таких метаболических нарушений, как гипогликемия, гипоксемия и ацидоз.
Фототерапия
Основным методом лечения непрямой гипербилирубинемии является фототерапия.
При неэффективности фототерапии и угрозе развития БЭ показано проведение обменного переливания крови (Уровень доказательности – A) [85, 120, 121, 122, 123] .
Виды фототерапии [ 124, 125].:
• Традиционная – проведение фототерапии с использованием одного источника света – люминесцентные лампы голубого света;
• LED фототерапия – фототерапия с использованием светодиодов, обеспечивает меньшие потери жидкости организмом;
• Фиброоптическая фототерапия – процедура с использованием одного источника света с волоконно-оптическим кабелем, через который световой луч проходит на гибкую светящуюся поверхность, на которую помещается ребенок или может быть обернута вокруг него (не требует защиты глаз). Может быть использована у недоношенных новорожденных;
• Комбинированная фототерапия – осуществляется с помощью двух и более источников света (две и более единицы или сочетание ламп обычной и фиброоптической фототерапии). Показана для лечения как доношенных, так и недоношенных новорожденных при наличии хотя бы одного признака:
— если почасовой прирост ОБС > 6,8 мкмоль/л/час;
— если через 72 часа уровень ОБС находится на уровне менее 50 мкмоль/л от порового значения для начала операции ЗПК;
— если после проведения фототерапии в течение 6 часов уровень ОБС повышается или не снижается.
Проведение фототерапии в непрерывном режиме (проводится в течение суток непрерывно, допустимы лишь перерывы на кормление и манипуляции (не более 30 минут) более предпочтительно (Уровень доказательности – A) [126].
Техника фототерапии при использовании установок с традиционными и LED-источниками света [120]:
Обнаженный ребенок помещается в кувез или в кроватку с термоматрасом (выбор режима зависит от гестационного возраста ребенка, особенностей терморегуляции, при этом температура тела ребенка должна быть в пределах 36,6 – 37,0 С) [127 ур 1+ ].
глаза ребенка и половые органы мальчиков должны быть защищены светонепроницаемым материалом.
источник фототерапии располагается над ребенком на высоте 50-55 см, если ребенок находится в кувезе, то расстояние от верхней стенки кувеза до лампы фототерапии должно быть 5,0 см.
фототерапия при помощи установок, не предназначенных для домашнего использования, должна проводится в палатах для новорожденных под контролем среднего медицинского персонала
каждые 1-2 часа фототерапии необходимо менять положение ребенка по отношению к источнику света, переворачивая его поочередно вверх животом или спиной [97 ур 1++]
каждые 2 часа необходимо измерять температуру тела ребенка,
при отсутствии противопоказаний необходимо сохранять кормление материнским молоком в полном объеме,
физиологическая потребность ребенка в жидкости увеличивается на 10-20%, при невозможности увеличения объема питания проводится инфузионная терапия [118 ур 1-, 119 ур 1+]
в процессе фототерапии нельзя ориентироваться на цвет кожных покровов, и показатели приборов для чрезкожного измерения билирубина
всем детям, получающим фототерапию, необходимо ежедневно проводить биохимический анализ крови на билирубин (при угрозе билирубиновой энцефалопатии – каждые 6-12 часов); только стандартный биохимический анализ крови может служить критерием эффективности фототерапии,
фототерапия может быть прекращена, если отсутствуют признаки патологического прироста билирубина, а концентрация общего билирубина в сыворотке крови стала ниже значений, послуживших основанием для начала фототерапии,
через 12 часов после окончания фототерапии необходимо контрольное исследование билирубина крови,
у некоторых детей в ответ на фототерапию может появиться аллергическая сыпь, участиться и измениться в цвете стул и появиться бронзовый оттенок кожи. Все три эффекта, как правило, бесследно исчезают после прекращения фототерапии.
Показания для фототерапии и операции ЗПК у доношенных и поздних недоношенных детей (боле 35 недель гестации) при непрямой гипербилирубинемии, не связанной с ГБН, в раннем неонатальном периоде основываются на определении пороговых значений общей концентрации билирубина сыворотки крови в зависимости от постнатального возраста в часах и наличия или отсутствия факторов риска. При быстром нарастании уровня билирубина и при критической гипербилирубинемии фототерапию необходимо проводить в непрерывном режиме (Уровень доказательности – C) [131]. Во всех случаях наличия у ребенка факторов риска, повышающих вероятность развития билирубиновой энцефалопатии, фототерапию необходимо начинать при минимальных значениях билирубина. Несмотря на то, что в отдельных Европейских странах в последнее десятилетие наметилась тенденция к пересмотру (повышению) пороговых значений концентрации билирубина в сыворотке крови [126], при которых рекомендовано начало фототерапии и проведение операции ЗПК новорожденным детям, по мнению экспертов РОН, в нашей стране на данном этапе развития перинатальных технологий наиболее целесообразно использовать показания, разработанные Американской Академией Педиатрии (AAP) в 2004 году, которые в графическом виде представлены на рис 4. (Уровень доказательности – D).
При снижении концентрации общего билирубина на фоне проводимой фототерапии лечение продолжается до момента, когда при плановом биохимическом исследовании билирубина его концентрация оказывается ниже значений (насколько ниже?), явившихся показанием к началу фототерапии. Через 12 часов после завершения фототерапии должно быть проведено контрольное исследование билирубина, чтобы убедиться что ребенок не нуждается в лечении гипербилирубинемии. Продолжение фототерапии при концентрациях билирубина ниже, указанных на рис 4, является необоснованным и потенциально опасным.
Рис 4. Показания к проведению фототерапии доношенных и поздних недоношенных детей (ГВ 35-37 нед) в раннем неонатальном периоде
После начала фототерапии, ее эффективность при непрямой гипербилирубинемии, не связанной с ГБН, должна оцениваться каждые 12 часов путем измерения концентрации общего билирубина в сывротке крови стандартными лабораторными методами. В случае неэффективности фототерапии – осуществляется подготовка и проведение операции ЗПК (Уровень доказательности – A) [14, 97, 85, 120, 122, 124]. Показания к проведению операции, разработанные Американской Академией Педиатрии (AAP) в 2004 году, представлены на рис 5. [128]
Рис 5. Показания к проведению операции обменного переливания крови у доношенных и поздних недоношенных детей (ГВ 35-37 нед) в раннем неонатальном периоде
Этапы подготовки и проведения операции [129]:
1. Обязательно получение от родителей информированного согласия на проведение ОЗПК.
2. Манипуляцию выполняют в палате/отделении реанимации и интенсивной терапии новорожденных (ПИТН/ОРИТН) (в акушерских отделениях медицинских организаций I уровня оказания перинатальной помощи — в процедурном кабинете).
3. До начала операции у новорожденных, которые находятся в тяжелом состоянии, стандартными методами интенсивной терапии должны быть устранены ацидоз, гипоксемия, гипогликемия, электролитные нарушения, гемодинамические расстройства, гипотермия и т.д.
4. ОЗПК проводит бригада, состоящая, как минимум, из двух человек: врача (неонатолога/анестезиолога-реаниматолога/педиатра) и детской медицинской сестры.
5. Обязательно в истории болезни заполняется протокол ОЗПК (прил. 1).
6. Обязательно строгое соблюдение правил асептики и антисептики.
7. Дети не должны получать энтеральное питание в течение последних 3 часов до предполагаемого начала операции.
8. В желудок перед операцией должен быть введен постоянный зонд, через который необходимо периодически удалять содержимое желудка.
9. Перед операцией необходимо сделать очистительную клизму.
10. В течение всего процесса подготовки к ОЗПК, выполнения операции и последующего ведения ребенка необходим постоянный мониторинг витальных функций (ЧСС, ЧД, сатурация, АД, температура тела).
11. Донорская кровь и (или) ее компоненты при ОЗПК переливаются из расчета 150-170 мл/кг массы тела для доношенного ребенка и 170-180 мл/кг для недоношенного (пример расчета объема замещения представлен в приложении 2).
12. Соотношение эритроцитарной массы/взвеси и свежезамороженной плазмы составляет 2 : 1.
13. Согласно Приказу Минздрава России от 2 апреля 2013 г. N 183н «Об утверждении правил клинического использования донорской крови и (или) ее компонентов» при трансфузии (переливании) донорской крови и (или) эритроцитсодержащих компонентов новорожденным:
— переливаются эритроцитсодержащие компоненты, обедненные лейкоцитами (эритроцитная взвесь, эритроцитная масса, отмытые эритроциты, размороженные и отмытые эритроциты);
— при подборе компонентов донорской крови для трансфузии (переливания) учитывается, что мать является нежелательным донором свежезамороженной плазмы для новорожденного, поскольку плазма матери может содержать аллоиммунные антитела против эритроцитов новорожденного, а отец является нежелательным донором эритроцитсодержащих компонентов, поскольку против антигенов отца в крови новорожденного могут быть антитела, проникшие из кровотока матери через плаценту;
— наиболее предпочтительной является трансфузия негативного по цитомегаловирусу эритроцитосодержащего компонента;
— не допускается переливание свежезамороженной плазмы вирус (патоген) инактивированной реципиентам детского возраста, находящимся на фототерапии.
Для заменного переливания крови используются эритроцитсодержащие компоненты со сроком хранения не более 5 дней с момента заготовки компонента.
Подбор компонентов донорской крови осуществляется в соответствие с группой крови и резус-фактором реципиента
Техника проведения ОЗПК:
уложить ребенка в заранее согретую открытую реанимационную систему с сервоконтролем;
зафиксировать конечности ребенка путем надежного пеленания, кожа живота остается открытой;
установить пупочный катетер с присоединенным к нему заранее тройником со строгим соблюдением правил асептики и антисептики и зафиксировать его;
при наличии противопоказаний для катетеризации пупочной вены ОЗПК проводят через любую другую центральную вену;
компоненты донорской крови предварительно необходимо согреть до температуры 36-370 С;
первую порцию выводимой крови необходимо отобрать для биохимического исследования на уровень билирубина;
далее последовательно проводят постепенное выведение крови ребенка и последующее восполнение выведенного объема;
объем одного замещения (однократного выведения крови) и одного восполнения (однократного введения компонентов крови) зависит от массы тела ребенка, ГВ и тяжести состояния ребенка (у доношенных — 10-20 мл/кг, у недоношенных – 5-10 мл/кг под обязательным контролем показателей гемодинамики, дыхания и функции почек);
скорость одного замещения – 3-4 мл/мин;
на 2 шприца эритроцитарной массы вводится 1 шприц свежезамороженной плазмы;
после каждых 100 мл замещающей среды (эритроцитарной массы и плазмы) ввести 1,0-2,0 мл 10% раствора глюконата кальция или 0,5 мл 10% раствора хлористого кальция, предварительно разведенных в 5,0 мл 5 % глюкозы (только между шприцами с эритроцитарной массой!);
перед окончанием операции осуществляется забор крови на билирубин;
в результате операции (с учетом крови, взятой на биохимическое исследование) суммарный объем вводимых компонентов донорской крови должен быть равен суммарному объему выведенной крови ребенка.
NB! О безусловной эффективности ОЗПК свидетельствует более чем 2-х кратное снижение билирубина к концу операции.
Ведение ребенка в послеоперационном периоде:
Продолжить мониторинг витальных функций;
Энтеральное питание начинать не ранее, чем через 3-4 часа после ОЗПК;
Продолжить фототерапию;
Продолжить поддерживающую и симптоматическую терапию;
Удаление пупочного катетера сразу после операции не рекомендуется в связи с вероятностью повторного проведения ОЗПК;
Контроль уровня билирубина выполняется через 12 часов после ОЗПК, далее по показаниям, но не реже 1 раза в 24 часа до 7 суток жизни;
Контроль гликемии через 1 час после ОЗПК, далее по показаниям;
Согласно Приказу МЗ РФ №183н после окончания трансфузии (переливания) донорской крови и (или) ее компонентов донорский контейнер с оставшейся донорской кровью и (или) ее компонентами (5 мл), а также пробирка с кровью реципиента, использованная для проведения проб на индивидуальную совместимость, подлежат обязательному сохранению в течение 48 часов при температуре 2-60 С в холодильном оборудовании.
В процессе операции ЗПК и в раннем постоперационном периоде возможно развитие следующих осложнений (Уровень доказательности – С) [130, 132, 133, 134].
1. Со стороны сердечно-сосудистой системы:
аритмия;
объемная перегрузка;
застойная сердечная недостаточность;
остановка кровообращения.
передозировка гепарина;
нейтропения;
тромбоцитопения;
реакция «трансплантант против хозяина».
бактериальные и вирусные инфекции.
ацидоз;
гипокальциемия;
гипогликемия;
гиперкалиемия;
гипернатриемия.
эмболии;
тромбозы;
некротизирующий энтероколит;
портальная гипертензия;
перфорация сосудов пуповины.
гипотермия.
Важно отметить, что показания к фототерапии и операции ЗПК, содержащиеся в рекомендациях AAP 2004 года, определяют тактику ведения только доношенных и поздних недоношенных детей ГВ более 35 недель, и ограничены ранним неонатальном периодом. В связи с недостаточностью объективных данных об условиях, при которых БЭ может возникнуть у новорожденных после окончания первой недели жизни, большинство экспертов РОН предлагает расширить действие этих рекомендаций до конца неонатального периода. Вместе с тем у доношенных детей с наследственными нарушениями обмена (например, с синдромом Криглера-Найара – см. ниже), нуждающихся в длительном проведении фототерапии, показания к операции ЗПК должны определяться консилиумом специалистов с учетом патогенеза заболевания и индивидуальной реакции ЦНС ребенка на хроническую непрямую гипербилирубинемию (Мнение экспертов РОН, уровень доказательности – D).
Показания к фототерапии и операции ЗПК у недоношенных детей
До 2007 года в нашей стране не было общепринятых показаний к лечению непрямой гипербилирубинемии у недоношенных и глубоконедоношенных детей. Национальное руководство по неонатологии (2007, 2013) предлагает для определения показаний к фототерапии и операции ЗПК ориентироваться на массу тела новорожденных. Вместе с тем, в прошедшее десятилетие были накоплены и обобщены клинические данные, позволившие составить рекомендации по лечению непрямой гипербилирубинемии недоношенных с учетом их ГВ (B) .
В настоящее время эксперты РОН для определения показаний к фототерапии и операции ЗПК у недоношенных, с учетом ГВ и дополнительных факторов риска рекомендует использовать модифицированные рекомендации AAP (Уровень доказательности – B) [126] Рис. 6,7.
Рис 6.Показания к проведению фототерапии в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
Рис 7. Показания к проведению операции обменного переливания крови в раннем неонатальном периоде у недоношенных детей разного гестационного возраста
Вместе с тем, учитывая высокий риск осложнений операции ЗПК у глубоконедоношенных детей, окончательное решение проведнии операции у детей, родившихся ранее 32 недели гестации должен принимать консилиум врачей-специалистов (Мнение экспертов РОН, уровень доказательности – D).
Неэффективные и потенциально опасные методы лечения, которые следует исключить из клинической практики:
1) Инфузионная терапия имеет ограниченные показания при гипербилирубинемии.
Токсическим действием обладает непрямой жирорастворимый билирубин, и его уровень не может быть снижен введением дополнительных водных растворов. Дополнительная инфузия водного раствора 5-10% глюкозы новорожденным с гипербилирубинемией показана только при развитии эксикоза на фоне интенсивной фототерапии, парентеральное введение жидкости может определяется другими показаниями (рвота, патологическая потеря жидкости, др.) (Мнение экспертов РОН, уровень доказательности – D).
2) Включение в программу инфузионной терапии свежезамороженной донорской плазмы и альбумина при гипербилирубинемии не рекомендуется и не оправдано с позиции доказательной медицины. Данные препараты должны применятся по строгим показаниям; (Уровень доказательности – B) [136].
3) Назначение фенобарбитала. Значимая индукция ферментов печени происходит не ранее 3 дней от момента его назначения, чаще к концу первой недели жизни. Кроме того, при лечении желтухи фенобарбиталом возникают нежелательные эффекты в виде вялости, угнетения дыхания и снижения активности сосания. По этим причинам в течение последних 15-20 лет фенобарбитал для лечения гипербилирубинемии не применяется (Уровень доказательности – A) [139].
4) Нет убедительных научных доказательств, и патогенетического обоснования для лечения непрямой гипербилирубинемии гепатопротективными и желчегонными препаратами, такими как Эссенциале, ЛИВ-52, Хофитол. Препараты урсодезоксихолевой кислоты показаны только при развитии синдрома холестаза (Мнение экспертов РОН, уровень доказательности – D).
Условия выписки из стационара доношенных новорожденных с непрямой гипербилирубинемией
Условия выписки доношенных новорожденных, получавших фототерапию по поводу непрямой гипербилирубинемии, не связанной с ГБН:
— удовлетворительное общее состояние,
— снижение интенсивности желтухи в динамике,
— концентрация билирубина сыворотки крови менее той, которая требует лечения спустя 12 и более часов после окончания фототерапии,
-в случае ранней выписки необходимо ориентироваться на центильную кривую Bhutani VK (см. выше) и учитывать реальные возможности педиатрической службы региона обеспечить динамическое наблюдение за новорожденным ребенком после выписки из стационара.
При выписки ребенка из ОПННД следует помнить, что непрямая гипербилирубинемия редко является единственным патологическим состоянием, определяющим длительность стационарного лечения. Сроки выписки ребенка зависят от результатов лечения основного и сопутствующих заболеваний.
Особенности наблюдения на амбулаторном этапе за новорожденным с непрямой гипербилирубинемией.
Наиболее опасным периодом с точки зрения риска развития БЭ является первые 7 дней жизни (Уровень доказательности – B) [135]. В данном случае тактика наблюдения и лечения ребенка не отличается от таковой в условиях стационара (см. выше). У детей старше 7 дней жизни риск БЭ уменьшается, однако недосточно объективных данных для изменения показаний к лечению в позднем неонатальном периоде (Мнение экспертов РОН, уровень доказательности – D).
Во всех случаях патологической желтухи, генез которой не уточнен, необходимо проведение дополнительного обследования:
Анамнестические данные
— Наличие указаний на патологическую желтуху в неонатальном периоде в семье и/или синдрома Жильбер
Клинические данные:
— степень выраженности желтухи, размеры печени и селезенки, цвет стула и мочи
— вид вскарливания, динамика веса
— наличие срыгиваний и/или рвот, кратность стула
Клинический анализ крови
Биохимия крови, включающая билирубин и его фракции, печеночные тесты: АЛТ, АСТ, ГГТ
Гормоны крови: Т4 св, ТТГ
Таким образом, поводом для госпитализации ребенка в ОПННД перинатального центра или детской больницы является как необходимость дополнительного обследования, которое трудно организаовать в условиях детской поликлиники, так и необходимость лечения патологической гипербилирубинемии.
Наличие косвенных признаков гемолиза эритроцитов у ребенка (снижение концентрации гемоглобина и уменьшение количества эритроцитов, повышение числа ретикулоцитов на фоне, увеличения размеров селезенки и печени) свидетельствует о гемолитическом генезе желтухи (рис). Дополнительное диагностическое значение при этом имеют сроки появления желтухи. Для ГБН характерно раннее развитие желтухи — в течение первых 24 часов жизни, — тогда как при наследственных гемолитических анемиях желтуха появляется не ранее 2–3-х суток жизни, а может возникать и в более поздние сроки.
Клиническая характеристика наиболее частых причин патологической непрямой гипербилирубинемии, возникающей в позднем неонатальном периоде.
Коньюгационные желтухи
Желтуха, связанная с составом грудного молока наблюдается у 0,5–2,5% здоровых доношенных детей, находящихся на грудном вскармливании. Ее развитие связывают с повышенным содержанием метаболитов прогестерона (32-20-β-прегнандиола, 5-β-прегнан-3α, 20-β-диол) и неэстерифицированных длинноцепочечных жирных кислот, которые конкурентно ингибируют глюкуронилтрансферазу, наличием глюкуронидазы, высокой активностью фермента липопротеинлипазы в молозиве и грудном молоке. Часто этот вариант гипербилирубинемии ассоциирован с приемом гормональных препаратов и некоторых других лекарственных средств во время беременности, стимуляцией родовой деятельности [137]. Не исключено влияние длительного, в течение всей беременности, приема поливитаминов. В отличие от детей с физиологической желтухой, у новорожденных с желтухой, связанной с составом грудного молока, наблюдается более высокая концентрация НБ в крови к 4–6 дням жизни, которая продолжает нарастать, достигая пика к 10–15 дням жизни. Состояние ребенка при этом удовлетворительное, отмечается хорошая прибавка в весе. Если ребенок продолжает получать грудное молоко, желтуха держится 4–6 недель и затем начинает постепенно ослабевать. Уровень НБ в крови нормализуется к 16-й неделе жизни. Прекращение грудного вскармливания на 48-72 часа способствует быстрому снижению концентрации НБ, как правило, не менее чем на 40%. После возобновления кормления грудью матери НБ может повыситься, но он не достигает исходного уровня и в дальнейшем постепенно снижается. Таким образом, кратковременная отмена грудного вскармливания имеет диагностическое значение при данном варианте гипербилирубинемии. Вместе с тем, длительная отмена грудного молока с целью полной нормализации билирубина нецелесообразна, так как в большинстве случаев уровень билирубина не превышает 340 мкмоль/л.
Транзиторная семейная гипербилирубинемия новорожденных (синдром Люцея — Дрискола) является разновидностью желтухи, связанной с составом грудного молока, так как механизм ее развития связывают с наличием неидентифицированного фактора, ингибирующего ферментную систему трансферазы глюкуроновой кислоты в грудном молоке [137]. Желтуха появляется с первых дней жизни, имеет тенденцию к прогрессивному нарастанию и затяжному течению. Уровень НБ в крови может превышать 340 мкмоль/л, что обусловливает необходимость своевременной диагностики и лечения. Отмена грудного вскармливания на 2-3 дня способствует снижению уровня билирубина и, следовательно, имеет диагностическое значение. Исследование химического состава грудного молока может позволить дифференцировать данный вариант гипербилирубинемии с другими желтухами, связанными с составом грудного молока, что не является принципиальным с практической точки зрения.
В основе желтухи, обусловленной исключительно грудным вскармливанием, лежит первоначально недостаточный объем питания, что способствует усилению липолиза и, как следствие, повышению в крови неэстерифицированных жирных кислот, нарушающих процесс захвата билирубина гепатоцитом и подавляющих активность глюкуронилтрансферазы [138]. Вторым фактором, способствующим гипербилирубинемии, является замедление пассажа по кишечнику и, как следствие, повышение реабсорбции билирубина. Этот вариант желтухи отмечается у детей, находящихся на грудном вскармливании в период становления лактации и не получающих должный объем питания.
Как правило, первоначальная потеря веса составляет 8–10% и более; общее состояние ребенка не страдает. По мере увеличения объема кормления нормализуются обменные процессы, восстанавливается пассаж по кишечнику и купируется желтуха. Желтуха, обусловленная грудным вскармливанием, встречается примерно у 12% детей, получающих исключительно грудное молоко. Она появляется на 2–4-е сутки жизни, пик приходится на 3–6-й день, купируется к концу первого месяца жизни при условии нормализации веса. В случае большой потери веса у детей на исключительно грудном вскармливании – необходимо обеспечить докорм ребенка.
При отсутствии самостоятельного стула, рекомендации по его восстановлению (изменения характера вскармливания, газоотводные трубочки, свечи, клизьмы и т.д.)
Конъюгационная желтуха при гипотиреозе [140]. Гормоны щитовидной железы регулируют активность глюкуронилтрансферразы и, следовательно, их дефицит может стать причиной нарушения конъюгации билирубина. Подтверждением диагноза является низкий уровень Т3, Т4 и повышение ТТГ в крови.
Наследственные формы конъюгационных желтух
Синдром Жильбера [2] — наследственное заболевание, передающееся по аутосомно-доминантному типу (подобная аномалия есть у одного из родителей) и связанное с нарушением захвата билирубина синусоидальной мембраной гепатоцита. Одновременно отмечается и некоторое снижение активности глюкуронилтрансферазы печени — до 50% от нормы. Частота этого синдрома в популяции составляет от 2 до 6%. Желтуха обычно выражена умеренно, в пределах 80–120 мкмоль/л, случаев ядерной желтухи не описано, общее состояние детей не нарушается. Клинические проявления могут отмечаться со 2–3- х суток жизни, причем интенсивность желтухи может меняться каждые 3–5 недель. С диагностической целью может быть использован фенобарбитал в терапевтической дозе 5 мг/кг/сут коротким курсом в течение 3 дней: характерно снижение билирубина на 50–60%, что позволяет с высокой вероятностью предположить данный синдром. Дополнительное диагностическое значение имеет анализ родословной, свидетельствующий о синдроме Жильбера в семье. Подтверждение диагноза возможно на основании генетического тестирования.
Синдром Криглера—Найяра [67,68] — наследуемая негемолитическая желтуха с повышением уровня НБ вследствие врожденной недостаточности глюкуронилтрансферазы. Механизм желтухи при синдроме Криглера — Найяра сводится к полной или почти полной неспособности печени конъюгировать билирубин. Известны две генетически гетерогенные формы данного синдрома и в связи с этим выделяют 2 типа.
Синдромом Криглера — Найяра 1 типа передается по аутосомно-рецессивному типу. Характерна интенсивная желтуха с 15–50-кратным превышением нормального уровня НБ сыворотки крови, которая во случаях (без лечения) сопровождается прокрашиванием ядер мозга, т. е. развитием ядерной желтухи. При этой форме гипербилирубинемия, как правило, развивается в течение первых дней после рождения и сохраняется всю жизнь. Назначение фенобарбитала с целью стимуляции глюкуронилтрансферазы печени не приводит к уменьшению сывороточной концентрации билирубина. Диагноз устанавливается на основании прогрессивного нарастания уровня непрямого билирубина, не связанного с гемолизом эритроцитов, и отсутствия эффекта от приема фенобарбитала. Подтверждается молекулярно-генетическими методами. Использование фототерапии является наиболее эффективным методом консервативного лечения детей раннего возраста, позволяющим несколько снизить уровень билирубина и зафиксировать его на некоторое время. В течение первых 10 дней жизни оптимально постоянное проведение фототерапии с целью поддержания уровня билирубина ниже 340 мкмоль/л. В дальнейшем чувствительность гематоэнцефалического барьера снижается, в связи с чем уровень билирубина может подниматься выше 340 мкмоль/л, но, по-видимому, не более чем до 500 мкмоль/л, поэтому продолжительность фототерапии может быть уменьшена до 10–16 часов в сутки. К сожалению, у детей старше месячного возраста нет однозначного мнения об уровне билирубина, который является токсичным. Имеющиеся в литературе данные имеют широкий диапазон колебаний — от 500 до 800 мкмоль/л. Наш собственный опыт наблюдения ребенка с синдромом Криглера — Найяра I типа свидетельствует о повышении билирубина до 650 мкмоль/л без развития признаков билирубиновой энцефалопатии. Радикальным методом лечения служит трансплантация печени или гепатоцитов. В ургентных ситуациях, при высоком риcке развития билирубиновой энцефалопатии, показано проведение операции ОПК или плазмафереза.
Синдром Криглера — Найяра II типа передается по аутосомно-доминантному типу, является прогностически более благоприятным заболеванием и сопровождается более слабой желтухой с 5–20-кратным повышением НБ сыворотки крови. Отличительной особенностью этой формы служит уменьшение сывороточной концентрации билирубина на фоне 3-дневного применения фенобарбитала не менее чем на 50–60%. При синдроме Криглера — Найяра II типа дефицит глюкуронилтрансферазы менее выражен, уровень билирубина в сыворотке крови широко варьирует (от 91 до 640 мкмоль/л), но чаще всего не превышает 340 мкмоль/л. Развитие билирубиновой энцефалопатии отмечается редко и в основном происходит в раннем неонатальном периоде при участии других патологических факторов. Динамический контроль за показателями НБ в сыворотке крови и раннее назначение фенобарбитала, своевременное и адекватное проведение фототерапии позволяют эффективно снизить уровень билирубина и предупредить развитие энцефалопатии. С целью подтверждения диагноза возможно проведение молекулярно-генетического исследования.
. [141]
Следует помнить, что патологическая непрямая гипербилирубинемия может быть вторичной вследствие повышения реабсорбции билирубина в кишечнике может быть обусловлено обструкцией желудочно-кишечного тракта или кишечной непроходимостью при пилоростенозе, болезни Гиршпрунга, мекониальном илеусе, при парезах кишечника и др.. Исключение врожденных и приобретенных заболеваний желудочно-кишечного тракта должно входить в план дополнительного обследования ребенка с поздней или «затянувшейся» желтухой.
Профилактика
Принципы профилактики БЭ
В случаях выявления патологической гипербилирубинемии, первоочередные усилия медицинских работников должны быть направлены на предотвращение критических концентраций билирубина в крови, при которых вероятно развитие БЭ.
Медицинские мероприятия, направленные на профилактику БЭ, можно условно разделить на 4 этапа:
1. Клинико-анамнестический и клинико-лабораторный скрининг новорожденных детей на возможность развития или наличие патологической гипербилирубинемии (выявление группы риска).
2. Определение степени и выявление ведущего патогенетического механизма развития гипербилирубинемии.
3. Подготовка и проведение лечебных мероприятий, направленных на уменьшение концентрации непрямого билирубина в сыворотке крови:
— cоздание оптимальных условий медицинского ухода и, при необходимости, проведение интенсивной терапии основного и сопутствующих заболеваний;
— фототерапия (использование оптимальных режимов);
— в случаях недостаточной эффективности фототерапии, подготовка и проведение операции заменного переливания крови; при необходимости — создание дополнительных условий, повышающих эффективность ЗПК;
— клинико-лабораторный мониторинг безопасности и эффективности комплекса лечебных мероприятий (до момента полного их завершения)
4. Выявление или подтверждение конкретной причины развития непрямой гипербилирубинемии, потребовавшей медицинского вмешательства; при необходимости (в диагностически сложных случаях) — продолжение дифференциально-диагностических мероприятий и лечения основного и сопутствующего заболеваний.
Первые три этапа должны быть организованы в любой медицинской организации (МО) акушерско-гинекологического или педиатрического профиля, независимо от ее функционального уровня. Для организации 4 этапа может потребоваться перевод ребенка в учреждение 3 уровня (в Перинатальный центр или детскую многопрофильную или специализированную больницу).
Информация
Источники и литература
-
Клинические рекомендации Российского общества неонатологов
- 1. Brown AK, Kim MH, Wu PYK, et al. Efficacy of phototherapy in prevention and
management of neonatal hyperbilirubinemia. Pediatrics 1985;75:393.
2. Kaplan M, Hammerman C, Renbaum P, et al. Gilbert’s syndrome and
hyperbilirubinaemia in ABO-incompatible neonates. Lancet 2000;356:652.
3. Gomella TL, Cunningham MD Neonatology: Management, Procedures, On Call
Problems, Diseases, and Drugs. 7th Edition. 2013
4. Newman ТВ, Escobar GJ, Gonzales VM, et al. Frequency of neonatal bilirubin testing
and hyperbilirubinemia in a large health maintenance organization. Pediatrics 1999;
104:1198.
5. Bhutani VK, Johnson L, Sivieri EM. Predictive ability of a predischarge hour-specific
serum bilirubin for subsequent significant hyperbilirubinemia in healthy-term and nearterm
newborns. Pediatrics 1999; 103:6.
6. Maisels MJ, FanaroffAA Stevenson DK, et al. Serum bilirubin levels in an international,
multiracial newborn population. Pediatr Res 1999;45:167A.
7. Ryan AS, Wenjun MS, Acosta A Breastfeeding continues to increase into the new
millennium. Pediatrics 2002; 110:1103. 8. Cashore WJ, Gartner LM, Oh W, et al. Clinical application of neonatal bilirubin-binding
determinations: current status. J Pecfafr» 1978;83:827.
9. Keren R, Tremont K, Luan X, et al. Visual assessment of jaundice in term and late
preterm infants. Arch Dis Child Fetal Neonatal Ed 2009;94:F317.
10. Maisels MJ, Pathak A, Nelson NM, et al. Endogenous production of carbon monoxide in
normal and erythroblastotic newborn infants. J Clin Invest 1971 ;50:1.
11. Ahdab-Barmada M. The neuropathology of kernicterus: definitions and debate. In:
Maisels MJ, Watchko JF, eds. Neonatal jaundice. London, UK: Harwood Academic
Publishers, 2000:75.
12. Turkel SB. Autopsy findings associated with neonatal hyperbilirubinemia. Clin Perinatol
1990;17:381.
13. Volpe JJ. Bilirubin and brain injury. In: Volpe JJ. Neurology of the newborn. 5th ed.
Philadelphia, PA W.B. Saunders, 2008:619
14. Wennberg RP, Ahlfors CE, Bhutani V, et al. Toward understanding kernicterus: a
challenge to improve the management of jaundiced newborns. Pediatrics 2006; 117:474.
15. Bellarosa C, Muchova L, Vitek L, et al. Bilirubin metabolism and transport. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:55.
16. Hansen TWR, Bratlid D. Physiology of neonatal unconjugated hyperbilirubinemia. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:65
17. Kaplan M, Muraca M, Hammerman C, et al. Imbalance between production and
conjugation of bilirubin: a fundamental concept in the mechanism of neonatal jaundice.
Pediatrics 2002; 110(4).
18. Bhutani VK, Stark AR, Lazzeroni LC, et al. Predischarge screening for severe neonatal
hyperbilirubinemia identifies infants who need phototherapy. J.Pediatrics 1999;103:6–14.
19. Brodersen R. Binding of bilirubin to albumin. CRC Crit Rev Clin Lab Sci 1980; 11:305
20. Maisels MJ, Newman ТВ. The epidemiology of neonatal hyperbilirubinemia. In:
Stevenson DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York:
McGraw Hill, 2012:97
21. Watchko JF, Lin Z. Genetics of neonatal jaundice. In: Stevenson DK, Maisels MJ,
Watchko JF, eds. Care ofthe jaundiced neonate. New York: McGraw Hill, 2012:1.
22. Engle WD, Jackson GL, Sendelbach D, et al. Assessment of a transcutaneous device in
the evaluation of neonatal hyperbilirubinemia in a primarily Hispanic population.
Pediatrics 2002; 110:61.
23. Bowman JM. The management of alloimmune fetal hemolytic disease. In: Maisels MJ,
Watchko JF, eds. Neonatal jaundice. London, UK: Harwood Academic Publishers,
2000:23.
24. Koenig JM. Evaluation and treatment of erythroblastosis fetalis in the neonate. In:
Christensen RD, ed. Hematologic problems ofthe neonate. Philadelphia, PA W.B.
Saunders Co., 2000:185.
25. Bowman JM. Immune hemolytic disease. In: Nathan DG, Orkin SH, eds. Hematology of
infancy and childhood, 5th ed. Philadelphia, PA: W.B. Saunders Company, 1998:54.
26. Bowman JM. RhD hemolytic disease of the newborn. N Engl J Med 1998;339:1775.
27. Rath MEA Smits-Wintjens VEHJ, Walther FJ, et al. Hematological morbidity and
management in neonates with hemolytic disease due to red cell alloimmunization. Early
Hum Dev 2011;87:583.
28. Ozolek J, Watchko J, Mimouni F. Prevalence and lack of clinical significance of blood
group incompatibility in mothers with blood type A or B. J Pediatry 994; 125:87. 29. Maisels MJ. Neonatal Jaundice. In: Sinclair JC, Bracken MB, eds. Effective care of the
newborn infant. Oxford, UK: Oxford University Press, 1992:507.
30. Newman ТВ, Liljestrand P, Escobar GJ. Jaundice noted in the first 24 hours after birth in
a managed care organization. Arch Pediatr Adolesc Med 2002; 156:1244.
31. Knudsen A. Prediction ofthe development of neonatal jaundice by increased umbilical
cord blood bilirubin. Acta Paediatr Scand 1989; 78:217.
32. Newman ТВ, Xiong B, Gonzales VM, et al. Prediction and prevention of extreme
neonatal hyperbilirubinemia in a mature health maintenance organization. Arch Pediatr
AdolescMed2000,IMA 140.
33. Maisels MJ, DeRidder JM, Kring EA, et al. Routine transcutaneous bilirubin
measurements combined with clinical risk factors improve the prediction of subsequent
hyperbilirubinemia. J Perinatol 2009; 29:612.
34. Yamauchi Y, Yamanouchi I. Difference in TcB readings between full term newborn
infants born vaginally and by cesarean section. Acta Paediatr Scand 1989;78:824.
35. Amato M, Fouchere JC, von Muralt G. Relationship between peri-intraventricular
hemorrhage and neonatal hyperbilirubinemia in very low birth weight infants. Am J
Perinatol 1987;4:275.
36. Silverman WA A difference in mortality rate and incidence of kernicterus among
premature infants allotted to two prophylactic antibacterial regimens. Pediatrics 1998;
102:225 (supplement).
37. Keren R, Luan X, Friedman S, et al. A comparison of alternative risk-assessment
strategies for predicting significant neonatal hyperbilirubinemia in term and near-term
infants. Pediatrics 2008; 121 :e170.
38. Bertini G, Dani C, Trochin M, etal. Is breastfeeding really favoring early neonatal
jaundice? Pediatrics 2001;107.
39. Yamauchi Y, Yamanouchi I. Breast-feeding frequency during the first 24 hours after
birth in full-term neonates. Pediatrics 1990;86:171.
40. Gartner U, Goeser T, Wolkoff AW. Effect of fasting on the uptake of bilirubin and
sulfobromophthalein by the isolated perfused rat liver. Gastroenterology 1997; 113:1707.
41. Maisels MJ, Kring EA. Length of stay, jaundice and hospital readmission. Pediatrics
1998; 101:995.
42. McDonald SJ, Middleton P. Effect of timing of umbilical cord clamping of term infants
on maternal and neonatal outcomes. Cochrane Database Syst Rev 2008;
16(2):CD004074.
43. Saigal S, O’Neill A, Surainder Y, et al. Placental transfusion and hyperbilirubinemia in
the premature. Pediatrics 1972;49:406.
44. Black VD, Lubchenco LO, Koops BL, et al. Neonatal hyperviscosity: randomized study
of effect of partial plasma exchange transfusion on longterm outcome. Pediatrics
1985;75:1048
45. Goldberg K, Wirth FH, Hathaway WE, et al. Neonatal hyperviscosity II. Effect of partial
plasma exchange transfusion. Pediatrics 1982;69:419.
46. Ultee CA, van der Deure J, Swart J, et al. Delayed cord clamping in preterm infants
delivered at 34-36 weeks’ gestation: a randomised controlled trial. Arch Dis Child Fetal
Neonatal Ed 2008;93(1 ):F20.
47. Frishberg Y, Zelicovic I, Merlob P, et al. Hyperbilirubinemia and influencing factors in
term infants. IsrJ Med Sci 1989;25:28.
48. Jahrig D, Jahrig K, Striet S, et al. Neonatal jaundice in infants of diabetic mothers. Acta
Paediatr Scand Suppl 1989;360:101. 49. Jahrig D, Jahrig K, Striet S, et al. Neonatal jaundice in infants of diabetic mothers. Acta
Paediatr Scand Suppl 1989;360:101.
50. Berk MA Mimouni F, Miodovnik M, et al. Macrosomia in infants of insulin-dependent
diabetic mothers. Pediatrics 1989;83:1029.
51. Chavalitdhamrong P-O, Escobedo MB, Barton LL, et al. Hyperbilirubinemia and
bacterial infection in the newborn. Arch Dis Child 1975;50:652.
52. Linder N, Yatsiv I, Tsur M, etal. Unexplained neonatal jaundice as an early diagnostic
sign ofsepticemia in the newborn. J Perinatol 1988;8:325.
53. Garcia FJ, Nager AL. Jaundice as an early diagnostic sign of urinary tract infection in
infancy. Pediatrics 2002; 109: 6.
54. Maisels MJ, Newman ТВ. Neonatal jaundice and urinary tract infections. Pediatrics
2003^ 12:1213.
55. Kaplan M, Hammerman C. Hemolytic disorders and their management. In: Stevenson
DK, Maisels MJ, Watchko JF, eds. Care ofthe jaundiced neonate. New York: McGraw
Hill, 2012:145.
56. Kaplan M, Hammerman C. Glucose-6-phosphate dehydrogenase-deficient neonates: a
potential cause for concern in North America. Pediatrics 2000; 106:1478.
57. Kaplan M, Algur N, Hammerman C. Onset of jaundice in glucose-6-phosphate
dehydrogenase-deficient neonates. Pediatrics 2001; 108:956.
58. Kaplan M, Beutler E, Vreman HJ, et al. Neonatal hyperbilirubinemia in glucose-6-
phosphate dehydrogenase deficient heterozygotes. Pediatrics 1999; 104:68.
59. Kaplan M, Hammerman C, Renbaum P, et al. Differing pathogenesis of perinatal
bilirubinemia in glucose-6-phosphate dehydrogenase-deficient versus normal neonates.
Pediatr Res 2001;50:532.
60. Bender GJ, Cashore WJ, Oh W. Ontogeny of bilirubin-binding capacity and the effect of
clinical status in premature infants born at less than 1300 grams. Pediatrics
2007;’120:1067.
61. Ross ME, Waldron PE, Cashore WJ, et al. Hemolytic disease of the fetus and newborn.
In: de Alarcon PA, Werner EJ, Christensen RD, eds. Neonatal hematology, pathogenesis,
diagnosis, and management of hematologic problems, 2nd ed. Cambridge UK:
Cambridge University Press, 2013:65.
62. Gallagher PG. Disorders of erythrocyte metabolism and shape. In: Christensen RD, ed.
Hematologic problems of the neonate. Philadelphia, PA W.B. Saunders Co, 2000:209.
63. Christensen RD, Henry E. Hereditary spherocytosis in neonates with hyperbilirubinemia.
Pediatrics 2010; 125:120.
64. Black VD, Lubchenco LO, Luckey DW, et al. Developmental and neurologic sequelae in
the neonatal hyperviscosity syndrome. Pediatrics 1982;69:426.
65. Watchko JF, Daood MJ, Biniwale M. Understanding neonatal hyperbilirubinaemia in the
era of genomics. Semin Neonatol 2002;7:143.
66. Kaplan M, Hammerman C, Maisels MJ. Bilirubin genetics for the nongeneticist:
hereditary defects of neonatal bilirubin conjugation. Pediatrics 2003; 111:886.
67. Job H, Hart G, Lealman G. Improvements in long term phototherapy for patients with
Crigler-Najjar syndrome type I. Phys Med Biol 1996;41 (11 ):2549.
68. Fox IJ, Roy-Chowdhury J, Kaufman SS, et al. Treatment of the Crigler-Najjar syndrome
type I with hepatocyte transplantation. N Engl J Med 1998;338:1422.
69. Vaz AR, Delgado-Esteban M, Brito MA, et al. Bilirubin selectively inhibits cytochrome с
oxidase activity and induces apoptosis in immature cortical neurons: assessment of the
protective effects of glycoursodeoxycholic acid. J Neurochem 2010; 112:56.
70. Wennberg RP. Cellular basis of bilirubin toxicity. NY State J Med 1991 ;91:493
- 1. Brown AK, Kim MH, Wu PYK, et al. Efficacy of phototherapy in prevention and
Информация
Коллектив авторов
Список сокращений
БЭ -билирубиновая энцефалопатия
Г-6-ФДГ — глюкозо-6-фосфат дегигдрогеназа
ГБН — гемолитическая болезнь новорожденных
КОС — кислотно-основное состояние
МКБ-10 — международная классификация болезней -10
ОБ — общий билирубин
ОБС — общий билирубин сыворотки
ОЗПК — операция заменного переливания крови
ОРИТН — отделение реанимации и интенсивной терапии новорожденных
ФТ — фототерапия
TcBr — билирубин, измеренный чрезкожно (транскутанно)
Методология
Методы, использованные для сбора/селекции доказательств:
поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
доказательной базой для рекомендаций являются публикации, вошедшие в Кохрановскую библиотеку, базы данных MEDLINE и EMBASE по состоянию на 1 сентября 2016 г.
Глубина поиска составляла 60 лет.
Методы, использованные для оценки качества и силы доказательств:
Консенсус экспертов;
Оценка значимости в соответствии с рейтинговой схемой (схема прилагается)
Рейтинговая схема для оценки силы рекомендаций представлена в таблице 1.
Таблица 1 — Уровни доказательности
Методы, использованные для формулирования рекомендаций:
консенсус экспертов.
Рейтинговая схема оценки силы рекомендаций представлена в таблице 2.
Таблица 2 – Рейтинговая схема оценки силы рекомендаций
Индикаторы доброкачественной практики (GoodPracticePoints – GPPs):
рекомендуемая доброкачественная практика базируется на клиническом опыте рабочей группы по разработке рекомендаций.
анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Методы валидизации рекомендаций:
Внешняя экспертная оценка;
Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций
Настоящие рекомендации в предварительной версии были рецензированы независимыми экспертами.
Получены комментарии со стороны врачей неонатологов из нескольких регионов первого и второго этапов выхаживания новорожденных детей (гг. Москва, Екатеринбург, Калужская область, Республика Карелия, Хабаровский край и др.) в отношении доступности, доходчивости и возможности применения рекомендаций в повседневной практике.
Все комментарии, полученные от экспертов, анализировались председателем и членами рабочей группы, вносились изменения с учетом рекомендаций.
Консультация и экспертная оценка
Предварительная версия была размещена для обсуждения на сайте http://neonatologynmo.geotar.ru, для того, чтобы широкий круг лиц имел возможность принять участие в обсуждении и совершенствовании рекомендаций.
Для окончательной редакции и контроля качества рекомендации были повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Силы рекомендаций (A-D), уровни доказательств (1++, 1+, 1-, 2++, 2+, 2-, 3, 4) и индикаторы доброкачественной практики — goodpracticepoints (GPPs) приводятся в ходе изложения текста рекомендаций.
Заключение.
Непрямая гипербилирубинемия является одним из наиболее частых транзиторных и патологических состояний, требующих повышенного внимание врачей- неонатолов и педиатров. Подробное описание этиологии и патогенеза желтух новорожденных, а также принципов дифференциальной диагностики и лечения, представлено в медицинских учебниках и врачебных руководствах наших великих учителей и наставников – В.А.Таболина, Г.М.Савельевой, Н.П.Шабалова, Н.Н.Володина, Сидельниковой В.М. А.Г.Антонова, Г.В.Яцык [142-147].
Представленные клинические рекомендации, основанные на последних достижениях перинатальной медицины, направлены в первую очередь на достижение двух основных целей: 1) повышение эффективности предупреждения билирубиновой энцефвалопатии у доношенных и недоношенных новорожденных детей; 2) уменьшение числа инвазивных и потенциально опасных медицинских вмешательств у новорожденных детей, сокращение необоснованных госпитализаций новорожденных.
Члены рабочей группы будут признательны за любые конструктивные замечания и предложения, направленные на совершенствование подходов к профилактике и лечению патологических непрямых гипербилирубинемий у новорожденных.
Электронная версия данного документа доступна на сайте Российского общества неонатологов (РОН) – www. neonatology.pro
Прикреплённые файлы
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники. Стандарты лечения
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Мобильное приложение «MedElement»

- Профессиональные медицинские справочники
- Коммуникация с пациентами: онлайн-консультация, отзывы, запись на приём
Скачать приложение для ANDROID / для iOS
Внимание!
Если вы не являетесь медицинским специалистом:
-
Занимаясь самолечением, вы можете нанести непоправимый вред своему здоровью.
-
Информация, размещенная на сайте MedElement и в мобильных приложениях «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта», не может и не должна заменять очную консультацию врача.
Обязательно
обращайтесь в медицинские учреждения при наличии каких-либо заболеваний или беспокоящих вас симптомов.
-
Выбор лекарственных средств и их дозировки, должен быть оговорен со специалистом. Только врач может
назначить
нужное лекарство и его дозировку с учетом заболевания и состояния организма больного.
-
Сайт MedElement и мобильные приложения «MedElement (МедЭлемент)», «Lekar Pro»,
«Dariger Pro», «Заболевания: справочник терапевта» являются исключительно информационно-справочными ресурсами.
Информация, размещенная на данном
сайте, не должна использоваться для самовольного изменения предписаний врача.
-
Редакция MedElement не несет ответственности за какой-либо ущерб здоровью или материальный ущерб, возникший
в
результате использования данного сайта.
Билитест – неинвазивный метод исследования, позволяющий определить уровень билирубина у новорожденных. Диагностика является безопасной и не имеет противопоказаний.
Что представляет собой билирубин? Нормы показателей для новорожденных по дням и месяцам
Билирубин представляет собой желчный пигмент, образующийся в результате распада эритроцитов. Данный пигмент имеет желто-коричневый окрас, благодаря чему при развитии патологий, связанных с повышением уровня билирубина, происходит окрашивание кожных покровов в желтый цвет.
Выводится пигмент преимущественно с мочой и калом под воздействием печеночных ферментов. В норме билирубин содержится в небольшом количестве. Однако при развитии различных патологий показатели могут значительно возрастать.
| Возраст ребенка | Норма (мкмоль/л) |
| Новорожденные дети (до суток) | 50-60 |
| Новорожденные от 2 до 7 суток | До 256 |
| Дети от 7 до 14 дней | От 60 до 100 |
| Груднички до 21 дня | От 8,5 до 20,5 |
| Новорожденные в возрасте от 1-го до 2-х месяцев | От 8,5 до 20,5 |
При рождении показатели желчного пигмента у детей, рожденных раньше срока, составляют от 70 до 110 мкмоль/л, у рожденных в срок – от 50 до 60 мкмоль/л. Для определения показателей может применяться специфический метод диагностики, иначе именуемый шкалой Крамера.
Показатели и проявления:
- Образование желтизны в области головы ребенка – 100 мкмоль/л.
- Пожелтение верхней части туловища – 150 мкмоль/л.
- Желтизна распространяется на нижнюю часть туловища, в том числе область ягодиц и бедер – 200 мкмоль/л.
- Пожелтение рук и ног – 250 мкмоль/л.
- Окрашивание кожных покровов и всего тела в желтый цвет – более 250 мкмоль/л.
Чем выше показатели, тем больше вероятность развития патологических процессов у ребенка в области печени и желчного пузыря (дискинезия). При отсутствии признаков заболевания уровень желчного пигмента в крови приходит в норму по прошествии 2-3-х недель после рождения ребенка.
Причины и последствия отклонения показателей от нормы
Билитест для новорожденных применяется независимо от того, присутствуют ли признаки болезни или нет. Аппарат необходим для постоянного контроля и отслеживания состояния ребенка первые несколько недель после его рождения.
Согласно статистическим данным патологическая форма желтухи развивается у 5-7% детей. Заболевание развивается на фоне распада фетального гемоглобина, провоцирующего токсическое поражение организма.
Возможные причины:
- Гемолитическая болезнь. Патология развивается на фоне несовместимости резус-фактора матери и ребенка.
- Наличие врожденных инфекционных заболеваний у ребенка. Вирусные агенты способствуют снижению связывающей способности билирубина, что приводит к развитию паренхиматозной формы желтухи.
- Преждевременные роды.
- Наличие у беременной сахарного диабета, в том числе развитие болезни на фоне беременности.
- Наследственные заболевания или врожденные аномалии. Патология развивается на фоне генетических отклонений, связанных с образованием и выработкой печеночных ферментов.
- Эндокринные заболевания у ребенка.
- Кровоизлиятельные процессы у новорожденного.
- Прием лекарственных препаратов во время беременности, использование антибиотиков у ребенка.
- Врожденные патологии желчевыводящих путей – дискинезия, обструкция.
- Тяжелые заболевания печени у новорожденного.
К группе риска также относятся двойни.
Несвоевременное лечение может вызывать различные осложнения и последствия, опасные для здоровья и жизни ребенка.
Последствия:
- задержка в развитии – физическая, психоэмоциональная;
- нарушения слуха, вплоть до полной его потери;
- судорожное состояние;
- паралич;
- токсическое поражение организма;
- ядерная форма желтухи – тяжелое нарушение, сопровождающееся поражением ЦНС.
В конечном итоге заболевание может привести к развитию детского церебрального паралича (ДЦП). При первых признаках заболевания необходимо обратиться к лечащему специалисту за дополнительной диагностикой и назначением лечения. Длительно сохраняющийся повышенный уровень билирубина требует незамедлительного лечения.
Что такое билитест?
Билитест – это высокотехнологичный прибор, используемый для измерения показателей билирубина в крови у новорожденных. При этом процедура проводится в домашних условиях.
Прибор представляет собой миниатюрное электронное устройство, оснащенное специальным индикатором, при помощи которого производится измерительная процедура. Аппарат позволяет определить концентрацию желчного пигмента в подкожных слоях у ребенка.
Достоинства и недостатки прибора
Главным достоинством прибора является его портативность и компактность. При этом аппарат предназначен для домашнего использования.
Достоинства:
- полностью автоматизированный процесс;
- отсутствие необходимости дополнительной настройки прибора;
- минимальная погрешность;
- удобство и простота в обслуживании устройства;
- скорость выполнения процедуры – не более 2-3 секунд;
- повторное тестирование возможно спустя 5-7 секунд после предыдущего замера;
- батареи хватает на 100 тыс. измерений;
- отсутствие необходимости забора крови (неинвазивность);
- не требуется включения/отключения системы питания.
К недостаткам относится погрешность измерений при наличии у ребенка чуть смугловатой или, наоборот, слишком светлой кожи. Также анализатор показывает результаты общего билирубина в крови, не подразделяя его на прямой и непрямой.
Характеристики
Прибор обладает широким диапазоном измерений – от 0 до 400 мкмоль/л. При этом количество измерений, которые можно провести с использованием 3-х элементов питания, составляет не менее 100 тыс. раз.
Характеристики и параметры:
- Масса устройства – 300 г в полной комплектации. Вес аппарата без комплектации составляет 150 г.
- Размеры — 171×70×37 мм.
- Элементы питания – литиевые батареи ААА (3 шт.).
- Количество разрядов на цифровой панели – 2.
- Коэффициент корреляции с сывороточным билирубином – 0,9.
Билитест 2000 для новорожденных
Устройство удобно и практично в применении и не занимает много места.
Что входит в комплект?
Билитест для новорожденных разрешено использовать только после ознакомления с правилами эксплуатации прибора. В комплект анализатора входит непосредственно сам прибор, футляр-упаковка, 2 контрольных световых фильтра, специальный стеклянный набор и 3 шт. элементов питания по 1,5 В.
В упаковке также содержится инструкции по эксплуатации прибора, способы проверки устройства на работоспособность, а также методические рекомендации.
Контроль работоспособности прибора
Перед использованием анализатора необходимо произвести контроль работоспособности устройства. Для проведения процедуры на футляре расположены специальные оптические контрольные меры. Иных контрольных мер работоспособности прибора не требуется.
Подготовка к анализу
Перед проведением анализа необходимо подготовить прибор. Для этого устройство требуется достать из футляра. При этом нет необходимости включать анализатор, так как он уже готов к работе.
Поверхность световодной головки рекомендуется обработать чистой сухой тканью или салфеткой, смоченной в спиртовом растворе. После чего обработанную поверхность необходимо протереть насухо чистой тканью. Процедуру следует проводить перед каждым измерением. Производить замеры с помощью прибора разрешается только после полного высыхания спиртового раствора.
Пациентам также рекомендуется подготовиться к проведению анализа. Для этого следует воздержаться от приема пищи за несколько часов до начала проведения процедуры. За несколько дней необходимо прекратить прием лекарственных препаратов, оказывающих влияние на уровень билирубина в крови.
Анализ следует проводить в утреннее время через 1-2 ч после пробуждения.
Как использовать анализатор?
Билитест для новорожденных необходимо применять согласно рекомендациям специалиста и указаниям руководства по эксплуатации.
Для проведения анализа необходимо подвижную часть головку устройства прислонить к поверхности кожных покровов ребенка, после чего следует нажимать на прибор до появления звукового сигнала. Устройство необходимо удерживать в зафиксированном положении до окончания звукового сигнала (обычно 1-3 с). По окончании прибор необходимо отвести от поверхности кожи.
Показатели измерения отображаются на дисплее в течение 30 с, после чего анализатор переходит в режим «ожидания». Для определения точных показателей процедуру рекомендуется повторить не менее 3-х раз на разных участках кожи. При этом необходимо выбрать среднее значение.
При отображении на табло символа «—» измерение требуется повторить, так как устройство, возможно, было удалено от поверхности кожи до окончания звукового сигнала. По окончании процедуры прибор необходимо убрать обратно в футляр, предварительно обработав подвижную головку спиртовым раствором. Устройство не требует выключения.
Меры предосторожности
При работе с устройством необходимо соблюдать меры предосторожности. Таким образом, не рекомендуется пользоваться анализатором лицам, не ознакомившимся с инструкцией и правилами работы с прибором.
Также запрещается подвергать устройство каким-либо механическим повреждениям, ударам. Не следует открывать футляр (упаковку) с анализатором в теплых помещениях после длительного пребывания на морозе. Рекомендуется соблюдать интервал не менее 4 ч.
При проведении анализа необходимо выполнять меры профилактики и предосторожности по обработке рабочего элемента устройства спиртовым раствором. Прибор рекомендуется хранить в оригинальной упаковке.
Где купить Билитест, цена
Билитест можно приобрести в любом специализированном магазине медтехники ил аптеке. Стоимость аппарата для новорожденных зависит от региона продаж и торговой сети. Цены на устройство варьируются от 105 до 175 тыс. руб.
Оформление статьи: Владимир Великий
Видео о билитесте
Обзор Билитеста АГФ 02:
Как сделать анализ на билирубин у новорожденного малыша не сдавая кровь? Аппарат Билитест позволяет определить уровень билирубина без прокола кожи и взятия крови на анализ. Билитест – уникальная разработка мирового класса.

Билитест это прибор отражательного типа, который измеряет степень желтизны подкожных тканей ребенка в зависимости от уровня билирубина. Используется два оптических канала измерения для более точного результата и снижения влияния пигментации и других параметров кожи ребенка на показатели теста. Проведение теста абсолютно безболезненно, занимает несколько секунд.
Как определить уровень билирубина с помощью Билитеста
Чтобы определить уровень билирубина в крови малыша с помощью Билитеста, необходимо всего лишь приложить головку прибора к коже ребенка на 1-2 секунды. Результат сразу виден на экране анализатора в единицах транскутанного билирубинового индекса (ТБИ), имеющему высокую степень корреляции с концентрацией сывороточного билирубина. Чтобы перевести результаты в мкмоль/л достаточно умножить показания прибора на 10. Обычно делают 3 замера: на лобике, на грудке и на ручках или ножках. Стоимость процедуры – 300 рублей.
СПЕЦПРЕДЛОЖЕНИЕ
ПОСМОТРЕТЬ ЦЕНЫ √ РАСПИСАНИЕ РАБОТЫ
Записаться на прием, получить консультацию:
+7 (423) 267-61-30; +7 (423) 274-32-22; +7 914-704-32-22.
Записаться на приём он-лайн:
Если остались вопросы, задайте их в форме комментариев ниже↓↓↓
Билитест для замера билирубина в кожных покровах нужен новорожденным при желтухе. Прибор представляет собой кожный анализатор, его прижимают к коже в трех местах (лоб, грудина и пятка) и сразу на табло высвечивается показатель. Его умножают на 10 и получают содержание желчного пигмента в крови.
У ребенка бывает естественное повышение и тяжелая ядерная желтуха, их отличить помогает Билитест, с его помощью контролируют лечение. Так как прибор очень дорогой (от 125 000 рублей), а нужен он не более 2 недель, то целесообразно взять его в аренду или вызывать специалиста с тестером на дом. Часто он предлагается вместе с лампами для фототерапии.
📌 Содержание статьи
- 1 Причины для измерения билирубина Билитестом
- 1.1 Достоинства и недостатки прибора
- 1.2 Нужна ли подготовка перед замером
- 1.3 Как измеряют у детей Билитестом
- 1.4 Меры предосторожности
- 2 Норма билирубина по Билитесту
- 3 Где измерить билирубин новорожденному Билитестом в Москве
- 4 Цена на прибор
- 5 Альтернативные методы измерения
- 6 Полезное видео
Причины для измерения билирубина Билитестом
Уровень билирубина Билитестом измеряют в стационаре при желтухе новорожденных для:
- отличия физиологической (неопасной формы) от крайне тяжелой ядерной с разрушением клеток мозга;
- контроля за лечением;
- определения возможности выписки из роддома;
- выявлении детей для углубленного обследования.
В домашних условиях Билитест используется для детей с физиологической желтухой, которым назначена фототерапия (световое лечение) или медикаменты.

А здесь подробнее о вариантах ламп от желтухи для новорожденного.
Достоинства и недостатки прибора
К достоинствам прибора относятся:
- простота использования;
- точность измерений, особенно при высоких показателях;
- прибор готов к работе, не нужного настраивать, работает от батареек;
- отличает билирубин и гемоглобин эритроцитов;
- можно повторить замер по мере необходимости несколько раз;
- не требуется забор крови у новорожденного;
- очень быстро узнают результата.
Недостатками кожного анализатора считают:
- погрешности при уровне желчного пигмента ниже 80 мкмоль/л;
- неточность показателей при слишком светлой или смуглой кожей;
- определяет только уровень общего билирубина, если нужно узнать его прямую и непрямую часть, то требуется пройти стандартный лабораторный анализ.
Нужна ли подготовка перед замером
Датчик прибора Билитест перед замером нужно протереть спиртовой салфеткой, а потом чистой сухой тканью, другой подготовки не нужно, так как прибор полностью готов к работе. Ребенку также не требуются особые ограничения, но для более точного контроля лучше всего замеры проводить через час после утреннего пробуждения до еды. Можно выбрать и другое удобное время с 7 до 12 часов.
Как измеряют у детей Билитестом
Чтобы измерить показатели билирубина Билитестом, нужно его прижать к коже ребенка под прямым углом и немного нажать. Обязательно следует дождаться звукового сигнала и после этого посчитать до двух. Потом надо снять анализатор с кожных покровов и сразу (на протяжении 30 секунд) зафиксировать значения на табло. Затем прибор переходит в режим ожидания.
Для точного определения важно провести не менее 3 измерений в разных точках и рассчитать средний показатель. Для ребенка берут чаще всего лоб, грудину, пятку.
Если прибор рано убрать от кожи, то на табло появится тире, что требует повторного кожного анализа. Ребенок при замерах может лежать на спине или быть на руках у родителя, прибором можно пользоваться и во время сна, так как измерения Билитестом не вызывают дискомфортных ощущений.
Меры предосторожности
Для того чтобы кожный анализатор билирубина работал правильно, нужно:
- перед началом измерений полностью изучить инструкцию;
- проводить замеры в местах с тонкой подкожной прослойкой (лоб, грудина, пяточная кость);
- оберегать Билитест от ударов, не помещать под яркий свет, хранить только в коробке;
- перед каждым исследованием протирать датчик спиртом;
- при поломках не пытаться разбирать и чинить самостоятельно;
- не открывать коробку в теплом помещении после транспортировки по морозу, следует выдержать в закрытой упаковке не менее 4 часов.
Норма билирубина по Билитесту
Норма билирубина по Билитесту не отличается от показателей, определенных по крови. Нужно только учитывать, что показатель на табло всегда умножают на 10 и получают уровень общего билирубина в крови в единицах мкмоль/л. Норма билирубина у новорожденных в крови и в коже по Билитесту указана в таблице.
|
Возраст новорожденного |
Уровень в крови мкмоль/л |
Показатель Билитеста |
|
В первые сутки |
50-60 |
5-6 |
|
С 2 по 7 сутки |
До 256 |
До 25 |
|
С 7 до 14 дней |
60-100 |
6-10 |
|
К концу 1 месяца |
До 20,5 |
До 2 |
Если билирубин по Билитесту у новорожденного высокий, то причинами этого могут быть:
- физиологическая желтуха из-за разрушения эритроцитов с фетальным гемоглобином (образованным до рождения);
- резусный конфликт с кровью матери;
- вирусный гепатит, в том числе врожденный;
- врожденные болезни с нарушением ферментов печени;
- недоношенность с незрелостью систем обезвреживания желчного пигмента;
- сниженная функция щитовидной железы;
- родовая травма;
- сахарный диабет у матери;
- врожденное сужение желчных путей;
- ядерная желтуха с энцефалопатией (повреждение головного мозга).
Точный диагноз ставится только после полного обследования, определение уровня билирубина Билитестом не даст обнаружить заболевание, поэтому его недостаточно.
Где измерить билирубин новорожденному Билитестом в Москве
Измерения билирубина новорожденному Билитестом в Москве можно провести в медицинском центре «21 век», вызывать специалиста из предприятия «Билирент» (они предлагают и фотолампы напрокат) или «Армед 03», «Медалнэт». Стоимость одного измерения приблизительно составляет 150 рублей.
Цена на прибор
Билитест можно купить в магазинах медицинской техники по цене примерно 125 000 рублей. Его чаще всего приобретают медцентры, так как для ребенка в большинстве случаев он нужен не более 2 недель.
Альтернативные методы измерения
Билирубин в крови можно измерить путем традиционного анализа крови в лаборатории. Это наиболее точный метод, он помогает уточнить, за счет какой части (прямой или непрямой) произошло повышение, что помогает поставить диагноз. В стационаре есть и аппараты, которые могут определить уровень желчного пигмента и срочно при помощи анализатора Билимет М.

А здесь подробнее о том, как быстро снизить билирубин у новорожденного.
Уровень билирубина можно измерить у новорожденных кожным анализатором Билитест. Он не требует прокола кожи, быстро проводит замер, но для постановки диагноза нужен обычный анализ крови в лаборатории.
Полезное видео
Смотрите на видео о приборе Билитест:
Норма билирубина у новорожденных: лабораторные показатели и методы лечения
Билирубин у новорожденных
Что такое билирубин
Какие анализы надо сдать для проверки билирубина
— Самый точный способ определить уровень билирубина в крови – это биохимический анализ крови. Именно его назначит врач, если заподозрит развитие патологической желтухи, — говорит Анна Левадная, педиатр, кандидат медицинских наук, автор блога в Инстаграме о педиатрии. — Также существует чрезкожный тест – специальный прибор, который определяет через кожу примерный уровень билирубина в крови. Такой тест самый быстрый, но очень приблизительный, поэтому его используют как вспомогательный.
Но для того, чтобы отличить нормальную физиологическую желтуху от патологической, помимо показателя уровня общего билирубина в крови, врач должен учитывать и другие факторы, поэтому новорожденному могут быть назначены дополнительные анализы. Например, проверить уровень гемоглобина и эритроцитов. При физиологической желтухе эти значения остаются в норме. Также учитывается уровень прямого и непрямого билирубина в крови. При физиологической желтухе прямой билирубин составляет менее 20 процентов.
Норма билирубина у новорожденных
— Повышение уровня билирубина в крови отмечается почти у всех новорожденных в первые 3-4 дня жизни, — говорит Анна Левадная. — Примерно у половины доношенных и почти всех недоношенных детей это сопровождается окрашиванием кожи в желтушный цвет. Это заметно глазу, если уровень билирубина в крови выше примерно 68 мкмольл. При физиологической желтухе у доношенных детей общий билирубин составляет менее 256 мкмольл, у недоношенных — менее 171 мкмольл. Если эти цифры выше, а также есть ряд других признаков, например, более раннее появление и длительное нарастание желтухи, темная моча и обесцвеченный стул, анемия, то требуются дополнительные обследования.
Если говорить о норме билирубина в крови у новорожденного (доношенного), то следует ориентироваться на такие показатели.
Повышенный билирубин у новорожденных
Чем опасен
Как привести в норму
При физиологической желтухе, когда уровень билирубина превышен незначительно, ребенок хорошо себя чувствует, никаких мер по его снижению принимать не нужно. Уровень билирубина постепенно нормализуется, как правило, это происходит к концу первого месяца жизни.
Если речь идет о более серьезном состоянии, когда уровень билирубина в крови новорожденного выше 256 мкмоль/л, требуются дополнительные обследования и обязательное лечение.
— Современный метод снижения билирубина – это фототерапия, — говорит Анна Левадная. – Ее длительность и интенсивность зависят от массы тела ребенка при рождении, а также насколько превышены показатели билирубина. В тяжелых случаях новорожденному могут назначить обменное переливание крови. Необходимость переливания, его кратность и объем определяет врач. Отмечу, что назначение сорбентов, таких препаратов, как фенобарбитал, Эссенциале, ЛИВ-52, ультрафиолетовое обогащение крови, электрофорез или избыточная инфузионная терапия при повышенном уровне билирубина неэффективны, а для фенобарбитала и не безопасно.
Популярные вопросы и ответы
Где можно проверить билирубин?
По показаниям уровень билирубина определяют новорожденным в роддоме. Также это можно сделать в лаборатории. Если ребенок находится дома, и участковый педиатр заподозрит серьезное превышение билирубина и развитие патологической желтухи, то новорожденного направляют в стационар для проверки уровня билирубина, обследования и лечения.
Когда необходимо обращаться к врачу?
Патологическую желтуху в большинстве случае врачи диагностируют в родильном доме, так как для нее характерно более раннее появление. Тем не менее, если уровень билирубина долго не снижается, желтуха не идет на спад и не проходит к концу первого месяца жизни – это повод для обращения к врачу и обследования. Также должны насторожить появившиеся на этом фоне темная моча, обесцвеченный стул, бледность кожных покровов.
Почему может не помогать лечение?
Длительность и интенсивность фототерапии, которая применяется для лечения желтухи, как мы уже отмечали, индивидуальна, и зависит и от показателей билирубина и веса новорожденного. Лечение может не помогать, если оно подобрано некорректно. Но такие ситуации очень редки.
— Одной из причин сохранения высоких показателей билирубина в крови новорожденного может быть так называемая «желтуха от грудного молока», когда уровень билирубина повышается потому, что в организм ребенка попадают определенные гормоны вместе с материнским молоком, — говорит Анна Левадная. — При такой желтушке уровень билирубина может оставаться повышенным дольше, чем обычно — более 6 недель. Точный диагноз можно поставить, если при отмене грудного вскармливания на 2-3 дня уровень билирубина начинает снижаться. Если цифры невысокие, и визуально уменьшается проявление желтухи, то через сутки-двое грудное вскармливание возобновляют и продолжают. При этом, женщина не должна забывать регулярно сцеживаться во время паузы, чтобы сохранить лактацию.
Нужно ли отказываться от прививок при повышенном уровне билирубина?
Этот вопрос молодые мамы задают довольно часто, отказываются от прививки от гепатита Б, первую из которых должны сделать в роддоме, сразу после рождения.
— Физиологическая желтуха, когда показатели билирубина превышены не значительно, не является противопоказанием к плановой вакцинации, — объясняет наш эксперт. — Вакцинация от гепатита Б не может быть причиной повышения уровня билирубина, так как влияет на печень не больше, чем любая другая вакцинация.
Норма билирубина у новорождённого, а также 3 совета родителям после выписки
После рождения детей в их организме происходит множество разного рода процессов, способствующих адаптации ребёнка к жизни вне утробы матери. Одним из лабораторных показателей, который обращает на себя внимание у детей после рождения — это билирубин. Далее будут рассмотрены механизмы образования, выведения его из организма, а также представлены нормы билирубина у новорожденных.
Билирубин в крови новорождённого
Что такое билирубин
Билирубин – желчный пигмент. Он придаёт окраску желчи.
Где образуется и как выводится из организма
Билирубин является продуктом, до которого расщепляются железосодержащие белки в нашем организме, такие как гемоглобин и цитохромы. Если же рассматривать путь расщепления гемоглобина, то образуются следующие вещества: вердоглобин, затем биливердин, потом билирубин. Происходит это в результате действия системы фагоцитирующих мононуклеаров, например, в селезёнке.
Билирубин циркулирует в плазме крови вместе с альбумином. В такой форме он называется свободным (непрямым). Затем с током крови он приносится в печень. В печени происходит процесс конъюгации (связывания) с глюкуроновой кислотой. Такая форма с кислотой называется конъюгированным (связанным, прямым) билирубином. Далее он попадает в желчный проток и желчь.
Таким образом билирубин попадает в кишечник, где под действием кишечной микрофлоры превращается в мезобилирубин. Далее он может превращаться в уробилиноген и выводиться с мочой. Другой путь – образование стеркобилиногена, который выводится с каловыми массами. Все эти вещества придают окраску тому биологическому материалу, с которым они выводятся из организма.
Причины высоких цифр билирубина у новорождённых
У новорождённых в процессе адаптации организма впервые дни жизни происходит избыточное выведение стероидных гормонов, например, эстрогенов. Путь их инактивации такой же, как и у билирубина. Эстрогены трaнcпортируются в печень и подвергаются конъюгации с глюкуроновой кислотой. В связи с тем, что печень «занята» инактивацией другого вещества, то билирубин накапливается в организме ребёнка, что приводит к так называемой физиологической желтухе новорождённых.
Кроме того, гемоглобин плода менее устойчив в колебания pH крови. Сразу после рождения происходит массовое разрушение фетального (плодового) гемоглобина с замещением его на более устойчивую «взрослую» форму, что также значительно повышает уровень билирубина в организме.
Что укладывается в понятие «норма»
Физиологическая желтуха сохраняется в течение 3 – 5 дней, полностью приходит в норму уровень билирубина через 10 – 14 дней. Повышается уровень свободного билирубина. Норма билирубина у новорожденных будет представлена ниже.
При каких состояниях возможно чрезмерное повышение билирубина у новорождённых
Повышение уровня билирубина может входить в норму при физиологической желтухе новорождённых. Уровень билирубина также будет повышен у недоношенных детей.
Помимо этого, высокие цифры билирубина могут указывать на усиленный распад гемоглобина, вызванный различного рода факторами, например, в результате гемолитической анемии, при резус-конфликте или талассемии.
Если же билирубин не приходит в норму, это может говорить о наличии какой-либо патологии печени, токсическом воздействии или инфекционном агенте.
Читать еще: 20 советов беременным женщинам
Чем опасно чрезмерное повышение уровня билирубина в крови новорождённых
Как уже упоминалось ранее, билирубин оказывает токсичное действие на клетки нервной системы, что может привести к неврологическим симптомам. Чрезмерно высокие цифры билирубина могут привести к развитию ядерной желтухи — необратимо поражаются ядра головного мозга, что приводит к нарушению развития малыша в дальнейшем.
Как выполняется анализ крови
Для анализа крови на билирубин потребуется венозная или капиллярная кровь.
Откуда берётся кровь
В связи с анатомическими и физиологическими особенностями организма ребёнка в первые дни жизни кровь берётся из пяточки. Этого небольшого количества крови достаточно для проведения анализа.
Каким методом определяется уровень билирубина
Для определения уровня билирубина используется колориметрический метод, то есть окраска раствора прямо пропорциональна концентрации вещества в крови.
В настоящее время уровень билирубина определяется на автоматических анализаторах, что снижает вероятность ошибочного определения уровня анализируемого вещества в крови.
Расшифровка анализа
Норма билирубина у новорождённых по дням жизни
При рождении норма билирубина в крови ребёнка достигает 50 – 60 мкмоль/л. Затем его уровень может повыситься на 3 – 7 день. К 1 месяцу содержание билирубина достигает уровня нормы для взрослых. Норма билирубина у новорождённых таблица представлена ниже.
Таблица. Норма билирубина у мecячного ребёнка.
Билирубин у новорожденных — норма и предельные отклонения в таблице по дням
Из статьи узнайте,какова норма билирубина у детей, и какие могут быть последствия его повышения. Норма билирубина у новорожденных значительно отличается от допустимых значений для взрослых пациентов. Замер показателя входит в комплекс обязательных лабораторных анализов с первых дней жизни малыша.
При наличии видимой билирубинемии может применяться Билитест (фотометрический прибор для определения уровня билирубинемии у новорожденных).
Важно вовремя дифференцировать нормальное физиологическое повышение билирубина в крови у новорождённого от атрезии желчевыводящих протоков. И если первое состояние не представляет угрозы, то атрезия – опасна для жизни малыша.
Билирубин и его фракции
Билирубин образуется в селезёнке и костном мозге в результате гибели красных кровяных телец (эритроцитов). Максимальный срок жизни зрелых эритроцитов – 120 суток. После cмepти они разрушаются с выделением железосодержащей части – гема. Разрушение гема приводит к отщеплению двухвалентного железа, а оставшийся белковый компонент преобразуется в билирубин.
Функция билирубина в организме – клеточный антиоксидант. Он замедляет окислительные процессы, улучшая обновление и функционирование клеточной мембраны.
Также билирубин является важнейшим компонентом желчи.
Общий билирубин разделяется на 2 фракции:
- непрямую – пигмент желчи, продукт распада гема после деградации эритроцитов. Особое свойство: токсичность и способность проникать через гемато-энцефалический барьер. Не растворяется в жидкости и не выводится в чистом виде из организма. Доставляется в клетки печени (гепатоциты);
- прямую – комплекс непрямой фракции с сахаросодержащими веществами (глюкуроновой кислотой) образуется в печени. Фракция растворяется в воде и не токсична. После образования выводится в системный кровоток с желчью и доставляется в кишечный тракт.
Дальнейший метаболизм прямой фракции приводит к отщеплению кислоты с восстановлением до уробилиногеновых телец. Часть их повторно всасывается и возвращается в печень, а оставшееся количество подвергается преобразованию кишечной микрофлоры и выделяется с калом.
Билирубин у новорожденных – норма и предельные значения с первых дней жизни
Важно: расшифровка анализа требует строгого подбора величин нормы билирубина в крови у младенцев по дням жизни.
Определение величины нормы общего билирубина и каждой фракции в отдельности имеет высокую диагностическую значимость и применяется для дифференциальной диагностики патологий.
При помощи колориметрического фотометрического метода определяется норма общего билирубина и прямой фракции в крови у новорождённых и старших детей. Величина непрямой фракции рассчитывается по формуле: общий билирубин минус прямой.
Для расшифровки удобна наглядная таблица нормы билирубина у новорожденных по дням жизни. Данные актуальны для обоих полов.
Величина прямой фракции не должна превышать 5 мкмоль/л в анализе крови, оставшееся количество приходится на долю непрямой.
Максимально высокий билирубин у новорождённых наблюдается в первые 2-4 дня жизни и является вариантом физиологической нормы (при исключении атрезии).
Причины появления высокого уровня билирубина в неонатальном периоде
Высокий уровень билирубина у новорождённых – следствие физиологической (неотальной) желтухи, атрезии желчевыводящих протоков, ядерной желтухи и т.д. По статистике каждый второй малыш в первую неделю жизни переносит физиологическую желтуху, среди недоношенных новорождённых частота встречаемости увеличивается до 80 %.
Физиологическая желтушка у новорождённого
Состояние характеризуется типичными клиническими проявлениями:
- умеренное окрашивание белков и кожи ребёнка в желтоватый оттенок;
- снижение аппетита;
- легкая слабость и сонливость;
- высокий уровень билирубина в крови у новорождённого (не выходящий за верхнюю границу нормы);
- отсутствие признаков поражения ЦНС.
Причина – недостаточная развитость печени у новорождённого ребёнка, вследствие чего непрямая фракция не трaнcформируется в прямой билирубин в полном объёме. Постепенный запуск полноценной работы ферментативной системы способствует самопроизвольному исчезновению симптомов физиологической желтухи.
Максимальная выраженность симптомов характерна для 3-4 дня жизни малыша.
Требуется ли лечение физиологической желтухи? Если симптомы исчезают через 2 недели, при этом в анализе крови регистрируется абсолютная норма билирубина у новорождённых, то такое состояние не требует лечения.
Пациентам может быть показано пребывание на солнце или проведение коротких курсов фототерапии.
В случае усиления выраженности симптомов и их продолжительности более двух недель врачом определяется тактика лечения. Предпочтительный метод лечения – фототерапия. Малыша освещают специальными лучами синего света (длина волны находится в диапазоне от 460 до 490 нм), что ускоряет процесс разложения и выведения билирубина из организма.
Важно: синий свет абсолютно безопасен для младенца и не провоцирует побочные явления (в редких случаях может наблюдаться сухость кожи).
При патологических типах желтухи (ядерная желтуха с поражением центральной нервной системы, гемолитическая анемия и т.д.) показано экстренное лечение в отделении патологии новорожденных или реанимации.
При достижении критических показателей показано переливание крови.
Атрезия желчевыводящих путей
Патология встречается крайне редко, 1 случай на 20 тысяч новорождённых. Отмечено, что чаще атрезия регистрируется у девочек.
Болезнь характеризуется непроходимостью желчевыводящих путей или их полным отсутствием. Симптомы:
- желтовато-зелёный оттенок белков глаз и кожи младенца прогрессирующий со временем;
- неестественно бледный цвет каловых масс;
- моча приобретает тёмно-бурый цвет.
В первые дни жизни заболевание ничем не отличается от физиологической желтухи. Однако не исчезает с течением времени, при этом фототерапия и переливание крови не дают положительного терапевтического эффекта.
Причины до конца не установлены. Достоверно известно, что патология не является следствием побочного воздействия медикаментозных препаратов или прививок, которые вводились в организм матери во время беременности.
Непроходимость желчевыводящих протоков связывают перенесением беременной женщины инфекционного заболевания (гepпeс, цитомегаловирус или краснуха). В результате заражения клетки печени и эндотелий желчных протоков развивающегося эмбриона повреждаются. Впоследствии это приводит к разрастанию соединительной ткани и невозможности нормального тока желчи.
Встречаются единичные сведения, когда атрезия развивалась у младенца уже после рождения в результате инфекционного заражения и склерозирования желчных протоков.
Отсутствие желчевыводящих путей – результат мутации и неправильной закладки органа в процессе онтогенеза. Желчный пузырь также отсутствует или является единственным звеном наружных желчевыводящих путей.
Прогноз достаточно нeблагоприятный. Отсутствие своевременного и адекватного лечения сокращает жизнь ребёнка до 16 месяцев. Единственный метод терапии – хирургическое вмешательство: трaнcплантация печени или реконструкция желчевыводящих протоков. Благоприятный прогноз достигается в 30 – 40 % случаев.
Как подготовить ребёнка к анализу?
Биоматериалом для исследования является сыворотка венозной или капиллярной крови. Предпочтение следует отдавать венозной крови, поскольку для данного вида биоматериала значительно снижен риск сворачивания и гемолиза (разрушения эритроцитов в пробирке). Правильное взятие биоматериала для исследования позволяет избежать необходимости повторного забора крови, столь неприятного для малышей.
Для исключения ложных результатов важно правильно подготовить ребёнка к анализу. Новорождённым детям берут кровь перед кормлением или через несколько часов после него. Малышам от 3 до 7 лет рекомендуется сделать перерыв после последнего приёма пищи 3 – 4 часа и только потом идти в лабораторию. Старшим детям желательно выдержать 6 – 8 часов перед сдачей крови.
Читать еще: Можно ли взрослым детское питание при гастрите?
Важно: необходимо поить ребёнка большим количеством чистой негазированной несладкой воды. Подобное правило позволяет значительно облегчить процедуру взятия биоматериала.
Следует максимально успокоить ребёнка, поскольку эмоциональный стресс может негативно сказаться на достоверности полученных данных. Спокойно посидеть минут 15, после чего заходить в процедурный кабинет.
Лечение и профилактика
Что может сделать мама, чтобы снизить количество билирубина в крови ребенка? В первую очередь – успокоиться и подходить к лечению с адекватной точки зрения.
Для начала ребёнку определяются диагностические мероприятия с целью выявления причин отклонения показателя от нормы. Среди них: дополнительные лабораторные анализы (копрограмма, холестерол, альбумин, аланинаминотрaнcфераза, аспартатаминотрaнcфераза и т.д.), диагностика на наличие инфекции и инструментальные методы исследования (УЗИ).
После сбора полного анамнеза, включая наследственную предрасположенность к заболеваниям, врач устанавливает окончательный диагноз и подбирает методы лечения.
Контрольный замер показателей крови проводится во время лечения (в динамике) и после его окончания. Также может применяться Билитест (для ежедневного определения уровня билирубина у новорожденного).
При этом положительная динамика по возвращению показателя к нормальным значениям свидетельствует об эффективности выбранной тактики. Отсутствие положительного эффекта определяет необходимость коррекции и подбора альтернативных методов лечения.
В случае необходимости назначения медикаментозных препаратов важно учитывать их противопоказания и минимально допустимый возраст. Также оценивается степень риска от назначения лекарств и их предполагаемая польза. При этом польза должна существенно превосходить риски.
- норма билирубина в крови у новорождённых подбирается с учётом возраста, в первый месяц – в отдельности для каждого дня;
- у новорождённых малышей повышенный билирубин в большинстве случаев является вариантом физиологической нормы, крайне редко – тяжёлой патологии (атрезии);
- не следует самостоятельно пытаться понижать ребёнку билирубин, особенно народными средствами. Подобное поведение может значительно усугубить степень тяжести патологии и привести к необратимому нeблагоприятному исходу.
Юлия Мартынович (Пешкова)
Дипломированный специалист, в 2014 году закончила с отличием ФГБОУ ВО Оренбургский госудаственный университет по специальности «микробиолог». Выпускник аспирантуры ФГБОУ ВО Оренбургский ГАУ.
В 2015г. в Институте клеточного и внутриклеточного симбиоза Уральского отделения РАН прошла повышение квалификации по дополнительной профессиональной программе «Бактериология».
Лауреат всероссийского конкурса на лучшую научную работу в номинации «Биологические науки» 2017 года.
Билирубин у новорожденных: норма, решение проблемы высокого показателя
Человек, в ходе своего взросления, проходит пять периодов развития, по мнению специалистов. Первый и второй – это дети новорожденные и период грудного вскармливания, третий – этап прорезывания молочных зубов, четвертый младший школьный возраст и пятый – старший школьный возраст. Поговорим о самом первом периоде развития – новорожденных детях.
Новорожденные дети в течении 28 дней (столько длится этот период) проходят значительную адаптацию и перестройку организма. Все органы начинают деятельность, хотя многие из них функционировать начали еще внутриутробно. Новорожденный с эндогенного способа питания переходит на автономный эндогенный. При этом некоторые естественные процессы в организме требуют к себе внимательного наблюдения со стороны матери ребенка и медперсонала.
Болезни периода новорожденных также имеют принципиальные особенности. Поговорим сегодня о физиологической желтухе или другими словами высокий билирубин у новорожденного. Физиологическая желтуха встречается у 60-70% новорожденных. Появляется после рождения на третий день и начинает угасать на 8-10 день. В отдельных случаях отмечается желтушное окрашивание на 2, а то и больше недели. Относительная незрелость печени и бурный распад эритроцитов обуславливает выработке билирубина.
Что такое билирубин у новорожденных
Билирубин – это один из элементов разложения гемоглобина (плодный гемоглобин является доминирующим в организме новорожденного, на момент рождения 80-85%). Вектор процесса следующий: эритроциты в период распада способствуют высвобождению гемоглобина, который вследствие этого распада принимает форму токсичности. Организм начинает профилактику токсинов, под действием ферментов выводится билирубином.
Норма билирубина у новорожденных
Коэффициент билирубин у новорожденных изменяется с момента первого дня рождения, его норма и предел показывает, какой показатель желтушного пигмента имеется в крови. Значение билирубина у новорожденных определяет, следует ли применять медикоментозное лечение.
В первую очередь, что должен сделать лечащий врач – это взять кровь на билирубин у новорожденных. Если показатели весомо отличаются от нормы, то этот факт свидетельствует о наличие патологических видов желтухи.
Состав билирубина в крови имеется всегда, но при его повышении, следует учитывать меры, благодаря которым можно способствовать его понижению. Итак, рассмотрим билирубин у новорожденных в таблице его нормы.
Для периода недоношенности у ребенка характерны особые состояния и показатели билирубина будет отличаться от указанной нормы выше в таблице. Весь этот процесс требует гигиенических условий и тщательного ухода за новорожденным, а также правильно организации грудного или искусственного вскармливания.
Обычно общее состояние недоношенных детей с повышенным показателем билирубина проходит сложнее, чем у доношенного ребенка. Все потому что билирубин для недоношенного младенца более токсичен, это связано с неразвитой нервной системой. Верхний предел уровня для них 171 мкмоль/л.
Значения нормы билирубина по дням и месяцам. Таблица
Уровень билирубина у новорожденного может меняться в зависимости от прожитых дней и месяцев. Билирубин подразделяется на два вида: прямой (растворимый) и непрямой (не растворимый). Нерастворимый билирубин не выводится с мочой. Соединяясь с белком альбумином поступает с кровотоком в печень, где он полностью поглощается и вследствие образуется прямой билирубин, который уже выводится с мочой.
Большинство детей переносят в первые дни жизни относительно физиологическую желтушку. Если показатели слишком завышены, то это говорит о том, что физиологическая желтуха здесь не диагноз. Лечение должно проходить в более тщательном обследовании новорожденного.
Способы определения билирубина
При определении билирубина, параметры исследуются по трем признакам: общий, прямой, непрямой. Отмечается при нормальном состоянии не больше 25 % прямого от общего параметра билирубина.
Уровень билирубина определяется тремя способами:
- Самый точный уровень билирубина у новорожденных определяется анализом крови на голове малыша из вены. Чем больше срок желтухи, тем вероятнее всего, что такой анализ необходимо сделать;
- Определение билирубина с помощью билитеста (устройство определяющее уровень желчного пигмента);
- Правило Крамера. Основывается на распространении желтого окраса: сначала на лице, потом по всему телу.
Билирубин при физиологической и патологической желтухе
Рассмотрим профилактику лечения при двух видах желтухи: физиологическая и патологическая.
При слабой быстротечной желтухе методы лечение не предпринимаются. В случае физиологической, билирубин в сыворотке крови наблюдается в допустимой норме. Она несете угрожающей опасности для здоровья новорожденного. Но есть вероятность, если должным образом не предоставить для малыша уход и грамотное питание, она может развиться в патологическую.
Кроме прикладывания малыша к гpyди, требуется по мере возможности подключить специальную ультрафиолетовую лампу над ребенком. Такая фототерапия быстро избавиться от желтого пигмента и, следовательно, снизит уровень билирубина. Под ее действием билирубин распадается на нетоксичные компоненты, которые в дальнейшем легко выводятся организмом.
В ряде случаев патологическая желтуха, которая требует срочной госпитализации, встречается у:
- Несовместимость крови матери и плода;
- При разных осложнениях в период беременности;
- Конфликт резус-фактора ребенка и матери;
- У недоношенных детей.
При сильно повышенном коэффициенте билирубина в крови может развиться билирубиновая энцефалопатия. Она развивается на высокого токсического воздействия на нервные ткани головного мозга.
Билирубиновая энцефалопатия может развиваться с сильно выраженной концентрации билирубина в сыворотке крови. На первых днях проявления желтушного окраса необходимо прикладывать новорожденного к гpyди.
Молозиво, образующее у матери, способно приводить процесс oпopoжнения активно без задержек в мочевом и кишечнике. Следовательно, билирубин не сможет задерживаться в организме надолго.
Барьер между кровеносной и нервной системой дает защиту от токсического воздействия. Когда билирубин выше нормы этот барьер становится проницательным, в следствии ткань мозга становится восприимчивой к токсинам.
Чтобы избежать такого диагноза рекомендовано каждый день следить за уровнем билирубина в крови.
Основные действия при повышенном билирубине
Из всего вышесказанного следует сделать несколько выводов:
- Ни в коем случае не заниматься самолечением;
- Если уровень билирубина 290 и выше ребенок нуждается в срочной медицинской помощи;
- Если наблюдаете желтый окрас кожи на протяжении 3 недель, при этом кал бесцветного оттенка, а моча темного цвета, это признак врожденного заболевания мочевыводящих путей.
- До семи дней желтушка в большинстве случаев сама по себе проходит и не требует особого лечения, главное консультироваться у детского лечащего врача.
Читать еще: Искусственные роды — показания к прерыванию беременности, проведение процедуры и последствия
Профилактика повышения билирубина у новорожденных
Мама должна позаботиться о своем малыше еще тогда, когда он находится в утробе. Она должна знать, от чего у новорожденных появляется желтушка. Поэтому ей не следует бездумно употрeблять вредную для печени пищу, чтобы не навредить ребенку. Желательно соблюдать сбалансированную диету с высоким содержанием железа и других полезных веществ, чтобы способствовать нормальной работе печени и кишечника. И естественно, во время беременности о вредных привычках лучше забыть.
Обязательно необходимо наблюдаться у врача во время беременности, чтобы он мог контролировать содержание антител в крови матери, выявлять инфекционные заболевания и вовремя их лечить.
Естественные роды без каких-либо обезболивающих часто помогают избежать возникновению желтухи у младенца.
Важно прикладывать к гpyди ребенка сразу после того как он родился. Чем чаще мама будет кормить ребенка своим молоком, тем меньше вероятности пострадать от желтухи.
Солнечный свет является отличной профилактикой от желтухи у младенца, так как под воздействием света билирубин быстрее выводится из организма. Младенцу полезно принимать солнечные ванны.
Ни в коем случае нельзя допускать возникновение запоров у новорожденного, так как токсины будут всасываться в кишечник и отравлять его.
Если вам сообщили медработники, что у вашего малыша повышена норма билирубина в крови, не отчаивайтесь и не отказывайтесь от лечения врачей. Все же довериться доктору – это лучше, чем прибегнуть к самолечению, поскольку неизвестно какие могут быть последствия. Особенно лишним будет придерживаться мнения других мам, так как каждый ребенок индивидуален и требует к себе особого внимания и определенного лечения.
Какой должен быть уровень билирубина у новорожденных: таблица норм по дням
Повышенный билирубин у новорожденных – достаточно актуальная проблема. Практически у половины малышей в первые 7-10 дней жизни проявляются первые признаки желтухи.
Кожа и слизистые поверхности (склеры глаз, поверхность языка и другие) могут приобрести в первые дни жизни младенца желтоватый оттенок. Подобное проявление является вполне нормальным.
Но это не означает, что перечисленные признаки можно пустить на самотек. Если не уделять желтухе новорожденных внимание, она может приобрести хронический характер и вызвать развитие осложнений.
Виды пигмента в организме
Билирубин является желчным пигментом зеленовато-желтого цвета. Он образуется в результате распада отживших свой срок плодных кровяных клеток (эритроцитов), которые после рождения становятся бесполезными для малыша.
Поскольку печень младенца является незрелой, она не способна справиться с полным объемом нагрузки и переработать весь объем отмерших кровяных телец.
Билирубин, присутствующий в крови малыша, может быть 2 видов:
- прямой (связанный). Выводится из организма с калом и мочой. Это растворимое в воде вещество, которое образуется в печени и без проблем выходит из организма;
- непрямой (свободный). Вступает в соединение с альбумином и поступает в печень, после чего переpaбатывается органом и выводится из организма вместе с продуктами распада (моча и кал) точно так же, как и прямой. Является нерастворимым в воде. Когда этот фермент попадает внутрь клеток, происходит нарушение работы клеточных механизмов, в результате чего начинается токсичное воздействие свободного билирубина на организм.
Также специалистами используется такое понятие, как общий билирубин. Это сумма промежуточных продуктов (связанного и свободного) в сыворотке крови.
Какой уровень билирубина в крови у новорожденного считается нормальным?
Нормой для рожденных в срок малышей является показатель 256 мкмоль/л. Если малыш появился на свет недоношенным, нормальной считается цифра 171 мкмоль/л.
При этом кожные покровы, склеры глаз и слизистая могут все равно иметь желтоватый оттенок, не представляя опасности для жизни и здоровья крохи. Как правило, подобная пигментация проходит сама по себе уже через 7 – 10 дней после появления малыша на свет.
Критическим показателем для рожденных в срок детей принято считать цифру 324 мкмоль/л, а для недоношенных крох – 150-250 мкмоль/л. При таких результатах специалисты обычно настаивают на проведении медикаментозного лечения. И их опасения и требования вполне оправданы. Отсутствие лечения может спровоцировать развитие серьезных осложнений или патологий хронического характера.
Таблица норм по дням
С течением времени количество плодного гемоглобина в организме уменьшается. Печень постепенно переpaбатывает отмершие кровяные тельца, в результате чего кожные покровы и слизистая приобретают нормальный оттенок, а состояние крохи нормализуется.
Получить полную информацию о допустимых показателях можно, просмотрев данные таблицы.
Таблица норм билирубина у новорожденных по дням:
Превышение указанных в таблице показателей является тревожным звоночком для специалистов. В подобных случаях требуется незамедлительное принятие медицинских мер и постоянный контроль за состоянием ребенка.
Верхний предел и отклонения от нормы
Верхним пределом билирубина у новорожденных являются указанные в таблице показатели нормы для младенцев в соответствии с днями жизни. В случае существенных отклонений от нормы требуется обязательное вмешательство специалистов.
Медицинская помощь при повышенных показателях
Как правило, для малыша, у которого была обнаружена желтушка, достаточно будет обычного наблюдения со стороны специалистов. Зачастую симптомы исчезают спустя 1-2 недели даже без применения серьезного медикаментозного лечения.
Эффективным способом понижения билирубина в крови являются солнечные ванны.
Если ребенок родился весной или летом, мама может во время прогулки открывать капюшон коляски, чтобы солнечные лучи попадали на ручки, ножки и личико новорожденного. Зимой солнечных дней меньше, поэтому и обеспечить малыша естественными солнечными ваннами будет не так уж просто.
Если же родителям удалось поймать солнечный день, можно вынести кроху на улицу и подставить его лицо под лучи солнца. И зимой, и летом необходимо следить за тем, чтобы солнечные лучи не светили малышу в открытые глазки. Несмотря на очевидную пользу солнца, новорожденному нельзя находиться под прямыми солнечными лучами более 10 минут.
В летние дни не рекомендуется проводить солнечные ванны с 11 утра до 17 вечера. В этот период солнце особенно жесткое и может навредить здоровью ребенка.
Для устранения желтушки в роддоме также могут проводиться процедуры фототерапии. Для этого требуется специальное оборудование.
Малыша помещают под синюю лампу, лучи которой способствуют преобразованию токсичного билирубина в обычный и его безболезненному выведению из организма. При этом ребенку в обязательном порядке надевают на глаза специальные очки или шапочку, поскольку лучи лампы вредны для зрения.
После завершения процедуры у многих малышей наблюдается появление шелушащейся кожи или разжижение стула. В особо сложных случаях малышам могут быть поставлены капельницы и даже сделано переливание крови.
Профилактика развития желтухи у новорожденных
Кормление по требованию также считается эффективной профилактической мерой. Народная медицина советует мамам, дети которых страдают от желтушки, допаивать кроху отваром шиповника, сладкой водичкой и прочими напитками для младенцев.
Такое суждение является ошибочным. Ни один из перечисленных вариантов жидкости не сможет понизить уровень содержания в организме билирубина. Лучше чаще прикладывать малыша к гpyди. В данном случае молоко мамы является лучшим профилактическим и лечебным средством для нормализации повышенного уровня билирубина.
Видео по теме
О последствиях и лечении повышенного билирубина в крови у новорожденного в видеоролике:
Билирубин является важным показателем здоровья как для взрослых, так и для малышей в первые дни жизни. Поэтому мамам новорожденных ни в коем случае не следует отказываться от сдачи крови новорожденного на анализ на билирубин.
При этом родителям следует быть готовыми к тому, что показатель будет повышен, и не паниковать по этому поводу. Своевременно принятые меры по устранению патологии и полный контроль состояния здоровья крохи со стороны специалистов позволят быстро избавиться от нарушения, исключив развитие осложнений и хронических патологий.
Важно знать родителям о здоровье:
FitoSpray для похудения (Фитоспрей)
FitoSpray для похудения ( Фитоспрей) FitoSpray — спрей для похудения Многие мечтают похудеть, стать стройными, обрести фигуру мечты. Неправильное питание,…
09 07 2023 1:56:24
Фитостеролы в продуктах питания
Фитостеролы в продуктах питания Фитостерины Существует много питательных веществ, которые, как утверждают исследователи, могут положительно повлиять на…
08 07 2023 4:20:10
Фитотерапевт
Фитотерапевт Фитотерапевт Я, Ирина Гудаева — травница, массажист, ведущая семинаров по созданию натуральной косметики и курса « Практическое травоведение»…
07 07 2023 13:35:43
Fitvid
Fitvid Брекеты: минусы, трудности, проблемы Брекет-системы помогли избавиться от комплексов миллионам людей. Это действительно эффективный инструмент,…
06 07 2023 8:37:38
Фониатр
Фониатр Фониатрия – один из разделов медицины. Фониатры изучают патологии голоса, методы их лечения, профилактики, а также способы коррекции…
03 07 2023 12:44:52
Форель
Форель Форель относится к отряду лососеобразных, семейству лососевых. Ее тело удлинено, немного сжато с боков, покрыто мелкой чешуей. Замечательной…
02 07 2023 9:33:33
Формула идеального веса
Формула идеального веса Калькулятор нормы веса Вес 65 кг относится к категории Норма для взрослого человека с ростом 170 см . Эта оценка основана на…
29 06 2023 3:41:18
Формулы расчета идеального веса
Формулы расчета идеального веса Фoрмулa «идeальнoго вeса» То, что ожирение шагает семимильными шагами по планете – это факт. И, несмотря на то, что…
28 06 2023 1:46:42
Фосфатида аммонийные соли
Фосфатида аммонийные соли Аммонийные соли фосфатидиловой кислоты ( Е442) Е442 – это пищевая добавка, которую относят к категории эмульгаторов. Вещество…
27 06 2023 20:44:32
Фототерапия новорожденных
Фототерапия новорожденных Фототерапия новорожденных Применение фототерапии для новорожденных С момента своего рождения организм ребенка начинает адаптацию…
26 06 2023 2:30:55
Фототерапия новорожденных при желтухе
Фототерапия новорожденных при желтухе Фототерапия новорожденных После появления ребенка на свет его организм адаптируется к совершенно иным условиям…
25 06 2023 7:31:33
Французская диета
Французская диета Французская диета Эффективность: до 8 кг за 14 дней Сроки: 2 недели Стоимость продуктов: 4000 рублей на 14 дней Общие правила…
24 06 2023 13:53:51
Фрукт Кумкват — что это такое?
Фрукт Кумкват — что это такое? Фрукт Кумкват — что это такое? Впервые упоминают необычный для европейцев фрукт китайские летописи 11 века. Португальские…
23 06 2023 18:53:39
Фруктовая диета
Фруктовая диета Фруктовая диета Эффективность: 2-5 кг за 7 дней Сроки: 3-7 дней Стоимость продуктов: 840-1080 рублей в неделю Общие правила Фруктовая…
21 06 2023 5:43:33
Фруктоза при диабете
Фруктоза при диабете Можно ли фруктозу при сахарном диабете? Для многих диабет является той проблемой, которая вносит в жизнь ряд ограничений. Так, к…
18 06 2023 23:26:41
Фрукт свити – польза и вред
Фрукт свити – польза и вред Свити — что это за фрукт? Что такое свити? Продолжаем разбирать цитрусовые, но как всегда идем не по верхам, а копаем глубже и…
15 06 2023 19:48:19
Фрукты и ягоды
Фрукты и ягоды Разница между фруктом и ягодой Фрукты и ягоды любят практически все. Ведь они такие вкусные и полезные! Мы любуемся лежащими на столе…
14 06 2023 6:18:58
Фтизиатр
Фтизиатр Врачи фтизиатры Москвы Фтизиатр — это дипломированный специалист в области фтизиатрии. Он специализируется на профилактике, диагностике, лечении…
12 06 2023 15:21:12
Фтор в организме человека
Фтор в организме человека Фтор в организме человека Дневная норма потрeбления Мужчины старше 60 лет Женщины старше 60 лет Беременные (2-я половина)…
11 06 2023 17:55:13
Боли в спине после рождения ребёнка
Боли в спине после рождения ребёнка Почему после родов болит спина У мамочек нередко болит спина после родов. Причем, дискомфорт может длиться довольно…
08 06 2023 7:13:32
Фунчоза: польза и вред
Фунчоза: польза и вред Фунчоза: польза и возможный вред Увлечение восточной кухней год от года растет. Принято считать, что такой рацион полезен для…
07 06 2023 12:21:24
Фундук
Фундук В рационе здорового человека обязательно присутствуют орехи в различных вариациях. Среди них выгодно выделяется фундук. Высокая пищевая ценность и…
06 06 2023 12:54:25
Фуросемид таблетки инструкция по применению
Фуросемид таблетки инструкция по применению Инструкция по применению: Цены в интернет-аптеках: Фуросемид – синтетическое диуретическое лекарственное…
03 06 2023 16:11:45
Галактоза
Галактоза Галактоза – это представитель класса простых молочных сахаров. В человеческий организм поступает преимущественно в составе молока,…
02 06 2023 15:49:21
Галанга
Галанга С древних времен растения играют важную роль в жизни человека, в том числе и для поддержания здоровья. Некоторые травы известны как лучшие…
01 06 2023 15:48:11
Галега лекарственная
Галега лекарственная Галега лекарственная (Galega officinalis) Син: козлятник лекарственный, козлятник аптечный, козья рута, французская сирень, солодянка…
31 05 2023 21:57:51
Боли в суставах при беременности
Боли в суставах при беременности Боли в суставах при беременности В период беременности у женщины могут возникать различные боли в самых разных местах….
28 05 2023 14:18:43
Гастрит и изжога
Гастрит и изжога Лучшие лекарства от изжоги и гастрита Многие пациенты с гастритом и другими заболеваниями Ж К Т страдают от изжоги. Данный симптом может…
27 05 2023 4:53:57
Где находится ключица у человека на фото?
Где находится ключица у человека на фото? Ключица человека: анатомия, строение, функции Ключица – это единственное костное образование в теле человека,…
24 05 2023 5:32:38