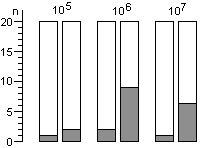В очередном выпуске рубрики #ДЕЗликбез расскажем о том, что такое индикаторы, для чего предназначены и как правильно их использовать.
Индикаторы – это полоски из пленки и термостойкой бумаги, они показывают, корректно или нет была проведена стерилизация. Индикаторы контролируют в случае паровой стерилизации – температуру, период ее воздействия, насыщенность водяного пара; при воздушном методе – температуру и срок ее воздействия.
На индикаторе есть маркировка и две цветные метки, одна из которых является индикаторной, а другая – эталоном сравнения.
Индикаторы бывают внешние и внутренние.
Внешние индикаторы для стерилизаторов
ВНЕШНИЕ индикаторы закладываются внутрь стерилизатора на полку по типу конверта в пять точек (по углам и в центре). Приклеивать индикаторы на лоток не нужно!
Если хоть одна индикаторная метка не достигла конечного цвета (не соответствует цвету эталона), это интерпретируется как отрицательный результат.
Если внешний индикатор показал отрицательный результат, то нестерильной считается вся загрузка проведенного цикла стерилизации.
Обратите внимание, что в этом случае стерилизатор требует технического осмотра и, возможно, ремонта. Не прогоревший индикатор может свидетельствовать о проблемах нагревательных элементов (тэнов), нарушении герметичности камеры стерилизатора и других неисправностях.
Индикаторы следует использовать во время каждого стерилизационного цикла. На один цикл нужно всего пять индикаторов независимо от того, сколько пакетов загружено в камеру.
Закладкой индикаторов занимается ответственное за дезинфекцию и стерилизацию лицо, назначенное приказом и прошедшее должное обучение (работа с автоклавом требует специальной подготовки — цикла обучения по работе с сосудами под давлением).
После использования внешний индикатор вклеивается в журнал контроля работы стерилизаторов. Этот документ используется как свидетельство правильно организованного дезинфекционно-стерилизационного режима и подлежит хранению в течение трех лет с момента окончания записей.
Внутренние индикаторы для стерилизаторов
ВНУТРЕННИЕ индикаторы закладываются в каждый пакет или клеятся на пакеты для стерилизации (крафт-пакеты), в зависимости от типа индикатора (внутренний или универсальный).
Сейчас в продаже есть пакеты как с индикаторами, так и без. Если вы приобрели пакеты для стерилизации без индикатора, вы обязаны приклеить его к пакету перед стерилизацией инструментов. При этом нужно понимать, что индикатор на пакете обычно I класса и показывает только то, что данный пакет нагревался, в то время как внутренние индикаторы обычно имеют IV класс и показывают, что пакет прошел полный цикл стерилизации.
Индикатор служит гарантом того, что внутри пакета были соблюдены все условия стерилизации, и инструмент можно считать стерильным.
Если внутренний индикатор дал отрицательный результат, то нестерильными считаются изделия только внутри данной упаковки. Например, из-за большого количества заложенных пакетов в сухожаре не было достаточной циркуляции нагретого воздуха.
Внутренние индикаторы не фиксируются ни в каком журнале, и их применение не освобождает от необходимости использования внешних индикаторов.
Надеемся, эта статья была полезной для вас! Если остались вопросы – спрашивайте в комментариях!
Посмотрите наше видео о том, как выглядят индикаторы и как их правильно использовать!
Утверждаю
Руководитель Департамента
госсанэпидемнадзора
Минздрава России
С.И.ИВАНОВ
от 18 декабря 2003 г. N 11-7/17-09
ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ ХИМИЧЕСКИХ ИНДИКАТОРОВ
ОДНОКРАТНОГО ПРИМЕНЕНИЯ (НПФ «ВИНАР», Г. МОСКВА)
ДЛЯ КОНТРОЛЯ УСЛОВИЙ СТЕРИЛИЗАЦИИ МЕДИЦИНСКИХ ИЗДЕЛИЙ
В ПАРОВЫХ И ВОЗДУШНЫХ СТЕРИЛИЗАТОРАХ
Согласовано:
Директор НИИ дезинфектологии
Минздрава России
академик РАМН
М.Г.ШАНДАЛА
15 сентября 2003 года
Генеральный директор
НПФ «ВИНАР»
В.С.АНДРЕЕВ
14 октября 2003 года
Инструкция разработана Государственным учреждением науки Научно-исследовательский институт дезинфектологии (ГУН НИИД) Минздрава России, Научно-производственной фирмой «ВИНАР» (НПФ «ВИНАР»).
Авторы:
от ГУН НИИД — Абрамова И.М., Дьяков В.В.
от НПФ «ВИНАР» — Иванов С.М., Андреев В.С., Червякова Н.Е.
Инструкция предназначена для персонала лечебно-профилактических учреждений (ЛПУ), работников дезинфекционной и санитарно-эпидемиологической служб, а также других учреждений, имеющих право осуществлять дезинфекционную деятельность.
1. ОБЩИЕ СВЕДЕНИЯ
1.1. Инструкция распространяется на химические индикаторы однократного применения (далее — индикаторы), разработанные и производимые НПФ «ВИНАР», предназначенные для химического метода контроля условий стерилизации медицинских изделий (далее — изделия), проводимой по соответствующим режимам в паровых и воздушных стерилизаторах, зарегистрированных в Российской Федерации и разрешенных в установленном порядке к применению в ЛПУ.
Примечание: индикаторы не предназначены для контроля условий стерилизации жидких лекарственных и иных средств в укупоренных сосудах.
1.2. Инструкция определяет действия персонала при контроле условий стерилизации с учетом типа индикатора, особенностей стерилизационного оборудования, вида стерилизуемых изделий.
1.3. В инструкции использованы термины и сведения, содержащиеся в российских и международных стандартах ГОСТ Р ИСО 11140, 11138, 11134, 13683, ИСО 14161 и EN 285.
1.4. Описываемые в инструкции индикаторы, в зависимости от типа, относятся к классу 1 (индикаторы процесса, или «свидетели»: индикаторы серий ИСПС, ИСВС), к классу 4 (многопараметрические индикаторы: индикаторы серий ИС, СТЕРИКОНТ-П и СТЕРИКОНТ-В, СТЕРИТЕСТ-П, ИНТЕСТ-П, МедИС) и к классу 5 (интегрирующие индикаторы серии СТЕРИТЕСТ-В) по классификации ГОСТ Р ИСО 11140 «Стерилизация медицинской продукции. Химические индикаторы. Часть 1. Общие требования».
1.5. Данные индикаторы зарегистрированы в установленном порядке Министерством здравоохранения Российской Федерации.
1.6. Целью применения индикаторов 1 класса является получение визуального отличия стерилизационных упаковок/стерилизационных коробок с изделиями, подвергнутых стерилизационной обработке конкретным методом, от еще не подвергнутых такой обработке. Применение данных индикаторов направлено на предотвращение смешения обработанных и необработанных стерилизационных упаковок или стерилизационных коробок.
Целью контроля условий стерилизации, осуществляемого с применением других индикаторов, указанных в п. 1.4 (индикаторы 4 — 5 класса), является подтверждение того, что при проведении цикла стерилизации критические параметры достигли определенных значений, требующихся для обеспечения стерилизации изделий соответствующим методом.
1.7. Критическими параметрами, то есть существенными для достижения надежной стерилизации и требующими контроля, являются:
— для воздушной стерилизации — температура стерилизации и время стерилизационной выдержки;
— для паровой стерилизации — температура стерилизации, время стерилизационной выдержки и наличие насыщенного водяного пара.
1.8. Для обеспечения эффективного контроля условий стерилизации, проводимого химическим методом с применением индикаторов 4 — 5 класса, необходимо контролировать:
— условия в камере стерилизатора снаружи стерилизационных упаковок/ стерилизационных коробок с изделиями (проведение наружного контроля с применением «наружного» индикатора);
— условия внутри стерилизационных упаковок/стерилизационных коробок с изделиями, в том числе внутри стерилизуемых изделий (проведение внутреннего контроля с применением «внутреннего» индикатора).
1.9. При проведении наружного контроля индикаторы 4 класса соответствующих типов, предназначенные для такого контроля, размещают снаружи стерилизационных упаковок или на бирках стерилизационных коробок со стерилизуемыми изделиями.
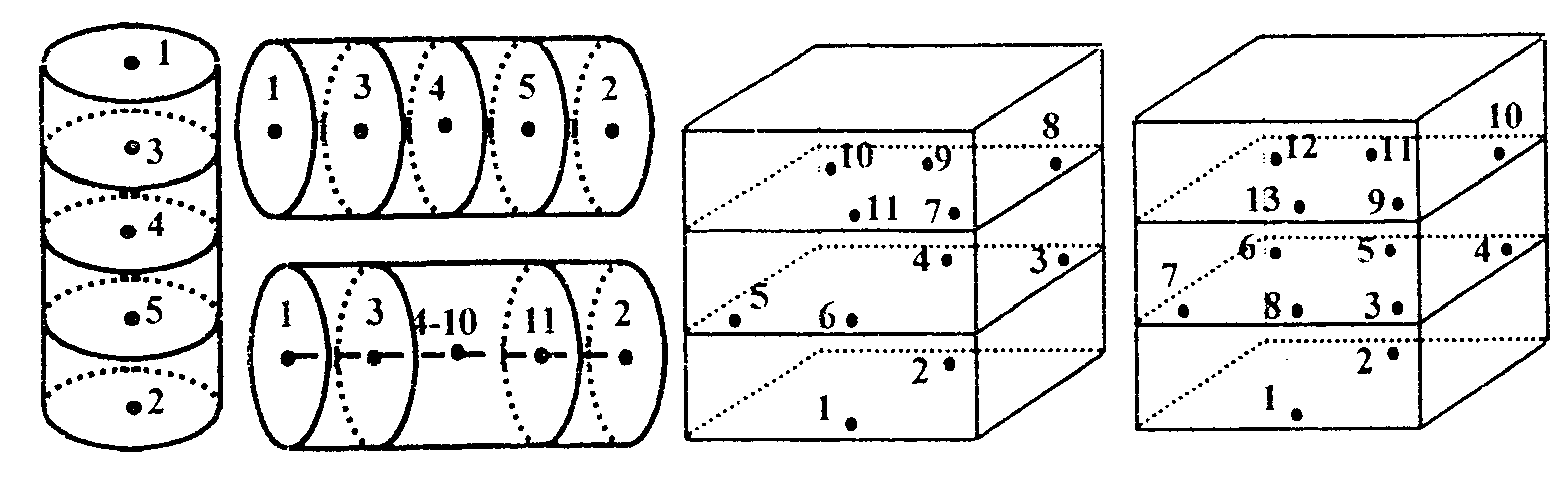
1.10. При проведении внутреннего контроля индикаторы 4 или 5 класса соответствующих типов, предназначенные для такого контроля, необходимо размещать в наиболее трудно стерилизуемых участках (зонах) загрузки, то есть в тех местах упакованных изделий, которые менее всего доступны для проникновения стерилизующего агента.
Примечание. Наиболее трудно стерилизуемыми участками загрузки являются:
— середина пористых изделий (центральная часть свертков из хлопчатобумажных материалов — сложенных простыней, халатов и т.п.);
— внутренние полости и каналы изделий из резин, пластмасс, стекла (внутренние полости пальцев резиновых перчаток, средняя часть каналов катетеров/зондов, полости пробирок, закрытых чашек Петри и т.п.).
1.11. При контроле условий снаружи стерилизационных упаковок/стерилизационных коробок с изделиями индикатор доступен для учета и документирования результата контроля персоналом, проводившим цикл стерилизации, сразу после завершения цикла стерилизации.
При контроле условий внутри стерилизуемых изделий индикатор доступен для учета и документирования результата контроля только при вскрытии упаковки с простерилизованными изделиями пользователем.
1.12. Индикаторы достигают конечного состояния, необратимо меняя цвет индикаторной метки при обеспечении определенных условий воздействия стерилизующего агента в цикле стерилизации.
1.13. Конечный цвет индикаторной метки индикатора 1 класса свидетельствует о том, что стерилизационные упаковки/стерилизационные коробки с изделиями подвергались стерилизационной обработке соответствующим методом, но не служит подтверждением достижения необходимых значений критических параметров в течение цикла стерилизации.
1.14. Конечный цвет индикаторной метки индикатора 4 — 5 класса подтверждает, что при проведении цикла стерилизации критические параметры достигли определенных значений, требующихся для стерилизации изделий соответствующим методом.
1.15. Изменение цвета индикаторной метки на конечный цвет (соответствие цвету эталона сравнения) интерпретируется как положительный результат и является основанием для разрешения применения простерилизованных изделий по назначению.
1.16. Если индикаторная метка не достигла конечного цвета (не соответствует цвету эталона), это интерпретируется как отрицательный результат.
Если отрицательный результат показал «наружный» индикатор, то нестерильной считается вся загрузка проведенного цикла.
Если отрицательный результат показал «внутренний» индикатор, то нестерильными считаются изделия внутри данной упаковки.
Изделия, отнесенные к нестерильным, запрещается использовать по назначению; они подлежат повторной стерилизации.
1.17. Применение индикаторов 4 — 5 класса позволяет обнаружить несоблюдение условий стерилизации, обусловленное технической неисправностью стерилизаторов, нарушением их загрузки, ошибкой в установке параметров режимов или их сбоем, и тем самым уменьшить риск использования изделий, подвергнутых стерилизационной обработке при значениях критических параметров, не соответствующих требуемым для конкретного метода и режима стерилизации.
1.18. Индикаторы можно использовать в качестве документа архива и подклеивать в рабочие журналы.
«Наружные» индикаторы подлежат осмотру непосредственно после завершения цикла стерилизации с последующим подклеиванием в журнал работы стерилизаторов (форма 257/у).
«Внутренние» индикаторы подлежат осмотру после вскрытия стерилизационной упаковки/стерилизационной коробки перед применением простерилизованных изделий. Эти индикаторы подклеивают, например, в операционный или процедурный журнал. Допускается (при децентрализованной стерилизации) их подклеивание в журнал работы стерилизаторов.
1.19. Химический метод контроля условий стерилизации должен применяться наряду с физическим (использование контрольно-измерительных и регистрирующих приборов) и биологическим (с применением биологических индикаторов) методами контроля.
Химическим методом, как и физическим, необходимо контролировать каждый цикл стерилизации.
Периодичность биологического контроля регламентируется специальными нормативными документами.
2. ИНДИКАТОРЫ ПАРОВОЙ СТЕРИЛИЗАЦИИ
2.1. Основные характеристики индикаторов паровой стерилизации медицинских изделий приведены в таблице 1.
Таблица 1
Характеристика индикаторов паровой стерилизации
|
Обозначение индикатора |
Вид индикатора |
Назначение индикатора |
Класс индикатора |
Контролируемые режимы стерилизации |
Метод удаления воздуха из стерилизационной камеры |
Цвет индикаторной метки |
Наличие и размещение эталона сравнения |
|
|
исходный |
конечный — цвет эталона сравнения |
|||||||
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
|
ИСПС-01 |
Этикетка с липким слоем (в листах) |
Индикатор — свидетель (для подтверждения факта проведения стерилизационной обработки) |
1 |
Все режимы паровой стерилизации |
Продувка паром или вакуумирование |
Желтый |
Коричневый |
Эталон отсутствует, конечный цвет обозначен словами |
|
ИСПС-02 |
Этикетка с липким слоем и дополнительными надписями (в листах) |
|||||||
|
ИС-120 |
Бумажная лента без липкого слоя (в рулоне) |
Наружный контроль |
4 |
120 °C, 45 мин |
Продувка паром |
От белого до светло-песочного |
От песочного до светло-коричневого |
Входит в виде отдельного отрезка ленты в комплект к каждому рулону ленты |
|
ИС-132 |
Бумажная лента без липкого слоя (в рулоне) |
Наружный контроль |
4 |
132 °C, 20 мин |
Продувка паром |
От белого до светло-песочного |
От песочного до светло-коричневого |
|
|
МедИс-120/45-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
120 °C, 45 мин |
Продувка паром |
Зеленый |
Коричневый <*> |
Нанесен на индикатор |
|
МедИс-120/45-02 |
Полоска с липким слоем |
|||||||
|
МедИс-126/30-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
126 °C, 30 мин |
Продувка паром |
Зеленый |
Коричневый <*> |
Нанесен на индикатор |
|
МедИс-126/30-02 |
Полоска с липким слоем |
|||||||
|
МедИс-132/20-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
132 °C, 20 мин |
Продувка паром |
Зеленый |
Коричневый <*> |
Нанесен на индикатор |
|
МедИс-132/20-02 |
Полоска с липким слоем |
|||||||
|
Стериконт-П-120/45-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
120 °C, 45 мин |
Продувка паром |
Желтый |
Сине-фиолетовый <*> |
Нанесен на индикатор |
|
Стериконт-П-120/45-01-1 |
Полоска с липким слоем |
|||||||
|
Стериконт-П-132/20-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
132 °C, 20 мин |
Продувка паром |
Желтый |
Сине-фиолетовый <*> |
Нанесен на индикатор |
|
Стериконт-П-132/20-01-1 |
Полоска с липким слоем |
|||||||
|
Стеритест-П-120/45-01 |
Полоска без липкого слоя |
Внутренний контроль |
4 |
120 °C, 45 мин |
Продувка паром |
Красно-оранжевый |
Темно-фиолетовый <*> |
Нанесен на индикатор |
|
Стеритест-П-120-45-02 |
Полоска с липким слоем |
|||||||
|
Стеритест-П-132/20-01 |
Полоска без липкого слоя |
Внутренний контроль |
4 |
132 °C, 20 мин |
Продувка паром |
Красно-оранжевый |
Темно-фиолетовый <*> |
Нанесен на индикатор |
|
Стеритест-П-132/20-02 |
Полоска с липким слоем |
|||||||
|
Интест-П-121/20-01 |
Полоска без липкого слоя |
Наружный и внутренний контроль |
4 |
121 °C, 20 мин |
Вакуумирование |
Красно-оранжевый |
Темно-фиолетовый <*> |
Нанесен на индикатор |
|
Интест-П-121/20-02 |
Полоска с липким слоем |
|||||||
|
Интест-П-126/10-01 |
Полоска без липкого слоя |
Наружный и внутренний контроль |
4 |
126 °C, 10 мин |
Вакуумирование |
Красно-оранжевый |
Темно-фиолетовый <*> |
Нанесен на индикатор |
|
Интест-П-126/10-02 |
Полоска с липким слоем |
|||||||
|
Интест-П-134/5-01 |
Полоска без липкого слоя |
Наружный и внутренний контроль |
4 |
134 °C, 5 мин |
Вакуумирование |
Красно-оранжевый |
Темно-фиолетовый <*> |
Нанесен на индикатор |
|
Интест-П-134/5-02 |
Полоска с липким слоем |
|||||||
|
Примечания: <*> Конечный цвет индикаторной метки может быть темнее цвета эталона сравнения (вплоть до черного). |
2.2. Индикаторы паровой стерилизации разных классов и типов применяют в соответствии с таблицей 2.
Таблица 2
Контроль паровой стерилизации с помощью индикаторов
производства НПФ «ВИНАР»
|
Наименование индикатора |
Назначение индикатора |
Периодичность контроля |
Место размещения индикатора относительно упаковки |
Минимальное количество индикаторов, используемых в одном цикле |
Кто размещает индикатор в загрузке перед стерилизацией |
Кто проверяет состояние индикатора после стерилизации |
Документирование индикатора |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
ИСПС-01 |
Индикатор-свидетель |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
По числу стерилизационных упаковок и/или стерилизационных коробок |
Персонал, проводящий стерилизацию или осуществляющий упаковывание изделий |
Персонал, проводящий стерилизацию, и потребитель стерилизованных изделий |
Не применяется |
|
ИСПС-02 |
|||||||
|
ИС-120 |
Наружный контроль |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки (может быть размещен под крышкой коробки) |
2 шт. (в контрольных точках N 1, 2 по методическим указаниям N 287-113) |
Персонал, проводящий стерилизацию изделий |
Персонал, проводящий стерилизацию изделий |
В журнале работы стерилизаторов |
|
ИС 132 |
|||||||
|
МедИС-120/45-01 |
Наружный контроль |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
2 шт. (в контрольных точках N 1, 2 по методическим указаниям N 287-113) |
Персонал, проводящий стерилизацию изделий |
Персонал, проводящий стерилизацию изделий |
В журнале работы стерилизаторов |
|
МедИС-120/45-02 |
|||||||
|
МедИС-126/30-01 |
|||||||
|
МедИС-126/30-02 |
|||||||
|
МедИС-132/20-01 |
|||||||
|
МедИС-132/20-02 |
|||||||
|
СТЕРИКОНТ-П-120/45-01 |
Наружный контроль |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
2 шт. (в контрольных точках N 1, 2 по методическим указаниям N 287-113) |
Персонал, проводящий стерилизацию изделий |
Персонал, проводящий стерилизацию изделий |
В журнале работы стерилизаторов |
|
СТЕРИКОНТ-П-120/45-01-1 |
|||||||
|
СТЕРИКОНТ-П-132/20-01 |
|||||||
|
СТЕРИКОНТ-П-132/20-01-1 |
|||||||
|
СТЕРИТЕСТ-П-120/45-01 |
Внутренний контроль |
Каждый цикл |
Внутри стерилизуемых изделий и упаковок |
В зависимости от объема камеры стерилизатора (в контрольных точках N 3 и более по методическим указаниям N 287-113) |
Персонал, осуществляющий упаковывание изделий |
Персонал, вскрывающий упаковку/потребитель простерилизованных изделий |
В журнале работы стерилизаторов или процедурном журнале |
|
СТЕРИТЕСТ-П- 120/45-02 |
|||||||
|
СТЕРИТЕСТ-П-132/20-01 |
|||||||
|
СТЕРИТЕСТ-П-132/20-02 |
2.3. Индикаторы-свидетели паровой стерилизации химические самоклеющиеся одноразовые серии ИСПС
2.3.1. Индикаторы-свидетели ИСПС (ТУ 9443-018-11764404) относятся к индикаторам 1 класса и представляют собой этикетки с нанесенными на их лицевой (рабочей) стороне индикаторной меткой желтого цвета и надписью «коричневый», описывающей конечный цвет индикаторной метки после проведения цикла стерилизации. На обратной стороне индикаторов нанесен липкий слой, закрытый защитной (антиадгезивной) подложкой. Индикаторы представлены в двух модификациях:
— ИСПС-01 без дополнительных записей;
— ИСПС-02 — имеет дополнительные (служебные) надписи «Дата ___», «Стерилизатор ___» и «Загрузка ___», предназначенные для записи соответствующей информации.
2.3.2. Индикаторы предназначены для применения на стерилизационных упаковках или на бирках стерилизационных коробок со стерилизуемыми изделиями при каждом цикле паровой стерилизации с целью получения свидетельства ее проведения, позволяя в дальнейшем отличать упаковки/коробки, подвергнутые стерилизационной обработке, от необработанных.
Индикаторы соответствуют классу 1 по классификации ГОСТ Р ИСО 11140-1-2000.
2.3.3. Индикаторы снимают с антиадгезивной подложки и наклеивают на каждую стерилизационную упаковку на участок, легко доступный для визуального осмотра, и/или бирку стерилизационной коробки. На индикаторах ИСПС-02 записывают необходимую информацию.
Наклеивание индикаторов на упаковку осуществляет персонал, упаковывающий изделия для стерилизации, или проводящий стерилизацию.
2.3.4. Визуальный осмотр индикаторов после стерилизации осуществляет персонал, проводивший цикл стерилизации, и пользователь простерилизованных изделий перед вскрытием упаковок/коробок.
После стерилизации происходит необратимое изменение цвета индикаторной метки с желтого на коричневый. Это свидетельствует о том, что упаковки с изделиями были подвергнуты стерилизационной обработке. Конечный цвет индикаторной метки не является свидетельством достижения в камере стерилизатора условий, требующихся для стерилизации изделий.
Примечание. В зависимости от режимов стерилизации, типа стерилизаторов, а также особенностей освещения при визуальном осмотре индикаторов конечный цвет индикаторной метки может иметь различную интенсивность окраски — от коричневого до коричнево-черного.
2.3.5. При повторном использовании разрешенных для этого упаковочных материалов новые индикаторы целесообразно наклеивать рядом с отработавшими, что позволяет контролировать кратность использования упаковочного материала.
2.3.6. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении при температуре от плюс 5 °C до плюс 40 °C и относительной влажности до 85% в защищенном от солнечного света месте.
2.3.7. Гарантийный срок годности — 12 месяцев со дня изготовления индикаторов.
2.4. Индикаторы контроля паровой стерилизации серии ИС
2.4.1. Индикаторы ИС-120 и ИС-132 (ТУ 0443-004-11764404-96) представляют собой бумажную ленту, на лицевой (рабочей) стороне которой равномерно нанесен индикаторный слой от белого до светло-песочного цвета. На обратной (нерабочей) стороне ленты имеется маркировка в виде цветных наклонных полос: голубого цвета на индикаторе ИС-120 и зеленого цвета — на ИС-132. В комплект индикаторов входит эталон сравнения, показывающий конечный цвет индикатора (от песочного до светло-коричневого — в зависимости от партии индикатора) при соблюдении критических параметров стерилизации.
2.4.2. Индикаторы предназначены для контроля соблюдения критических параметров в камере паровых стерилизаторов, работающих с удалением воздуха методом продувки паром.
Контролируемые режимы стерилизации приведены в табл. 1. Индикаторы соответствуют классу 4 по классификации ГОСТ Р ИСО 11140-1-2000.
2.4.3. Расположение индикаторов в камере стерилизатора должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.).
2.4.4. Отрезок ленты длиной около 3 см закрепляют индикаторным слоем наружу с внешней стороны стерилизационной упаковки или на бирку стерилизационной коробки, помещаемой в контрольную точку. Закрепление осуществляют самоклеющейся лентой для паровой стерилизации.
Примечание. Допускается размещать индикаторы непосредственно под крышкой стерилизационных коробок, но не в толще стерилизуемых изделий.
2.4.5. Все операции с индикаторами: их размещение в стерилизационной камере, осмотр после окончания цикла стерилизации, интерпретацию результатов и документирование — осуществляет персонал, проводящий стерилизацию.
Примечание. При размещении индикаторов под крышкой стерилизационной коробки указанные операции с индикаторами осуществляет пользователь, вскрывающий стерилизационную коробку.
2.4.6. Учет результатов контроля проводят, оценивая изменение цвета индикаторного слоя каждого индикатора. Если цвет индикаторного слоя всех индикаторов соответствует цвету эталона сравнения или темнее его, это свидетельствует о соблюдении требуемых значений критических параметров режима стерилизации.
Примечание. На индикаторном слое после проведения цикла стерилизации допускается наличие темных точечных вкраплений, не влияющих на общую индикаторную окраску.
Если цвет индикаторного слоя хотя бы одного индикатора светлее эталона сравнения, то это свидетельствует о несоблюдении требуемых значений критических параметров режима стерилизации в камере стерилизатора. В этом случае все изделия загрузки считаются непростерилизованными и подлежат повторной стерилизации.
ВНИМАНИЕ! Номера партии индикаторов и эталона сравнения должны совпадать. Во избежание неправильной интерпретации результатов не допускается использовать при учете результатов контроля индикатор и эталон сравнения разных партий.
2.4.7. Индикаторы следует хранить в упаковке изготовителя в отапливаемом помещении, при температуре не выше + 25 °C и относительной влажности не выше 90%, в защищенном от солнечного света месте.
2.4.8. Гарантийный срок годности — 12 месяцев с даты изготовления индикаторов.
2.5. Индикаторы контроля паровой стерилизации серии МедИС.
2.5.1. Индикаторы серии МедИС (ТУ 9398-027-11764404-2003) представляют собой бумажные прямоугольные полоски с нанесенными на одной стороне двумя цветными метками (индикаторная и эталон сравнения) и маркировкой. Зеленый цвет индикаторной метки необратимо меняется в зависимости от достигнутых значений критических параметров в течение цикла паровой стерилизации. Коричневый эталон сравнения показывает конечный цвет индикаторной метки при соблюдении требуемых значений критических параметров. Индикаторы представлены в двух модификациях:
— МедИС-120/45-01, МедИС-126/30-01, МедИС-132/20-01 — без липкого слоя;
— МедИС-120/45-02, МедИС-126/30-02, МедИС-132/20-02 — с липким слоем на обратной стороне индикатора, закрытым защитной бумагой.
2.5.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в каждом цикле стерилизации в камере паровых стерилизаторов с удалением воздуха методом продувки паром при размещении индикаторов снаружи стерилизационных упаковок и на бирках стерилизационных коробок со стерилизуемыми изделиями.
Контролируемые режимы стерилизации приведены в табл. 1.
Индикаторы соответствуют классу 4 по классификации ГОСТ Р ИСО 11140-1-2000.
2.5.3. Расположение индикаторов в камере стерилизатора должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.). Упаковки с прикрепленными индикаторами размещают в точках 1 и 2.
2.5.4. Для закрепления индикатора с липким слоем с его обратной стороны удаляют часть защитного бумажного покрытия, закрывающего липкий слой. Закрепление индикаторов осуществляют:
— при использовании комбинированных упаковок (прозрачная синтетическая пленка плюс бумага) — на пленку;
— при использовании бумажных пакетов — на заклеивающий клапан пакета;
— при использовании листовых бумажных оберточных материалов — на остающийся свободным после завертывания угол бумаги;
— при использовании стерилизационных коробок — на бирку коробки.
Для закрепления индикатора без липкого слоя используют самоклеющуюся ленту для паровой стерилизации, прикрепляя индикатор участком, свободным от цветовых меток.
Примечание. Для удобства закрепления индикатора без липкого слоя на стерилизационной коробке допускается вкладывать его в комбинированную упаковку или в бумажный пакет, которые затем прикрепляют к коробке самоклеющейся лентой для паровой стерилизации.
Все операции с индикаторами: их размещение, выемку, интерпретацию результатов и документирование — осуществляет персонал, проводящий стерилизацию.
2.5.5. После окончания цикла стерилизации оценивают изменение цвета индикаторной метки каждого индикатора. Если на всех индикаторах цвет индикаторной метки изменился на коричневый, соответствующий цвету эталона сравнения или стал темнее его, это свидетельствует о соблюдении требуемых значений критических параметров режимов стерилизации.
Примечание. Оттенки коричневого цвета эталона сравнения индикаторов разных партий могут иметь незначительные различия в пределах погрешности цветопередачи при печати (изготовлении) индикаторов.
Если индикаторная метка хотя бы одного индикатора полностью или частично сохранила зеленый или коричнево-зеленый цвет, легко отличимый от цвета эталона сравнения, это свидетельствует о несоблюдении требуемых значений критических параметров режимов стерилизации в камере стерилизатора, все изделия загрузки считаются нестерильными и подлежат повторной стерилизации. В этом случае проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров, переупаковывают изделия в новые упаковки (за исключением упаковок из материалов, допускающих повторную стерилизацию), заменяют все индикаторы в контрольных точках и подвергают изделия повторной стерилизации.
При повторении неудовлетворительных результатов контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
2.5.6. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении, при температуре от +5 °C до +40 °C и относительной влажности не выше 85%, в защищенном от солнечного света месте.
2.5.7. Гарантийный срок годности — 12 месяцев с даты изготовления индикаторов.
2.6. Индикаторы контроля паровой стерилизации серии СТЕРИКОНТ-П
2.6.1. Индикаторы СТЕРИКОНТ-П (ТУ 9443-007-11764404-01) представляют собой прямоугольные полоски бумажно-пленочного основания с нанесенными на него желтой индикаторной меткой и сине-фиолетовым эталоном сравнения. Индикаторы представлены в двух модификациях:
— СТЕРИКОНТ-П-120/45-01, СТЕРИКОНТ-П-132/20-01 — без липкого слоя;
— СТЕРИКОНТ-П-120/45-01-1, СТЕРИКОНТ-П-132/20-01-1 — с липким слоем.
2.6.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в каждом цикле стерилизации и камере паровых стерилизаторов с удалением воздуха из камеры методом продувки паром при размещении индикаторов снаружи стерилизационных упаковок или на бирках стерилизационных коробок со стерилизуемыми изделиями.
Контролируемые режимы стерилизации приведены в табл. 1.
Индикаторы соответствуют классу 4 по классификации ГОСТ Р ИСО 11140-1-2000.
2.6.3. Расположение контрольных точек должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.). Упаковки с прикрепленными индикаторами размешают в контрольных точках 1 и 2.
2.6.4. Для закрепления индикатора с липким слоем с его обратной стороны удаляют часть защитного бумажного покрытия, закрывающего липкий слой. Закрепление индикаторов осуществляют:
— при использовании комбинированных упаковок (прозрачная синтетическая пленка плюс бумага) — на пленку;
— при использовании бумажных пакетов — на заклеивающий клапан пакета;
— при использовании листовых бумажных оберточных материалов — на остающийся свободным после завертывания угол бумаги;
— при использовании стерилизационных коробок — на бирку коробки.
Для закрепления индикатора без липкого слоя используют самоклеющуюся ленту для паровой стерилизации, прикрепляя индикатор участком, свободным от цветовых меток.
Примечание. Для удобства закрепления индикатора без липкого слоя на стерилизационной коробке допускается вкладывать его в комбинированную упаковку или в бумажный пакет, которые затем прикрепляют к коробке самоклеющейся лентой для паровой стерилизации.
2.6.5. Все операции с индикаторами — их размещение, выемку, интерпретацию результатов и документирование — осуществляет персонал, проводящий стерилизацию.
2.6.6. По окончании цикла стерилизации цвет индикаторной метки каждого индикатора сравнивают с цветом эталона сравнения. При соблюдении требуемых значений критических параметров режимов стерилизации желтый цвет индикаторной метки должен необратимо измениться на темный сине-фиолетовый (конечный цвет). Если цвет индикаторной метки хотя бы одного индикатора полностью или частично сохранил желтый цвет, либо изменил цвет на зеленый, легко отличимый от цвета эталона сравнения, все изделия, обработанные в данном цикле, считают непростерилизованными. В этом случае проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров, переупаковывают изделия в новые упаковки (за исключением упаковок из материалов, допускающих повторную стерилизацию), заменяют все индикаторы в контрольных точках и подвергают изделия повторной стерилизации.
Примечания:
1. Оттенки темно-сине-фиолетового цвета эталона сравнения индикаторов разных партий могут иметь незначительные различия в пределах погрешности цветопередачи при печати (изготовлении) индикаторов.
2. В зависимости от особенностей освещения при учете результатов контроля конечный темный сине-фиолетовый цвет индикаторной метки может иметь различные оттенки темного сине-фиолетового вплоть до черного.
3. При любом освещении любые оттенки желтого или зеленого цвета индикаторной метки, не достигшей своего конечного цвета, имеют ясное визуальное отличие от цвета эталона сравнения.
При повторении неудовлетворительных результатов контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
2.6.8. Хранить индикаторы следует в упаковке изготовителя, в отапливаемом помещении, при температуре от + 5 °C до + 40 °C и относительной влажности не выше 85%, в защищенном от солнечного света месте.
2.6.9. Гарантийный срок годности — 12 месяцев со дня изготовления индикаторов.
2.7. Индикаторы контроля паровой стерилизации серии СТЕРИТЕСТ-П
2.7.1. Индикаторы СТЕРИТЕСТ-П (ТУ 9398-042-11764404-2003) представляют собой прямоугольные полоски бумажно-пленочного или пленочного основания с нанесенными на него красно-оранжевой индикаторной меткой и темно-фиолетовым эталоном сравнения. Индикаторы представлены в двух модификациях:
— СТЕРИТЕСТ-П-120/45-01, СТЕРИТЕСТ-П-132/20-01 — без липкого слоя;
— СТЕРИТЕСТ-П-120/45-02, СТЕРИТЕСТ-П-132/20-02 — с липким слоем.
2.7.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в каждом цикле стерилизации в камере паровых стерилизаторов с удалением воздуха из камеры методом продувки паром при размещении индикаторов внутри стерилизуемых изделий и стерилизационных упаковок с изделиями.
Контролируемые режимы стерилизации приведены в табл. 1.
Индикаторы соответствуют классу 4 по ГОСТ Р ИСО 11140-1-2000.
2.7.3. Индикаторы помещают в трудно стерилизуемые участки внутри загрузки:
— середина пористых изделий (центральная часть свертков из хлопчатобумажных материалов — сложенных простыней, халатов и т.п.);
— внутренние полости и каналы изделий из резин, пластмасс, стекла (внутренние полости пальцев резиновых перчаток, средняя часть каналов катетеров/зондов, полости пробирок, закрытых чашек Петри и т.п.).
ВНИМАНИЕ! Не допускается размещать индикаторы СТЕРИТЕСТ-П под крышкой стерилизационной коробки вне находящихся в ней упаковок и изделий, поскольку это место, как правило, не является трудно стерилизуемым участком загрузки. Такое размещение индикаторов приводит к ошибочным результатам контроля.
При стерилизации изделий в неупакованном виде индикаторы СТЕРИТЕСТ-П не используют.
2.7.4. Минимальное количество индикаторов, закладываемых в стерилизуемые упаковки, зависит от объема камеры. Число и расположение контрольных точек должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.).
Упаковки с индикаторами внутреннего контроля размещают в контрольных точках N 3 и более (во всех контрольных точках, кроме 1 и 2).
Для повышения надежности контроля рекомендуется размещать индикатор в каждой отдельной упаковке, а при стерилизации в упаковке комплекта разнородных изделий размещать внутри разных изделий два или более индикатора.
2.7.5. Размещение индикаторов внутри упаковок и изделий проводит персонал, осуществляющий упаковывание изделий перед стерилизацией.
2.7.6. Извлечение индикаторов из упаковок и изделий, прошедших стерилизацию, учет и интерпретацию результатов контроля проводит персонал, вскрывающий упаковку и готовящий простерилизованные изделия к использованию.
Индикаторную метку каждого извлеченного индикатора сравнивают с эталоном сравнения. При соблюдении критических параметров стерилизации красно-оранжевый цвет индикаторной метки должен необратимо измениться на темно-фиолетовый (конечный цвет). Если индикаторная метка хотя бы одного индикатора полностью или частично сохранила красно-оранжевый цвет либо изменила цвет на коричневый, легко отличимый от цвета эталона сравнения (неудовлетворительный результат), то все изделия, обработанные в данной упаковке, считают непростерилизованными. В этом случае о неудовлетворительном результате контроля сообщают в стерилизационное отделение, проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров режима стерилизации, переупаковывают изделия в новую упаковку (за исключением упаковки, допускающей повторную стерилизацию), заменяют индикатор и подвергают изделия повторной стерилизации.
При повторении неудовлетворительного результата контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
Примечания:
1. Оттенки темно-фиолетового цвета эталона сравнения индикаторов разных партий могут иметь незначительные различия в пределах погрешности цветопередачи при печати (изготовлении) индикаторов.
2. В зависимости от особенностей освещения при учете результатов контроля конечный цвет индикаторной метки может иметь различные оттенки темно-фиолетового вплоть до черного.
3. При любом освещении любые оттенки красно-оранжевого или коричневого цвета индикаторной метки, не достигшей своего конечного цвета, имеют ясное визуальное отличие от цвета эталона сравнения.
2.7.7. Учет и интерпретацию результатов контроля проводит медицинский персонал, вскрывающий упаковку с простерилизованным изделием (изделиями) при подготовке изделий к использованию по назначению.
Если необходимо получить предварительный результат контроля сразу после завершения цикла стерилизации, в каждом цикле одну из упаковок/стерилизационных коробок следует заполнять изделиями, аналогичными стерилизуемым изделиям в других упаковках, и с аналогичным размещением индикаторов. Такая упаковка/стерилизационная коробка маркируется и является контрольной, и изделия в ней не подлежат использованию в качестве стерильных. После завершения цикла стерилизации контрольную упаковку вскрывают и учитывают результат контроля. При удовлетворительном результате контроля принимают предварительное решение о соблюдении критических параметров режимов стерилизации внутри всех упаковок, простерилизованных в этом цикле.
ВНИМАНИЕ! Окончательное решение принимают только после учета результатов контроля при вскрытии упаковок с простерилизованными изделиями по п. 2.7.6.
2.7.8. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении, при температуре от плюс 5 °C до плюс 40 °C и относительной влажности не выше 85%, в защищенном от солнечного света месте.
2.7.9. Гарантийный срок годности — 24 месяца с даты изготовления индикаторов.
2.8. Индикаторы контроля паровой стерилизации серии ИНТЕСТ-П
2.8.1. Индикаторы ИНТЕСТ-П (ТУ 9398-041-11764404-2003) представляют собой прямоугольные полоски бумажно-пленочного основания с нанесенными на него красно-оранжевой индикаторной меткой и темно-фиолетовым эталоном сравнения. Индикаторы представлены в следующих модификациях:
— ИНТЕСТ-П-121/20-01, ИНТЕСТ-П-126/10-01, ИНТЕСТ-П-134/5-01 — без липкого слоя;
— ИНТЕСТ-П-121/20-02, ИНТЕСТ-П-126/10-02, ИНТЕСТ-П-134/5-02 — с липким слоем.
2.8.2. Индикаторы предназначены для применения в каждом цикле стерилизации для наружного и внутреннего контроля условий стерилизации в стерилизаторах с полным удалением воздуха из стерилизационной камеры методом многоступенчатого вакуумирования.
Режимы стерилизации указаны в таблице 1.
Индикаторы соответствуют классу 4 по ГОСТ Р ИСО 11140-1-2000.
2.8.3. При соблюдении критических параметров режимов стерилизации красно-оранжевый цвет индикаторной метки должен измениться на темный сине-фиолетовый, соответствующий цвету эталона сравнения (конечный цвет). Если индикаторная метка полностью или частично сохранила красно-оранжевый цвет либо изменила цвет на коричневый, легко отличимый от цвета эталона сравнения (неудовлетворительный результат), то требуемые параметры режима стерилизации не были достигнуты, а изделия считаются непростерилизованными и подлежат повторной стерилизации.
Примечания:
1. Оттенки темного сине-фиолетового цвета эталона сравнения индикаторов разных партий могут иметь незначительные различия в пределах погрешности цветопередачи при печати (изготовлении) индикаторов.
2. В зависимости от особенностей освещения при учете результатов контроля конечный темный сине-фиолетовый цвет индикаторной метки может иметь различные оттенки сине-фиолетового вплоть до черного.
3. При любом освещении любые оттенки красно-оранжевого или коричневого цвета индикаторной метки, не достигшей своего конечного цвета, имеют ясное визуальное отличие от цвета эталона сравнения.
2.8.5. Число и расположение контрольных точек должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.).
2.8.6. Проведение наружного контроля.
2.8.6.1. Размещение индикаторов наружного контроля, их выемку, интерпретацию результатов и документирование осуществляет персонал, проводящий стерилизацию.
2.8.6.2. Для наружного контроля индикаторы закрепляют на внешней стороне стерилизационных упаковок или на бирках стерилизационных коробок со стерилизуемыми изделиями, придерживаясь расположения контрольных точек 1 и 2. Перед закреплением индикатора с липким слоем с обратной стороны индикатора удаляют часть защитного бумажного покрытия, закрывающего липкий слой. Закрепление индикаторов осуществляют:
— при использовании комбинированных упаковок (прозрачная синтетическая пленка плюс бумага) — на пленку;
— при использовании бумажных пакетов — на заклеивающий клапан пакета;
— при использовании листовых бумажных оберточных материалов — на остающийся свободным после завертывания угол бумаги;
— при использовании стерилизационных коробок — на бирку коробки.
Для закрепления индикатора без липкого слоя используют самоклеющуюся ленту для паровой стерилизации, прикрепляя индикатор участком, свободным от цветовых меток.
Примечание. Для удобства закрепления индикатора без липкого слоя на стерилизационной коробке допускается вкладывать его в комбинированную упаковку или в бумажный пакет, которые затем прикрепляют к коробке самоклеющейся лентой для стерилизации.
2.8.6.3. Упаковки с прикрепленными снаружи индикаторами размещают в контрольных точках 1 и 2.
2.8.6.4. По окончании цикла стерилизации индикаторную метку каждого наружного индикатора сравнивают с цветом эталона сравнения. Если хотя бы один индикатор показал отрицательный результат контроля, все изделия, обработанные в данном цикле, считают нестерильными. В этом случае проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров, переупаковывают изделия в новые упаковки (за исключением упаковок из материалов, допускающих повторную стерилизацию), заменяют все индикаторы в контрольных точках и подвергают изделия повторной стерилизации.
При повторении отрицательного результата контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
2.8.7. Проведение внутреннего контроля.
2.8.7.1. Размещение индикаторов для внутреннего контроля проводит персонал, осуществляющий упаковывание изделий перед стерилизацией.
2.8.7.2. Для внутреннего контроля индикаторы помешают в наиболее трудно стерилизуемые места внутри загрузки, которые находятся:
— в середине пористого изделия (простыни, халаты, марля и т.п.), расположенного в центре упаковки или стерилизационной коробки;
— внутри полостей изделий (трубчатые изделия, перчатки, сосуды и т.п.);
— между складками и слоями сложенных изделий (клеенка, полимерные пленки и т.п.).
ВНИМАНИЕ! Не допускается размещать индикаторы ИНТЕСТ-П под крышкой стерилизационной коробки вне находящихся в ней упаковок и изделий, поскольку это место, как правило, не является трудно стерилизуемым местом загрузки. Такое размещение индикаторов приводит к ошибочным результатам контроля.
При стерилизации изделий простой формы в неупакованном виде индикаторы ИНТЕСТ-П используют только для наружного контроля.
2.8.7.3. Минимальное количество индикаторов внутреннего контроля, закладываемых в стерилизуемые упаковки, зависит от объема камеры. Упаковки с индикаторами внутреннего контроля размещают в контрольных точках N 3 и более (во всех контрольных точках, кроме 1 и 2) согласно табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.).
Для повышения надежности контроля рекомендуется размещать индикатор в каждой отдельной упаковке, а при стерилизации в упаковке комплекта разнородных изделий размещать внутри разных изделий два или более индикатора.
2.8.7.4. Извлечение индикаторов из упаковок и изделий, прошедших стерилизацию, и интерпретацию результатов проводит персонал, вскрывающий упаковку и готовящий стерилизованные изделия к использованию.
2.8.7.5. Индикаторную метку каждого извлеченного индикатора сравнивают с эталоном сравнения. При получении отрицательного результата контроля все изделия, обработанные в данной упаковке, считают нестерильными. В этом случае об отрицательном результате контроля сообщают в стерилизационное отделение, проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров, переупаковывают изделия в новую упаковку (за исключением упаковки, допускающей повторную стерилизацию), заменяют индикатор и подвергают изделия повторной стерилизации.
При повторении неудовлетворительных результатов контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
2.8.7.6. Результат контроля внутри изделий может быть получен только в чистом (стерильном) помещении, в месте подготовки стерилизованных изделий к использованию по назначению, поскольку индикатор нельзя извлечь из загрузки без вскрытия упаковки, а следовательно, без риска контаминации стерильных изделий.
Если необходимо получить предварительный результат внутреннего контроля сразу после завершения цикла стерилизации, в каждом цикле одну из упаковок/стерилизационных коробок следует заполнять изделиями, аналогичными стерилизуемым изделиям в других упаковках и с аналогичным размещением индикаторов. Такая упаковка/коробка маркируется и является контрольной, и изделия в ней не подлежат использованию в качестве стерильных. После завершения цикла стерилизации контрольную упаковку вскрывают и смотрят результат контроля. При положительном результате контроля принимают предварительное решение о соблюдении критических параметров стерилизации внутри всех упаковок, стерилизованных в этом цикле.
ВНИМАНИЕ! Окончательное решение принимается только после получения результатов контроля в месте вскрытия упаковок со стерильными изделиями по п. 2.8.7.5.
2.8.8. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении, при температуре от плюс 5 °C до плюс 40 °C и относительной влажности не выше 85%, в защищенном от солнечного света месте.
2.8.9. Гарантийный срок годности — 24 месяца с даты изготовления индикаторов.
3. ИНДИКАТОРЫ ВОЗДУШНОЙ СТЕРИЛИЗАЦИИ
3.1. Основные характеристики индикаторов воздушной стерилизации медицинских изделий приведены в таблице 3.
Таблица 3
Характеристика индикаторов воздушной стерилизации
|
Обозначение индикатора |
Вид индикатора |
Назначение индикатора |
Класс индикатора |
Контролируемые режимы стерилизации |
Цвет индикаторной метки |
Наличие и размещение эталона сравнения |
|
|
исходный |
конечный цвет эталона сравнения |
||||||
|
ИСВС-01 |
Этикетка с липким слоем (в листах и рулонах) |
Индикатор — свидетель (для подтверждения факта проведения стерилизационной обработки) |
1 |
Все режимы воздушной стерилизации |
Фиолетовый |
Коричневый |
Эталон отсутствует |
|
ИСВС-02 |
Этикетка с липким слоем и дополнительными надписями (в листах и рулонах) |
||||||
|
ИС-160 |
Бумажная лента без липкого слоя (в рулоне) |
Наружный контроль |
4 |
160 °C, 150 мин |
От белого до светло-песочного |
От коричневого до темно-коричневого |
Входит в виде отдельного отрезка ленты в комплект к каждому рулону ленты |
|
ИС-180 |
Бумажная лента без липкого слоя (в рулоне) |
Наружный контроль |
4 |
180 °C, 60 мин |
От белого до светло-песочного |
От коричневого до темно-коричневого |
Входит в виде отдельного отрезка ленты в комплект к каждому рулону ленты |
|
Стериконт-В-160/150-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
160 °C, 150 мин |
Голубой |
Коричневый |
Эталон сравнения нанесен на индикатор |
|
Стериконт-В-160/150-02 |
Полоска с липким слоем |
||||||
|
Стериконт-В-180/60-01 |
Полоска без липкого слоя |
Наружный контроль |
4 |
180 °C, 60 мин |
Голубой |
Коричневый |
Эталон сравнения нанесен на индикатор |
|
Стериконт-В-180/60-02 |
Полоска с липким слоем |
||||||
|
Стеритест-В-01 |
Полоска без липкого слоя |
Внутренний контроль |
5 |
160 °C, 150 мин |
Зеленый |
Коричневый |
Эталон сравнения нанесен на индикатор |
|
180 °C, 60 мин |
|||||||
|
Стеритест-В |
Полоска с липким слоем |
200 °C, 30 мин |
3.2. Индикаторы воздушной стерилизации, относящиеся к разным классам, применяют в соответствии с таблицей 4.
Таблица 4
Контроль воздушной стерилизации с помощью индикаторов
производства НПФ «ВИНАР»
|
Наименование индикатора |
Назначение индикатора |
Периодичность контроля |
Место размещения индикатора относительно упаковки |
Минимальное количество индикаторов, используемых в одном цикле |
Кто размещает индикатор в загрузке перед стерилизацией |
Кто проверяет состояние индикатора после стерилизации |
Документирование индикатора |
|
ИСВС-01 |
Индикатор-свидетель |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
По числу стерилизационных упаковок и/или стерилизационных коробок |
Персонал, проводящий стерилизацию или осуществляющий упаковывание изделий |
Персонал, проводящий стерилизацию, и потребитель стерилизованных изделий |
Не применяется |
|
ИСВС-02 |
|||||||
|
ИС-160 |
Наружный контроль |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
В зависимости от объема камеры стерилизатора (N МУ-287-113 от 30.12.98 г.) |
Персонал, проводящий стерилизацию изделий |
Персонал, проводящий стерилизацию изделии |
В журнале работы стерилизаторов |
|
ИС-180 |
|||||||
|
СТЕРИКОНТ-В-160/150-01 |
Наружный контроль |
Каждый цикл |
Снаружи стерилизационной упаковки или на бирке стерилизационной коробки |
В зависимости от объема камеры стерилизатора (N МУ-287-113 от 30.12.98 г.) |
Персонал, проводящий стерилизацию изделий |
Персонал, проводящий стерилизацию изделий |
В журнале работы стерилизаторов |
|
СТЕРИКОНТ-В-160/150-02 |
|||||||
|
СТЕРИКОНТ-В-180/60-01 |
|||||||
|
СТЕРИКОНТ-В-180/60-02 |
|||||||
|
СТЕРИТЕСТ-В-01 |
Внутренний контроль |
Каждый цикл |
Внутри стерилизуемых изделий и упаковок |
В зависимости от объема камеры стерилизатора (N МУ-287-113 от 30.12.98 г.) |
Персонал, осуществляющий упаковывание изделий |
Потребитель стерилизованных изделий |
В журнале работы стерилизаторов |
|
СТЕРИТЕСТ-В |
3.3. Индикаторы-свидетели воздушной стерилизации серии ИСВС
3.3.1. Индикаторы-свидетели ИСВС-01 и ИСВС-02 (ТУ 9398-040-11764404-2003) представляют собой этикетки с нанесенными на их лицевой (рабочей) стороне индикаторной меткой фиолетового цвета и надписью «коричневый», описывающей конечный цвет индикаторной метки после проведения цикла стерилизации. На обратной стороне индикаторов нанесен липкий слой, закрытый защитной (антиадгезивной) подложкой. Индикаторы представлены в двух модификациях:
— ИСВС-01 — без дополнительных записей;
— ИСВС-02 — имеет дополнительные (служебные) надписи «Дата __», «Стерилизатор __» и «Загрузка __», предназначенные для записи соответствующей информации.
3.3.2. Индикаторы предназначены для применения на стерилизационных упаковках или на бирках стерилизационных коробок со стерилизуемыми изделиями при каждом цикле воздушной стерилизации с целью получения свидетельства ее проведения, позволяя в дальнейшем отличать упаковки/коробки, подвергнутые стерилизационной обработке, от необработанных.
Индикаторы соответствуют классу 1 по классификации ГОСТ Р ИСО 11140-1-2000.
3.3.3. Индикаторы снимают с антиадгезивной подложки и наклеивают на каждую стерилизационную упаковку на участок, легко доступный для визуального осмотра, и/или бирку стерилизационной коробки. На индикаторах ИСВС-02 записывают необходимую информацию.
Наклеивание индикаторов на упаковку осуществляет персонал, упаковывающий изделия для стерилизации, или проводящий стерилизацию.
3.3.4. Визуальный осмотр индикаторов после стерилизации осуществляет персонал, проводивший цикл стерилизации, и пользователь простерилизованных изделий перед вскрытием упаковок/коробок.
После стерилизации происходит необратимое изменение цвета индикаторной метки с фиолетового на коричневый. Это свидетельствует о том, что упаковки с изделиями были подвергнуты стерилизационной обработке. Конечный цвет индикаторной метки не является свидетельством достижения в камере стерилизатора условий, требующихся для стерилизации изделий.
Примечание. В зависимости от режимов стерилизации, типа стерилизаторов и особенностей освещения при визуальном осмотре индикаторов конечный цвет индикаторной метки может иметь различную интенсивность окраски — от коричневого до темно-коричневого.
3.3.5. При повторном использовании разрешенных для этого упаковочных материалов новые индикаторы целесообразно наклеивать рядом с отработавшими, что позволяет контролировать кратность использования упаковочного материала.
3.3.6. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении при температуре от плюс 5 °C до плюс 40 °C и относительной влажности до 85% в защищенном от солнечного света месте. При хранении и применении избегать попадания влаги на индикатор.
3.3.7. Гарантийный срок годности — 24 месяца со дня изготовления индикаторов.
3.4. Индикаторы контроля воздушной стерилизации серии ИС
3.4.1. Индикаторы ИС-160 и ИС-180 (ТУ 9443-004-11764404-1996) представляют собой бумажную ленту, на лицевой (рабочей) стороне которой равномерно нанесен индикаторный слой от белого до светло-песочного цвета. На обратной (нерабочей) стороне ленты имеется маркировка в виде цветных наклонных полос: желтого цвета — на индикаторе ИС-160 и серого цвета — на индикаторе ИС-180. В комплект индикаторов входит эталон сравнения, показывающий конечный цвет полос на индикаторе (от коричневого до темно-коричневого — в зависимости от партии индикатора) при соблюдении критических параметров режимов стерилизации.
3.4.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в каждом цикле стерилизации в камере воздушных стерилизаторов и размещаются снаружи стерилизационных упаковок или на бирках стерилизационных коробок со стерилизуемыми изделиями.
Контролируемые режимы стерилизации приведены в табл. 3.
Индикаторы соответствуют классу 4 по классификации ГОСТ Р ИСО 11140-1-2000.
3.4.3. Расположение индикаторов в камере стерилизатора зависит от объема камеры и должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.). Упаковки с прикрепленными индикаторами наружного контроля размещают во всех контрольных точках камеры.
3.4.4. Отрезок ленты длиной около 3 см закрепляют индикаторным слоем наружу с внешней стороны стерилизационной упаковки или бирки стерилизационной коробки, помещаемой в контрольную точку. Закрепление осуществляют самоклеющейся лентой для воздушной стерилизации. Упаковки размещают в камере таким образом, чтобы расстояние от индикатора до стенки камеры было не менее 5 см.
3.4.5. Все операции с индикаторами: их размещение в стерилизационной камере, осмотр после окончания цикла стерилизации, интерпретацию результатов и документирование — осуществляет персонал, проводящий стерилизацию.
3.4.6. Учет результатов контроля проводят, оценивая изменение цвета индикаторного слоя каждого индикатора. Если цвет индикаторного слоя всех индикаторов соответствует цвету или темнее его, это свидетельствует о соблюдении требуемых значений критических параметров режима стерилизации.
Если цвет индикаторного слоя хотя бы одного индикатора светлее эталона сравнения, то это свидетельствует о несоблюдении требуемых значений критических параметров режима стерилизации в камере стерилизатора. В этом случае все изделия загрузки считаются непростерилизованными и подлежат повторной стерилизации.
ВНИМАНИЕ! Номера партии индикаторов и эталона сравнения должны совпадать. Во избежание неправильной интерпретации результатов не допускается использовать при учете результатов контроля индикатор и эталон сравнения разных партий.
3.4.7. Индикаторы следует хранить в упаковке изготовителя в отапливаемом помещении при температуре не выше плюс 25 °C и относительной влажности не выше 90% в защищенном от солнечного света месте.
3.4.8. Гарантийный срок годности — 12 месяцев с даты изготовления индикаторов.
3.5. Индикаторы контроля воздушной стерилизации серии СТЕРИКОНТ-В
3.5.1. Индикаторы серии СТЕРИКОНТ-В (ТУ 9443-006-11764404-1998) представляют собой прямоугольные полоски бумажно-пленочного основания в листах с перфорацией между индикаторами с нанесенными на него голубой индикаторной меткой и коричневым эталоном сравнения. Индикаторы представлены в двух модификациях:
— СТЕРИКОНТ-В-160/150-01, СТЕРИКОНТ-В-180/60-01 — без липкого слоя;
— СТЕРИКОНТ-В-160/150-02, СТЕРИКОНТ-В-180/60-02 — с липким слоем.
3.5.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в каждом цикле стерилизации в камере воздушных стерилизаторов при размещении индикаторов снаружи стерилизационных упаковок или на бирках стерилизационных коробок со стерилизуемыми изделиями.
Контролируемые режимы стерилизации приведены в табл. 3.
Индикаторы соответствуют классу 4 по классификации ГОСТ Р ИСО 11140-1-2000.
3.5.3. Расположение контрольных точек должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.). Упаковки с прикрепленными индикаторами размещают во всех контрольных точках камеры.
3.5.4. От листа с индикаторами по линиям перфорации отрывают необходимое количество индикаторов. Для закрепления индикатора с липким слоем с его обратной стороны удаляют часть защитного бумажного покрытия, закрывающего липкий слой. Закрепление индикаторов осуществляют:
— при использовании листовых бумажных оберточных материалов — на остающийся свободным после завертывания угол бумаги;
— при использовании стерилизационных коробок — на бирку коробки.
Для закрепления индикатора без липкого слоя используют самоклеющуюся ленту для воздушной стерилизации, прикрепляя индикатор участком, свободным от цветовых меток.
Для снятия индикатора с упаковки после стерилизации необходимо оторвать индикатор по линии перфорации от приклеенной части. Приклеенная часть без цветных меток не удаляется с упаковки и доходит до потребителя, что позволяет контролировать кратность использования тех упаковочных материалов, для которых допускается повторное использование.
3.5.5. Все операции с индикаторами: их размещение, выемку, интерпретацию результатов и документирование — осуществляет персонал, проводящий стерилизацию.
3.5.7. По окончании цикла стерилизации цвет индикаторной метки каждого извлеченного индикатора сравнивают с цветом эталона сравнения. При соблюдении требуемых значений критических параметров режимов стерилизации голубой цвет индикаторной метки должен необратимо измениться на коричневый (конечный цвет). Если индикаторная метка хотя бы одного индикатора полностью или частично сохранила голубой цвет либо изменила цвет на зеленый, легко отличимый от цвета эталона сравнения, все изделия, обработанные в данном цикле, считают непростерилизованными. В этом случае проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров, переупаковывают изделия в новые упаковки (за исключением упаковок, допускающих повторную стерилизацию), заменяют все индикаторы в контрольных точках и подвергают изделия повторной стерилизации.
При повторении неудовлетворительных результатов контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
3.5.8. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении при температуре от плюс 5 °C до плюс 40 °C и относительной влажности не выше 85% в защищенном от солнечного света месте. При хранении и применении избегать попадания влаги на индикатор.
3.5.9. Гарантийный срок годности — 24 месяца с даты изготовления индикаторов.
3.6. Индикаторы контроля воздушной стерилизации серии СТЕРИТЕСТ-В
3.6.1. Индикаторы СТЕРИТЕСТ-В (ТУ 9398-019-11764404-2002) представляют собой прямоугольные полоски бумажного основания в листах с перфорацией между индикаторами с нанесенными на него зеленой индикаторной меткой и коричневым эталоном сравнения. Индикаторы представлены в двух модификациях:
— СТЕРИТЕСТ-В-01 — без липкого слоя;
— СТЕРИТЕСТ-В-02 с липким слоем.
3.6.2. Индикаторы предназначены для контроля соблюдения критических параметров режимов в воздушных стерилизаторах при размещении индикаторов внутри стерилизуемых изделий и стерилизационных упаковок с изделиями.
Контролируемые режимы стерилизации приведены в табл. 3.
Индикаторы соответствуют классу 5 по ГОСТ Р ИСО 11140-1-2000.
3.6.3. Индикаторы помещают в трудно стерилизуемые участки внутри загрузки:
— внутренние полости стеклянной посуды небольшого объема (пробирки, склянки, закрытые чашки Петри, стерилизуемые в индивидуальной упаковке);
— внутренние полости стеклянной посуды большого объема (склянки, стерилизуемые в упаковке или без нее);
— внутри массивных изделий, стерилизуемых в индивидуальной упаковке;
— центральную часть упаковок со стерилизуемыми изделиями.
При стерилизации изделий простой формы в индивидуальной упаковке или в неупакованном виде индикаторы СТЕРИТЕСТ-В не используют.
3.6.4. Минимальное количество индикаторов, закладываемых в стерилизуемые упаковки, зависит от объема камеры. Число и расположение контрольных точек должно соответствовать табл. П.5.2 «Методических указаний по дезинфекции, предстерилизационной очистке и стерилизации изделий медицинского назначения» (N МУ-287-113 от 30.12.98 г.).
3.6.5. Размещение индикаторов внутри упаковок и изделий проводит персонал, осуществляющий упаковывание изделий перед стерилизацией.
3.6.6. Извлечение индикаторов из упаковок и изделий, прошедших стерилизацию, учет и интерпретацию результатов контроля проводит персонал, вскрывающий упаковку и готовящий простерилизованные изделия к использованию.
Индикаторную метку каждого извлеченного индикатора сравнивают с эталоном сравнения. При соблюдении критических параметров режимов стерилизации зеленый цвет индикаторной метки должен необратимо изменяться на коричневый (конечный цвет). Если индикаторная метка хотя бы одного индикатора полностью или частично сохранила зеленый цвет, легко отличимый от цвета эталона сравнения (неудовлетворительный результат), то все изделия, обработанные в данной упаковке, считают непростерилизованными. В этом случае о неудовлетворительном результате контроля сообщают в стерилизационное отделение, проверяют соблюдение правил загрузки стерилизатора и правильность установки параметров режима стерилизации, переупаковывают изделия в новую упаковку (за исключением упаковки, допускающей повторную стерилизацию), заменяют индикатор и подвергают изделия повторной стерилизации.
При повторении неудовлетворительного результата контроля эксплуатацию стерилизатора прекращают и проверяют его техническую исправность.
3.6.7. Учет и интерпретацию результатов контроля проводит медицинский персонал, вскрывающий упаковку с простерилизованным изделием (изделиями) при подготовке изделий к использованию по назначению.
Если необходимо получить предварительный результат контроля сразу после завершения цикла стерилизации, в каждом цикле одну из упаковок/стерилизационных коробок следует заполнять изделиями, аналогичными стерилизуемым изделиям в других упаковках, и с аналогичным размещением индикаторов. Такая упаковка/коробка маркируется и является контрольной, и изделия в ней не подлежат использованию в качестве стерильных. После завершения цикла стерилизации контрольную упаковку вскрывают и учитывают результат контроля. При положительном результате контроля принимают предварительное решение о соблюдение критических параметров режима стерилизации внутри всех упаковок, простерилизованных в этом цикле.
ВНИМАНИЕ! Окончательное решение принимают только после учета результатов контроля при вскрытии упаковок с простерилизованными изделиями по п. 3.6.6.
3.6.8. Хранить индикаторы следует в упаковке изготовителя в отапливаемом помещении при температуре от плюс 5 °C до плюс 40 °C и относительной влажности не выше 85% в защищенном от солнечного света месте. При хранении и применении избегать попадания влаги на индикатор.
3.6.9. Гарантийный срок годности — 24 месяца с даты изготовления индикаторов.
Биологические индикаторы (БИ), согласно определению ANSI/AAMI и ISO, это тест-системы, содержащие жизнеспособные микроорганизмы, обеспечивающие определенную устойчивость к конкретному процессу стерилизации. Биологический индикатор предоставляет информацию о том, были ли выполнены необходимые условия для уничтожения определенного количества микроорганизмов для данного процесса стерилизации, обеспечивая уровень уверенности в этом процессе. Эндоспоры, или бактериальные споры, — это микроорганизмы, которые в основном используются в БИ. Они считаются одними из самых жизнеспособных. Кроме того, бактериальные споры выбираются для конкретного процесса стерилизации на основании их известной устойчивости (резистентности) к этому процессу. Например, споры Geobacillus stearothermophilus демонстрируют высокую устойчивость к воздействию пара и плазмы перекиси водорода и поэтому используются в БИ, контролирующих эти процессы стерилизации.
Преимущества биологических индикаторов в процессе стерилизации
Биологические индикаторы, в зависимости от конкретного типа, могут использоваться для различных процессов стерилизации с использованием пара, перекиси водорода, этиленоксида и других.
Несколько факторов, таких как опыт оператора, подготовка загрузки и состояние стерилизатора, могут влиять на цикл стерилизации. БИ обеспечивают прямое определение летальности процесса, и поэтому использование БИ для регулярного мониторинга стерилизаторов дает уверенность в эффективности процесса стерилизации.
БИ обычно используются в устройствах контроля процесса (УКП/PCD — process challenge device), которые предназначены для имитирования наиболее сложных изделий, подвергаемых стерилизации. Результат использования БИ в рамках этой задачи демонстрирует, что стерилизатор эффективен в уничтожении большого количества высокоустойчивых бактериальных спор, предоставляя пользователям определенный уровень уверенности в процессе стерилизации.
Процедура тестирования биологических индикаторов
Биологический индикатор состоит из материала-носителя, на который нанесены бактериальные споры с определенной устойчивостью к процессу стерилизации. Материал носителя заключен в стеклянную оболочку или флакон. БИ подвергается стерилизации, а затем инкубируется при определенных условиях, чтобы определить, выжили ли какие-либо споры после процесса стерилизации. Если споры не выживают, и роста не происходит испытание считается пройденным. Если обнаружен рост, то тест провален.
Персонал всегда должен следовать инструкциям по применению (IFU — instruction for use) при использовании биологических индикаторов для контроля стерилизации независимо от типа и программы процесса.
Биологические индикаторы для стерилизации паром (автоклавирование)
Биологические индикаторы (внутри УКП) часто используются для рутинного мониторинга, квалификации и контроля загрузки парового стерилизатора. Биологические индикаторы предназначены для демонстрации того, были ли условия во время парового (автоклавного) цикла достаточными для достижения определенного уровня инактивации микроорганизмов. Для паровой стерилизации БИ обычно используются внутри УКП. AAMI ST79: 2017* рекомендует использовать УКП еженедельно, желательно ежедневно, для мониторинга работы стерилизаторов и в каждой загрузке, содержащей имплантаты.
УКП, содержащее БИ и/или химический индикатор, должно быть помещено в наиболее труднодоступное место камеры. В паровом стерилизаторе это обычно находится на нижней полке рядом со сливом. По завершению цикла УКП извлекается и БИ инкубируются. После инкубации считывается результат. Инкубаторы обеспечат окончательный результат стерилизации: «пройдена» или «не пройдена» в течение определенного периода времени.
Согласно AAMI ST79:2017, УКП, содержащие биологические индикаторы, должны использоваться для рутинного мониторинга циклов паровой стерилизации по крайней мере еженедельно, предпочтительно ежедневно, и в каждой загрузке, содержащей имплантаты. Сотрудники, проводящие стерилизацию должны следовать указаниям производителя для надлежащего размещения в стерилизаторе УКП, содержащего БИ.
Помимо рутинного контроля стерилизатора, УКП, содержащие БИ, также используются для других задач, перечисленных ниже:
- Регулярный мониторинг загрузки изделий, не относящихся к имплантатам
- Рутинный мониторинг загрузок с имплантатами. AAMI ST79: 2017 рекомендует использовать УКП, содержащее БИ и интегрирующий индикатор 5 типа. Персонал, проводящий стерилизацию, также может использовать УКП, содержащий БИ и химический индикатор 6 типа. В любом случае загрузки, содержащие имплантаты, должны быть помещены на карантин до тех пор, пока не будут известны результаты инкубации БИ, за исключением случаев чрезвычайной ситуации
- Квалификация стерилизаторов после установки, перемещения, капитального ремонта, неисправности и сбоев процесса стерилизации
- Периодические проверки качества продукции
Биологические индикаторы для стерилизации плазмой перекиси водорода
Биологические индикаторы также используются для мониторинга процессов стерилизации плазмой перекиси водорода. Плазменные стерилизаторы часто включают несколько циклов, предназначенных для эффективной стерилизации широкого спектра хирургических инструментов и устройств, и биологический индикатор для плазменной стерилизации должен быть использованы в каждом из таких циклов. Биологические индикаторы для контроля стерилизации перекисью водорода включают автономные биологические индикаторы, тестовые пакеты или испытательные пакеты. AAMI ST58: 2013 рекомендует использовать УКП с БИ ежедневно, желательно каждый цикл, для контроля стерилизаторов и в каждой загрузке, содержащей имплантаты.
Типы биологических индикаторов для процессов стерилизации
Существуют различные типы биологических индикаторов в зависимости от потребностей и процесса стерилизации. Наиболее распространенным типом являются автономные биологические индикаторы (АБИ). Эти индикаторы объединяют материал-носитель со спорами и питательной средой в один флакон, устраняя необходимость асептического переноса. После стерилизации флакон активируется, позволяя спорам смешаться с питательной средой, и инкубируется, чтобы обеспечить рост спор. Некоторые конструкции АБИ используют систему обнаружения на основе ферментов, которая может определять ферментативную активность быстрее, с более коротким временем инкубации.
Независимо от конструкции, биологические индикаторы используются во время процессов паровой, плазменной или этиленоксидной стерилизации для гарантии эффективности и летальности процесса.
Где купить биологические индикаторы?
Медицинские учреждения и производители должны приобретать БИ в надежном и доступном источнике для легкого повторного заказа. Биологические индикаторы можно приобрести у компаний, предлагающих материалы для стерилизации и профилактики инфекций. Факторы, которые могут учитываться при принятии решения о приобретении биологических индикаторов, включают: время инкубации, фирменное наименование, стоимость, ассортимент и разнообразие продуктов, валидируемые области применения и простоту использования.
Рекомендуется использовать ISO 11138-7: 2019 для получения дополнительной информации о выборе поставщика.
* – ANSI / AAMI ST79: 2017 Комплексное руководство по стерилизации паром и обеспечению стерильности в медицинских учреждениях. Ассоциация по продвижению медицинского приборостроения; 2017.
Значение биологических индикаторов для оценки эффективности стерилизации
Статьи
Опубликовано в журнале:
Дезинфекционное дело »» № 4’98 Материалы Второго научного симпозиума по значению биологических индикаторов для контроля стерилизации, состоявшегося в Москве 09 декабря 1998 г.
М.И. Леви, Ю.Г. Сучков, В.Я. Бессонова, Ю.С. Зуева, В.Г. Слизкова, М.М. Лившиц, Н.Н. Панкова, Г.И. Рубан, С.М. Савенко, А.П. Митюков, И.И. Корнев, А.И. Воронков
Испытательный лабораторный центр МГЦД, КБ УД Президента РФ,
Московская медицинская академия им. Сеченова, ЦКБ МЦ УД Президента РФ
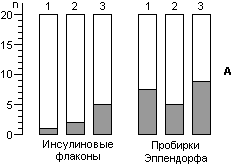
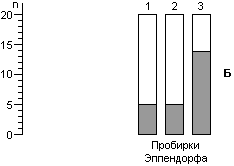
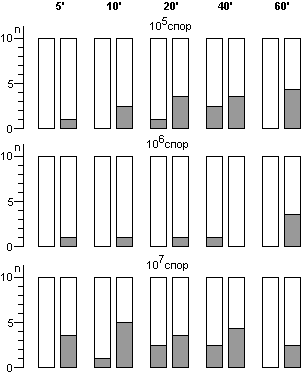
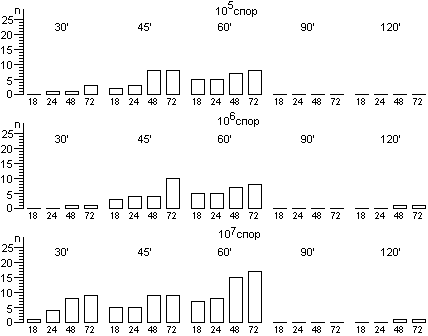
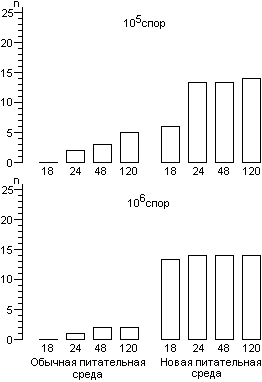
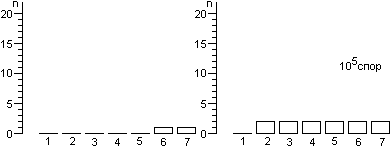
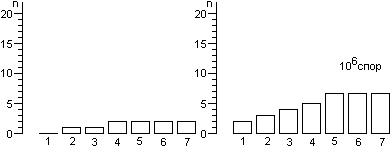
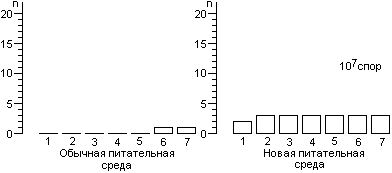
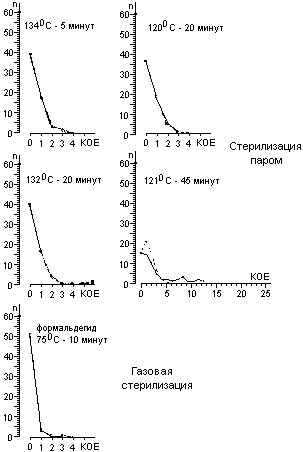
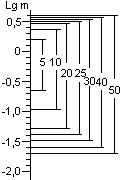
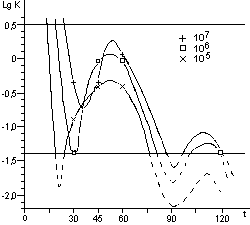
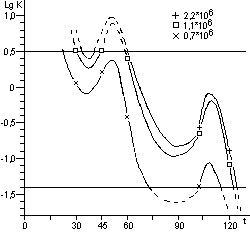
Для расчета среднего значения числа жизнеспособных спор, приходящихся на один биологический индикатор, целесообразно воспользоваться распределением Пуассона. Линейный характер зависимости логарифма числа жизнеспособных клеток от времени стерилизации не подтверждается результатами экспериментов. Использование в экспериментах по контролю стерилизации значительного числа биологических индикаторов, высокоинформативной питательной среды и длительных сроков культивирования биологических индикаторов позволило обнаруживать в них жизнеспособные споры после стерилизации чаще, чем обычно и практически при всех употребляющихся в практике режимах. Высевы содержимого биологических индикаторов после стерилизации на плотную питательную среду подтвердили соответствие распределения чашек Петри по числу выросших колоний распределению Пуассона, а это означает случайное и изолированное распределение жизнеспособных спор в биологических индикаторах. В некоторых экспериментах число биологических индикаторов с жизнеспособными спорами после относительно длительных сроков стерилизации превышало число таковых после коротких сроков стерилизации, что не находило себе объяснения в рамках принятых представлений о стерилизации. Мы предположили, что стерилизация представляет собой затухающий волнообразный автоколебательный процесс, это и составляет сущность зависимости логарифма числа жизнеспособных спор в биологических индикаторах от времени стерилизации.
Контроль стерилизаторов, эксплуатируемых в лечебных учреждениях Москвы, показал, что во всех случаях остаются биологические индикаторы, содержавшие жизнеспособные споры после стерилизации. Рекомендованная в стандартах вероятность неудовлетворительных результатов анализа биологических индикаторов (10-6) значительно меньше той, которая достигнута в наших исследованиях.
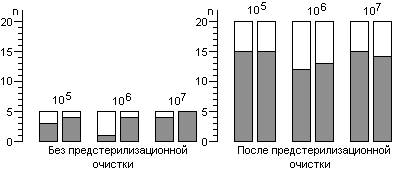
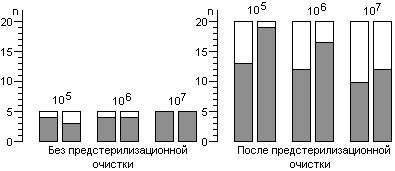
Экспериментальная паровая стерилизация отрезков трубочек из синтетических материалов после предстерилизационной очистки сопровождалась неблагоприятными результатами, аналогичными тем, которые были получены с биологическими индикаторами.
Число жизнеспособных спор в биологическом индикаторе после стерилизации является вероятностной величиной, а их обнаружение зависит от числа индикаторов в стерилизационной камере, качества питательной среды и длительности культивирования при подходящей температуре.
Адекватным инструментом оценки эффективности стерилизации являются биологические индикаторы, которые в значительной мере имитируют обсемененные микроорганизмами медицинские изделия, подвергающиеся стерилизации. Последняя избыточна в том смысле, что она рассчитана на уничтожение такого количества микробов, которые обычно на изделиях не обнаруживают, но которые в принципе хоть и в редких случаях исключить нельзя [11, 18, 19]. Поэтому биологические индикаторы содержат устойчивые к стерилизующему агенту споры в количестве на 2-3 порядка выше того количества, которое обычно встречается на стерилизуемых изделиях [4, 23]. Такой подход диктуется массовым применением стерилизации в медицинской практике и необходимостью исключения риска заражения больных и здоровых за счет неэффективной стерилизации.
В связи с тем, что большинство исследователей придерживается убеждения, что логарифм числа микроорганизмов в биологическом индикаторе или на медицинских изделиях является линейной функцией времени стерилизации, то временные рамки могут быть рассчитаны с достаточной определенностью [23, 24]. К настоящему времени в практике применяются несколько видов стерилизации — паровая, горячевоздушная, газовая, радиационная, лучевая и некоторые другие. Известны крупные производители стерилизационной аппаратуры — «МММ», «Луки», «Джонсон и Джонсон» и др.
Мы задались целью определить оптимальные условия для применения биологических индикаторов в процессе стерилизации. Основным объектом исследований явились биологические индикаторы для оценки паровой стерилизации. Биологические индикаторы готовились и оценивались в нашей лаборатории в соответствии с принятыми нормами [4, 10, 12, 16, 22]. Методические особенности настоящего исследования описаны в ходе изложения полученных результатов.
Всякий раз, когда готовится очередная партия спор Bacillus stearothermophilus для биологических индикаторов, контролирующих паровую стерилизацию, испытывают их термоустойчивость. Требуется, чтобы готовые биологические индикаторы (примерно 106 спор в индикаторе) содержали жизнеспособные споры после 5-минутной паровой стерилизации при 120-121оС, но после 15 минутной стерилизации при указанных условиях таковых не содержали. Производственные серии биологических индикаторов, которые выпускает наше учреждение, отвечают этим требованиям. Наш опыт охватывает уже свыше 70 производственных серий спор В. stearothermophilus, из которых были изготовлены миллионы биологических индикаторов. Каждую серию биологических индикаторов неоднократно проверяли на термоустойчивость, в связи с чем накопился изрядный материал. Мы смогли убедиться в том, что к 15 минутам пребывания в автоклаве при 121оС обычно жизнеспособные споры в биологических индикаторах не обнаруживаются, однако в редких случаях из 10 индикаторов (как правило, такое число индикаторов брали на одну экспозицию) 1 или 2 теста содержали живые споры.
В международных стандартах рекомендуется для определения числа спор в биологических индикаторах после разных экспозиций при 120-121оС производить высевы содержимого индикаторов на плотную питательную среду, а затем культивировать в термостате и подсчитывать число колоний. Такую методику рекомендуют для тех экспозиций, где предполагается обнаружить число колониеобразующих единиц (КОЕ) больше 50 и меньше 1000 [20].
Для тех экспозиций, при которых предполагается среднее число спор в биологическом индикаторе менее 1 (то есть не в каждом индикаторе будут обнаружены жизнеспособные споры), рекомендовано использовать для подсчетов распределение редких и случайных событий — распределение Пуассона [7, 11, 20].
Ниже приведен способ применения распределения Пуассона для указанных целей.
Рх= e-m * mx/x!
где Рх — доля биологических индикаторов с конкретным числом жизнеспособных спор х;
х — конкретное число спор в индикаторе;
х! — произведение целых чисел в последовательности х (х-1) (х-2)…[х-(х-1)];
m — среднее число спор в группе биологических индикаторов;
е — экспонента.
Если некоторое число биологических индикаторов не содержит жизнеспособных спор (х = 0), тогда
P0= k/n,
где k — число биологических индикаторов, не содержащих живые споры;
n — число биологических индикаторов в группе.
Прологарифмируем приведенное уравнение распределения Пуассона:
ln Рх= ln (e-m * mx/x!).
Учитывая, что 0! = 1, а m0 = 1, то (ln k — ln n) = -m; m = ln n — ln k.
Иными словами, среднее число спор на один биологический индикатор в группе равно разности натуральных логарифмов числа всех биологических индикаторов и числа биологических индикаторов без живых спор. Справедливость приведенного способа определения среднего числа спор на один биологический индикатор подтверждается высевами на агар (рис. 8).
Рис. 8. Результаты испытания биологических индикаторов со спорами, высушенными на хроматографической бумаге (106 спора биологическом индикаторе, паровая стерилизация 121оС — 45 мин., индикатор типа Attest). По оси ординат — число биологических индикаторов. Левый столбик — результаты испытаний для обычных биологических индикаторов, правый — для биологических индикаторов с новой питательной средой. Заштрихованная часть столбиков — число биологических индикаторов с жизнеспособными спорами.
Приводим пример расчетов. В стерилизационную камеру поместили 20 биологических индикаторов, а после экспозиции в каждый биологический индикатор прилили цветную питательную среду (используемые в нашей лаборатории серии питательной среды реагировали изменением цвета на присутствие единичных живых спор в биологическом индикаторе при культивировании в термостате при 55oС) [6, 9, 10, 27, 29]. Из 20 использованных в примере биологических индикаторов изменение сиреневого цвета питательной среды на желтый отмечено в 14, а в 6 индикаторах цвет среды остался прежним после культивирования в термостате. Отсюда m = (ln 20 — ln 6) = 2,996 — 1,792 = 1,204. Теперь если мы хотим включить эту величину m в систему координат десятичного логарифма числа спор в биологических индикаторах и времени необходимо взять lg m = lg 1,204 = 0,081.
При многочисленных определениях термоустойчивости спор изредка наблюдалось такое явление, когда 1-2 биологических индикатора из 10 содержали жизнеспособные споры после 15-минутного автоклавирования. В некоторых экспериментах мы расширили набор экспозиций, включив экспозиции в 20, 25, 30 и 35 мин. автоклавирования. В некоторых, хотя и редких случаях, мы отмечали существование живых спор в биологических индикаторах и после относительно длительных экспозиций автоклавирования. Трактовка подобных неожиданных результатов как случайных не могла быть признана правомочной, так как не имела объяснений. Наиболее правдоподобным выглядело предположение о существовании в популяции спор термоустойчивых особей, которые поэтому остаются жизнеспособными после длительных экспозиций. Однако это предположение не подтвердилось, так как потомство спор из пожелтевших биологических индикаторов после 20-40 — минутного автоклавирования обладали термоустойчивостью того же уровня, что и исходная взвесь спор [11, 23].
К описанной проблеме прибавилась и другая, связанная с сомнениями в линейной зависимости логарифма числа спор в биологическом индикаторе от времени стерилизации [11, 17, 24]. Складывалось впечатление, что если и наблюдается линейная зависимость, то она проявляется лишь на отдельных участках графика. Что касается сроков изменения окраски питательной среды в биологических индикаторах после автоклавирования, то в практической деятельности они ограничивались 48 часами (такой срок рекомендован в инструкциях, имеющих хождение в России, США и европейских странах, хотя еще 10 лет тому назад, когда не использовались цветные среды, наблюдение за появлением мутности в питательном бульоне длилось не менее 7 дней). Однако в наших экспериментах было замечено, что изменение цвета питательной среды при культивировании в термостате наступает не только в первые 48 час., но и в последующие дни, особенно в тех биологических индикаторах, которые относительно долго пребывали в стерилизационной камере.
Если в прежние годы мы использовали в качестве носителя спор инсулиновые флаконы, то в последнее время перешли на пробирки Эппендорфа из полипропилена емкостью 1,5 мл [8, 9, 10, 11]. Эта емкость оказалась гораздо удобнее в качестве носителя спор, чем инсулиновые флаконы.
Учитывая все вышесказанное, мы решили применить в настоящем исследовании биологические индикаторы, приготовленные следующим образом. Взвесь спор, которую мы использовали для изготовления производственных серий биологических индикаторов, разводили дистиллированной водой таким образом, чтобы в 0,02 мл оказалось нужное число спор, которое и вносилось в каждую пробирку Эппендорфа. Затем биологические индикаторы оставляли на 24 час. при 37оС для высушивания спор, после чего биологический индикатор (пробирку Эппендорфа оставляли открытой) помещали в специальный пакет фирмы Wipack medical, снабженный бумажным ранним индикатором процесса стерилизации. После автоклавирования в каждый индикатор приливали 0,5 мл цветной питательной среды и помещали в термостат при 55оС на 7 дней с ежедневной регистрацией изменения цвета питательной среды на желтый. Если это случалось, то признавали существование жизнеспособных спор на момент окончания времени автоклавирования.
Легко убедиться в том, что число биологических индикаторов, в которых удавалось обнаружить жизнеспособные споры, зависело от исходного числа индикаторов, помещенных в стерилизационную камеру. Если биологические индикаторы имитируют обсемененные микроорганизмами медицинские изделия, то мы вправе заподозрить, что доля биологических индикаторов с жизнеспособными спорами после стерилизации может соответствовать доле оставшихся нестерильными медицинских изделий. В этом и есть смысл применения контроля стерилизации с помощью биологических индикаторов. Но их число не может быть увеличено до больших чисел, во всяком случае до числа стерилизуемых медицинских изделий. При принятых в России нормах в относительно небольших автоклавах размещают по 5 биологических индикаторов, а в больших — до 13 [12]. Нам представляется, что обозначенного числа биологических индикаторов для изучения пороков стерилизации явно недостаточно, поэтому в представленных ниже экспериментах для контроля стерилизации использовали гораздо большее число индикаторов.
Итак, в наших экспериментах использовали не только большее, чем обычно число биологических индикаторов, но и дольше наблюдали их после стерилизации во время культивирования в термостате. Наконец, мы использовали не только то число спор в индикаторе, которое рекомендовано в стандартах (106 спор), но и несколько меньшее (105), и несколько большее (107). В стерилизационную камеру автоклава в большинстве случаев кроме биологических индикаторов ничего не помещали, чтобы избежать упреков в избыточном заполнении камеры.
Данные, представленные на рис. 1, свидетельствуют о том, что единичные индикаторы содержали жизнеспособные споры даже после 120-минутного автоклавирования (само собой разумеется, что при использовании 5 или 10 биологических индикаторов этот факт не был бы «замечен»). В данном опыте использовали споры двух штаммов В. stearothermophilus — ВКМ-718 (производственный штамм, применяющийся не только в России, но и в других странах, а также недавно выделенный штамм КК [15], обладающий повышенной термоустойчивостью). Неожиданным оказалось то обстоятельство, что иногда индикаторы с жизнеспособными спорами встречались после 45 или 60 мин. автоклавирования не реже, чем после 30-минутной стерилизации.
| Споры В. stearothermophilus | |
| ВК-718 | КК |
| 107 | 2,2*106 |
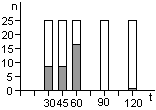 |
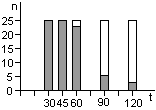 |
| 106 | 1,1*106 |
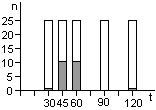 |
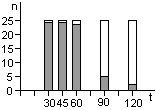 |
| 105 | 0,7*106 |
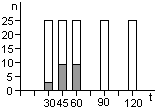 |
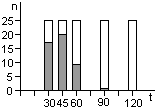 |
Рис. 1. Влияние стерилизации паром в автоклаве ВК-75 (121oС без вакуума в стерилизационной камере) на жизнеспособность спор В. stearothermophilus (штаммы ВК-718 и КК). По оси ординат — число биологических индикаторов на каждую экспозицию (25 биологических индикаторов), по оси абсцисс — время стерилизации (мин.). Закрашенная часть столбиков — число биологических индикаторов с жизнеспособными спорами.
Расхождение полученных данных с ожидаемыми заставило нас разработать новую питательную среду, возможности которой в проявлении жизнеспособных спор в биологических индикаторах, прошедших стерилизацию, были гораздо выше, чем у прежней питательной среды.
Наряду с прежней питательной средой испытали две новых рецептуры, причем одна из них оказалась весьма информативной (рис. 2).
Рис. 2. Влияние питательной среды на проявление жизнеспособности спор В. stearothermophilus в биологических индикаторах (носители — инсулиновые флаконы или пробирки Эппендорфа) после стерилизации паром (121oС — 45 мин.). n — число биологических индикаторов в каждой экспозиции, закрашенная часть столбиков — число биологических индикаторов с жизнеспособными спорами. А — эксперименты с производственной серией 71, число спор в биологическом индикаторе 3,4*105, Б — эксперименты с производственной серией 69, число спор в биологическом индикаторе 106. Номерами 1, 2, 3 обозначены пробы с разными питательными средами.
Таким образом, наряду с повышенным числом биологических индикаторов, удлинением сроков наблюдения за культивируемыми в термостате индикаторами, использовали не только принятую питательную среду, но и новую среду, которая оказалась более информативной, чем прежняя. Не лишне упомянуть, что в один пакет помещали три биологических индикатора с разным числом спор, пакеты размещали в стерилизационной камере случайным образом, после стерилизации биологические индикаторы одновременно заливали одной и той же серией питательной среды и оставляли в одном и том же термостате. Если употребляли прежнюю и новую питательные среды, то число пакетов удваивалось.
Если в прежних опытах автоклавировали биологические индикаторы при 121oС в течение 45 мин., то в опыте, представленном на рис. 3, биологические индикаторы стерилизовали паром при температуре 132oС (оба режима осуществляли в автоклаве отечественного производства — ВК-75).
Рис. 3. Влияние стерилизации паром при 132oС на биологические индикаторы в зависимости от исходного числа спор в них (105, 106 и 107 и времени автоклавирования биологических индикаторов (5, 10, 20, 40 и 60 мин.). По оси ординат — число биологических индикаторов в опыте. В каждой паре столбцов слева — результаты определения числа биологических индикаторов с жизнеспособными спорами при их культивировании в обычной питательной среде, справа — число биологических индикаторов с жизнеспособными спорами при их культивировании в новой питательной среде. Закрашенная часть столбика — число биологических индикаторов с жизнеспособными спорами.
В представленных на рис. 3 данных употребляли различные экспозиции, в числе их и ту (20 мин.), которая рекомендована в соответствующем режиме. Можно отметить, что с помощью новой питательной среды, а иногда даже и с применением прежней, удалось обнаружить жизнеспособные споры в биологических индикаторах после автоклавирования в течение 20-60 мин. Более того, складывается впечатление, что время автоклавирования в указанных на рис. 3 пределах, не очень заметно сказалось на доле биологических индикаторов с жизнеспособными спорами.
Полученные результаты анализа биологических индикаторов после стерилизации побудили нас охарактеризовать те режимы паровой стерилизации, которые приняты в России (рис. 4). Первые два режима осуществлены в аппарате ВК-75, а третий и четвертый — в аппарате фирмы «МММ» (Германия). Само собой разумеется, что все стерилизационные аппараты, использованные в наших исследованиях, находились в полной технической исправности.
| 121oС, 45 мин. | 132oС, 20 мин. |
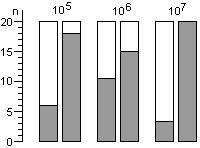 |
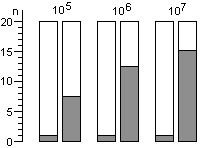 |
| 120oC, 20 мин. + вакуум в стерилизационной камере |
134oC, 5 мин. + вакуум в стерилизационной камере |
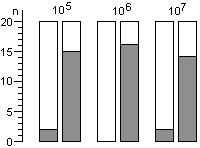 |
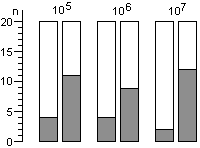 |
Рис. 4. Влияние питательной среды на результаты бактериологического контроля стерилизации. По оси ординат — число биологических индикаторов в опыте. Над каждой парой столбиков указано исходное число спор в биологических индикаторах. В каждой паре столбцов слева — результаты определения числа биологических индикаторов с жизнеспособными спорами при их культивировании в обычной питательной среде, справа — число биологических индикаторов с жизнеспособными спорами при их культивировании в новой питательной среде. Закрашенная часть столбика — число биологических индикаторов с жизнеспособными спорами. Режимы стерилизации приведены над столбиками.
Легко заметить, что ни один из испытанных режимов стерилизации не сопровождался полным освобождением биологических индикаторов от жизнеспособных спор В. stearothermophilus, особенно при употреблении новой питательной среды. Нужно отметить, что процент биологических индикаторов с жизнеспособными спорами несколько увеличивается, если наблюдение за цветом прежней питательной среды в термостате вести не 48 час., а 72 час. (рис. 5, по данным рис. 1 для штамма ВКМ-718).
Рис. 5. Динамика пророста биологических индикаторов (105, 106, 107 спор в биологических индикаторах) после автоклавирования при 121oС в течение 30, 45, 60, 90 и 120 мин. На каждую пробу брали 25 биологических индикаторов. Учет пророста биологических индикаторов вели через 18, 24, 48 и 72 часа их культивирования при 55oС. Столбики указывают число биологических индикаторов с жизнеспособными спорами на данный срок учета результатов.
Применение новой питательной среды явно ускоряет после стерилизации появление максимального числа биологических индикаторов с жизнеспособными спорами при культивировании в термостате при 55oС (рис. 6).
Рис. 6. Динамика пророста биологических индикаторов (по 105 или 106 спор в биологических индикаторах) после автоклавирования (121oС, 45 мин.). На каждую пробу брали 20 биологических индикаторов. Учет пророста вели через 18, 24, 48 или 120 час. культивирования при 55oС в разных питательных средах.
Оказалось, что и газовая стерилизация с помощью формальдегида (аппарат фирмы «МММ», Германия) не освобождает биологические индикаторы от жизнеспособных спор В. stearothermophilus (рис. 7.)
Стерилизация формальдегидом 75oС — 10 мин.
Рис. 7. Влияние питательной среды на результаты бактериологического контроля стерилизации. Обозначения в верхней части рисунка — те же, что и на рис. 4. В нижней части рисунка представлена динамика пророста биологических индикаторов. Под столбиками — время культивирования в сутках. Обозначения — те же, что и на рис. 5.
Тем не менее результаты стерилизации формальдегидом, по крайней мере при использовании прежней питательной среды, выглядят несколько лучше, чем результаты контроля паровой стерилизации.
В наших опытах споры в биологических индикаторах высушивались непосредственно в пробирках Эппендорфа, в то время как в американских биологических индикаторах (Attest) фирмы «3М» споры высушивались на полосках бумаги и в таком виде вносились в пластмассовые емкости, которые снабжены ампулой с цветной питательной средой. После стерилизации ампулу разбивают простым нажатием на корпус индикатора, питательная среда изливается на бумагу с высушенными спорами, а затем при культивировании в термостате удается зафиксировать жизнеспособные споры, если цвет среды меняется на желтый [21, 26]. Мы изготовили некоторое подобие индикатора Attest и проявили их с прежней и новой питательными средами. Оказалось, что применение новой питательной среды заметно улучшило результаты биологического индикатора, аналогичного Attest.
Итак, в наших экспериментах мы, как правило, вносили 120 биологических индикаторов (каждый пакет с биологическими индикаторами занимал объем около 0,1 л) с разной исходной концентрацией спор. Половину индикаторов исследовали с прежней питательной средой, а другую половину — с новой. В большинстве случаев те биологические индикаторы, которые исследовали с помощью новой питательной среды, после автоклавирования вначале заполнялись небольшим объемом жидкости. Половина этого объема использовалась для засева на питательный агар, а к остальной части добавляли питательную среду. Культивирование осуществляли в термостате при 55oС. Выросшие колонии подсчитывали.
Эти наблюдения послужили основанием для сопоставления распределения чашек Петри с агаром по числу выросших колоний с теоретическим распределением Пуассона (наличие чашек без выросших колоний позволяло исчислить среднее значение числа колоний на одну чашку, а затем по таблицам [2] определить теоретическое распределение и сопоставить его с наблюдаемым в эксперименте). Мы исходили из положения о том, что сумма пуассоновских распределений есть тоже пуассоновское распределение; в подсчеты включали данные по всем трем группам биологических индикаторов (105, 106, 107). Поэтому в каждой группе оказалось 60 чашек Петри.
Из данных, представленных на рис. 9., следует, что при всех изученных режимах распределение чашек Петри по числу выросших колоний соответствовало распределению Пуассона. А это, в свою очередь, говорит о том, что оставшиеся после стерилизации жизнеспособные споры представляли собой отдельные независимые друг от друга сущности. Исключение составили данные по режиму паровой стерилизации 121oС — 45 мин., где теоретическая кривая существенно отклонялась от полученной в эксперименте. В этом последнем случае приходится признать, что указанные расхождения связаны с образованием комочков или глыбок спор в биологическом индикаторе, которые распадаются на отдельные споры при рассеве содержимого на поверхности агара. Так или иначе, но не возникает сомнения, что после стерилизации жизнеспособными в биологических индикаторах остаются единичные споры, в то время как подавляющая масса спор погибает. По крайней мере такая картина вырисовывается при избранном числе биологических индикаторов, помещенных в стерилизационную камеру.
Рис. 9. Соответствие фактических материалов (число колоний на агаре) при разных режимах паровой и газовой стерилизации распределению редких и случайных событий. По оси ординат — общее число биологических индикаторов стерилизации (суммирование результатов для трех групп биологических индикаторов с 105, 106 и 107 спорами). По оси абсцисс — число КОЕ (колониеобразующих единиц), выросших на агаре после посева материала биологических индикаторов. Сплошная линия — фактические данные, прерывистая линия — расчетная линия в соответствии с распределением случайных и редких событий (отсутствие на графике прерывистой линии указывает на совпадение расчетных и экспериментальных данных).
Одним из поражающих воображение парадоксов является существенное отклонение экспериментальных данных от линейной зависимости логарифма числа спор в биологических индикаторах от времени стерилизации. Совершенно не соответствовали сложившимся представлениям данные об обнаружении жизнеспособных спор в более поздние от начала стерилизации сроки. И уж совсем не укладывались в сознание данные о более частом обнаружении жизнеспособных спор в более поздние сроки, чем в ранние, что отмечалось в некоторых экспериментах. Случалось даже такое, когда при 15-минутной экспозиции споры в биологических индикаторах нежизнеспособны, а после 45-минутной экспозиции в том же опыте обнаруживаются хоть и единичные, но жизнеспособные споры.
В настоящей работе мы представляем свою интерпретацию процесса гибели спор при стерилизации. Приводимое здесь предположение не имеет пока достаточных доказательств, однако объясняет упомянутый выше парадокс.
Мы предполагаем, что зависимость логарифма числа спор в биологических индикаторах от времени стерилизации носит не линейный, а волнообразный характер. По данным рис. 1 мы дали свою интерпретацию зависимости логарифма числа спор от времени стерилизации, воспользовавшись теми средними величинами числа спор в биологических индикаторах, которые были исчислены с помощью распределения Пуассона (рис. 11, 12). Но вначале мы представляем зависимость зоны определения средних величин от числа биологических индикаторов (рис. 10).
Рис. 10. Область применения распределения Пуассона для определения средних значений (m) при различном числе биологических индикаторов в группе (числа в середине рисунка).
Рис. 11. Влияние стерилизации паром в автоклаве ВК-75 (121oС без вакуума в стерилизационной камере) на жизнеспособность спор В. stearothermophilus, штамм ВК-718. Волнообразные кривые — интерпретация фактических данных. По оси ординат — десятичный логарифм средней концентрации спор в биологическом индикаторе, по оси абсцисс — время стерилизации (мин.). Горизонтальные прямые ограничивают область применения распределения Пуассона для определения средних значений.
Рис. 12. Влияние стерилизации паром в автоклаве ВК-75 (121oС без вакуума в стерилизационной камере) на жизнеспособность спор В. stearothermophilus, штамм КК. Волнообразные кривые — интерпретация фактических данных. По оси ординат — десятичный логарифм средней концентрации спор в биологическом индикаторе, по оси абсцисс — время стерилизации (мин.). Горизонтальные прямые ограничивают область применения распределения Пуассона для определения средних значений.
Для определения средней величины необходимо иметь биологические индикаторы без жизнеспособных спор, а для обозначения границ зоны значений средних нужно, чтобы хотя бы один биологический индикатор содержал жизнеспособные споры, или, напротив, чтобы хотя бы один биологический индикатор оказался без жизнеспособных спор. Из сопоставления различных зон можно заключить, что с увеличением числа биологических индикаторов в наибольшей мере увеличиваются возможности нижней зоны, в то время как верхняя ее часть расширяется незначительно. Распределение Пуассона табулировано, а использование вышесказанного позволяет рассчитать необходимое число биологических индикаторов, которое позволяет надеяться на обнаружение гораздо большего числа жизнеспособных спор после стерилизации.
Представление фактических данных с помощью волнообразных кривых позволяет понять, почему в некоторых экспериментах столь причудливо выстраиваются на графиках биологические индикаторы с жизнеспособными спорами. Ведь выбор точек на оси времени носит случайный характер, не связанный с закономерностями гибели спор, не учитывающий предполагаемый волнообразный характер. Более того, вполне может случиться, что нижняя. часть волны в районе 15 мин. может оказаться за пределами возможности обнаружения в биологических индикаторах (при избранном их количестве) жизнеспособных спор, в то время как при более длительной экспозиции выбор временной точки совпал с верхней частью волны и позволил обнаружить биологические индикаторы с жизнеспособными спорами.
Мы полагаем, что зависимость между логарифмом числа спор в биологическом индикаторе от времени стерилизации отражает затухающий волнообразный автоколебательный процесс, связанный с тем, что не только споры, но и окружающие их условия определяют результат стерилизации.
В нижеследующей таблице собраны результаты контроля различных видов стерилизации с помощью биологических индикаторов в аппаратах, используемых в практических лечебных учреждениях по тем режимам, которые предусмотрены существующими стандартами. Мы использовали полный цикл стерилизации, значительное число биологических индикаторов, длительное их культивирование после стерилизации, прежнюю и новую питательные среды.
Сводная таблица результатов биологического контроля стерилизации
|
№ п/п |
Стерилизационный аппарат | Стерилизация | Биологические индикаторы | ||||||||
| наименование |
фирма- производитель, страна |
год выпуска |
объем стерили- зационной камеры |
вид | режим |
тест- культура |
число спор |
число индика- торов в стерилизац. |
% с жизнеспо- собными спорами после стерилизац. |
||
|
обычная питат. среда |
новая питат. среда |
||||||||||
| 1. | ГК-100-ЗМ | Тюменский з-д медоборудования, Россия |
1993 | 100 л | Паровая | 121oС, 45 мин. |
В. stearo- themophilus |
106 | 40 | 0 | 10 |
| 2. | » | » | » | » | » | » | » | » | 40 | 10 | 25 |
| 3. | BK-75 | » | » | 75 л | » | » | » | 3*105 | 120 | 20 | 45 |
| 4. | » | » | » | » | » | » | » | 106 | 60 | 25 | 65 |
| 5. | » | » | » | » | » | » | » | 105 | 80 | 25 | 75 |
| 106 | 80 | 3 | 100 | ||||||||
| 107 | 80 | 13 | 100 | ||||||||
| 6. | » | » | » | » | » | » | » | 105 | 75 | 0 | 7 |
| 106 | 75 | 0 | 8 | ||||||||
| 107 | 75 | 20 | 20 | ||||||||
| 7. | » | » | » | » | » | » | » | 105 | 75 | 0 | 12 |
| 106 | 75 | 0 | 13 | ||||||||
| 107 | 75 | 20 | 22 | ||||||||
| 8. | ГК-100-ЗМ | » | » | 100 л | » | » | » | 105 | 40 | 15 | 20 |
| 106 | 40 | 0 | 15 | ||||||||
| 107 | 40 | 0 | 35 | ||||||||
| 9. | BK-75 | » | 1992 | 75 л | » | 121oС, 45 мин. |
» | 105 | 40 | 0 | 5 |
| 106 | 40 | 0 | 25 | ||||||||
| 107 | 40 | 0 | 25 | ||||||||
| 10. | » | » | » | » | » | » | » | 106 | 40 | 20 | 50 |
| 107 | 40 | 5 | 60 | ||||||||
| 11. | BK-75 | » | 1992 | 75 л | Паровая | 121oС, 45 мин. |
В. stearo- themophilus |
105 | 40 | 30 | 95 |
| 106 | 40 | 50 | 90 | ||||||||
| 107 | 40 | 15 | 100 | ||||||||
| 12. | » | » | » | » | » | » | » | 104 | 40 | 35 | 75 |
| 106 | 40 | 25 | 35 | ||||||||
| 107 | 40 | 50 | 40 | ||||||||
| 13. | ГК-100-3М**) | » | 1988 | 100 л | » | » | » | 105 | 40 | 10 | 10 |
| 106 | 40 | 10 | 10 | ||||||||
| 107 | 40 | 10 | 15 | ||||||||
| 14. | ГК-100-3М**) | » | » | » | » | » | » | 105 | 40 | 5 | 0 |
| 106 | 40 | 0 | 10 | ||||||||
| 107 | 40 | 5 | 0 | ||||||||
| 15. | ГКД-560 | «ЛАД», Россия |
1996 | 560 л | » | 120oС, 20 мин. |
105 | 40 | 10 | 5 | |
| 106 | 40 | 55 | 10 | ||||||||
| 107 | 40 | 65 | 55 | ||||||||
| 16. | Секурокс | «МММ», Германия |
1993 | 0,5 м3 | » | » | » | 105 | 40 | 15 | 30 |
| 106 | 40 | 20 | 45 | ||||||||
| 17. | » | » | » | » | » | » | » | 105 | 40 | 25 | 70 |
| 106 | 40 | 10 | 75 | ||||||||
| 18. | « | » | » | » | » | » | » | 105 | 40 | 10 | 80 |
| 106 | 40 | 0 | 80 | ||||||||
| 107 | 40 | 10 | 75 | ||||||||
| 19. | Castle м/с 3622 |
USA | 1997 | 680 л | » | » | » | 105 | 40 | 0 | 0 |
| 106 | 40 | 0 | 5 | ||||||||
| 106*) | 0 | 0 | — | ||||||||
| 107 | 40 | 0 | 0 | ||||||||
| 20. | Селектомак | «МММ», Германия |
1993 | 100 л | Паровая | » | » | 105 | 40 | 0 | 0 |
| 106 | 40 | 0 | 10 | ||||||||
| 107 | 40 | 5 | 20 | ||||||||
| 21. | ГК-100-3М**) | Тюм. з-д медооор., Россия |
1993 | 100 л | » | 132oС, 20 мин. |
» | 105 | 40 | 0 | 0 |
| 106 | 40 | 0 | 5 | ||||||||
| 107 | 40 | 10 | 0 | ||||||||
| 22. | ВК-75 | » | 1992 | 75 л | » | » | » | 105 | 40 | 5 | 40 |
| 106 | 40 | 5 | 60 | ||||||||
| 107 | 40 | 5 | 75 | ||||||||
| 23. | Селектомак | «МММ», Германия |
1993 | 100 л | Паровая | 134oС, 5 мин. |
В. stearo- themophilus |
105 | 40 | 0 | 0 |
| 106 | 40 | 0 | 20 | ||||||||
| 107 | 40 | 5 | 10 | ||||||||
| 24. | ГКД-560 | «ЛАД», Россия |
1996 | 560 л | Паровая | 134oС, 5 мин. |
» | 105 | 40 | 45 | 25 |
| 106 | 40 | 50 | 35 | ||||||||
| 107 | 40 | 35 | 100 | ||||||||
| 25. | Секурекс | «МММ», Германия |
1993 | 500 л | » | » | » | 105 | 40 | 20 | 55 |
| 106 | 40 | 20 | 45 | ||||||||
| 107 | 40 | 10 | 70 | ||||||||
| 26. | Castle м/с 3622 |
USA | 1997 | 680 л | » | 134oС, 10 мин. |
» | 105 | 40 | 0 | 0 |
| 106 | 40 | 0 | 20 | ||||||||
| 106*) | 20 | 0 | — | ||||||||
| 107 | 40 | 20 | 25 | ||||||||
| 27. | » | » | » | » | » | » | » | 105 | 40 | 0 | 25 |
| 106 | 40 | 5 | 15 | ||||||||
| 107 | 40 | 5 | 30 | ||||||||
| 28. | Комбимак | «МММ», Германия |
1993 | 70 л | Газовая (формаль- дегид) |
75oC, 10 мин. |
» | 105 | 40 | 5 | 20 |
| 106 | 40 | 10 | 45 | ||||||||
| 107 | 40 | 5 | 20 |
Примечание: *) — Для контроля применили биологические индикаторы Biosign фирмы Castle, содержащие фирменную питательную среду.
**) — Накануне испытаний поставлена новая стерилизационная камера.
Самым общим признаком результатов контроля стерилизации является то, что не удалось убедиться в стерильности всех биологических индикаторов по окончании времени стерилизации. Таким образом, этот важнейший контроль свидетельствует о неэффективности в принятом смысле стерилизации, причем наиболее надежной паровой стерилизации. Так как доза 107 спор в биологическом индикаторе может быть признана чрезмерно высокой, то целесообразно рассмотреть отдельно результаты контроля стерилизации биологическими индикаторами, содержавшими 105 и 106 спор. При использовании новой питательной среды какая-то часть биологических индикаторов после стерилизации во всех случаях содержала жизнеспособные споры. Если же использовали прежнюю питательную среду, то в трех случаях при контроле аппарата ВК-75 (30%) биологические индикаторы не содержали жизнеспособных спор. Чаще подобные результаты отмечены при контроле аппаратов зарубежного производства и это может служить некоторым указанием на качественное превосходство над российскими автоклавами.
Причины сложившейся ситуации неясны, как и возможные предложения по совершенствованию стерилизации. Что касается применения бумажных индикаторов стерилизации, то вряд ли следует рассчитывать на большее, нежели контроль состояния некоторых технических характеристик стерилизационного аппарата, особенно вначале процесса. Полное доверие показаниям бумажных индикаторов может способствовать ложному заключению об эффективной стерилизации.
До сих пор речь шла о судьбе биологических индикаторов в процессе стерилизации, что может не во всех случаях отражать особенности реальной стерилизации медицинских изделий. Для стерилизации в качестве «медицинских изделий» брали отрезки трубочек из поливинилхлорида длиной в 1 см, после тщательной промывки их обсеменяли спорами В. stearothermophilus в объеме 0,02 мл, высушивали и подвергали предстерилизационной очистке кипячением в 2% растворе соды в течение 15 мин. [14]. После отмывки в стерильной дистиллированной воде отрезки трубочек на следующий день стерилизовали в пакетах (121oС — 45 мин.), после чего каждый отрезок помещали в стерильную пробирку Эппендорфа и заливали питательной средой. Культивирование отрезков проводили в термостате при 55oС. Контрольные отрезки обсеменяли спорами, но не подвергали предстерилизационной обработке. Иными словами, в этом опыте подражали экспериментам с биологическими индикаторами.
Полученные результаты поражают своей неожиданностью — отрезки трубочек, обработанные раствором соды при 100oС, оказались после стерилизации столь же обсемененными, что и не подвергавшиеся предварительной очистке, которая в настоящее время занимает важное место в методике стерилизации [1, 3, 14].
Рис. 13. Результаты стерилизации отрезков трубки из поливинилхлорида после их предстерилизационной очистки и без нее. В каждой паре столбиков слева — число отрезков трубки с жизнеспособными спорами при культивировании с обычной питательной средой, справа — с новой питательной средой. Цифры над столбиками — число спор В. stearothermophilus, нанесенных изначально на внутреннюю поверхность отрезков трубки.
В другом опыте отрезки трубочек из силиконовой резины размером в 1 см после тщательной промывки в дистиллированной воде обсеменяли спорами В. stearothermophilus, затем оставляли на 1 час при комнатной температуре. По окончании указанного времени опытные отрезки на 30 мин. погружали в 0,2% раствор дезинфицирующего средства «Септабик» [14], отрезки тщательно промывали в дистиллированной воде, просушивали на фильтровальной бумаге. Контрольные отрезки обсеменяли спорами, но не обрабатывали средством «Септабик». На следующий день все отрезки закладывали в пакеты и стерилизовали в автоклаве (121oС — 45 мин.), после чего каждый отрезок помещали в пробирку Эппендорфа, заливали питательной средой и культивировали при 55oС.
В опыте (рис. 14) результаты испытаний были несколько лучше, чем в предыдущем, так как наблюдалась все же разница в доле проросших опытных и контрольных отрезков трубочек из силиконовой резины, однако эти различия не были впечатляющими. Во всяком случае даже после предстерилизационной очистки стерилизация макетов медицинских изделий оказалась неэффективной. И это несмотря на то, что обрабатывать небольшие отрезки трубочек гораздо легче, чем большие и сложные изделия, где возможные места обсеменения микроорганизмами менее доступны для дезинфицирующих растворов.
Рис. 14. Результаты стерилизации отрезков силиконовой трубки после их предстерилизационной очистки и без нее. В каждой паре столбиков слева — число отрезков трубки с жизнеспособными спорами при культивировании с обычной питательной средой, справа — с новой питательной средой. Числа над столбиками — число спор В. stearothermophilus, нанесенных изначально на внутреннюю поверхность отрезков трубки.
Ввиду необычности полученных результатов необходимо убедиться в том, что не были допущены технические погрешности. На протяжении всего времени исследований и помещениях и в ламинарном боксе расставлялись чашки с питательным агаром, но ни разу бактерии В. stearothermophilus иыделены не были, как и не были выделены из питательной среды и других использованных ингредиентов (в каждом опыте делали посевы питательной среды и дистиллированной воды на 10 агаровых чашек и 10 пробирок Эппендорфа с питательной средой, но безрезультатно). Предположение о том, что число бактерий в биологических индикаторах возрастает во время высушивания, не подтвердилось (известно, что В. stearothermophilus не размножается при 37oС).
Таким образом полученные результаты являются неутешительными, но все же, по крайней мере, для некоторых авторов ожидаемыми. Из всей огромной массы литературы по термоинактивации споровых бактерий, в том числе фундаментальных исследований [5, 23, 25, 28], ближе всех к нашей трактовке стоит монография Мунблитн, Тальрозе и Трофимова [13], которые экспериментов не ставили и пользовались лишь данными литературы. Эти авторы, придерживающиеся объяснения термоинактивации спор за счет термоповреждений жизненно важных белков и сублетальных повреждений мембраны, высказали опасения относительно эффективности стерилизации: «…стандартные условия теплового воздействия (120oС, 30 мин.) в некоторых случаях не обеспечивают высокой надежности стерилизации», «…существует принципиальная опасность восстановления и размножения в организме человека микроорганизмов, которые были признаны погибшими». По нашим данным даже такие облигатные и непатогенные термофилы как В. stearothermophilus способны к ограниченному размножению при 37oС, если к питательной среде добавить кровь человека.
Не только биологические индикаторы изредка содержали жизнеспособные споры после стерилизации, но и макеты обсемененных спорами медицинских изделий. Более того, предстерилизационная обработка макетов раствором кипящей соды или 0,2% раствора препарата «Септабик» не сопровождалась достаточным эффектом — стерилизация была неэффективной.
Теперь задача заключается в том, чтобы разработать новые методы, которые смогут гарантировать эффективность стерилизации. Наше представление о кинетике стерилизационного процесса позволили апробировать новые методические предложения, которые оказались перспективными, но требуют разносторонней проверки.
Выводы
1. Распределение редких и случайных событий позволяет рассчитывать среднее число спор на один биологический индикатор для условий, когда число жизнеспособных спор мало и встречаются они далеко не в каждом индикаторе.
2. Имеется достаточно оснований, чтобы усомниться в линейном характере зависимости между логарифмом числа спор в биологических индикаторах и временем от начала стерилизации. Жизнеспособные споры были обнаружены в биологических индикаторах даже через 1-2 часа пребывания в автоклаве при регламентированной температуре.
3. В экспериментах по контролю паровой стерилизации применяли значительное число биологических индикаторов, высокоэффективную цветную питательную среду и недельный срок культивирования в термостате, что в конечном итоге позволило обнаруживать жизнеспособные споры в биологических индикаторах после стерилизации чаще, чем обычно и практически при большинстве употребляющихся в практике режимах.
4. При высевах содержимого биологических индикаторов после стерилизации на плотную питательную среду в ряде случаев обнаруживались единичные колонии В. stearothermophilus, причем в большинстве случаев распределение агаровых чашек Петри по числу колоний в точности соответствовало распределению Пуассона, а это означало, что жизнеспособные споры не зависят друг от друга и расположены изолированно и случайно.
5. В некоторых экспериментах процент биологических индикаторов с жизнеспособными спорами после длительных сроков стерилизации превышал таковой после коротких сроков стерилизации, что не находило удовлетворительного объяснения. Мы предположили волнообразный характер зависимости логарифма числа жизнеспособных спор в биологических индикаторах от времени стерилизации.
6. Контроль стерилизаторов, установленных в практических лечебных учреждениях, показал, что во всех случаях та или иная часть биологических индикаторов содержала жизнеспособные споры после стерилизации, а вероятность неудовлетворительных результатов анализа индикаторов оказалась гораздо выше той, которая рекомендована в стандартах.
7. Экспериментальная паровая стерилизация отрезков трубочек из синтетических материалов, обсемененных спорами, после предстерилизационной очистки закончилась обнаружением жизнеспособных спор у более, чем половины экземпляров, т. е. результатами, аналогичными тем, которые были получены с биологическими индикаторами.
8. Число жизнеспособных спор в биологическом индикаторе после стерилизации является вероятностной величиной, а их обнаружение, кроме всего прочего, зависит от числа индикаторов в стерилизационной камере.
Литература
1. Абрамова И.М. Новые разработки в области стерилизации изделий медицинского назначения. Дезинфекционное дело, 1998, №3, с. 25.
2. Большев А.Н., Смирнов Н.В. Таблицы математической статистики. М., 1965.
3. Вашков В.И. Антимикробные средства и методы дезинфекции при инфекционных заболеваниях. М., 1977.
4. Гутерман Р.Л. Средства контроля термической стерилизации изделий медицинского назначения. Дисс. канд. мед. наук. М., 1993.
5. Кашнер Д. Жизнь микробов в экстремальных условиях. М., 1981.
6. Леви М.И., Бессонова В.Я., Лившиц М.М. Применение цветных питательных сред в процессе контроля стерилизации. Клиническая лабораторная диагностика, 1993, № 2, с. 65-67.
7. Леви М.И. Анализ неблагоприятных результатов паровой и воздушной стерилизации. Дезинфекционное дело, 1996, № 4, с. 58-63.
8. Леви М.И. Значение контроля стерилизации с помощью бумажных индикаторов и биотестов. Дезинфекционное дело, 1997, № 3, с. 24-28.
9. Леви М.И., Сучков Ю.Г., Рубан Г.И., Мищенко А.В. Новые формы бактериальных тестов для контроля разных режимов стерилизации. Там же, с. 29-33.
10. Леви М.И., Сучков Ю.Г., Лившиц М.М. Оптимизация биотестов для контроля паровой стерилизации. Дезинфекционное дело, 1998, № 2, с. 30-33.
11. Леви М.И. Численное определение величины D, стерилизационного времени и выбор контрольных биотестов. Там же, с. 34-42.
12. Методические указания по контролю паровых и воздушных стерилизаторов. Минздрав СССР, от 28.02.91 № 15/6-5.
13. Мунблит В.Я., Тальрозе В.Л., Трофимов В.И. Термоинактивация микроорганизмов. М., 1985.
14. Под ред. Озерецковского Н.А. и Останина Г.И. Бактерийные и вирусные лечебно-профилактические препараты. Аллергены. Дезинфекционно-стерилизационные режимы поликлиник. С.-Петербург, 1998.
15. Сучков Ю.Г., Леви М.И., Бессонова В.Я. Новый термофильный штамм для бактериологического контроля паровой стерилизации (сообщение 1), Дезинфекционное дело, 1996, № 3, с. 28-33.
16. Biological systems for testing sterilizers — Part 1: General requirements. European standard, Draft pr EN 866-1.1995.
17. Farrell J., Rose A.N. Temperature effect on microorganisms. In: «Thermobiology», p. 147-218. Acad. press, London-New-York, 1967.
18. Graham G.S. Biological indicators for hospital and industrial sterilization, p. 54-72. In: «Sterilization of medical product». Johnson and Johnson. Moscow, 1991.
19. Greene V.W. Principles and practice of disinfection, preservation and sterilization. Oxford, 1982.
20. International standard ISO/DIS 14161. Sterilization of health care products — guidence for the selection, use and interpretation of results. 1998.
21. McCormick P.J., Scoville J.R. — патент USA № 4.743.537, 1988 г.
22. Medical devices — Estimation of the population of microorganisms on product. Part 2 guidence, pr EN 1174-2.1994 г.
23. Russel A.D. The destruction of bacterial spores. Acad. press, London-New-York, 1982.
24. Russel A.D. Fundamental aspects of microbial resistance to chemical and physical agents. In: «Sterilization of medical product», v. V, p. 22-42. Johnson and Johnson, 1991.
25. Sussman A., Halvorson H. Spores, their dormancy and germinatiom. New-York-London, 1967.
26. Wicks J.H., Foltz W.E. Европейский патент № 0414.968 A1, 1991 г.
27. Журавлева В.И., Большедворская З.Ф. Оценка питательных сред для культивирования тест-микроорганизмов, используемых при контроле эффективности стерилизации в автоклавах. Лабораторное дело, 1988, № 11, с. 63-64.
28. Калинина Н.М., Шилова С.В., Мотина Г.Л., Чайковская С.М. Изучение термоустойчивости спор культуры Вас. stearothermophilus, используемой для приготовления биоиндикаторов. Антибиотики, 1982, № 2, с. 117-120.
29. Калинина Н.М., Мотина ГЛ., Чайковская С.М., Шилова С.В. Приготовление биоиндикаторов для контроля эффективности процессов стерилизации. Антибиотики, 1983, № 10, с. 600-603.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)