Брамитоб (Bramitob)
💊 Состав препарата Брамитоб
✅ Применение препарата Брамитоб
Описание активных компонентов препарата
Брамитоб
(Bramitob)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2020.06.23
Владелец регистрационного удостоверения:
Код ATX:
J01GB01
(Тобрамицин)
Лекарственная форма
| Брамитоб |
Р-р д/ингаляций 300 мг/4 мл: амп. 56 шт. рег. №: ЛСР-003882/08 |
Форма выпуска, упаковка и состав
препарата Брамитоб
Раствор для ингаляций от светло-желтого до желтого цвета, прозрачный.
Вспомогательные вещества: натрия хлорид — 4.5 мг, натрия гидроксид 1M — до pH 4.5-5.5, серная кислота 1M — 0.4 мл до pH 4.5-5.5, вода д/и — до 1 мл.
4 мл — ампулы пластиковые (4) — стрипы алюминиевые (14) — пачки картонные.
Фармакологическое действие
Антибиотик группы аминогликозидов, продуцируется грибами вида Streptomyces tenebrarius. Угнетает синтез белка в микробной клетке, что приводит к нарушению проницаемости клеточной мембраны, ее повреждению и гибели бактериальной клетки.
Активен в отношении широкого спектра грамотрицательных микроорганизмов, включая Pseudomonas aeruginosa. Бактерицидные концентрации тобрамицина равны или немного превышают минимальные ингибирующие концентрации в отношении Pseudomonas aeruginosa (МИК).
При ингаляционном применении тобрамицина у большинства пациентов с муковисцидозом концентрация тобрамицина в мокроте была в 25 раз выше МИК для Pseudomonas aeruginosa.
В группу чувствительных к тобрамицину микроорганизмов входят: Pseudomonas aeruginosa, Haemophilus influenzae, Staphylococcus aureus.
Нечувствительными являются: Burkholderia cepacia, Stenotrophomonas maltophilia, Alcaligenes xylosoxidans.
Фармакокинетика
Тобрамицин не активно проникает через мембраны эпителиальных клеток. Системная биодоступность тобрамицина после ингаляции зависит только от фракции активного вещества, достигнувшей дыхательных путей, т.к. тобрамицин не всасывается при приеме внутрь. Биодоступность тобрамицина индивидуальная и зависит от анатомических и функциональных особенностей дыхательных путей и от свойств ингалятора. Через 10 мин после ингаляции 300 мг тобрамицина средняя концентрация тобрамицина в мокроте составляет 1237 мкг/г (35-7414 мкг/г). Тобрамицин не накапливается в мокроте. После 20 недель применения средняя концентрация активного вещества в мокроте через 10 мин после ингаляции составляет 1154 мкг/г (39-7414 мкг/г). Спустя 2 ч после ингаляции содержание тобрамицина в мокроте составляет 14% от его концентрации в мокроте через 10 мин после ингаляции.
Средняя концентрация тобрамицина в плазме через 1 ч после ингаляции в дозе 300 мг у пациентов с муковисцидозом составляет 0.95 мкг/мл (максимально допустимое содержание тобрамицина в плазме крови — 3.62 мкг/мл). Через 20 недель после начала лечения средняя концентрация тобрамицина в плазме крови спустя 1 ч после ингаляции составляет 1.05 мкг/мл. После ингаляции тобрамицин, в основном, концентрируется в дыхательных путях. Связывание тобрамицина белками плазмы крови незначительно.
Тобрамицин не метаболизируется и в неизмененном виде выводится почками.
Тобрамицин выводится почками путем клубочковой фильтрации в неизменном виде.
T1/2 тобрамицина из плазмы крови после ингаляции 300 мг составляет 3 ч у пациентов с муковисцидозом.
Показания активных веществ препарата
Брамитоб
Длительное лечение хронической легочной инфекции, вызванной Pseudomonas aeruginosa (синегнойной палочкой), у пациентов с муковисцидозом в возрасте от 6 лет и старше.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Предназначен только для ингаляционного применения у взрослых и детей старше 6 лет.
Применяют по 300 мг 2 раза/сут в течение 28 дней независимо от массы тела пациента. Интервал между ингаляциями препарата должен составлять около 12 ч, но не менее 6 ч. После проведения 28-дневного курса терапии перерыв в применении препарата должен составлять 28 дней.
Побочное действие
Со стороны пищеварительной системы: редко — тошнота, потеря аппетита, рвота, язвы ротовой полости; очень редко — диарея, абдоминальная боль и кандидоз ротовой полости.
Со стороны крови и лимфатической системы: редко — лимфаденопатия.
Со стороны нервной системы: редко — головокружение, вкусовые нарушения, очень редко — сонливость.
Со стороны дыхательной системы: нечасто — изменения голоса (включая охриплость), афония, одышка, усиление кашля, фарингит; редко — бронхоспазм, стеснение в области грудины, кашель, задержка дыхания, легочные нарушения, увеличение количества мокроты, кровохарканье, снижение легочной функции, ларингит, носовые кровотечения, ринит, обострение бронхиальной астмы; очень редко — гипервентиляция, гипоксия, синусит; частота не известна — боль в ротоглотке.
Со стороны органа слуха и лабиринтные нарушения: редко — шум в ушах, снижение/потеря слуха; очень редко — боль в ушах.
Со стороны кожи и подкожных тканей: редко — сыпь; частота не известна — гиперчувствительность, зуд, крапивница.
Общие реакции: редко — боль в груди, астения, лихорадка, головная боль; очень редко — аллергические реакции, включая крапивницу и кожный зуд, грибковая инфекция, общее недомогание, боль в спине.
Противопоказания к применению
Повышенная чувствительность к тобрамицину и другим аминогликозидам; беременность, период грудного вскармливания; детский возраст до 6 лет.
С осторожностью
При нарушениях функции слухового или вестибулярного аппаратов, при установленном или предполагаемом заболевании почек, у пациентов с нейромышечными расстройствами, такими как паркинсонизм или другими заболеваниями, сопровождающимися мышечной слабостью, включая тяжелую псевдопаралитическую миастению (myasthenia gravis).
Поскольку при ингаляции с помощью небулайзера возможна активация кашлевого рефлекса, у пациентов с кровохарканьем применяют только в тех случаях, когда ожидаемая польза от терапии превышает потенциальный риск развития легочного кровотечения.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
Тобрамицин не метаболизируется ферментами печени, следовательно, изменения системной биодоступности тобрамицина у пациентов с печеночной недостаточностью маловероятны.
Применение при нарушениях функции почек
С осторожностью следует назначать препарат пациентам с установленными или предполагаемыми заболеваниями почек,
Применение у детей
Противопоказано применение препарата у детей до 6 лет.
Применение у пожилых пациентов
Режим дозирования у пациентов старше 65 лет устанавливается индивидуально с учетов состояния функции почек.
Особые указания
Терапию препаратом следует проводить только под наблюдением врача, имеющего опыт лечения муковисцидоза.
Лечение с чередованием курсов терапии с перерывами проводят до тех пор, пока сохраняется клинический эффект. При ухудшении течения заболевания на фоне лечения следует рассмотреть вопрос о назначении дополнительной антимикробной терапии, активной в отношении Pseudomonas aeruginosa.
До и после вдыхания необходимо определить функцию внешнего дыхания — ОФВ1. При развитии бронхоспазма у больных, не получающих бронхолитическую терапию, определение ОФВ1 необходимо повторить, в отдельных случаях с применением бронходилататоров. Если бронхоспазм не устраняется после использования бронходилататоров, то причиной его развития может быть повышенная чувствительность к тобрамицину. При подозрении на аллергическую реакцию ингаляции тобрамицина следует прекратить и начать соответствующую бронхолитическую терапию.
Учитывая потенциальную нефротоксичность аминогликозидов при парентеральном использовании, перед началом терапии необходимо провести оценку функции почек.
Через каждые 6 полных циклов терапии повторно определяют содержание мочевины и креатинина в плазме крови.
Учитывая потенциальную ототоксичность аминогликозидов, во время лечения необходимо проводить определение остроты слуха у больных с любыми нарушениями слуха (шум в ушах, снижение остроты слуха), а также при риске появления таких осложнений (особенно при наличии предшествующей длительной системной терапии аминогликозидами или при сопутствующей парентеральной терапии аминогликозидными антибиотиками).
У пациентов, получавших ранее длительное системное лечение аминогликозидами, до применения тобрамицина в виде ингаляций необходимо провести определение остроты слуха.
При наличии признаков нефротоксичности или ототоксичности лечение следует прекратить до тех пор, пока содержание тобрамицина в плазме крови не станет ниже 2 мкг/мл. После этого по усмотрению врача лечение может быть возобновлено. У пациентов с нормальной функцией почек через 1 ч после ингаляции тобрамицина сывороточная концентрация препарата приблизительно равна 1 мкг/мл.
У пациентов с нарушением слуха и/или функции почек, а также получающих сопутствующую парентеральную терапию аминогликозидами необходимо регулярно определять концентрацию тобрамицина в плазме крови.
Учитывая риск развития кумулятивной токсичности, необходимо обеспечить наблюдение за пациентами, получающими сопутствующую парентеральную терапию другими аминогликозидными антибиотиками.
Аминогликозиды могут оказывать курареподобное действие на нейромышечную передачу и усиливать мышечную слабость.
Существует теоретически возможный риск, что у пациентов при лечении ингаляционным тобрамицином может развиться резистентность Pseudomonas aeruginosa к в/в тобрамицину.
Влияние на способность к управлению транспортными средствами и механизмами
В связи с возможным возникновением головокружения или сонливости пациенты должны соблюдать осторожность при вождении транспортных средств или работе с механизмами.
Лекарственное взаимодействие
Следует избегать одновременного и/или последовательного применения тобрамицина в виде ингаляций с препаратами, обладающими нефротоксичностью или ототоксичностью.
Некоторые диуретики могут усиливать токсичность аминогликозидов путем изменения концентраций антибиотика в плазме крови и тканях. Тобрамицин в виде ингаляций не следует применять вместе с этакриновой кислотой, фуросемидом, мочевиной или маннитолом.
Следующие препараты также могут увеличивать потенциальную токсичность вводимых парентерально аминогликозидов: амфотерицин В, цефалотин, циклоспорин, полимиксины (возможно усиление нефротоксического эффекта); соединения платины (возможно усиление нефротоксического и ототоксического действия); антихолинэстеразные препараты, ботулотоксин (воздействие на нейромышечную систему).
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Брамитоб — инструкция по применению
Синонимы, аналоги
Статьи
ИНСТРУКЦИЯ
по медицинскому применению препарата
Регистрационный номер. ЛСР — 003882/08-210508
Торговое название.
Брамитоб
Международное непатентованное название.
тобрамицин
Лекарственная форма.
Раствор для ингаляций.
Состав.
1 мл препарата содержит:
Активное вещество:
Тобрамицин 75 мг
Вспомогательные вещества:
Натрия хлорид, натрия гидроксид, серная кислота, вода для инъекций.
Описание.
От светло-желтого до желтого цвета прозрачный раствор в герметично запаянной пластиковой ампуле.
Фармакотерапевтическая группа.
Антибиотик — аминогликозид.
Код АТХ.
J01GB01
Фармакологические свойства.
Тобрамицин — аминогликозидный антибиотик, продуцируемый микроорганизмами рода Streptomyces tenebrarius. Основной механизм его действия — нарушение синтеза белка, что ведет к изменению проницаемости клеточной мембраны, нарастающему повреждению клеточной оболочки и последующей гибели клетки. Тобрамицин обладает бактерицидным действием в концентрациях, равных или несколько превышающих подавляющие концентрации.
Тобрамицин проявляет активность, главным образом, в отношении грамотрицательных аэробных микроорганизмов, обладая низкой активностью в отношении анаэробных микроорганизмов и большинства грамположительных бактерий.
Тобрамицин более активен, чем гентамицин, в отношении Pseudomonas aeruginosa и некоторых штаммов протея; около 50% штаммов Pseudomonas aeruginosa, устойчивой к гентамицину, являются чувствительными к тобрамицину.
При ингаляционном введении минимальная подавляющая концентрация (МПК) тобрамицина в мокроте больных муковисцидозом существенно выше, чем при парентеральном введении.
Фармакокинетика.
После ингаляции 300 мг БРАМИТОБА больными муковисцидозом через 30 минут в мокроте достигается максимальная концентрация, равная примерно 1289 мкг/г, в то время как в плазме максимальная концентрация, равная 758 нг/мл, достигается примерно через 1,5 часа. Период полувыведения составляет 4,5 часа.
Выведение препарата, всосавшегося в кровь, происходит через почки путем клубочковой фильтрации.
Показания.
Лечение инфекций дыхательных путей, вызванных Pseudomonas aeruginosa у больных с муковисцидозом.
Противопоказания.
- повышенная чувствительность к препарату;
- детский возраст до 6 лет;
С осторожностью.
Ишемическая болезнь сердца, хроническая сердечная недостаточность в стадии декомпенсации, сахарный диабет, беременность. Почечная недостаточность, нарушение слуха, дисфункция вестибулярного аппарата или нейромышечная патология, такая как паркинсонизм или другие состояния, характеризующиеся мышечной слабостью, в том числе myasthenia gravis, острое кровохарканье.
Беременность и лактация.
Применение препарата в период беременности возможно, только если ожидаемая польза для матери превышает возможный риск для плода.
При необходимости применения препарата в период лактации, необходимо прекратить грудное вскармливание.
Способ применения и дозы.
Ингаляционно, с использованием небулайзера. Взрослые и дети старше 6 лет:
— по одной ампуле (300 мг) два раза в сутки (утром и вечером) в течение 28 дней. Интервал между ингаляциями должен составлять около 12 часов, но не менее 6 часов.
После применения БРАМИТОБА в течение 28 дней, необходимо сделать перерыв на 28 дней, после чего, продолжить терапию в течение последующих 28 дней.
Режим дозирования не учитывает массу тела. Всем пациентам следует назначать по одной ампуле Брамитоба (300 мг тобрамицина) два раза в сутки.
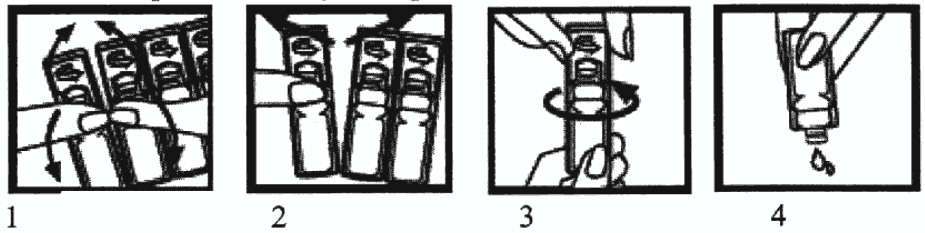
Указания к правильному использованию.
- Согнуть отделяемую ампулу от полоски в обоих направлениях.
- Отделить ампулу от полоски, вначале верхнюю часть, затем среднюю.
- Открыть ампулу, повернув ее верхнюю часть относительно корпуса в направлении, указанном стрелкой.
- Умеренно нажимая на стенки, вылить лекарственный препарат в стеклянное горлышко небулайзера.
Содержимое одной ампулы (300 мг), перелитое в небулайзер, вводится путем ингаляции за 10-15 минут с помощью многоразового небулайзера PARI LC PLUS с компрессорами, которые при подсоединении к небулайзеру PARI LC Plus, обеспечивают поставку 4-6 л/мин и/или обратное давление, равное 110-217 кПа.
Ингаляции Брамитоба проводятся в положении больного сидя или стоя, при обычном дыхании через загубник небулайзера. Носовой зажим может помочь пациенту дышать ртом.
Указания по очистке и дезинфекции небулайзера.
После окончания процедуры ингаляции небулайзер следует разобрать, отдельные его части (за исключением трубки) тщательно промыть горячей водой и жидким моющим средством, прополоскать и насухо вытереть чистой сухой тряпочкой, не оставляющей волокон. Для регулярной дезинфекции небулайзера рекомендуется опустить его отдельные части (кроме трубки), очищенные в соответствии с данными выше указаниями, в раствор, состоящий из одной части 9% уксусной кислоты и трех частей горячей воды, на один час, затем промыть горячей водой и насухо вытереть чистой тряпочкой.
После завершения дезинфекции использованный раствор следует сразу же вылить.
В качестве альтернативы дезинфекцию можно проводить путем кипячения в течение 10 минут.
Побочное действие.
| Очень редко |
Редко |
Не часто |
|
< 1/10000 |
1/10000-1/1000 |
1/1000-1/100 |
Со стороны костно-мышечной системы
- очень редко: боли в спине.
Со стороны крови и лимфатической системы:
- очень редко: лимфоаденопатия;
Со стороны органов чувств:
- редко: звон в ушах, потеря слуха;
- очень редко: вестибулярные и лабиринтные нарушения, боли в ухе.
Со стороны центральной и периферической нервной системы:
- редко: головная боль, головокружение;
- очень редко: сонливость.
Со стороны желудочно-кишечного тракта:
- редко: тошнота, язвенный стоматит, рвота, изменение вкуса;
- очень редко: диарея.
Со стороны органов дыхания:
- нечасто: изменение голоса, одышка, усиление кашля, фарингит;
- редко: бронхоспазм, усиление образования мокроты, кровохарканье, ухудшение функций легких, ларингит, носовое кровотечение, ринит.
- очень редко: гипервентиляция, гипоксия, синусит.
Местные реакции:
- очень редко: грибковые инфекции, кандидоз полости рта.
Другие:
- редко: кожная сыпь, анорексия, боли в грудной клетке, астения, лихорадка.
- очень редко: боль и дискомфорт в животе.
Передозировка.
Симптомом передозировки может быть выраженная осиплость голоса.
При случайном попадании БРАМИТОБА внутрь токсическое действие маловероятно, поскольку тобрамицин плохо всасывается из желудочно-кишечного тракта.
При случайном внутривенном введении БРАМИТОБА могут развиться симптомы и признаки передозировки тобрамицина, такие как головокружение, потеря слуха, звон в ушах, вертиго, респираторный дистресс-синдром, блокада нейромышечной проводимости и нарушение функции почек.
В случае проявления признаков передозировки БРАМИТОБ следует немедленно отменить и провести исследование показателей функции почек. Для контроля передозировки может быть полезным определение концентраций тобрамицина в сыворотке крови.
Взаимодействие с другими лекарственными средствами.
Не выявлено значимого лекарственного взаимодействия БРАМИТОБА при совместном применении с муколитиками, β 2- адреномиметиками, ингаляционными кортикостероидами и другими пероральными и парентеральными антибиотиками с антипсевдомонадной активностью.
Следует избегать одновременного или последовательного применения ингаляционного тобрамицина и других потенциально нефро- или ототоксичных лекарственных препаратов. Некоторые диуретики могут усиливать токсичность аминогликозидов, изменяя концентрации антибиотика в сыворотке и тканях. Ингаляционный тобрамицин не следует назначать одновременно с этакриновой кислотой, фуросемидом, мочевиной или маннитолом.
Токсичность аминогликозидов может увеличиваться при парентеральном введении следующих препаратов: амфотерицина В, цефалотина, циклоспорина, такролимуса, полимиксинов (риск усиления нефротоксичности), препаратов платины (риск усиления нефротоксичности и ототоксичности) а так же ингибиторов холинэстеразы и ботулотоксина (нейромышечные эффекты).
Особые указания.
Лечение БРАМИТОБОМ должен назначать врач, имеющий опыт ведения больных муковисцидозом. Длительность курсового лечения определяется врачом, исходя из клинической картины заболевания. В случае подтвержденного ухудшения легочных функций следует назначить дополнительную антибактериальную терапию.
При ингаляционном применении БРАМИТОБА может развиться бронхоспазм. Первую дозу БРАМИТОБА следует вводить под наблюдением врача, назначив перед ингаляцией бронходилататор, если он уже входит в используемую схему лечения больного. До и после процедуры следует измерить ОФВ1 (объем форсированного выдоха). При появлении признаков ятрогенного бронхоспазма у больного, не получающего бронходилататор, применение препарата нужно повторить отдельно, с использованием бронходилататора. Появление бронхоспазма на фоне применения бронходилататора может указывать на аллергическую реакцию. При подозрении на аллергическую реакцию применение БРАМИТОБА следует прекратить. Для купирования бронхоспазма следует проводить соответствующую патогенетическую терапию.
Во время лечения БРАМИТОБОМ пациенту следует продолжать стандартную физиотерапию грудной клетки. Применение бронходилататоров должно продолжаться по клиническим показаниям. При использовании нескольких методов лечения дыхательных нарушений рекомендуется следующий порядок: бронходилататор, дыхательная физиотерапия, другие ингаляционные лекарственные средства и в конце — Брамитоб.
Брамитоб не следует смешивать с другими ингаляционными лекарственными средствами.
БРАМИТОБ следует применять с большой осторожностью у больных с паркинсонизмом или другими состояниями, характеризующимися мышечной слабостью, включая myasthenia gravis, поскольку аминогликозиды могут усиливать мышечную слабость из-за возможного курареподобного действия на нейромышечную проводимость.
Препарат следует применять с осторожностью у больных с доказанной или подозреваемой почечной недостаточностью, при условии мониторинга концентраций тобрамицина в сыворотке крови.
Необходимо периодически оценивать показатели функции почек (уровень мочевины и креатинина не менее одного раза в течение 6 курсов терапии БРАМИТОБОМ). При появлении признаков нефротоксичности, лечение тобрамицином следует прервать до снижения минимальных концентраций препарата в сыворотке менее 2 мкг/мл. Затем лечение БРАМИТОБОМ можно возобновить по медицинским показаниям. Пациентов, одновременно получающих парентеральную терапию другими аминогликозидами, следует тщательно наблюдать из-за возможности развития кумулятивной токсичности.
При использовании аминогликозидов возможно развитие ототоксичности (гипоакузия, системное и несистемное головокружение, атаксия).
Врач должен учесть возможность того, что аминогликозиды могут обладать вестибулярной и кохлеарной токсичностью и в ходе терапии БРАМИТОБОМ должен оценивать функцию слуха. Больным, принимавшим ранее аминогликозиды в течение длительного времени, рекомендуется прохождение аудиометрических тестов до начала терапии БРАМИТОБОМ. При лечении головокружения следует принимать во внимание, что оно является проявлением ототоксичности. При возникновении головокружения или снижения слуха в ходе терапии БРАМИТОБОМ, необходимо проведение аудиологического обследования.
При ингаляции возможно появление кашлевого рефлекса. Применение ингаляционного тобрамицина у больных с острым кровохарканьем должно проводиться только в том случае, если польза от лечения превышает риск провокации дальнейшего кровотечения.
У некоторых больных, получавших тобрамицин, отмечается повышение МПК аминогликозидов в отношении изученных выделенных штаммов P. aeruginosa. Возможно развитие резистентности штаммов P. aeruginosa, к внутривенно вводимому тобрамицину.
Форма выпуска.
Раствор для ингаляций 300 мг/4 мл.
По 4 мл в герметично запаянную пластиковую ампулу. Полоска по 4 ампулы помещается в алюминиевый стрип. По 4, 7 или 14 стрипов с инструкцией по применению помещают в картонную пачку.
Срок годности.
2 года.
Не использовать позже даты, указанной на упаковке.
Условия хранения.
При температуре + 2-8°С, в оригинальной упаковке для защиты от света, вдали от нагревательных приборов. Не замораживать. Хранить в недоступном для детей месте.
Условия отпуска из аптек.
По рецепту.
Производитель.
Chiesi Farmacetutici S.p.A.
Via Palermo 26/A
Parma, Italy.
Произведено:
Holopack Verpackungstechnik GmbH
Bahnhofstrabe 74429 Sulzbach-Laufen, Germany.
Кьези Фармацевтичи С.П.А.,
26/A, ВИА ПАЛЕРМО,
ПАРМА, Италия
Голопак Ферпакунгстехник ГмбХ
Банхофштрассе 74429 Зульцбах-Лауфен, Германия.
Претензии потребителей направлять по адресу:
ООО «Кьези Фармасьютикалс»
125190, г. Москва, ул. Усиевича, д.20, стр.1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Общая характеристика
Прозрачный желтоватый раствор (не более чем Y3).
Состав лекарственного средства
Каждый мл содержит: активный ингредиент: тобрамицин 75 мг; другие ингредиенты: кислота серная разведенная 2 М до pH 4,5–5,5, раствор натрия гидроксида 1 М до pH 4,5–5,5, натрия хлорид, вода для инъекций до 1 мл.
Антибактериальные средства для системного применения. Аминогликозидные антибиотики.
Код ATX: J01GB01.
Фармакологические свойства
Фармакодинамика
Тобрамицин является антибиотиком группы аминогликозидов, вырабатываемым Streptomyces tenebrarius. Его основной механизм действия заключается в прерывании синтеза белка с последующих изменением проницаемости клеточной мембраны, прогрессирующим разрывом клеточной оболочки и последующей гибелью клеток бактерий. Препарат оказывает бактерицидное действие при концентрациях, равных или немного превышающих ингибирующие концентрации.
Контрольные точки
Установленные контрольные точки чувствительности для парентерального введения тобрамицина не применимы для препарата в форме аэрозоля. Мокрота кистозного фиброза (КФ) ингибирует местную биологическую активность аминогликозидов в форме ингаляции. Вследствие этого концентрации тобрамицина в форме аэрозоля в мокроте должны быть в 10–25 раз выше минимальной ингибирующей концентрации (МИК) для подавления роста P. aeruginosa и бактерицидного действия соответственно. В рамках контролируемых клинических исследований 90 % пациентов, принимавших тобрамицин, достигали концентраций в мокроте в 10 раз превышавших максимальную МИК P. aeruginosa в посеве пациента, а 84 % пациентов, принимавших тобрамицин, достигали концентраций в 25 раз выше максимальной МИК. Клиническая польза достигается у большинства пациентов со штаммами, значения МИК которых превышают контрольные точки при парентеральном введении.
Чувствительность
Ввиду отсутствия стандартных контрольных точек чувствительности для ингаляций, следует проявлять осторожность при определении организмов как чувствительных, так и нечувствительные к тобрамицину для небулайзера.
Клинические исследования тобрамицина в форме ингаляции показали, что большинство пациентов (88 %) с изолятами P. aeruginosa при МИК тобрамицина < 128 мкг/мл в начале исследования показали улучшение легочной функции после терапии тобрамицином. Пациенты с изолятом P. aeruginosa при МИК ≥ 128 мкг/мл в начале исследования менее вероятно показывают клинический ответ.
На основании данных in vitro и/или опыта проведения клинических исследований, организмы, вызывающие легочные инфекции при КФ, могут показать следующий ответ на терапию тобрамицином:
| Чувствительные | Pseudomonas aeruginosa Haemophilus influenzae Staphylococcus aureus |
| Нечувствительные | Burkholderia cepacia Stenotrophomonas maltophilia Alcaligenes xylosoxidans |
Клинические исследования применения тобрамицина показали незначительное, однако выраженное повышение минимальных ингибирующих концентраций тобрамицина, амикацина и гентамицина к исследованным изолятам P. aeruginosa. Каждые дополнительные 6 месяцев терапии привели к постепенному росту, схожему с установленным в ходе 6 месяцев контролируемых исследований. Основным механизмом резистентности к аминогликозидам, установленным для P. aeruginosa, выделенной у пациентов при КФ с хроническими инфекциями, является непроницаемость, определяемая как отсутствие чувствительности ко всем аминогликозидам. P. aeruginosa, выделенная у пациентов с КФ, также показала адаптивную устойчивость к аминогликозидам, которая характеризуется восстановлением чувствительности после отмены антибиотика.
Прочая информация
Контролируемые клинические исследования показали, что терапия препаратом Брамитоб, проведенная в соответствии с описанными выше поочередными циклами, привела к улучшению легочной функции, причем результаты сохранялись выше исходных показателей на протяжении всего периода терапии и 28 последующих дней.
Клинические исследования тобрамицина не представляют данных по возрастной группе пациентов до 6 лет.
Не доказано, что пациенты, принимающие тобрамицин до 18 месяцев, подвержены повышенному риску приобретения B. cepacia, S. maltophilia или А. xylosoxidans, по сравнению с пациентами, не принимавшими тобрамицин. Виды Aspergillus чаще обнаруживались в мокроте пациентов, принимавших тобрамицин; тем не менее такие клинические осложнения как аллергический бронхолегочный аспергиллез (ABPA) регистрировались редко и с той же частотой, что и в контрольной группе.
Фармакокинетика
Абсорбция и распределение
После приема внутрь только 0,3–0,5 % препарата обнаруживается в моче, что отражает системную абсорбцию. После введения через небулайзер 6 пациентам с кистозным фиброзом средняя абсолютная биодоступность составила около 9,1 % дозы. Системная абсорбция тобрамицина незначительна при ингаляции аэрозоля и при ограниченном поступлении вдыхаемого препарата в большой круг кровообращения. По оценке около 10 % массы изначально распыленного препарата оседает в легких, а оставшиеся 90 % остается в небулайзере, оседает в ротоглотке, проглатывается или выдыхается в атмосферу.
Концентрации в мокроте: через 10 минут после вдыхания первой дозы Брамитоба 300 мг средняя концентрация тобрамицина в мокроте составила 695,6 мкг/г (диапазон: 36–2638 мкг/г). Тобрамицин не кумулирует в мокроте; после 20 недель терапии Брамитобом средняя концентрация тобрамицина в мокроте через 10 минут после ингаляции составила 716,9 мкг/г (диапазон: 40–2530 мкг/г). Установлены значительные вариации концентрации тобрамицина в мокроте. Через два часа после ингаляции концентрация в мокроте уменьшились примерно до 14 % от уровней тобрамицина, установленных через 10 минут после ингаляции.
Концентрации в сыворотке крови: медианная концентрация тобрамицина в сыворотке крови через 1 час после ингаляции однократной дозы Брамитоба 300 мг пациентами с КФ составила 0,68 мкг/мл (диапазон: 0,06–1,89 мкг/мл). После 20 недель терапии тобрамицином медианная концентрация тобрамицина в сыворотке крови через 1 час после дозирования составила 1,05 мкг/мл (диапазон: ниже лимита количественного определения – 3,41 мкг/мл).
Выведение
Выведение тобрамицина в форме ингаляции не исследовали. После внутривенного введения системно абсорбированный тобрамицин, в основном, выводится клубочковой фильтрацией. Период полувыведения тобрамицина из сыворотки крови составляет около 2 часов. Менее 10 % тобрамицина связывается с белками плазмы крови.
Неабсорбированный тобрамицин после приема препарата, в основном, выводится с мокротой при откашливании.
Показания
Лечение хронической легочной инфекции, вызванной Pseudomonas aeruginosa, у пациентов с кистозным фиброзом в возрасте 6 лет и старше.
Брамитоб предназначен исключительно для ингаляций, а не для парентерального применения.
Следует учитывать официальные инструкции по надлежащему применению антибактериальных средств.
Терапию должен начинать терапевт, имеющий опыт лечения кистозного фиброза.
Рекомендованная доза для взрослых и детей старше 6 лет: один контейнер с однократной дозой (300 мг) два раза в сутки (утром и вечером) на протяжении 28 дней. Интервалы между применениями должны быть максимально близки к 12 часам. После 28 дней терапии Брамитобом пациенты должны прекратить прием препарата на протяжении следующих 28 дней. Следует чередовать циклы по 28 дней активной терапии и 28 дней без лечения (28-днейвный терапевтический цикл и 28 дней без лечения).
Дети до 6 лет
Эффективность и безопасность препарата Брамитоб не установлена в популяции пациентов в возрасте до 6 лет.
Пожилые пациенты
Тобрамицин следует с осторожностью назначать пожилым пациентам с нарушением почечной функции.
Пациенты с почечной недостаточностью
Тобрамицин следует с осторожностью назначать пациентам с известным или предположительным нарушением почечной функции. Брамитоб следует отменить в случае нефротоксичности, пока концентрация тобрамицина в сыворотке крови не станет меньше 2 мкг/мл.
Пациенты с печеночной недостаточностью
При печеночной недостаточности изменение дозы Брамитоба не требуется.
Доза не корректируется в зависимости от массы тела. Всем пациентам следует назначать один контейнер с однократной дозой препарата Брамитоб (300 мг тобрамицина) два раза в сутки.
Лечение тобрамицином должно продолжаться циклично на протяжении периода, пока терапевт считает, что пациент получает клиническую пользу от включения Брамитоба в терапевтический режим. При проявлении признаков клинического ухудшения легочного статуса следует рассмотреть возможность назначения дополнительной антисинегнойной терапии.
Способ применения
Контейнер с однократной дозой следует открывать непосредственно перед применением. Любой не использованный незамедлительно раствор следует утилизировать и не хранить для повторного использования.
Брамитоб следует применять в соответствии с общими санитарно-гигиеническими стандартами. Используемое устройство должно быть чистым и правильно работать; небулайзер, предназначенный только для личного использования, должен регулярно проходить очистку и дезинфекцию.
При очистке и дезинфекции небулайзера необходимо следовать инструкциям, прилагаемым к устройству.
Максимальная переносимая суточная доза
Максимальная переносимая суточная доза препарата Брамитоб не установлена.
Инструкция по вскрытию контейнера
Согните контейнер с однократной дозой в двух направлениях
Отделите контейнер с однократной дозой от пластины, сначала сверху, а затем посередине
Откройте контейнер с однократной дозой, вращая клапан по стрелке
Прилагая умеренное давление на стенки контейнера с однократной дозой, влейте препарат в стеклянную трубку небулайзера.
Содержимое одного контейнера с однократной дозой (300 мг), извлеченное в небулайзер, следует применять в форме ингаляции примерно за 15 минут, используя небулайзер для многократного применения PARI LC PLUS, оборудованный компрессором PARI TURBO BOY (скорость подачи препарата 6,2 мг/мин, общая подача препарата 92,8 мг, средний массовый аэродинамический диаметр: D10 0,65 мкм, D50 3,15 мкм, D90 8,99 мкм) или PARI LC SPRINT, оборудованный компрессором PARI BOY Sx (скорость подачи препарата 6,7 мг/мин, общая подача препарата 99,8 мг, средний массовый аэродинамический диаметр: D10 0,70 мкм, D50 3,36 мкм, D90 9,41 мкм).
Ингаляцию Брамитоба проводят в положении сидя или стоя при нормальных вдохах через наконечник небулайзера. Носовые зажимы могут способствовать вдыханию через рот. Пациент должен придерживаться стандартного режима физиотерапии грудной клетки. Применение необходимых бронхолитических средств продолжается согласно клинической необходимости. Пациентам, получающим несколько различных респираторных терапий, рекомендовано принимать их в следующем порядке: бронхолитическое средство, дыхательная физиотерапия, прочие препараты для ингаляции и Брамитоб.
Брамитоб не следует смешивать с иными препаратами для ингаляции.
Контролируемые клинические исследования и неконтролируемые клинические исследования препарата Брамитоб (565 пациентов принимали препарат) показали, что наиболее частые реакции приходились на дыхательные пути (кашель и дисфония).
Заявленные в ходе клинических исследований нежелательные реакции (см. ниже) классифицировали следующим образом: часто (≥ 1/100 и < 1/10); нечасто (≥ 1/1000 и < 1/100); редко (≥ 1/10 000 и < 1/1000); очень редко (< 1/10 000).
| Класс системы органов | Нежелательная реакция | Частота развития |
| Инфекции и инвазии | Грибковая инфекция, кандидоз ротовой полости | Нечасто |
| Нарушения со стороны нервной системы | Головная боль | Нечасто |
| Нарушения со стороны органов слуха и лабиринта | Вертиго, тугоухость, нейросенсорная тугоухость (см. раздел 4.4) | Нечасто |
| Респираторные, торакальные и медиастинальные нарушения | Кашель, дисфония | Часто |
| Уменьшение объема форсированного выдоха, одышка, хрипы, кровохарканье, ротоглоточная боль, кашель с мокротой | Нечасто | |
| Нарушения со стороны желудочно-кишечного тракта | Повышенное слюноотделение, воспаление языка, боль в верхней части живота, тошнота | Нечасто |
| Нарушения со стороны кожи и подкожной ткани | Сыпь | Нечасто |
| Общие нарушения и состояния в месте применения | Астения, ощущение дискомфорта в грудной клетке, сухость слизистой оболочки | Нечасто |
| Обследования | Повышенный уровень трансаминаз | Нечасто |
В рамках контролируемых клинических исследований других препаратов для ингаляций, содержащих тобрамицин, дисфония и звон в ушах были единственными нежелательными явлениями, заявленными у значительно большего количества пациентов, по сравнению с группой тобрамицина (13 % в группе тобрамицина по сравнению с 7 % в контрольной группе) и (3 % в группе тобрамицина по сравнению с 0 % в контрольной группе).
Данные эпизоды звона в ушах имели временный характер и устранялись без отмены терапии тобрамицином. Они не вызывали постоянную тугоухость согласно результатам аудиографического анализа. Риск развития звона в ушах не повышался при повторных циклах применения тобрамицина. Дополнительные нежелательные явления, отдельных из них были следствием фонового заболевания, однако, возможно, имели причинно-следственную связь с тобрамицином: изменение цвета мокроты, инфекция дыхательных путей, миалгия, носовой полип и отит среднего уха. Кроме того, сводные постмаркетинговые данные о применении содержащих тобрамицин препаратов для небулайзера включали следующие нежелательные реакции (представленная выше классификация частоты развития):
| Класс системы органов | Нежелательная реакция | Частота развития |
| Инфекции и инвазии | Ларингит | Редко |
| Грибковая инфекция, кандидоз ротовой полости | Очень редко | |
| Нарушения со стороны крови и лимфатической системы | Лимфаденопатия | Очень редко |
| Нарушения со стороны иммунной системы | Повышенная чувствительность | Очень редко |
| Расстройства метаболизма и питания | Анорексия | Редко |
| Нарушения со стороны нервной системы | Головокружение, головная боль, афония | Редко |
| Сонливость | Очень редко | |
| Нарушения со стороны органов слуха и лабиринта | Звон в ушах, тугоухость (см. раздел 4.4) | Редко |
| Нарушения со стороны органов слуха, боль в ушах | Очень редко | |
| Респираторные, торакальные и медиастинальные нарушения | Кашель, фарингит, дисфония, одышка | Нечасто |
| Бронхоспазм, ощущение дискомфорта в грудной клетке, легочные нарушения, кровохарканье, носовое кровотечение, ринит, астма, кашель с мокротой | Редко | |
| Гипервентиляция, гипоксия, синусит | Очень редко | |
| Нарушения со стороны желудочно-кишечного тракта | Дисгевзия, образование язв в ротовой полости, рвота, тошнота | Редко |
| Диарея, боль в животе | Очень редко | |
| Нарушения со стороны кожи и подкожной ткани | Сыпь | Редко |
| крапивница, зуд | Очень редко | |
| Нарушения со стороны опорно-двигательного аппарата, соединительных тканей и костей | Боль в пояснице | Очень редко |
| Общие нарушения и состояния в месте применения | Астения, пирексия, боль в груди, боль, тошнота | Редко |
| Недомогание | Очень редко | |
| Обследования | Понижение легочной функции | Редко |
Открытые исследования и постмаркетинговый опыт показали, что у некоторых пациентов после продолжительного предыдущего или комплексного внутривенного введения аминогликозидов развивалась тугоухость. Парентеральное введение аминогликозидов приводит к повышенной чувствительности, ототоксичности и нефротоксичности.
Прием Брамитоба противопоказан всем пациентам с повышенной чувствительностью к тобрамицину, другим аминогликозидам или любым вспомогательным веществам.
Препарат также противопоказан пациентам, принимающим сильнодействующие диуретики, такие как фуросемид или этакриновая кислота, ототоксичность которых доказана.
Симптомы
Прием препарата в форме ингаляции обеспечивает низкую системную биодоступность тобрамицина. Симптомы передозировки аэрозолем могут включать тяжелую охриплость голоса.
При случайном проглатывании Брамитоба токсическое воздействие маловероятно, поскольку тобрамицин слабо абсорбируется из здорового желудочно-кишечного тракта.
При случайном внутривенном введении Брамитоба могут развиться признаки и симптомы парентеральной передозировки тобрамицином, например: головокружение, звон в ушах, вертиго, тугоухость, затруднение дыхания и/или нейромышечная блокада и нарушение функции почек.
Лечение
Острую токсичность следует лечить незамедлительной отменой Брамитоба; необходимо провести базовые анализы почечной функции. Концентрации тобрамицина в сыворотке крови позволят контролировать передозировку. В случае любой передозировки следует учитывать возможность лекарственных взаимодействий с изменением скорости выведения Брамитоба или других лекарственных средств.
Общие предостережения
Тобрамицин следует с осторожностью назначать пациентам с известным или предположительным нарушением функции почек, органов слуха, вестибулярного аппарата или нейромышечными нарушениями, а также с острым активным кровохарканьем.
Функция почек и черепного нерва требует строгого контроля у пациентов с известной или предполагаемой почечной недостаточностью, а также у пациентов с первоначально нормальной функцией почек, у которых, однако, развиваются признаки нарушения почечной функции в период терапии. В случае подтверждения нарушения функции почек, вестибулярного аппарата и/или органов слуха необходимо отменить препарат или изменить дозировку.
Концентрацию тобрамицина в сыворотке крови также следует контролировать посредством забора образца крови из вены, а не из пальца, поскольку последний не является валидированным методом дозирования. Установлено, что загрязнение кожи пальцев после приготовления и небулизации тобрамицина может привести к ложному повышению уровней препарата в сыворотке крови. Такое загрязнение невозможно полностью устранить мытьем рук перед проведением анализа.
Бронхоспазм
Бронхоспазм может развиваться после ингаляций лекарственных средств и заявлен при применении тобрамицина с помощью небулайзера. Первая доза Брамитоба назначается под контролем медицинского работника с предварительным применением бронхолитического средства перед ингаляцией из небулайзера, если оно уже включено в текущий терапевтический режим пациента. ОФВ1 (объем форсированного выдоха) необходимо измерить до и после ингаляции. При подтверждении вызванного терапией бронхоспазма у пациента, не принимающего бронхолитическое средство, анализ необходимо повторить на частном случае, используя бронхолитическое средство. Развитие бронхоспазма в ходе бронхолитической терапии может указывать на аллергическую реакцию. При подозрении на аллергическую реакцию к тобрамицину Брамитоб следует отменить. Бронхоспазм следует лечить приемлемыми клиническими средствами.
Нейромышечные нарушения
Тобрамицин следует с особой осторожностью назначать пациентам с нейромышечными нарушениями, например, паркинсонизм или иными состояниями, которые характеризуются миастенией, включая миастению gravis, поскольку аминогликозид может усилить мышечную слабость вследствие потенциального курареподобного действия на нейромышечную функцию.
Нефротоксичность
Несмотря на то, что парентеральная терапия аминогликозидом связана с нефротоксичностью, клинические исследования тобрамицина не выявили нефротоксичности. Препарат следует с осторожностью назначать пациентам с подтвержденной или предположительной почечной недостаточностью и контролировать концентрации тобрамицина в сыворотке крови, например, проводить количественное определение уровней вещества в сыворотке крови после двух или трех дозирований, чтобы при необходимости можно было скорректировать дозу, а также каждые три – четыре дня в ходе терапии. В случае изменения функции почек уровни вещества в сыворотке крови следует измерять чаще, а также корректировать дозу или интервалы между дозированиями. Пациентов с острой почечной недостаточностью (креатинин сыворотки крови > 2 мг/дл (176,8 мкмоль/л)) не включали в клинические исследования.
Согласно рекомендациям текущей клинической практики, необходимо проводить оценку начальной почечной функции. Кроме того, функцию почек необходимо время от времени измерять повторно за счет регулярного мониторинга уровней мочевины и креатинина по меньшей мере после каждых 6 полных циклов терапии тобрамицин (180 дней лечения ингаляциями тобрамицина). Если нефротоксичность подтвердится, терапию тобрамицином следует отменить до тех пор, пока минимальные уровни вещества в сыворотке крови не упадут ниже 2 мкг/мл. Затем терапию тобрамицином можно возобновить после консультации с врачом. Пациенты, комплексно принимающие аминогликозид парентерально, требуют строгого контроля ввиду риска накопительной токсичности.
Особенно важно контролировать функцию почек у пожилых пациентов, у которых почечная функция может быть понижена, чего не выявляют анализы в рамках планового осмотра, например, анализы уровня мочевины в крови или креатинина сыворотки крови. Более полезным может быть определение клиренса креатинина.
Следует провести анализ мочи на повышенный уровень белка, клеток и осадка. Креатинин сыворотки крови или клиренс креатинина (более предпочтительно, чем мочевина крови) должны периодически измеряться.
Ототоксичность
Ототоксичность, которая проявляется в форме слуховой и вестибулярной токсичности, установлена при парентеральном применении аминогликозидов. Вестибулярная токсичность может проявляться в форме вертиго, атаксии или головокружения.
В рамках контролируемых клинических исследований тобрамицина установлены умеренные гипакузия и вертиго, а слуховая токсичность при применении иных препаратов тобрамицина в форме ингаляции согласно жалобам на тугоухость или аудиометрическим измерениям не установлена в ходе контролируемых клинических исследований.
В рамках открытых исследований и постмаркетингового опыта у некоторых пациентов с предыдущим или комплексным внутривенным введением аминогликозидов в анамнезе зарегистрирована тугоухость. Терапевт должен учитывать вероятность того, что аминогликозиды могут вызывать вестибулярную и кохлеарную токсичность, и должен оценивать слуховую функцию на протяжении всего курса лечения препаратом Брамитоб. Пациентам с фактором предрасположенности ввиду продолжительной системной терапии аминогликозидами в прошлом может потребоваться аудиологическая оценка перед началом терапии тобрамицином. Следует проявлять осторожность при развитии звона в ушах, поскольку он представляет собой симптом ототоксичности. Если пациент сообщает о звоне в ушах или тугоухости в ходе терапии аминогликозидами, врач должен определить, необходимо ли проводить аудиологические тесты. При возможности следует периодически проводить аудиограммы у пациентов на продолжительной терапии, и, по этой причине, особенно у пациентов, подверженных высокому риску ототоксичности. Пациенты, комплексно проходящие парентеральную терапию аминогликозидами, должны проходить контроль согласно клинической необходимости с учетом риска накопительной токсичности.
Кровохарканье
Ингаляции растворами из небулайзеров могут стимулировать кашлевой рефлекс. Ингаляции Брамитоба у пациентов с активным тяжелым кровохарканьем показаны только в том случае, если польза от терапии превосходит риски усиления кровотечения.
Устойчивость микроорганизмов
Клинические исследования показали, что у некоторых пациентов, получающих ингаляции тобрамицина, наблюдается повышение минимальной ингибирующей концентрации аминогликозида к исследованным изолятам P. aeruginosa. Имеется теоретический риск того, что при ингаляции тобрамицина пациенты подвержены развитию изолятов P. aeruginosa, устойчивых к тобрамицину для внутривенного введения. Клинические исследования не включают данных о пациентах с инфекциями Burkholderia cepacia.
Беременность и лактация
Брамитоб следует принимать в период беременности или лактации только в том случае, если польза для матери превосходит риски для плода или ребенка.
Беременность
Не имеется достаточных данных о применении тобрамицина в форме ингаляции беременными женщинами. Исследования на животных не выявили тератогенного действия тобрамицина. Тем не менее аминогликозиды могут наносить вред плоду (например, врожденная глухота) при достижении высоких системных концентраций в организме беременной женщины. При применении Брамитоба в период беременности, а также в случае диагностирования беременности в период терапии Брамитобом пациентку необходимо уведомить о потенциальной опасности для плода.
Лактация
При системном воздействии тобрамицин выделяется в грудное молоко. Неизвестно, обеспечат ли ингаляции тобрамицина концентрации в сыворотке крови, достаточно высокие для обнаружения тобрамицина в грудном молоке.
Ввиду потенциального риска ототоксичности и нефротоксичности тобрамицина у новорожденных необходимо принять решение о прекращении грудного вскармливания или отмене Брамитоба.
Влияние на способность управлять автомобилем и другими механизмами
Не проводили исследования влияния на способность управлять автомобилем и другими механизмами.
На основании сообщений о нежелательных реакциях можно сделать вывод, что тобрамицин маловероятно влияет на способность управлять автомобилем и другими механизмами. Тем не менее, ввиду возможного развития головокружения и/или вертиго, следует предупредить пациентов, намеренных управлять автомобилем или работать с механизмами.
Следует избегать комплексного и/или последующего применения Брамитоба с иными препаратами, обладающими нефротоксичным или ототоксичным потенциалом. Некоторые диуретики могут усиливать токсичность аминогликозида за счет изменения концентраций антибиотика в сыворотке крови и тканях. Брамитоб не следует комплексно назначать с фуросемидом, этакриновой кислотой, мочевиной или маннитолом.
Прочие препараты, повышающие потенциальную токсичность аминогликозидов при парентеральном введении, включают:
амфотерицин В, цефалотин, циклоспорин, такролимус, полимиксины (риск повышения нефротоксичности); компоненты платины (риск повышения нефротоксичности и ототоксичности);
антихолинэстеразы, ботулинический токсин. Ввиду нейромышечных эффектов данных веществ, следует избегать их комплексного применения с тобрамицином.
Прочее:
Клинические исследования показали, что пациенты, принимающие тобрамицин в форме ингаляции комплексно с дорназой альфа, муколитическими средствами, β-агонистами, кортикостероидами для ингаляции и иными аминогликозидными антибиотиками для приема внутрь или парентерального введения, склонны к развитию тех же нежелательных явлений, что и пациенты в контрольной группе.
Условия и срок хранения
При температуре +2–8 °C, в оригинальной упаковке для защиты от света, вдали от нагревательных приборов.
Хранить в недоступном для детей месте.
Срок годности 2 года. Не использовать после истечения указанного срока годности.
Первичная упаковка.
По 4 мл в герметично запаянную пластиковую ампулу.
Полоска по 4 ампулы помещается в стрип из ПЕТ/ПЕ/алюминия.
Вторичная упаковка
По 14 стрипов с инструкцией по применению помещают в картонную пачку
Информация о производителе/заявителе
Кьези Фармацевтичи С.п.А.
Виа Сан Леонардо, 96, 43100 Парма, Италия.
-
По рецепту
Внешний вид товара может отличаться
Брамитоб раствор для ингаляций 300 мг 4 мл ампулы 56 шт.
Товара нет в наличии.
🏥 Купить Брамитоб раствор для ингаляций 300 мг 4 мл ампулы 56 шт. в наших аптеках в Москве
💊 Брамитоб раствор для ингаляций 300 мг 4 мл ампулы 56 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки
- Форма выпуска:раствор
- Дозировка:300 мг/4 мл
Это термолабильный препарат — перевозится в специальном контейнере, для сохранения оптимальной температуры.
Учтите это при самовывозе.
Доставка и самовывоз только по Москве
все формы выпуска Брамитоб,
1 шт.
🏥 Купить Брамитоб раствор для ингаляций 300 мг 4 мл ампулы 56 шт. в наших аптеках в Москве
💊 Брамитоб раствор для ингаляций 300 мг 4 мл ампулы 56 шт. в интернет-аптеке «WER.RU»
🚚 Доставка со склада в Москве от 1-го дня
⚠ Отпускается по рецепту в торговом зале аптеки
Инструкция по медицинскому
применению Брамитоб
ИМЕЮТСЯ ПРОТИВОПОКАЗАНИЯ, ПЕРЕД ПРИМЕНЕНИЕМ НЕОБХОДИМО
ПРОКОНСУЛЬТИРОВАТЬСЯ СО СПЕЦИАЛИСТОМ
Сертификаты и лицензии
Состав
1 мл препарата
содержит:
Активное
вещество:
Тобрамицин 75 мг
Вспомогательные
вещества:
Натрия хлорид
4,5 мг, натрия гидроксид 1М до рН 4,5–5,5, кислота серная 1М 0,4 мл
до рН 4,5–5,5, вода для инъекций до 1 мл.
Описание
От
светло-желтого до желтого цвета прозрачный раствор в герметично запаянной
пластиковой ампуле.
Фармакокинетика
После ингаляции
300 мг БРАМИТОБА больными муковисцидозом через 30 минут в мокроте достигается
максимальная концентрация, равная примерно 1289 мкг/г, в то время как в плазме
максимальная концентрация, равная 758 нг/мл, достигается примерно через 1,5
часа. Период полувыведения составляет 4,5 часа.
Выведение
препарата, всосавшегося в кровь, происходит через почки путем клубочковой
фильтрации.
Иммунобиологические свойства
Тобрамицин —
аминогликозидный антибиотик, продуцируемый микроорганизмами рода Streptomyces
tenebrarius. Основной механизм его действия — нарушение синтеза белка, что
ведет к изменению проницаемости клеточной мембраны, нарастающему повреждению
клеточной оболочки и последующей гибели клетки. Тобрамицин обладает
бактерицидным действием в концентрациях, равных или несколько превышающих
подавляющие концентрации.
Тобрамицин
проявляет активность, главным образом, в отношении грамотрицательных аэробных
микроорганизмов, обладая низкой активностью в отношении анаэробных
микроорганизмов и большинства грамположительных бактерий.
Тобрамицин более
активен, чем гентамицин, в отношении Pseudomonas aeruginosa и некоторых
штаммов протея; около 50% штаммов Pseudomonas aeruginosa, устойчивой
к гентамицину, являются чувствительными к тобрамицину.
При
ингаляционном введении минимальная подавляющая концентрация (МПК) тобрамицина в
мокроте больных муковисцидозом существенно выше, чем при парентеральном
введении.
Брамитоб: Показания
·
Лечение
инфекций дыхательных путей, вызванных Pseudomonas aeruginosa у больных
с муковисцидозом.
Способ применения и дозы
Ингаляционно, с
использованием небулайзера.
Взрослые и дети
старше 6 лет:
—
по
одной ампуле (300 мг) два раза в сутки (утром и вечером) в течение 28 дней.
Интервал между ингаляциями должен составлять около 12 часов, но не менее 6
часов.
После применения
БРАМИТОБА в течение 28 дней, необходимо сделать перерыв на 28 дней, после
чего, продолжить терапию в течение последующих 28 дней.
Режим
дозирования не учитывает массу тела. Всем пациентам следует назначать по одной
ампуле БРАМИТОБА (300 мг тобрамицина) два раза в сутки.
Указания к правильному
использованию.
1) Согнуть
отделяемую ампулу от полоски в обоих направлениях.
2) Отделить ампулу
от полоски, вначале верхнюю часть, затем среднюю.
3) Открыть ампулу,
повернув ее верхнюю часть относительно корпуса в направлении, указанном
стрелкой.
4) Умеренно нажимая
на стенки, вылить лекарственный препарат в стеклянное горлышко небулайзера.

Содержимое одной
ампулы (300 мг), перелитое в небулайзер, вводится путем ингаляции за 10–15
минут с помощью многоразового небулайзера PARI LC PLUS с компрессорами, которые
при подсоединении к небулайзеру PARI LC PLUS, обеспечивают поставку 4–6 л/мин
и/или обратное давление, равное 110–217 кПа.
Ингаляции
БРАМИТОБА проводятся в положении больного сидя или стоя, при обычном дыхании
через загубник небулайзера. Носовой зажим может помочь пациенту дышать ртом.
Указания по
очистке и дезинфекции небулайзера.
После окончания
процедуры ингаляции небулайзер следует разобрать, отдельные его части
(за исключением трубки) тщательно промыть горячей водой и жидким моющим
средством, прополоскать и насухо вытереть чистой сухой тряпочкой, не
оставляющей волокон. Для регулярной дезинфекции небулайзера рекомендуется
опустить его отдельные части (кроме трубки), очищенные в соответствии с данными
выше указаниями, в раствор, состоящий из одной части 9% уксусной кислоты и трех
частей горячей воды, на один час, затем промыть горячей водой и насухо вытереть
чистой тряпочкой.
После завершения
дезинфекции использованный раствор следует сразу же вылить.
В качестве
альтернативы дезинфекцию можно проводить путем кипячения в течение 10 минут.
Применение при беременности и кормлении грудью
Применение
препарата в период беременности возможно, только если ожидаемая польза для
матери превышает возможный риск для плода.
При
необходимости применения препарата в период лактации, необходимо прекратить
грудное вскармливание.
Брамитоб: Противопоказания
·
Повышенная
чувствительность к препарату;
·
Детский
возраст до 6 лет.
С осторожностью
Ишемическая
болезнь сердца, хроническая сердечная недостаточность в стадии декомпенсации,
сахарный диабет, беременность. Почечная недостаточность, нарушение слуха,
дисфункция вестибулярного аппарата или нейромышечная патология, такая как
паркинсонизм или другие состояния, характеризующиеся мышечной слабостью, в том
числе myasthenia gravis, острое кровохарканье.
Брамитоб: Побочные действия
|
Очень редко |
Редко |
Не часто |
|
<1/10000 |
1/10000–1/1000 |
1/1000–1/100 |
Со стороны
костно-мышечной системы:
—
Очень
редко: боли в спине.
Со стороны крови
и лимфатической системы:
—
Очень
редко: лимфоаденопатия.
Со стороны
органов чувств:
—
Редко:
звон в ушах, потеря слуха;
—
Очень
редко: вестибулярные и лабиринтные нарушения, боли в ухе.
Со стороны
центральной и периферической нервной системы:
—
Редко:
головная боль, головокружение;
—
Очень
редко: сонливость.
Со стороны
желудочно-кишечного тракта:
—
Редко:
тошнота, язвенный стоматит, рвота, изменение вкуса;
—
Очень
редко: диарея.
Со стороны
органов дыхания:
—
Нечасто:
изменение голоса, одышка, усиление кашля, фарингит;
—
Редко:
бронхоспазм, усиление образования мокроты, кровохарканье, ухудшение функций
легких, ларингит, носовое кровотечение, ринит;
—
Очень
редко: гипервентиляция, гипоксия, синусит.
Местные реакции:
—
Очень
редко: грибковые инфекции, кандидоз полости рта.
Другие:
—
Редко:
кожная сыпь, анорексия, боли в грудной клетке, астения, лихорадка.
—
Очень
редко: боль и дискомфорт в животе.
Передозировка
Симптомом
передозировки может быть выраженная осиплость голоса.
При случайном
попадании БРАМИТОБА внутрь токсическое действие маловероятно, поскольку тобрамицин
плохо всасывается из желудочно-кишечного тракта.
При случайном
внутривенном введении БРАМИТОБА могут развиться симптомы и признаки
передозировки тобрамицина, такие как головокружение, потеря слуха, звон в ушах,
вертиго, респираторный дистресс-синдром, блокада нейромышечной проводимости и
нарушение функции почек.
В случае
проявления признаков передозировки БРАМИТОБ следует немедленно отменить и
провести исследование показателей функции почек. Для контроля передозировки
может быть полезным определение концентраций тобрамицина в сыворотке крови.
Взаимодействие
Не выявлено
значимого лекарственного взаимодействия БРАМИТОБА при совместном применении с
муколитиками, β2-адреномиметиками, ингаляционными кортикостероидами
и другими пероральными и парентеральными антибиотиками с антипсевдомонадной
активностью.
Следует избегать
одновременного или последовательного применения ингаляционного тобрамицина и
других потенциально нефро- или ототоксичных лекарственных препаратов. Некоторые
диуретики могут усиливать токсичность аминогликозидов, изменяя концентрации
антибиотика в сыворотке и тканях. Ингаляционный тобрамицин не следует назначать
одновременно с этакриновой кислотой, фуросемидом, мочевиной или маннитолом.
Токсичность
аминогликозидов может увеличиваться при парентеральном введении следующих
препаратов: амфотерицина В, цефалотина, циклоспорина, такролимуса, полимиксинов
(риск усиления нефротоксичности), препаратов платины (риск усиления
нефротоксичности и ототоксичности) а так же ингибиторов холинэстеразы и
ботулотоксина (нейромышечные эффекты).
Особые указания
Лечение
БРАМИТОБОМ должен назначать врач, имеющий опыт ведения больных муковисцидозом.
Длительность курсового лечения определяется врачом, исходя из клинической
картины заболевания. В случае подтвержденного ухудшения легочных функций
следует назначить дополнительную антибактериальную терапию.
При
ингаляционном применении БРАМИТОБА может развиться бронхоспазм. Первую дозу
БРАМИТОБА следует вводить под наблюдением врача, назначив перед ингаляцией
бронходилататор, если он уже входит в используемую схему лечения больного. До и
после процедуры следует измерить ОФВ1 (объем форсированного выдоха). При
появлении признаков ятрогенного бронхоспазма у больного, не получающего
бронходилататоров, применение препарата нужно повторить отдельно,
с использованием бронходилататора. Появление бронхоспазма на фоне
применения бронходилататора может указывать на аллергическую реакцию. При
подозрении на аллергическую реакцию применение БРАМИТОБА следует прекратить. Для
купирования бронхоспазма следует проводить соответствующую патогенетическую
терапию.
Во время лечения
БРАМИТОБОМ пациенту следует продолжать стандартную физиотерапию грудной клетки.
Применение бронходилататоров должно продолжаться по клиническим показаниям. При
использовании нескольких методов лечения дыхательных нарушений рекомендуется
следующий порядок: бронходилататор, дыхательная физиотерапия, другие
ингаляционные лекарственные средства и в конце — БРАМИТОБ.
БРАМИТОБ не
следует смешивать с другими ингаляционными лекарственными средствами.
БРАМИТОБ следует
применять с большой осторожностью у больных с паркинсонизмом или другими
состояниями, характеризующимися мышечной слабостью, включая myasthenia gravis,
поскольку аминогликозиды могут усиливать мышечную слабость из-за возможного
курареподобного действия на нейромышечную проводимость.
Препарат следует
применять с осторожностью у больных с доказанной или подозреваемой почечной
недостаточностью, при условии мониторинга концентраций тобрамицина в сыворотке
крови.
Необходимо
периодически оценивать показатели функции почек (уровень мочевины и креатинина
не менее одного раза в течение 6 курсов терапии БРАМИТОБОМ. При появлении
признаков нефротоксичности, лечение тобрамицином следует прервать до снижения
минимальных концентраций препарата в сыворотке менее 2 мкг/мл. Затем лечение
БРАМИТОБОМ можно возобновить по медицинским показаниям. Пациентов, одновременно
получающих парентеральную терапию другими аминогликозидами, следует тщательно
наблюдать из-за возможности развития кумулятивной токсичности.
При
использовании аминогликозидов возможно развитие ототоксичности (гипоакузия,
системное и несистемное головокружение, атаксия).
Врач должен
учесть возможность того, что аминогликозиды могут обладать вестибулярной и кохлеарной
токсичностью и в ходе терапии БРАМИТОБОМ должен оценивать функцию слуха.
Больным, принимавшим ранее аминогликозиды в течение длительного времени,
рекомендуется прохождение аудиометрических тестов до начала терапии БРАМИТОБОМ.
При лечении головокружения следует принимать во внимание, что оно является
проявлением ототоксичности. При возникновении головокружения или снижения слуха
в ходе терапии БРАМИТОБОМ, необходимо проведение аудиологического
обследования.
При ингаляции
возможно появление кашлевого рефлекса. Применение ингаляционного тобрамицина у
больных с острым кровохарканьем должно проводиться только в том случае, если
польза от лечения превышает риск провокации дальнейшего кровотечения.
У некоторых
больных, получавших тобрамицин, отмечается повышение МПК аминогликозидов в
отношении изученных выделенных штаммов P. aeruginosa. Возможно развитие
резистентности штаммов P. aeruginosa, к внутривенно вводимому
тобрамицину.
Форма выпуска
Раствор для
ингаляций 300 мг/4 мл.
По 4 мл в
герметично запаянную пластиковую ампулу. Полоска по 4 ампулы помещается в алюминиевый
стрип. По 4, 7 или 14 стрипов с инструкцией по применению помещают в картонную
пачку.
Условия отпуска
Производитель
|
Chiesi |
Кьези |
|
Via Palermo |
26/А, ВИА |
|
Parma, Italy. |
ПАРМА, Италия |
|
Произведено: |
|
|
Holopack |
Голопак |
|
Bahnhofstraße |
Банхофштрассе |
|
Sulzbach-Laufen, |
Зульцбах-Лауфен, |
Претензии
потребителей направлять по адресу:
ООО «Кьези
Фармасьютикалс»
101509, г.
Москва, ул. Лесная, д. 43, офис 701
Тел.
представительства в России:
+7 495
9671212, факс + 7 495 9671211
Основные сведения
Торговое название
Брамитоб
Действующее вещество (МНН)
Тобрамицин
Дозировка или размер
75 мг/мл
Форма выпуска
раствор для ингаляций
Первичная упаковка
ампула пластиковая
Производитель
Chiesi Farmaceutical
Условия хранения
В защищенном от света месте, при температуре 2–8 °C (не замораживать)
Представлено описание активных веществ лекарственного препарата. Описание препарата основано на официально утвержденной инструкции по применению от компании-производителя. Приведенное описание носит исключительно информационный характер и не может быть использовано для принятия решения о возможности применения конкретного лекарственного препарата.