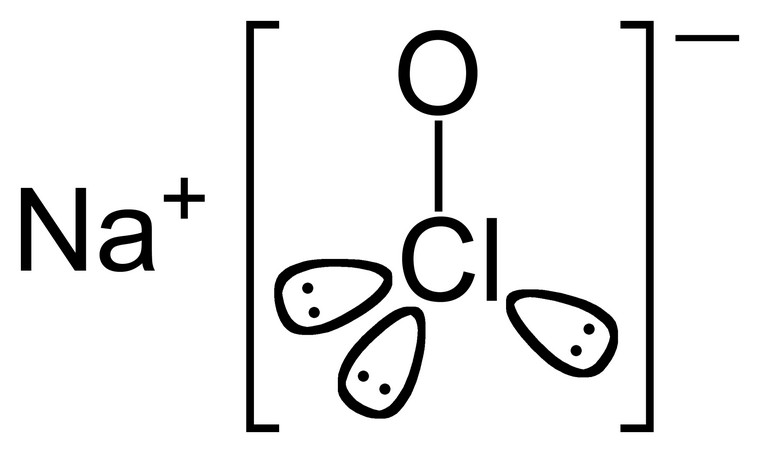Гипохлорит натрия — NaClO, получают хлорированием водного раствора едкого натра (NaOH) молекулярным хлором (Cl2) или же электролизом раствора поваренной соли (NaCl). Подробно о методах получения гипохлорита натрия (ГПХН) можно прочитать в статье. В РФ состав и свойства ГПХН, выпускаемого промышленностью должен соответствовать требованиям, предъявляемым в ГОСТе или ТУ.
Водные растворы Гипохлорита натрия весьма неустойчивы и со временем разлагаются даже при обычной температуре (со скоростью 0,08 до 0,1 % в сутки). На скорость распада ГПХН влияет воздействие солнечного света, наличие катионов тяжелых металлов и хлоридов щелочных металлов. При этом наличие в водном растворе сульфата магния или кальция, борной кислоты, силикатов и пр. замедляют процесс разложения ГПХН. Следует заметить, что наиболее устойчивы растворы с сильнощелочной средой (значение pH > 10).
Кислоты с содержанием хлора представлены разными типами. В общей сложности основных пять:
- бескислородная соляная;
- хлорноватистая;
- хлористая;
- хлорноватая;
- хлорная.
Каждая из них является сильным окислителем с широким спектром действия, повсеместно применятся в промышленности, процессах химического синтеза. Хлорноватистая – самая слабая и в то же время важная кислота. Ее составляющая натрий гипохлорит – активно применяемый в быту элемент.
Содержание
- 1 Обеззараживание питьевой воды гипохлоритом натрия. Хлорноватистая кислота и ее соли
- 2 Количественная оценка эффективности химических бактерицидов и их квалификация. Спектральная активность дезинфицирующих средств
- 3 История открытия и использования вещества
- 4 Дезинфекционные свойства хлора и гипохлорита натрия. Гипохлорит натрия для обработки питьевой воды
- 5 Аналоги гипохлорита натрия
- 6 Натрий гипохлорит: формула, применение. Обеззараживание воды гипохлоритом натрия
- 7 Дезинфекция питьевой воды
- 8 Расчет расхода гипохлорита натрия для очистки питьевой воды. Выбор концентрации рабочего раствора
- 9 Очистка воды гипохлоритом натрия безопаснее хлора – эксперты
Обеззараживание питьевой воды гипохлоритом натрия. Хлорноватистая кислота и ее соли
Хлорноватистая кислота – самая слабая из перечня в плане действия, зато она легко высвобождается из солей, демонстрирует отличные дезинфицирующие, окислительные, антибактериальные качества. Состав нестабильный, поэтому обычно используется не сама кислота, а ее соли. Основные:
- гипохлорит калия;
- натрий гипохлорит;
- гипохлорит кальция.
В обычных условиях среды эти соли представляют собой твердые кристаллы, разлагающиеся при значительном нагреве и выделяющие свободный хлор. При условии правильной транспортировки, хранения соли незаменимы в медицине, промышленности, хозяйстве.
Количественная оценка эффективности химических бактерицидов и их квалификация. Спектральная активность дезинфицирующих средств
Если разбираться в составе молекул солей, то количественное соотношение элементов будет выглядеть так:
<оl>
- 48% хлора;
- 31% натрия;
- 21% кислорода.
Заряженный положительно ион натрия связывается за счет ионных взаимодействий с хлорит-ионом. Внутри хлорит-иона связи образуются по ковалентному полярному механизму – неспаренный один ион хлора и шесть электронов соединяются с атомом кислорода. Ион имеет общий заряд CLO-. Химическая формула гипохлорита натрия указывает на строение его молекулы, степени диссоциации внутри водного раствора.
История открытия и использования вещества
Микроэлемент стал известен в 18 веке, когда известный химик К. Шееле открыл элемент хлор. Позже Бертолле обнаружил, что при растворении газа в воде образуется кислотная смесь, которая оказывает отбеливающее и дезинфицирующее действие. Смесь была названа белильной жидкостью, централизовано основали ее массовое производство. Со временем стало ясно, что в данной форме хранить и транспортировать вещество неудобно, так как оно начинает быстро разлагаться под влиянием света, температуры, просто на открытом воздухе. Способ получения компонента был доработан и усовершенствован – едкий хлор стали пропускать через поташ. В результате получался стабильный KCLO. Соединение было названо жавелевой водой, стало активно использоваться в бытовых целях.
Единственный недостаток поташа – высокая цена. В начале 19 века А. Лабаррак заменил поташ на дешевую каустическую соду. Натрий гипохлорит NaCLO до сих пор активно применяется в разных хозяйственных отраслях.
Дезинфекционные свойства хлора и гипохлорита натрия. Гипохлорит натрия для обработки питьевой воды
Физические параметры соединение имеет те же, что другие соли хлорноватистой кислоты. Визуально оно представлено кубическими кристаллами без цвета и запаха, аромат хлора едкий, но слабый. В воде соль растворяется хорошо в любых количествах, реакция среды получается щелочной. Плавятся кристаллы при 18-240С, замерзают в широком диапазоне температур – от -10С до -300С с учетом концентрации раствора. При нагревании на 300 С и более вещество разлагается с освобождением свободного хлора, при еще более высоких температурах разложение может сопровождаться взрывами.
Плотность гипохлорита натрия составляет 1250-1265 кг/м³. Кристаллы на открытом воздухе самопроизвольно плавятся и становятся жидкими. Цвет водного раствора бледно-зеленый, слабый характерный запах присутствует. Соединение начинает быстро разлагаться при внешних воздействиях, попадании в емкость посторонних предметов. Вероятно выделение токсичного хлора, опасного для органов зрения и кожи. Окисляющая реакция сильная.
Натрий гипохлорит из водного раствора выделяется выпариванием с образованием игольчатых кристаллов. С учетом условий среды при разложении могут образовываться различные вещества и продукты. В обычных условиях это соль с кислородом, при нагревании – соль поваренная и хлорат натрия. При действии кислот реакция сопровождается выделением свободного хлора. Окислительные свойства выражены со всеми восстановителями. Соли преобразуют сульфита с нитритами в сульфаты и нитраты, растворяют мышьяк и фосфор с образованием кислот, переводят аммиак в гидразин. Коррозионные свойства выраженные, поэтому вещество для обработки металлических изделий не используется. Главное действие – окисляющее.
Аналоги гипохлорита натрия
Среди аналогов гипохлорита натрия выделяют:
<оl>
- Гипохлорит кальция – в гранулах, таблетках или порошке. Препараты отличает значительное включение активного хлора, высокая растворимость в воде, низкая гигроскопичность, стабильность.
- Хлорную известь – популярное ранее средство дезинфекции. На данный момент известь применяется, но намного реже в силу популяризации электролитических методов по получению хлора с гипохлоритом.
- Диоксид хлора – нормально растворяется в воде, не вступая с ней в различные реакции. Дезинфицирующее действие более выраженное, чем у хлора, компонент высоко ценят за его бактерицидные, спорицидные, вирицидные свойства. Уничтожает лишние привкусы, запахи. Остаточное содержание в воде значительное, специальные хранилища не нужны.
- Перманганат калия – главное средство дезинфекции трубопроводов, применение специального сложного оборудования не требует.
- Йод – с аммиаком, прочими аналогичными веществами не взаимодействует. В продаже йод найти непросто, стоимость он имеет высокую, что усложняет его использование.
- Хлорид брома – по дезинфицирующим свойствам во многом схож с хлором, может образовывать бромированные соединения.
- Серебро – уничтожает большинство вредных микроорганизмов, не токсично для человека. Минус средства – дороговизна.
Перечисленные средства не всегда дают требуемые результаты, поскольку ряд организмов к воздействию данных веществ просто не чувствителен. По этой причине широко применяются органические дезинфектанты. К ним относят:
- альдегиды, кислоты, спирты;
- фенольные соединения;
- хлоризоцианураты;
- кислоты хлорциануровые.
Фенолы применяются преимущественно в медицинско й отрасли в роли дезинфектантов. Среди популярных фенольных соединений – алкилфенолы, галоидфенолы, бифенолы, пр.
Натрий гипохлорит: формула, применение. Обеззараживание воды гипохлоритом натрия
Жавелевую воду получают в промышленных и лабораторных условиях, способы для этого могут использоваться разные.
Первый – хлор пропускается через гидроксид натрия раствор с получением конечного продукта. Это химический способ.
Второй вариант – электрохимический. Он предполагает подвергание электролизу раствора NaCL либо морской воды. Оба решения находят свое повсеместное применение на производствах. Лабораторный синтез предполагает получение малых порций продукта. Он предполагает пропускание хлора через раствор каустика/карбоната натрия.
Дезинфекция питьевой воды
Обеззараживание жидким хлором имеет более широкое применение, чем ГПХН. Жидкий хлор вводится в обрабатываемую воду или используется в хлораторе. Удобнее всего применять в целях дезинфекции хлоратор непрерывного действия. Вакуумные устройства идут с газовыми или жидкостными измерителями расхода хлора.
При прямом хлорировании нужно создавать условия для быстрого распределения хлора в обрабатываемых жидкостях. Хлор вводится с применением диффузора, могут использоваться также смесители – их крепят непосредственно перед контактными резервуарами. Самая простая модель смесителя – ершовая. Она имеет вид лотка с пятью вертикально расположенными перегородками. Эти перегородки сужают сечение, приводят к образованию вихревых потоков, смешиванию хлорной воды с обрабатываемой. Дно лотка обязательно должно иметь уклон.
Расчет расхода гипохлорита натрия для очистки питьевой воды. Выбор концентрации рабочего раствора
За расчетную принимается доза хлора, обеспечивающая указанное количество остаточного элемента. Для осветленной речной воды она составляет 1.5-3 мг/л, для подземной 1 -1,5 мг/л. Увеличение дозы хлора возможно при наличии в воде закисного железа.
Когда будет введен хлорагент, нужно обеспечить его тщательное смешивание с водой. Контакт происходит с водой до момента ее подачи потребителю. Он осуществляется в резервуаре либо трубопроводе, если длины последнего хватает для решения текущих задач. Если один резервуар останавливается для ремонта или промывки, доза хлора повышается в 2 раза.
В ряде случаев целесообразным является проведение предварительного хлорирования. Оно способствует активизации процессов коагуляции, окисляет органические соединения, снижает объемное содержание коагулянта, поддерживает очистные сооружения в отличном санитарном состоянии. Для проведения предварительного хлорирования может потребоваться повышение доз хлора. За счет введения хлора до и после сооружений очистки снижается общий расход вещества в сравнении с его расходом в ходе предварительного хлорирования. Методика называется двойной.
Очистка воды гипохлоритом натрия безопаснее хлора – эксперты
Степень опасности такого токсичного вещества хлора минимизируется за счет принятия ряда мер по организации хранения и использования элемента, в том числе благодаря организации санитарно-защитных зон и складов реагента с радиусом до 1000 м. Поначалу это помогало, но потом начался активный рост городов, жилая застройка стала приближаться к границам территорий, а иногда размещалась на них. Возросла опасности транспортировок реагентов – именно во время перевозок происходит более половины всех химических аварий. В то же время токсичность хлора, которая усиливается высокими концентрациями реагента, негативно влияет на промышленную безопасность, антитеррористическую стойкость систем водообеспечения.
За последние годы нормативная законодательная база в сфере промышленной безопасности при обращении с хлористыми соединениями ужесточается. У эксплуатирующих организаций возникает потребность перехода к безопасному способу обеззараживания водных сред, который был бы не поднадзорен Федеральной службе экологического, технологического и атомного надзора, но обеспечивал выполнение требований СанПиНа. Главной альтернативой хлора является гипохлорит натрия (ГПХН).
Оценка: 
Загрузка…
Применение гипохлорита натрия в водоочистке
Дезинфекция питьевой воды
Технический гипохлорит натрия является наиболее предпочтительным реагентом на стадии предварительного окисления и для стерилизации воды в конце обработки перед подачей ее в распределительную сеть. Он используется также для дезинфекции насосных станций и водонапорных башен, канализации, вспомагательных устройств.
К гипохлориту натрия, применяемому вместо жидкого хлора для дезинфекции питьевой воды, предъявляются определенные требования, касающиеся концентрации щелочи и тяжелых металлов, например железа, стабильности, цветности.
Обычно в систему водоочистки гипохлорит натрия вводят после предварительного разбавления. После разбавления в 100 раз гипохлорита натрия, содержащего 12,5% активного хлора и имеющего рН 12-13, происходит понижение рН до 10-11 и концентрации активного хлора до 0,125 (в действительности величина рН имеет более низкое значение).
При использовании вместо газообразного хлора гипохлорита натрия в процессе ввода этого реактива в систему трубопроводов для его разбавления там образуется осадок, состоящий из гидроксида магния и диоксида кремния, забивающий водные каналы.Поэтому концентрация щелочи в гипохлорите натрия должна быть такой, чтобы не вызывать образования осадка. Для обработки питьевой воды применяется гипохлорит натрия характеризующийся следующими показателями:
| Содержание активного хлора, % | 5 |
|---|---|
| Содержание свободной щелочи, % | 2 |
| Нерастворимая часть, % | 0,01 |
| Mg, млн -1 | 1 |
| Mg, млн -1 | 1 |
| Mg, млн -1 | 1 |
Проведенные в Японии исследования показали, что при использовании гипохлорита натрия для дезинфекции воды необходимо учитывать концентрацию щелочи в гипохлорите и поддерживать ее ниже определенного уровня. Концентрация остаточной щелочи в момент окончания реакции хлорирования влияет на концентрацию растворенных в готовом продукте ионов тяжелых металлов, поэтому следует по мере возможности снижать остаточную концентрацию щелочи.
В отличие от хлора гипохлориты имеют щелочной характер и могут применяться для повышения уровня рН обрабатываемой воды. С изменением рН обрабатываемой воды меняются соотношения между хлорноватистой кислотой и ионами гипохлорита. С возрастанием рН хлорноватистая кислота распадается на ионы Н и ClO. Так, например, при рН 6 доля HСlO составляет 97%, а доля гипохлоритных ионов 3%. При рН7 доля HСlO составляет 78%, а гипохлорита — 22%, при рН 8 доля HСlO — 24%, гипохлорита — 76%. Таким образом, при высоких значениях рН в воде HСlO превращается в неактивный гипохлорит ион. Помимо значения рН на дезинфицирующие свойства оказывают влияние температура и содержание свободного активного хлора.
Данные по избытку активного хлора, необходимому для полной стерилизации питьевой воды, при различных температурах, времени воздействия и величине рН
| Температура воды, С0 | Время воздействия, мин | Требуемый избыток хлора, мг/л | ||
|---|---|---|---|---|
| pН 6 | pН 7 | pН 8 | ||
| 10 | 5 | 0,5 | 0,7 | 1,2 |
| 10 | 0,3 | 0,4 | 0,7 | |
| 30 | 0,1 | 0,12 | 0,20 | |
| 45 | 0,07 | 0,07 | 0,14 | |
| 60 | 0,05 | 0,05 | 0,01 | |
| 20 | 5 | 0,3 | 0,4 | 0,7 |
| 10 | 0,2 | 0,20 | 0,4 | |
| 15 | 0,1 | 0,15 | 0,25 | |
| 30 | 5 | 0,06 | 0,12 | |
| 45 | 0,04 | 0,04 | 0,08 | |
| 60 | 0,03 | 0,03 | 0,06 |
Наиболее допустимое содержание гипохлорита натрия в воде, по данным ФРГ, составляет 0,3 мг/л активного хлора. Допускается повышение содежания активного хлора в питьевой воде до 0,06 мг/л, если это временно совершенно необходимо для обеззараживания воды (такие же концентрации поддерживаются при обработки воды хлором, гипохлоритом кальция, хлорной известью). После обработки воды в ней должно содержаться не менее 0,1 мг/л свободного хлора.
Для осуществления дезинфекции питьевой воды все шире применяются электрические установки для получения гипохлорита натрия.
Дезинфекция воды плавательных бассейнов и прудов
Обычно для этой цели используются разбавленные растворы гипохлорита натрия. Их умеренная цена, эффективность по отношению к водорослям и бактериям, а также безвредность для человека делают этот продукт наиболее пригодным для обработки воды в бассейнах. Технический гипохлорит натрия позволяет получить чистую прозрачную воду, лишенную водорослей и бактерий. Он обеспечивает полноту дезинфекции воды и осуществляет ее защиту от бактериальных загрязнений.
Как и при дезинфекции питьевой воды, при использовании гипохлорита для дезинфекции воды плавательных бассейнов большое значение придается контролю за содержанием активного хлора. Важное значение имеет также поддержание рН на определенном уровне, обычно 7,4-8,0, а еще лучше 7,0-7,4. Регулирование рН осуществляется с помощью растворов соляной или серной кислоты.
Проведенные в России исследования по дезинфекции воды плавательных бассейнов показали, что эффективное обеззараживание при поддержании остаточного хлора на уровне 0,3-0,5 мг/л. Надежное обеззараживание в течение 30 мин обеспечивают растворы, содержащие 0,1-0,2% гипохлорита натрия. Содержание хлора в зоне дыхания не должно превышать 0,1 мг/м 3 в публичных плавательных бассейнах и 0,03 мг/м 3 в спортивных бассейнах. Замена газообразного хлора гипохлоритом натрия приводит к снижению выделения хлора в воздух и, кроме того, позволяет легче поддерживать остаточное количество активного хлора воде. Несмотря на появление новых более перспективных дезинфицирующих средств, гипохлорит натрия продолжает использоваться для дезинфекции воды плавательных бассейнов.
Обработка бытовых и промышленных сточных вод
Гипохлорит натрия применяется для обработки бытовых и промышленных вод, для разрушения животных и растительных микроорганизмов, устранения запахов (особенно образующихся из серосодержащих веществ), обезвреживания промышленных стоков, например, от цианистых соединений.
Он может быть использован для обработки воды, содержащей аммоний. Процесс осуществляют при температуре выше 70 0 С в щелочной среде с добавлением CaCl2 или СаСО3 для разложения соединений аммиака.
Для очистки от фенолов (содержание 0,42-14,94 мг/л) используют 9% раствор гипохлорита натрия в количестве 0,2-8,6 мг/л. Степень очистки достигает 99,99%. При обработке гипохлоритом воды, содержащей фенолы, происходит образование фенолоксифенолов.
В ходе обработки вод, содержащих гуминовые вещества, последние превращаются в хлороформы, дихлоруксусную кислоту, трихлоруксусную кислоту, хлоральдегиды и некоторые другие вещества, концентрация которых в воде значительно ниже. Известны данные об использовании гипохлорита натрия для удаления ртути из сточных вод.
Использование гипохлорита натрия в пищевой промышленности
В начале восьмидесятых годов институт биологии и ее применения к проблемам питания в Дижоне (Франция) провел изучение дезинфицирующих средств, используемых в пищевой промышленности. Гипохлорит натрия был оценен среди этих продуктов по первому классу как наиболее пригодный для этих целей и наиболее экономичный. Он показал высокую эффективность в отношении почти всех растительных клеток, спор и бактерий. По этой причине гипохлорит натрия находит широкое применение в пищевой промышленности для дезинфекции с целью уничтожения ракообразных и моллюсков; для различных промывок; для борьбы против бактериофагов в сыроваренной промышленности; для дезинфекции резервуаров, загонов для скота.
Гипохлорит натрия относится к числу средств используемых в пивоваренной промышленности. Обычно применяют раствор, содержащий 30-40 мг/л активного хлора. Гипохлорит натрия является отличным антимикробным агентом. В частности в США его применяют для обработки зерна.
Использование гипохлорита натрия в молочной промышленности
На предприятиях молочной промышленности основное назначение дезинфицирующих мероприятий — предупреждение микробного инфицирования молочных продуктов.
Гипохлорит натрия является достаточно эффективным средством, используемым для этой цели. В России применяют для этих целей гипохлорит натрия марки А. Он содержит 170 г/л активного хлора и 40- 60 г/л щелочи. Бактерицидное действие гипохлорита натрия проявляется при 20-25 0 С и экспозиции 3-5 минут.Для снижения корозирующего действия гипохлорита был предложен препарат ГИПОХЛОР. Его получают смешением гипохлорита натрия, каустической соды и метасиликата натрия. Коррозирующее действие этого препарата на металлические поверхности в 10-15 раз меньше, чем обычного гипохлорита натрия. В молочной промышленности традиционные средства дезинфекции начинают вытесняться новыми препаратами, обладающими одновременно и моющими и дезинфицирующими свойствами.
Наиболее перспективными из них являются натриевая и калиевая соли трихлоризоциануровой кислоты.
Использование гипохлорита в рыбоводстве
Гипохлорит натрия в виде разбавленных растворов уничтожает все виды патогенных агентов и используется для дезинфекции водоемов с твердым дном и берегами. Кроме того он используется при дезинфекции рыболовных сетей, сачков и баков из пластика для хранения рыбы.
Использование гипохлорита в здравоохранении
В комплексе профилактических мероприятий, направленных на ограничение больничных инфекции, важную роль играет дезинфекция. Для этой цели может быть использован гипохлорит натрия. В частности, в ПНР для этих целей используют гипохлорит натрия производства Тарновского азотного предприятия, с содержанием активного хлора не менее 55. Гипохлорит натрия оказывает дезинфицирующее действие на грамм-положительные и грамм-отрицательные бактерии, туберкулезные палочки, споры бактерий, болезнетворные грибки и вирусы. Имеются сведения (Россия) использования растворов гипохлорита натрия (0,03-0,05%) для лечения гнойных абцессов, гнойных гайморитов, розовых угрей и трофических язв как наружное средство и средство для инъекций.
Другие области применения
Гипохлорит входит в составы синтетических моющих средств, используемых в бытовой химии, в составы дезинфицирующей пасты с отбеливающим эффектом, дезинфицирующих средств с окислительными, хлорирующими и бактерицидными свойствами.
В настоящее время за рубежом и в России наметилась тенденция развития использования гипохлорита натрия для дезинфекции небольших объемов воды с применением электролитического метода его получения. Этот метод находит все большую популярность во всем мире.
Хотя гипохлорит натрия продолжает использоваться в пищевой, молочной промышленности, но он все более вытесняется другими видами средств, обладающими сочетанием моющих и дезинфицирующих свойств. Все чаще его вводят в составы таких средств.
← Вернуться к списку
Цена: 3 500,00 руб.
ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ РАСТВОРА ГИПОХЛОРИТА НАТРИЯ ДЛЯ ЦЕЛЕЙ ДЕЗИНФЕКЦИИ
Гипохлорит натрия — эффективный дезинфицирующий агент.
Что такое Натрий гипохлорит?
Натрий гипохлорит (формула NaOCl) является неорганическим соединением, натриевой солью хлорноватистой кислоты. Также его могут называть «лабарраковой/жавелевой водой» или просто «гипохлоритом натрия».
Свойства
Это соединение имеет вид неустойчивого бесцветного кристаллического вещества, которое легко разлагается даже при комнатной температуре. Во время данного процесса выделяется кислород, а если температуру условий повысить до 70оС, то реакция сопровождается взрывом. Растворенный в воде натрий гипохлорит — это очень сильный окислитель. Ели к нему добавить соляную кислоту, то образуются вода, хлорид натрия и газообразный хлор. А при реакции углекислого газа с охлажденным раствором обсуждаемого сейчас вещества получается разбавленная хлорноватистая кислота.
Применение
Благодаря своей высокой антибактериальной активности и спектру действия на разного рода микроорганизмы, натрий гипохлорит применяется в различных направлениях человеческой деятельности:
- При обеззараживании воды в бассейнах и питьевой воды; Для производства отбеливающих средств;
- При обеззараживании сточных вод;
- При дезинфекции медицинских помещений и мест общественного питания.
Гипохлорит натрия (NaClO) при растворении в воде образует хлорноватистую кислоту и является сильным окислителем, благодаря чему и обеспечивается полная дезинфекция воды. Также данное дезинфицирующее средство используют при обработке технологического оборудования для производства продуктов питания.
В нашей компании продажа натрия гипохлорита осуществляется в канистрах по 25 кг и соответствует следующим стандартам:
- жидкость имеет зеленовато-желтый цвет;
- коэффициент светопропускания составляет не менее 20%;
- массовая концентрация активного хлора составляет не менее 190 г/л (марка А), 170 г/л (марка Б);
- массовая концентрация щелочи в перерасчете на NaOH составляет в пределах 10-20 г/л (марка А), 40-60 г/л (марка Б);
- массовая концентрация железа составляет не более 0,02 г/л (марка А), 0,06 г/л (марка Б).
Сроки хранения натрия гипохлорита составляют один год с падением концентрации на 15% в нераспечатанной таре в прохладном и темном месте. Период полураспада гипохлорита под прямыми лучами солнца составляет всего 40 минут.
Характеристики
| Страна производитель | Россия |
| Цвет | зеленовато-желтый |
| Срок хранения | 1 год |
| Коэффициент светопропускания | не менее 20% |
| Массовая концентрация щелочи в перерасчете на NaOH | в пределах 10-20 г/л (марка А), 40-60 г/л (марка Б) |
| Массовая концентрация активного хлора | не менее 190 г/л (марка А), 170 г/л (марка Б) |
| Форма выпуска | Жидкость |
| Массовая концентрация железа | не более 0,02 г/л (марка А), 0,06 г/л (марка Б) |
| Фасовка | канистры, 25 кг |
ИНСТРУКЦИЯ ПО ПРИМЕНЕНИЮ РАСТВОРА ГИПОХЛОРИТА НАТРИЯ ДЛЯ ЦЕЛЕЙ ДЕЗИНФЕКЦИИ:
1. Общие положения:
Гипохлорит натрия является солью хлорноватистой кислоты. Раствор получают заводским способом — поглощением хлора раствором едкого натра. В некоторых отраслях промышленности растворы гипохлоритов являются отходами производств. В соответствии с техническими условиями растворы гипохлорита натрия выпускают трех марок А, Б и В, отличающихся друг от друга по содержанию активного хлора, остаточной щелочности и внешнему виду. Марки А и Б — прозрачные зеленовато-желтые жидкости (допускается взвесь) с содержанием активного хлора 17%. Марка В — жидкость от желтого до коричневого цвета, выпускается I и II сортов, содержащих 12 и 9,5% активного хлора соответственно.
На заводах-изготовителях растворы гипохлоритов заливают в стальные гуммированные цистерны или контейнеры, а также в полиэтиленовые канистры или бочки емкостью 20—60 л. Раствор гипохлорита натрия разлагается при хранении, в связи с чем его хранят в закрытом, сухом, прохладном, хорошо проветриваемом нежилом помещении.
В виду слабой стойкости раствора гипохлорита и возможных нарушений правил хранения и приготовления рабочих растворов необходимо проводить проверку препаратов и приготовленных рабочих растворов иодометрическим методом на содержание активного хлора. Гипохлорит обладает бактерицидным и спорицидным действием.
2. Применение растворов гипохлорита натрия и кальция:
Раствор гипохлорита натрия используют взамен хлорной извести и ДТСГК. при текущей, заключительной и профилактической дезинфекции для обеззараживания различных предметов и выделений в очагах инфекционных заболеваний, а также для обеззараживания специальных объектов. Обеззараживание проводят орошением, протиранием, мытьем, замачиванием объектов, не портящихся при таком способе обработки. Белье и прочие ткани, а также металлические предметы, если они не защищены от коррозии, и окрашенные вещи обеззараживанию растворами гипохлоритов не подлежат. При инфекциях, вызванных вегетативными формами микроорганизмов, раствор гипохлорита натрия применяют по следующим режимам:
• Обеззараживание помещений (пол, стены), простой деревянной мебели, надворных установок проводят орошением растворами в концентрации 1% по активному хлору из расчета 300—500 мл/м2 при экспозиции 1 час. По окончании дезинфекции помещения обязательно проветривают.
• Для обеззараживания малоценных мягких вещей, а также ветоши, уборочного материала применяют растворы, содержащие 1 % активного хлора, из расчета 4—5 л на 1 кг сухого веса вещей и выдерживают в течение 1 часа.
• Посуду обеззараживают при полном погружении в 0,25— 1% по активному хлору раствор, в зависимости от наличия остатков пищи, на 1 час из расчета 1,5 л раствора на 1 комплект. По окончании дезинфекции посуду тщательно промывают водой.
• Ванны, унитазы, раковины и другое санитарно-техническое оборудование двукратно обильно орошают растворами 1 % концентрации.
• Жидкие выделения, остатки пищи и другие отбросы заливают неразведенными растворами гипохлоритов в соотношении 1 : 1. Для обеззараживания ночной посуды после удаления обеззараженного содержимого используют 0,25% по активному хлору растворы гипохлоритов, после чего посуду промывают водой.
• Обеззараживание верхних слоев почвы, асфальта и других объектов вне помещения производят растворами гипохлоритов в концентрации 1% по активному хлору из расчета 1,5 мл/м2.
3. Меры личной профилактики
При выполнении дезинфекционных работ раствором гипохлорита натрия каждый работающий обязан строго соблюдать меры личной безопасности, для чего следует пользоваться индивидуальными средствами защиты (респиратор РУ-60 с патроном марки А; защитные очки, резиновые перчатки; защитные передники). При попадании раствора гипохлорита натрия на кожу и слизистую глаз необходимо быстро и обильно промыть струей чистой воды.
4. Приготовление рабочих растворов гипохлорита натрия
|
Содержание активного хлора в растворе натрия гипохлорита, % |
Количество в мл раствора гипохлорита, необходимое для приготовления 10 л рабочего раствора |
|
|
0,25% по активному хлору |
1% по активному хлору |
|
|
17 |
150 |
600 |
|
12 |
210 |
840 |
|
10 |
250 |
1000 |
|
9 |
280 |
1110 |
|
8 |
315 |
1250 |
|
5 |
500 |
2000 |
Отходы промышленности, содержащие гипохлориты с нестандартным количеством активного хлора, могут быть также использованы для целей дезинфекции в порядке, предусмотренном данной инструкцией.
Источник: Санитарно-эпидемиологическое управление Минздрава СССР
Химическое название
Натриевая соль хлорноватистой кислоты
Химические свойства
Гипохлорит Натрия — что это такое? Это неорганическое соединение, в составе которого находится до 95% активного хлора. Вещество имеет несколько нетривиальных, исторических названий: «лабарракова вода», «жавелевая вода». Химическая формула гипохлорита натрия: NaOCl. Молекулярная масса соединения = 74,4 грамма на моль. В связи с тем, что вещество достаточно неустойчиво в свободном состоянии, оно чаще всего применяется в форме пентагидрата или водного раствора. У раствора сильный, резкий запах хлора. Безводная форма вещества синтезируется в виде бесцветных кристаллов, которые хорошо растворяются в воде. Пентагидрат обладает желто-зеленым оттенком, кристаллы ромбической формы.
По своим химическим свойствам – это сильный окислитель. Гипохлорид легко разлагается до хлорида Na и кислорода, при нагревании подвергается диспропорционированию. В воде диссоциирует на ионы. Вещество подвергает коррозии большинство металлов.
Гипохлорит Натрия производится в огромных количествах. Около половины синтезированного вещества применяют в бытовой химии и медицине, остальное – в промышленности. Существует два метода производства средства: химический, хлорирование водного раствора натрия гидроксида (концентрированный и основной) и электролитический, используют электролизные установки для электролиза водного хлорида натрия.
Химическое соединение активно применяется в промышленности:
- в качестве отбеливателя ткани, древесины и других продуктов;
- при промышленной и санитарно-гигиенической обработке зерна, трубопроводов, резервуаров в виноделии и пивоварении и т. д.;
- в химическом производстве антраниловой кислоты, хлорпикрина, аскорбиновой кислоты, крахмала, а аналитической химии при фотометрии;
- для обеззараживания и очистки промышленных стоков и воды в системах коммунального водоснабжения;
- в пищевой промышленности и фармацевтике;
- в военном деле при дегазации отравляющих веществ.
Вещество используют в бытовой химии, его часто можно обнаружить в составе отбеливателей, средств для дезинфекции и очистки. В медицине используют наружно или местно в качестве противовирусного, бактерицидного и противогрибкового средства; в небольших концентрациях — для обработки операционных ран, в гинекологии и акушерстве, оториноларингологии, в стоматологии (эндодонтия).
Химическое соединение может оказывать вредное воздействие на организм человека, при вдыхании оказывать удушающий и раздражающий эффект. При попадании средства в глаза вещество вызывает химический ожог, может привести к потере зрения. Средство раздражает кожу, в больших концентрациях вызывает отмирание тканей, язвы и ожоги. После приема внутрь 3-6% раствора у человека развивается ацидоз, раздражение пищевода, более высокие концентрации могут вызвать перфорацию пищеварительного тракта. Несмотря на это, при соблюдении рекомендации по использованию препаратов, воды и бытовой химии, гипохлорит считается достаточно безопасным средством. Не обладает канцерогенными, мутагенными и тератогенными средствами. Токсическая доза при внутривенном введения для человека составляет 45 мг на кг веса; пероральная – 1 грамм на кг. Также считается, что вещество не создает экологических проблем, так как в окружающей среде быстро разлагается до воды, кислорода и поваренной соли. Класс опасности для концентрированных растворов (до 20%): 1 – по химической активности; 3 – опасность для здоровья человека. Не территории Российской Федерации гипохлорит Na выпускают по ГОСТу 11086-76.
Фармакологическое действие
Дезинфицирующее, детоксицирующее, антисептическое, противомикробное.
Фармакодинамика и фармакокинетика
Натрия Гипохлорит – одно из сильнейших антибактериальных средств. Гипохлорит-ион проявляет высокую активность по отношению к множеству известных микроорганизмов, причем действует в достаточно низких концентрациях. Наивысшая активность проявляется при нейтральном рН. Образующиеся при разложении вещества частицы окисляют биополимеры в структуре вредоносных агентов, разрушают молекулы практически всех орг. субстратов. Средство проявляет активность по отношению к грамотрицательным бактериям, кишечной палочке, серрации, синегнойной палочке, грамположительным бактериям, патогенным грибам, простейшим, вирусам. Однако лекарство не действует на возбудители криптоспоридиоза и лямблиоза. Средство не обладает тератогенными, канцерогенными и мутагенными свойствами.
Показания к применению
Применяют наружно и вводят внутрь полости в концентрации 0,06%:
- для профилактики при операциях на грудной клетке, плевральной и брюшной полости;
- при ранениях, распространенном перитоните, абсцессе, остеомиелите;
- при проведении перитонеального диализа на брюшной полости;
- пациентам с эмпинемой плевры (туберкулез, гной в плевральной полости);
- при обработке влагалища перед операцией и после операции, при кольпите, бартолините, трихомониазе, эндометриозе, хламидиозе, аднексите, лапароскопии, гистероскопии, чревосечении;
- в качестве профилактического средства и для лечения гнойно-септических осложнений после кесарева сечения;
- после операций на мочевых путях и почках, после простатэктомии;
- при гнойном отите, фарингите, насморке;
- для лечения микозов и дифтерии;
- при истинной экземе и экземе микробной этиологии;
- пациентам со стафилодермией, стрептодермией, простым герпесом и угревой сыпью.
Раствор применяют для инъекционного введения при эндо- и экзотоксикозах, отравлениях, сепсисе, ожогах, заболеваниях печени и почек.
В виде жидкости и гелей вещество используют для дезинфекции оборудования в пищевой промышленности, при обработке поверхностей.
Противопоказания
Натрия Гипохлорит противопоказан к применению:
- при аллергии;
- гиповолемическом синдроме, гипогликемии (внутривенное введение);
- внутривенно, во время беременности.
Побочные действия
Редко вещество вызывает:
- аллергические реакции;
- ощущение сухости и жжения в месте нанесения;
- при инъекционном введении – снижение артериального давления, сахара в крови;
- при быстром внутривенном введении – флебит, экстравазацию.
Гипохлорит Натрия, инструкция по применению (Способ и дозировка)
Вещество используют для обработки помещения и различных поверхностей в соответствии с рекомендациями.
Лекарство применяют внутривенно, наружно и вводят в полости в форме 0,06% раствора. Следует соблюдать инструкцию по применению.
Передозировка
Нельзя превышать рекомендуемую дозировку и пренебрегать правилами использования гипохлорита Na. Средство может раздражать дыхательные пути, кожу, вызывать эрозии и перфорации ЖКТ, раздражать глаза.
Взаимодействие
Вещество не рекомендуется сочетать с прочими антисептическими средствами и мылом. Перед применением других лекарственных средств рекомендуется тщательно промыть обрабатываемый участок.
Особые указания
Раствором гипохлорита нельзя обрабатывать хирургические инструменты и материалы.
Не допускать попадания средства в глаза и дыхательные пути.
При беременности и лактации
Вещество не используют для инъекционного введения у беременных женщин.
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня:
Средство является активным действующим компонентом препаратов Амукин, Унисепт. Его добавляют в состав дезинфицирующих растворов.
Отзывы
Сложно переоценить значение универсального дезинфицирующего средства Гипохлорит Натрия. У вещества достаточно широкая область применения, оно успешно используется в медицине, в особенности в хирургии. В интернете редко встречаются отрицательные отзывы на препараты на основе данного вещества. Резко отрицательных отзывов не обнаружено.
Цена Гипохлорита Натрия, где купить
Купить Гипохлорит Натрия в Москве для бытового использования можно по предварительному заказу.
Обеззараживание воды гипохлоритом натрия
Гипохлорит натрия применяется в сфере водоподготовки, дезинфекции воды, предназначенной для питья. Вещество отличается безопасностью в употреблении, транспортировке, складировании, не требуя дополнительных мер безопасности.
Применение его в процедурах обеззараживания практикуется в водных распределительных системах на небольших предприятиях, частных домовладениях.
- Что такое гипохлорит натрия;
- Сущность метода обеззараживания;
- Когда следует использовать методику;
- История открытия и применения;
- Определение концентрации;
- Преимущества методики;
- Сколько нужно гипохлорита натрия для обеззараживания;
- Сроки годности вещества;
- Другие сферы применения;
- Использование NaClO безопаснее хлора.
Что такое гипохлорит натрия?
NaClO получается посредством хлорирования водяного раствора едкого натра (NaOH) частичками молекулярного хлора (Cl2) либо электролизом раствора обычной поваренной соли (NaCl).
Смеси ГПХН отличаются неустойчивостью. Скорость процесса распада увеличивается под воздействием солнечных лучей, присутствия в жидкости тяжелых металлов, щелочей.
Наличие некоторых примесей (например, сульфата кальция или борной кислоты), напротив, тормозит разложение NaClO. Самыми стабильными считаются растворы, имеющие pH более 10.
Хлор присутствует в пяти различных кислотах:
- бескислородной соляной;
- хлористой;
- хлорноватистой;
- хлорноватой;
- хлорной.
Каждая обладает собственными особенностями и свойствами, выступает сильным окислителем, имеющим широчайший спектр применения. Они используются в процедурах синтеза, на промышленных предприятиях.
Хлорноватистую кислоту по своему действию принято считать наиболее слабой. Но ее преимуществом выступают великолепные дезинфицирующие свойства. Соединение отличается неустойчивостью, поэтому для обеззараживания воды и других целей применяется не кислота, а ее соли. В том числе натрий гипохлорит – элемент, активно используемый в быту.
Сущность метода обеззараживания NaClO
Чтобы запустить процессы окисления содержащихся в жидкости железа, сероводорода, марганца, различных органических соединений, а также выполнить дезинфекцию, используется методика дозирования пропорционально.
Для этого необходим специальный насос дозации и действенный гипохлорит натрия для обеспечения эффективного обеззараживания. Устройство срабатывает по расходу жидкости, данные о котором поступают от импульсного водосчетчика.
Когда следует использовать методику?
Обеззараживание воды гипохлоритом применяется в ситуациях, когда применение напорной аэрации не рекомендовано. К таким случаям относятся большие концентрации в жидкости:
- сероводорода (более 0,01 мг/литр);
- марганца (более 0,7 мг/литр);
- железа (более 8-10 мг/литр);
- органики (показатель перманганатной окисляемости более 4,5).
В подобных обстоятельствах гипохлорит, применяемый для очистки воды, является наиболее приемлемым и действенным вариантом.
История открытия и применения
Микроэлемент (NaClO) известен с XVIII столетия, начав свою историю после открытия шведским химиком-фармацевтом Карлом Вильгельмом Шееле химического элемента – хлора.
Позднее француз К. Бертолле выявил, что после растворения в H2O газа происходит образование кислотной смеси, оказывающей отбеливающее, обеззараживающий эффект. Составу дали наименование белильной жидкости. Было основано массовое производство раствора.
В дальнейшем стало понятно, что хранение, транспортировка вещества в подобном виде характеризуется множеством неудобств. Ведь химикат разлагался под воздействием температур, света, даже открытого воздуха. Поэтому был усовершенствован способ получения – едкий хлор стал пропускаться через поташ. Реакция приводила к получению KClO, отличавшегося стабильностью. Соединение назвали жавелевой водой, начав использовать его в быту.
Недостатком этой методики стала высокая стоимость поташа. В первом десятилетии XIX века А. Лабаррак решил заменить поташ, выбрав альтернативой для него каустическую соду, которая дешевле.
Итогом стало получение натрий гипохлорита. Вещество до настоящего времени применяется в разнообразных целях, множестве отраслей.
Определение концентрации раствора
Использовать гипохлорит натрия для процедуры обеззараживания следует после расчета концентрации вредных веществ. Потребуется справочник Лурье, который помогает установить предел растворимости в условиях определенной температуры.
Подобные расчеты приобрели особую важность, когда точность дозирования насосным оборудованием значительно повысилась. Применение растворов для работы, отличающихся высокой концентрацией, обуславливается затруднениями в процессе нахождения подходящих мест монтажа крупных резервуаров.
Концентрация действующего химиката зависит и от материалов, из которых смонтирована проточная часть. Сегодня чаще используется полипропилен, имеющий уплотнения из этиленпропилена. Головки дозации выполняются из поливинилхлорида с политетрафторэтиленовыми (тефлон) либо стальными (нержавейка) уплотнениями, гарантирующими длительность эксплуатацию.
Показатели стойкости материалов присутствуют в табличке совместимости. Они позволяют определять, что при температурном режиме воды до 40˚С материалы хорошо совместимы с гипохлоритом натрия, концентрация смеси которого не превышает 2%.
Преимущества методики
Использование гипохлорита для обеззараживающих, очистительных процедур в водопроводе бытового, промышленного назначения обладает перечнем преимуществ (по сравнению с методом аэрации). Они включают:
- 1. Дешевизну – небольшая цена раствора значительно снижает затраты на процедуру.
- 2. Бесшумность – работа насоса дозации значительно тише функционирования компрессорного оборудования.
- 3. Мощность – ГПХЛ является сильным окислителем стремительного действия, который не требует наличия контактных емкостей.
- 4. Точный расчет – доза может рассчитываться самостоятельно, а точное количество воздуха для аэрации посчитать нереально.
- 5. Гибкость настроек дозации – доступны различные варианты и модификации насосного оборудования, отличающегося по мощности, управлению и прочим характеристикам.
Сколько нужно гипохлорита натрия?
Для примера продемонстрируем, какая необходима доля NaClO для выполнения обеззараживания воды с концентрацией вещества 2% (2 мг/литр). Для выполнения расчетов используем рабочий раствор плотностью 1130 г/литр и показатель расхода воды в 10000 л/час.
С помощью несложных подсчетов определяем, что ежечасно потребуется 0,88 литра раствора. В течение суток насосное оборудование должно выдавать 21,23 литра.
Показатель плотности смеси для очистки воды равен 1260 г/литр, концентрация – 15%. Следует подсчитать, какое количество товарного раствора потребуется для создания непосредственно применяемой рабочей смеси.
Изначально необходимо вычислить массу, которая составляет 113000 гр. Доля хлора составляет 2260 гр. (масса умножается на концентрацию и делится на 100). Показатель массы товарного раствора равен 15066 гр. Чтобы определить его объем, который нужен для получения рабочего состава, следует разделить его на плотность.
В результате получается 11,9 литра товарного раствора, необходимого, чтобы выполнить обеззараживание воды.
Сроки годности вещества
До того, как использовать гипохлорит натрия для водоподготовки, дезинфекции, обеззараживания воды, следует четко уяснить, что это вещество постепенно теряет свое действие. Процесс происходит под воздействием разнообразных внешних факторов. За 12 месяцев концентрация активного Cl в среднем снижается до 110 г/литр (со 190).
Поэтому с течением времени потребуется повышать концентрацию рабочей смеси. Кроме того, запасать канистры NaClO впрок – не лучшая идея. Тем более, что стоимость вещества невелика, он повсеместно доступен и не требует накопления.
Другие сферы применения
Гипохлорит натрия в нынешнее время используется не только для водоподготовки, очищения, обеззараживания воды в водопроводных системах. Химикат отличается широкой сферой применения, которая включает следующие направления:
- 1. Дезинфекция в прудах, бассейнах. Применяются разбавленные растворы. Умеренная стоимость, эффективность против разнообразных бактерий, водорослей, безопасность для человеческого организма делает ГПХН популярным в этой сфере.
- 2. Обработка стоков. Комплексное обеззараживание сточных вод на бытовых объектах, предприятиях осуществляется в целях устранения микроорганизмов, ликвидации неприятных запахов, обезвреживания некоторых вредоносных примесей (цианистых соединений, аммония, фенолов).
- 3. Пищевая промышленность. Вещество нужно для реализации дезинфекционных процедур, выполняемых для эффективного и экономичного удаления различных растительных клеток, бактерий, спор, а также моллюсков, ракообразных.
NaClO – прекрасный антимикробный агент, что также делает вещество ценным для предприятий пищевой отрасли.
- 4. Рыболовство. Использование разбавленных смесей химиката ликвидирует патогенные агенты в процессе выполнения дезинфекции водоемов, характеризующихся твердыми берегами, донной поверхностью. Им также дезинфицируют рыболовные сети, пластиковые резервуары для хранения.
- 5. Здравоохранение. Гипохлорит натрия для медицинской сферы – неотъемлемый раствор при выполнении комплексных мероприятий профилактического характера, направленных на сдерживание развития инфекций.
Подходит для дезинфекционных работ, обработки поверхностей от грамм-позитивных, грамм-негативных бактерий, бактериальных спор, палочек туберкулеза, всевозможных вирусов, грибков.
Есть информация о применении вещества в процессе лечения гайморитов, абсцессов гнойной разновидности, трофических язв в качестве наружного и инъекционного средства.
- 6. Прочие сферы. Действенный гипохлорит встречается в составах моющих препаратов, бытовой химии, паст с эффектом отбеливания, дезинфицирующих средств с хлорирующим, окислительным и действием бактерицидного характера.
Использование NaClO безопаснее хлора
Выполнение очистки воды с помощью ГПХН безопаснее применения в аналогичном процессе хлора. Во-первых, хлор – токсичен, часто в ходе транспортировки становится причиной возникновения аварий. Во-вторых, происходит постоянное ужесточение законов и нормативов, которые касаются обращения с хлористыми соединениями.
Применение NaClO не включается под надзор Федеральной службы по экологическому, технологическому, атомному надзору. При этом эффективность соединения неоднократно доказывалась практикой. Главное, выполнить правильный расчет гипохлорита натрия для обеззараживания питьевой воды и придерживаться этих дозировок.