Содержание
-
Русское название
-
Английское название
-
Латинское название
-
Фармакологическая группа вещества Глекапревир + Пибрентасвир
-
Нозологическая классификация
-
Фармакологическое действие
-
Характеристика
-
Фармакология
-
Применение вещества Глекапревир + Пибрентасвир
-
Противопоказания
-
Ограничения к применению
-
Применение при беременности и кормлении грудью
-
Побочные действия вещества Глекапревир + Пибрентасвир
-
Взаимодействие
-
Передозировка
-
Способ применения и дозы
-
Меры предосторожности
-
Источники информации
-
Торговые названия с действующим веществом Глекапревир + Пибрентасвир
Русское название
Глекапревир + Пибрентасвир
Английское название
Glecaprevir + Pilbrentasvir
Латинское название
Glecaprevirum + Pilbrentasvirum (род. Glecapreviri + Pilbrentasviri)
Фармакологическая группа вещества Глекапревир + Пибрентасвир
Нозологическая классификация
Фармакологическое действие
—
противовирусное.
Характеристика
Комбинация пангенотипных противовирусных ЛС прямого действия.
Фармакология
Фармакодинамика
Механизм действия
Глекапревир (ингибитор протеазы NS3/4A) и пибрентасвир (ингибитор NS5A) воздействуют на различные этапы жизненного цикла вируса гепатита С (ВГС).
Глекапревир представляет собой ингибитор протеазы NS3/4A, которая необходима для протеолитического расщепления кодирующего ВГС полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз ВГС NS3/4A из клинических изолятов генотипов la, lb, 2а, 2b, 3а, 4а, 5а и 6а со значениями IC50 от 3,5 до 11,3 нМ.
Пибрентасвир является пангенотипным ингибитором белка NS5A ВГС, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная активность
Значения ЕС50 глекапревира и пибрентасвира против полноразмерных или гибридных репликонов, кодирующих NS3 или NS5A из лабораторных штаммов, представлены в табл. 1.
Таблица 1
Активность глекапревира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
| Подтип ВГС | ЕС50 глекапревира, нМ | ЕС50 пибрентасвира, нМ |
| 1a | 0,85 | 0,0018 |
| 1b | 0,94 | 0,0043 |
| 2a | 2,2 | 0,0023 |
| 2b | 4,6 | 0,0019 |
| 3a | 1,9 | 0,0021 |
| 4a | 2,8 | 0,0019 |
| 5a | Н/П | 0,0014 |
| 6a | 0,86 | 0,0028 |
Н/П — неприменимо.
Значения ЕС50 глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в табл. 2.
Таблица 2
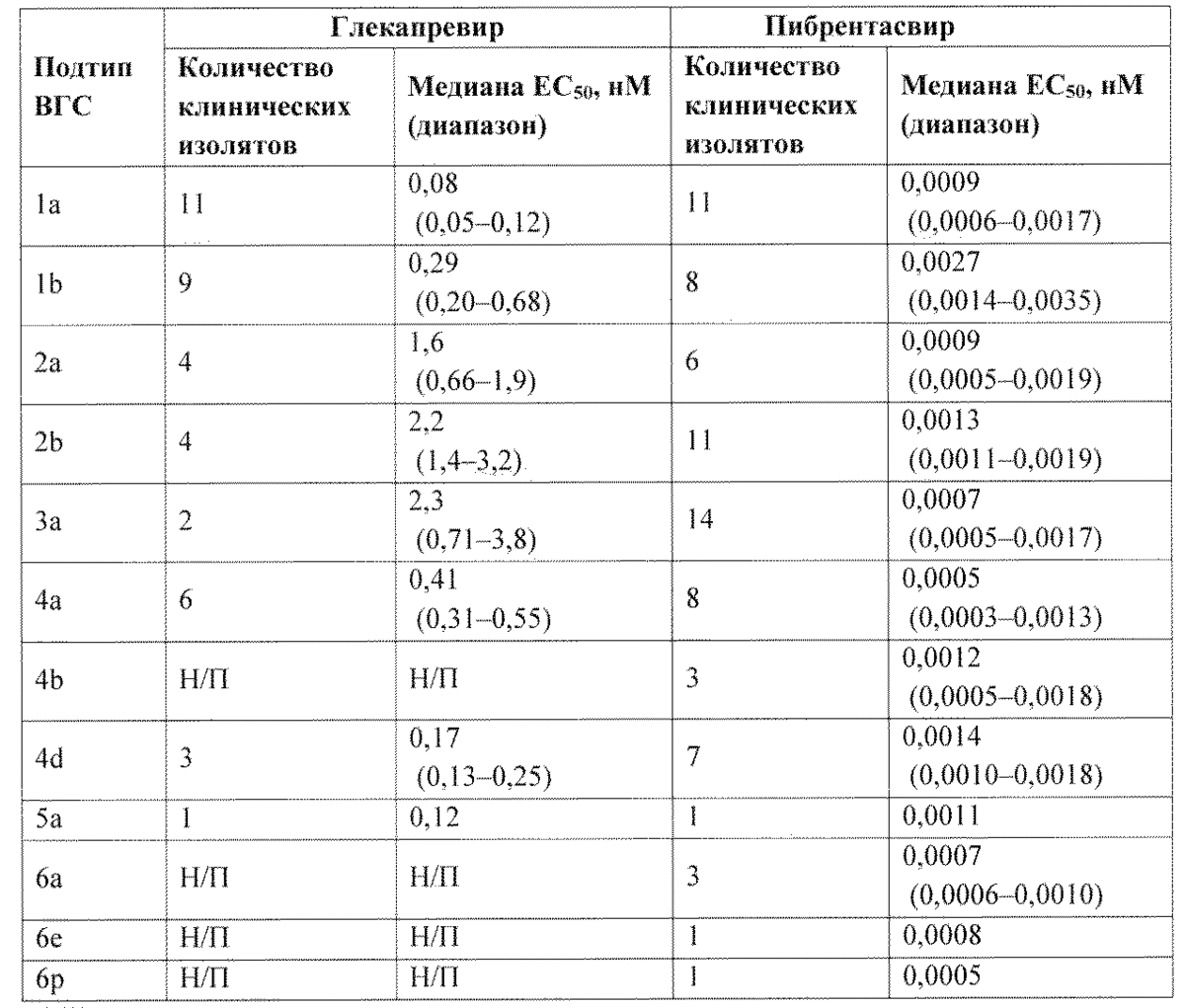
Активность глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1–6
| Подтип ВГС | Глекапревир | Пибрентасвир | ||
| Количество клинических изолятов | Медиана ЕС50, нМ (диапазон) | Количество клинических изолятов | Медиана ЕС50, нМ (диапазон) | |
| 1a | 11 | 0,08 (0,05–0,12) | 11 | 0,0009 (0,0006–0,0017) |
| 1b | 9 | 0,29 ( 0,2–0,08) | 8 | 0,0027 (0,0014–0,0035) |
| 2a | 4 | 1,6 (0,66–1,9) | 6 | 0,0009 (0,0005–0,0019) |
| 2b | 4 | 2,2 (1,4–3,2) | 11 | 0,0013 (0,0011–0,0019) |
| 3a | 2 | 2,3 (0,71–3,8) | 14 | 0,0007 (0,0005–0,0017) |
| 4a | 6 | 0,41 (0,31–0,55) | 8 | 0,0005 (0,0003–0,0013) |
| 4b | Н/П | Н/П | 3 | 0,0012 (0.0005–0,0018) |
| 4d | 3 | 0,17 (0,13–0,25) | 7 | 0,0014 (0,001–0,0018) |
| 5a | 1 | 0,12 | 1 | 0,0011 |
| 6a | Н/П | Н/П | 3 | 0,0007 (0,0006–0,001) |
| 6e | Н/П | Н/П | 1 | 0,0008 |
| 6p | Н/П | Н/П | 1 | 0,0005 |
Н/П — неприменимо.
Активность in vitro
Оценка комбинации глекапревира и пибрентасвира на репликонных клеточных культурах генотипа ВГС-1 не выявила каких-либо признаков антагонизма противовирусной активности.
Резистентность
В культуре клеток. Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A, выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54, 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапревира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1–4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе 3а, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58, 92 или 93 в NS5A в генотипах 1–6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе 3а аминокислотные замены А30К или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и 3а (включая A30K+Y93H в генотипе 3а) демонстрируют снижение чувствительности к пибрентасвиру. В репликоне генотипа 3b присутствие встречающихся в природе полиморфизмов К30 и М31 в белке NS5A снижало чувствительность к пибрентасвиру в 24 раза по сравнению с активностью пибрентасвира в репликоне генотипа 3а.
Фармакокинетика
Фармакокинетические свойства компонентов комбинации глекапревир + пибрентасвир представлены в табл. 3
Таблица 3
Фармакокинетические свойства компонентов комбинации глекапревир + пибрентасвир у здоровых добровольцев
| Параметры | Глекапревир | Пибрентасвир |
| Всасывание | ||
| Tmax, ч1 | 5 | 5 |
| Влияние пищи (по сравнение с приемом натощак)2 , % | ↑83–163 | ↑40–53 |
| Распределение | ||
| Связывание с белками плазмы, % | 97,5 | >99,9 |
| Коэффициент распределения кровь/плазма | 0,57 | 0,62 |
| Биотрансформация | ||
| Метаболизм | Вторичный | Отсутствует |
| Выведение | ||
| Основной путь выведения | С желчью | С желчью |
| T1/2 в равновесном состоянии, ч | 6–9 | 23–29 |
| Выведение с мочой, %3 | 0,7 | 0 |
| Выведение с калом, %3 | 92,14 | 96,6 |
| Клеточный транспорт | ||
| Субстрат для транспортера | P-gp, BCRP и OATP1B1/3 | P-gp и не исключая BCRP |
1 Медиана Тmах у здоровых добровольцев после приема однократной дозы глекапревира и пибрентасвира.
2 Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров.
3 Прием однократной дозы [14С] глекапревира или [14С] пибрентасвира в исследованиях массового баланса.
4 Окислительные метаболиты или их продукты обмена составляли 26% радиоактивной дозы. Метаболиты глекапревира в плазме не наблюдались.
У пациентов с хроническим гепатитом С без цирроза после 3 дней монотерапии глекапревиром 300 мг в день (N=6) или пибрентасвиром 120 мг в день (N=8) геометрическое среднее значение AUC24 составило 13600 для глекапревира и 459 нг·ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекрестного взаимодействия глекапревира и пибрентасвира. Основываясь на популяционной фармакокинетической модели для комбинации глекапревир + пибрентасвир при хроническом гепатите С, установившиеся значения AUC24 для глекапревира и пибрентасвира были 4800 и 1430 нг·ч/мл у пациентов без цирроза (N=1804) и 10500 и 1530 нг·ч/мл у пациентов с циррозом печени (N=280) соответственно. По сравнению со здоровыми пациентами (N=230), популяционные оценки AUC24ss были аналогичны (разница в 10%) для глекапревира и на 34% ниже для пибрентасвира у пациентов, инфицированных ВГС, без цирроза.
Линейность
AUC глекапревира увеличивалась в степени большей, чем пропорциональная увеличению дозы (при приеме 1200 мг 1 раз в день наблюдалась экспозиция в 516 раз больше, чем при приеме 200 мг 1 раз в день). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная увеличению дозы до 120 мг (при дозе 120 мг 1 раз в день наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг 1 раз в день), но установлена линейная фармакокинетика в дозах ≥120 мг. Нелинейное увеличение экспозиции в дозах <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром в 3 раза выше по сравнению с применением пибрентасвира в монотерапии. У глекапревира наблюдалось меньшее влияние пибрентасвира.
Особые группы пациентов
Раса/этническая принадлежность. Не требуется коррекция дозы комбинации глекапревир + пибрентасвир в зависимости от расы или этнической принадлежности.
Пол/масса тела. Не требуется коррекция дозы комбинации глекапревир + пибрентасвир в зависимости от пола или массы тела.
Пожилой возраст. У пациентов пожилого возраста коррекция дозы комбинации глекапревир + пибрентасвир не требуется. Популяционный фармакокинетический анализ пациентов, инфицированных ВГС, в возрасте от 12 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапревира и пибрентасвира.
Дети. У детей в возрасте 12 лет и старше коррекция дозы комбинации глекапревир + пибрентасвир не требуется. Содержание глекапревира и пибрентасвира в плазме крови у детей было сопоставимо с таковым у взрослых в исследованиях II/III фазы. Фармакокинетика глекапревира и пибрентасвира не изучалась у детей в возрасте до 12 лет.
Нарушение функции почек. Значение AUC глекапревира и пибрентасвира повышалось не более чем на 56% у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с показателями пациентов с нормальной функцией почек. Значение AUC глекапревира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница ≤18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапревира на 86% выше, а пибрентасвира на 54% выше, чем у пациентов с нормальной функцией почек. При оценке концентрации глекапревира и пибрентасвира, не связанных с белками плазмы, может наблюдаться более выраженный рост AUC. В целом, изменения воздействия комбинации глекапревир + пибрентасвир у ВГС-инфицированных пациентов с нарушением функции почек, на диализе или без него, не были клинически значимыми.
Печеночная недостаточность. При приеме рекомендованнной дозы значение AUC глекапревира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью было на 33% выше, класса В — на 100 % выше, а класса С — в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени.
Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26% выше у пациентов с печеночной недостаточностью класса В и на 114% — класса С. При оценке концетрации несвязанных глекапревира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема комбинации глекапревир + пибрентасвир пациентами с ВГС и компенсированным циррозом печени воздействие глекапревира было примерно в 2 раза выше, а пибрентасвира — аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапревира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Взаимодействие с другими ЛС. Были проведены исследования взаимодействия глекапревира и пибрентасвира с другими ЛС, которые могут вступать с ними во взаимодействие или часто применяются в исследованиях ФКВ. В таблицах ниже показаны фармакокинетические эффекты при взаимодействии глекапревира и пибрентасвира с другими ЛС, которые показали потенциально клинически значимые изменения.
Таблица 4
Изменения фармакокинетических параметров глекапревира (ГЛЕ) или пибрентасвира (ПИБ) в присутствии одновременно назначаемого ЛС
| Совместное ЛС (доза) | Доза ГЛЕ/ПИБ, мг | N | Противовирусное ЛС | Соотношение центральных значений (90% ДИ) | ||
| Cmax | AUC | Cmin | ||||
| Карбамазепин (200 мг 2 раза в день) | 300/120 однократно | 10 | ГЛЕ | 0,33 (0,27; 0,41) | 0,34 (0,28; 0,4) | — |
| ПИБ | 0,5 (0,42; 0,59) | 0,49 (0,43; 0,55) | — | |||
| Рифампицин (600 мг, первая доза) | 300/120 однократно | 12 | ГЛЕ | 6,52 (5,06; 8,41) | 8,55 (7,01; 10,4) | — |
| ПИБ | ↔ | ↔ | — | |||
| Рифампицин (600 мг 1 раз в день) | 300/120 однократно1 | 12 | ГЛЕ | 0,14 (0,11; 0,19) | 0,12 (0,09; 0,15) | — |
| ПИБ | 0,17 (0,14; 0,2) | 0,13 (0,11; 0,15) | — | |||
| Циклоспорин (100 мг однократно) | 300/120 1 раз в день | 12 | ГЛЕ2 | 1,3 (0,95; 1,78) | 1,37 (1,13; 1,66) | 1,34 (1,12; 1,6) |
| ПИБ | ↔ | ↔ | 1,26 (1,15; 1,37) | |||
| Циклоспорин (400 мг однократно) | 300/120 однократно | 11 | ГЛЕ | 4,51 (3,63; 6,05) | 5,08 (4,11; 6,29) | — |
| ПИБ | ↔ | 1,93 (1,78; 2,09) | — | |||
| Атазанавир + ритонавир (300 + 100 мг 1 раз в день) | 300/120 1 раз в день3 | 12 | ГЛЕ | ≥4,06 (3,15; 5,23) | ≥6,52 (5,25; 8,14) | ≥14,3 (9,85; 20,7) |
| ПИБ | ≥1,29 (1,15; 1,45) | ≥1,64 (1,48; 1,82) | ≥2,29 (1,95; 2,68) | |||
| Дарунавир + ритонавир (800 + 100 мг 1 раз в день) | 300/120 1 раз в день | 8 | ГЛЕ | 3,09 (2,26; 4,2) | 4,97 (3,62; 6,84) | 8,25 (4,4; 15,4) |
| ПИБ | ↔ | ↔ | 1,66 (1,25; 2,21) | |||
| Лопинавир/ритонавир (400/100 мг 2 раза в день) | 300/120 1 раз в день | 9 | ГЛЕ | 2,55 (1,84; 3,52) | 4,38 (3,02; 6,36) | 18,6 (10,4; 33,5) |
| ПИБ | 1,4 (1,17; 1,67) | 2,46 (2,07; 2,92) | 5,24 (4,18; 6,58) |
↔ Без изменений (соотношение центральных значений от 0,8 до 1,25).
1 Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
2 У пациентов после трансплантации печени, инфицированных ВГС, которые получали лечение циклоспорином в дозе 100 мг или менее в день, экспозиция глекапревира была в 2,4 раза выше по сравнению с пациентами, которые не принимали циклоспорин.
3 Было отмечено влияние атазанавира и ритонавира на концентрацию глекапревира и пибрентасвира после приема первой дозы глекапревира и пибрентасвира.
Таблица 5
Фармакокинетические параметры совместно применяемых ЛС
| Совместное ЛС (доза) | Доза ГЛЕ/ПИБ, мг | N | Соотношение центральных значений (90% ДИ) | ||
| Cmax | AUC | Cmin | |||
| Дигоксин (0,5 мг однократно) | 400/120 1 раз в день | 12 | 1,72 (1,45; 2,04) | 1,48 (1,4; 1,57) | — |
| Дабигатран (в виде этексилата, 150 мг однократно) | 300/120 1 раз в день | 11 | 2,05 (1,72; 2,44) | 2,38 (2,11; 2,7) | — |
| Правастатин (10 мг 1 раз в день) | 400/120 1 раз в день | 12 | 2,23 (1,87; 2,65) | 2,3 (1,91; 2,76) | — |
| Розувастатин (5 мг 1 раз в день) | 400/120 1 раз в день | 11 | 5,62 (4,8; 6,59) | 2,15 (1,88; 2,46) | — |
| Аторвастатин (10 мг 1 раз в день) | 400/120 1 раз в день | 11 | 22 (16,4; 29,6) | 8,28 (6,06; 11,3) | — |
| Ловастатин (10 мг 1 раз в день) | 300/120 1 раз в день | 12 | ↔ | 1,7 (1,4; 2,06) | — |
| Метаболит ловастатина, ловастатиновая кислота | 5,73 (4,65; 7,07) | 4,1 (3,45; 4,87) | — | ||
| Симвастатин (5 мг 1 раз в день) | 300/120 1 раз в день | 12 | 1,99 (1,6; 2,48) | 2,32 (1.93; 2,79) | — |
| Метаболит симвастатина, симвастатиновая кислота | 10,7 (7,88; 14,6) | 4,48 (3,11; 6,46) | — | ||
| Этинилэстрадиол/норгестимат (35/250 мкг 1 раз в день) | 300/120 1 раз в день | 11 | 1,31 (1,24; 1,38) | 1,28 (1,23; 1,32) | 1,38 (1,25; 1,52) |
| Норгестрел | 1,54 (1,34; 1,76) | 1,63 (1,5; 1,76) | 1,75 (1,62; 1,89) | ||
| Норгестромин | ↔ | 1,44 (1,34; 1,54) | 1,45 (1,33; 1,58) | ||
| Этинилэстрадиол/левоноргестрел (20/100 мкг 1 раз в день) | 300/120 1 раз в день | 12 | 1,3 (1,18; 1,44) | 1,4 (1,33; 1,48) | 1,56 (1,41; 1,72) |
| Норгестрел | 1,37 (1,23; 1,52) | 1,68 (1,57; 1,8) | 1,77 (1,58; 1,98) |
↔ Без изменений (соотношение центральных значений от 0,8 до 1,25).
Применение вещества Глекапревир + Пибрентасвир
Лечение хронического гепатита С у взрослых и детей с 12 лет.
Противопоказания
Повышенная чувствительность к любому действующему веществу комбинации; тяжелая печеночная недостаточность (класс С по шкале Чайлд-Пью); совместное применение со следующими ЛС: атазанавир, аторвастатин, симвастатин, дабигатрана этексилат, содержащими эстрадиол, сильными индукторами Р-gp и CYP3A, например рифампицин, карбамазепин, ЛС, содержащие зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин, примидон (см. «Взаимодействие»); детский возраст до 12 лет.
Ограничения к применению
Комбинацию глекапревир + пибрентасвир не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг в день). Следует применять с осторожностью со следующими ЛС: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
Применение при беременности и кормлении грудью
Данные о применении глекапревира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности.
Исследования глекапревира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапревира, что исключило возможность дальнейших исследований. В качестве меры предосторожности, комбинацию глекапревир + пибрентасвир не рекомендуется применять во время беременности.
Неизвестно, выделяется ли глекапревир или пибренгасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапревира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию комбинацией глекапревир + пибрентасвир или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины.
Фертильность
Исследования влияния глекапревира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапревира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз.
Побочные действия вещества Глекапревир + Пибрентасвир
Резюме профиля безопасности
Оценка безопасности комбинации глекапревир + пибрентасвир у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам регистрационных исследований II и III фазы, в которых участвовали около 2300 пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6, получавших комбинацию в течение 8, 12 или 16 нед.
Наиболее частыми нежелательными реакциями (частота ≥10%) были головные боли и утомляемость. Менее чем у 0,1% пациентов, получавших комбинацию глекапревир + пибрентасвир, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение комбинацией глекапревир + пибрентасвир по причине развития нежелательных реакций, составила 0,1%. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Нежелательные реакции
Ниже приведены нежелательные реакции у пациентов, получавших комбинацию глекапревир + пибрентасвир, сгруппированные по классам систем органов и частоте встречаемости. Частота встречаемости определялась как очень часто (>1/10); часто (>1/100, <1/10); нечасто (от >1/1000 до <1/100); редко (от >1/10000 до <1/1000) и очень редко (<1/10000).
Со стороны нервной системы: очень часто — головная боль.
Со стороны ЖКТ: часто — тошнота, диарея.
Общие нарушения и реакции в месте введения: очень часто — повышенная утомляемость; часто — астения.
Описание отдельных нежелательных реакций
Нежелательные реакции у взрослых пациентов с тяжелым нарушением функции почек, включая пациентов на диализе. Безопасность комбинации глекапревир + пибрентасвир у пациентов с хронической болезнью почек (стадия 4 или 5, включая находящихся на диализе) и хронической инфекцией, вызванной ВГС генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него), оценивалась у 104 пациентов. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17,3%) и повышенная утомляемость (11,5%).
Нежелательные реакции у взрослых пациентов после трансплантации почек или печени. Безопасность комбинации глекапревир + пибрентасвир оценивалась у 100 пациентов после трансплантации печени или почек, инфицированных ВГС генотипов 1, 2, 3, 4 или 6 без цирроза печени. Общий профиль безопасности у пациентов после трансплантации печени или почек был сопоставим с профилем безопасности у пациентов в исследованиях II и III фазы. Наблюдались следующие нежелательные реакции с частотой, равной или более 5%, у пациентов, получавших комбинацию глекапревир + пибрентасвир в течение 12 нед: головная боль (17%), усталость (16%), тошнота (8%) и зуд (7%). У 81% пациентов, получавших комбинацию глекапревир + пибрентасвир, сообщалось о нежелательных реакциях легкой степени тяжести. У 2% пациентов наблюдались серьезные нежелательные реакции. Не было ни одного случая полной отмены комбинации глекапревир + пибрентасвир из-за нежелательных реакций.
Оценка безопасности у взрослых пациентов с коинфекцией ВГС и ВИЧ-1. Общий профиль безопасности у пациентов с коинфекцией ВГС и ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови. У 1% пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше ВГН, что было связано с глекапревиропосредованным ингибированием белков — переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ.
Дети
Безопасность комбинации глекапревир + пибрентасвир у детей, инфицированных ВГС генотипов 1–6 оценивалась в открытом исследовании II/III фазы с участием 47 пациентов в возрасте от 12 до 18 лет, получавших терапию в течение 8–16 нед. Нежелательные реакции, зафиксированные в ходе данного исследования, были сопоставимы с наблюдаемыми у взрослых пациентов.
Взаимодействие
Возможное влияние комбинации глекапревир + пибрентасвир на другие ЛС
Глекапревир и пибрентасвир — ингибиторы Р-gp, BCRP и полипептида, транспортирующего органические анионы (ОАТР1В1/3).
Одновременное применение с комбинацией глекапревир + пибрентасвир может привести к повышению концентрации в плазме ЛC, являющихся субстратами Р-gp (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или ОАТР1В1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). Для других субстратов Р-gp, BCRP и ОАТР1В1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир — слабые ингибиторы изоферментов CYP3A и уридинглюкуронозилтрансферазы (UGT) 1А1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1A1 (ралтегравир) при одновременном применении с комбинацией глекапревир + пибрентасвир.
Применение глекапревира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1А2, CYP2C9, CYP2C19, CYP2D6, UGT1А6, UGT1А9, UGT1A4, UGT2B7, ОСТ1, ОСТ2, ОАТ1, ОАТЗ, МАТЕ1 и МАТЕ2К.
Пациенты, получающие антагонисты витамина К
На фоне комбинации глекапревир + пибрентасвир может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг МНО.
Потенциальное влияние других ЛС на комбинацию глекапревир + пибрентасвир
Совместное применение с сильными индукторами Р-gp/CYP3А. Сильные индукторы Р-gp и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон) могут вызвать существенное снижение концентрации глекапревира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта и потере вирусологического ответа. Применение таких ЛС одновременно с комбинацией глекапревир + пибрентасвир противопоказано (см. «Противопоказания»).
Применение комбинации глекапревир + пибрентасвир одновременно с ЛС, которые являются умеренными индукторами Р-gp и CYP3A, может вызвать снижение концентрации глекапревира и пибрентасвира в плазме крови (окскарбазепин, эсликарбазепин, лумакафтор, кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. «Меры предосторожности»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков Р-gp и/или BCRP. Глекапревир также является субстратом транспортеров печеночного захвата ОАТР1В1/3. Применение комбинации глекапревир + пибрентасвир одновременно с ингибиторами Р-gp и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир) может замедлить выведение глекапревира и пибрентасвира и увеличить экспозицию противовирусных ЛС в плазме крови. ЛС, являющиеся ингибиторами OATP1B1/3 (элвитегравир, циклоспорин, дарунавир, лопинавир), могут вызвать повышение системной концентрации глекапревира.
Установленные и другие потенциально возможные взаимодействия
В табл. 6 приведены данные (средние значения фармакокинетических параметров, вычисленные методом наименьших квадратов (90% ДИ) о влиянии на концентрацию компонентов комбинации глекапревир + пибрентасвир и сопутствующих ЛС. Направление стрелки указывает изменение воздействия (Сmах и AUC) глекапревира, пибрентасвира и сопутствующего ЛC (↑ — увеличение более чем на 25%, ↓ — снижение более чем на 20%, ↔ — нет изменения (снижение ≤20% или увеличение на ≤25%).
Таблица 6
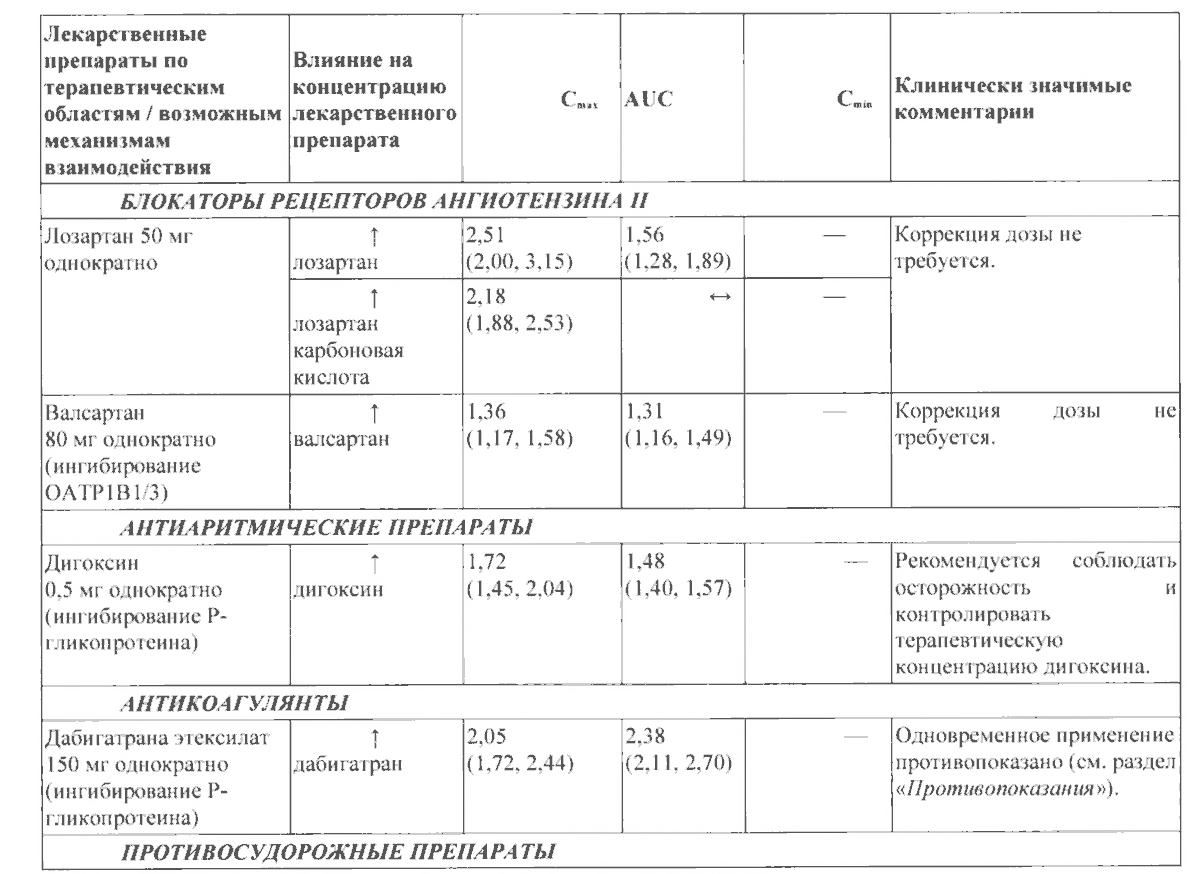
Взаимодействие комбинации глекапревир + пибрентасвир с другими ЛС
| Фармакологическая группа, ЛС, возможный механизм действия | Влияние на концентрацию ЛС | Cmax | AUC | Cmin | Клинически значимые комментарии |
| АРА II | |||||
| Лозартан, 50 мг однократно | ↑ лозартан | 2,51 (2; 3,15) | 2,18 (1,88; 2,53) | — | Коррекция дозы не требуется |
| ↑ лозартанкарбоновая кислота | 2,18 (1,88; 2,53) | ↔ | — | ||
| Валсартан, 80 мг однократно (ингибирование OATP1B1/3) | ↑ валсартан | 1,36 (1,17; 1,58) | 1,31 (1.16; 1,49) | — | Коррекция дозы не требуется |
| Антиаритмические ЛС | |||||
| Дигоксин, 0,5 мг однократно (ингибирование P-gp) | ↑ дигоксин | 1,72 (1,45; 2,04) | 1,48 (1,4; 1,57) | — | Рекомендуется соблюдать осторожность и контролировать терапевтическую концентрацию дигоксина |
| Антикоагулянты | |||||
| Дабигатрана этексилат, 150 мг однократно (ингибирование P-gp) | ↑ дабигатран | 2,05 (1,72; 2,44) | 2,38 (2.11; 2,7) | — | Одновременное применение противопоказано |
| Противосудорожные ЛС | |||||
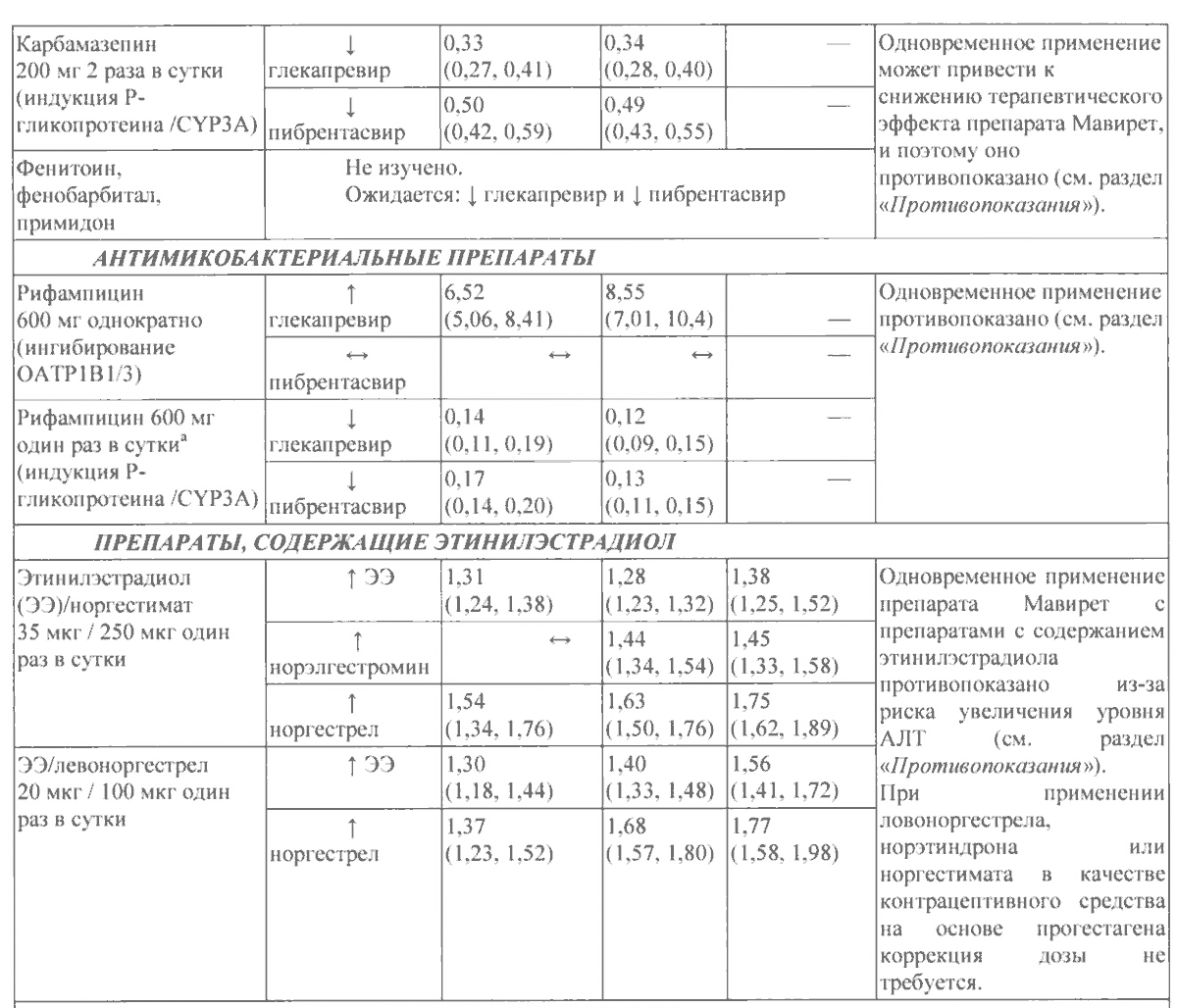
| Карбамазепин, 200 мг 2 раза в сутки (индукция P-gp/CYP3A) | ↓ глекапревир | 0,33 (0,27; 0,41) | 0,34 (0,28; 0,4) | — | Одновременное применение может привести к снижению терапевтического эффекта комбинации глекапревир + пибрентасвир и поэтому противопоказано |
| ↓ пибрентасвир | 0,5 (0,42; 0,59) | 0,49 (0,43; 0,55) | — | ||
| Фенитоин, фенобарбитал, примидон | Не изучено. Ожидается: ↓ глекапревир и ↓ пибрентасвир | ||||
| Антимикобактериальные ЛС | |||||
| Рифампицин, 600 мг однократно (ингибирование OATP1B1/3) | ↑ глекапревир | 6,52 (5,06; 8,41) | 8,55 (7,01; 10,4) | — | Одновременное применение противопоказано |
| ↔ пибрентасвир | ↔ | ↔ | — | ||
| Рифампицин, 600 мг 1 раз в сутки1 (индукция P-gp/CYP3A) | ↓ глекапревир | 0,14 (0,11; 0,19) | 0,12 (0,09; 0,15) | — | |
| ↓ пибрентасвир | 0,17 (0,14; 0,2) | 0,13 (0,11; 0,15) | — | ||
| ЛС, содержащие этинилэстрадиол | |||||
| Этинилэстрадиол/норгестимат, 35/250 мкг 1 раз в сутки | ↑ этинилэстрадиол | 1,31 (1,24; 1,38) | 1,28 (1.23; 1,32) | 1,38 (1,25; 1,52) | Одновременное применение комбинации глекапревир + пибрентасвир с препаратами, содержащими этинилэстрадиол противопоказано из-за риска увеличения уровня АЛТ. При применении левоноргестрела, норэтиндрона или норгестимата в качестве контрацептивного средства на основе прогестагена коррекция дозы не требуется |
| ↑ норэлгестромин | ↔ | 1,44 (1,34; 1,54) | 1,45 (1,33; 1.58) | ||
| ↑ норгестрел | 1,54 (1.34; 1,76) | 1,63 (1,5; 1,76) | 1,75 (1,62; 1,89) | ||
| Этинилэстрадиол/левоноргестрел, 20/100 мкг 1 раз в сутки | ↑ этинилэстрадиол | 1,3 (1,18; 1,44) | 1,4 (1,33; 1,48) | 1,56 (1,41; 1,72) | |
| ↑ норгестрел | 1,37 (1.23; 1,52) | 1,68 (1,57; 1,8) | 1,77 (1,58; 1,98) | ||
| ЛС растительного происхождения | |||||
| Зверобой продырявленный (Hypericum perforatum) (индукция Р-gp/CYP3A) | Не изучено. Ожидается: ↓ глекапревир и ↓ пибрснтасвир | Одновременное применение может привести к снижению терапевтического эффекта комбинации глекапревир + пибрентасвир и поэтому противопоказано | |||
| Противовирусные ЛС для лечения ВИЧ-инфекции | |||||
| Атазанавир + ритонавир, 300/100 мг 1 раз в сутки2 | ↑ глекапревир | ≥4,06 (3,15; 5,23) | ≥6,53 (5,24; 8,14) | ≥14,3 (9,85; 20,7) | Одновременное применение комбинации глекапревир + пибрентасвир с атазанавиром противопоказано из-за риска увеличения уровня АЛТ |
| ↑ пибрентасвир | ≥1,29 (1,15; 1,45) | ≥1,64 (1,48; 1,82) | ≥2,29 (1,95; 2,68) | ||
| Дарунавир + ритонавир, 800/100 мг 1 раз в сутки | ↑ глекапревир | 3,09 (2,26; 4,2) | 4,97 (3,62; 6,84) | 8,24 (4,4; 15,4) | Одновременное применение с дарунавиром не рекомендуется |
| ↔ пибрентасвир | ↔ | ↔ | 1,66 (1,25; 2,21) | ||
| Эфавиренз/ эмтрицитабин/ тенофовира дизопроксила фумарат 600/300/200 мг 1 раз в сутки | ↑ тенофовир | ↔ | 1,29 (1,23; 1,35) | 1,38 (1,31; 1,46) | Одновременное применение с эфавирензом может привести к снижению терапевтического эффекта комбинации глекапревир + пибрентасвир и не рекомендуется. Не ожидается клинически значимого взаимодействия комбинации глекапревир + пибрентасвир с тенофовира дизопроксила фумаратом |
| Влияние на глекапревир и пибрентасвир не оценивалось в данном исследовании, но воздействие глекапревира и пибрентасвира было значительно ниже, чем в других исследованиях подобных доз | |||||
| Элвитегравир/ кобинистат/ эмтрицитабин/ тенофовира алафенамид (ингибирование Р-gp, BCRP и ОАТР кобицистатом, ингибирование ОАТР элвитегравиром) | ↔ тенофовир | ↔ | ↔ | ↔ | Коррекция дозы не требуется |
| ↑ глекапревир | 2,5 (2,08; 3,0) | 3,05 (2,55; 3,64) | 4,58 (3,15; 6,65) | ||
| ↑ пибрентасвир | ↔ | 1,57 (1,39; 1,76) | 1,89 (1,63; 2.19) | ||
| Лопинавир/ ритонавир, 400/100 мг 2 раза в сутки | ↑ глекапревир | 2,55 (1,84; 3,52) | 4,38 (3,02; 6,36) | 18,6 (10,4; 33,5) | Одновременное применение не рекомендуется |
| ↑ пибрентасвир | 1,4 (1,17; 1,67) | 2,46 (2,07; 2,92) | 5,24 (4,18; 6,58) | ||
| Ралтегравир, 400 мг 2 раза в день (ингибирование UGT1A1) | ↑ ралтегравир | 1,34 (0,89; 1,98) | 1,47 (1,15; 1,87) | 2,64 (1,42; 4,91) | Коррекция дозы не требуется |
| Софосбувир, 400 мг однократно (ингибирование Р-gp/BCRP) | ↑ софосбувир | 1,66 (1,23; 2,22) | 2,25 (1,86; 2,72) | — | Коррекция дозы не требуется |
| ↑ GS-331007 | ↔ | ↔ | 1,85 (1,67; 2,04) | ||
| ↔ глекапревир | ↔ | ↔ | ↔ | ||
| ↔ пибрентасвир | ↔ | ↔ | ↔ | ||
| Ингибиторы ГМГ-КоА-редуктазы | |||||
| Аторвастатин, 10 мг 1 раз в сутки (ингибирование ОАТР1В1/3, Р-gp, BCRP, CYP3A) | ↑ аторвастин | 22 (16,4; 29,5) | 8,28 (6,06; 11,3) | — | Одновременное применение комбинации глекапревир + пибрентасвир и симвастатина противопоказано |
| Симвастатин, 5 мг 1 раз в сутки (ингибирование ОАТР1В1/3, Р-gp, BCRP) | ↑ симвастатин | 1,99 (1,6; 2,18) | 2,32 (1,93; 2,79) | — | |
| ↑ симвастатиновая кислота | 10,77 (7,88; 14,6) | 4,48 (3,11; 6,46) | — | ||
| Ловастатин, 10 мг 1 раз в сутки (ингибирование ОАТР1В1/3, Р-gp, BCRP) | ↑ ловастатин | ↔ | 1,7 (1,4; 2,06) | — | Одновременное применение не рекомендуется. При применении ловастатина доза не должна превышать 20 мг в день, а пациенты должны находиться под наблюдением |
| ↑ ловастатиновая кислота | 5,73 (4,65; 7,07) | 4,1 (3,45; 4,87) | — | ||
| Правастатин, 10 мг 1 раз в сутки (ингибирование ОАТР1В1/3) | ↑ правастатин | 2,23 (1,87; 2,65) | 2,3 (1,91; 2,76) | — | Рекомендуется соблюдать осторожность. Доза правастатина не должна превышать 20 мг/сут, а розувастатина — 5 мг/сут |
| Розувастатин, 5 мг 1 раз в сутки (ингибирование ОАТР1В1/3, BCRP) | ↑ розувастатин | 5,62 (4,8; 6,59) | 2,15 (1,88; 2,46) | — | |
| Флувастатин, питавастатин | Не изучено. Ожидается: ↑ флувастатин и ↑ питавастатин | Возможно взаимодействие с флувастатином и питавастатином, рекомендуется соблюдать осторожность при одновременном применении. Рекомендуется применение статина в низкой дозе при начале лечения противовирусным ЛС прямого действия | |||
| Иммунодепрессанты | |||||
| Циклоспорин, 100 мг однократно | ↑ глекапревир3 | 1,3 (0,95; 1,78) | 1,37 (1,13; 1,66) | 1,34 (1,12; 1,6) | Комбинация глекапревир + пибрентасвир не рекомендуется для лечения пациентов, которым требуется прием стабильной дозы циклоспорина >100 мг/сут |
| ↑ пибрентасвир | ↔ | ↔ | 1,26 (1,15; 1,37) | ||
| Циклоспорин, 400 мг однократно | ↑ глекапревир | 4,51 (3,63; 6,05) | 5,08 (4,11; 6,29) | — | |
| ↑ пибрентасвир | ↔ | 1,93 (1,78; 2,09) | — | ||
| Такролимус, 1 мг однократно (ингибирование CYP3A4/P-gp) | ↑ такролимус | 1,5 (1,24; 1,82) | 1,45 (1,24; 1,7) | — | Комбинацию глекапревир + пибрентасвир в сочетании с такролимусом следует принимать с осторожностью. Возможно увеличение концентрации такролимуса. Рекомендуется мониторинг концентрации такролимуса и соответствующая коррекция дозы |
| ↔ глекапревир | ↔ | ↔ | ↔ | ||
| ↔ пибрентасвир | ↔ | ↔ | ↔ | ||
| Ингибиторы протонного насоса | |||||
| Омепразол, 20 мг 1 раз в сутки (повышение значения pH в желудке) | ↓ глекапревир | 0,78 (0,6; 1) | 0,71 (0,58; 0,86) | — | Одновременное применение с омепразолом в дозе 40 мг 1 раз в сутки может привести к снижению терапевтического эффекта комбинации глекапревир + пибрентасвир и не рекомендуется |
| ↔ пибрентасвир | ↔ | ↔ | — | ||
| Омепразол, 40 мг 1 раз в сутки (за 1 ч до приема пищи) | ↓ глекапревир | 0,36 (0,21; 0,59) | 0,49 (0,35; 0,68) | — | |
| ↔ пибрентасвир | ↔ | ↔ | — | ||
| Омепразол, 40 мг 1 раз в сутки ежедневно (вечером, отдельно от приема пищи) | ↓ глекапревир | 0,54 (0,44; 0,65) | 0,51 (0,45; 0,59) | — | |
| ↔ пибрентасвир | ↔ | ↔ | — | ||
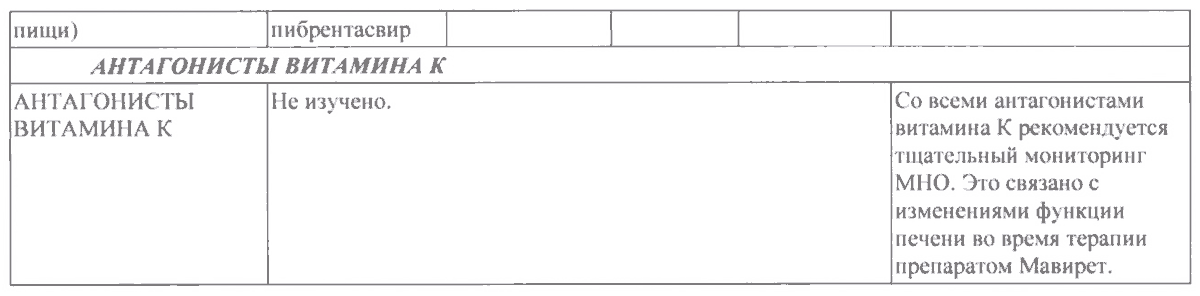
| Антагонисты витамина K | |||||
| Антагонисты витамина K | Не изучено | Со всеми антагонистами витамина К рекомендуется тщательный мониторинг МНО. Это связано с изменениями функции печени во время терапии комбинацией глекапревир + пибрентасвир |
1 Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
2 Указано влияние атазанавира и ритонавира на первую дозу глекапревира и пибрентасвира.
3 Экспозиция глекапревира у инфицированных ВГС пациентов после трансплантации, получавших циклоспорин в дозе 100 мг/сут или меньше, была в 4 раза выше, чем у неполучавших циклоспорин.
Дополнительные исследования межлекарственного взаимодействия проводились со следующими лекарственными препаратами: абакавир, амлодипин, бупренорфин, кофеин, декстрометорфан, долутегравир, эмтрицитабин, фелодипин, ламивудин, ламотриджин, метадон, мидазолам, налоксон, норэтиндрон или другие контрацептивные средства, содержащие прогестин, рилпивирин, тенофовир алафенамид и толбутамид. Клинически значимого взаимодействия не выявлено.
Передозировка
Наибольшая задокументированная доза, полученная здоровыми добровольцами, составила 1200 мг 1 раз в день в течение 7 дней для глекапревира и 600 мг 1 раз в день в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5× ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапревира (700 или 800 мг) 1 раз в день в течение ≥7 дней. В случае передозировки необходимо контролировать состояние пациента на наличие признаков токсического поражения. Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапревира и пибрентасвира.
Способ применения и дозы
Внутрь, во время еды, 1 раз в сутки.
Меры предосторожности
Реактивация вирусного гепатита В
Во время лечения противовирусными ЛС прямого действия сообщалось о реактивации вируса гепатита В, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие вируса гепатита B. Пациенты с коинфекцией вируса гепатита B и ВГС подвержены риску реактивации вируса гепатита В, поэтому следует проводить мониторинг состояния этих пациентов и ведение с соблюдением современных рекомендаций.
Потенциальные эффекты полной элиминации ВГС из организма ЛС прямого противовирусного действия
У пациентов может наблюдаться улучшение функционирования печени в результате лечения хронического вирусного гепатита С, выражающееся в улучшении метаболизма глюкозы в печени. Для пациентов с диабетом это означает улучшение показателей уровня глюкозы в крови. Редкие случаи симптоматической гипогликемии были зарегистрированы в рамках терапии ЛС прямого противовирусного действия, поэтому у пациентов с диабетом рекомендуется проводить тщательный мониторинг уровня глюкозы в крови для определения целесообразности коррекции доз гипогликемических ЛС.
Нарушение функции печени
Комбинацию глекапревир + пибрентасвир не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и она противопоказана пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. «Противопоказания»).
Влияние на способность управлять транспортными средствами, механизмами. Комбинация глекапревир + пибрентасвир не оказывает влияния или оказывает незначительное влияние на способность к управлению транспортными средствами и механизмами.
Источники информации
Обобщенные материалы www.grls.rosminzdrav.ru, 2019.
Торговые названия с действующим веществом Глекапревир + Пибрентасвир
| Торговое название | Цена за упаковку, руб. |
|---|---|
| Мавирет |
210563.00 |
Мавирет — инструкция по применению
Синонимы, аналоги
Статьи
РЕГИСТРАЦИОННЫЙ НОМЕР
ЛП-004804
ТОРГОВОЕ НАИМЕНОВАНИЕ
Мавирет
МЕЖДУНАРОДНОЕ НЕПАТЕНТОВАННОЕ ИЛИ ГРУППИРОВОЧНОЕ НАИМЕНОВАНИЕ
Глекапревир + Пибрентасвир
ЛЕКАРСТВЕННАЯ ФОРМА
Таблетки, покрытые пленочной оболочкой
СОСТАВ
Действующие вещества: глекапревир 100.0 мг, пибрентасвир 40.0 мг
Вспомогательные вещества: коповидон К 28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия. натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadryu II 32F240023)’. гипромеллоза 2910. лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
ОПИСАНИЕ
Продолговатые двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета с гравировкой «NXT» на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА
Противовирусное средство
КОД ATX
Не присвоен.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Механизм действия
Препарат Мавирет — это комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах — глекапрсвира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Глекапревир
Глекапревир представляет собой ингибитор протеазы вируса гепатита С (ВГС) NS3/4A. которая необходима для протеолитического расщепления кодирующего вирус гепатита С полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A, и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз вируса гепатита С NS3/4A из клинических изолятов вируса генотипов la, lb, 2а, 2Ь, За, 4а. 5а и 6а со значениями IC50 от 3,5 до 11,3 нМ.
Пибрентасвир
Пибрентасвир является пангенотипным ингибитором белка NS5A вируса гепатита С, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная иктивностъ
Значения ЕС5о глекапрсвира и пибрентасвира против полноразмерных или гибридных репликонов. кодирующих NS3 или NS5A из лабораторных штаммов, представлены в таблице 1.
Таблица 1. Активность глекапрсвира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
|
Подтип ВГС |
ЕС50 глекапрсвира, нМ |
ЕС50 пибрентасвира, нМ |
|
1а |
0.85 |
0,0018 |
|
lb |
0.94 |
0,0043 |
|
2а |
2,2 |
0,0023 |
|
2Ь |
4,6 |
0,0019 |
|
За |
1,9 |
0,0021 |
|
4а |
2.8 |
0,0019 |
|
5а |
Н/П |
0,0014 |
|
6а |
0.86 |
0,0028 |
Н/П — неприменимо.
Значения ЕС50 глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в таблице 2.
Таблица 2. Активность глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1-6
Н/П — неприменимо.
Активность in vitro
Оценка комбинации глекапрсвира и пибрентасвира на репликонных клеточных культурах генотипа ВГС 1 не выявила каких-либо признаков антагонизма противовирусной активности. Резистентность
В культуре клеток
Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A. выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54. 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапрсвира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1-4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе За, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58. 92 или 93 в NS5A в генотипах 1-6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе За замены в аминокислотах А30К или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и За (включая A30K+Y93H в генотипе За) демонстрируют снижение чувствительности к пибрентасвиру. Применение у детей
Нет данных о применении препарата у детей.
Применение у пациентов пожилого возраста
В клинические исследования препарата Мавирет были включены 328 пациентов в возрасте 65 лет и старте (13,8% от общего числа пациентов). Частота достижения вирусологического ответа в группе пациентов в возрасте > 65 лет была аналогична таковой у пациентов в возрасте < 65 лет.
Фармакокинетика
Фармакокинетические свойства компонентов препарата Мавирет представлены в таблице 3.
|
Таблица 3. Фармакокинетические свойства компонентов препарата Мавирет у здоровых добровольцев |
||||||||||||||||||||||||||||||||||||||||||
|
a. Медиана Ттах у здоровых добровольцев после приема однократной дозы глекапрсвира и пибрентасвира
b. Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров
c. Прием однократной дозы [14С] глекапрсвира или [|4С] пибрентасвира в исследованиях массового баланса
d. Окислительные метаболиты или их продукты обмена составляли 26 % радиоактивной дозы. Метаболиты глекапрсвира в плазме нс наблюдались.
У пациентов с хроническим гепатитом С без цирроза, после 3 дней монотерапии либо только глекапревиром 300 мг в день (N=6) или только пибрентасвиром 120 мг в день (N=8), геометрическое среднее значения AUC24 составило 13600 нг-ч/мл для глекапрсвира и 459 нг-ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекресного взаимодействия между глекапревиром и пибрентасвиром. Основываясь на популяционной фармакокинетической модели для препарата Мавирет при хроническом гепатите С, установившиеся значения AUC24 для глекапрсвира и пибрентасвира были 4800 и 1430 нг-ч/мл у пациентов без цирроза (N=1804), и 10500 и 1530 нг-ч/мл у пациентов с циррозом печени (N=280), соответственно. По сравнению со здоровыми пациентами (N=230), популяционные оценки AUC24, ss были аналогичны (разница в 10%) для глекапрсвира и на 34 % ниже для пибрентасвира у пациентов, инфицированных вирусом гепатита С без цирроза.
Линейность / нелинейность
AUC глекапрсвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы (при приеме 1200 мг один раз в день, наблюдалась в 516 раз больше экспозиция, чем 200 мг один раз в день). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы до 120 мг (120 мг один раз в день наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг один раз в день), но установленная линейная фармакокинетика в дозах > 120 мг. Нелинейное увеличение экспозиции <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром составляет в 3 раза выше по сравнению с применением только пибрентасвира. У глекапрсвира наблюдалось меньшее влияние пибрентасвира.
Особые группы пациентов
Раса/этническая принадлежность
Не требуется коррекция дозы препарата Мавирет в зависимости от расы или этнической принадлежности.
Пол/масса тела
Не требуется коррекция дозы препарата Мавирет в зависимости от пола или массы тела. Пациенты пожилого возраста
У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется. Популяционный фармакокинетический анализ ВГС-инфицированных пациентов в возрасте от 18 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапрсвира и пибрентасвира.
Пациенты с нарушением почечной функции
Значение AUC глекапрсвира и пибрентасвира повышалось не более, чем на 56 % у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с пациентами с нормальной функцией почек. Значение AUC глекапрсвира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница <18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапрсвира на 86 % выше, а пибрентасвира на 54 % выше, чем у
пациентов с нормальной функцией почек. Мри оценке концентраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
В целом, изменения воздействия препарата Мавирет у ВГС-инфицированных пациентов с нарушением функции почек на диализе или без него, не были клинически значимыми. Пациенты с печеночной недостаточностью
Мри приеме рекомендованнной дозы значение AUC глекапрсвира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Мью было на 33 % выше, класса 13 — на 100% выше, а класса С — в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени. Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26 % выше у пациентов с печеночной недостаточностью класса В и на 114% — класса С. При оценке концетраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема препарата Мавирет пациентами с ВГС и компенсированным циррозом печени, воздействие глекапрсвира было примерно в 2 раза выше, а пибрентасвира — аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапрсвира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Показания к применению
Лечение хронического гепатита С у взрослых.
Противопоказания
• Повышенная чувствительность к любому действующему веществу препарата или к
любому из вспомогательных веществ.
• Пациенты с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью), см.
разделы «Способ применения и дозы» и «Фармакокинетика».
• Совместное применение со следующими препаратами: атазанавир. аторвастатин,
симвастатин, дабигатрана этексилат, препараты, содержащие эстрадиол, сильными индукторами Р-гликопротеина и CYP3A, например, рифампицин, карбамазепин, препараты зверобоя продырявленного Hypericum perjoratum, фенобарбитал, фенитоин, примидон, (см. раздел «Взаимодействие с другими лекарственными средствами»).
• Детский возраст до 18 лет.
• Дефицит лактазы, недостаточность лактозы, глюкозо-галактозная мальабсорбция.
С ОСТОРОЖНОСТЬЮ
Препарат Мавирет не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг в день).
Препарат Мавирет следует применять с осторожностью со следующими препаратами: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ Беременность
Данные о применении глекапрсвира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности. Исследования глекапрсвира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапрсвира. что исключило возможность дальнейших исследований. В качестве меры предосторожности, препарат Мавирет не рекомендуется применять во время беременности.
Период грудного вскармливания
Неизвестно, выделяется ли глекапревир или пибрентасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапрсвира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию препаратом Мавирет или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины. Фертильность
Исследования влияния глекапрсвира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапрсвира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз препаратов.
Способ применения и дозы
Для приема внутрь.
1аблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать. Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С.
Дозы
Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг (три таблетки по 100 мг/40 мг) один раз в сутки во время еды.
В таблицах 1 и 2 представлена рекомендуемая продолжительность лечения препаратом Мавирет на основе данных, полученных на популяции пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. с компенсированным циррозом печени или без него.
|
Таблица 1. Рекомендованная продолжительность лечения для пациентов, ранее не получавших лечение |
||||||||
|
|
Таблица 2. Рекомендованная продолжительность лечения для пациентов, не ответивших на предыдущую терапию пегилированным интерфероном (пег-ИНФ) + рибавирнн (совместно с софосбувиром или без него) или софосбувир + рибавирин |
|||||||||||
|
|||||||||||
|
Для пациентов, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A см информацию в разделе «Особые указания». |
Пропуск приема препарата
В случае пропуска приема препарата Мавирет его можно осуществить в течение 18 часов после планового времени приема. Если с момента планового времени приема препарата Мавирет прошло более 18 часов, не следует принимать пропущенную дозу, а следующую дозу следует принять в обычное время по расписанию. Не следует принимать двойную дозу препарата.
Если в течение 3 часов после приема препарата Мавирет произошла рвота, то необходимо принять дополнительную дозу препарата. Если рвота произошла позднее 3 часов после применения препарата Мавирет, то прием дополнительной дозы не требуется.
Применение у пациентов пожилого возрасти
У пожилых пациентов коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушенной функцией почек
У пациентов почечной недостаточности, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушением функции печени
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата Мавирет не требуется. Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью) (см. разделы «Противопоказания», «Особые указания»). Дети
Отсутствуют данные о безопасности и эффективности применения препарата Мавирет у детей и подростков в возрасте до 18 лет.
Пациенты после трансплантации печени
Пациентам после трансплантации печени препарат Мавирет необходимо применять в течение как минимум 12 недель (см. раздел «Особые указания»).
Следует рассмотреть увеличение продолжительности терапии (в течение 16 недель) у пациентов с генотипом 3, которые ранее получали терапию пег-ИФН + рибавирин (совместно с софосбувиром или без него) или софосбувир + рибавирин.
Пациенты с ко-инфекцией ВГС/ВИЧ-1
Следует выполнять рекомендации, указанные в Таблице 1 и 2. Рекомендации по дозированию препарата Мавирет при совместном применении с препаратами для терапии ВИЧ-1 представлены в разделе «Взаимодействие с другими лекарственными средствами».
Побочное действие
Резюме профиля безопасности
Оценка безопасности препарата Мавирет у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам исследований фазы 2 и 3, в которых участвовали около 2 300 пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. получавших Мавирет в течение 8, 12 или 16 недель.
Наиболее частыми нежелательными реакциями (частота > 10 %) были головные боли и утомляемость. Менее чем у 0,1 % пациентов, получавших лечение препаратом Мавирет, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение препаратом Мавирет по причине развития нежелательных реакций, составила 0.1 %. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Таблица нежелательных реакций
Сообщалось о развитии следующих нежелательных реакций у пациентов, получавших лечение препаратом Мавирет. Ниже приведен список нежелательных реакций, сгруппированных согласно классу систем органов и по частоте встречаемости. Частота встречаемости определяется следующим образом: очень часто (> 1/10), часто (от >1/100 до < 1/10), нечасто (от > 1/1 000 до < 1/100), редко (от >1/10 000 до < 1/1 000) и очень редко (< 1/10 000).
Таблица 1. Нежелательные реакции, наблюдавшиеся при приеме препарата Мавирет
|
Частота развития |
Нежелательные реакции |
|
Нарушения со стороны нервной системы |
|
|
Очень часто |
Головная боль |
|
Нарушения со стороны желудочно-кишечного тракта |
|
|
Часто |
Тошнота, диарея |
|
Общие нарушения и реакции в месте введения |
|
|
Очень часто |
Утомляемость |
|
Часто |
Астения |
Описание отдельных нежелательных реакций
Нежелательные реакции у пациентов с тяжелым нарушением функции почек, включая пациентов на диализе
Безопасность препарата Мавирет у пациентов с хронической болезнью почек (стадия 4 или стадия 5, включая пациентов на диализе) и хронической инфекцией, вызванной вирусом гепатита С генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него) была оценена на 104 пациентах. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17 %) и утомляемость (12 %).
Оценка безопасности у пациентов с коинфекцией ВГС/ВИЧ-1
Общий профиль безопасности у пациентов с коинфекцией ВГС/ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови
У 1,3 % пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше верхней границы нормы, что было связано с глекапревир-опосредованным ингибированием белков-переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ. Прямая гипербилирубинемия наблюдалась у 0,3 % пациентов.
ПЕРЕДОЗИРОВКА
Наибольшая задокументированная доза, принятая здоровыми добровольцами, составила 1200 мг один раз в день в течение 7 дней для глекапрсвира и 600 мг один раз в день в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5 раз ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапрсвира (700 мг или 800 мг) 1 раз в день в течение > 7 дней. В случае передозировки, необходимо контролировать состояние пациента на наличие признаков токсического поражения (см. раздел «Побочное действие»). Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапрсвира и пибрентасвира.
Взаимодействие с другими лекарственными препаратами
Возможное влияние препарата Мавирет на другие лекарственные препараты
Глекапревир и пибрентасвир — это ингибиторы Р-гликопротеина (P-GP), белка резистентности рака молочной железы (BCRP) и полипептида, транспортирующего органические анионы (ОАТР) 1В1/3.
Одновременное применение с препаратом Мавирет может привести к повышению концентрации в плазме препаратов, являющихся субстратами Р-гликопротеина (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или ОАТР1В1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). См. рекомендации по лекарственному взаимодействию с чувствительными субстратами Р-гликопротеина, BCRP и ОАТР1В1/3 в таблице 1. Для других субстратов Р-гликопротеина. BCRP и ОАТР1В1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир — это слабые ингибиторы изоферментов системы цитохрома Р450 CYP3A и уридин-глюкуронозилтрансферазы (UGT) 1А1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1AI (ралгегравир) при одновременном приеме с препаратом Мавирет.
Применение глекапрсвира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1A2, CYP2C9, CYP2C19, CYP2D6. UGT1А6, UGT1А9. UGT1А4, UGT2B7, OCTI, ОСТ2, ОАТ1, ОАТЗ, МАТЕ1 и МАТЕ2К.
Пациенты, получающие антагонисты витамина К
На фоне лечения препаратом Мавирет может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг международного нормализованного отношения (МНО). Потенциальное влияние других лекарственных препаратов на препарат Мавирет
Совместный прием с сильными индукторами Р-гликопротеина/СУРЗА
Лекарственные препараты, являющиеся сильными индукторами Р-гликопротеина и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон), могут вызвать существенное снижение концентрации глекапрсвира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта препарата Мавирет и потере вирусологического ответа. Применение таких препаратов одновременно с препаратом Мавирет противопоказано (см. раздел «Противопоказания»).
Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются умеренными индукторами Р-гликопротеина и CYP3A, может вызвать снижение концентрации глекапрсвира и пибрентасвира в плазме крови (окскарбазепин. эсликарбазепин, лумакафтор. кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. раздел «Особые указания»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков Р-гликопротеина и (или) BCRP. Глекапревир также является субстратом транспортеров печеночного захвата ОАТР1В1/3. Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются ингибиторами Р-гликопротеина и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир), может замедлить выведение глекапрсвира и пибрентасвира и может вызвать повышение экспозиции противовирусных препаратов в плазме крови. Лекарственные препараты, являющиеся ингибиторами ОАТР1В1/3 (элвитегравир. циклоспорин, дарунавир. лоиинавир), могут вызвать повышение системной концентрации глекапрсвира.
Установленные и другие потенциально возможные лекарственные взаимодействия
В таблице 1 приведено влияние отношения средних значений, вычисленных методом наименьших квадратов (90-процентный доверительный интервал) на концентрацию препарата Мавирет и сопутствующих лекарственных препаратов. Направление стрелки указывает направление изменения воздействия (Сmax и AUC) глекапрсвира, пибрентасвира и сопутствующего лекарственного препарата ( ↑—увеличение более чем на 25 %, ↓ — снижение более чем на 20 %, ↔ — нет изменения (снижение на менее или равно 20 % или увеличение на менее или равно 25 %).
Таблица 1. Взаимодействия между препаратом Мавирет и другими лекарственными средствами
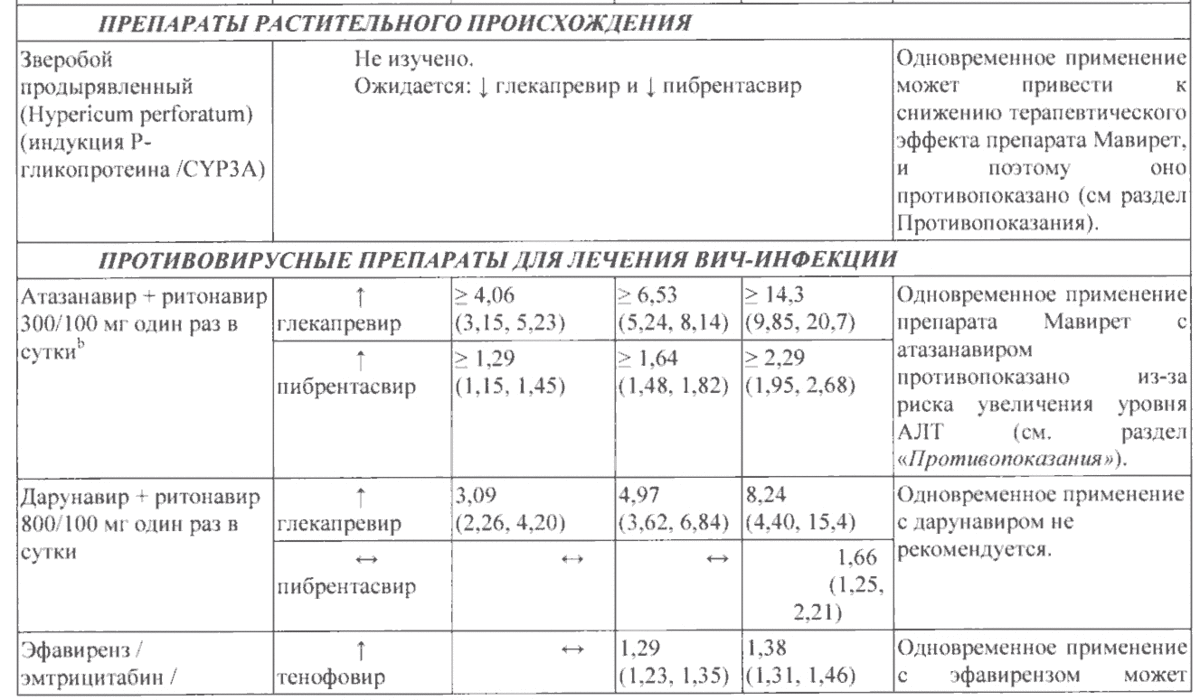


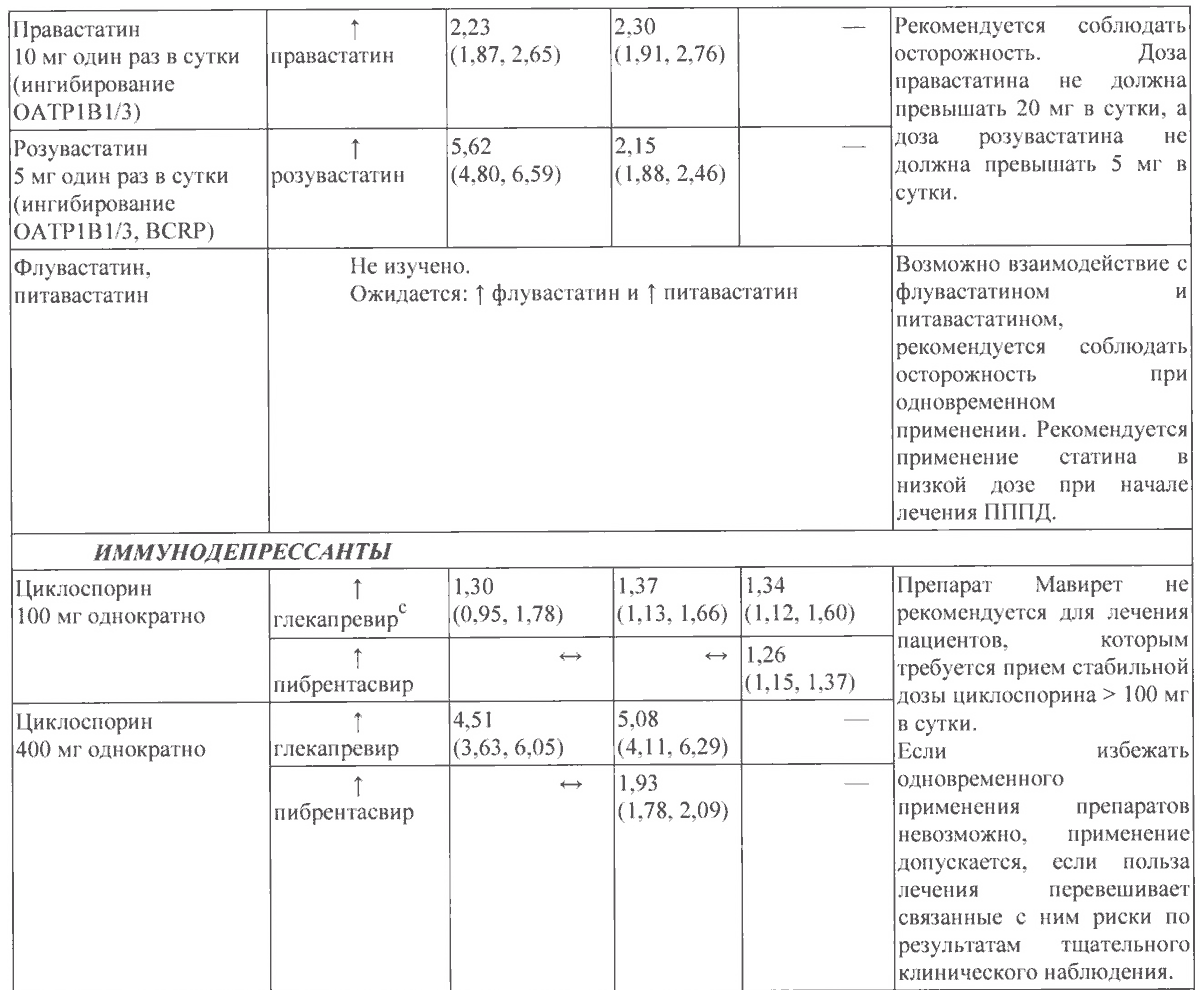

Г1ППД — противовирусный препарат прямого действия
a. Влияние рифампицина на глекапревир и пибрентасвир через 24 часа после приема последней дозы рифампицина.
b. Указано влияние атазанавира и ритонавира на первую дозу глекапрсвира и пибрентасвира.
c. Экспозиция глекапрсвира у инфицированных ВГС пациентов после трансплантации, получавших циклоспорин в дозе 100 мг в сутки или меньше, была в 4 раза выше, чем у тех. кто нс получал циклоспорин.
Дополнительные исследования межлекарственного взаимодействия проводились со следующими лекарственными препаратами: абакавир. амлодипин, бупренорфин, кофеин, декстрометорфан, долутегравир. эмтрицитабин. фелодипин. ламивудин. ламотриджин, метадон, мидазолам. налоксон, норэтиндрон или другие контрацептивные средства, содержащие прогестин, рилпивирин, тенофовир алафенамид и толбутамид. Клинически значимого взаимодействия не выявлено.
ОСОБЫЕ УКАЗАНИЯ
Реактивация вирусного гепатита В
Во время лечения противовирусными препаратами прямого действия сообщалось о реактивации вируса гепатита В, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие ВГВ. Пациенты с коинфекцией ВГВ/ВГС подвержены риску реактивации ВГВ. поэтому следует проводить их мониторинг и ведение с соблюдением современных рекомендаций.
Пациенты после трансплантации печени
Безопасность и эффективность применения препарата Мавирет у пациентов, перенесших трансплантацию печени, не оценивались. Лечение препаратом Мавирет в соответствии с рекомендованным способом применения и дозами (см. раздел «Способ применения и дозы») должно основываться на оценке потенциальной пользы и рисков для каждого конкретного пациента.
Нарушение функции печени
Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. разделы «Способ применения и дозы», «Противопоказания»).
Пациенты, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A
Была изучена вероятность развития устойчивости к глекапревиру/пибрентасвиру у пациентов, инфицированных вирусом генотипа 1, и ограниченного количества пациентов, инфицированных вирусом генотипа 4, не ответивших на предшествующую схему терапии. Как и ожидалось, риск неудачи терапии был выше у пациентов с предшествующей терапией включающей оба класса препаратов (ингибиторы NS5A и NS3/4A). Методика для прогнозирования неудачи терапии на основе исходных данных об устойчивости к терапии не определена. Развитие устойчивости к обоим классам препаратов было основной находкой у пациентов, не ответивших на терапию глекапревиром/пибрентасвиром. Данные о повторном лечении пациентов, инфицированных вирусом генотипов 2, 3, 5 и 6, отсутствуют. Применение препарата Мавирет не рекомендуется для повторного лечения пациентов, ранее получавших лечение ингибиторами NS3/4A и/или NS5A.
Взаимодействие с другими лекарственными препаратами
Подробную информацию см. в разделе «Взаимодействие с другими лекарственными средствами».
Влияние на способность управлять транспортных средствами, механизмами
Препарат Мавирет не оказывает влияния или оказывает незначительное влияние на способность к вождению транспортных средств и управлению механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые пленочной оболочкой. 100 мг + 40 мг.
По 3 таблетки, покрытые пленочной оболочкой, в блистере из поливинилхлорид/полиэтилен/полихлоротрифторэтилена и алюминиевой фольги.
По 7 блистеров в пачке картонной, по 4 пачки картонных вместе с инструкцией по применению в пачке картонной.
СРОК годности
2 года. Не использовать после истечения срока годности, указанного на упаковке.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 25 °C.
Хранить в местах, недоступных для детей.
УСЛОВИЯ ОТПУСКА
Отпускается по рецепту.
ВЛАДЕЛЕЦ РЕГИСТРАЦИОННОГО УДОСТОВЕРЕНИЯ
ООО «ЭббВи», Россия
125047, г. Москва, ул. Лесная, д. 7, этаж 4, помещение 1
Производитель
Производитель готовой лекарственной формы
Фурнье Лэбораториз Айрлэнд Лимитед, Ирландия / Fournier Laboratories Ireland Limited, Ireland Эннгроув, Карригтвохилл, Ко. Корк, Ирландия / Anngrove, Carrigtwohill, Со. Cork. Ireland Фасовщик (первичная упаковка), упаковщик (вторичная упаковка), выпускающий контроль
качества
ЭббВи Дойчланд ГмбХ и Ко.КГ, Германия / AbbVie Deutschland GmbH & Со.KG. Germany Кыолльштрассе, 67061 Людвигсхафен, Германия / Knollstrasse. 67061 Ludwigshafen. Germany
НАИМЕНОВАНИЕ И АДРЕС ОРГАНИЗАЦИИ, УПОЛНОМОЧЕННОЙ ПРИНИМАТЬ ПРЕТЕНЗИИ НА ЛЕКАРСТВЕННЫЙ ПРЕПАРАТ
ООО «ЭббВи», Россия
125047, г. Москва, ул. Лесная, д.7,
БЦ «Белые Сады», здание «А»
тел. (495) 258 42 77
факс(495)258 42 87
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Мавирет (Mavyret) инструкция по применению
📜 Инструкция по применению Мавирет
💊 Состав препарата Мавирет
✅ Применение препарата Мавирет
📅 Условия хранения Мавирет
⏳ Срок годности Мавирет
Описание лекарственного препарата
Мавирет
(Mavyret)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2021 года.
Дата обновления: 2023.03.30
Владелец регистрационного удостоверения:
Контакты для обращений:
ЭббВи ООО
(Россия)
Код ATX:
J05AP57
(Глекапревир и пибрентасвир)
Лекарственная форма
| Мавирет |
Таб., покр. пленочной оболочкой, 100 мг+40 мг: 84 шт. рег. №: ЛП-004804 |
Форма выпуска, упаковка и состав
препарата Мавирет
Таблетки, покрытые пленочной оболочкой розового цвета, продолговатые, двояковыпуклые, с гравировкой «NXT» на одной стороне.
Вспомогательные вещества: коповидон К28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия, натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadry® II 32F240023): гипромеллоза 2910, лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
3 шт. — блистеры (7) — пачки картонные (4) — пачки картонные.
Фармакологическое действие
Механизм действия
Мавирет – комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах – глекапревира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Глекапревир
Глекапревир представляет собой ингибитор протеазы вируса гепатита С (ВГС) NS3/4A, которая необходима для протеолитического расщепления кодирующего вирус гепатита С полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз вируса гепатита С NS3/4A из клинических изолятов вируса генотипов 1a, 1b, 2a, 2b, 3а, 4а, 5а и 6а со значениями IC50 от 3.5 до 11.3 нМ.
Пибрентасвир
Пибрентасвир является пангенотипным ингибитором белка NS5A вируса гепатита С, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная активность
Значения ЕС50 глекапревира и пибрентасвира против полноразмерных или гибридных репликонов, кодирующих NS3 или NS5A из лабораторных штаммов, представлены в таблице 1.
Таблица 1. Активность глекапревира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
Н/П – неприменимо.
Значения ЕС50 глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в таблице 2.
Таблица 2. Активность глекапревира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1–6
Н/П – неприменимо.
Активность in vitro
Оценка комбинации глекапревира и пибрентасвира на репликонных клеточных культурах генотипа ВГС 1 не выявила каких-либо признаков антагонизма противовирусной активности.
Резистентность
В культуре клеток
Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A, выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54, 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапревира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1–4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе 3a, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58, 92 или 93 в NS5A в генотипах 1–6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе 3a аминокислотные замены A30K или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и 3а (включая A30K+Y93H в генотипе 3а) демонстрируют снижение чувствительности к пибрентасвиру. В репликоне генотипа 3b присутствие встречающихся в природе полиморфизмов K30 и M31 в белке NS5A снижало чувствительность к пибрентасвиру в 24 раза по сравнению с активностью пибрентасвира в репликоне генотипа 3a.
Фармакокинетика
Фармакокинетические свойства компонентов препарата Мавирет представлены в таблице 3.
Таблица 3. Фармакокинетические свойства компонентов препарата Мавирет у здоровых добровольцев
a Медиана Tmax у здоровых добровольцев после приема однократной дозы глекапревира и пибрентасвира.
b Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров.
c Прием однократной дозы [14C] глекапревира или [14C] пибрентасвира в исследованиях массового баланса.
d Окислительные метаболиты или их продукты обмена составляли 26% радиоактивной дозы. Метаболиты глекапревира в плазме не наблюдались.
У пациентов с хроническим гепатитом С без цирроза после 3 дней монотерапии либо только глекапревиром 300 мг/сут (N=6) или только пибрентасвиром 120 мг/сут (N=8) геометрическое среднее значение AUC24 составило 13600 нг×ч/мл для глекапревира и 459 нг×ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекрестного взаимодействия между глекапревиром и пибрентасвиром. Основываясь на популяционной фармакокинетической модели для препарата Мавирет при хроническом гепатите С, установившиеся значения AUC24 для глекапревира и пибрентасвира были 4800 и 1430 нг×ч/мл у пациентов без цирроза (N=1804) и 10500 и 1530 нг×ч/мл у пациентов с циррозом печени (N=280) соответственно. По сравнению со здоровыми пациентами (N=230) популяционные оценки AUC24,ss были аналогичны (разница в 10%) для глекапревира и на 34% ниже для пибрентасвира у пациентов, инфицированных вирусом гепатита С без цирроза.
Линейность/нелинейность
AUC глекапревира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы (при приеме 1200 мг 1 раз/сут наблюдалась в 516 раз больше экспозиция, чем при приеме 200 мг 1 раз/сут). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы до 120 мг (при приеме 120 мг 1 раз/сут наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг 1 раз/сут), но установленная линейная фармакокинетика в дозах ≥120 мг. Нелинейное увеличение экспозиции <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром в 3 раза выше по сравнению с применением только пибрентасвира. У глекапревира наблюдалось меньшее влияние пибрентасвира.
Фармакокинетика у особых групп пациентов
Раса/этническая принадлежность. Не требуется коррекция дозы препарата Мавирет в зависимости от расы или этнической принадлежности.
Пол/масса тела. Не требуется коррекция дозы препарата Мавирет в зависимости от пола или массы тела.
Пациенты пожилого возраста. У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется. Популяционный фармакокинетический анализ ВГС-инфицированных пациентов в возрасте от 12 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапревира и пибрентасвира.
Дети. У детей в возрасте 12 лет и старше коррекция дозы препарата Мавирет не требуется. Содержание глекапревира и пибрентасвира в плазме крови у детей было сопоставимо с таковым у взрослых в исследованиях фазы 2/3. Фармакокинетика глекапревира и пибрентасвира не изучалась у детей в возрасте до 12 лет.
Пациенты с нарушением функции почек. Значение AUC глекапревира и пибрентасвира повышалось не более чем на 56% у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с пациентами с нормальной функцией почек. Значение AUC глекапревира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница ≤18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапревира на 86% выше, а пибрентасвира на 54% выше, чем у пациентов с нормальной функцией почек. При оценке концентраций глекапревира и пибрентасвира, не связанных с белками плазмы, может наблюдаться более выраженный рост AUC. В целом, изменения воздействия препарата Мавирет у ВГС-инфицированных пациентов с нарушением функции почек на диализе или без него не были клинически значимыми.
Пациенты с печеночной недостаточностью. При приеме в рекомендуемой дозе значение AUC глекапревира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью было на 33% выше, класса B – на 100% выше, а класса С – в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени. Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26% выше у пациентов с печеночной недостаточностью класса B и на 114% – класса С. При оценке концентраций несвязанных глекапревира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема препарата Мавирет пациентами с ВГС и компенсированным циррозом печени воздействие глекапревира было примерно в 2 раза выше, а пибрентасвира – аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапревира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Взаимодействие с другими лекарственными препаратами
Были проведены исследования взаимодействия глекапревира/пибрентасвира с другими лекарственными препаратами, которые могут вступать во взаимодействия с глекапревиром/пибрентасвиром и препаратами, которые часто применяются в исследованиях фармакокинетического взаимодействия. В таблицах 4 и 5 ниже представлены фармакокинетические эффекты при взаимодействии глекапревира/пибрентасвира с другими лекарственными препаратами, которые показали потенциальные клинически значимые изменения.
Таблица 4. Лекарственное взаимодействие: изменения фармакокинетических параметров глекапревира (ГЛЕ) или пибрентасвира (ПИБ) в присутствии одновременно назначаемого лекарственного препарата
↔ = без изменений (соотношение центральных значений от 0.80 до 1.25).
a Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
b У пациентов после трансплантации печени, инфицированных ВГС, которые получали лечение циклоспорином в дозе 100 мг/сут или менее, экспозиция глекапревира была в 2.4 раза выше по сравнению с пациентами, которые не принимали циклоспорин.
c Было отмечено влияние атазанавира и ритонавира на концентрацию глекапревира и пибрентасвира после приема первой дозы глекапревира и пибрентасвира.
Таблица 5. Лекарственное взаимодействие: фармакокинетические параметры для совместно применяемого препарата при одновременном применении с глекапревиром/пибрентасвиром
↔ = без изменений (соотношение центральных значений от 0.80 до 1.25).
Показания препарата
Мавирет
- лечение хронического гепатита С у взрослых и детей с 12 лет.
Режим дозирования
Для приема внутрь.
Таблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать.
Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С.
Взрослые и дети в возрасте от 12 лет
Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг в один прием (3 таб. по 100 мг/40 мг) 1 раз/сут.
В таблицах 6 и 7 представлена рекомендуемая продолжительность лечения препаратом Мавирет на основе данных, полученных на популяции пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6, с компенсированным циррозом печени или без него.
Таблица 6. Рекомендуемая продолжительность лечения для пациентов, ранее не получавших лечение
Таблица 7. Рекомендуемая продолжительность лечения для пациентов, не ответивших на предыдущую терапию
1 В клинических исследованиях пациенты получали предшествующую терапию, содержащую ледипасвир и софосбувир или даклатасвир с пегилированным интерфероном и рибавирином.
2 В клинических исследованиях пациенты получали предшествующую терапию, содержащую симепревир и софосбувир, или симепревир, боцепревир, или телапревир с пегилированным интерфероном или рибавирином.
Пропуск приема препарата
В случае пропуска приема препарата Мавирет его можно осуществить в течение 18 ч после планового времени приема. Если с момента планового времени приема препарата Мавирет прошло более 18 ч, не следует принимать пропущенную дозу, а следующую дозу следует принять в обычное время по расписанию. Не следует принимать двойную дозу препарата.
Если в течение 3 ч после приема препарата Мавирет произошла рвота, необходимо принять дополнительную дозу препарата. Если рвота произошла позднее 3 ч после применения препарата Мавирет, прием дополнительной дозы не требуется.
Особые группы пациентов
У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется.
У пациентов с почечной недостаточностью, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата Мавирет не требуется. Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью).
У детей в возрасте 12 лет и старше коррекция дозы не требуется. Отсутствуют данные о безопасности и эффективности применения препарата Мавирет у детей в возрасте до 12 лет.
Пациенты после трансплантации печени или почки
Пациенты после трансплантации печени или почки могут применять препарат Мавирет в течение 12 недель (см. раздел «Особые указания»). В случае если пациенту назначена более длительная терапия (в течение 16 недель), и во время терапии была проведена трансплантация печени, то 16-недельный курс лечения должен быть доведен до конца.
Пациенты с ко-инфекцией ВГС/ВИЧ-1
Следует выполнять рекомендации, указанные в Таблицах 6 и 7. Рекомендации по дозированию препарата Мавирет при совместном применении с препаратами для терапии ВИЧ-1 представлены в разделе «Лекарственное взаимодействие».
Побочное действие
Резюме профиля безопасности
Оценка безопасности препарата Мавирет у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам регистрационных исследований фазы 2 и 3, в которых участвовали около 2300 взрослых пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6, получавших Мавирет в течение 8, 12 или 16 недель.
Наиболее частыми нежелательными реакциями (частота ≥10%) были головные боли и утомляемость. Менее чем у 0.1% пациентов, получавших лечение препаратом Мавирет, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение препаратом Мавирет по причине развития нежелательных реакций, составила 0.1%. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Таблица нежелательных реакций
У пациентов, получавших лечение препаратом Мавирет, сообщалось о развитии нежелательных реакций, представленных ниже. Список нежелательных реакций сгруппирован согласно классу систем органов и по частоте встречаемости. Частота встречаемости определяется следующим образом: очень часто (>1/10), часто (от >1/100 до <1/10), нечасто (от >1/1000 до <1/100), редко (от >1/10000 до <1/1000) и очень редко (<1/10000).
Таблица 8. Нежелательные реакции, наблюдавшиеся при приеме препарата Мавирет
Описание отдельных нежелательных реакций
Нежелательные реакции у взрослых пациентов с тяжелым нарушением функции почек, включая пациентов на диализе
Безопасность препарата Мавирет у пациентов с хронической болезнью почек (стадия 4 или стадия 5, включая пациентов на диализе) и хронической инфекцией, вызванной вирусом гепатита С генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него) оценивалась у 104 пациентов. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17.3%) и утомляемость (11.5%).
Нежелательные реакции у взрослых пациентов после трансплантации почек или печени
Безопасность препарата Мавирет оценивалась у 100 пациентов после трансплантации печени или почек, инфицированных вирусом гепатита С генотипами 1, 2, 3, 4 или 6 без цирроза печени. Общий профиль безопасности у пациентов после трансплантации печени или почек был сопоставим с профилем безопасности у пациентов в исследованиях 2 и 3 фазы. Наблюдались следующие нежелательные реакции с частотой равной или более 5% у пациентов, принимавших Мавирет в течение 12 недель: головная боль (17%), усталость (16%), тошнота (8%) и зуд (7%). У 81% пациентов, принимавших препарат Мавирет, отмечались нежелательные реакции легкой степени тяжести. У 2% пациентов наблюдались серьезные нежелательные реакции. Не было ни одного случая полной отмены препарата из-за нежелательных реакций.
Оценка безопасности у взрослых пациентов с ко-инфекцией ВГС/ВИЧ-1
Общий профиль безопасности у пациентов с ко-инфекцией ВГС/ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови
У 1% пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше ВГН, что было связано с глекапревир-опосредованным ингибированием белков-переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ.
Нежелательные реакции у детей
Безопасность препарата Мавирет у детей, инфицированных ВГС генотипов 1-6, оценивалась в открытом исследовании 2/3 фазы с участием 47 пациентов в возрасте от 12 до 18 лет, получавших терапию в течение 8-16 недель. Нежелательные реакции, зафиксированные в ходе данного исследования, были сопоставимы с реакциями, наблюдаемыми у взрослых пациентов (см. таблицу 8).
Пострегистрационные данные
В результате пострегистрационного наблюдения при применении препарата Мавирет были выявлены нежелательные реакции. Т.к. данные реакции были получены добровольно от неопределенной группы пациентов, установить частоту этих реакций или их связь с приемом препарата Мавирет не представляется возможным.
Нарушения со стороны иммунной системы: ангионевротический отек.
Нарушения со стороны кожи и подкожно-жировой клетчатки: зуд.
Противопоказания к применению
- повышенная чувствительность к любому действующему веществу препарата или к любому из вспомогательных веществ;
- пациенты с тяжелой печеночной недостаточностью (класс C по шкале Чайлд-Пью);
- совместное применение со следующими препаратами: атазанавир, аторвастатин, симвастатин, дабигатрана этексилат, препаратами, содержащими эстрадиол, сильными индукторами Р-гликопротеина и CYP3A, например, рифампицин, карбамазепин, препараты зверобоя продырявленного (Hypericum perforatum), фенобарбитал, фенитоин, примидон;
- детский возраст до 12 лет;
- дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция.
С осторожностью
Препарат Мавирет не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг/сут).
Препарат Мавирет следует применять с осторожностью со следующими препаратами: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
Применение при беременности и кормлении грудью
Беременность
Данные о применении глекапревира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности.
Исследования глекапревира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапревира, что исключило возможность дальнейших исследований. В качестве меры предосторожности, препарат Мавирет не рекомендуется применять во время беременности.
Период грудного вскармливания
Неизвестно, выделяются ли глекапревир или пибрентасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапревира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию препаратом Мавирет или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины.
Фертильность
Исследования влияния глекапревира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапревира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз препаратов.
Применение при нарушениях функции печени
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата не требуется.
Препарат не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью).
Применение при нарушениях функции почек
У пациентов с почечной недостаточностью, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
Применение у детей
Противопоказано применение препарата в детском возрасте до 12 лет.
Применение у пожилых пациентов
У пациентов пожилого возраста коррекция дозы препарата не требуется.
Особые указания
Реактивация вирусного гепатита В
Во время лечения противовирусными препаратами прямого действия сообщалось о реактивации вируса гепатита B, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие ВГВ. Пациенты с ко-инфекцией ВГВ/ВГС подвержены риску реактивации ВГВ, поэтому следует проводить их мониторинг и ведение с соблюдением современных рекомендаций.
Потенциальные эффекты полной элиминации ВГС из организма препаратами прямого противовирусного действия
У пациентов может наблюдаться улучшение функционирования печени в результате лечения ХВГС, выражающееся в улучшении метаболизма глюкозы в печени. Для пациентов с сахарным диабетом это означает улучшение показателей концентрации глюкозы в крови. Редкие случаи симптоматической гипогликемии были зарегистрированы в рамках терапии препаратами прямого противовирусного действия, поэтому у пациентов с сахарным диабетом рекомендуется проводить тщательный мониторинг концентрации глюкозы в крови для определения целесообразности коррекции доз гипогликемических препаратов.
Нарушение функции печени
Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс B по шкале Чайлд-Пью) и противопоказан пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. разделы «Режим дозирования», «Противопоказания»).
Взаимодействие с другими лекарственными препаратами
Подробную информацию см. в разделе «Лекарственное взаимодействие».
Влияние на способность к управлению транспортными средствами и механизмами
Препарат Мавирет не оказывает влияния или оказывает незначительное влияние на способность к вождению транспортными средствами и управлению механизмами.
Передозировка
Наибольшая задокументированная доза, принятая здоровыми добровольцами, составила 1200 мг 1 раз/сут в течение 7 дней для глекапревира и 600 мг 1 раз/сут в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5 раз ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапревира (700 мг или 800 мг) 1 раз/сут в течение ≥7 дней.
Лечение: в случае передозировки необходимо контролировать состояние пациента на наличие признаков токсического поражения (см. раздел «Побочное действие»). Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапревира и пибрентасвира.
Лекарственное взаимодействие
Возможное влияние препарата Мавирет на другие лекарственные препараты
Глекапревир и пибрентасвир – ингибиторы Р-гликопротеина (P-GP), белка резистентности рака молочной железы (BCRP) и полипептида, транспортирующего органические анионы (OATP) 1B1/3.
Одновременное применение с препаратом Мавирет может привести к повышению концентрации в плазме препаратов, являющихся субстратами Р-гликопротеина (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или OATP1B1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). См. рекомендации по лекарственному взаимодействию с чувствительными субстратами P-гликопротеина, BCRP и OATP1B1/3 в таблице 9. Для других субстратов P-гликопротеина, BCRP и OATP1B1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир – слабые ингибиторы изоферментов системы цитохрома P450 CYP3A и уридинглюкуронозилтрансферазы (UGT) 1A1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1A1 (ралтегравир) при одновременном приеме с препаратом Мавирет.
Применение глекапревира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1A2, CYP2C9, CYP2C19, CYP2D6, UGT1A6, UGT1A9, UGT1A4, UGT2B7, OCT1, OCT2, OAT1, OAT3, MATE1 и MATE2K.
Пациенты, получающие антагонисты витамина К
На фоне лечения препаратом Мавирет может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг МНО.
Потенциальное влияние других лекарственных препаратов на препарат Мавирет
Совместный прием с сильными индукторами P-гликопротеина/CYP3A
Лекарственные препараты, являющиеся сильными индукторами P-гликопротеина и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон), могут вызвать существенное снижение концентрации глекапревира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта препарата Мавирет и потере вирусологического ответа. Применение таких препаратов одновременно с препаратом Мавирет противопоказано.
Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются умеренными индукторами P-гликопротеина и CYP3A, может вызвать снижение концентрации глекапревира и пибрентасвира в плазме крови (окскарбазепин, эсликарбазепин, лумакафтор, кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. раздел «Особые указания»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков P-гликопротеина и/или BCRP. Глекапревир также является субстратом транспортеров печеночного захвата OATP1B1/3. Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются ингибиторами P-гликопротеина и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир), может замедлить выведение глекапревира и пибрентасвира и может вызвать повышение экспозиции противовирусных препаратов в плазме крови. Лекарственные препараты, являющиеся ингибиторами OATP1B1/3 (элвитегравир, циклоспорин, дарунавир, лопинавир), могут вызвать повышение системной концентрации глекапревира.
Установленное и другое потенциально возможное лекарственное взаимодействие
В таблице 9 приведено влияние отношения средних значений, вычисленных методом наименьших квадратов (90-процентный доверительный интервал) на концентрацию препарата Мавирет и сопутствующих лекарственных препаратов. Направление стрелки указывает направление изменения воздействия (Cmax и AUC) глекапревира, пибрентасвира и сопутствующего лекарственного препарата (↑ – увеличение более чем на 25%, ↓ – снижение более чем на 20%, ↔ – нет изменения (снижение на ≤20% или увеличение на ≤25%).
Таблица 9. Взаимодействие между препаратом Мавирет и другими лекарственными средствами
ПППД — препарат прямого противовирусного действия.
a Влияние рифампицина на глекапревир и пибрентасвир через 24 ч после приема последней дозы рифампицина.
b Указано влияние атазанавира и ритонавира на первую дозу глекапревира и пибрентасвира.
c Экспозиция глекапревира у инфицированных ВГС пациентов после трансплантации, получавших циклоспорин в дозе 100 мг/сут или меньше, была в 4 раза выше, чем у тех, кто не получал циклоспорин.
Дополнительные исследования межлекарственного взаимодействия проводились со следующими лекарственными препаратами: абакавир, амлодипин, бупренорфин, кофеин, декстрометорфан, долутегравир, эмтрицитабин, фелодипин, ламивудин, ламотриджин, метадон, мидазолам, налоксон, норэтиндрон или другие контрацептивные средства, содержащие прогестин, рилпивирин, тенофовира алафенамид и толбутамид. Клинически значимого взаимодействия не выявлено.
Условия хранения препарата Мавирет
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Мавирет
Срок годности — 3 года. Не применять после истечения срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ЭББВИ ООО
(Россия)

|
|
125196 Москва, ул. Лесная, д. 7 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Мавирет — инструкция по применению
РЕГИСТРАЦИОННЫЙ НОМЕР
ЛП-004804
ТОРГОВОЕ НАИМЕНОВАНИЕ
Мавирет
МЕЖДУНАРОДНОЕ НЕПАТЕНТОВАННОЕ ИЛИ ГРУППИРОВОЧНОЕ НАИМЕНОВАНИЕ
Глекапревир + Пибрентасвир
ЛЕКАРСТВЕННАЯ ФОРМА
Таблетки, покрытые пленочной оболочкой
СОСТАВ
Действующие вещества: глекапревир 100.0 мг, пибрентасвир 40.0 мг
Вспомогательные вещества: коповидон К 28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия. натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadryu II 32F240023)’. гипромеллоза 2910. лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
ОПИСАНИЕ
Продолговатые двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета с гравировкой «NXT» на одной стороне.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА
Противовирусное средство
КОД ATX
Не присвоен.
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Механизм действия
Препарат Мавирет — это комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах — глекапрсвира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Глекапревир
Глекапревир представляет собой ингибитор протеазы вируса гепатита С (ВГС) NS3/4A. которая необходима для протеолитического расщепления кодирующего вирус гепатита С полипротеина (для дальнейшего превращения в зрелые формы белков NS3, NS4A, NS4B, NS5A, и NS5B) и имеет важное значение для репликации вируса. В биохимических исследованиях глекапревир ингибировал протеолитическую активность рекомбинантных протеаз вируса гепатита С NS3/4A из клинических изолятов вируса генотипов la, lb, 2а, 2Ь, За, 4а. 5а и 6а со значениями IC50 от 3,5 до 11,3 нМ.
Пибрентасвир
Пибрентасвир является пангенотипным ингибитором белка NS5A вируса гепатита С, который необходим для репликации вирусной РНК и сборки вириона. Механизм действия пибрентасвира был изучен в ходе исследований противовирусной активности на клеточных культурах и исследований по определению характера лекарственной резистентности.
Противовирусная иктивностъ
Значения ЕС5о глекапрсвира и пибрентасвира против полноразмерных или гибридных репликонов. кодирующих NS3 или NS5A из лабораторных штаммов, представлены в таблице 1.
Таблица 1. Активность глекапрсвира и пибрентасвира против клеточных линий репликона генотипов ВГС 1-6
|
Подтип ВГС |
ЕС50 глекапрсвира, нМ |
ЕС50 пибрентасвира, нМ |
|
1а |
0.85 |
0,0018 |
|
lb |
0.94 |
0,0043 |
|
2а |
2,2 |
0,0023 |
|
2Ь |
4,6 |
0,0019 |
|
За |
1,9 |
0,0021 |
|
4а |
2.8 |
0,0019 |
|
5а |
Н/П |
0,0014 |
|
6а |
0.86 |
0,0028 |
Н/П — неприменимо.
Значения ЕС50 глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов, представлены в таблице 2.
Таблица 2. Активность глекапрсвира и пибрентасвира против гибридных репликонов, кодирующих NS3 или NS5A из клинических изолятов вируса ВГС генотипов 1-6
Н/П — неприменимо.
Активность in vitro
Оценка комбинации глекапрсвира и пибрентасвира на репликонных клеточных культурах генотипа ВГС 1 не выявила каких-либо признаков антагонизма противовирусной активности. Резистентность
В культуре клеток
Для репликонов был проведен фенотипический анализ аминокислотных замен в белках NS3 или NS5A. выделенных в культуре клеток или значимых для класса ингибиторов.
Замены, значимые для класса ингибиторов протеазы ВГС, в положениях 36, 43, 54. 55, 56, 155, 166 или 170 в белке NS3 не оказывают влияния на активность глекапрсвира. Для генотипа 2 аминокислотные замены в NS3 в положении 168 не оказывают влияния, в то время как некоторые замены в положении 168 вызывают снижение чувствительности к глекапревиру до 55 раз (генотипы 1, 3, 4) или снижение чувствительности более чем в 100 раз (генотип 6). Некоторые замены в положении 156 вызывают снижение чувствительности к глекапревиру более чем в 100 раз (генотипы 1-4). Аминокислотные замены в положении 80 не снижают чувствительность к глекапревиру, кроме замены Q80R в генотипе За, которая снижает чувствительность к глекапревиру в 21 раз.
Единичные замены, важные для класса ингибиторов протеазы NS5A в положениях 24, 28, 30, 31, 58. 92 или 93 в NS5A в генотипах 1-6 не оказывают никакого влияния на активность пибрентасвира. Например, в генотипе За замены в аминокислотах А30К или Y93H не влияют на активность пибрентасвира. Некоторые комбинации замен в генотипах 1а и За (включая A30K+Y93H в генотипе За) демонстрируют снижение чувствительности к пибрентасвиру. Применение у детей
Нет данных о применении препарата у детей.
Применение у пациентов пожилого возраста
В клинические исследования препарата Мавирет были включены 328 пациентов в возрасте 65 лет и старте (13,8% от общего числа пациентов). Частота достижения вирусологического ответа в группе пациентов в возрасте > 65 лет была аналогична таковой у пациентов в возрасте < 65 лет.
Фармакокинетика
Фармакокинетические свойства компонентов препарата Мавирет представлены в таблице 3.
|
Таблица 3. Фармакокинетические свойства компонентов препарата Мавирет у здоровых добровольцев |
||||||||||||||||||||||||||||||||||||||||||
|
a. Медиана Ттах у здоровых добровольцев после приема однократной дозы глекапрсвира и пибрентасвира
b. Среднее системное воздействие при приеме с пищей со средним и высоким содержанием жиров
c. Прием однократной дозы [14С] глекапрсвира или [|4С] пибрентасвира в исследованиях массового баланса
d. Окислительные метаболиты или их продукты обмена составляли 26 % радиоактивной дозы. Метаболиты глекапрсвира в плазме нс наблюдались.
У пациентов с хроническим гепатитом С без цирроза, после 3 дней монотерапии либо только глекапревиром 300 мг в день (N=6) или только пибрентасвиром 120 мг в день (N=8), геометрическое среднее значения AUC24 составило 13600 нг-ч/мл для глекапрсвира и 459 нг-ч/мл для пибрентасвира. Оценка фармакокинетических параметров с использованием популяционных фармакокинетических моделей имеет присущую им неопределенность из-за нелинейности дозы и перекресного взаимодействия между глекапревиром и пибрентасвиром. Основываясь на популяционной фармакокинетической модели для препарата Мавирет при хроническом гепатите С, установившиеся значения AUC24 для глекапрсвира и пибрентасвира были 4800 и 1430 нг-ч/мл у пациентов без цирроза (N=1804), и 10500 и 1530 нг-ч/мл у пациентов с циррозом печени (N=280), соответственно. По сравнению со здоровыми пациентами (N=230), популяционные оценки AUC24, ss были аналогичны (разница в 10%) для глекапрсвира и на 34 % ниже для пибрентасвира у пациентов, инфицированных вирусом гепатита С без цирроза.
Линейность / нелинейность
AUC глекапрсвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы (при приеме 1200 мг один раз в день, наблюдалась в 516 раз больше экспозиция, чем 200 мг один раз в день). Данное явление может быть вызвано насыщением механизмов транспорта или эффлюксных переносчиков.
AUC пибрентасвира увеличивалась в степени большей, чем пропорциональная степень увеличения дозы до 120 мг (120 мг один раз в день наблюдалось увеличение экспозиции более чем в 10 раз по сравнению с приемом 30 мг один раз в день), но установленная линейная фармакокинетика в дозах > 120 мг. Нелинейное увеличение экспозиции <120 мг может быть связано с насыщением эффлюксных переносчиков.
Биодоступность пибрентасвира при взаимодействии с глекапревиром составляет в 3 раза выше по сравнению с применением только пибрентасвира. У глекапрсвира наблюдалось меньшее влияние пибрентасвира.
Особые группы пациентов
Раса/этническая принадлежность
Не требуется коррекция дозы препарата Мавирет в зависимости от расы или этнической принадлежности.
Пол/масса тела
Не требуется коррекция дозы препарата Мавирет в зависимости от пола или массы тела. Пациенты пожилого возраста
У пациентов пожилого возраста коррекция дозы препарата Мавирет не требуется. Популяционный фармакокинетический анализ ВГС-инфицированных пациентов в возрасте от 18 до 88 лет показал, что возраст не оказывает клинически значимого влияния на действие глекапрсвира и пибрентасвира.
Пациенты с нарушением почечной функции
Значение AUC глекапрсвира и пибрентасвира повышалось не более, чем на 56 % у пациентов без ВГС с легкой, умеренной и тяжелой степенью нарушения функции почек, не получавших диализ, по сравнению с пациентами с нормальной функцией почек. Значение AUC глекапрсвира и пибрентасвира было одинаковым у пациентов без ВГС на диализе и пациентов, не получающих его (разница <18%). В популяционном фармакокинетическом анализе у пациентов с ВГС и терминальной стадией почечной недостаточности, на диализе или без него, наблюдались значения AUC глекапрсвира на 86 % выше, а пибрентасвира на 54 % выше, чем у
пациентов с нормальной функцией почек. Мри оценке концентраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
В целом, изменения воздействия препарата Мавирет у ВГС-инфицированных пациентов с нарушением функции почек на диализе или без него, не были клинически значимыми. Пациенты с печеночной недостаточностью
Мри приеме рекомендованнной дозы значение AUC глекапрсвира у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Мью было на 33 % выше, класса 13 — на 100% выше, а класса С — в 11 раз выше, чем у пациентов без ВГС с нормальной функцией печени. Значение AUC пибрентасвира не менялось у пациентов с печеночной недостаточностью класса А по шкале Чайлд-Пью и было на 26 % выше у пациентов с печеночной недостаточностью класса В и на 114% — класса С. При оценке концетраций несвязанных глекапрсвира и пибрентасвира может иметь место более выраженный рост AUC.
Популяционный фармакокинетический анализ показал, что после приема препарата Мавирет пациентами с ВГС и компенсированным циррозом печени, воздействие глекапрсвира было примерно в 2 раза выше, а пибрентасвира — аналогичным таковому у пациентов с ВГС без цирроза. Механизм различий между экспозицией глекапрсвира у пациентов с хроническим гепатитом С с циррозом или без цирроза неизвестен.
Показания к применению
Лечение хронического гепатита С у взрослых.
Противопоказания
- Повышенная чувствительность к любому действующему веществу препарата или к
- любому из вспомогательных веществ.
- Пациенты с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью), см.
- разделы «Способ применения и дозы» и «Фармакокинетика».
- Совместное применение со следующими препаратами: атазанавир. аторвастатин, симвастатин, дабигатрана этексилат, препараты, содержащие эстрадиол, сильными индукторами Р-гликопротеина и CYP3A, например, рифампицин, карбамазепин, препараты зверобоя продырявленного Hypericum perjoratum, фенобарбитал, фенитоин, примидон, (см. раздел «Взаимодействие с другими лекарственными средствами»).
- Детский возраст до 18 лет.
- Дефицит лактазы, недостаточность лактозы, глюкозо-галактозная мальабсорбция.
С ОСТОРОЖНОСТЬЮ
Препарат Мавирет не рекомендуется применять совместно с омепразолом (40 мг), дарунавиром/ритонавиром, эфавирензом, лопинавиром/ритонавиром, ловастатином, циклоспорином (>100 мг в день).
Препарат Мавирет следует применять с осторожностью со следующими препаратами: дигоксин, правастатин, розувастатин, флувастатин, питавастатин, такролимус.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ Беременность
Данные о применении глекапрсвира или пибрентасвира у беременных женщин ограничены или отсутствуют. За время исследований имело место менее 300 случаев беременности. Исследования глекапрсвира и пибрентасвира на крысах и мышах не продемонстрировали наличие прямого токсического действия на репродуктивную функцию. Наличие токсического воздействия на беременную самку с последующим выкидышем наблюдалось у кроликов при применении глекапрсвира. что исключило возможность дальнейших исследований. В качестве меры предосторожности, препарат Мавирет не рекомендуется применять во время беременности.
Период грудного вскармливания
Неизвестно, выделяется ли глекапревир или пибрентасвир с грудным молоком. Доступные данные исследований фармакокинетики у животных показали экскрецию глекапрсвира и пибрентасвира с молоком, поэтому нельзя исключить риск для новорожденных и детей первого года жизни. Должно быть принято решение либо прекратить грудное вскармливание, либо прекратить терапию препаратом Мавирет или воздержаться от нее, принимая во внимание соотношение пользы грудного вскармливания для ребенка и пользы терапии для женщины. Фертильность
Исследования влияния глекапрсвира и/или пибрентасвира на фертильность у человека не проводились. Исследования у животных не показали негативного воздействия глекапрсвира или пибрентасвира на фертильность при экспозиции, превышающей значения, достигаемые у пациентов в результате приема рекомендованных доз препаратов.
Способ применения и дозы
Для приема внутрь.
1аблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать. Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С.
Дозы
Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг (три таблетки по 100 мг/40 мг) один раз в сутки во время еды.
В таблицах 1 и 2 представлена рекомендуемая продолжительность лечения препаратом Мавирет на основе данных, полученных на популяции пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. с компенсированным циррозом печени или без него.
|
Таблица 1. Рекомендованная продолжительность лечения для пациентов, ранее не получавших лечение |
||||||||
|
|
Таблица 2. Рекомендованная продолжительность лечения для пациентов, не ответивших на предыдущую терапию пегилированным интерфероном (пег-ИНФ) + рибавирнн (совместно с софосбувиром или без него) или софосбувир + рибавирин |
|||||||||||
|
|||||||||||
|
Для пациентов, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A см информацию в разделе «Особые указания». |
Пропуск приема препарата
В случае пропуска приема препарата Мавирет его можно осуществить в течение 18 часов после планового времени приема. Если с момента планового времени приема препарата Мавирет прошло более 18 часов, не следует принимать пропущенную дозу, а следующую дозу следует принять в обычное время по расписанию. Не следует принимать двойную дозу препарата.
Если в течение 3 часов после приема препарата Мавирет произошла рвота, то необходимо принять дополнительную дозу препарата. Если рвота произошла позднее 3 часов после применения препарата Мавирет, то прием дополнительной дозы не требуется.
Применение у пациентов пожилого возрасти
У пожилых пациентов коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушенной функцией почек
У пациентов почечной недостаточности, включая пациентов на диализе, коррекция дозы препарата Мавирет не требуется.
Пациенты с нарушением функции печени
У пациентов с печеночной недостаточностью легкой степени тяжести (класс А по шкале Чайлд-Пью) коррекция дозы препарата Мавирет не требуется. Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с печеночной недостаточностью тяжелой степени (класс С по шкале Чайлд-Пью) (см. разделы «Противопоказания», «Особые указания»). Дети
Отсутствуют данные о безопасности и эффективности применения препарата Мавирет у детей и подростков в возрасте до 18 лет.
Пациенты после трансплантации печени
Пациентам после трансплантации печени препарат Мавирет необходимо применять в течение как минимум 12 недель (см. раздел «Особые указания»).
Следует рассмотреть увеличение продолжительности терапии (в течение 16 недель) у пациентов с генотипом 3, которые ранее получали терапию пег-ИФН + рибавирин (совместно с софосбувиром или без него) или софосбувир + рибавирин.
Пациенты с ко-инфекцией ВГС/ВИЧ-1
Следует выполнять рекомендации, указанные в Таблице 1 и 2. Рекомендации по дозированию препарата Мавирет при совместном применении с препаратами для терапии ВИЧ-1 представлены в разделе «Взаимодействие с другими лекарственными средствами».
Побочное действие
Резюме профиля безопасности
Оценка безопасности препарата Мавирет у пациентов с компенсированной функцией печени (с циррозом печени или без него) была проведена по результатам исследований фазы 2 и 3, в которых участвовали около 2 300 пациентов, инфицированных ВГС генотипов 1, 2, 3, 4, 5 или 6. получавших Мавирет в течение 8, 12 или 16 недель.
Наиболее частыми нежелательными реакциями (частота > 10 %) были головные боли и утомляемость. Менее чем у 0,1 % пациентов, получавших лечение препаратом Мавирет, развились серьезные нежелательные реакции (транзиторная ишемическая атака). Доля пациентов, которые окончательно прекратили получать лечение препаратом Мавирет по причине развития нежелательных реакций, составила 0.1 %. Тип и тяжесть нежелательных реакций у пациентов с циррозом печени были сопоставимы с таковыми у пациентов без цирроза печени.
Таблица нежелательных реакций
Сообщалось о развитии следующих нежелательных реакций у пациентов, получавших лечение препаратом Мавирет. Ниже приведен список нежелательных реакций, сгруппированных согласно классу систем органов и по частоте встречаемости. Частота встречаемости определяется следующим образом: очень часто (> 1/10), часто (от >1/100 до < 1/10), нечасто (от > 1/1 000 до < 1/100), редко (от >1/10 000 до < 1/1 000) и очень редко (< 1/10 000).
Таблица 1. Нежелательные реакции, наблюдавшиеся при приеме препарата Мавирет
|
Частота развития |
Нежелательные реакции |
|
Нарушения со стороны нервной системы |
|
|
Очень часто |
Головная боль |
|
Нарушения со стороны желудочно-кишечного тракта |
|
|
Часто |
Тошнота, диарея |
|
Общие нарушения и реакции в месте введения |
|
|
Очень часто |
Утомляемость |
|
Часто |
Астения |
Описание отдельных нежелательных реакций
Нежелательные реакции у пациентов с тяжелым нарушением функции почек, включая пациентов на диализе
Безопасность препарата Мавирет у пациентов с хронической болезнью почек (стадия 4 или стадия 5, включая пациентов на диализе) и хронической инфекцией, вызванной вирусом гепатита С генотипов 1, 2, 3, 4, 5 или 6 с компенсированной печеночной недостаточностью (с циррозом печени или без него) была оценена на 104 пациентах. Наиболее частыми нежелательными реакциями у пациентов с тяжелым нарушением функции почек были кожный зуд (17 %) и утомляемость (12 %).
Оценка безопасности у пациентов с коинфекцией ВГС/ВИЧ-1
Общий профиль безопасности у пациентов с коинфекцией ВГС/ВИЧ-1 был сравним с таковым у пациентов с моноинфекцией ВГС.
Повышение уровня билирубина в сыворотке крови
У 1,3 % пациентов наблюдалось повышение уровня общего билирубина как минимум в 2 раза выше верхней границы нормы, что было связано с глекапревир-опосредованным ингибированием белков-переносчиков билирубина и метаболизма билирубина. Повышение уровня билирубина было бессимптомным, временным и обычно возникало на ранней стадии лечения. Повышение уровня билирубина возникало преимущественно за счет непрямой фракции и не было ассоциировано с повышением уровня АЛТ. Прямая гипербилирубинемия наблюдалась у 0,3 % пациентов.
ПЕРЕДОЗИРОВКА
Наибольшая задокументированная доза, принятая здоровыми добровольцами, составила 1200 мг один раз в день в течение 7 дней для глекапрсвира и 600 мг один раз в день в течение 10 дней для пибрентасвира. Бессимптомное повышение АЛТ в сыворотке (>5 раз ВГН) наблюдалось у 1 из 70 здоровых добровольцев после приема нескольких доз глекапрсвира (700 мг или 800 мг) 1 раз в день в течение > 7 дней. В случае передозировки, необходимо контролировать состояние пациента на наличие признаков токсического поражения (см. раздел «Побочное действие»). Соответствующее симптоматическое лечение должно быть начато немедленно. Гемодиализ в незначительной степени способствует выделению из организма глекапрсвира и пибрентасвира.
Взаимодействие с другими лекарственными препаратами
Возможное влияние препарата Мавирет на другие лекарственные препараты
Глекапревир и пибрентасвир — это ингибиторы Р-гликопротеина (P-GP), белка резистентности рака молочной железы (BCRP) и полипептида, транспортирующего органические анионы (ОАТР) 1В1/3.
Одновременное применение с препаратом Мавирет может привести к повышению концентрации в плазме препаратов, являющихся субстратами Р-гликопротеина (дабигатрана этексилат, дигоксин), BCRP (розувастатин) или ОАТР1В1/3 (аторвастатин, ловастатин, правастатин, розувастатин, симвастатин). См. рекомендации по лекарственному взаимодействию с чувствительными субстратами Р-гликопротеина, BCRP и ОАТР1В1/3 в таблице 1. Для других субстратов Р-гликопротеина. BCRP и ОАТР1В1/3 может потребоваться коррекция дозы.
Глекапревир и пибрентасвир — это слабые ингибиторы изоферментов системы цитохрома Р450 CYP3A и уридин-глюкуронозилтрансферазы (UGT) 1А1 in vivo. Не отмечалось клинически значимого увеличения системного воздействия для чувствительных субстратов CYP3A (мидазолам, фелодипин) и UGT1AI (ралгегравир) при одновременном приеме с препаратом Мавирет.
Применение глекапрсвира и пибрентасвира ингибирует помпу, экспортирующую желчные кислоты (BSEP) in vitro.
Не ожидается клинически значимого ингибирования субстратов CYP1A2, CYP2C9, CYP2C19, CYP2D6. UGT1А6, UGT1А9. UGT1А4, UGT2B7, OCTI, ОСТ2, ОАТ1, ОАТЗ, МАТЕ1 и МАТЕ2К.
Пациенты, получающие антагонисты витамина К
На фоне лечения препаратом Мавирет может наступить изменение функции печени, поэтому рекомендуется тщательный мониторинг международного нормализованного отношения (МНО). Потенциальное влияние других лекарственных препаратов на препарат Мавирет
Совместный прием с сильными индукторами Р-гликопротеина/СУРЗА
Лекарственные препараты, являющиеся сильными индукторами Р-гликопротеина и CYP3A (рифампицин, карбамазепин, зверобой продырявленный (Hypericum perforatum), фенобарбитал, фенитоин и примидон), могут вызвать существенное снижение концентрации глекапрсвира и пибрентасвира в плазме крови, привести к снижению терапевтического эффекта препарата Мавирет и потере вирусологического ответа. Применение таких препаратов одновременно с препаратом Мавирет противопоказано (см. раздел «Противопоказания»).
Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются умеренными индукторами Р-гликопротеина и CYP3A, может вызвать снижение концентрации глекапрсвира и пибрентасвира в плазме крови (окскарбазепин. эсликарбазепин, лумакафтор. кризотиниб). Одновременное применение с умеренными индукторами не рекомендуется (см. раздел «Особые указания»).
Глекапревир и пибрентасвир являются субстратами эффлюксных переносчиков Р-гликопротеина и (или) BCRP. Глекапревир также является субстратом транспортеров печеночного захвата ОАТР1В1/3. Применение препарата Мавирет одновременно с лекарственными препаратами, которые являются ингибиторами Р-гликопротеина и BCRP (циклоспорин, кобицистат, дронедарон, итраконазол, кетоконазол, ритонавир), может замедлить выведение глекапрсвира и пибрентасвира и может вызвать повышение экспозиции противовирусных препаратов в плазме крови. Лекарственные препараты, являющиеся ингибиторами ОАТР1В1/3 (элвитегравир. циклоспорин, дарунавир. лоиинавир), могут вызвать повышение системной концентрации глекапрсвира.
Установленные и другие потенциально возможные лекарственные взаимодействия
В таблице 1 приведено влияние отношения средних значений, вычисленных методом наименьших квадратов (90-процентный доверительный интервал) на концентрацию препарата Мавирет и сопутствующих лекарственных препаратов. Направление стрелки указывает направление изменения воздействия (Сmax и AUC) глекапрсвира, пибрентасвира и сопутствующего лекарственного препарата ( ↑—увеличение более чем на 25 %, ↓ — снижение более чем на 20 %, ↔ — нет изменения (снижение на менее или равно 20 % или увеличение на менее или равно 25 %).
ОСОБЫЕ УКАЗАНИЯ
Реактивация вирусного гепатита В
Во время лечения противовирусными препаратами прямого действия сообщалось о реактивации вируса гепатита В, в некоторых случаях со смертельным исходом. Перед началом терапии все пациенты должны проходить обследование на наличие ВГВ. Пациенты с коинфекцией ВГВ/ВГС подвержены риску реактивации ВГВ. поэтому следует проводить их мониторинг и ведение с соблюдением современных рекомендаций.
Пациенты после трансплантации печени
Безопасность и эффективность применения препарата Мавирет у пациентов, перенесших трансплантацию печени, не оценивались. Лечение препаратом Мавирет в соответствии с рекомендованным способом применения и дозами (см. раздел «Способ применения и дозы») должно основываться на оценке потенциальной пользы и рисков для каждого конкретного пациента.
Нарушение функции печени
Препарат Мавирет не рекомендуется назначать пациентам с печеночной недостаточностью средней степени тяжести (класс В по шкале Чайлд-Пью) и противопоказан пациентам с тяжелой печеночной недостаточностью (класс С по шкале Чайлд-Пью) (см. разделы «Способ применения и дозы», «Противопоказания»).
Пациенты, которые не ответили на предшествующую схему терапии, включающую ингибиторы NS5A и/или NS3/4A
Была изучена вероятность развития устойчивости к глекапревиру/пибрентасвиру у пациентов, инфицированных вирусом генотипа 1, и ограниченного количества пациентов, инфицированных вирусом генотипа 4, не ответивших на предшествующую схему терапии. Как и ожидалось, риск неудачи терапии был выше у пациентов с предшествующей терапией включающей оба класса препаратов (ингибиторы NS5A и NS3/4A). Методика для прогнозирования неудачи терапии на основе исходных данных об устойчивости к терапии не определена. Развитие устойчивости к обоим классам препаратов было основной находкой у пациентов, не ответивших на терапию глекапревиром/пибрентасвиром. Данные о повторном лечении пациентов, инфицированных вирусом генотипов 2, 3, 5 и 6, отсутствуют. Применение препарата Мавирет не рекомендуется для повторного лечения пациентов, ранее получавших лечение ингибиторами NS3/4A и/или NS5A.
Взаимодействие с другими лекарственными препаратами
Подробную информацию см. в разделе «Взаимодействие с другими лекарственными средствами».
Влияние на способность управлять транспортных средствами, механизмами
Препарат Мавирет не оказывает влияния или оказывает незначительное влияние на способность к вождению транспортных средств и управлению механизмами.
ФОРМА ВЫПУСКА
Таблетки, покрытые пленочной оболочкой. 100 мг + 40 мг.
По 3 таблетки, покрытые пленочной оболочкой, в блистере из поливинилхлорид/полиэтилен/полихлоротрифторэтилена и алюминиевой фольги.
По 7 блистеров в пачке картонной, по 4 пачки картонных вместе с инструкцией по применению в пачке картонной.
СРОК годности
2 года. Не использовать после истечения срока годности, указанного на упаковке.
УСЛОВИЯ ХРАНЕНИЯ
При температуре не выше 25 °C.
Хранить в местах, недоступных для детей.
УСЛОВИЯ ОТПУСКА
Отпускается по рецепту.
Инструкция по применению Мавирет таблетки п.п.о. 100 мг+40 мг №84
Противовирусное средство
Форма выпуска
таблетки покрытые пленочной оболочкой
Показания к применению
Лечение хронического гепатита С у взрослых.
Рекомендации по применению
Таблетки следует глотать целиком во время еды, не разжевывать, не раздавливать и не ломать. Лечение препаратом Мавирет должно назначаться специалистом и проводиться под наблюдением врача, обладающего опытом лечения пациентов с хроническим гепатитом С. Рекомендуемая доза препарата Мавирет составляет 300 мг/120 мг (три таблетки по 100 мг/40 мг) один раз в сутки во время еды.
Условия хранения
При температуре не выше 25 °C. Срок годности: 2 года.
Условия отпуска
Отпускается по рецепту
Действие
Препарат Мавирет — это комбинация двух пангенотипных противовирусных средств прямого действия в фиксированных дозах — глекапрсвира (ингибитора протеазы NS3/4A) и пибрентасвира (ингибитора NS5A), воздействующих на различные этапы жизненного цикла вируса гепатита С.
Состав
Актитвные вещества: глекапревир 100.0 мг, пибрентасвир 40.0 мг;
Вспомогательные вещества: коповидон К 28, D-альфа-токоферола макрогола сукцинат, кремния диоксид коллоидный, кроскармеллоза натрия. натрия стеарилфумарат, пропиленгликоля монокаприлат тип II; пленочное покрытие Опадрай II розовый (Opadryu II 32F240023)’. гипромеллоза 2910. лактозы моногидрат, титана диоксид, макрогол 3350, железа оксид красный.
Противопоказания
Повышенная чувствительность к любому действующему веществу препарата или к
любому из вспомогательных веществ.