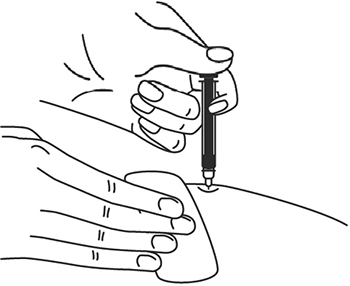
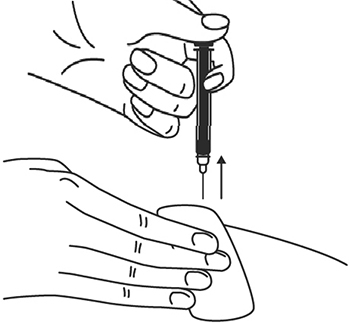
активное вещество — глицерол 6,14 мл,
вспомогательное вещество — вода очищенная.
При ректальном введении осмотические слабительные средства, такие как глицерин, очень слабо абсорбируются, и не подвергаются биологической переработке в тонкой кишке.
— для устранения симптомов кратковременного и эпизодического запора (для местного применения)
— дискомфорт в месте введения
— боль, зуд, раздражение в анальной области
— гиперчувствительность к каким-либо компонентам препарата.
— аноректальные заболевания, язвенный колит и воспаленные геморроидальные узлы
— абдоминальные боли и колики, тошнота, рвота или другие признаки аппендицита, а так же абдоминальные боли неясной этиологии
— при кишечной непроходимости
— острые воспалительные заболевания пищеварительного тракта
— детский возраст до 12 лет
Не сообщалось
В случае появления крови в кале, раздражения и боли в кишечнике, а так же в случае отсутствия нормализации стула, необходимо прекратить лечение и проконсультироватся с врачом.
При печеночной или почечной недостаточности нет необходимости в коррекции дозы.
У пациентов с тяжелыми заболеваниями, в частности сердечно-сосудистыми, препарат может применяться лишь под наблюдением врача.
Препарат не следует применять в течение более 7 дней, кроме как по медицинским показаниям.
Применение препарата возможно только лишь в том случае, если польза для матери превышает потенциальный риск для плода или ребенка.
Не влияет на способность управлять автотранспортом или потенциально опасными механизмами.
Злоупотребление и длительное применение данного препарата может привести к синдрому «раздраженного кишечника».
По 4 аппликатора вместе с инструкцией по медицинскому применению на государственном и русском языках вкладывают в коробку из картона.
Хранить при температуре не выше 25 °С.
Хранить в недоступном для детей месте!
3 года
Не применять по истечении срока годности.
Без рецепта
Casen Recordati, S.L., Испания
Autovia de Logrono, km. 13,300
50180 UTEBO (Zaragoza) Испания
Владелец регистрационного удостоверения
Casen Recordati, S.L., Испания
Наименование, адрес и контактные данные организации на территории Республики Казахстан, принимающей претензии (предложения) по качеству лекарственных средств от потребителей и ответственной за пострегистрационное наблюдение за безопасностью лекарственного средства:
Представительство ТОО «FIC MEDICAL» (ФИК МЕДИКАЛЬ) в Республике Казахстан, ул. Толе би 69, офис 33, 050000, Алматы, Казахстан
тел.: +7 (727) 272 93 08, факс: +7 (727) 272 90 25
e-mail:
fic_kz@ficmedical.kz
КоВамлосет — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-004711 — 260218
Торговое наименование:
Ко-Вамлосет
Международное непатентованное или группировочное наименование:
амлодипии + валсартан + гидрохлоротиазид
Лекарственная форма:
таблетки, покрытые пленочной оболочкой
Состав:
на 1 таблетку 5 мг + 160 мг+ 12,5 мг/ 10 мг + 160 мг + 12,5 мг/ 10 мг + 160 мг + 25 мг
Ядро:
Действующие вещества:
Амлодипина безилат (амлодипина бесилат) 6,94 мг/13.88 мг/13.88 мг. эквивалентно амлодипину 5,00 мг/10,00 мг/ 10,00 мг
Валсартан А. субстанция-гранулы 251.35 мг/251,35 мг/251,35 мг
[Действующее вещество субстанций-гранул: валсартан 160.00 мг/160,00 мг/160.00 мг
Вспомогательные вещеcmва субстанций-гранул: целлюлоза микрокристаллическая, кроскармеллоза натрия, повидон, натрия лаурил сульфат]
Гидрохлоротиазид 12,50 мг/12,50 мг/25,00 мг
Вспомогательные вещества:
Маннитол, магния стеарат, кремния диоксид коллоидный
Оболочка пленочная:
Пленкообразующая смесь:
— поливиниловый спирт.
— макрогол-3350,
— титана диоксид (Е 171).
— тальк.
— краситель железа оксид красный (Е172) (для таблеток 10 мг + 160 мг + 12.5 мг).
— краситель железа оксид желтый (Е172) (для таблеток 10 мг + 160 мг + 25 мг)
Описание
Таблетки 5 мг + 160 мг + 12.5мг:
Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой белого или почти белого цвета с гравировкой К1 на одной стороне.
Вид на изломе: белая или почти белая шероховатая масса с пленочной оболочкой белого или почти белого цвета.
Таблетки 10 мг + 160 мг + 12,5 мг:
Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой розового цвета с гравировкой К2 на одной стороне.
Вид на изломе: белая или почти белая шероховатая масса с пленочной оболочкой розового цвета.
Таблетки 10 мг + 160 мг + 25 мг:
Овальные, двояковыпуклые таблетки, покрытые пленочной оболочкой коричнево-желтого цвета с гравировкой К4 на одной стороне.
Вид на изломе: белая или почти белая шероховатая масса с пленочной оболочкой коричнево-желтого цвета.
Фармакотерапевтическая группа:
гипотензивное средство комбинированное (блокатор «медленных» кальциевых каналов [БМКК] + ангиотензина II рецепторов антагонист [АРА II] + диуретик)
Koд ATX: C09DX01
Фармакологические свойства
Фармакодинамика
Препарат Ко-Вамлосст является комбинацией трех гипотензивных компонентов с дополняющим друг друга механизмом контроля артериального давления (АД): амлодипина (производное дигидропиридина) — БМКК. валcapтана АРА II и гидрохлоротиазида (ГХТЗ) ти аз иди о го диуретика. Комбинация этих компонентов приводит к более выраженному снижению АД по сравнению с таковым на фоне монотерапии каждым препаратом в отдельности.
Амлодипин
Амлодипин, входящий в состав препарата Ко-Вамлосет. ингибирует трансмембранное поступление ионов кальция в кардиомиоциты и гладкомьппечные клетки сосудов.
Механизм антигипертензивного действия амлолипииа связан с прямым расслаоляюшим эффектом на гладкие мышцы сосудов, выбывающим уменьшение общего периферического сосудистого сопротивления (OIICC) и снижение ЛД. Экспериментальные данные показывают, что амлодипин связывается с дигидро- и недигидропиридиновым и активными центрами рецептора. Сокращение кардиомиоцитов и миоцитов стенок сосудов происходит благодаря проникновению в них ионов кальция через кальциевые каналы.
У пациентов с артериальной гинергензией применение амлодипипа в терапевтических дозах вызывает расширение сосудов, приводящее к снижению ЛД (в положении пациента «лежа» и «стоя»). Снижение АД не сопровождается существенным изменением частоты сердечных сокращений (ЧСС) и активности катехоламинов при длительном применении. Концентрации препарата в плазме крови коррелируют с терапевтическим ответом, как у молодых пациентов, так и у пациентов пожилого возраста. При артериальной гипертензии у пациентов с нормальной функцией почек амлодипин в терапевтических дозах приводит к уменьшению сопротивления почечных сосудов, увеличению скорости клубом ко вой фильтрации и эффективного почечного кровотока плазмы без изменения фильтрационной фракции и выраженности протеинурии.
Также, как и при применении других БМКК, на фоне приема амлодипина у пациентов с нормальной функцией левого желудочка (ЛЖ) наблюдалось изменение гемодинамических показателей функции сердца в покос и при физической нагрузке: небольшое увеличение сердечного индекса без значительного влияния на максимальную скорость нарастания давления в Л Ж, на конечио-диастолическое давление и объем ЛЖ. Гемодинамические исследования у интактных животных и здоровых добровольцев показали, что снижение АД под влиянием амлодипина в диапазоне терапевтических доз не сопровождается отрицательным инотропным действием даже при одновременном применении с бета-адреноблокаторами.
Амлодипин не изменяет функцию синоатриалыюго узла и не влияет на атриовентрикулярную проводимость у интактных животных и здоровых добровольцев. При применении амлодипина в комбинации с бета-адреноблокаторами у пациентов с артериальной гинергензией или со стенокардией снижение АД не сопровождается нежелательными изменениями электрокардиографических параметров. Доказана клиническая эффективность амлодипина у пациентов со стабильной стенокардией, вазос пасти чес кой стенокардией и ангиографически подтвержденным поражением коронарных артерий.
Валсартан
Валсартан — активный и специфический АРА II. предназначенный для приема внутрь. Он действует избирательно па рецепторы подтипа AT1, которые ответственны за эффекты ангиотензина II. Увеличение плазменной концентрации несвязанного ангиотензина II вследствие блокады AT1 -рецепторов под влиянием валсартана может стимулировать незаблокированиые АТ2-рецепторы, которые противодействуют эффектам стимуляции AT 1-рецепторов. Валсартан не имеет сколько-нибудь выраженной агонистической активности в отношении AT 1 -рецепторов. Сродство валсартана к рецепторам подтипа AТ1 примерно в 20 000 раз выше, чем к рецепторам подтипа АТ2.
Валсартан не ингибирует ангиотензинпревращающий фермент (АПФ), который превращает ангиотензин I в апгиотензин II и вызывает разрушение брадикинина. Так как при применении АРА II не происходит ингибирование АПФ и накопление брадикинина или субстанции Р, развитие сухого кашля маловероятно.
В сравнительных клинических исследованиях валсартана с ингибитором АПФ частота развития сухого кашля была достоверно ниже (р<0,05) у пациентов, получавших валсартан (у 2,6 % пациентов, получавших валсартан. и у 7,9 % — получавших ингибитор АПФ). В клиническом исследовании, включавшем пациентов, у которых ранее при лечении ингибитором АПФ развивался сухой кашель, при лечении вал сарган ом это осложнение было отмечено в 19,5% случаев, при лечении тиазидным диуретиком — в 19,0% случаев. В то же время в группе пациентов, получавших лечение ингибитором АПФ. кашель наблюдался в 68.5 % случаев (р < 0,05).
Валсартан не вступает во взаимодействие и не блокирует рецепторы других гормонов или ионные каналы, имеющие важное значение для регуляции функций сердечно-сосудистой системы.
При лечении валсартаном пациентов с артериальной гипертен.шей отмечается снижение АД, не сопровождающееся изменением ЧСС.
Антигипергензивный эффект проявляется в течение 2 часов у большинства пациентов после однократного приема валсартана внутрь. Максимальное снижение АД развивается через 4-6 часов. После приема валсартана длительность антигипертензивного эффекта сохраняется более 24 часов. При повторном применении максимальное снижение АД вне зависимости от принятой дозы внутрь обычно достигается в пределах 2-4 недель и поддерживается на достигнутом уровне в ходе длительной терапии. Резкое прекращение приема валсартана не сопровождается резким повышением АД или другими нежелательными клиническими последствиями. Применение валсартана у пациентов с хронической сердечной недостаточностью (ХСН) (II-IV функционального класса по классификации NYHA) приводит к значительному снижению числа госпитализаций по поводу сердечно-сосудистых заболеваний (что особенно выражено у пациентов, не получающих ингибиторы АПФ или бета-адреноблокаторы). При приеме валсартана у пациентов с левожелудочковой недостаточностью (со стабильными показателями гемодинамики) или с нарушением функции ЛЖ после перенесенного инфаркта миокарда отмечается снижение сердечно-сосудистой смертоности.
ГХТЗ
Точкой приложения действия тиазидных диуретиков являются дистальные извитые почечные канальцы. При воздействии тиазидных диуретиков на высокочувствительные рецепторы дистальных канальцев коркового слоя почек происходит подавление реабсорбции ионов натрия и хлора. Подавление ко-транспортной системы ионов натрия и хлора, по-видимому, происходит за счет конкуренции за участки связывания ионов хлора в данной системе. В результате этого выведение ионов натрия и хлора увеличивается примерно в равной степени. В результате диуретического действия наблюдается уменьшение объема циркулирующей крови (ОЦК), вследствие чего повышается активность ренина, секреция альдостерона. выведение почками калия и следовательно. снижение содержания калия в сыворотке крови.
Фармакокинетика
Фармакокинетические показатели амлодипина, валсартана и ГХТЗ характеризуются линейностью.
Амлодипин
Всасывание
После приема внутрь амлодипина в терапевтических лозах максимальная концентрация (Сmax) в плазме крови достигается через 6-12 часов. Абсолютная биодоступность составляет в среднем 64-80 %. Прием пищи не влияет на биодоступпость амлодипина.
Распределение
Объем распределения составляет приблизительно 21 л/кг. В исследованиях с амлодипином в условиях in vitro показано, что у пациентов с артериальной гипертензией приблизительно 97.5 % циркулирующего амлодипина связывается с белками плазмы крови.
Метаболизм
Амлодипин интенсивно (приблизительно 90 %) метаболизирустся в печени с образованием активных метаболитов.
Выведение
Выведение из плазмы крови носит двухфазный характер с периодом полувыведения (IV,) приблизительно от 30 до 50 часов. Равновесные концентрации в плазме крови достигаются после продолжительного применения и течение 7-8 дней. 10% выводится в неизмененном виде, 60 % — в виде метаболитов.
Валсартан
Всасывание
После приема внутрь валсартана Сmax в плазме крови достигается через 2-4 часа. Средняя абсолютная биодоступность составляет 23 %.
При приеме с пищей отмечается снижение биодоступности (по значению площади под кривой «концентрация-время» [АUС]) на 40 % и Сmах в плазме крови — почти на 50 %. хотя приблизительно через 8 часов после приема валсартапа внутрь концентрации вал сарган а в плазме крови у людей, принимавших его с пищей, и в группе, получавшей валcартанан натощак, выравниваются. Снижение AUC, однако, не сопровождается клинически значимым уменьшением терапевтического эффекта, поэтому вал сарган можно назначать вне зависимости от времени приема пищи.
Распределение
Объем распределения (Vd) валсартана в период равновесною состояния после внутривенного введения составлял около 17 л, что указывает на отсутствие экстенсивного распределения валсартана в тканях. Валсартан в значительной степени связывается с белками сыворотки крови (94-97 %), преимущественно с альбуминами.
Метаболизм
Валсартан не подвергается выраженному метаболизму (около 20 % принятой дозы определяется в виде метаболитов). Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее чем 10% от AUC валсартана). Этот метаболит фармакологически неактивен.
Выведение
Фармакокинетическая кривая валсартана носит нисходящий мулы и экспоненциальный характер (T1/2α < 1 часа и T1/2β около 9 часов). Валсартан выводится в основном а неизмененном виде через кишечник (около 83% дозы) и почками (около 13% дозы). После внутривенного введения плазменный клиренс валсартана составляет около 2 л/час и его почечный клиренс составляет 0.62 л/час (около 30 % от общего клиренса). Т1/2 составляет 6 часов. ГХТЗ
Всасывание
Всасывание ГХТЗ после приема внутрь быстрое (время достижения Сmax в плазме крови около 2 часов). В среднем повышение AUC носит линейный характер и пропорционально принятой внутрь дозе в терапевтическом диапазоне. При одновременном приеме пищи сообщалось как о повышении, так и о снижении системной биодостунности ГХТЗ по сравнению с приемом препарата натощак. Величина этого влияния небольшая и клинически незначима. Абсолютная биодоступность ГХТЗ после приема внутрь составляет 70 %.
Распределение
Кинетика распределения и элиминации в целом описывается как биэкспоненциальная убывающая функция с Т1/2 -6-15 часов. При многократном применении кинетика ГХТЗ не изменяется, и при применении 1 раз в день кумуляция минимальна. Видимый объем распределения — 4-8 л/кг. 40-70% циркулирующего в плазме крови ГХТЗ связывается с белками плазмы крови, главным образом, с альбуминами. ГХТЗ также накапливается в эритроцитах в концентрациях примерно в 3 раза превышающих таковые в плазме крови.
Метаболизм
ГХТЗ выводится в неизмененном виде.
Выведение
Т1/2 конечной фазы составляет 6-15 часов. При повторном применении препарата кинетика ГХТЗ не изменяется, при назначении препарата однократно в сутки накопление препарата минимально. Более 95% абсорбированной дозы ГХТЗ выводится в неизмененном виде почками.
Амлодипин + валсартан + ГХТЗ
После приема внутрь препарата С max амлодипина валсартана и ГХТЗ в плазме крови достигаются через 6-8, 3 и 2 часа, соответственно.
Фармакокинетика у отдельных групп пациентов
Пациенты до 18 лет
Фармакокинетические особенности применения препарата Ко-Вамлосет у детей до 18 лет не установлены.
Пациенты пожилого возраста (старше 65 лет}
Время достижения Сmax амлодипина в плазме крови у молодых и пациентов пожилого возраста одинаково. У пациентов пожилого возраста клиренс амлодипина незначительно снижен, что приводит к увеличению AUC и Т1/2.
У пациентов пожилого возраста системное воздействие валсартана было несколько более выраженным, чем у пациентов молодо со возраста, однако это не было клинически значимым.
Имеются ограниченные данные о снижении системного клиренса ГХТЗ у пациентов старше 65 лет (здоровых добровольцев или пациентов с артериальной гипертензией) по сравнению с молодыми пациентами.
Пациенты с нарушениями функции почек
У пациентов с нарушениями функции почек фармакокинетические параметры амлодипина существенно не изменяются.
Не выявлено корреляции между функцией почек (клиренс креатинина [КК]) и системной экспозицией валсартана (AUC) у пациентов с различной степенью нарушения функции почек.
При наличии почечной недостаточности средние Сmax в плазме крови и значения AUC ГХТЗ увеличиваются, а скорость экскреции снижается. У пациентов с нарушением функции почек от легкой до умеренной степени тяжести IV, удлиняется практически вдвое. Почечный клиренс ГХТЗ у пациентов с нарушением функции почек снижен по сравнению с нормальными показателями (около 300 мл/мин).
Препарат Ко-Вамлосет противопоказан к применению у пациентов с тяжелой почечной недостаточностью (КК < 30 мл /мин), анурией и должен применяться с осторожностью у пациентов с нарушением функции почек умеренной степени тяжести (расчетная скорость клубочковой фильтрации [СКФ| > 30 мл/мин/1.73 м2 площади поверхности тела, но < 60 мл/мин/73 м2 площади поверхности тела).
Пациенты с нарушениями функции печени
Имеются лишь ограниченные клинические данные о применении амлодипина у пациентов с нарушением функции печени. Пациенты с нарушениями функции печени имеют сниженный клиренс амлодипина, что приводит к повышению AUC приблизительно па 40-60 %. В среднем у пациентов с нарушениями функции печени легкой (5-6 баллов по шкале Чайлд-Пыо) и умеренной (7-9 баллов по шкале Чайлд-Пью) степени тяжести биодоступность (по AUC) валсартана удваивается по сравнению со здоровыми добровольцами (соответствующего возраста, пола и массы тела). Препарат Ко-Вамлосет противопоказан пациентам с нарушением функции печени (см. разделы «Противопоказания» и «Способ применения и дозы»)
Показании к применению
• Артериальная гипертензня II и III степени.
Притивопоказания
- Повышенная чувствительность к амлодипину, валсаргану, ГХТЗ, другим производным сульфонамида и ди гидропиридинового ряда, а также другим вспомогательным компонентам препарата.
- Наследственный ангионевротический отек, либо отек у пациентов на фоне предшествующей терапии АРА II.
- Беременность, планирование беременности и период грудного вскармливания.
- Печеночная недостаточность, билиарный цирроз и холестаз.
- Тяжелые нарушения функции почек (КК <30 мл/мин), анурия, пациенты на гемодиализе.
- Рефрактерные к адекватной терапии гипокалиемия, гипонатриемия. гиперкальциемия, а также гиперурикемия с клиническими проявлениями.
- Возраст до 18 лет (эффективность и безопасность не установлены).
- Тяжелая артериальная гипотензия (систолическое АД < 90 мм рт. ст.), коллапс, кардиогенный шок.
- Клинически значимый стеноз аорты.
- Гемодинамически нестабильная сердечная недостаточность после острого инфаркта миокарда.
- Одновременное применение с алискирепом и препаратами, содержащими алискиреп. у пациентов с сахарным диабетом и/или умеренными и тяжелыми нарушениями функции почек (СКФ менее 60 мл/мин/1,73 м 2 площади поверхности тела).
- Одновременное применение с ингибиторами АПФ у пациентов с диабетической нефропатией.
С осторожностью
Если у вас одно из перечисленных заболеваний перед приемом препарата обязательно проконсультируйтесь с врачом.
Следует соблюдать осторожность при применении препарата у пациентов с односторонним или двусторонним стенозом почечных артерий или стенозом артерии единственной почки, при состояниях, сопровождающихся снижением ОЦК и водно-электролитными нарушениями: нефропатии, сопровождающиеся потерей солей. иреренальиое (кардиогенное) нарушение функции почек, пациентам с гиперкальциемией, у пациентов с митральным или аортальным стенозом, гипертрофической обструктивной кардиомиопатией, гипокалиемией, атриемией, гипомагниемией. гипохлоремией. у пациентов с ХСН III-IV функционального класса по классификации NYIIA. с острым коронарным синдромом, с сахарным диабетом, с системной красной волчанкой, с гиперурикемией, повышенными концентрациями холестерина и триглицеридов в плазме крови, у пациентов с закрыто угольной глаукомой, а также у пациентов после трансплантации почки. Следует соблюдать осторожность при применении препарата пациентами пожилого возраста.
Следует соблюдать осторожность при одновременном применении препарата Ко-Вамлосет с солями калия, калийсберегаюшими диуретиками, калий содержащими заменителями пищевой соли, а также с лекарственными средствами, которые могут вызывать повышение содержания калия в плазме крови (например, гепарином).
Применение при беременности и и период грудного вскармливания
Как и любой препарат, оказывающий влияние на ренин-ашиотензин-альдостероновую систему (РААС), препарат Ко-Вамлосет не должен применяться у женщин, планирующих беременность. При назначении любого препарата, воздействующего на РААС, врачу следует проинформировать женщин детородного возраста о потенциальной опасности этих препаратов во время беременности.
Применение препарата Ко-Вамлосет при беременности противопоказано. Известно, что применение ингибиторов АПФ, оказывающих влияние па РААС, во II и III триместрах беременности приводит к повреждению или гибели развивающегося плода. Учитывая механизм действия АРА II, нельзя исключить риск для плода. По данным ретроспективного анализа применения ингибиторов АПФ в I триместре беременности сопровождалось развитием патологии плода и новорожденного.
ГХТЗ проникает через плаценту. При применении тиазидных диуретиков, включая ГХТЗ, при беременности возможно развитие эмбриональной или неонатальпой желтухи или тромбоцитопении. а также других нежелательных реакций, наблюдающихся у взрослых пациентов. При непреднамеренном приеме валсартана у беременных описаны случаи развития спонтанных абортов, маловодия и нарушения функции почек у новорожденных. Данных о применении амлодипина у беременных недостаточно, чтобы судить о его воздействии па плод.
Если беременность диагностирована в период лечения препаратом Ко-Вамлосет, препарат следует отменить как можно быстрее.
Неизвестно, выделяется ли валсартан и/ил и амлодипин с грудным молоком. В экспериментальных исследованиях отмечено выделение валсартана с грудным молоком. ГХТЗ также выделяется с грудным молоком. Ко-Вамлосет не следует применять в период грудного вскармливания.
Способ применения и дозы
Препарат Ко-Вамлосет следует принимать внутрь, запивая небольшим количеством воды, независимо от времени приема пищи.
Рекомендуемая суточная доза — 1 таблетка, содержащая амлодипин + валсартан + ГХТЗ в дозе 5 мг+160 мг+12,5 мг. 10 мг+160 мг + 12.5 мг (в виде препарата Ко-Вамлосет таблетки, покрытые пленочной оболочкой, 5 мг+160 мг + 12,5 мг., 10мг + 160 мг + 12.5 мг) или 1 таблетка, содержащая амлодипин + валсартан + ГХТЗ в дозе 10 мг + 160 мг +25 мг (в виде препарата Ко-Вамлосет, таблетки, покрытые пленочной оболочкой, 10 мг + 160 мг + 25 мг). Препарат Ко-Вамлосет принимается 1 раз в сутки.
Для удобства пациенты, получающие терапию амлодипином, валсартаном и ГХТЗ в отдельных таблетках, могут быть переведены па терапию препаратом Ко-Вамлосет, содержащим те же дозы активных компонентов. При недостаточном контроле АД на фоне двойной комбинированной терапии (валсартан + ГХТЗ, амлодипин + валсартан и амлодипин + ГХТЗ) пациенты могут быть переведены на тройное комбинированное лечение препаратом Ко-Вамлосет в соответствующих дозах. Доза препарата Ко-Вамлосет подбирается после ранее проведенного титрования доз монокомпонентных лекарственных препаратов, содержащих действующие вещества, входящие в состав препарата Ко-Вамлосет. Если потребуется изменение дозы одного из действующих веществ в составе препарата Ко-Вамлосет (например, в связи с вновь диагностированным заболеванием. изменением состояния пациента или лекарственным взаимодействием), то необходим индивидуальный подбор доз отдельных компонентов.
У пациентов с дефицитом натрия и/или гиповолемией, например, у пациентов. получающих высокие дозы диуретиков, возможно развитие симптоматической артериальной гипотензии в начале терапии препаратом Ко-Вамлосет. Данную комбинацию следует применять только после коррекции гипопатриемии и/ил и гиповолемии.
В случае если у пациента отмечаются дозозависимые побочные эффекты при применении двойной комбинированной терапии любыми компонентами препарата Ко-Вамлосет, для достижения сопоставимого снижения АД возможно применение препарата Ко-Вамлосет, содержащего более низкую дозу активного компонента, вызвавшего данный побочный аффект.
Увеличивать дозу можно через 2 педели после начала терапии.
Максимальный антигииертеизивиый мрфект препарата отмечается через 2 недели после увеличения дозы. Максимальная доза препарата составляет 10 мг + 320 мг + 25 мг в сутки.
Применение у пациентов старше 65 лет
Коррекции дозы препарата не требуется. У пациентов данной категории при необходимости возможно уменьшение начальной дозы до содержащей наименьшую дозу амлодипина. т. е. 1 таблетка, содержащая амлодипин + валсартан + ГХТЗ в дозе 5 мг + 160 мг+12.5 мг (в виде препарата Ко-Вамлосет, таблетки, покрытые пленочной оболочкой, 5 мг + 160 мг +12,5 мг) или 5 мг+160 мг + 25 мг (в виде препарата Ко-Вамлосет, таблетки, покрытые пленочной оболочкой, 5 мг — 160 мг + 25 мг).
Применение у детей и подростков в возрасте до 18 лет
Поскольку безопасность и эффективность препарата Ко-Вамлосет у детей и подростков (младше 18 лет) не установлены, препарат не рекомендуется применять у пациентов данной категории.
Пациенты с нарушением функции почек
Для пациентов с нарушением функции почек легкой и умеренной степени тяжести (СКФ> 30 мл/мин/1,73 м2 площади поверхности тела, но <90 мл/мии/1,73 м2 площади поверхности тела) коррекция начальной дозы не требуется. Препарат не следует применять у пациентов с нарушением функции почек тяжелой степени (СКФ < 30 мл/мин/1,73 м2 площади поверхности тела) вследствие наличия в составе препарата ГХТЗ.
Применение тиазидных диуретиков в монотерапии у пациентов с нарушениями функции почек тяжелой степсни (СКФ < 30 мл /мин/1.73 м2 площади и поверхности чела) неэффективно, однако одновременное применение с «петлевыми» диуретиками у пациентов данной категории возможно.
Пациенты с нарушением функции печени
Вследствие наличия в составе валсартана, ГХТЗ и амлодипина препарат Ко-Вамлосет противопоказан у пациентов с нарушением функции печени тяжелой степени (> 9 баллов по шкале Чайлд-Пью). У пациентов с нарушением функции печени легкой или умеренной степени без холестаза максимальная рекомендованная доза составляет 80 мг валсартана. и, поэтому препарат Ко-Вамлосет (содержит 160 мг валсартана) не может быть применен у данной группы пациентов (см. разделы «Противопоказания», «Особые указания» и «Фармакокинетика»). Рекомендации по дозированию амлодипина у пациентов с нарушением функции печени легкой или умеренной степени не разработаны. У пациентов данной категории при необходимости следует назначать препарат с наименьшей дозой амлодипина.
Побочное действие
Ниже представлен профиль безопасности комбинации амлодипин + валсартан + ГХТЗ, основанный на клинических исследованиях при применении комбинации амлодипип + валсартан + ГХТЗ и известном профиле безопасности отдельных компонентов: амлодипин, валсартан и ГХТЗ.
Краткий обзор профиля безопасности
Безопасность применения комбинации амлодипип + валсартан + ГХТЗ оценивали при применении максимальной дозы 10 мг + 320 мг t-25 мг в одном контролируемом краткосрочном (8 недель) клиническом исследовании с участием 2271 пациентов, 582 из которых получали валсартан в комбинации с амлодипином и ГХТЗ. Нежелательные реакции, как правило, были легкими и кратковременными и лишь в редких случаях требовали прекращения лечения. В данном клиническом исследовании с активным контролем самыми распространенными причинами прекращения терапии комбинацией амлодипин + валсартан + ГХТЗ были головокружение и артериальная гипотензия (0.7 %).
В 8-недельном контролируемом клиническом исследовании отсутствовали значимые новые и неожиданные нежелательные реакции при трех компонентной терапии в сравнении с известными эффектами монотерапии или двухкомпонентной терапии.
В 8-недельном контролируемом клиническом исследовании изменения лабораторных показателей при применении комбинации амлодииин + валсартан + ГХТЗ были слабо выраженным и и соответствовали фармакологическому механизму действия отдельных компонентов. Присутствие валсартана в трех компонентной комбинации ослабляло гипокалиемический эффект ГХТЗ.
Перечень нежелательных реакций в форме таблицы
Следующие нежелательные реакции, классифицированные по классам с несем органов MedDRA и частоте встречаемости, относятся к комбинации амлодипин + валсартан + ГХТЗ и амлодипипу, валсартан у и ГХТЗ по отдельности.
Классификация частоты развития побочных эффектов, рекомендуемая Всемирной организацией здравоохранения (ВОЗ):
очень часто ≥ 1/10
часто от ≥1/100 до < 1 /10
нечасто от ≥ 1/1000 до < 1/100
редко от ≥ 1 /10000 до < 1 /1000
очень редко < 1/10000
частота неизвестна — не может быть оценена на основе имеющихся данных.
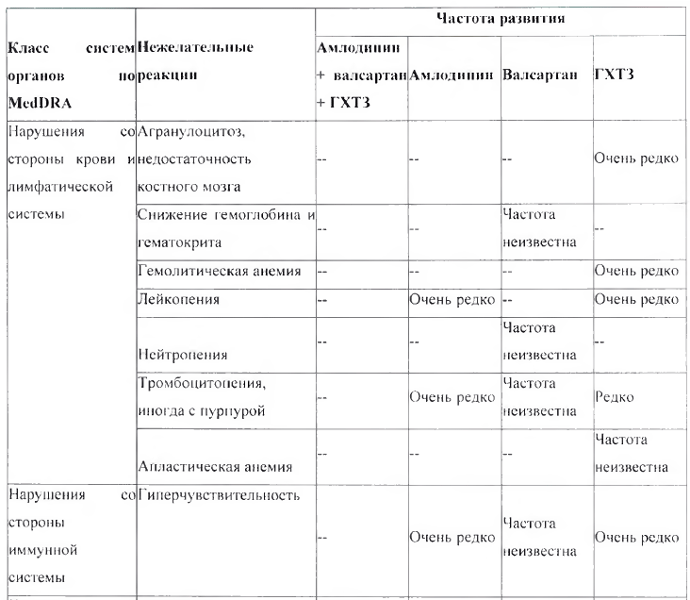
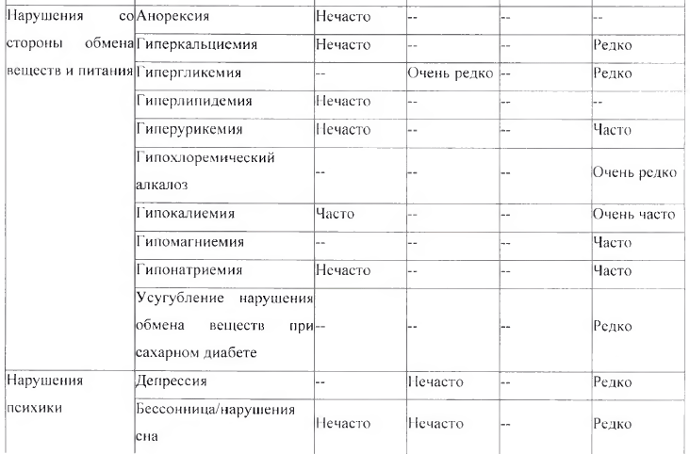
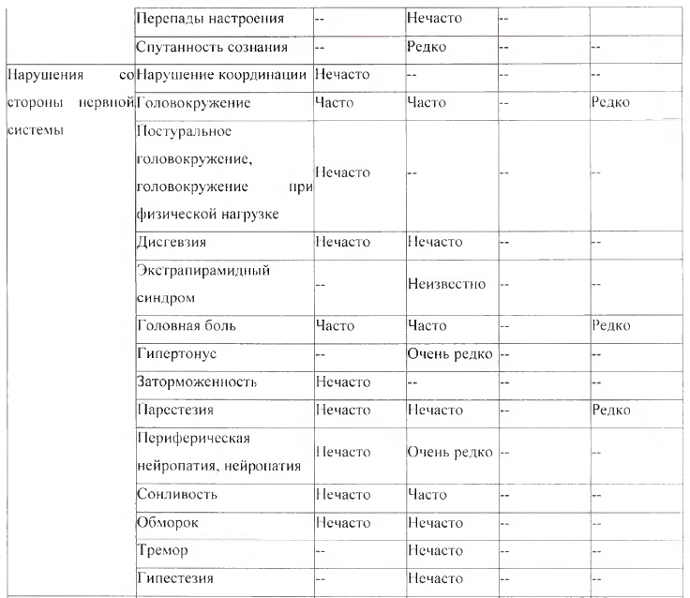
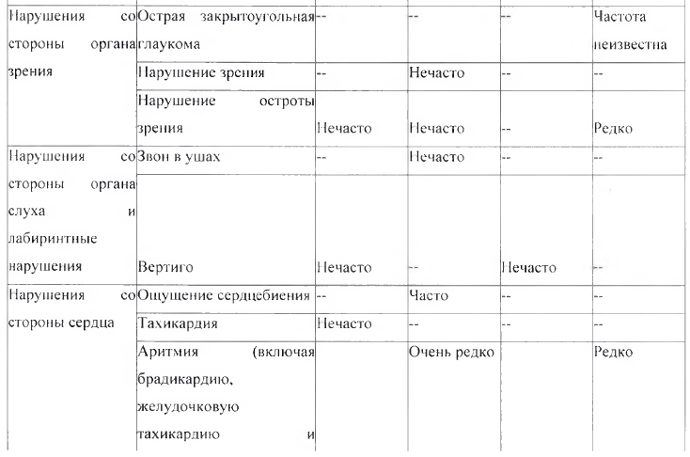
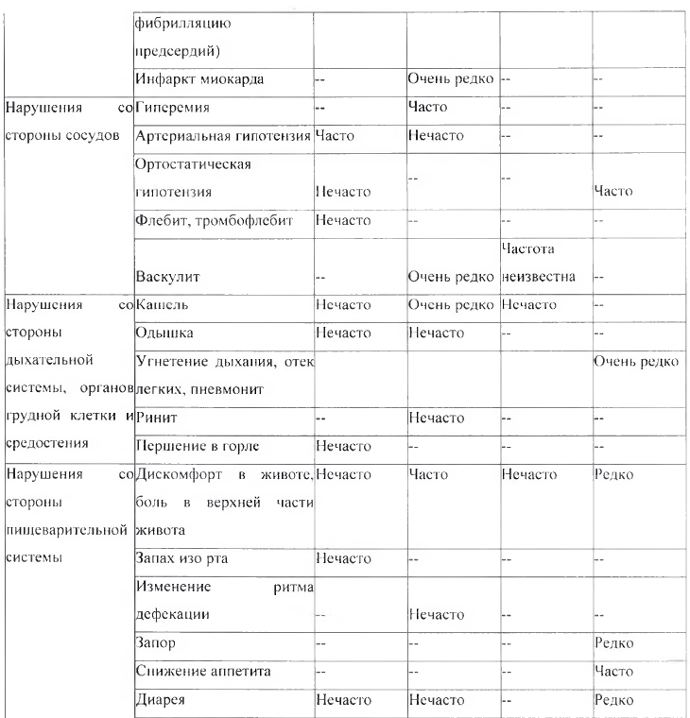
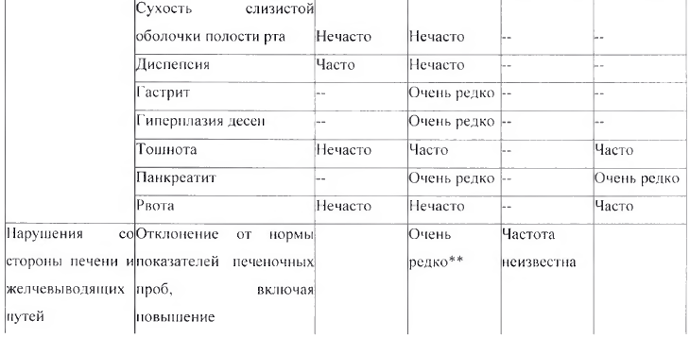
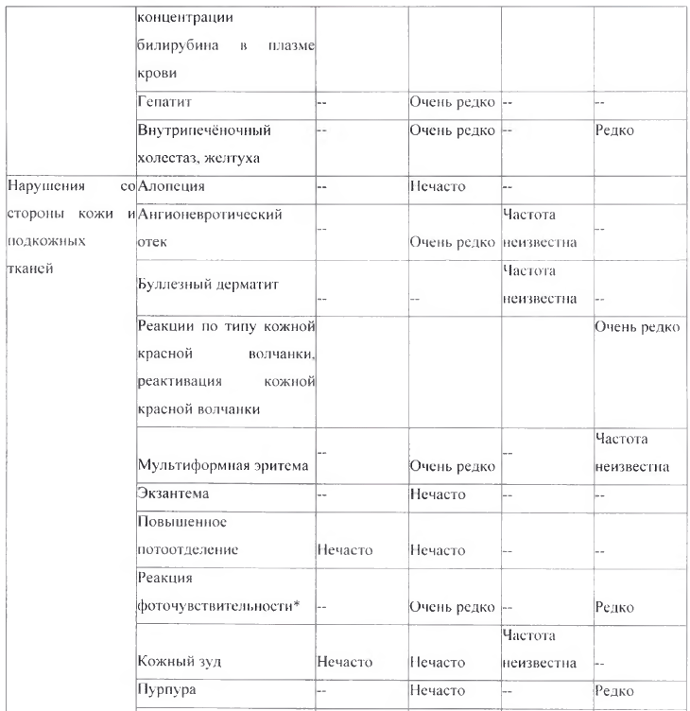
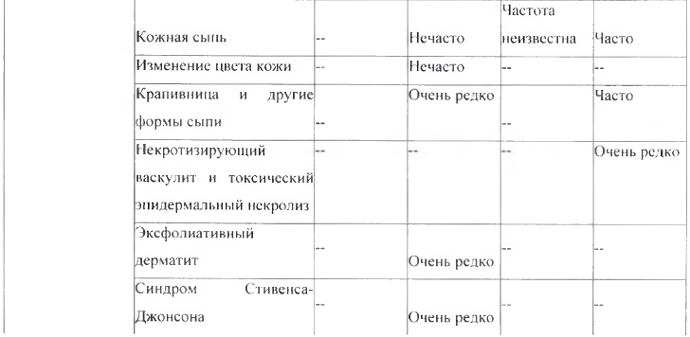
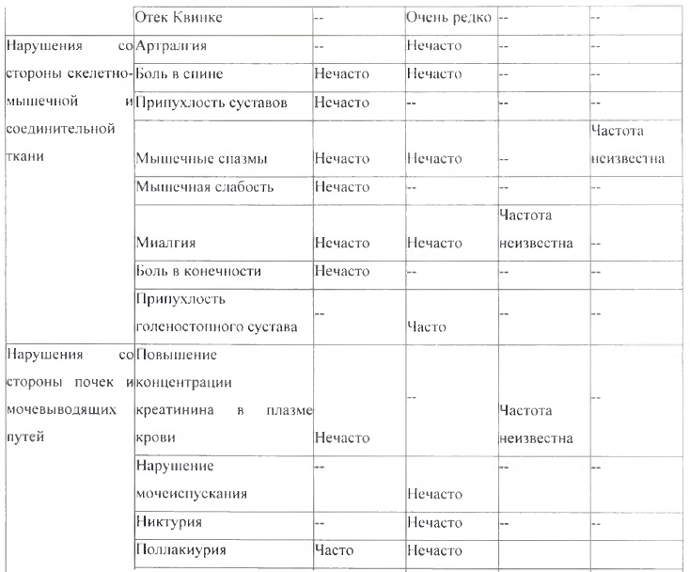

* См. раздел «Особые указания», подраздел «Реакция фоточувствительности»
** B основном соответствует холестазу
Передозировка
Данные о случаях передозировки препарата в настоящее время отсутствуют.
Валсартан
Мри передозировке валсартана можно ожидать развитие выраженного снижения АД и головокружения.
Амлодипин
Передозировка амлодипина может привести к чрезмерной периферической вазодилатации и возможной рефлекторной тахикардии. Сообщал ос ь также о возникновении выраженного и длительного снижения АД вплоть до развития шока с летальным исходом.
В случае возникновения выраженного снижения АД. пациенту следует придать горизонтальное положение c приподнятыми ногами, и принять активные меры по поддержанию деятельности сердечно-сосудистой системы, включая регулярный контроль деятельности сердца и дыхательной системы. ОЦК и количества выделяемой мочи.
Для поддержания нормального тонуса сосудов при отсутствии противопоказаний возможно применение вазон рессорных препаратов. Если препарат Ко-Вамлосет был принят недавно, рвота или промывание желудка могут быть эффективными. Применение активированного угля у здоровых добровольцев со про ни ждалось снижением абсорбции амлодипина.
Валсартан и амлодипин с помощью гемодиализа не удаляются, тогда как для выведения ГХТЗ гемодиализ может быть эффективным.
Взаимодействие с другими лекарственными средствами
Общие лекарственные взаимодействия для валсартана и ГХТЗ
Препараты лития
При одновременном применении препаратов лития с ингибиторами ЛИФ. ЛРЛ II или тиазидными диуретиками отмечалось обратимое увеличение содержания лития и сыворотке крови и связанное с этим усиление токсических проявлений. Риск токсических проявлений, связанных с применением препаратов лития, может дополнительно увеличиваться при одновременном применении с препаратом Ко-Вамлосет, поскольку почечный клиренс препаратов лития замедляется под воздействием тиазидных диуретиков. В связи с этим рекомендуется проводить тщательный контроль содержания лития в сыворотке крови.
Амлодипин
При моногерапии амлодипином не отмечается клинически значимого взаимодействия с тиазидными диуретиками, бета-адреноблокаторами, ингибиторами АПФ, нитратами длительного действия, нитроглицерином для подъязычного применения, дигоксином, варфарином, аторвастатином, силденафилом, алюминия гидроксидом и магния гидроксидом, симетиконом, циметидином, нестероидными противовоспалительными препаратами (НПВП), антибиотиками и гипогликемическими лекарственными средствами для приема внутрь.
Одновременный прием амлодипина и этанола не влияет на фармакокинетику последнего.
Ингибиторы изофермента CYP3A4
При одновременном применении амлодипина в дозе 5 мг/сут с дилгиаземом в дозе 180мг/сут у пациентов пожилого возраста с артериальной гииертензией отмечалось увеличение системной экспозиции амлодипина в 1.6 раз. При применении амлодипина с мощными ингибиторами изофермента CYP3A4 (например, кетоконазол, итраконазол и ритонавир) возможно ещё более выраженное увеличение системной экспозиции амлодипина. Необходимо с осторожностью применять амлодипин с ингибиторами изофермента CYP3A4.
В связи с ипгибировапием изофермента CYP3A4 при одновременном приеме с грейпфрутовым соком биодоступность амлодипина может увеличиваться. 13 клиническом исследовании у здоровых добровольцев, однако, не было выявлено значительных изменений фармакокинетики при приеме амлодипина в дозе 10 мг с 240 мл грейпфрутового сока.
Индукторы изофермента CYP3A4
Поскольку применение амлодипина с индукторами изофермента CYP3A4 (например, карбамазепин, фенобарбитал, фенитоин, фосфенитоин, примидон, рифампицин, растительные препараты, содержащие Зверобой продырявленный) может приводить к выраженному уменьшению его концентрации а плазме крови, следует соблюдать осторожность при применении амлодипина с индукторами изофермента CYP3A4.
Симвастатин
Многократное одновременное применение симвастатиниа в дозе 80 мг/сут и амлодипина в дозе 10 мг/сут ведет к увеличению экспозиции симвастатина в плазме крови на 77%. Рекомендуется уменьшить дозу симвастатина до 20 мг/сут у пациентов, принимающих амлодипин.
Такролимус
Существует риск увеличения сывороточной концентрации такролимуса при одновременном применении с амлодипин ом. Для того чтобы избежать токсичности такролимуса. при применении амлодипина у пациентов, получающих такролимус, необходимы мониторинг сывороточной концентрации такролимуса и коррекция его дозы в случае необходимости.
Кларитромицин
Кларитромицин является ингибитором изофермента CYP3A4. Существует повышенный риск развития артериальной гипотензии у пациентов, одновременно применяющих кларитромицин с амлодипином. При одновременном применении амлодипина с кл эритромицином рекомендуется тщательное наблюдение пациентов.
Валсартан
Установлено, что при монотсрапии валсартаном отсутствует клинически значимое взаимодействие со следующими лекарственными средствами: циметидином, варфарином, фуросемидом, дигоксином, атенололом, индометацином, ГХТЗ, амлодипином, глибенкламидом.
Двойная блокада РААС при применении АРА II, ингибиторов АПФ или алискирена
Одновременное применение АРА II с препаратами, содержащими алискирен, противопоказано у пациентов с сахарным диабетом и/или с умеренной или тяжелой почечной недостаточностью (СКФ менее 60 мл/мин/1,73 м2 площади поверхности тела) и не рекомендуется у других пациентов. Одновременное применение АРА II с ингибиторами АПФ противопоказано у пациентов с диабетической нефропатией и не рекомендуется у других пациентов.
Одновременное применение АРА II с другими препаратами, влияющими па РААС. приводит к увеличению частоты возникновения случаев артериальной гипотензии, гиперкалиемии, нарушению функции почек. Необходимо контролировать показатели АД, функции почек, а также содержание электролитов плазмы крови при применении препарата Ко-Вамлосет с другими препаратами, влияющими на РААС.
Препараты и вещества, влияющие на содержание калия в сыворотке крови
При одновременном применении с биологически активными добавками, содержащими калий, калийсберегающими диуретиками, эплереноном, калийсодержащими заменителями соли, или с другими препаратами, которые могут вызывать увеличение содержания калия в плазме крови (например, с гепарином), следует соблюдать осторожность и проводить регулярный контроль содержания калия плазмы крови.
НПВП, включая селективные ингибиторы циклооксигеназы-2 (ЦОГ-2)
Возможно уменьшение диуретического и антигипертспзивного действия валсартана при одновременном применении с НПВП. включая селективные ингибиторы ЦОГ-2, например, с производными салициловой кислоты, индометацином. Более того у пациентов пожилого возраста с сопутствующей гиповолемией (в том числе вследствие приема диуретиков) или с нарушенной функцией почек, одновременное применение АРА II и НПВП, включая селективные ингибиторы ЦОГ-2, может привести к ухудшению функции почек. У пациентов данной группы рекомендовано проведение контроля функции почек.
Белки-переносчики
Одновременное применение валсартана с ингибиторами белка-переносчика OATP1B1 (рифампицин, циклоспорин) и с ингибитором белка-переносчика MRP2 (ритонавир) может проводить к увеличению системной биодоступности валсартана.
ГХТЗ
Другие гипотензивные препараты
Тиазидные диуретики усиливают антигипертензинный эффект других гипотензивных препаратов (в том числе гуанетидина. метиядопы, бета-адреноблокаторов., вазодилатирующих средств, БМКК, ингибиторов АПФ. АРА II, прямых ингибиторов ренина).
Курареподобные миорелаксанты
Тиазидные диуретики, включая ГХТЗ, потенцируют действие курареподобных миорелаксантов, например, тубокурарина хлорид).
НПВП
Возможно уменьшение диуретического и антшипертензивного действия тиазидного компонента препарата Ко-Вамлосет при одновременном применении с НПВП, например, с ацетилсалициловой кислотой, индометацином. Сопутствующая гиповолемия может привести к развитию острой почечной недостаточности.
Лекарственные препараты, влияющие на содержание калия в сыворотке крови
Риск развития гипокалиемии увеличивается при одновременном применении других диуретиков, глюкокортикостероидов, адренокортикотропного гормона, амфотерицина В, карбеноксолона и ацетилсалициловой кислоты (в дозе более 3 г).
Лекарственные препараты, влияющие на содержание натрия в сыворотке крови
Гипонатриемический эффект, вызываемый диуретиками, может усиливаться при одновременном применении с антидепрессантами, антипсихотическими, противосудорожными препаратами и т. д. Следует соблюдать осторожность при длительном одновременном применении препарата Ко-Вамлосет с вышеуказанными препаратами.
Гипогликемические средства
При применении ГХТЗ отмечается изменение толерантности к глюкозе, в связи с чем у пациентов с сахарным диабетом может потребоваться коррекция доз инсулина и гипогликемических средств для приема внутрь.
Поскольку при применении ГХТЗ с метформииом возможно развитие лактоацидоза (вследствие нарушения функции почек на фоне терапии ГХТЗ), следует соблюдать осторожность при применении препарата Ко-Вамлосет у пациентов, получающих лечение метформииом.
Сердечные гликозиды
Гипокалиемия и гиномагниемия (нежелательные эффекты тиазидных диуретиков) могут способствовать развитию нарушений ритма сердца у пациентов, получающих сердечные гликозиды.
Н- и м-холиноблокаторы
Н- и м—холиноблокаторы (в т. ч. атропин, бипериден) могут увеличивать биодоступность ГХТЗ, что связано с уменьшением перистальтики желудочно-кишечного тракта и скорости опорожнения желудка. Соответственно, стимуляторы моторики желудочно-кишечного тракта (цизаприд) могут уменьшать биодоступность ГХТЗ.
Анионообменные смолы
Всасывание ГХТЗ уменьшается в присутствии колестирамина и колестипола. ГХТЗ следует принимать за 4 часа или через 4-6 часов после приема укачанных соединений.
Витамин D и соли кальция
Одновременный прием ГХТЗ с витамином D или препарата, который может приводить к увеличению содержания кальция в сыворотке крови.
Циклоспорин
При одновременном применении ГХТЗ и циклоспорина увеличивается риск развития гиперурикемии и появление симптомов, напоминающих подагру.
Метимдопа
Сообщалось о случаях развития гемолитической анемии при одновременном применении ГХТЗ и метилдопы.
Другие виды взаимодействия
Одновременное применение тиазидных диуретиков, включая ГХТЗ. может привести к увеличению частоты реакций гиперчувствитсльности к аллопуринолу, увеличению риска развития побочных эффектов амантадина, усилить гипергликемический эффект диазоксида, уменьшению выведения почками препаратов, обладающих цитотоксическим действием (например, циклофосфамида, метотрексата), к потенцированию их миелосупрессииного действия. Также ГХТЗ может уменьшать ответ организма на введение прессорных аминов (норадреналин), однако этот эффект клинически не значим и не может препятствовать одновременному применению препаратов.
Этанол, барбитураты и наркотические средства
Одновременное применение с ГХТЗ может способствовать развитию ортостатической гипотензии.
Особые указания
Безопасность и эффективность применения амлодипина при гипертоническом кризе не установлена.
Дефицит натрия и/или гиповолемия
Выраженная артериальная гипотензия, включая ортостатическую гинотензию, отмечалась у 1,7 % пациентов, получавших максимальную дозу комбинации амлодипин валсартан — ГХТЗ (10 мг + 320 мг + 25 мг) по сравнению с 1,8 % пациентов, получавших комбинацию валсартан + ГХТЗ (320мг + 25 мг), 0.4 % пациентов, получавших комбинацию амлодипин — валсартан (10 мг + 320 мг) и 0.2% пациентов, получавших комбинацию амлодипин -ГХТЗ (25мг+10мг) в контролируемом исследовании с участием пациентов с неосложненной артериальной гипертензией умеренной или тяжелой степени.
У пациентов с дефицитом натрия и/или гппонолсмией. например, у пациентов, получающих высокие дозы диуретиков, возможно развитие симптоматической г и потен а и в начале терапии препаратом Ко-Вамлоеет. Данную комбинацию следует применять только после коррекции гипонатриемии и/ил и гиповолемии.
В случае развития выраженной артериальной гипотензии на фоне применения препарата Ко-Вамлосет пациента следует привести и положение лежа на спине и, если необходимо, провести внутривенную инфузию 0.9 % раствора натрия хлорида. Лечение препаратом можно продолжить после стабилизации АД.
Изменения содержания электролитов в плазме крови
Ко-Вамлосет
В контролируемом исследовании у многих пациентов при применении комбинации амлодипин + валсартан + ГХТЗ эффекты валсартана в дозе 320 мг и ГХТЗ в дозе 25 мг на содержание калия в сыворотке крови почти уравновешивали друг друга. У других пациентов один из эффектов мог преобладать. Периодическое определение содержания электролитов в плазме крови с целью выявления возможного дисбаланса электролитов следует выполнять через установленные интервалы времени.
Периодическое определение содержания электролитов, в частности калия, в сыворотке крови следует проводить с соответствующими интервалами с целью выявления возможных электролитных нарушений, особенно у пациентов с факторами риска, например, с нарушением функции почек, применением других лекарственных препаратов или наличием электролитных нарушений в анамнезе.
Валсартан
Одновременное применение с биологически активными добавками, содержащими калий, калий сберегающими диуретиками, эплереноном, калийсодержащими заменителями соли или с другими препаратами, которые могут вызывать увеличение содержания калия в плазме крови (например, с гепарином), не рекомендуется. Следует контролировать содержание калия в плазме крови.
ГХТЗ
Терапию препаратом Ко-Вамлосст следует начинать только после устранения гипокалиемии и сопутствующей гипомагниемии. Тиазидные диуретики могут способствовать повторному возникновению гипокалиемии или усугублять уже имеющуюся гипокалиемию. Тиазидные диуретики следует применять с осторожностью у пациентов с состояниями, при которых отмечаются повышенные потери калия, например, при нефропатиии преренальным (кардиогенным) нарушением функции почек. Если гипокалиемия развивается на фоне лечения ГХТЗ, применение препарата Ко-Вамлосет следует прекратить до стабильной нормализации содержания калия в плазме крови.
Тиазидные диуретики могут способствовать повторному развитию гипопатриемии и гипохлоремического алкалоза либо усугублять уже имеющуюся гипонатриемию.
Отмечалась гипопатриемия, сопровождающаяся неврологическими симптомами (тошнота, прогрессирующая дезориентация, апатия). Лечение ГХ’ГЗ следует начинать только после устранения уже имеющейся гипонатриемии. В случае тяжелой или быстро развивающейся гипонатриемии на фоне применения комбинации амлодипин + валсартан + ГХТЗ лечение необходимо прекратить до нормализации содержания натрия в плазме крови.
У всех пациентов, получающих тиазидные диуретики, необходимо периодически контролировать состояние на предмет электролитных нарушений, особенно содержания калия, натрия и магния в плазме крови.
Нарушение функшш почек
Тиазидные диуретики могут способствовать развитию азотемии у пациентов с хроническим заболеванием почек. При применении препарата Ко-Вамлосет у пациентов с нарушением функции почек рекомендовано периодически контролировать содержание электролитов (включая калий), концентрации креатинина и мочевой кислоты в сыворотке крови. Препарат Ко-Вамлосет противопоказан пациентам с тяжелым нарушением функции почек, анурией и пациентам, находящимся на диализе (см. раздел «Противопоказания»).
Пациентам с нарушением функции почек легкой и умеренной степени (СКФ > 30 мл/мин/!,73 м2 площади поверхности тела) коррекция дозы препарата Ко-Вамлосет не требуется.
Стеноз почечной артерии
У пациентов с односторонним или двусторонним стенозом почечной артерии или стенозом артерии единственной почки прием препарата Ко-Вамлосет может сопровождаться повышением концентраций мочевины и креатинипа в сыворотке крови. поэтому у таких пациентов препарат Ко-Вамлосет должен применяться с осторожностью.
Трансплантация почки
На сегодняшний день отсутствуют данные о безопасном применении комбинации амлодипин + валсартап + ГХТЗ у пациентов после трансплантации почки.
Нарушение функции печени
Валсартан выводится, главным образом, в неизмененной форме с желчью. Т1/2 амлодипина длительный, и значения AUC выше у пациентов с нарушением функции печени; рекомендаций по подбору дозы нет. У пациентов с нарушением функции печени легкой или умеренной степени без холестаза максимальная рекомендованная доза составляет 80 mi- вал саргана, поэтому препарат Ко-Вамлосет противопоказан этим пациентам.
Аигионевротический отек
У пациентов, получавших валсартан. отмечался апгиопевротический ore к, включая отек гортани и глотки, вызывающий обструкцию дыхательных путей и/или осек лица, губ. гортани и/или языка. У некоторых из данных пациенток ранее отмечался ангноневротический отек на фоне применения других лекарственных препаратов, включая ингибиторы АИФ. В случае развития ангионевротического отека, прием препарата Ко-Вамлосет следует незамедлительно прекратить и не применять препарат повторно.
ХСН и ишемическая болезнь сердца, состояние после инфаркта миокарда
У восприимчивых пациентов возможны изменения функции почек вследствие иигибирования РААС. У пациентов, функция почек которых зависит от активности РААС (например, пациенты с ХСН III-IV функционального класса [по классификации NYНA]). терапия ингибиторами АПФ и АРАII может сопровождаться олигурией и/или прогрессирующей азотемией и в редких случаях может приводить к острой почечной недостаточности и смерти. Аналогичные исходы отмечались на фоне терапии валсартаном. Оценка состояния пациентов с ХСН или состояния после инфаркта миокарда всегда должна включать обследование функции почек.
В долгосрочном плацебо-коптролируемом исследовании (PRAISE-2) амлодипина у пациентов с ХСН III и IV функционального класса по классификации NYНA неишемической этиологии па фоне применения амлодипина отмечалась повышенная частота встречаемости отека легких, несмотря на незначительное различие в частоте развития усугубления сердечной недостаточности в сравнении с плацебо. У пациентов с ХСН III и IV функционального класса но классификации NYHA БМКК. включая амлодипин, следует применять с осторожностью, поскольку они могут увеличить риск развития сердечно-сосудистых событий и смерти.
Рекомендуется соблюдать осторожность у пациентов с ХСН и ишемической болезнью сердца, поскольку имеющиеся данные в этих популяциях пациентов ограничены.
Стеноз аортального и митрального кшпана
Как и при применении других сосудорасширяющих средств, следует соблюдать осторожность у пациентов со стенозом митрального клапана или выраженным стенозом аортального клапана, имеющим невысокую степень тяжести.
Беременность
Терапию АРЛ II не следует начинать во время беременности. Пациентки, планирующие беременность, должны перейти на альтернативную гипотензивную терапию с установленным профилем безопасности применения во время беременности. В случае диагностики беременности терапию АРЛ II следует немедленно прекратить или перейти на альтернативную гипотензивную терапию с установленным профилем безопасности применения во время беременности.
Первичный гиперальдостеронизм
Пациенты с первичным гиперальдостеронизмом не должны применять АРА II (в том числе валсартан). поскольку РААС у таких пациентов не активирована. Поэтому препарат Ко-Вамлосет не следует применять в данной популяции.
Системная красная волчанка
При применении тиазидных диуретиков, включая ГХТЗ, сообщалось об усугублении течения или развитии системной красной волчанки.
Другие метаболические нарушения
Тиазидные диуретики, включая ГХТЗ, могут изменять толерантность к глюкозе и повышать концентрацию холестерина, три гл и пер и до в и мочевой кислоты в сыворотке крови. У пациентов с сахарным диабетом может потребоваться коррекция дозы инсулина или гипоксемических препаратов для приема внутрь.
В связи с содержанием компонента ГХТЗ препарат Ко-Вамлосет противопоказан при симптоматической гиперурнкемии. ГХТЗ может повышать концентрацию мочевой кислоты в сыворотке крови в связи со снижением клиренса мочевой кислоты и вызывать либо усугублять гиперуриксмию. а также способствовать развитию подагры у восприимчивых пациентов.
Тиазиды уменьшают выведение кальция почками и могут вызывать периодическое и незначительное повышение концентрации сывороточного кальция при отсутствии известных нарушений метаболизма кальция. Препарат Ко-Вамлосет противопоказан пациентам с гиперкальциемией и его следует применять только после устранения имеющейся гиперкальциемии. Прием препарата Ко-Вамлосет следует прекратить, если во время лечения развивается гинеркалышемия. Следует периодически контролировать сывороточную концентрацию кальция во время терапии тиазидами. Выраженная гиперкальциемия может быть признаком скрытого Еиперпаратиреоза. Перед исследованием функции паращитовидных желез следует прервать терапию тиазидами.
Фоточувствительность
При применении тиазидных диуретиков были зарегистрированы случаи реакции фоточувствительности (см. раздел «Побочное действие»). При развитии реакции фоточувствительности во время лечения препаратом Ко-Вамлосет рекомендуется прекратить терапию. При необходимости повторного применения диуретика рекомендуется зашита участков кожи, подвергающихся воздействию солнечных лучей или искусственного УФА излучения.
Острая зикрытоугольная глаукома
ГХТЗ, будучи сульфонамидом, вызывает идиосинкразическую реакцию, приводящую к развитию острой транзиторной миопии и острой закрытоугольной глаукомы. Симптомы включают внезапное снижение остроты зрения или появление боли в глазу, как правило, в течение нескольких часов или недели после начала применения препарата. При отсутствии лечения острая закрытоугольная глаукома может привести к стойкой потере зрения
Первичная терапия состоит в прекращении применения ГХТЗ в кратчайшие возможные сроки. Если внутриглазное давление остается неконтролируемым, может потребоваться неотложное консервативное или хирургическое лечение. Факторами риска развития острой закрытоугольной глаукомы могут быть анамнестические данные об аллергических реакциях на сульфаниламиды и пенициллин.
Общие
Следует соблюдать осторожность у пациентов, ранее имевших гипсрчувствитслыюсть к другим АРА II. Реакции гиперчувствительности к ГХТЗ более вероятны у пациентов с аллергией и бронхиальной астмой.
Пациенты пожилого возраста (> 65 лет)
Следует соблюдать осторожность, включая частый контроль АД, у пациентов пожилого возраста, поскольку имеющиеся данные в данной популяции пациентов ограничены.
Двойная блокада РААС
Одновременное применение ингибиторов АПФ, АРА II или алискирена сопровождается более высокой частотой развития нежелательных явлений, таких как артериальная гипотензия. гиперкалиемия и снижение функции почек (включая острую почечную недостаточность). Если комбинированная терапия путем двойной блокады РААС считается абсолютно необходимой, ее необходимо проводить только под наблюдением специалиста и при тщательном контроле функции почек, содержания электролитов в плазме крови и АД.
Одновременное применение АРА II с препаратами, содержащими алискирен.
Противопоказано у пациенток с сахарным диабетом и/или с умеренной или тяжелой почечной недостаточностью (СКФ менее 60 мл/мин/1.73 м2 плошали поверхности тела) и не рекомендуется у других пациентов. Одновременное применение АРА II с ингибиторами АПФ противопоказано у нацистов с диабетической нефропатией и не рекомендуется у других пациентов.
Гипартонический криз
Не следует применять препарат Ко-Вамлосет для купирования гипертонических кризов.
Допинг тест
При применении препарата Ко-Вамлосет у спортсменов возможны положительные результаты допинг-теста (в связи с наличием в составе препарата ГХТЗ).
Влияние на способность управлять транспортыми средствами, механизмами
Некоторые побочные эффекты препарата, в том числе головокружение или зрительные нарушения, могут отрицательно влиять на способность к выполнению потенциально опасных видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций (управление транспортными средствами, работа с движущимися механизмами). Пациентам, принимающим препарат Ко-Вамлосет, следует соблюдать осторожность при управлении транспортными средствами и при работе с движущимися механизмами.
Форма выпуска
Таблетки, покрытые пленочной оболочкой. 5 мг + 160 мг + 12,5 мг, 10 мг + 160 мг + 12,5 мг, 10 мг + 160 мг + 25 мг.
По 7, 10, 14, 15 таблеток в контурной ячейковой упаковке из комбинированного материала ОПА/Ал/ПВХ и фольги алюминиевой. 1, 2, 4, 8, 12, 14 контурных ячейковых упаковок (по 7 таблеток); 1, 2, 3, 6, 9 контурных ячейковых упаковок (по 10 таблеток); 1, 2, 4, 6, 7 контурных ячейковых упаковок (по 14 таблеток); 1, 2, 4, 6 контурных ячейковых упаковок (по 15 таблеток) вместе с инструкцией по применению помещают в пачку из картона.
Условия хранения
При температуре не выше 25 °С, в оригинальной упаковке. Хранить в недоступном для детей месте.
Срок годности
2 года. Не применять препарат по истечении срока годности.
Условия отпуска
Отпускают по рецепту.
Наименование юридического лица, на имя которого выдано регистрационное удостоверение, адрес
ООО «КРКА-РУС», 143500. Россия, Московская обл., г. Истра, ул. Московская, д. 50
Производитель
ООО «КРКА-РУС». 143500. Россия, Московская обл., г. Истра, ул. Московская, д. 50
Наименование и адрес организации, принимающей претензии потребителей
ООО «КРКА-РУС», 125212. г. Москва. Головинское шоссе, дом 5, корпус 1
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
445 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
РЕКОМЕНДУЕМ
от 65 000 ₽ / шт.
В наличии
УпаковочноеДело — Фасовочно-упаковочное оборудование
Доставка из Ростов-на-Дону
Хит продаж
2 800 ₽ / Упаковка
от 2 Упаковка 2 500 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
1 000 ₽
В наличии
ПРОМЫШЛЕННОЕ ОБОРУДОВАНИЕ
Доставка из Москвы
900 ₽
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
252 ₽
В наличии
ЦЕНТРПРОМКОМПЛЕКТ
Доставка из Москвы
10 080 ₽ / кг
от 1 кг 10 000 ₽ / кг
В наличии
ООО «Аллхим»
Доставка из Белгорода
Цену уточняйте
В наличии
ООО «Нуметек групп»
Доставка из Омска
Цену уточняйте
В наличии
Europa World-Trends
Доставка из Италии
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
223 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
РЕКОМЕНДУЕМ
Цену уточняйте
В наличии
УпаковочноеДело — Фасовочно-упаковочное оборудование
Доставка из Ростов-на-Дону
Новинка
2 700 ₽ / Упаковка
от 2 Упаковка 2 450 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
Цену уточняйте
В наличии
ПРОМЫШЛЕННОЕ ОБОРУДОВАНИЕ
Доставка из Москвы
Цену уточняйте
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
252 ₽
В наличии
ЦЕНТРПРОМКОМПЛЕКТ
Доставка из Москвы
5 467 ₽ / флак
В наличии
ООО «Аллхим»
Доставка из Белгорода
Цену уточняйте
В наличии
ООО «Нуметек групп»
Доставка из Омска
Цену уточняйте
В наличии
Europa World-Trends
Доставка из Италии
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
241 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
2 750 ₽ / Упаковка
от 2 Упаковка 2 500 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
Цену уточняйте
В наличии
ПРОМЫШЛЕННОЕ ОБОРУДОВАНИЕ
Доставка из Москвы
Цену уточняйте
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
8 400 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
Цену уточняйте
В наличии
Europa World-Trends
Доставка из Италии
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
396 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Новинка
2 800 ₽ / Упаковка
от 2 Упаковка 2 100 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
Цену уточняйте
В наличии
ПРОМЫШЛЕННОЕ ОБОРУДОВАНИЕ
Доставка из Москвы
Цену уточняйте
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
от 4 708 ₽ / уп
от 5 уп 4 500 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
Цену уточняйте
В наличии
Europa World-Trends
Доставка из Италии
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
1 732 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
2 700 ₽ / Упаковка
от 2 Упаковка 2 450 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
Цену уточняйте
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
от 3 410 ₽ / уп
от 5 уп 3 300 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
82,05 ₽ / кг
от 1000 кг 71,34 ₽ / кг
В наличии
ООО «Снабтехмет»
Доставка из Екатеринбурга
220 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
3 000 ₽ / Упаковка
от 2 Упаковка 2 450 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
Цену уточняйте
В наличии
АЛЬФА-ГРУПП
Доставка из Москвы
от 7 590 ₽ / уп
от 5 уп 7 400 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
528 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Рекомендуем
2 850 ₽ / Упаковка
от 2 Упаковка 2 500 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
от 8 855 ₽ / кг
В наличии
ООО «Аллхим»
Доставка из Белгорода
681 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Рекомендуем
2 850 ₽ / Уп
от 2 Уп 2 500 ₽ / Уп
В наличии
Bezdiet.biz
Доставка из Москвы
от 10 994 ₽ / кг
В наличии
ООО «Аллхим»
Доставка из Белгорода
155 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
2 750 ₽ / Уп
от 2 Уп 2 500 ₽ / Уп
В наличии
Bezdiet.biz
Доставка из Москвы
от 9 680 ₽ / уп
от 5 уп 9 500 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
2 296 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
3 000 ₽ / Упаковка
от 2 Упаковка 2 450 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
от 6 842 ₽ / уп
от 5 уп 6 700 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
3 856 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Хит продаж
3 000 ₽ / Упаковка
от 2 Упаковка 2 450 ₽ / Упаковка
В наличии
Bezdiet.biz
Доставка из Москвы
от 21 296 ₽ / уп
от 5 уп 20 800 ₽ / уп
В наличии
ООО «Аллхим»
Доставка из Белгорода
718 ₽
В наличии
ООО «Вардер»
Доставка из Москвы
Илсира® (Ilsira) инструкция по применению
📜 Инструкция по применению Илсира®
💊 Состав препарата Илсира®
✅ Применение препарата Илсира®
📅 Условия хранения Илсира®
⏳ Срок годности Илсира®
Описание лекарственного препарата
Илсира®
(Ilsira)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для печатного издания справочника Видаль 2023 года.
Дата обновления: 2022.11.11
Владелец регистрационного удостоверения:
Контакты для обращений:
БИОКАД АО
(Россия)
Код ATX:
L04AC
(Ингибиторы интерлейкина)
Лекарственная форма
| Илсира® |
Р-р д/п/к введения 180 мг/1 мл: шприцы 0.9 мл 2 или 4 шт. в компл. с салфетками рег. №: ЛП-006244 |
Форма выпуска, упаковка и состав
препарата Илсира®
Раствор для п/к введения прозрачный, желто-коричневого цвета; возможно наличие легкой опалесценции.
* предварительно наполненный шприц.
Вспомогательные вещества: натрия ацетата тригидрат — 0.392 мг, глицин — 6.8 мг, маннитол — 20.7 мг, кислота уксусная ледяная — до pH 5.0, вода д/и — до 0.9 мл.
0.9 мл — шприцы трехкомпонентные из бесцветного стекла (1) — упаковки ячейковые контурные (2) в комплекте с салфетками спиртовыми (2 шт.) — пачки картонные.
0.9 мл — шприцы трехкомпонентные из бесцветного стекла (1) — упаковки ячейковые контурные (4) в комплекте с салфетками спиртовыми (4 шт.) — пачки картонные.
На каждый шприц наклеивают самоклеящуюся этикетку.
Фармакологическое действие
Левилимаб — рекомбинантное моноклональное антитело подкласса IgG1, высокогомологичное нативным человеческим антителам, связывающееся с α-субъединицей рецептора к интерлейкину-6 (ИЛ-6). Молекула левилимаба содержит вариабельные фрагменты легких и тяжелых цепей глубокой оптимизации и константные домены с полностью человеческой последовательностью. Левилимаб связывается и блокирует как растворимые (рИЛ6Р), так и мембранные рецепторы ИЛ-6 (мИЛ6Р). Блокада обеих форм рецептора позволяет предотвратить реализацию ИЛ-6-ассоциированного провоспалительного каскада, препятствует активации антиген-представляющих клеток, В- и Т-лимфоцитов, моноцитов и макрофагов, эндотелиальных клеток и фибробластов, и избыточной продукции других провоспалительных цитокинов. ИЛ-6 является ключевым элементом синдрома массивного высвобождения цитокинов (синдрома «цитокинового шторма», гемофагоцитарного лимфогистиоцитоза или синдрома активации макрофагов), который может привести к острому респираторному дистресс-синдрому, полиорганной недостаточности и являться причиной летального исхода. Массивное высвобождение цитокинов («цитокиновый шторм») наблюдается у пациентов, получающих иммуносупрессивную терапию, включая деплецирующие агенты (в частности моноклональные антитела к рецепторам Т- и В-лимфоцитов), а также при тяжелых инфекционных заболеваниях, в т.ч. у пациентов с COVID-19. Высокий уровень ИЛ-6 в крови ассоциирован с более тяжелым течением новой коронавирусной инфекции и выраженными изменениями легких, что обусловливает потребность в интенсивной терапии и увеличивает риск летального исхода при COVID-19. ИЛ-6 – единственный цитокин, непосредственно индуцирующий синтез острофазовых белков в гепатоцитах: С-реактивного белка (СРБ), фибриногена, сывороточного амилоидного белка А-SAA, гепсидина, лептина. Кроме того, ИЛ-6 участвует в активации и поддержании местных воспалительных реакций (образование паннуса в синовии, стимуляция остеокластогенеза — эрозии хрящевой ткани, остеопороз), что наблюдается в патогенезе ревматоидного артрита.
Специфическая противовоспалительная активность левилимаба продемонстрирована в тестах in vitro и in vivo. Левилимаб оказывает антипролиферативное действие на культуру клеток DS-1, вызывая дозозависимое ингибирование роста клеток. На модели коллаген-индуцированного артрита у яванских макак (Macaca fascicularis) многократное (1 раз в неделю в течение 7 недель) п/к введение левилимаба сопровождается снижением выраженности воспалительной реакции в суставах, что подтверждено при гистологическом исследовании (значимое снижение выраженности воспалительных и дегенеративных изменений хрящевой ткани).
Изменение параметров фармакодинамических маркеров (нарастание концентрации рИЛ6Р, насыщение мИЛ6Р, нарастание концентрации ИЛ-6) свидетельствует о высокоэффективной дозозависимой нейтрализации препаратом левилимаб обеих форм рецептора ИЛ-6, что в свою очередь сопровождается быстрым и выраженным снижением сывороточной концентрации СРБ, отражающим эффективное подавление воспалительного процесса. В клинических исследованиях левилимаба продемонстрировано блокирование до 90% мембранных рецепторов к ИЛ-6 в течение первых 2 часов от момента однократного п/к введения препарата в дозе 1.6 мг/кг и более.
Фармакокинетика
Всасывание и распределение
При однократном п/к введении левилимаба наблюдается дозозависимый рост его концентрации в сыворотке крови. После введения препарат начинает обнаруживаться в сыворотке крови пациентов через 2-12 ч, и его концентрация нарастает, достигая максимальных значений через 96 [72-168] ч. Дозы препарата, превышающие 2.0 мг/кг, продемонстрировали двухфазный характер увеличения концентрации: первый пик наблюдался в период 48-72 ч, второй – к 168 ч с последующим снижением до неопределяемых значений к 70 дню.
После однократного п/к введения препарата в дозе 162 мг Cmax левилимаба в сыворотке крови составляла 17543 [10975; 28323] нг/мл, а значения показателя AUC, рассчитанного в период 0-168 ч (AUC0-168) – 1866231 [1297632-3719014] нг/мл×ч.
При многократном введении левилимаба пациентам с ревматоидным артритом значения суммарной AUC, рассчитанной в период 0-2016 ч после введения (AUC0-2016), составили 189580779 [134794695; 230680771] нг/мл×ч при введении 1 раз в неделю и 50763951 [34465213.5; 65810194.5] нг/мл×ч при введении 1 раз в 2 недели. Показатель Сmax-mult при повторных введениях нарастал и достигал значений 201024 [151563-246408] нг/мл при еженедельном введении препарата и 51570 [37201-71740] нг/мл при введении 1 раз в 2 недели. При этом Tmax составляло 1848 [1512; 2016] ч при еженедельном введении препарата и 1848 [1512; 1848] ч при введении 1 раз в 2 недели соответственно. Стационарный Vd составил 7871.029 [4226.795; 13363.547] мл при введении препарата 1 раз в неделю и 7130.453 [5532.978; 11387.959] мл при введении 1 раз в 2 недели.
При повторных введениях отмечается накопление препарата, с ростом Cmax в 6.5-14.2 раза при еженедельном введении и в 1.9-4.2 раза при введении препарата 1 раз в 2 недели. Коэффициент кумуляции (AR) составил 10.932 [6.446; 14.178] для еженедельного введения препарата и 2.593 [1.902; 4.164] для введения 1 раз в 2 недели.
Таким образом, у пациентов с ревматоидным артритом многократное п/к введение левилимаба 1 раз в неделю обеспечивает более высокую сывороточную концентрацию и экспозицию по сравнению с введением 1 раз в 2 недели.
Выведение
Общий клиренс (Cl) левилимаба после однократного введения в дозе 2.2 мг/кг составил 35.288±11.7 мл/ч, а в дозе 2.9 мг/кг показатель Cl – 25.974±1.1 мл/ч. T1/2 однократной п/к дозы 2.9 мг/кг составил 133.683 [92.754; 197.197] ч. Значения показателей, характеризующих период элиминации, обладают дозозависимостью (показатели среднего времени пребывания препарата в организме (MRT) и T1/2 нарастают с увеличением введенной дозы, а Cl – снижается), что говорит о нелинейной фармакокинетике препарата, обусловленной мишень-опосредованными распределением и элиминацией.
Фармакокинетика у особых групп пациентов
Пациенты с почечной и печеночной недостаточностью: специальных исследований у данной категории пациентов не проводилось; фармакокинетические данные у больных с почечной и печеночной недостаточностью отсутствуют.
Пациенты в возрасте старше 65 лет: фармакокинетические данные у лиц в возрасте старше 65 лет отсутствуют.
Показания препарата
Илсира®
Новая коронавирусная инфекция (COVID-19)
- патогенетическая терапия синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (CОVID-19).
Ревматоидный артрит
- ревматоидный артрит умеренной или высокой степени активности у взрослых с отсутствием адекватного ответа на терапию одним или несколькими болезнь-модифицирующими противоревматическими препаратами, в т.ч. для торможения рентгенологической прогрессии. Левилимаб применяется в комбинированной терапии с метотрексатом и/или другими синтетическими базисными противовоспалительными препаратами.
Режим дозирования
Для п/к введения.
Препарат Илсира® предназначен для введения как в амбулаторно-поликлинических, так и в стационарных условиях.
Применение левилимаба должно осуществляться под контролем врача. В случае длительного применения препарата, в частности для терапии ревматоидного артрита, если врач считает это возможным, после соответствующего обучения технике п/к инъекций пациенты могут самостоятельно вводить себе препарат.
Препарат Илсира® вводят п/к с помощью преднаполненного шприца в область передней брюшной стенки (отступая не менее 5 см от пупка), передней и боковой поверхности бедра или средней трети наружной части плеча.
Не следует вводить препарат в места с поврежденной или измененной кожей (с наличием уплотнений, покраснений, новообразований, гиперпигментаций или повышенной чувствительности).
С целью патогенетической терапии синдрома высвобождения цитокинов при тяжелом течении новой коронавирусной инфекции (CОVID-19) рекомендуемая доза препарата Илсира® составляет 324 мг однократно в виде двух п/к инъекций по 162 мг каждая. В случае недостаточного эффекта первой дозы левилимаба возможно повторное введение препарата через 48–96 ч в дозе 324 мг в виде двух п/к инъекций по 162 мг каждая. Решение о необходимости повторного введения принимается исключительно врачом.
Для терапии ревматоидного артрита рекомендуемая доза препарата Илсира® составляет 162 мг 1 раз в неделю.
При достижении ремиссии заболевания возможно применение в режиме 162 мг п/к 1 раз в 2 недели. Пациентам, не достигшим ремиссии, рекомендовано продолжить применение препарата в дозе 162 мг п/к 1 раз в неделю. Пациентам, имеющим нарастание активности заболевания после снижения кратности введений, рекомендовано возобновить применение препарата в дозе 162 мг п/к 1 раз в неделю.
При развитии нежелательных явлений в ходе терапии ревматоидного артрита, связанных с изменением лабораторных показателей, следует провести коррекцию дозы и режима введения в соответствии с рекомендациями в таблицах 1, 2 и 3.
Таблица 1. Рекомендации по коррекции дозы при повышении активности печеночных ферментов АЛТ или АСТ
Таблица 2. Рекомендации по коррекции дозы при снижении абсолютного числа нейтрофилов (АЧН)
Таблица 3. Рекомендации по коррекции дозы при снижении количества тромбоцитов
Пропуск дозы при терапии ревматоидного артрита
При пропуске очередного введения по любой причине инъекция препарата Илсира® должна быть произведена как можно быстрее. Новый отсчет для даты следующего введения начинают с момента фактически проведенной инъекции препарата Илсира®.
Указания по применению
Подготовка к проведению п/к инъекции
- Тщательно вымойте руки.
img_ilsira_0.tif|jpg
- Извлеките упаковку со шприцем из холодильника. Затем извлеките шприц с лекарственным препаратом из картонной пачки. Осмотрите шприц, а также лекарственный препарат, находящийся в нем. Нельзя использовать шприц в случае:
- помутнения раствора, наличия в препарате посторонних видимых частиц;
- изменения цвета;
- повреждения любых частей шприца;
- истечения срока годности (годен до …), указанного на картонной пачке, а также на этикетке шприца.
- Оставьте шприц при комнатной температуре приблизительно на 25-30 мин. Не следует согревать шприц с препаратом каким-либо другим способом.
img_ilsira_2-1.tif|jpg
- Подготовьте спиртовую салфетку/ватный тампон.
На данном этапе не следует снимать колпачок шприца.
Техника выполнения п/к инъекции препарата Илсира® в преднаполненном шприце
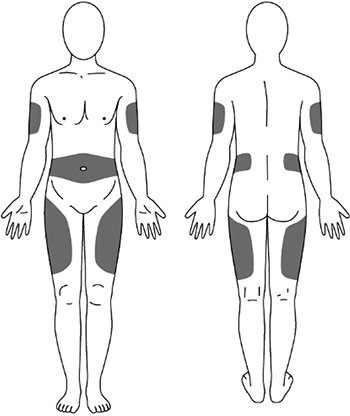
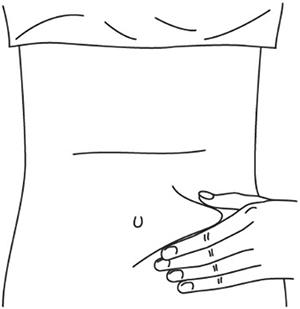
1. Выберите место инъекции (передняя брюшная стенка (отступая не менее 5 см от пупка), передняя и боковая поверхность бедра или средняя треть наружной части плеча (возможные места для инъекций закрашены на рисунке ниже)).
2. Нельзя вводить препарат в место на коже, где имеется болезненность, покраснение, уплотнение или кровоподтек. Эти признаки могут указывать на наличие инфекции. Также не следует вводить препарат в места родинок, гиперпигментаций и шрамов.
3. Место укола необходимо обработать спиртовой салфеткой круговыми движениями.
4. Шприц не встряхивать.
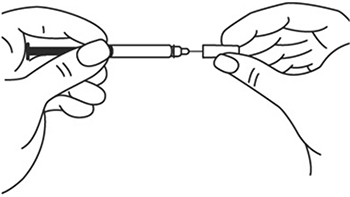
5. Снимите колпачок с иглы, не дотрагиваясь до иглы и избегая прикосновения к другим поверхностям.
6. Одной рукой возьмите в складку обработанную кожу.
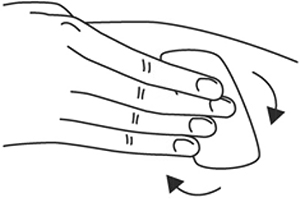
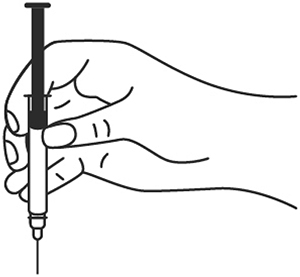
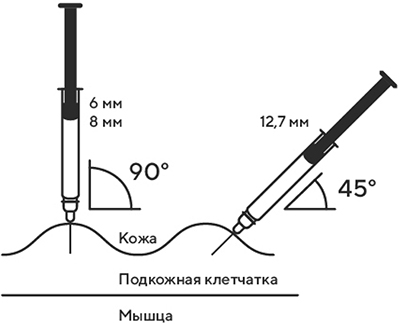
7. В другую руку возьмите шприц, держа его градуированной поверхностью вверх. Введение препарата необходимо осуществлять под углом 45 или 90 градусов к поверхности кожи в зависимости от толщины кожи и выраженности подкожно-жирового слоя (у худощавых пациентов введение препарата осуществляется под углом 45 градусов, у пациентов с толщиной кожной складки более 1.5 см допустимо введение под углом 90 градусов).
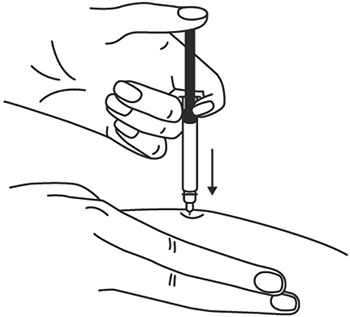
8. Одним быстрым движением полностью введите иглу в кожную складку.
9. После введения иглы отпустите складку кожи.
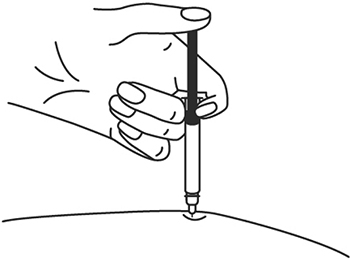
10. Введите весь раствор медленным постоянным надавливанием на поршень шприца в течение 2-5 сек.
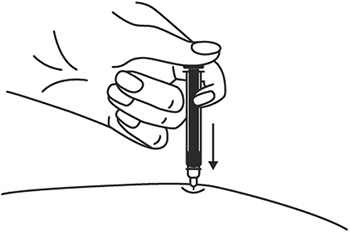
11. Когда шприц будет пустым, выньте иглу из кожи под тем же углом.
12. Кусочком марли слегка прижмите область инъекции в течение 10 сек, но ни в коем случае не трите поверхность. Из места инъекции может выделиться небольшое количество крови. При желании можно воспользоваться пластырем.
13. После инъекции шприц повторно не использовать.
14. Вторую инъекцию препарата Илсира® для достижения общей дозы 324 мг выполнить аналогичным образом.
15. При последующих инъекциях следует менять место введения.
Утилизация расходного материала
Неиспользованный раствор препарата, использованные шприцы, салфетки/ватные тампоны и другие расходные материалы подлежат утилизации с применением закрывающегося контейнера, устойчивого к проколам для острых предметов из пластика или стекла.
Не допускать хранения использованных шприцев в местах, доступных для детей.
Побочное действие
В рамках проведенных клинических исследований у здоровых добровольцев, пациентов с ревматоидным артритом и тяжелым течением новой коронавирусной инфекции (COVID-19) препарат Илсира® показал благоприятный профиль безопасности. Наиболее частыми нежелательными реакциями в проведенных клинических исследованиях были повышение активности АЛТ и АСТ, нейтропения и повышение уровня липидов в крови. Спектр зарегистрированных нежелательных явлений, связанных с применением препарата Илсира®, был ожидаемым для класса ингибиторов рецепторов ИЛ-6. Летальных исходов, связанных с терапией препаратом Илсира®, в ходе клинических исследований не было.
В данной инструкции нежелательные реакции представлены в соответствии с международным словарем нежелательных реакций MedDRA. Ниже приведен перечень нежелательных реакций, зарегистрированных у пациентов, получавших левилимаб в рамках клинических исследований, и имеющих определенную, вероятную или возможную степень связи с приемом препарата. Частота указана с учетом следующих критериев: очень часто (≥1/10), часто (от ≥1/100 до <1/10), нечасто (от ≥1/1000 до <1/100), редко (от ≥1/10000 до <1/1000), очень редко (≤10000).
* В клинических исследованиях регистрировались местные реакции в виде эритемы и кожного зуда.
** Данное НР проявлялось повышением АСТ и АЛТ и не сопровождалось другими симптомами токсического гепатита на фоне множественной лекарственной терапии.
Также в ходе клинической разработки регистрировались единичные нежелательные явления, для которых в настоящее время связь с применением левилимаба не установлена достоверно: воспаление очага кожного поражения, астения, анемия, лимфаденит, лимфоцитоз, отклонение от нормы процедуры визуализации легких, снижение активности АСТ.
В качестве нарушений со стороны иммунной системы в пострегистрационном периоде наблюдались единичные реакции гиперчувствительности (анафилактический шок, ангиоотек), что согласуется с известным профилем безопасности препаратов класса ингибиторов рецепторов ИЛ-6.
Противопоказания к применению
- гиперчувствительность к левилимабу, а также к любому из вспомогательных веществ препарата;
- клинически значимые активные инфекции, включая туберкулез;
- сепсис, обусловленный патогенами, отличными от COVID-19;
- вирусный гепатит В;
- нейтропения менее 0.5×109/л;
- тромбоцитопения менее 50×109/л;
- повышение активности АСТ или АЛТ более чем в 5 раз;
- печеночная недостаточность тяжелой степени (класс С по классификации Чайлд-Пью);
- почечная недостаточность тяжелой степени и в терминальной стадии (СКФ менее 30 мл/мин);
- детский и подростковый возраст до 18 лет;
- беременность;
- период грудного вскармливания;
- комбинированное применение с ингибиторами ФНОα или применение в течение 1 месяца после терапии моноклональными антителами к ФНОα.
С осторожностью
Следует соблюдать осторожность при назначении левилимаба следующим категориям пациентов:
- с хроническими и рецидивирующими инфекциями или с указаниями в анамнезе на них;
- с сопутствующими заболеваниями, предрасполагающими к развитию инфекций;
- в периоде ранней реконвалесценции после тяжелых и среднетяжелых инфекционных заболеваний;
- после недавно проведенной вакцинации живыми аттенуированными вакцинами;
- с печеночной недостаточностью легкой и средней степени тяжести (класс А и В по классификации Чайлд-Пью);
- с почечной недостаточностью средней степени тяжести (СКФ <60 мл/мин и ≥30 мл/мин);
- с дивертикулитом, дивертикулезом и язвенным поражением органов ЖКТ, в т.ч. в анамнезе, в связи с риском перфорации ЖКТ;
- с демиелинизирующими заболеваниями;
- у получающих иммуносупрессивную терапию после трансплантации органов.
В связи со способностью левилимаба подавлять реакции острой фазы воспаления следует проявлять особую осторожность в отношении раннего выявления инфекционных заболеваний на фоне терапии.
В связи с ограниченными данными клинических исследований о применении левилимаба у пациентов пожилого возраста следует соблюдать осторожность при назначении препарата пациентам этой возрастной группы.
Применение при беременности и кормлении грудью
Беременность
Исследований влияния на плод у беременных женщин не проводилось. Известно, что моноклональные антитела могут проникать через плацентарный барьер. Препарат Илсира® противопоказан к применению во время беременности. Женщины детородного возраста и их половые партнеры должны использовать эффективные средства контрацепции в период проведения терапии левилимабом.
Период грудного вскармливания
Неизвестно, проникает ли левилимаб в грудное молоко. Учитывая то, что иммуноглобулины класса G, к которым относится левилимаб, могут выделяться с грудным молоком, препарат Илсира® противопоказан к применению в период грудного вскармливания.
Фертильность
Данные о влиянии препарата на фертильность у людей отсутствуют.
Применение при нарушениях функции печени
Противопоказано применение препарата при печеночной недостаточности тяжелой степени (класс С по классификации Чайлд-Пью).
С осторожностью следует назначать препарат пациентам с печеночной недостаточностью легкой и средней степени тяжести (класс А и В по классификации Чайлд-Пью).
Применение при нарушениях функции почек
Противопоказано применение препарата при почечной недостаточности тяжелой степени и в терминальной стадии (СКФ менее 30 мл/мин).
С осторожностью следует назначать препарат пациентам с почечной недостаточностью средней степени тяжести (СКФ <60 мл/мин и ≥30 мл/мин).
Применение у детей
Противопоказано применение препарата в детском и подростковом возрасте до 18 лет.
Применение у пожилых пациентов
Следует соблюдать осторожность при назначении препарата пациентам пожилого возраста.
Особые указания
Прослеживаемость
В целях улучшения прослеживаемости биотехнологических лекарственных препаратов наименование и номер серии назначаемого лекарственного препарата левилимаб должны указываться в медицинской документации пациента.
Инфекции
Наличие таких потенциально тяжелых инфекций как ВИЧ, активный гепатит В, сифилис, туберкулез, относится к противопоказаниям для назначения левилимаба. Левилимаб не следует применять у пациентов с активным течением инфекционных заболеваний, включая локализованные инфекции. Учитывая иммуносупрессивное действие левилимаба, терапия этим препаратом потенциально может приводить к обострению хронических инфекций и повышению риска первичного инфицирования.
При реактивации гепатита В или развитии серьезных инфекций терапию левилимабом следует прекратить и назначить соответствующую этиотропную терапию.
Соблюдение осторожности требуется в отношении пациентов с рецидивирующими инфекционными заболеваниями в анамнезе, а также лиц, имеющих факторы риска развития инфекций в виде сопутствующих заболеваний или сопутствующей терапии.
С учетом подавления левилимабом реакций острой фазы воспаления симптомы инфекционного заболевания могут быть стерты, что следует учитывать при раннем выявлении серьезных инфекций у пациентов, получающих препарат Илсира®. При появлении любых симптомов, свидетельствующих о развитии инфекционного заболевания на фоне применения левилимаба, пациенту следует немедленно обратиться к врачу для своевременной диагностики и назначения терапии.
Туберкулез
Пациентам с активным туберкулезом терапия препаратом Илсира® противопоказана. Перед назначением препарата Илсира® и в ходе терапии необходимо проводить стандартный скрининг на туберкулез. Пациентам с латентным туберкулезом рекомендуется пройти стандартный курс противотуберкулезной терапии перед началом терапии препаратом Илсира®.
Лабораторные показатели
Нейтропения. В клинических исследованиях препарата Илсира® отмечалось снижение числа нейтрофилов. При длительной терапии пациентов с ревматоидным артритом снижение АЧН не сопровождалось более высокой частотой развития инфекций, в т.ч. серьезных. Следует соблюдать осторожность при лечении препаратом Илсира® пациентов с АЧН <2×109/л. При снижении АЧН <0.5×109/л терапию препаратом Илсира® следует отменить. Следует оценивать число нейтрофилов через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Тромбоцитопения. В клинических исследованиях препарата Илсира® отмечалось снижение числа тромбоцитов. При длительной терапии пациентов с ревматоидным артритом снижение числа тромбоцитов не сопровождалось развитием кровотечений. Следует соблюдать осторожность при назначении терапии препаратом Илсира® при числе тромбоцитов ниже 100×103/мкл. Лечение не рекомендуется при числе тромбоцитов <50×103/мкл. Следует оценивать число тромбоцитов через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Ферменты печени. В клинических исследованиях препарата Илсира® отмечалось повышение активности печеночных трансаминаз без признаков печеночной недостаточности. Частота возникновения подобных изменений может возрастать при совместном использовании с препаратами, обладающими потенциальным гепатотоксическим действием (например, метотрексатом, антибактериальными препаратами и другими). Следует соблюдать осторожность при назначении терапии препаратом Илсира® у пациентов с показателями АЛТ или АСТ, превышающими ВГН более чем в 1.5 раза. Следует оценивать показатели активности печеночных трансаминаз (АЛТ и АСТ) через 4-8 недель после начала терапии, а в дальнейшем в соответствии с клинической практикой.
Изменение показателей липидного обмена. В клинических исследованиях препарата Илсира® отмечалось повышение концентрации липидов (холестерин общий и/или ТГ). Следует оценивать показатели липидного обмена через 4-8 недель после начала терапии левилимабом, а в дальнейшем в соответствии с клинической практикой. При ведении пациентов с гиперлипидемией следует учитывать национальные рекомендации.
Реакции гиперчувствительности
При использовании левилимаба потенциально возможно развитие реакции гиперчувствительности. В рамках проведенных клинических исследований левилимаба реакций гиперчувствительности не зарегистрировано. В ходе пострегистрационного периода оценки препарата Илсира® описаны единичные случаи анафилактических реакций и реакций гиперчувствительности. При возникновении анафилактических или других серьезных аллергических реакций применение препарата Илсира® следует немедленно прекратить и начать соответствующую симптоматическую терапию.
Злокачественные новообразования
У пациентов с РА наблюдается повышенный риск злокачественных новообразований, который может усугубляться при длительном применении иммуносупрессивных лекарственных средств. Объем клинических данных по препаратам класса ингибиторов рецептора ИЛ-6 в целом и левилимабу в частности недостаточен для установления частоты развития злокачественных образований и подтверждение наличия причинно-следственной связи с терапией. Продолжается изучение безопасности левилимаба в ходе долгосрочного применения.
Наличие алкогольной или наркотической зависимости
Наличие алкогольной или наркотической зависимости, а также психических расстройств может стать причиной несоблюдения пациентом графика лечения левилимабом, что, в свою очередь может привести к снижению эффективности терапии. Необходимо более тщательное наблюдение за пациентами с указанными состояниями в связи с отсутствием результатов клинических исследований у данной категории пациентов и возможностью повышенного риска развития гепатотоксичности и других неблагоприятных последствий.
Иммуногенность
В ходе клинических исследований препарата Илсира®, в т.ч. при долгосрочном (в течение года) лечении ревматоидного артрита, выработки связывающих антител к левилимабу выявлено не было.
Пациенты в возрасте старше 65 лет
Данные об эффективности и безопасности препарата у пациентов в возрасте старше 65 лет ограничены. Не предполагается наличия существенных возрастных различий в распределении и выведении препарата.
Пациенты с нарушениями функции почек и печени
Эффективность и безопасность препарата у данной категории пациентов не изучались.
Использование в педиатрии
Исследование эффективности и безопасности препарата у детей и подростков в возрасте до 18 лет не проводилось.
Вакцинация
Не следует проводить иммунизацию живыми аттенуированными вакцинами в ходе лечения препаратом Илсира®, т.к. клиническая оценка безопасности данного взаимодействия в рамках клинических исследований не проводилась. Вакцинация живыми аттенуированными вакцинами до начала терапии препаратом Илсира®, а также интервал между вакцинацией и началом терапии должны соответствовать действующим клиническим рекомендациям.
Демиелинизирующие заболевания
С учетом данных по профилю безопасности препаратов класса ингибиторов рецепторов ИЛ-6 следует соблюдать осторожность при применении левилимаба у пациентов с демиелинизирующими заболеваниями. Необходимо тщательно контролировать появление симптомов, указывающих на развитие демиелинизирующего заболевания ЦНС, несмотря на то, что способность левилимаба вызывать демиелинизирующие заболевания ЦНС в настоящее время не установлена.
Влияние на способность к управлению транспортными средствами и механизмами
Отсутствуют данные о влиянии препарата Илсира® на способность управлять транспортными средствами и работать с машинами и/или механизмами. Учитывая то, что при терапии другими ингибиторами рецептора ИЛ-6 отмечались эпизоды головокружения, пациентам, испытывающим головокружение при применении препарата Илсира®, не рекомендуется управлять транспортными средствами и механизмами до тех пор, пока головокружение не прекратится.
Передозировка
Клинические данные о передозировке препарата Илсира® отсутствуют. Максимальная переносимая доза левилимаба для человека не установлена. В клинических исследованиях при п/к введении левилимаба в максимальной суточной дозе 324 мг двукратно с интервалом 48-96 ч новых нежелательных реакций, изменяющих представление о профиле безопасности препарата, не зарегистрировано.
Лечение: специфический антидот отсутствует; проводят симптоматическую терапию.
Лекарственное взаимодействие
Сведений о наличии неблагоприятного лекарственного взаимодействия левилимаба с другими лекарственными препаратами до настоящего времени не получено.
Смешивание препарата с другими лекарственными средствами строго запрещено.
Условия хранения препарата Илсира®
Препарат следует хранить в защищенном от света, недоступном для детей месте при температуре от 2° до 8°С; не замораживать.
Срок годности препарата Илсира®
Срок годности — 2 года. Не применять по истечении срока годности.
Условия реализации
Препарат отпускают по рецепту.
Контакты для обращений
БИОКАД АО
(Россия)

|
|
198515 Санкт-Петербург, |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Основу соединительной ткани составляет специальный белок – коллаген. С возрастом организм вырабатывает его недостаточно, поэтому, чтобы замедлить старение и предупредить проблемы с костями и суставами, коллаген необходимо принимать дополнительно.
Содержание:
-
Характеристика препарата
-
Как действуют таблетки с коллагеном и витамином С
-
Показания для приема биодобавки
-
О противопоказаниях
-
Рекомендации по дозированию
-
Как хранить
-
Сколько стоит в аптеке, где купить
-
Отзывы
-
Аналоги
Характеристика препарата
Коллаген с витамином С – это биологически активное средство, не относящееся к лекарствам. Производится российской компанией Эвалар в виде таблеток белого цвета, имеющих массу 1,2 г. Упаковка содержит 90 штук.
Состав таблеток представлен пептидами (гидролизованным коллагеном) и ингредиентами покрытия: загустителем гидроксипропилметилцеллюлозой, носителями – кроскарамеллозой и целлюлозой микрокристаллической, глазирователем полиэтиленгликолем, а также стеаратом кальция и витамином С в виде аскорбата кальция.
В суточной дозе содержится 6 000 мг коллагена и 90 мг витамина С.
Коллаген с витамином С от Эвалар – это препарат:
-
с высокой биодоступностью, так как содержит коллаген животного происхождения в легкоусвояемой форме;
-
с усиленным составом, благодаря витамину С в организме активизируется выработка коллагена. Данное вещество действует как антиоксидант, укрепляет иммунитет. Принимая данный БАД, не нужно пить аскорбиновую кислоту дополнительно.
Как действуют таблетки с коллагеном и витамином С
Сочетание данных веществ помогает:
-
замедлить старение организма;
-
улучшить состояние кожи;
-
сделать ее более ровной, упругой, эластичной, разгладить неглубокие морщинки;
-
ускорить регенерацию тканей при травмах – ранах, ожогах, царапинах;
-
повысить подвижность суставных соединений и хрящей;
-
снизить вероятность разрушения костей и суставов;
-
уменьшить болезненность в суставах, укрепить связочный аппарат,
-
сделать здоровыми ногти и волосы.
Прием биодобавки способствует восстановлению собственных запасов белка коллагена, активизирует производство гиалуроновой кислоты и коллагена в организме.
На фоне курсового приема ускоряется заживление тканей, в том числе после операций, быстрее восстанавливается костная ткань после переломов.
Показания для приема биодобавки
БАД с коллагеном и аскорбиновой кислотой назначается как дополнительный источник витамина С и коллагенового белка в легкоусвояемой форме, а также при признаках нехватки коллагена и витамина С.
Заподозрить нехватку коллагена можно при:
-
жалобах на хрупкость костей;
-
появлении морщин в раннем возрасте;
-
болях в суставах;
-
патологиях позвоночника – появлении протрузий и грыж;
-
расшатывании зубов.
Дефицит собственного коллагена тесно связан с недостаточным поступлением в организм витамина С. О появлении гиповитаминоза свидетельствуют частые случаи ОРВИ, анемия, плохая заживляемость ран, кровоточивость десен.
О противопоказаниях
Таблетки не разрешаются к применению лицам с личной непереносимостью любого компонента из состава, а также беременным и кормящим грудью женщинам.
При наличии хронических заболеваний прием лучше согласовать со специалистом.
Рекомендации по дозированию
В соответствии с инструкцией таблетки предназначены только для взрослых. В день необходимо принимать по две штуки трижды в день. Курсовой прием составляет один месяц. Допускаются повторные курсы.
Как хранить
Баночку с таблетками хранят при температуре до 25°С, срок годности составляет три года.
Сколько стоит в аптеке, где купить
Цена биодобавки с коллагеном и аскорбиновой кислотой в аптеке находится в интервале 900-1 200 руб. КупитьБАД в Москве можно без наличия рецепта. Заказать препарат с выгодой можно в интернет аптеке AptStore. На сайте содержится только актуальная информация о ценах и лекарствах в наличии, действующих акциях и скидках. При заказе через интернет аптеку предусмотрена доставка, также доступен самовывоз.
Отзывы
В интернете встречаются разные отзывы о биодобавке с коллагеном от Эвалар. Некоторые женщины отмечают результат от применения уж после месячного курса: разглаживаются мелкие морщинки, проходит хруст в коленных и локтевых суставах, кожа становится мягче и эластичнее.
Также в сети можно встретить отзывы об отсутствии видимых эффектов после разового курса. Это объясняется тем, что прием коллагенсодержащих препаратов имеет накопительный эффект. В первую очередь белок поступает к суставам, мышцам, а затем уже к волосам, ногтям и коже. Чтобы добиться стойкого улучшения внешнего состояния БАД необходимо принимать длительно. При приеме коллагена нельзя придерживаться низкобелковой диеты.
Аналоги
Компанию Эвалар отличает широкий ассортимент биодобавок различного действия. Аналогом Коллагена с витамином С можно считать Морской коллаген данного производителя.
БАД выпускается в форме порошка, расфасованного в пакеты, содержащие 120 порций. Также можно заказатьпрепарат в порционных пакетах по 20 штук в упаковке.
Содержит рыбный коллаген и витамин С. Препарат имеет высокую биодоступность и отличное качество, так как поставки коллагена ведутся из Японии.
Порошок не имеет специфического вкуса. Принимать по три чайных ложки в день или по одному саше однократно в день. Порошок рекомендуется добавлять к стакану любой жидкости. Базовый курс приема составляет один месяц, разрешается его продление.
Биодобавку нельзя отнести к дешевым – стоимость упаковки находится в диапазоне 1 400-1 600 руб.
Аптечные сети предлагают разнообразные препараты с коллагеном, различающиеся производителями, составом и ценами:
-
Коллаген ультра с витамином С, производитель ООО «Веда». Упаковка содержит 7 пакетов. Цена начинается от 290 руб.;
-
Коллагеновый напиток Лора, выпускается в саше, дополнительно содержит гиалуроновую кислоту. Предназначен для улучшения состояния кожи, борьбы с морщинами, ломкостью волос и ногтей. Стоимость 10 саше составляет в среднем 1 000 руб.