Ксеплион (Xeplion) инструкция по применению
📜 Инструкция по применению Ксеплион
💊 Состав препарата Ксеплион
✅ Применение препарата Ксеплион
📅 Условия хранения Ксеплион
⏳ Срок годности Ксеплион
Описание лекарственного препарата
Ксеплион
(Xeplion)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2017
года, дата обновления: 2017.07.28
Владелец регистрационного удостоверения:
Код ATX:
N05AX13
(Палиперидон)
Лекарственные формы
| Ксеплион |
Сусп. д/в/м введения пролонгир. действия 25 мг/0.25 мл: шприц 1 шт. в компл. с иглами д/и (2 шт.) рег. №: ЛСР-009014/10 |
|
|
Сусп. д/в/м введения пролонгир. действия 50 мг/0.5 мл: шприц 1 шт. в компл. с иглами д/и (2 шт.) рег. №: ЛСР-009014/10 |
||
|
Сусп. д/в/м введения пролонгир. действия 75 мг/0.75 мл: шприц 1 шт. в компл. с иглами д/и (2 шт.) рег. №: ЛСР-009014/10 |
||
|
Сусп. д/в/м введения пролонгир. действия 100 мг/1 мл: шприц 1 шт. в компл. с иглами д/и (2 шт.) рег. №: ЛСР-009014/10 |
||
|
Сусп. д/в/м введения пролонгир. действия 150 мг/1.5 мл: шприц 1 шт. в компл. с иглами д/и (2 шт.) рег. №: ЛСР-009014/10 |
Форма выпуска, упаковка и состав
препарата Ксеплион
Суспензия для в/м введения пролонгированного действия белого или почти белого цвета, свободная от посторонних включений.
Вспомогательные вещества: полисорбат 20 — 12 мг, макрогол 4000 (полиэтиленгликоль 4000) — 30 мг, лимонной кислоты моногидрат — 5 мг, натрия гидрофосфат — 5 мг, натрия дигидрофосфата моногидрат — 2.5 мг, натрия гидроксид — 2.84 мг, вода д/и — до 1 мл.
0.25 мл — шприцы из циклолефинового сополимера с наконечником из бромбутила и уплотнителем из бромбутила с покрытием FluroTec®, снабженные ограничителем обратного хода поршня (1) в комплекте с 2 иглами д/в/м инъекций (в дельтовидную и ягодичную мышцу) — поддоны пластиковые, закрытые полиэтиленовой пленкой (1) — пачки картонные.
0.5 мл — шприцы из циклолефинового сополимера с наконечником из бромбутила и уплотнителем из бромбутила с покрытием FluroTec®, снабженные ограничителем обратного хода поршня (1) в комплекте с 2 иглами д/в/м инъекций (в дельтовидную и ягодичную мышцу) — поддоны пластиковые, закрытые полиэтиленовой пленкой (1) — пачки картонные.
0.75 мл — шприцы из циклолефинового сополимера с наконечником из бромбутила и уплотнителем из бромбутила с покрытием FluroTec®, снабженные ограничителем обратного хода поршня (1) в комплекте с 2 иглами д/в/м инъекций (в дельтовидную и ягодичную мышцу) — поддоны пластиковые, закрытые полиэтиленовой пленкой (1) — пачки картонные.
1 мл — шприцы из циклолефинового сополимера с наконечником из бромбутила и уплотнителем из бромбутила с покрытием FluroTec®, снабженные ограничителем обратного хода поршня (1) в комплекте с 2 иглами д/в/м инъекций (в дельтовидную и ягодичную мышцу) — поддоны пластиковые, закрытые полиэтиленовой пленкой (1) — пачки картонные.
1.5 мл — шприцы из циклолефинового сополимера с наконечником из бромбутила и уплотнителем из бромбутила с покрытием FluroTec®, снабженные ограничителем обратного хода поршня (1) в комплекте с 2 иглами д/в/м инъекций (в дельтовидную и ягодичную мышцу) — поддоны пластиковые, закрытые полиэтиленовой пленкой (1) — пачки картонные.
Фармакологическое действие
Механизм действия
Палиперидона пальмитат гидролизуется до палиперидона. Последний является центральнодействующим активным антагонистом преимущественно серотониновых 5-HT2A-рецепторов, а также дофаминовых D2-рецепторов, α1— и α2-адренорецепторов и гистаминовых Н1-рецепторов. Палиперидон не связывается с м-холинорецепторами и с β1— и β2-адренорецепторами. Фармакологическая активность (+) и (-) энантиомеров палиперидона количественно и качественно одинакова.
Предполагается, что терапевтическая эффективность препарата при шизофрении обусловлена комбинированной блокадой D2 и 5-HT2A-рецепторов.
Фармакокинетика
Всасывание и распределение
Из-за исключительно низкой растворимости в воде палиперидона пальмитат после в/м введения медленно растворяется и всасывается в системный кровоток. После однократного в/м введения концентрация палиперидона в плазме крови медленно увеличивается, достигая максимума через 13-14 дней (медиана) после введения в дельтовидную мышцу и 13-17 дней после введения в ягодичную мышцу. Высвобождение вещества обнаруживается уже в 1-й день и сохраняется, по меньшей мере, 126 дней. Характеристики высвобождения активного компонента и схема дозирования препарата Ксеплион обеспечивают длительное поддержание терапевтической концентрации.
После однократного введения в дозе 25-150 мг в дельтовидную мышцу максимальная концентрация (Сmax) в среднем на 28% больше, чем после введения в ягодичную мышцу. В начале терапии введение препарата в дельтовидную мышцу помогает быстрее достичь терапевтической концентрации палиперидона (150 мг в 1-й день и 100 мг на 8-й день), чем введение в ягодичную мышцу. После многократных инъекций разница в воздействии менее очевидна.
Среднее отношение Cmax и равновесной концентрации (Css) палиперидона после введения 4 инъекций препарата Ксеплион в дозе 100 мг в ягодичную мышцу равнялось 1.8, а после введения в дельтовидную мышцу – 2.2. При дозах палиперидона 25-150 мг площадь под кривой «концентрация-время» (AUC) палиперидона изменялась пропорционально дозе, а Сmax при дозах более 50 мг увеличивалась в меньшей степени, чем пропорционально дозе.
Медиана периода полувыведения (Т1/2) палиперидона после введения препарата Ксеплион в дозах 25-150 мг колебалась в пределах 25-49 дней.
После введения препарата (-)-энантиомер палиперидона частично превращается в (+)-энантиомер, и отношение AUC (+)- и (-)-энантиомеров составляет примерно 1.6-1.8.
В популяционном анализе кажущийся объем распределения (Vd) палиперидона равнялся 391 л; палиперидон связывается с белками плазмы крови на 74%.
Метаболизм и выведение
За неделю после однократного перорального приема 1 мг препарата 14C-палиперидона с немедленным высвобождением активного компонента с мочой в неизмененном виде выводится 59% введенной дозы; это указывает на отсутствие существенного метаболизма препарата в печени. Примерно 80% введенной радиоактивности обнаруживалось в моче и 11% — в кале.
Известны 4 пути метаболизма препарата in vivo, но ни один из них не обусловливает метаболизм более чем 6.5% введенной дозы: дезалкилирование, гидроксилирование, дегидрогенизация, отщепление бензизоксазольной группы. Хотя исследования in vitro позволяют предположить определенную роль изоферментов CYP2D6 и CYP3A4 в метаболизме палиперидона, данных о существенной роли этих изоферментов в метаболизме палиперидона in vivo нет. Популяционный фармакокинетический анализ не выявил заметного различия клиренса палиперидона после перорального приема препарата людьми с активным и слабым метаболизмом CYP2D6. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ингибирует метаболизм лекарственных средств изоферментами CYP1A2, CYP2A6, CYP2D6,CYP2E1, CYP3A4 и CYP3A5.
В исследованиях in vitro палиперидон проявлял свойства субстрата P-гликопротеина, а в высоких концентрациях — свойства слабого ингибитора P-гликопротеина. Соответствующих данных in vivo нет, и клиническая значимость этих сведений неясна.
В целом, концентрация палиперидона в плазме крови в период нагрузки после в/м введения препарата Ксеплион лежала в том же диапазоне, что и после приема палиперидона пролонгированного действия перорально с высвобождением активного компонента в дозах между 6 и 12 мг. Использованная схема нагрузки палиперидона обеспечивает поддержание концентрации в этом диапазоне даже в конце междозового интервала (8-й и 36-й день). Индивидуальные различия фармакокинетики палиперидона после введения препарата Ксеплион у разных пациентов были меньше, чем после приема палиперидона пролонгированного действия перорально. Из-за различия характера изменения медианы концентрации палиперидона в плазме крови при применении двух препаратов, следует проявлять осторожность при прямом сравнении их фармакокинетики.
Особые категории пациентов
Нарушение функции печени. Палиперидон не подвергается существенному метаболизму в печени. Хотя применение препарата Ксеплион у больных с нарушением функции печени легкой или средней степени тяжести не изучалось, при таких нарушениях функции печени коррекция дозы не требуется. В исследовании применение палиперидона перорально у больных с нарушением функции печени средней степени тяжести (класс В по Чайлд-Пью) концентрация свободного палиперидона в плазме крови была такой же, как у здоровых добровольцев. У больных с нарушением функции печени тяжелой степени применение палиперидона не изучалось.
Нарушение функции почек. Для больных с нарушением функции почек легкой степени тяжести дозу палиперидона следует уменьшить; Ксеплион не рекомендуется применять у больных с нарушением функции почек средней степени тяжести и тяжелой степени. Было изучено распределение палиперидона после однократного приема внутрь таблетки палиперидона пролонгированного действия 3 мг больными с разной степенью нарушения функций почек. С уменьшением клиренса креатинина (КК) выведение палиперидона ослаблялось: при нарушении функций почек легкой степени тяжести (КК 50-80 мл/мин) — на 32%, при средней степени тяжести (КК 30-50 мл/мин) – на 64%, при тяжелой степени (КК 10-30 мл/мин) – на 71%, в результате чего AUC0-∞ увеличилась по сравнению со здоровыми добровольцами соответственно в 1.5, 2.6 и 4.8 раза. Исходя из небольшого количества данных о применении препарата Ксеплион у больных с нарушением функции почек легкой степени тяжести и из результатов моделирования фармакокинетики, рекомендуемая нагрузочная доза палиперидона для таких больных составляет 75 мг в 1-й и 8-й день; после этого ежемесячно (каждые 4 недели) вводят по 50 мг.
Пожилые больные. Возраст сам по себе не является фактором, требующим коррекции дозы. Однако такая коррекция может потребоваться из-за возрастного уменьшения КК.
Раса. Популяционный фармакокинетический анализ результатов исследования палиперидона для приема внутрь не выявил различия фармакокинетики палиперидона после приема препарата людьми разных рас.
Пол. Клинически значимых различий фармакокинетики палиперидона у мужчин и женщин не найдено.
Влияние курения на фармакокинетику препарата. Согласно исследованиям с использованием микросом печени человека in vitro, палиперидон не является субстратом CYP1A2, поэтому курение не должно влиять на фармакокинетику палиперидона. В соответствии с этими данными in vitro, популяционный фармакокинетический анализ не выявил различия фармакокинетики палиперидона у курящих и не курящих людей.
Показания препарата
Ксеплион
- лечение шизофрении у взрослых пациентов;
- профилактика рецидивов шизофрении у взрослых пациентов;
- терапия шизоаффективных расстройств в качестве монотерапии или в составе комбинированной терапии с нормотимиками и антидепрессантами у взрослых пациентов.
Режим дозирования
У пациентов, никогда не принимавших палиперидон перорально или рисперидон перорально или парентерально, перед началом лечения препаратом Ксеплион рекомендуется в течение 2-7 дней проверить переносимость палиперидона или рисперидона перорально.
При необходимости лечения инъекционными препаратами пролонгированного действия у пациентов с психотическими состояниями легкой и средней степени тяжести, у которых ранее наблюдался ответ на терапию пероральными формами палиперидона или рисперидона, Ксеплион может применяться без предварительной стабилизации пероральными препаратами данной группы.
Шизофрения
Рекомендуется начинать лечение препаратом Ксеплион с дозы 150 мг в 1-й день и 100 мг через 1 неделю (обе инъекции в дельтовидную мышцу). Рекомендуется поддерживающая доза 75 мг 1 раз в месяц; эффект может наблюдаться от приема больших или меньших доз, в диапазоне 25-150 мг в зависимости от индивидуальной переносимости и/или эффективности. После второй начальной дозы последующие поддерживающие инъекции можно проводить в дельтовидную или ягодичную мышцу.
Шизоаффективное расстройство
Рекомендуется начинать лечение препаратом Ксеплион с дозы 150 мг в 1-й день и 100 мг через 1 неделю (обе инъекции в дельтовидную мышцу). Рекомендуется поддерживающая доза в диапазоне 25–150 мг в зависимости от индивидуальной переносимости и/или эффективности. Применение дозы 25 мг при шизоаффективном расстройстве не изучали. После 2-й начальной дозы последующие поддерживающие инъекции можно проводить в дельтовидную или ягодичную мышцу.
Поддерживающую дозу можно корректировать ежемесячно. При этом следует учитывать длительное высвобождение активного компонента из палиперидона пальмитата, т.к. эффект изменения дозы может полностью проявиться только через несколько месяцев.
Пропуск дозы
Избегание пропуска доз. Вторую нагрузочную дозу палиперидона рекомендуется вводить через 1 неделю после первой дозы. Если это невозможно, то ее можно ввести на 4 дня раньше или позже. Аналогично, третью и последующие дозы рекомендуется вводить ежемесячно, но если это невозможно, то инъекцию можно сделать на 7 дней раньше или позже.
Если вторая инъекция препарата Ксеплион не была сделана вовремя (1 неделя ± 4 дня), рекомендуется возобновление лечения в зависимости от времени, которое прошло со дня первой инъекции.
Пропуск второй начальной дозы (срок менее 4 недель). Если со дня первой инъекции прошло менее 4 недель, пациенту следует ввести вторую инъекцию в дозе 100 мг в дельтовидную мышцу как можно скорее. Третью инъекцию препарата Ксеплион в дозе 75 мг следует сделать в дельтовидную или ягодичную мышцу через 5 недель после первой инъекции (не учитывая время второй инъекции). В дальнейшем должен соблюдаться ежемесячный курс инъекций в дозе от 25 мг до 150 мг в дельтовидную или ягодичную мышцу в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (срок от 4 до 7 недель). Если со дня первой инъекции препарата Ксеплион прошло от 4 до 7 недель, лечение возобновляют введением двух инъекций в дозе 100 мг по следующей схеме: первую инъекцию в дельтовидную мышцу делают как можно скорее; через 1 неделю делают вторую инъекцию в дельтовидную мышцу, затем продолжают ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск второй начальной дозы (более 7 недель). Если с момента первой инъекции препарата Ксеплион прошло более 7 недель, лечение начинают так же, как в случае инициации лечения препаратом Ксеплион.
Пропуск поддерживающей дозы (срок от 1 месяца до 6 недель). После начала лечения рекомендуется проводить инъекции препарата Ксеплион ежемесячно. Если с момента последней инъекции прошло менее 6 недель, то следует как можно скорее ввести очередную дозу, равную предыдущей. После этого вводить препарат ежемесячно.
Пропуск поддерживающей дозы (срок от 6 недель до 6 месяцев). Если с момента последней инъекции препарата Ксеплион прошло более 6 недель, рекомендуется следующее:
Для пациентов, стабилизированных дозой от 25 мг до 100 мг:
- Делают инъекцию препарата в дельтовидную мышцу как можно скорее в той дозе, на которой прошла стабилизация состояния пациента до пропуска инъекции.
- Следующую инъекцию в дельтовидную мышцу (такая же доза) делают через неделю на 8-й день.
- Далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Для пациентов, стабилизированных дозой 150 мг:
- Как можно скорее вводят дозу 100 мг в дельтовидную мышцу.
- Через 1 неделю вводят еще одну дозу 100 мг (8-й день) в дельтовидную мышцу.
- Далее возобновляют ежемесячный курс инъекций в дельтовидную или ягодичную мышцу в дозе от 25 мг до 150 мг в зависимости от индивидуальной переносимости и/или эффективности.
Пропуск поддерживающей дозы (срок >6 месяцев). Если с момента последней инъекции препарата Ксеплион прошло более 6 месяцев, то лечение начинают заново, как описано выше для начала лечения.
Способ применения
Ксеплион предназначен только для в/м введения. Препарат медленно вводят глубоко в мышцу. Инъекции должен проводить только медицинский работник. Всю дозу вводят за один раз; нельзя вводить дозу за несколько инъекций. Нельзя вводить препарат в сосуды или п/к. Следует избегать случайного попадания в кровеносный сосуд. Для этого перед началом введения препарата поршень шприца оттягивают назад для проверки на предмет попадания иглы в крупный кровеносный сосуд. В случае если при этом в шприц поступает кровь, следует извлечь иглу и шприц из мышцы пациента и утилизировать их.
Рекомендуемый размер иглы для введения препарата Ксеплион в дельтовидную мышцу определяется массой тела пациента. Для больных с массой тела ≥90 кг рекомендуется длинная игла с серым корпусом из набора. Для больных с массой тела <90 кг рекомендуется короткая игла с голубым корпусом из набора. Следует поочередно вводить препарат в правую и левую дельтовидную мышцу.
Для введения препарата Ксеплион в ягодичную мышцу рекомендуется длинная игла с серым корпусом из набора. Инъекции нужно проводить в верхний наружный квадрант ягодицы. Следует поочередно вводить препарат в правую и левую ягодичную мышцу.
Поскольку палиперидон является основным активным метаболитом рисперидона, следует соблюдать осторожность при одновременном применении в течение длительного периода времени препарата Ксеплион и рисперидона или пероральной формы палиперидона. Данные по безопасности одновременного применения препарата Ксеплион и других антипсихотиков ограничены.
Пациенты с нарушением функции печени
Применение препарата Ксеплион у пациентов с нарушением функции печени не изучалось. Исходя из результатов исследования палиперидона для приема внутрь, для пациентов с нарушением функции печени легкой или средней степени тяжести коррекции дозы не требуется. Применение препарата Ксеплион у пациентов с нарушением функций печени тяжелой степени не изучалось.
Пациенты с нарушением функции почек
Применение препарата Ксеплион у пациентов с нарушением функции почек систематически не изучалось. У пациентов с нарушением функции почек легкой степени тяжести (КК от ≥50 до <80 мл/мин) рекомендуется начинать применение препарата Ксеплион с дозы 100 мг в 1-й день и 75 мг через 1 неделю (обе инъекции в дельтовидную мышцу). После этого через 1 месяц вводят инъекцию в дозе 50 мг в дельтовидную или ягодичную мышцу, и далее изменяют дозу от 25 мг до 100 мг в зависимости от индивидуальной переносимости и/или эффективности.
Ксеплион не рекомендуется применять у пациентов с нарушением функции почек средней или тяжелой степени (КК <50 мл/мин).
Пациенты пожилого возраста
В целом, для пациентов пожилого возраста с нормальной функцией почек рекомендуется та же доза препарата Ксеплион, что и для более молодых пациентов с нормальной функцией почек. У пациентов пожилого возраста функция почек может быть снижена, и на таких больных распространяются приведенные выше рекомендации для пациентов с нарушением функции почек.
Подростки и дети
Безопасность и эффективность применения препарата Ксеплион у пациентов в возрасте до 18 лет не изучалась.
Другие особые категории пациентов
Коррекции дозы препарата Ксеплион в зависимости от пола, расы пациентов и курения не требуется.
Перевод с других нейролептиков
Данные о переводе больных шизофренией или шизоаффективным расстройством с других нейролептиков на Ксеплион или о его применении одновременно с другими нейролептиками систематически не собирались. Для пациентов, которые никогда не принимали пероральный палиперидон или пероральный или инъекционный рисперидон, должна быть исследована переносимость с пероральным палиперидоном или пероральным рисперидоном перед началом лечения препаратом Ксеплион. В начале лечения препаратом Ксеплион ранее применявшиеся перорально нейролептики можно постепенно отменить. Ксеплион следует назначать, как описано выше. Если пациент получает инъекционные нейролептики пролонгированного действия, лечение препаратом Ксеплион начинают сразу с поддерживающей дозы в момент очередной запланированной инъекции. Следует продолжать лечение препаратом Ксеплион 1 раз в месяц. Начальная доза на первой неделе лечения не требуется.
У пациентов, которые были стабилизированы различными дозами препарата Рисполепт Конста®, суспензия для в/м введения пролонгированного действия, равновесные концентрации активного вещества могут достигать схожих значений в течение поддерживающей терапии препаратом Ксеплион 1 раз в месяц согласно следующей схеме:
Отмену предыдущего антипсихотика следует провести в соответствии с инструкцией по медицинскому применению. При отмене препарата Ксеплион следует учитывать длительное высвобождение активного компонента. Как и в случае с другими нейролептиками, следует периодически оценивать необходимость продолжения применения средств профилактики развития экстрапирамидных расстройств.
Указания по применению
Шприц предназначен только для однократного введения.
- Интенсивно встряхнуть шприц в течение 10 секунд для получения однородной суспензии.
- Выбрать соответствующую иглу.
Для введения в дельтовидную мышцу пациентам массой тела <90 кг используют короткую иглу (с голубым корпусом), а пациентам массой тела ≥90 кг – длинную иглу (с серым корпусом).
Для введения в ягодичную мышцу используют длинную иглу (с серым корпусом).
- Держа шприц вертикально, снять с него резиновый колпачок путем аккуратного вращения по часовой стрелке.
- Наполовину открыть упаковку безопасной иглы, взяться за колпачок иглы через упаковку и подсоединить иглу к луеровскому колпачку шприца путем аккуратного вращения по часовой стрелке.
- Снять с иглы колпачок, потянув его вдоль иглы. Не вращать колпачок, т.к. это может ослабить соединение иглы со шприцем.
- Направить шприц иглой вверх и выдавить из шприца воздух, слегка надавив на поршень.
- Ввести все содержимое шприца в выбранную мышцу (дельтовидную или ягодичную). Не вводить препарат в кровеносный сосуд или подкожно.
- После завершения инъекции привести защиту иглы в рабочее положение большим или указательным пальцем или надавив шприцем о твердую поверхность. Защита иглы должна зафиксироваться со щелчком. Шприц с иглой утилизировать так, как это полагается.
Побочное действие
Наиболее частыми нежелательными реакциями, зарегистрированными в клинических исследованиях, были бессонница, головная боль, беспокойство, инфекции верхних дыхательных путей, реакции в месте введения, паркинсонизм, повышение веса, акатизия, возбуждение, седация, сонливость, тошнота, запор, головокружение, скелетно-мышечная боль, тахикардия, тремор, боль в животе, рвота, диарея, усталость, дистония. Из них дозозависимыми оказались седация и сонливость.
Большинство нежелательных побочных реакций (НПР) были слабыми или средней тяжести.
Ниже указаны нежелательные реакции, наблюдавшиеся у пациентов с шизофренией. Частоту нежелательных реакций классифицировали следующим образом: очень часто (≥10%), часто (≥1% и <10%), нечасто (≥0.1% и <1%), редко (≥0.01% и <0.1%) и очень редко (<0.01%).
Инфекции: часто – инфекции мочевыделительной системы, грипп, инфекции верхних дыхательных путей; нечасто — акародерматит, бронхит, воспаление подкожной жировой клетчатки, инфекции уха, инфекции глаза, пневмония, инфекции дыхательных путей, синусит, подкожный абсцесс, тонзиллит, цистит; редко – онихомикоз.
Со стороны иммунной системы: нечасто – гиперчувствительность; редко – анафилактические реакции.
Со стороны кровеносной и лимфатической системы: нечасто – анемия, снижение гематокрита, увеличение количества эозинофилов, уменьшение количества белых кровяных клеток; редко – тромбоцитопения, нейтропения, агранулоцитоз.
Со стороны эндокринной системы: часто – гиперпролактинемия; редко – неадекватная секреция антидиуретического гормона; с неизвестной частотой – глюкоза в моче.
Метаболические нарушения: часто – гипергликемия, снижение массы тела, увеличение концентрации триглицеридов в плазме крови, повышение массы тела; нечасто – гиперинсулинемия, анорексия, снижение аппетита, повышение аппетита, сахарный диабет, увеличение концентрации холестерина в крови; редко – полидипсия, гипогликемия, водная интоксикация, диабетический кетоацидоз.
Психиатрические расстройства: очень часто – бессонница; часто – беспокойство, депрессия, возбуждение; нечасто – снижение либидо, нервозность, ночные кошмары, состояние замешательства, нарушение сна, мании; редко – аноргазмия, эмоциональная уплощенность.
Со стороны нервной системы: очень часто – головная боль; часто – седация, дистония, дискинезия, тремор, акатизия, головокружение, экстрапирамидные симптомы, сонливость, паркинсонизм; нечасто – судороги (в т.ч. эпилептические судороги), рассеянность внимания, постуральное головокружение, дизартрия, гипестезия, парестезия, психомоторная гиперактивность, обморок, тяжелая дискинезия, дисгевзия; редко – злокачественный нейролептический синдром, церебральная ишемия, отсутствие реакции на раздражители, потеря сознания, снижение уровня сознания, диабетическая кома, нарушения равновесия, нарушения координации, дрожание головы.
Офтальмологические нарушения: нечасто – сухость глаз, нечеткость зрительного восприятия, конъюнктивит; редко – глаукома, светобоязнь, увеличение слезотечения, покраснение глаз, непроизвольное движение глазного яблока, ротаторный нистагм.
Со стороны органа слуха и равновесия: нечасто – вертиго, шум в ушах, боль в ухе.
Со стороны сердечно-сосудистой системы: часто – брадикардия, тахикардия, повышение АД; нечасто – снижение АД, атриовентрикулярная блокада, нарушение проводимости, нарушения на ЭКГ, увеличение интервала QT на ЭКГ, сердцебиение, синдром постуральной ортостатической тахикардии, фибрилляция предсердий, ортостатическая гипотензия; редко – тромбоз глубоких вен, синусовая аритмия, эмболия легочной артерии, ишемия, приливы.
Со стороны дыхательной системы: часто – кашель, заложенность носа; нечасто – диспноэ, носовое кровотечение, боль в глоточно-гортанной области, свистящее дыхание, заложенность легких; редко – гипервентиляция, аспирационная пневмония, заложенность дыхательных путей, дисфония, синдром апноэ во сне.
Желудочно-кишечные нарушения: часто – диспепсия, боль в верхней части живота, запор, диарея, тошнота, зубная боль, рвота; нечасто – дискомфорт в области живота, сухость слизистой оболочки полости рта, метеоризм, гастроэнтерит; редко – панкреатит, недержание кала, отек языка, дисфагия, кишечная непроходимость, каловые камни, хейлит.
Со стороны гепатобилиарной системы: часто – повышение активности печеночных трансаминаз; нечасто – увеличение активности ГГТ, увеличение активности ферментов печени; редко – желтуха.
Со стороны костно-мышечной системы и соединительной ткани: часто – боль в спине, боль в конечностях, скелетно-мышечная боль; нечасто – артралгия, скованность суставов, мышечные спазмы, боль в шее; редко – опухание суставов, рабдомиолиз, повышение активности креатинфосфокиназы, мышечная слабость, нарушение осанки.
Со стороны кожи: часто – кожная сыпь; нечасто – акне, сухость кожи, экзема, эритема, крапивница, зуд, алопеция; редко – ангионевротический отек, гиперкератоз, изменения цвета кожи, себорейный дерматит, перхоть, лекарственная сыпь.
Со стороны мочевыделительной системы: нечасто – дизурия, поллакиурия, недержание мочи; редко – задержка мочевыведения.
Со стороны репродуктивной системы и молочной железы: нечасто – задержка менструации, нарушения менструации, аменорея, галакторея, гинекомастия, сексуальная дисфункция, нарушения эякуляции, эректильная дисфункция, вагинальные выделения; редко – приапизм, боль в молочных железах, дискомфорт в молочных железах, нагрубание молочных желез, увеличение молочных желез, выделения из молочных желез.
Влияние на течение беременности, послеродовые и перинатальные состояния: редко – синдром отмены у новорожденных.
Прочие: часто – лихорадка, астенические расстройства, слабость, местные реакции (боль, зуд, уплотнение в месте инъекции); нечасто – боль в груди, дискомфорт в области груди, отек лица, нарушение походки, недомогание, уплотнение в месте укола, отеки (в т.ч. генерализованный отек, периферический отек, мягкий отек), падение; редко – озноб, повышение температуры тела, снижение температуры тела, жажда, синдром отмены, киста в месте введения, гипотермия, абсцесс в месте введения инъекции, воспаление подкожной клетчатки в месте введения инъекции, гематома в месте введения инъекции.
Нежелательные реакции, зарегистрированные при применении рисперидона
Палиперидон является активным метаболитом рисперидона, поэтому профили побочных реакций рисперидона и палиперидона взаимосвязаны. В дополнение к вышеперечисленным, при применении рисперидона были отмечены следующие побочные реакции, которые могут возникнуть и при применении препарата Ксеплион:
Со стороны нервной системы: нарушение мозгового кровообращения.
Офтальмологические нарушения: интраоперационный синдром дряблой радужки.
Со стороны дыхательной системы, органов грудной клетки и средостения: хрипы.
Общие нарушения и нарушения в месте введения (наблюдались при применении инъекционной формы рисперидона): некроз в месте введения инъекции, язва в месте введения инъекции.
Шизоаффективное расстройство
Профиль безопасности препарата Ксеплион у пациентов с шизоаффективным расстройством схож с таковым у пациентов с шизофренией.
Описание отдельных побочных реакций
Анафилактические реакции
Редкие случаи анафилактических реакций при введении препарата Ксеплион были зафиксированы в пострегистрационном периоде у пациентов, ранее хорошо переносивших терапию пероральными формами рисперидона или палиперидона.
Реакции в месте введения
Наиболее часто сообщавшейся реакцией в месте введения была боль, которая в большинстве случаев была слабой или средней степени тяжести. Согласно оценке с использованием визуальной аналоговой шкалы, частота и интенсивность боли со временем снижалась во всех клинических исследованиях II и III фазы. Инъекции в дельтовидную мышцу воспринимаются как немного более болезненные по сравнению с инъекциями в ягодичную мышцу. Другие реакции в месте введения в основном были легкой степени тяжести и включали уплотнение (часто), зуд (нечасто) и узелки (редко).
Экстрапирамидные симптомы (ЭС)
ЭС включают следующие термины: паркинсонизм (включает гиперсаливацию, скелетно-мышечную скованность, паркинсонизм, слюнотечение, ригидность по типу «зубчатого колеса», брадикинезию, гипокинезию, маскоподобное лицо, мышечное напряжение, акинезию, ригидность затылочных мышц, мышечную ригидность, паркинсоническую походку, нарушение глабеллярного рефлекса и паркинсонический тремор покоя), акатизию (включает акатизию, возбужденное состояние, гиперкинезию и синдром беспокойных ног), дискинезию (включает дискинезию, подергивание мышц, хореоатетоз, атетоз и миоклонию), дистонию (включает дистонию, гипертонию, кривошею, непроизвольные мышечные сокращения, миогенную контрактуру, блефароспазм, движение глазного яблока, паралич языка, спазм лица, ларингоспазм, миотонию, опистотонус, орофарингеальный спазм, плеврототонус, спазм языка и судорожное стискивание челюстей) и тремор. В данный список включен более широкий спектр симптомов, которые могут иметь не экстрапирамидное происхождение.
Увеличение массы тела
В 13-недельном клиническом исследовании с использованием начальной дозы 150 мг было показано, что аномальное увеличение массы тела >7% является дозозависимым. Увеличение массы тела отмечалось с частотой 5% в группе плацебо и с частотой 6%, 8% и 13% при применении Ксеплиона в дозе 25 мг, 100 мг и 150 мг соответственно.
В течение 33-недельного открытого периода перехода на терапию Ксеплионом или поддерживающей терапии Ксеплионом долгосрочного клинического исследования у пациентов с шизофренией 12% пациентов, получавших лечение Ксеплионом, соответствовали данному критерию (увеличение массы тела на >7% от двойной слепой фазы до конечной точки).
Класс-эффекты
При применении антипсихотиков возможны удлинение интервала QT, возникновение желудочковых аритмий (желудочковая фибрилляция, желудочковая тахикардия), внезапная необъяснимая смерть, остановка сердца и тахикардия типа «пируэт». При применении антипсихотиков сообщается о случаях развития (с неизвестной частотой) венозного тромбоэмболизма, включая случаи легочной эмболии и тромбоза глубоких вен.
Противопоказания к применению
- гиперчувствительность к палиперидону или любому компоненту препарата;
- поскольку палиперидон является активным метаболитом рисперидона, Ксеплион противопоказан пациентам с известной гиперчувствительностью к рисперидону.
С осторожностью
Следует с осторожностью применять Ксеплион в следующих случаях (см. более подробную информацию в разделе «Особые указания»):
- у пациентов с сердечно-сосудистыми заболеваниями (например, сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению АД (например, обезвоживание, уменьшение объема циркулирующей крови, применение гипотензивных препаратов);
- у пациентов, имеющих в анамнезе судороги или другие состояния, при которых может снижаться судорожный порог;
- у пациентов, которые могут подвергаться воздействиям, повышающим температуру тела, например, сильной физической нагрузке, высокой температуре окружающей среды, воздействию препаратов с активностью м-холинолитиков, а также обезвоживанию;
- у пациентов, имеющих в анамнезе аритмию или врожденное удлинение интервала QT, либо принимающих препараты, удлиняющие интервал QT;
- при применении в комбинации с другими лекарственными средствами, действующими на ЦНС, и алкоголем. Палиперидон может ослаблять эффект леводопы и агонистов дофамина;
- у пациентов с деменцией, болезнью Паркинсона или деменцией с тельцами Леви;
- у пациентов с возможными пролактинзависимыми опухолями.
- у пациентов с нарушением функции печени или почек.
Применение при беременности и кормлении грудью
Беременность
Безопасность применения препарата Ксеплион в/м или палиперидона перорально при беременности у людей не установлена. При применении высоких доз палиперидона перорально наблюдалось небольшое увеличение смертности плодов у животных. Ксеплион при в/м введении не влиял на течение беременности крыс, но высокие дозы его были токсичны для беременных самок. Дозы палиперидона при приеме внутрь и препарата Ксеплион при в/м введении, которые создают концентрации, превышающие максимальные терапевтические дозы у человека соответственно в 20-22 раза и в 6 раз, не влияли на потомство лабораторных животных.
Ксеплион можно применять при беременности только в случае, если предполагаемая польза для матери превышает потенциальный риск для плода. Влияние препарата Ксеплион на схватки и роды у людей неизвестно.
В случае если женщина принимала антипсихотические препараты (включая палиперидон) в III триместре беременности, у новорожденных существует риск возникновения экстрапирамидных расстройств и/или синдрома отмены различной степени тяжести. Эти симптомы могут включать ажитацию, гипертонию, гипотонию, тремор, сонливость, респираторные нарушения и нарушение вскармливания.
Грудное вскармливание
В исследованиях применения палиперидона у животных и рисперидона у людей обнаружено выведение палиперидона с грудным молоком. Поэтому женщины, получающие Ксеплион, не должны кормить детей грудью.
Применение при нарушениях функции печени
У пациентов с нарушением функции печени применение препарата Ксеплион не изучалось. Исходя из результатов исследования палиперидона для приема внутрь, для пациентов с нарушением функции печени легкой или средней степени тяжести коррекции дозы не требуется.
Применение препарата Ксеплион у пациентов с нарушением функции печени тяжелой степени не изучалось.
Применение при нарушениях функции почек
Применение препарата Ксеплион у пациентов с нарушением функции почек систематически не изучалось. У пациентов с нарушением функции почек легкой степени тяжести (КК от ≥50 до <80 мл/мин) рекомендуется начинать применение препарата Ксеплион с дозы 100 мг в 1-й день и 75 мг через 1 неделю (обе инъекции в дельтовидную мышцу). После этого через 1 месяц вводят по 50 мг ежемесячно в дельтовидную или ягодичную мышцу, и далее изменяют дозу от 25 мг до 100 мг в зависимости от индивидуальной переносимости и/или эффективности.
Ксеплион не рекомендуется применять у пациентов с нарушением функции почек средней или тяжелой степени (КК <50 мл/мин).
Применение у детей
Безопасность и эффективность применения препарата Ксеплион у детей и подростков в возрасте до 18 лет не изучалась.
Применение у пожилых пациентов
Следует проявлять осторожность при назначении препарата Ксеплион пациентам пожилого возраста с деменцией.
Пациентам пожилого возраста с нормальной функцией почек рекомендуется та же доза препарата Ксеплион, что и для более молодых больных с нормальной функцией почек. У пациентов пожилого возраста функция почек может быть снижена, и на таких больных распространяются приведенные выше рекомендации для больных с нарушением функции почек.
Особые указания
Применение препарата Ксеплион при остром психомоторном возбуждении или при тяжелом психотическом состоянии
Не рекомендуется применять препарат Ксеплион при остром психомоторном возбуждении или при тяжелом психотическом состоянии, когда необходим незамедлительный контроль симптомов.
Интервал QT
Следует соблюдать осторожность при применении палиперидона у пациентов с известными сердечно-сосудистыми заболеваниями или с удлинением интервала QT в анамнезе, а также при совместном применении лекарственных средств, которые могут приводить к удлинению интервала QT.
Злокачественный нейролептический синдром
При применении нейролептиков, в т.ч. палиперидона, зарегистрировано развитие злокачественного нейролептического синдрома (ЗНС), характеризуемого повышением температуры тела, мышечной ригидностью, нестабильностью вегетативной нервной системы, нарушением сознания и повышением концентрации креатинфосфокиназы сыворотки крови. Кроме того, могут наблюдаться миоглобинурия (рабдомиолиз) и острая почечная недостаточность. При появлении симптомов, позволяющих предположить ЗНС, все нейролептики, включая Ксеплион, отменяют.
Поздняя дискинезия
Применение препаратов, обладающих свойствами антагонистов дофаминовых рецепторов, сопровождается развитием поздней дискинезии, характеризующейся ритмичными, непроизвольными движениями, главным образом языка и/или лицевых мышц. При появлении симптомов поздней дискинезии следует рассмотреть возможность отмены всех нейролептиков, включая Ксеплион.
Реакции гиперчувствительности
Несмотря на то, что переносимость пероральных форм палиперидона или рисперидона должна быть проверена до инициации терапии препаратом Ксеплион, сообщается об очень редких случаях возникновения анафилактических реакций в ходе пострегистрационного применения у пациентов, ранее переносивших пероральные формы палиперидона или рисперидона.
В случае возникновения реакций гиперчувствительности необходимо прекратить применение препарата Ксеплион, принять необходимые поддерживающие клинические меры и проводить наблюдение за состоянием пациента до исчезновения симптомов.
Гипергликемия и сахарный диабет
При лечении препаратом Ксеплион наблюдались гипергликемия, сахарный диабет и обострение уже имеющегося сахарного диабета. Установление взаимосвязи между применением атипичных антипсихотических препаратов и нарушением обмена глюкозы осложнено повышенным риском развития сахарного диабета у пациентов с шизофренией и шизоаффективным расстройством и распространенностью сахарного диабета в общей популяции. Учитывая эти факторы, взаимосвязь между применением атипичных антипсихотических препаратов и развитием побочных действий, связанных с гипергликемией, установлена не полностью. У всех пациентов необходимо проводить клинический контроль на наличие симптомов гипергликемии и сахарного диабета (см. раздел «Побочное действие»).
Увеличение массы тела
При лечении атипичными антипсихотиками наблюдалось значительное увеличение массы тела. Необходимо проводить контроль массы тела пациентов.
Гиперпролактинемия
Исследования культур ткани указывают на то, что рост опухоли молочной железы у человека может стимулироваться пролактином. Несмотря на то, что до сих пор в клинических и эпидемиологических исследованиях не была продемонстрирована прямая связь с применением антипсихотиков, следует соблюдать осторожность при применении палиперидона у пациентов с возможными пролактинзависимыми опухолями.
Ортостатическая гипотензия
Обладая активностью альфа-адреноблокатора, палиперидон у некоторых больных может вызывать ортостатическую гипотензию. Ксеплион следует с осторожностью применять у больных с сердечно-сосудистыми заболеваниями (например, сердечной недостаточностью, инфарктом или ишемией миокарда, нарушением сердечной проводимости), нарушениями мозгового кровообращения или состояниями, предрасполагающими к снижению АД (например, обезвоживанием, уменьшением объема циркулирующей крови, применением гипотензивных препаратов).
Судороги
Как и другие нейролептики, Ксеплион следует с осторожностью применять у больных, имеющих в анамнезе судороги или другие состояния, при которых может снижаться судорожный порог.
Почечная недостаточность
Концентрация палиперидона в плазме повышена у пациентов с нарушением функции почек. У пациентов с нарушением функции почек легкой степени рекомендуется коррекция дозы. Ксеплион не рекомендуется применять у пациентов с нарушением функции почек средней или тяжелой степени (КК 50 мл/мин).
Печеночная недостаточность
Применение препарата Ксеплион у пациентов с нарушением функций печени тяжелой степени (класс С по шкале Чайлда-Пью) не изучалось. Следует соблюдать осторожность при применении палиперидона у таких пациентов.
Пациенты пожилого возраста с деменцией
Перекрестный анализ результатов исследований показал повышенную смертность пациентов пожилого возраста с деменцией, получавших атипичные нейролептики, в т.ч. рисперидон, арипипразол, оланзапин и кветиапин, по сравнению с плацебо. Среди пациентов, получавших рисперидон и плацебо, смертность составляла соответственно 4% и 3.1%.
Применение препарата Ксеплион у пожилых пациентов с деменцией не изучалось. Поскольку палиперидон является активным метаболитом рисперидона, то следует учитывать опыт применения рисперидона. Среди пожилых пациентов с деменцией, принимающих рисперидон, наблюдалась повышенная смертность у пациентов, принимавших фуросемид и рисперидон, по сравнению с группой, принимавшей только рисперидон, и группой, принимавшей только фуросемид. Не установлено патофизиологических механизмов, объясняющих данное наблюдение. Тем не менее, следует соблюдать особую осторожность при назначении препарата в таких случаях. Не обнаружено увеличения смертности у пациентов, одновременно принимающих другие диуретики вместе с рисперидоном. Независимо от лечения, обезвоживание является общим фактором риска смертности и должно тщательно контролироваться у пожилых пациентов с деменцией.
Нарушения мозгового кровообращения
Согласно данным плацебо-контролируемых исследований, частота нарушений мозгового кровообращения (преходящих и инсульта), в т.ч. со смертельным исходом, повышается в 3 раза у пожилых пациентов с деменцией, получавших некоторые атипичные нейролептики, в т.ч. рисперидон, арипипразол и оланзапин, по сравнению с применением плацебо. Механизм данного явления неизвестен.
Лейкопения, нейтропения, агранулоцитоз
Лейкопения, нейтропения и агранулоцитоз отмечались при применении антипсихотических средств, в т. ч. при применении препарата Ксеплион. Агранулоцитоз отмечался очень редко в течение пострегистрационных наблюдений. Пациентам с клинически значимым уменьшением количества лейкоцитов в анамнезе или препарат-зависимой лейкопенией/нейтропенией рекомендуется проведение полного анализа крови в течение первых месяцев терапии, прекращение лечения препаратом Ксеплион должно быть рассмотрено при первом клинически значимом уменьшении количества лейкоцитов при отсутствии других возможных причин. Пациентам с клинически значимой нейтропенией рекомендуется наблюдаться на предмет повышения температуры или возникновения симптомов инфекции и начинать лечение немедленно при возникновении таких симптомов. Пациенты с тяжелой формой нейтропении (абсолютное количество нейтрофилов менее 1×109/л) должны прекратить применение препарата Ксеплион до тех пор, пока количество лейкоцитов не нормализуется.
Венозные тромбоэмболии
При применении антипсихотических препаратов были отмечены случаи венозной тромбоэмболии. Поскольку пациенты, принимающие антипсихотические препараты, часто имеют риск развития венозной тромбоэмболии, все возможные факторы риска должны быть выявлены до и во время лечения препаратом Ксеплион, и должны быть предприняты предупреждающие меры.
Болезнь Паркинсона и деменция с тельцами Леви
Врач должен сопоставить риск и пользу применения нейролептиков, включая Ксеплион, у пациентов с болезнью Паркинсона или деменцией с тельцами Леви, т.к. у обеих этих категорий пациентов может быть повышен риск развития злокачественного нейролептического синдрома (ЗНС) и риск повышенной чувствительности к нейролептикам. Проявления повышенной чувствительности могут включать спутанность сознания, притупление болевой чувствительности, неустойчивость позы с частыми падениями, а также экстрапирамидные симптомы.
Приапизм
Имеются данные о способности препаратов, обладающих свойствами альфа-адреноблокаторов, вызывать приапизм. Приапизм зарегистрирован в рамках постмаркетингового контроля применения палиперидона. Пациенту необходимо обратиться к врачу, если симптомы приапизма не исчезают в течение 3-4 ч.
Влияние на регуляцию температуры тела
С применением нейролептиков связывают ухудшение способности организма снижать температуру тела. Рекомендуется проявлять осторожность при назначении препарата Ксеплион пациентам, которые могут подвергаться воздействиям, повышающим температуру тела, например сильной физической нагрузке, высокой температуре окружающей среды, воздействию препаратов с активностью м-холинолитиков, а также обезвоживанию.
Противорвотное действие
В доклинических исследованиях палиперидона обнаружено противорвотное действие. Появление этого эффекта у пациента может маскировать признаки и симптомы передозировки некоторых лекарств или, например, такие состояния, как непроходимость кишечника, синдром Рейе или опухоль мозга.
Введение
При в/м введении следует проявлять осторожность во избежание случайного попадания препарата в кровеносный сосуд.
Интраоперационный синдром дряблой радужки (ИСДР)
ИСДР наблюдался во время проведения оперативного вмешательства по поводу наличия катаракты у пациентов, получающих терапию препаратами, являющимися антагонистами α1-адренорецепторов, такими как Ксеплион.
ИСДР увеличивает риск возникновения осложнений, связанных с органом зрения, во время и после проведения операционного вмешательства. Врач, проводящий такую операцию, должен быть заблаговременно проинформирован о том, что пациент принимал или принимает в настоящее время препараты, обладающие активностью антагонистов α1-адренорецепторов. Потенциальная польза отмены терапии антагонистами α1-адренорецепторов перед оперативным вмешательством не установлена, и должна оцениваться с учетом рисков, связанных с отменой терапии антипсихотическими препаратами.
Влияние на способность к управлению транспортными средствами и механизмами
Ксеплион может нарушать выполнение действий, требующих концентрации внимания и быстроты психомоторных реакций, и может влиять на зрение. Поэтому пациентам следует рекомендовать не управлять транспортными средствами и движущимися механизмами, пока не будет установлена их индивидуальная чувствительность.
Передозировка
Поскольку Ксеплион предназначен для введения медработниками, то вероятность его передозировки пациентами мала.
Симптомы
В целом, ожидаемые признаки и симптомы соответствуют усилению известного фармакологического действия палиперидона, т.е. сонливость, заторможенность, тахикардия, снижение АД, удлинение интервала QT, экстрапирамидные симптомы. Полиморфная желудочковая тахикардия типа «пируэт» и фибрилляция желудочков были отмечены при передозировке перорального палиперидона. В случае острой передозировки следует учитывать возможность получения пациентами нескольких препаратов.
Лечение
При оценке потребности в лечении и восстановлении больных следует учитывать длительное высвобождение активного вещества и большой период полувыведения палиперидона. Специфического антидота для палиперидона не существует. Следует осуществлять общие поддерживающие меры, обеспечить и поддерживать проходимость дыхательных путей, достаточную вентиляцию легких и насыщение крови кислородом. Следует немедленно начать контроль функции сердечно-сосудистой системы, включая постоянный мониторинг ЭКГ для выявления возможной аритмии. В случае снижения АД и циркуляторного коллапса следует предпринимать соответствующие меры, например, в/в введение растворов и/или симпатомиметиков. При развитии тяжелых экстрапирамидных симптомов применяют антихолинергические препараты. Следует тщательно контролировать состояние пациента до его восстановления.
Лекарственное взаимодействие
Как и другие антипсихотики, палиперидон может увеличивать интервал QT, поэтому его следует с осторожностью сочетать с другими лекарственными средствами, увеличивающими интервал QT, такими как антиаритмические лекарственные средства (в т.ч. хинидин, дизопирамид, прокаинамид, амиодарон, соталол), антигистаминные лекарственные средства, антипсихотические лекарственные средства (хлорпромазин, тиоридазин); антибиотики (в т.ч. гатифлоксацин, моксифлоксацин), некоторые лекарственные средства против малярии (в т.ч. мефлохин).
Поскольку палиперидона пальмитат гидролизуется до палиперидона, то при оценке возможности лекарственного взаимодействия следует учитывать результаты исследований палиперидона для приема внутрь.
Способность препарата Ксеплион влиять на другие препараты
Не ожидается, что палиперидон будет проявлять клинически значимое фармакокинетическое взаимодействие с препаратами, метаболизируемыми изоферментами системы цитохрома Р450. Исследования с использованием микросом печени человека in vitro показали, что палиперидон существенно не ослабляет метаболизм веществ изоферментами CYP1A2, CYP2A6, CYP2C8/9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5. Поэтому не ожидается, что палиперидон будет клинически значимо уменьшать клиренс препаратов, метаболизируемых этими изоферментами. Также не ожидается, что палиперидон будет проявлять свойства индуктора изоферментов, т.к. в исследованиях in vitro палиперидон не индуцировал активность изоферментов CYPA2, CYPC19 или CYP3A4.
Палиперидон в высоких концентрациях является слабым ингибитором Р-гликопротеина. Однако данных in vivo в этом отношении нет, и клиническая значимость этого явления неизвестна.
Учитывая действие палиперидона на ЦНС, следует с осторожностью применять Ксеплион в комбинации с другими лекарственными средствами центрального действия и алкоголем. Палиперидон может ослаблять эффект леводопы и агонистов дофаминовых рецепторов.
Из-за способности препарата Ксеплион вызывать ортостатическую гипотензию может наблюдаться аддитивное усиление этого эффекта при применении препарата Ксеплион совместно с другими препаратами, обладающими такой способностью.
Следует с осторожностью сочетать палиперидон с лекарственными средствами, снижающими судорожный порог, такими как фенотиазины, бутирофеноны, трициклические производные, селективные ингибиторы обратного захвата серотонина, трамадол, мефлохин и т.д.
Одновременный прием перорального палиперидона в дозе 12 мг 1 раз/сут и таблеток дивалпроекса натрия пролонгированного действия (в дозе 500–2000 мг 1 раз/сут) не влияет на фармакокинетику вальпроата.
Фармакокинетическое взаимодействие между препаратом Ксеплион и литием маловероятно.
Способность других препаратов влиять на Ксеплион
Палиперидон не является субстратом изоферментов CYP1A2, CYP2A6, CYP2C9, CYP2C19 и CYP3A5. Это позволяет предположить слабую вероятность взаимодействия с ингибиторами и индукторами этих изоферментов. Хотя исследования in vitro показывают возможность минимального участия CYP2D6 и CYP3A4 в метаболизме палиперидона, в настоящее время нет данных о том, что эти ферменты могут играть существенную роль в метаболизме палиперидона in vitro или in vivo. Исследования in vitro свидетельствуют о том, что палиперидон является субстратом P-гликопротеина.
Палиперидон в ограниченной степени метаболизируется изоферментом CYP2D6. В исследовании взаимодействия палиперидона для приема внутрь с активным ингибитором CYP2D6 пароксетином у здоровых добровольцев не обнаружено клинически значимого изменения фармакокинетики палиперидона.
Прием палиперидона с длительным высвобождением активного компонента (1 раз/сут) перорально одновременно с карбамазепином (200 мг 2 раза/сут) приводил к снижению средней Сmax и AUC палиперидона примерно на 37%. Это снижение в значительной степени обусловлено увеличением почечного клиренса палиперидона на 35%, вероятно, за счет активации почечного P-гликопротеина карбамазепином. Очень небольшое уменьшение количества препарата, выводимого через почки в неизмененном виде, позволяет предположить, что карбамазепин лишь слабо влияет на метаболизм в печени или биодоступность палиперидона. При начале применения карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, увеличить. Наоборот, при отмене карбамазепина дозу препарата Ксеплион следует пересмотреть и, при необходимости, уменьшить.
Палиперидон при физиологической рН является катионом и в основном выводится в неизмененном виде через почки – половина путем фильтрации, а половина – путем активной секреции. Одновременное применение триметоприма, который ингибирует систему активного транспорта катионов в почках, не влияло на фармакокинетику палиперидона.
При одновременном назначении перорального палиперидона пролонгированного действия в дозе 12 мг 1 раз/сут и таблеток пролонгированного действия дивалпроекса натрия (2 таблетки по 500 мг 1 раз/сут) наблюдалось увеличение Cmax и AUC палиперидона на 50%, вероятно, в результате увеличения абсорбции препарата при пероральном приеме. Поскольку не наблюдалось значительного влияния на общий клиренс, не ожидается клинически значимого взаимодействия между дивалпроексом натрия, таблетки длительного высвобождения, и препаратом Ксеплион. Следует рассмотреть возможность уменьшения дозы препарата Ксеплион при одновременном назначении с вальпроатом на основании клинической оценки пациента. Исследований взаимодействия с препаратом Ксеплион не проводилось.
Фармакокинетическое взаимодействие лития и палиперидона маловероятно.
Применение препарата Ксеплион совместно с рисперидоном или с пероральной формой палиперидона
Поскольку палиперидон является активным метаболитом рисперидона, следует соблюдать осторожность при одновременном применении в течение длительного периода времени препарата Ксеплион и рисперидона или пероральной формы палиперидона. Данные по безопасности одновременного применения препарата Ксеплион и других антипсихотиков ограничены.
Условия хранения препарата Ксеплион
Препарат следует хранить в недоступном для детей месте при температуре не выше 30°С.
Срок годности препарата Ксеплион
Срок годности — 2 года. Не применять после истечения срока годности.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ЯНССЕН, ФАРМАЦЕВТИЧЕСКОЕ ПОДРАЗДЕЛЕНИЕ ООО «ДЖОНСОН & ДЖОНСОН»

|
|
ЯНССЕН, 121614 Москва, ул. Крылатская, д. 17, корп. 2 |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Ксеплион
Палиперидон (9-гидроксирисперидон) представляет собой активный метаболит рисперидона, первоначально представленный в виде перорального препарата с пролонгированным высвобождением (ORal Osmotic System, OROS®, Alza Corporation) (Invega®, Janssen). Палиперидон для инъекций длительного действия (PLAI) в настоящее время разработан в виде суспензии нанокристаллов палиперидона пальмитата в водной композиции (Invega Sustenna®, Xeplion®), вводимой ежемесячно внутримышечно (в дельтовидную или ягодичную область). Дозы PLAI могут быть выражены либо в миллиграммах-эквивалентах (мг-экв) пальмитата палиперидона, либо в миллиграммах активной фракции палиперидона. Рекомендуемый режим начала приема: 150 мг экв (234 мг) в день 1 и 100 мг экв (156 мг) в день 8 (оба вводятся в дельтовидную мышцу), быстро достигает терапевтических уровней в крови без необходимости перорального приема. Ежемесячные поддерживающие дозы палиперидона пальмитата колеблются от 25 до 150 мг экв. (39–234 мг; рекомендуемая доза 75 мг экв. вводят в дельтовидную (с помощью иглы с отрегулированным весом) или ягодичную мышцу (с использованием иглы 1,5 дюйма 22 G). . Дозу на 8-й день можно вводить +/- 2 дня, а ежемесячные дозы +/- 7 дней без клинически значимого воздействия на концентрации в плазме.
У пациентов с легкой почечной недостаточностью (клиренс креатинина [CrCL]: 50-80 мл / мин) дозировку следует скорректировать. У пациентов с печеночной недостаточностью легкой или средней степени тяжести коррекции дозы не требуется; в настоящее время нет данных относительно тяжелой печеночной недостаточности. Пожилые пациенты с нормальной функцией почек должны получать ту же дозу, что и более молодые взрослые пациенты с нормальной функцией почек. В случае возрастного снижения CrCL следует соответствующим образом скорректировать дозировку. Лечение палиперидона пальмитатом можно начинать на следующий день после прекращения предыдущего перорального лечения антипсихотиками.
Ксеплион , может быть, не при чем?
Известно, что смертность, обусловленная шизофренией, в два-три раза выше, чем у населения в целом, что соответствует сокращению продолжительности жизни на 10-25 лет. На естественную смерть приходится около 60% смертности больных шизофренией, и такие пациенты с большей вероятностью погибают от ишемической болезни сердца. Поскольку было высказано предположение, что более половины внезапных смертей у больных шизофренией имеют сердечное происхождение, внезапная сердечная смерть в основном ответственна за сокращение продолжительности их жизни. В преждевременной смерти больных шизофренией играют роль многие факторы, включая более высокую распространенность курения, плохое питание, более малоподвижный образ жизни и большую вероятность алкоголизма и злоупотребления психоактивными веществами.
Дислипидемия , диабет и коморбидная дислипидемия и диабет чаще встречались в группе необъяснимых случаев смерти больных в психиатрической больнице. Интересно отметить, что необъяснимые внезапные смерти не были связаны с более частым использованием нейролептиков первого или второго поколения. Кроме того, было показано, что более чем у 50% людей с шизофренией шансы на достижение психосоциальных целей снижаются.
Пролонгация сегмента QT
Удлиненный интервал QTc может вызвать потенциально опасные для жизни аритмии. Практически все препараты, применяемые в психиатрической практике, способны удлинять интервал QTc. Есть некоторые признаки того, что психиатры недостаточно осведомлены о рисках удлинения интервала QTc в . Составив список факторов риска, связанных с удлинением интервала QTc, и максимально скорректировав эти факторы, можно снизить общий риск потенциально летальных аритмий и назначить более подходящее фармакологическое лечение.
Влияние нейролептиков на сердечно-сосудистую систему больных шизофренией
Диапазон механизмов, посредством которых нейролептики могут влиять на сердечно-сосудистую систему больных шизофренией , очень широк и включает: блокаду рецепторов; нарушение проводимости (например, блокада ножки пучка Гиса); замедленную реполяризацию желудочков (удлинение интервала QTc); дисфункцию левого желудочка; аномалии синусового узла; миокардит; постуральную гипотензию; синдром полидипсии-гипонатриемии; увеличение веса; непереносимость глюкозы. Из них удлинение интервала QTc с риском прогрессирования до потенциально фатальной желудочковой тахиаритмии Torsades de Pointes (TdP) вызывает особую озабоченность, поскольку эта аритмия непредсказуема и ее трудно контролировать.
Протокол введения ксеплиона
Ксеплион вводят в дозах 150 мг в первый день, 100 мг в 8-й день и 75 мг после 4-й недели. Почти 85% пациентов положительно отвечают на лечение. Обострения психопатологических симптомов шизофрении не обнаружено в ходе лечения ксеплионом. Начало клинического ответа составляло 8 дней у пациентов, получавших рекомендованные начальные 150 мг экв. доза палиперидона пальмитата внутримышечно в дельтовидную мышцу на 1-й день.
Причины смерти на фоне терапии ксеплионом
С момента выпуска инъекционного антипсихотика средства длительного действия палиперидона пальмитата (XEPLION) в 2013 г. до 2014 г. было зарегистрировано 32 смертельных случая (предполагаемое количество пользователей составляет примерно 11 000 пациентов) , зафиксированных на раннем постмаркетинговом этапе. Наиболее частой причиной смерти была внезапная смерть (12 случаев были внезапной смертью, определенной кодами 96.0 и 96.1 МКБ-10, и 4 случая предполагали внезапную смерть), затем следовали самоубийство (7 случаев) и злокачественный нейролептический синдром (4 случая). Несколько смертей произошли с участием пациентов с серьезными соматическими расстройствами, такими как злокачественная опухоль или пневмония. . Риск смертности от всех причин на XEPLION был невысок по сравнению с другими исследованиями; риск внезапной смерти на XEPLION может быть выше, чем на ZODIAC.
Категория сообщения в блог:
Товары из категории — Препараты для лечения неврологических заболеваний
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 11 435
Немного фактов
Лекарственное средство Ксеплион входит в категорию препаратов нейролептиков, призванных облегчить и купировать симптомы шизофрении.
Детальный состав и лекарственная форма
Препарат Ксеплион обладает выраженным антипсихотическим действием, благодаря действующему веществу в его составе. В данном средстве активные терапевтические функции выполняются палиперидона пальмитатом (156 мг), соответствующему дозировке чистого палиперидона в количестве 100 мг.
Кроме активной составляющей для придания препарату необходимой лекарственной формы производитель пользуется вспомогательными элементами, рассчитанными на создание 1 мл суспензии для инъекций.
Медикамент производится в следующих дозировках:
- 25 мг на 0,25 мл;
- 50 мг в 0,5 мл;
- 75 мг на 0,75 мл;
- 0,1 г в 1 мл;
- 0,15 г в 1,5 мл средства.
Суспензия имеет вид белого однородного вещества. Необходимым количеством предварительно наполняются полимерные шприцы, дополнительно упаковывающиеся в пластмассовые формы, закрытые полиэтиленовым слоем. В комплекте с каждым шприцом находятся короткая и длинная иголки для инъекций в m. Deltoideus или m. Gluteus Maximus.
В картонную коробочку вкладывается один набор из наполненного шприца и двух иголок, а также официальная инструкция по применению, в которой содержатся рекомендации к подбору дозировки, использованию и информация о побочных действиях, представленные в ознакомительных целях.
Для начала применения обязательно получение рекомендаций психиатра и назначение им медикамента. Без врачебного рецепта медпрепарат не отпускается из аптеки.
Фармакологические возможности
Ксеплион является атипичным нейролептиком с не до конца выясненным механизмом действия. Известно, что, с помощью гидролиза, в организме палиперидона пальмитат переходит в палиперидоновую форму. Данное вещество способно связываться с серотониновыми (5-НТ2А), допаминовыми (D2), адренергическими (Альфа-1, альфа-2) и гистаминовыми (Н1) рецепторами, не затрагивая при этом М-холинергические и бета-1-, бета-2-адеренергические.
Все энантиомеры активного компонента Ксеплиона демонстрируют одинаковую результативность в любых отношениях.
Предполагаемое действие средства при шизофренических расстройствах личности связано с одновременным воздействием на большое количество серотониновых и допаминовых рецепторов.
От традиционных нейролептиков средство отличается меньшим количеством побочных эффектов в виде каталепсии, снижения двигательной активности и заторможенности движений, а также сниженный риск возникновения экстрапирамидальных расстройств.
Особенностью медикамента является продолжительность действия, вызванная медленным всасыванием средства в системное кровообращение и увеличением концентрации.
При внутримышечном введении одной дозы средства максимальная плазменная концентрация фиксируется на 13-ый день после приема. При этом средство начинает поступать в кровоток с первого дня и наблюдается свыше четырех месяцев.
Особенности использования у разных категорий пациентов
При функциональной недостаточности печени в легких и средних проявлениях плазменная концентрация средства не менялась, сравнительно со здоровыми людьми, что означает отсутствие необходимости изменения режима дозирования.
Легкие почечные заболевания приводят к необходимости корректировки дозы медикамента в сторону уменьшения. У пациентов со средней и тяжелой формами почечной недостаточности применение препарата Ксеплиона запрещено. Рекомендованная доза для людей с легкими формами функциональных патологий почек представлена 75 мг в первые два приема (1-ые, 8-ые сутки), а затем 50 мг в каждый запланированный прием (раз в месяц).
Замечено увеличение вероятности развития побочных явлений при возрастных ухудшениях почечного состояния. При нормальной почечной работе у людей старшего возраста коррекция дозы не требуется.
Не выявлено клинической разницы в эффективности медикамента при использовании у представителей различных рас обоих полов.
Изменения активности у курящих пациентов не выявлено.
Воздействие средства на детей и подростков до 18 лет не изучалось в достаточной мере.
Показания к использованию средства
Препарат создан для предупреждения проявления симптоматики шизоидных расстройств у пациентов взрослого возраста, предварительно прошедших курс лечения палиперидоном или респеридоном, и находящихся в стабильном состоянии.
Возможно использование у пациентов без предварительной стабилизации, если в анамнезе пациентов есть результативная терапия антипсихотическими препаратами (палиперидон, респеридон), а симптомы расстройства выражены в легкой или средней мере и требуют лечения инъекционными формами медикаментов с высокой продолжительностью действия.
В международной классификации болезней (МКБ-10) показания, при которых необходимо использование Ксеплиона имеют номер F20.
Способ применения и дозировка
Ксеплион создан исключительно для внутримышечных инъекций.
Для основной категории больных начальная рекомендованная доза составляет 0,15 г (первая нагрузочная доза) и 0,1 г на восьмые сутки после первого введения. Оба укола следует делать в m. Deltoideus. Дальнейшие инъекции для поддержания плазменной концентрации вводятся каждые четыре недели в дозировке 75 мг. При необходимости возможно корректирование последующих доз в пределах 25-150 мг с каждым последующим приемом, в зависимости от результативности и чувствительности.
При невозможности введения второй нагрузочной дозы на 8-ые сутки, рекомендуется использование средства за 2 дня до или после указанной даты без изменения схемы лечения. Также введение инъекций с поддерживающими целями возможно за или после 7 дней.
Если вторая начальная доза просрочена менее чем на 4 недели, необходимо незамедлительно сделать укол в объеме 100 мг активного компонента. Третью инъекцию проводят спустя 5 недель после начальной нагрузочной дозы в стандартной дозировке без учета времени второй. В дальнейшем сохраняется стандартная 4-недельная схема.
При опоздании второй инъекции на 4-7 недель курс продолжают введением двух доз по 100 мг с недельным интервалом, в дальнейшем соблюдается стандартная схема лечения Ксеплионом.
При превышении 7-недельного разрыва между первой и второй инъекцией терапию начинают заново.
Опоздание любой из последующих инъекций, поддерживающих эффект, на 4-6 нед. необходимо компенсировать скорейшим введением дозы идентичной предыдущей, а затем соблюдать классическую схему.
Пропуск от 1,5 до 6 мес. должен компенсироваться при соблюдении следующих рекомендаций:
- После предыдущей стабилизации дозой 25-100 мг Ксеплион вводится в аналогичном количестве в дельтовидную мышцу, а следующий укол делают спустя семь суток;
- При предыдущей поддерживающей дозе 150 мг, используют 100 мг средства дважды с недельным промежутком.
При интервале между инъекциями больше полугода терапия начинается заново с введения первой нагрузочной дозы.
Первые две инъекции делаются в дельтовидную мышцу короткой иглой при весе до 90 кг и длинной при весе более 90 кг. Дальнейшие уколы могут проводиться, как в дельтовидную, так и в ягодичную (длинной иглой) мышцы.
При переходе с другого антипсихотика возможна его отмена с соблюдением инструкции по применению.
Противопоказания
Абсолютным противопоказанием к применению препарата Ксеплиона является индивидуальная непереносимость элементов состава средства или респеридона в прошлом, а также умеренная или тяжелая почечная недостаточность.
Побочные эффекты
При приеме препарата возможно возникновение следующих побочных явлений:
- Респираторных инфекций, акародерматита, бронхита, подкожного абсцесса и др. инфекций;
- Кожно-аллергических реакций;
- Нейтропении, тромбоцитопении, агранулоцитоза;
- Нарушений секреции вазопрессина;
- Изменений аппетита, веса, повышения или понижения количества сахара в крови, сахарного диабета, кетоацидоза;
- Нарушений сна, кошмаров, тревожности, депрессий, цефалгии, акатизии, головокружений, экстрапирамидальных расстройств, сонливости, паркинсонизма, дезориентации, потери концентрации, судорог, дискинезии, дизартрии, дистонии, парестезии, гиперактивности, обмороков;
- Нечеткости зрения, сухости роговицы, слезотечения, непроизвольных движений глаз;
- Вертиго;
- Гипертензии, атриовентрикулярной блокады, брадикардии, пальпитации, нарушений сердечного ритма, фибрилляции предсердий и желудочков, ортостатической гипотензии, тромбоза;
- Кашля, одышки, ринита, апноэ во сне;
- Абдоминальных болей, нарушения дефекации, диспепсических явлений, метеоризма, отека языка, панкреатита, желтухи;
- Боли в мышцах и суставах, скованность движений;
- Акне, эритемы, зуда, выпадения волос;
- Патологий мочеиспускания;
- Аменореи, галактореи, гинекомастии, половой дисфункции.
При выявлении побочных эффектов рекомендуется врачебная оценка целесообразности лечения Ксеплионом.
Передозировка
Ксеплион редко приводит к передозировке, так как вводится медработниками.
Превышение дозы увеличивает вероятность появления побочных действий и усиления терапевтического эффекта.
Период беременности и лактации
Средство лучше не использовать в периоды гестации и грудного вскармливания.
Лекарственное взаимодействие
Не рекомендуется одновременное использование с другими средствами, оказывающими влияние на нервную систему и поведенческие реакции (анксиолитиками, нейролептиками, трициклическими антидепрессантами, опиатами, алкогольными напитками).
Следует соблюдать осторожность при терапии препаратами, повышающими вероятность судорог (фенотиазинами, бутирофенонами, трамадолом и др.)
Ксеплион не рекомендуется употреблять совместно с карбамазепином из-за снижения максимальной концентрации. С учетом этого необходима коррекция дозы в сторону увеличения.
Особое внимание необходимо уделять одновременному лечению с респеридоном и пероральными формами палиперидона из-за повышенной вероятности возникновения побочных действий.
Условия хранения
Ксеплион особых условий хранения. Использовать в течение 24 месяцев с даты производства.
Аналоги
Заменителями с таким же действующим веществом являются: Инвега, Тревикта.
Цены на Ксеплион в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 11 435 руб.
Сертификаты и лицензии
В психиатрии, как и в других областях медицины, существует значительная часть пациентов, не принимающих лекарства в соответствии с назначенной схемой. Ее величина, по разным оценкам, составляет от 10 до 50%. Примерно у трети пациентов, получающих пероральную антипсихотическую (АП) терапию, нарушения лекарственного комплайенса возникают в первые 1,5 мес. лечения, и только одна четверть пациентов сохраняют приверженность АП-терапии в течение 2-х лет [24]. Эти соотношения реализуются как при назначении классических АП (нейролептиков), так и при использовании атипичных АП-препаратов [20]. Роль методик улучшения лекарственного комплайенса становится особенно значимой на внебольничном отрезке АП-терапии, когда контроль за приемом лекарств не может осуществляться так же, как в стационаре.
В психиатрии, как и в других областях медицины, существует значительная часть пациентов, не принимающих лекарства в соответствии с назначенной схемой. Ее величина, по разным оценкам, составляет от 10 до 50%. Примерно у трети пациентов, получающих пероральную антипсихотическую (АП) терапию, нарушения лекарственного комплайенса возникают в первые 1,5 мес. лечения, и только одна четверть пациентов сохраняют приверженность АП-терапии в течение 2-х лет [24]. Эти соотношения реализуются как при назначении классических АП (нейролептиков), так и при использовании атипичных АП-препаратов [20]. Роль методик улучшения лекарственного комплайенса становится особенно значимой на внебольничном отрезке АП-терапии, когда контроль за приемом лекарств не может осуществляться так же, как в стационаре.
Повышение приверженности пациента проводимой терапии с привлечением психообразования, несмотря на очевидную важность, не может быть определено как заведомо успешное мероприятие. Опрос врачей показывает, что, на основании собственного опыта, большинство из них считает наиболее важным для успешности лечения оптимизацию фармакологических стратегий с предпочтительным использованием пролонгированных инъекционных форм. В этом случае соблюдение врачебных назначений становится легкоконтролируемым мероприятием. Помимо улучшения лекарственного комплайенса этот путь отличается рядом дополнительных преимуществ, главным из которых является стабильная концентрация препарата в крови [24].
Несмотря на наличие нескольких десятков АП-препаратов обоих групп (типичные и атипичные), препаратов пролонгированного действия значительно меньше. Такие представители этой группы, как флуфеназин (в виде флуфеназин-энантата и флуфеназин- деканоата) и галоперидол (в форме галоперидол-деканоата1) широко применяются до настоящего времени. Эти лекарственные средства находятся в ассортименте психиатров в течение нескольких десятков лет.
Сама история депонированных АП-препаратов началась вскоре после появления первых нейролептиков. В 1950-х гг. проводились работы по синтезу длительно действующих гормональных препаратов, которые завершились появлением пропионатов – соединений, представлявших собой сложный эфир пропионовой (пропановой) кислоты. При введении в мышечную ткань такое соединение всасывалось в течение более длительного времени, чем неэстерифицированный гормон, что значительно снижало частоту требуемых инъекций (до 1–2 раз в неделю).
Инициатором исследования по применению аналогичного подхода к новому тогда нейролептику флуфеназину был английский фармаколог Джеральд Даниел. Исследователи этерифицировали гидроксильную группу (–ОН) препарата, присоединив таким образом к эфирной связи карбоновую гептановую (энантановую) кислоту, что позволило значительно замедлить поступление активного вещества из сформировавшегося в месте инъекции лекарственного депо в кровоток. В 1967 г. флуфеназин-энантат стал доступен для широкого применения, став первым АП лекарственным средством замедленного действия. Препарат был предназначен для использования в виде внутримышечных инъекций, которые требовалось проводить 1 раз в 2–3 нед. Это позволило заменить регулярный прием таблетированных форм нейролептиков.
Как пишет D. Johnson (2009), новая концепция инъекционного препарата длительного действия первоначально не была принята клиническими психиатрами, авторитетными специалистами. Главным в этих опасениях было недоверие к новой организации лечебного процесса. В печатных работах того времени высказывались сомнения в том, что одна инъекция на протяжении нескольких недель действительно способна обеспечить стабильное поступление действующего вещества. В первоначальных рекомендациях предлагалось с началом применения пролонгированного АП не прекращать прием таблетированной формы, оставив ее «для подстраховки». Другим аргументом были опасения по поводу предполагаемого возрастания частоты и продолжительности побочных эффектов. Эти настроения специалистов были поддержаны потребителями психиатрических служб, к которым была обращена антипсихиатрическая риторика того времени, оперировавшая впечатляющими эпитетами («лекарственные кандалы», «химическое оглушение»). Тем не менее, внимание клиницистов к проблеме несоблюдения регулярных врачебных предписаний, особенно при длительных курсах, а также последовательное увеличение объема научной информации о новых препаратах привели к тому, что удельный вес пролонгированных инъекционных АП существенно возрос. В серии исследований была показана эффективность пролонгированных инъекционных АП при хронической и приступообразной шизофрении [10, 14, 27–29]. Депонированные формы оказались эффективнее таблетированных при длительных курсах терапии (более 1 года) [11]. В результате, к 1990-м гг. частота их назначений для поддерживающей терапии у внебольничного контингента составляла от 20% в США до 80% – в Великобритании [15, 17]. Практические врачи также оценили возможность улучшенного контроля за введением препарата, что является особенно актуальным у пациентов с тенденцией к несоблюдению назначенной АП-терапии.
Впоследствии было обнаружено, что удлинение карбоновой цепи (с 7 до 10 и более атомов углерода) еще более замедляет поступление препарата в кровь. Второй препарат пролонгированного действия – комплексный эфир флуфеназина и декановой (каприновой) кислоты (флуфеназин-деканоат) – был выведен на рынок через полтора года после первого. Рекомендованный для него интервал между инъекциями был доведен до 3–4 нед. Исследователями под руководством P. Janssena была разработана и нашла широкое применение депонированная форма эталонного нейролептика – галоперидола (галоперидол-деканоат). Также были получены и депонированные формы различных групп АП-препаратов первого поколения (флупентиксол-деканоат, зуклопентиксол-деканоат, бромперидол-деканоат, пипотиазин-пальмитат и др.).
Такие этерифицированные АП-средства (напр., в виде деканоатов) растворяются в масляном наполнителе. Выбор последнего определяет коэффициент соотношения водной и масляной составляющих, что влияет на скорость высвобождения препарата из жировой ткани в общий кровоток. Чаще производителями использовалось растительное (кунжутное) масло, реже – создавался особый, как правило, патентованный, наполнитель (смесь триглицеридов для зуклопентиксола и флупентиксола) с подходящими к конкретному препарату показателями скорости растворения и распада.
После инъекции комплексный эфир диффундирует из масляного раствора и гидролизуется мышечными эстеразами, высвобождая действующее вещество (рис. 1). Скорость этой диффузии является основным фактором, определяющим интервал между инъекциями и дозу препарата.
Назначение депонированных форм АП-препаратов должно учитывать рассмотренные фармакологические особенности. Инъекции необходимо проводить глубоко внутрь ягодичной мышцы, избегая попадания в седалищный нерв. В качестве альтернативы m. gluteus часто возможна инъекция препаратов-депо внутрь m. deltoideus. Первая инъекция препарата, в случае, если пациент его ранее не получал, должна проводиться в минимальной дозе с возможностью последующего ее изменения.
Для достижения равновесного состояния препарата необходимо примерно 2–3 мес. С этой целью рекомендуется в начальном периоде терапии пролонгом (от нескольких недель до 1–2 мес.) делить дозу между пероральной и депонированной инъекционной формами.
Главными проблемами, связанными с пролонгированными АП-препаратами первого поколения, были экстрапирамидные расстройства, а также болезненность и воспаления в месте инъекции. Существенные трудности возникали и из-за того, что по достижении стабильного равновесного состояния препарата также на долгое время стабилизировались вызванные им побочные эффекты; их разрешение после уменьшения дозы или отмены препарата требовало существенного времени из-за длительного периода его элиминации.
Несмотря на указанные недостатки, депонированные АП назначались достаточно широко. Примерно 30–45% пациентов на постстационарном этапе лечения получали терапию инъекциями антипсихотика-пролонга. По мере замещения оральных АП-нейролептиков атипичными АП-препаратами, обладавшими рядом преимуществ, данный показатель снизился до 20–25% и в дальнейшем сохранялся на этом уровне [24].
При назначении данных препаратов также необходимо учитывать, что некоторые пациенты отрицательно относятся к инъекциям пролонгов и не сразу дают согласие на такой метод лечения [1]. В распоряжении врача относительно немного информации о сравнительных характеристиках пролонгированных форм различных препаратов с учетом их фармакологических особенностей.
Ниже представлены краткие характеристики некоторых пролонгированных АП-препаратов первого поколения (табл. 1).
Галоперидол-деканоат. Помимо психотических состояний, в т.ч. сопровождающихся агрессией, одним из важных показаний к назначению препарата традиционно является профилактика маниакальных состояний. Его период полувыведения является наиболее длительным среди всех пролонгированных нейролептиков (3 нед.), таким образом, интервал между инъекциями в индивидуальных случаях может быть доведен до 6–8 нед. Вследствие выраженного дофаминблокирующего действия галоперидола особое внимание необходимо уделять профилактике и купированию экстрапирамидных осложнений.
Флуфеназин-деканоат. Отличается быстрым пикообразным нарастанием концентрации препарата в крови непосредственно после инъекции на период до 24 ч. В этом периоде могут проявляться транзиторные нежелательные эффекты препарата, такие как острая дистония. В дальнейшем этот показатель уменьшается примерно на 2/3 с последующим еще более плавным снижением.
Флупентиксол-деканоат. Поскольку до появления атипичных АП-препаратов обычная практика состояла в назначении нейролептиков в высоких дозах для преодоления резистентности, флупентиксол-деканоат с широким диапазоном применяемых доз (вплоть до максимального значения 400 мг 1 раз/нед.) получил широкое распространение. Рекомендуется начинать терапию препаратом с тестовой дозы 20–50 мг с последующим индивидуальным подбором до адекватного значения.
Необходимо учитывать, что медленное высвобождение действующего вещества из лекарственного депо существенным образом видоизменяет фармакокинетические параметры препарата, который в таком виде заметно отличается от пероральной формы:
1. Поскольку препарат назначается внутримышечно, эффект первого прохождения через печень минимизирован, что приближает его биодоступность к 100%. Вследствие этого прямой перерасчет дозы таблетированной формы в инъекционную пролонгированную будет неверным, т.к. концентрация препарата в крови при переводе на инъекции пролонга станет выше.
2. Для пероральной формы определяющей фармакокинетической характеристикой является скорость лекарственного метаболизма, в то время как для инъекционной пролонгированной – скорость абсорбции. В случае, если последний показатель оказывается меньше, чем скорость выведения, фармакокинетический профиль носит скачкообразный характер.
3. Депонированным лекарственным средствам требуется существенно большее время от начала применения и до достижения равновесного состояния. Эти препараты не должны использоваться в качестве первоочередных у пациентов, не получавших АП-терапию до этого.
4. Из-за замедленной абсорбции и, как следствие, элиминации действие препарата продолжается в течение длительного времени (до нескольких месяцев) после последнего введения. Таким образом, ухудшение состояния может быть отсрочено после прекращения терапии на 3–6 и более месяцев.
Внедрение препаратов пролонгированного действия явилось большим шагом в психофармакологии, во многом изменившим терапевтические алгоритмы по проведению поддерживающей терапии и лечению хронических форм шизофрении. Однако, хотя появившиеся не менее 20 лет назад атипичные АП-препараты отличаются улучшенным профилем эффективности и безопасности по сравнению с препаратами-нейролептиками, ассортимент депонированных АП-средств еще до недавнего времени был ограничен только перечисленными выше препаратами. Проблему усугубляет тот факт, что таблетированные формы атипичных АП против ожидания клиницистов не привели к улучшению лекарственного комплайенса пациентов [16]. Таким образом, разработка пролонгированных лекарственных форм для новых препаратов явилась насущной необходимостью. Начальной проблемой, которую пришлось решать фармакологам при разработке пролонгированных форм таких атипичных антипсихотиков, как рисперидон и оланзапин, было отсутствие у них концевой гидроксильной (-OH) группы, к которой при этерификации могла бы быть присоединена цепь карбоновой кислоты. В каждом из этих случаев было найдено оригинальное решение.
Первым атипичным АП длительного действия была депонированная инъекционная форма рисперидона (Конста)2, представлявшая собой немодифицированное активное вещество, физически внедренное в состав биодеградируемых микросфер лактидно-гликолидной полимерной структуры (система Medisorb). Подобные биосоставы изначально разрабатывались для использования в качестве медицинского шовного материала. Скорость их водного растворения определяет время действия препарата в интервале до 6 нед. при отсутствии риска воспаления в месте инъекции. Необходимость в атипичном АП-препарате-пролонге была достаточно велика, вследствие чего вскоре после своего появления рисперидон (Конста) занял ведущее место среди препаратов для пролонгированной терапии в ряде стран, в то время как частота назначения ранее наиболее распространенного из его предшественников флупентиксол-деканоата значительно уменьшилась. Препарат поставляется в порошкообразном виде и должен храниться при пониженной температуре. Введение препарата, напротив, требует комнатной температуры; таким образом, он должен быть подготовлен к инъекции заранее. Непосредственно перед инъекцией препарат разводится водосодержащим растворителем. После введения внутрь мышцы полимер гидратируется и постепенно растворяется, при этом активное вещество попадает в кровоток. После единичной инъекции максимальная концентрация препарата в плазме достигается через 4–5 нед. Рекомендован 2-недельный интервал введения, при котором стабильная концентрация препарата достигается в течение 8 нед. На протяжении этого периода необходим дополнительный пероральный прием препарата. Доза препарата составляет 25 мг каждые 2 нед. с возможным повышением до 37,5–50 мг. Некоторые больные могут жаловаться на болезненность в месте инъекции, хотя такие явления отмечаются реже, чем при инъекциях масляных растворов пролонгированных АП.
Сравнительная оценка показала отсутствие значимых отличий между группами больных, получавших пероральную и пролонгированную инъекционную формы рисперидона длительными (до 1 года) курсами, как в отношении терапевтического эффекта, так и переносимости [5]. Тем не менее, существуют отдельные указания, что такие характеристики, как субъективная оценка качества жизни и динамика негативных симптомов, могут быть лучшими у больных, получающих пероральную терапию, в то время как для депонированной формы характерны более высокие показатели инсайта, лучшая динамика продуктивных симптомов и более благоприятный профиль лекарственного комплайенса при, в свою очередь, большей частоте экстрапирамидных расстройств [4, 31].
Широкое использование другого АП-пролонга – моногидратного оланзапина памоата (RELPREVV)3 – к сожалению, оказалось ограниченным из-за реализации требования американской Администрации по пищевым и лекарственным продуктам (FDA) об обязательном назначении препарата только в стационарных условиях с последующим наблюдением и контролем АД в течение как минимум 3 ч для выявления серьезного и потенциально фатального осложнения – чрезмерной седации с делириозным помрачением сознания в рамках так называемого постинъекционного синдрома делириозной седации (PDSS). Этот феномен был впервые отмечен у некоторых пациентов в ходе регистрационных исследований4. Также противопоказано назначение оланзапина памоата пациентам пожилого возраста с деменцией.
В отличие от других депонированных АП-препаратов памоат оланзапина представляет собой не комплексный эфир, а соль памоевой кислоты. Процесс ее диссоциации в мышечной ткани протекает медленно, что приводит к постепенному поступлению высвобожденного оланзапина в кровь в течение 2–4 нед. [9]. Для минимизации нежелательных явлений введение пролонгированного оланзапина требует четкого соблюдения инструкции по применению в отношении локализации и техники проведения инъекции. В дополнение к этим ограничениям в США препарат доступен только в рамках специальной программы распространения RELPREVV Patient Care Program, предусматривающей наличие подготовленного лечащего врача, стационара (или дневного стационара) и прошедшего тренинг сестринского персонала. В литературе приводятся данные о том, что пациенты, получающие пролонгированный оланзапин, характеризуются наилучшими показателями переносимости и соблюдения врачебных предписаний: в течение года показатели выбывания пациентов не превышают уровня 27%. Стоит, однако, отметить, что эти данные были получены в ходе строго формализованных и регламентированных регистрационных клинических исследований и не могут быть однозначно аппроксимированы в повседневную клиническую практику [3, 21].
Общей особенностью применения двух рассмотренных препаратов является требующая предварительного обучения процедура приготовления инъекционного раствора непосредственно перед введением.
Как видно из изложенных выше данных, пролонгированные формы двух атипичных АП-средств (рисперидона в лекарственной форме Конста и оланзапина памоата) значительно отличаются от препаратов-предшественников как фармакологией активного вещества, так и реализацией механизма его замедленного поступления. Во многом именно вследствие этих причин рассмотренные препараты и обладают рядом свойств, усложняющих и ограничивающих их применение, которое оказывается значительно меньшим в сравнении с препаратами-пролонгами первого поколения.
Еще один препарат в ряду атипичных АП пролонгированного действия – палиперидон-пальмитат, доступный в РФ под торговым наименованием Ксеплион (фармацевтическая компания «Янссен»), – призван преодолеть большинство перечисленных выше недостатков.
Образуемое этим пролекарством активное вещество – палиперидон (син. 9-гидроксирисперидон) – соответствует основному активному метаболиту рисперидона, являющемуся продуктом его биотрансформации в печени и в значительной степени отвечающему за терапевтический эффект, регистрируемый при назначении рисперидона.
Фармакологическое действие палиперидона и рисперидона сходно. Палиперидон связывается с центральными D2-допаминовыми и 5-HT2A-серотониновыми рецепторами, оказывая антагонистическое действие. Эта первичная активность препарата, предположительно, лежит в основе механизма терапевтического эффекта.
Также препарат является антагонистом α1 и α2-адренергических и, в меньшей степени, H1-гистаминергических рецепторов. Он не оказывает действия на холинергические мускариновые рецепторы, а также на β1- и β2-адренергические. В противоположность рисперидону, лишенному стереоизомерии, у молекулы палиперидона в месте присоединения гидроксильной группы (–OH) появляется хиральный центр, что определяет для него существование двух стереоизомеров. В отличие от метаболического биогенного палиперидона лекарственный синтетический палиперидон представляет собой рацемическую смесь право- и левовращающего изомеров. Их фармакологическая активность, однако, определена как сходная в качественном и количественном отношениях [13].
Метаболизм палиперидона протекает двояко. Основная часть препарата (до 80%) выводится в неизмененном виде почками. Анализ печеночного пути метаболизма палиперидона показывает наличие 4 метаболитов; доля каждого из них не превышает 10% от начальной дозы палиперидона. Не отмечено влияния печеночного метаболического пути на активность изоэнзимов системы цитохрома P450. Такие факторы, как курение, возраст, пол и расовая принадлежность не являются факторами, значимо влияющими на метаболизм палиперидона [6].
Нарушение функции почек влияет на клиренс палиперидона. По этой причине доза палиперидона должна быть уменьшена у пациентов с почечной недостаточностью; также назначение препарата не рекомендуется при почечной недостаточности выраженной степени [13].
При назначении необходимо учитывать, что палиперидон проникает в грудное молоко; таким образом, пациентки, принимающие его, должны воздержаться от кормления грудью [Gilday, 2012].
Палиперидон-пальмитат — это сложный эфир, находящийся в состоянии стабилизированной водной суспензии. Его водорастворимость очень невелика. После инъекции препарат крайне медленно растворяется и гидролизуется до палиперидона ферментами мышечной ткани (рис. 2). Среднее значение времени полувыведения палиперидон-пальмитата после единичной инъекции в дозе 50–150 мг⋅экв составляет 25–49 дней. Инъекции должны проводиться 1 раз в месяц. Поступление палиперидона в кровь начинается в день инъекции и продолжается до 126 дня [13]. Таким образом, назначение палиперидон-пальмитата не требует поддерживающего начального периода перорального приема АП до достижения стабильной концентрации. Однако для оценки переносимости рекомендуется назначение тестовой дозы перорального палиперидона (или рисперидона) пациентам, не принимавшим ранее этот препарат.
Инъекции палиперидон-пальмитата могут быть назначены в дозах 50, 75, 100 и 150 мг⋅экв, которые соответствуют суточным дозам 3, 6, 9 и 12 мг перорального палиперидона. В случае, если происходит перевод с другого пролонгированного АП-препарата, инъекция палиперидон-пальмитата должна быть проведена в срок и вместо предстоящей инъекции пролонга. Дозы палиперидон-пальмитата 50, 75 и 100 мг⋅экв 1 раз в 4 нед. соответствуют дозам 25, 37,5 и 50 мг 1 раз в 2 нед. пролонгированной инъекционной формы рисперидона [6].
Препарат поставляется в готовых к использованию заполненных шприцах и не требует разведения. Хранение может осуществляться при комнатной температуре. Как уже упоминалось, препарат доступен в различных дозах: 78, 117, 156 и 234 мг, что соответствует 50, 75, 100 и 150 мг активного вещества (мг⋅экв). Первые две инъекции (в 1-й и на 8-й дни) должны проводиться в области дельтовидной мышцы, однако последующие поддерживающие инъекции могут быть локализованы как в дельтовидной, так и в ягодичной мышцах в соответствии с желанием пациента. При этом считается, что положение точки инъекции влияет на максимальную концентрацию препарата в крови: при инъекции в m. gluteus этот показатель оказывается на 1/3 ниже, чем при инъекции в m. deltoideus [13].
Клиническое применение
Действие палиперидон-пальмитата оценивалось у пациентов с обострением шизофрении на протяжении 9- и 13-недельных курсов терапии. Также была проведена оценка эффективности препарата в качестве средства длительной поддерживающей и профилактической терапии, начинающейся после становления лекарственной ремиссии. Их результаты свидетельствуют об эффективности палиперидон-пальмитата в каждом из этих применений.
Активная терапия
В серии клинических исследований была показана эффективность палиперидон-пальмитата в дозе 50–150 мг⋅экв суммарно у 1805 пациентов с обострением шизофрении. Клинический эффект в целом может быть охарактеризован как дозозависимый. Определенный диапазон эффективных доз совпал с диапазоном доступных дозировок препарата, хотя исследователями подчеркивается, что данные по группе пациентов, получавших препарат в дозе 150 мг⋅экв, нуждаются в дальнейшем уточнении. Становление терапевтического эффекта может быть отнесено уже к 8-му дню терапии. Пациентам с большей остротой состояния, как правило, требуется быстрое увеличение дозы до уровня 150 мг⋅экв (рис. 3).
Поддерживающая терапия
Оценка длительной поддерживающей терапии палиперидон-пальмитатом в течение полутора лет показала, что медианное время наступления рецидива в группе плацебо составило 163 дня, аналогичный показатель для терапевтической группы не может быть определен из-за незначительного количества рецидивов (менее 25%). Общий показатель риска возникновения рецидива составил менее 10% в группе поддерживающей терапии в сравнении с 35% в контрольной группе [12]. Результаты длительной профилактической терапии дозами 75–100 мг⋅экв палиперидон-пальмитата в течение года также свидетельствуют о его высокой эффективности: 83% безрецидивных наблюдений в сравнении с 76% в контрольной группе (рис. 4).
Безопасность и переносимость
В клинических исследованиях были зарегистрированы следующие нежелательные явления, связанные с назначением палиперидон-пальмитата: болезненность в месте инъекции, головокружение, экстрапирамидные расстройства, включая акатизию, а также седация. Частота каждого из них находилась на уровне 5%. Большинство участников исследований при использовании препарата в дозе 50–150 мг⋅экв в течение 25 и более недель хорошо переносили терапию [25].
Для пациентов, получающих поддерживающую или профилактическую терапию длительными курсами, необходим выбор препарата с минимальным потенциалом развития эндокринных и метаболических нарушений.
Эффект гиперпролактинемии при лечении палиперидон-пальмитатом в большей степени выражен у женщин и имеет тенденцию к стабилизации в течение 1–2 мес. терапии. Он может быть охарактеризован как дозозависимый – клинически значимые случаи были связаны с дозой препарата 150 мг⋅экв [7]. То же можно сказать и об эффекте увеличения массы тела на 7% и более: 5% больных при минимальной дозе, 8% – при 100 мг 13% – при 150 мг⋅экв в сравнении с 5% в группе плацебо-контроля. Также необходимо отметить, что не отмечено клинически значимых нарушений уровня глюкозы, инсулина и липидов в сыворотке крови – симптомов, свидетельствующих о риске развития так называемого метаболического синдрома – предболезненного состояния, предрасполагающего к развитию сахарного диабета, гипертонической болезни и ишемической болезни сердца и проявляющегося абдоминальным ожирением, артериальной гипертензией и снижением толерантности к глюкозе.
Представляют интерес данные L. Alphs и соавт. [2], проанализировавших данные о 33 906 инъекциях палиперидон-пальмитата 3817 пациентам и обнаруживших, что ни в одном из этих случаев не было зарегистрировано развития PDSS, и только 2 (0,006%) инъекции сопровождались развитием седации средней степени выраженности. Предполагается, что, с одной стороны, менее выраженное (по сравнению с оланзапином) седативное действие, с другой, – замедленная растворимость лекарственной формы, которая не изменяется в зависимости от окружающих лекарственное депо сред и тканей, способствуют такому улучшению безопасности и переносимости препарата.
С учетом клинического опыта и на основании вышеприведенных выводов могут быть сформулированы общие формализованные рекомендации по проведению терапии инъекционными антипсихотиками пролонгированного действия (рис. 5). Конкретный выбор препарата предлагается основывать на необходимом профиле терапевтического действия (способность купировать психомоторное возбуждение, потенциал воздействия на продуктивную/негативную симптоматику и др.), а также с учетом вопросов безопасности и фармакоэкономических факторов.
Заключение
Порядка 80% пациентов с первым эпизодом шизофрении достигают лекарственной ремиссии. К сожалению, большая их часть сталкивается с рецидивами заболевания, наступающими примерно у 50% из них в течение 1–2 лет [19]. Одной из причин этого является высокий удельный вес отказов от проведения поддерживающей терапии. Именно данный факт делает целесообразным назначение инъекционных пролонгированных форм АП-препаратов оправданным применительно ко всем этапам терапии. Прогресс фармакологии, который привел к появлению высокотехнологичных и высокоэффективных АП-пролонгов нового поколения, позволит улучшить качество жизни пациентов и оптимизировать терапевтические подходы как на активном, так и поддерживающем/профилактическом этапах лечения.
1 В соответствии с химической номенклатурой названия комплексных эфиров должны писаться слитно, при этом название радикала используется в именительном падеже, а кислотного остатка — с суффиксом «-ат» (напр., галоперидолдеканоат). Поскольку такое написание не соответствует сложившейся в фармакологии традиции, мы в настоящей работе используем «промежуточный» вариант с написанием через дефис (галоперидол-деканоат). В противоположность этому, названия солей пишутся нами согласно номенклатуре – раздельно с названием катиона в родительном падеже, аниона — в именительном (напр., оланзапина памиат).
2 Препарат производится компанией Янссен и поставляется в РФ под торговой маркой Рисполепт Конста.
3 Препарат Zyprexa RELPREVV компании «Эли-Лилли» в настоящее время для применения в РФ не зарегистрирован.
4 Точный механизм этого осложнения в настоящее время до конца не выяснен. Одно из возможных объяснений состоит в том, что случайное попадание инъекционной иглы в сосуд мелкого калибра или в достаточно густую капиллярную сеть в толще мышечной ткани приводит к проникновению нерасчетной дозы оланзапина — высокопотентного препарата с выраженным седативным эффектом — в сосудистое русло. В условиях непрерывного кровотока диссоциация памоата оланзапина многократно ускоряется, и происходит выраженное повышение содержания оланзапина в крови, сопровождающееся симптомами PDSS. Спонтанное разрешение в большинстве случаев происходит в диапазоне 3–72 ч. Медицинская помощь обычно ограничивается наблюдением с контролем витальных показателей. Кумулятивный риск возникновения PDSS у пациента в течение года при постоянном применении препарата оценивается в 0,7–1,2% [26].
Литература
1. Аведисова А.С., Ястребов Д.В. и др. Мотивы отказов больных шизофренией от длительной антипсихотической терапии // Психиатрия и психофармакотерапия. 2009.
2. Alps L., Gopal S. et al.. Are the Long-Acting Intramuscular Formulations of Risperidone or Paliperidone Palmitate Associated with Post-Injection Delirium/Sedation Syndrome? An Assessment of Safety Databases // Current Drug Safety. 2011. Vol. 6. P. 43–45.
3. Ascher-Svanum H., Montgmery W. et al. Treatment completion rates of olanzapine and risperidone in long acting injectable formulations for the treatment of schizophrenia: a comparison of single arm open-label studies // Schizophr. Res. 2008 (Suppl. 2). P. 278.
4. Basu A., Pereira J. et al. The pharmacological management of schizophrenia // Sem. General Adult Psychiatry. 2007. P. 238–294.
5. Chue P., Eerdekens M. et al. Efficacy and safety of long-acting risperidone microspheres and risperidone oral tablets // Schizophr. Res. 2002. Vol. 53 (Suppl. 3). P. 174–175.
6. Citrome L. Paliperidone palmitate: review of the efficacy, safety, and cost of a new second-generation depot antipsychotic medication // Int. J. Clin. Pract. 2010. Vol. 64. P. 216–239.
7. Coppola D., Liu Y. A one-year prospective study of the safety, tolerability and pharmacokinetics of the highest available dose of paliperidone palmitate in patients with schizophrenia. BMC Psychiatry 2012, 12:26
8. Gopal S., Vijapurkar U. et al. A 52-week open-label study of the safety and tolerability of paliperidone palmitate in patients with schizophrenia // J. Psychopharmacol. 2011. Vol. 25(5). P. 685–697.
9. Gulliver A., Detke H., McDonnell D.P. Olanzapine long acting injection: pharamcokinetics and dose correspondence data relative to oral olanzapine // Int. J. Neuropsychopharamcol. 2008. Vol. 11(Suppl. 1). P. 152–153.
10. Hirsch S.R., Gaind R. et al. Outpatient maintenance of chronic schizophrenic patients with long acting phenothiazines // BMJ. 1973; i: 633–637.
11. Hogarty G.E., Schooler N.R. et al. Fluphenazine and social therapy in the aftercare of schizophrenic patients. Relapse analyses of a two-year controlled study of fluphenazine decanoate and fluphenazine hydrochloride // Arch. Gen. Psychiatry. 1979. Vol. 36. P. 1283–1294.
12. Hough D., Gopal S. et al. Paliperidone palmitate maintenance treatment in delaying the time-to- relapse in patients with schizophrenia: a randomized, double-blind, placebo-controlled study // Schizophr. Res. 2010. Vol. 116(2–3). P. 107–117.
13. Hoy S.M., Scott L.J., Keating G.M. Intramuscular paliperidone palmitate // CNS Drugs. 2010. Vol. 24. P. 227–244.
14. Johnson D.A.W. Observations on the use of long-acting depot neuroleptic injections in the maintenance treatment of schizophrenia // J. Clin. Psychiatry. 1984. Vol. 45. P. 13–21.
15. Johnson D.A.W. United Kingdom: neuroleptic relapse prevention // Guidelines for Neuroleptic Relapse Prevention in Schizophrenia (под ред. W. Kissling). Springer, 1991. P. 45.
16. Johnson D.A.W. Historical perspective on antipsychotic long-acting injections // Brit. J. Psychiatry. 2009. Vol. 195. S. 7–12.
17. Kissling W. (ред). Neuroleptic relapse prevention // Guidelines for Neuroleptic Relapse Prevention in Schizophrenia. Springer, 1991. P. 50–52.
18. Kramer M., Litman R. et al. Paliperidone palmitate, a potential long-acting treatment for patients with schizophrenia. Results of a randomized, double-blind, placebo-controlled efficacy and safety study // Int. J. Neuropsychopharmacol. 2010. Vol. 13(5). P. 635–647.
19. Leucht C., Heres S. et al. Oral versus depot antipsychotic drugs for schizophrenia — a critical systematic review and meta-analysis of randomised long-term trials // Schizophr. Res. 2011. Vol. 127, № 1–3. P. 83–92.
20. Lieberman J.A., Stroup T.S. et al. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia // N. Engl. J. Med. 2005. Vol. 353. P. 1209–1223.
21. Lindenmayer J.P. Long-acting injectable antipsychotics: focus on olanzapine pamoate // Neuropsychiatr. Dis. Treat. 2010. Vol. 24 (6). P. 261–267.
22. Marcus S.C., Olfson M. Outpatient antipsychotic treatment and inpatient costs of schizophrenia // Schizophr. Bull. 2008. Vol. 34 (1). P. 173–180.
23. Markowitz M., Fu D.-J. и др. Long-acting injectable paliperidone palmitate versus oral paliperidone extended release: a comparative analysis from two placebo-controlled relapse prevention studies. Annals of General Psychiatry. 2013, 12: 22.
24. Nasrallah H. A. The case for long-acting antipsychotic agents in the post-CATIE era // Acta Psychiatr. Scand. 2007. Vol. 115. P. 260–267.
25. Nasrallah H.A., Gopal S. et al. A controlled, evidence-based trial of paliperidone palmitate, a long-acting injectable antipsychotic, in schizophrenia // Neuropsychopharmacol. 2010. Vol. 35(10). P. 2072–2082.
26. Novakovic V., Adel T. et al. Long-acting injectable antipsychotics and the development of postinjection delirium/sedation syndrome (PDSS) // Clin. Neuropharmacol. 2013. Vol. 36(2). P. 59–62.
27. Pietzcker A., Gaebel W. et al. A German multicenter study on the neuroleptic long-term therapy of schizophrenic patients // Pharmacopsychiatry. 1986. Vol. 19. P. 161–166.
28. Rifkin A., Quitkin F., Rabiner C.J. Fluphenazine decanoate, fluphenazine hydrochloride given orally and placebo in remitted schizophrenia: relapse rate over one year // Arch. Gen. Psychiatry. 1977. Vol. 34. P. 43–47.
29. Schooler N.R., Levine J. et al. Prevention of relapse in schizophrenia: an evaluation of fluphenazine decanoate // Arch. Gen. Psychiatry. 1980. Vol. 37. P. 16–24.
30. Stip E., Abdel-Baki A. et al. An expert opinion from the Association des médecins psychiatres du Québec // Can. J. Psychiatry. 2011. Vol. 56, № 6. P. 367–376.
31. Zhornitsky S., Stip E. Oral versus long-Acting injectable antipsychotics in the treatment of schizophrenia and special populations at risk for treatment nonadherence: a systematic review // Schizophr. Res. Treatment. 2012. 12 p.
Большинство нежелательных побочных реакций были слабыми или средней тяжести.
Ниже указаны нежелательные реакции, наблюдавшиеся у пациентов. Частоту нежелательных реакций классифицировали следующим образом: очень часто (≥10%); часто (≥1% и <10%); нечасто (≥0,1% и <1%); редко (≥0,01% и <0,1%) и очень редко (<0,01%).
Инфекции: часто — инфекции верхних дыхательных путей; нечасто — акродерматит, бронхит, воспаление подкожной жировой клетчатки, инфекции уха, инфекции глаза, грипп, онихомикоз, пневмония, инфекции дыхательных путей, синусит, подкожный абсцесс, тонзиллит, инфекции мочевыделительной системы.
Со стороны иммунной системы: нечасто — гиперчувствительность.
Со стороны кровеносной и лимфатической системы: нечасто — нейтропения, уменьшение количества белых кровяных клеток; редко — тромбоцитопения; очень редко — агранулоцитоз.
Со стороны эндокринной системы: редко — неадекватная секреция АДГ.
Метаболические нарушения: часто — повышение массы тела; нечасто — анорексия, гипергликемия, снижение аппетита, повышение аппетита, снижение массы тела, полидипсия, сахарный диабет; редко — гипогликемия; очень редко — диабетический кетоацидоз, водная интоксикация.
Психические расстройства: очень часто — бессонница, возбуждение; часто — ночные кошмары, беспокойство; нечасто — депрессия, нарушение сна, мании.
Со стороны нервной системы: очень часто — головная боль; часто — акатизия, головокружение, экстрапирамидные симптомы, сонливость, паркинсонизм (в т.ч. акинезия, брадикинезия, ригидность по типу зубчатого колеса, слюнотечение, экстрапирамидные симптомы, отклонение глабеллярного рефлекса, мышечная ригидность, скованность в мышцах, скелетно-мышечная неподвижность); нечасто — нарушение координации, цереброваскулярные нарушения, судороги (в т.ч. эпилептические судороги), рассеянность внимания, постуральное головокружение, дизартрия, дискинезия (в т.ч. атетоз, хорея, хореоатетоз, нарушение движения, мышечные сокращения, клонические судороги), дистония (в т.ч. блефароспазм, спазм шеи, эмпростотонус, спазм лица, ларингоспазм, непроизвольные мышечные сокращения, миотония, движения глазного яблока, опистотонус, орофарингеальный спазм, плеврототонус, сардоническая улыбка, тетания, паралич языка, спазм языка, кривошея, судорожное стискивание челюстей), гипестезия, парестезия, психомоторная гиперактивность, обморок, тяжелая дискинезия, тремор.
Офтальмологические нарушения: нечасто — сухость глаз, увеличение слезотечения, окулярная гиперемия, непроизвольное движение глазного яблока, нечеткость зрительного восприятия.
Со стороны органа слуха и равновесия: нечасто — вертиго, боль в ухе.
Со стороны ССС: часто — повышение АД; нечасто — AV блокада, брадикардия, нарушение проводимости, нарушения на ЭКГ, увеличение интервала QT на ЭКГ, сердцебиение, синдром постуральной ортостатической тахикардии, синусовая аритмия, тахикардия, фибрилляция предсердий, ортостатическая гипотензия; редко — тромбоз глубоких вен; очень редко — эмболия легочной артерии.
Со стороны дыхательной системы: нечасто — кашель, диспноэ, носовое кровотечение, заложенность носа, боль в глоточно-гортанной области, заложенность дыхательных путей, свистящее дыхание, заложенность легких; очень редко — синдром апноэ во сне.
Желудочно-кишечные нарушения: часто — боль в верхней части живота, запор, диарея, сухость слизистой оболочки полости рта, тошнота, зубная боль, рвота, дискомфорт в области живота; нечасто — диспепсия, дисфагия, недержание кала, метеоризм, гастроэнтерит, отек языка, дисгевзия; редко — панкреатит.
Со стороны гепатобилиарной системы: очень редко — желтуха.
Со стороны костно-мышечной системы и соединительной ткани: часто — боль в конечностях, скелетно-мышечная боль; нечасто — артралгия, боль в спине, скованность суставов, опухание суставов, мышечные спазмы, боль в шее.
Со стороны кожи: нечасто — акне, сухость кожи, экзема, эритема, гиперкератоз, крапивница, зуд, сыпь, алопеция; редко — ангиоэдема.
Со стороны мочевыделительной системы: нечасто — дизурия, поллакиурия, недержание мочи; редко — задержка мочевыведения.
Со стороны репродуктивной системы и молочных желез: нечасто — аменорея, галакторея, гинекомастия, сексуальная дисфункция, нарушения эякуляции, эректильная дисфункция, вагинальные выделения; очень редко — приапизм.
Влияние на течение беременности, послеродовые и перинатальные состояния: очень редко — синдром отмены у новорожденных.
Прочие: часто — астенические расстройства, слабость, местные реакции (боль, зуд, уплотнение в месте инъекции); нечасто — дискомфорт в области груди, озноб, отек лица, нарушение походки, уплотнение в месте укола, отек (в т.ч. генерализованный отек, периферический отек, мягкий отек), жажда, повышенная температура тела; редко — гипотермия, абсцесс в месте введения инъекции, воспаление подкожной клетчатки в месте введения инъекции, гематома в месте введения инъекции; очень редко — киста в месте введения инъекции, некроз в месте введения инъекции, язва в месте введения инъекции.
Изменения лабораторных показателей: нечасто — увеличение активности ГГТ, ферментов печени, трансаминаз, концентрации холестерина в крови, концентрации триглицеридов в крови, гипергликемия.





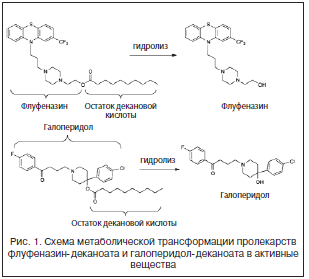
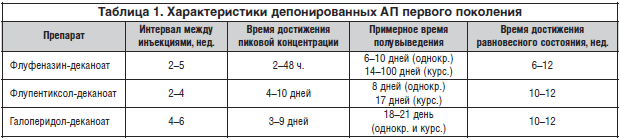
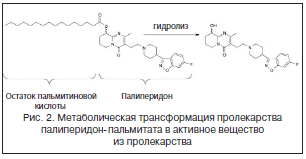
![Рис. 3. Эффект разных доз палиперидон-пальмитата (РР) в сравнении с плацебо (Placebo) при лечении обострения у больных шизофренией; размер эффекта рассчитан по изменению суммарного балла PANSS [данные Gopal S., 2011; Kramer M., 2010; Nasrallah H.A., 2010; Pandina, 2010]](https://www.rmj.ru/data/articles/Image/t21/n30/1610-4.gif)
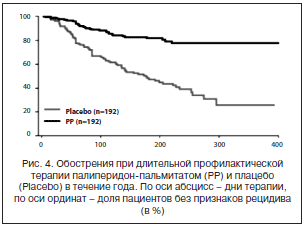
![Рис. 5. Алгоритм назначения АП-терапии с использованием пероральных и депонированных (ДАП) инъекционных препаратов [по E. Stip [30], с изм.]](https://www.rmj.ru/data/articles/Image/t21/n30/1610-6.gif)