Навитен® (Naviten) инструкция по применению
📜 Инструкция по применению Навитен®
💊 Состав препарата Навитен®
✅ Применение препарата Навитен®
📅 Условия хранения Навитен®
⏳ Срок годности Навитен®
⚠️ Срок действия регистрационного удостоверения данного продукта истёк 14.10.10
Описание лекарственного препарата
Навитен®
(Naviten)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2008
года, дата обновления: 2007.06.19
Владелец регистрационного удостоверения:
Код ATX:
C09CA02
(Эпросартан)
Лекарственная форма
| Навитен® |
Таб., покр. оболочкой, 600 мг: 14, 28 или 56 шт. рег. №: ЛС-000837 |
Форма выпуска, упаковка и состав
препарата Навитен®
Таблетки, покрытые оболочкой белого цвета, овальные, двояковыпуклые, с гравировкой «5046» на одной стороне и «SOLVAY» — на другой.
Вспомогательные вещества: целлюлоза микрокристаллическая, лактозы моногидрат, крахмал кукурузный прежелатинизированный, кросповидон, магния стеарат, вода очищенная.
Состав оболочки таблеток: Opadry белый OY-S-9603 (гипромеллоза, макрогол, полисорбат 80, краситель титана диоксид (Е171)).
14 шт. — блистеры (1) — пачки картонные.
14 шт. — блистеры (2) — пачки картонные.
14 шт. — блистеры (4) — пачки картонные.
Фармакологическое действие
Антигипертензивный препарат, блокатор рецепторов ангиотензина II.
Эпросартан избирательно действует на АТ1-рецепторы, расположенные в сосудах, сердце, почках и коре надпочечников, образует с ними прочную связь с последующей медленной диссоциацией.
Ангиотензин II связывается с АТ1-рецепторами во многих тканях (в т.ч. в гладкой мускулатуре сосудов, надпочечниках, почках, сердце) и вызывает вазоконстрикцию, задержку натрия и высвобождение альдостерона, поражение органов-мишеней — гипертрофию миокарда и сосудов.
Эпросартан предупреждает развитие или ослабляет эффекты ангиотензина II. Оказывает вазодилатирующее, гипотензивное и опосредованное диуретическое действие.
Уменьшает артериальную вазоконстрикцию, ОПСС, давление в малом круге кровообращения, реабсорбцию воды и натрия в проксимальном сегменте почечных канальцев, секрецию альдостерона. При длительном применении подавляет пролиферативное влияние ангиотензина II на клетки гладких мышц сосудов и миокарда.
Постоянный антигипертензивный эффект сохраняется в течение 24 ч без развития ортостатической артериальной гипотензии в ответ на первую дозу. Стабилизация антигипертензивного действия при регулярном приеме наступает через 2-3 недели, без изменения ЧСС.
У пациентов с артериальной гипертензией эпросартан не влияет на концентрации ТГ, общего холестерина (Хс) или Хс-ЛПНП в крови, определяемых натощак. Кроме того, эпросартан не влияет на концентрацию глюкозы в крови натощак.
Оказывает нефропротекторное действие, снижая выведение альбуминов при сохранении почечной ауторегуляции вне зависимости от степени почечной недостаточности.
Не оказывает влияния на пуриновый обмен, не оказывает значимого влияния на выведение мочевой кислоты с мочой.
Эпросартан не усиливает такие эффекты, связываемые с брадикинином и опосредуемые АПФ, как, например, кашель. Частота случаев сухого, упорного кашля у пациентов, получающих эпросартан — 1.5%. При замене ингибитора АПФ эпросартаном у пациентов, страдавших кашлем, частота сухого упорного кашля соответствует плацебо.
Прекращение лечения эпросартраном не вызывает синдрома отмены.
Фармакокинетика
Всасывание
После приема внутрь в разовой дозе 300 мг биодоступность препарата составляет 13%. Cmax эпросартана в плазме крови достигается через 1-2 ч.
При приеме эпросартана одновременно с пищей наблюдается клинически незначимое снижение абсорбции (менее 25%), Cmax в плазме крови и значения AUC.
Распределение
Связывание с белками плазмы составляет 98% и имеет постоянный характер в диапазоне терапевтических концентраций.
Vd — 13 л. Практически не кумулирует.
Выведение
T1/2 составляет 5-9 ч. Общий клиренс — 130 мл/мин.
Выводится в основном в неизмененном виде — с калом 90%, с мочой — 7%. Незначительная часть (менее 2%) выводится почками в виде глюкуронидов. 20% от концентрации в моче составляет ацилглюкуронид эпросартана, 80% — неизмененный эпросартан.
Фармакокинетика в особых клинических случаях
Степень связывания с белками плазмы не зависит от пола, возраста, функции печени и не изменяется при незначительно выраженной или умеренной почечной недостаточности, но может снижаться при тяжелой почечной недостаточности.
У лиц моложе 18 лет фармакокинетика не изучена.
При применении эпросартана у пациентов с хронической почечной недостаточностью средней степени тяжести (КК от 30 до 59 мл/мин) значения AUC и Сmax на 30% выше, а с тяжелой степенью (КК от 5 до 29 мл/мин) — на 50% выше по сравнению со здоровыми людьми.
При печеночной недостаточности значение AUC (но не Сmax) возрастает, в среднем, на 40%, что не требует коррекции режима дозирования.
У лиц пожилого возраста значения Сmax и AUC возрастают в среднем в 2 раза, что не требует коррекции режима дозирования.
Масса тела, половые и рассовые различия не оказывают влияния на фармакокинетику эпросартрана.
Показания препарата
Навитен®
- артериальная гипертензия.
Режим дозирования
Препарат принимают внутрь независимо от приема пищи.
Рекомендуемая доза составляет 600 мг 1 раз/сут утром. Подбора начальной дозы не требуется для пациентов пожилого возраста и для больных, страдающих печеночной недостаточностью.
Для пациентов с почечной недостаточностью тяжелой или средней степени тяжести (КК менее 60 мл/мин) суточная доза не должна превышать 600 мг.
Длительность применения Навитена не ограничена.
Побочное действие
Общая частота побочных эффектов, зарегистрированных у пациентов, принимающих эпросартан, сравнима с таковой при приеме плацебо. Эти эффекты, как правило, были слабо выраженными и непродолжительными, поэтому прекращение курса лечения потребовалось лишь у 4.1% пациентов, получавших эпросартан в ходе плацебо-контролируемых клинических исследований (6.5% — в группе плацебо).
Со стороны ЦНС: редко — головная боль, головокружение, астения.
Со стороны сердечно-сосудистой системы: очень редко — снижение АД (в т.ч. постуральная гипотензия).
Дерматологические реакции: очень редко — сыпь, кожный зуд.
Аллергические реакции: редко — крапивница; очень редко — ангионевротический отек, отек лица.
Прочие: редко — кашель.
Противопоказания к применению
- беременность;
- период лактации;
- детский и подростковый возраст до 18 лет (эффективность и безопасность не установлены);
- повышенная чувствительность к компонентам препарата.
С осторожностью следует применять препарат при тяжелой сердечной недостаточности (III и IV функциональный класс по классификации NYHA); двустороннем стенозе почечных артерий; стенозе почечной артерии единственной почки; снижении ОЦК в результате рвоты, диареи, приема диуретиков в высоких дозах.
Безопасность применения Навитена у пациентов с терминальной почечной недостаточностью (КК менее 5 мл/мин, уремия II степени), а также у пациентов, находящихся на гемодиализе, не установлена.
Применение при беременности и кормлении грудью
Навитен противопоказан при беременности и в период лактации.
В случае диагностирования беременности препарат следует отменить и предупредить пациентку о возможных нежелательных последствиях.
При необходимости применения препарата в период лактации грудное вскармливание следует прекратить.
Применение при нарушениях функции печени
Подбора начальной дозы не требуется для пациентов, страдающих печеночной недостаточностью.
Применение при нарушениях функции почек
Для пациентов с почечной недостаточностью тяжелой или средней степени тяжести (КК менее 60 мл/мин) суточная доза не должна превышать 600 мг.
Безопасность применения Навитена у пациентов с терминальной почечной недостаточностью (КК менее 5 мл/мин, уремия II степени), а также у пациентов, находящихся на гемодиализе, не установлена.
Особые указания
При уменьшении ОЦК, обезвоживании или уменьшении содержания электролитов (например, в период лечения высокими дозами диуретиков, многократной рвоте, длительной диарее, бессолевой и гипосолевой диете) прием препарата может вызвать резкое снижение АД (симптоматическая гипотензия). Перед назначением Навитена такие нарушения следует устранить.
Транзиторное снижение АД не является причиной отмены препарата, т.к. в этом случае АД стабилизируется при дальнейшем приеме.
У пациентов, почечная функция которых зависит от активности ренин-ангиотензин-альдостероновой системы (РААС) (например, у пациентов с тяжелой сердечной недостаточностью, при двустороннем стенозе почечной артерии или стенозе артерии единственной почки), во время лечения ингибиторами АПФ может развиться олигурия и/или прогрессирующая азотемия и в редких случаях — тяжелая почечная недостаточность. В связи с недостаточным опытом применения антагонистов рецепторов ангиотензина II у пациентов с тяжелой сердечной недостаточностью или стенозом почечной артерии нельзя исключить нарушения почечной функции на фоне применения Навитена вследствие подавления РААС.
Перед назначением Навитена пациентам с почечной недостаточностью и периодически в течение курса следует контролировать функцию почек. Если в этот период наблюдается ухудшение функции почек, лечение следует пересмотреть.
Навитен можно применять в сочетании с тиазидными диуретиками (в т.ч. с гидрохлоротиазидом) и блокаторами кальциевых каналов (в т.ч. с нифедипином пролонгированного действия); с гиполипидемическими средствами (в т.ч. с ловастатином, симвастатином, правастатином, фенофибратом, гемфиброзилом и никотиновой кислотой).
Влияние на способность к управлению транспортными средствами и механизмами
На основании фармакодинамических свойств эпросартан не должен оказывать влияние на способность к управлению автомобилем и использованию машин и механизмов.
В период лечения артериальной гипертензии необходимо соблюдать осторожность при вождении автотранспорта и занятии потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, в связи с тем, что могут возникать головокружение и слабость.
Передозировка
Имеются ограниченные данные о передозировке у человека. Препарат хорошо переносится при приеме внутрь. Показана эффективность препарата в суточных дозах до 1.2 г при приеме в течение 8 недель, при этом зависимость частоты неблагоприятных эффектов от дозы не выявлена.
Симптомы: наиболее вероятно выраженное снижение АД.
Лечение: проведение симптоматической терапии.
Лекарственное взаимодействие
Клинически значимого взаимодействия Навитена с другими лекарственными препаратами не наблюдалось.
При одновременном применении Навитен не оказывал влияния на фармакокинетику дигоксина и фармакодинамику варфарина, глибенкламида.
Не наблюдалось изменений фармакокинетических параметров Навитена при его одновременном применении с ранитидином, кетоконазолом, флуконазолом.
При одновременном применении Навитена с тиазидными диуретиками (в т.ч. с гидрохлоротиазидом), с блокаторами медленных кальциевых каналов (в т.ч. с нифедипином пролонгированного действия) наблюдается усиление гипотензивного эффекта, при этом не предполагается развитие клинически значимых нежелательных реакций.
При одновременном применении ингибиторов АПФ с препаратами лития возможно обратимое повышение концентрации лития в плазме крови и увеличение риска появления его токсических эффектов. Нельзя исключить данное взаимодействие и при применении эпросартана (необходим тщательный мониторинг концентрации лития у пациентов, получающих такую комбинацию).
Условия хранения препарата Навитен®
Список Б. Препарат следует хранить в недоступном для детей, сухом месте при температуре не выше 25°С.
Срок годности препарата Навитен®
Условия реализации
Препарат отпускается по рецепту.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Состав и форма выпуска препарата
Таблетки, покрытые оболочкой белого цвета, овальные, двояковыпуклые, с гравировкой «5046» на одной стороне и «SOLVAY» — на другой.
| 1 таб. | |
| эпросартана мезилат | 735.8 мг, |
| что соответствует содержанию эпросартана | 600 мг |
Вспомогательные вещества: целлюлоза микрокристаллическая, лактозы моногидрат, крахмал кукурузный прежелатинизированный, кросповидон, магния стеарат, вода очищенная.
Состав оболочки таблеток: Opadry белый OY-S-9603 (гипромеллоза, макрогол, полисорбат 80, краситель титана диоксид (Е171)).
14 шт. — блистеры (1) — пачки картонные.
14 шт. — блистеры (2) — пачки картонные.
14 шт. — блистеры (4) — пачки картонные.
Фармакологическое действие
Антигипертензивное средство, синтетический антагонист рецепторов ангиотензина II, небифениловое производное тетразола.
Эпросартан избирательно связывается с АТ1-рецепторами, расположенными в сосудах, сердце, почках и коре надпочечников, образует с ними прочную связь с последующей медленной диссоциацией.
Ангиотензин II связывается с АТ1-рецепторами во многих тканях (в т.ч. в гладкой мускулатуре сосудов, надпочечниках, почках, сердце) и вызывает вазоконстрикцию, задержку натрия и высвобождение альдостерона, поражение органов-мишеней — гипертрофию миокарда и сосудов.
Эпросартан предупреждает развитие или ослабляет эффекты ангиотензина II. Угнетает активность РААС. Оказывает вазодилатирующее, гипотензивное и опосредованно — диуретическое действие.
Уменьшает артериальную вазоконстрикцию, ОПСС, давление в малом круге кровообращения, реабсорбцию жидкости и ионов натрия в проксимальном сегменте почечных канальцев, секрецию альдостерона. При длительном применении подавляет пролиферативное влияние ангиотензина II на клетки гладких мышц сосудов и миокарда.
У пациентов с артериальной гипертензией эпросартан не влияет на концентрации ТГ, общего холестерина (Хс) или Хс-ЛПНП в крови, определяемых натощак. Кроме того, эпросартан не влияет на концентрацию глюкозы в крови натощак.
Увеличивает почечный кровоток и скорость клубочковой фильтрации, уменьшает выведение альбуминов (нефропротекторное действие), при сохранении почечной саморегуляции вне зависимости от степени выраженности почечной недостаточности.
Прекращение лечения эпросартаном не сопровождается синдромом отмены.
Эпросартан не угнетает изоферменты CYP1A, 2А6, 2С9/8, 2С19, 2D6, 2Е и 3А in vitro.
Гипотензивное действие после приема однократной дозы сохраняется в течение 24 ч, стойкий терапевтический эффект проявляется при регулярном приеме — через 2-3 недели без изменения ЧСС.
Фармакокинетика
После приема внутрь разовой дозы 300 мг биодоступность составляет примерно 13%. При приеме эпросартана одновременно с пищей наблюдается клинически незначимое снижение абсорбции (менее 25%), Cmax в плазме крови и значения AUC. Cmax достигается через 1-2 ч. Связывание с белками плазмы составляет 98% и имеет постоянный характер в диапазоне терапевтических концентраций. Выделяется с грудным молоком. Vd – 13 л, общий клиренс – 130 мл/мин. Практически не кумулирует. T1/2 составляет 5-9 ч. Выводится в основном в неизмененном виде — через кишечник (90%), почками (7%). Незначительная часть (менее 2%) выводится почками в виде глюкуронидов. 20% от концентрации в моче составляет ацилглюкуронид эпросартана, 80% — неизмененный эпросартан.
У лиц пожилого возраста значения Сmax и AUC возрастают в среднем в 2 раза, что не требует коррекции режима дозирования. При хронической почечной недостаточности средней степени тяжести (КК от 30 до 59 мл/мин) величины AUC и Cmax на 30%, а при тяжелой степени (КК от 5 до 29 мл/мин) — на 50% выше по сравнению со здоровыми людьми. При печеночной недостаточности после приема внутрь разовой дозы AUC (но не Cmax) возрастает почти на 40% по сравнению со здоровыми людьми. Практически не выводится при гемодиализе (клиренс — менее 1 л/ч).
Показания
Лечение артериальной гипертензии.
Противопоказания
Гемодинамически значимый двусторонний стеноз почечных артерий и стеноз артерии единственной почки; беременность; период лактации (грудного вскармливания); детский и подростковый возраст до 18 лет (эффективность и безопасность не установлены); повышенная чувствительность к эпросартану.
Дозировка
Принимают внутрь независимо от приема пищи. Рекомендуемая доза составляет 600 мг 1 раз/сут утром. Максимальный антигипертензивый эффект развивается, как правило, через 2-3 недели лечения.
Эпросартан применяют как в виде монотерапии, так и в составе комбинированной терапии (в т.ч. с тиазидными диуретиками, блокаторами кальциевых каналов).
Для пациентов с почечной недостаточностью при КК менее 60 мл/мин суточная доза не должна превышать 600 мг.
Побочные действия
Со стороны неврной системы: очень часто — головная боль; часто — головокружение, астения.
Со стороны сердечно-сосудистой системы: нечасто — выраженное снижение АД.
Со стороны дыхательной системы: ринит.
Со стороны кожных покровов и подкожно-жировой клетчатки: часто —
Со стороны пищеварительной системы: часто — неспецифические жалобы со стороны ЖКТ (например, тошнота, диарея, рвота).
Со стороны мочеполовой системы: нарушение функции почек, в т.ч. острая почечная недостаточность, особенно у пациентов группы риска (например, со стенозом почечной артерии).
Аллергические реакции: кожные проявления (в т.ч. кожная сыпь, зуд); нечасто — ангионевротический отек (в т.ч. лица, губ, языка, глотки).
Со стороны иммунной системы: нечасто — гиперчувствительность.
Лекарственное взаимодействие
Эпросартан можно применять в сочетании с тиазидными диуретиками (в т.ч. с гидрохлоротиазидом) и блокаторами медленных кальциевых каналов (в т.ч. нифедипином пролонгированного действия), не ожидая клинически значимого нежелательного взаимодействия, при этом происходит взаимное усиление гипотензивного эффекта.
При одновременном применении эпросаратана с калийсберегающими диуретиками, пищевыми добавками, содержащими калий, заменителями поваренной соли, содержащими калий и другими препаратами, повышающими уровень калия в сыворотке крови (например, гепарином) возможно повышение уровня калия в сыворотке крови. Во время лечения препаратами, воздействующими на РААС возможно развитие гиперкалиемии, особенно, у пациентов с почечной и/или печеночной недостаточностью.
Антигипертензивное действие эпросартана может быть потенцировано другими антигипертензивными средствами.
Известны случаи обратимого повышения концентрации лития в сыворотке крови и развития токсических реакций при одновременном приеме препаратов лития с ингибиторами АПФ. Нельзя исключать возможность развития подобного эффекта после приема эпросартана (при данной комбинации рекомендуется контроль концентрации лития в плазме крови).
При одновременном применении эпросартана с НПВС имеется вероятность ухудшения функции почек, включая риск развития острой почечной недостаточности, и повышения уровня калия в сыворотке крови, особенно у пациентов с уже имеющимся нарушением функции почек (данные комбинации следует применять с осторожностью, особенно у пациентов пожилого возраста; рекомендуется контроль функции почек).
Особые указания
Не рекомендуется применять для лечения пациентов с первичным гиперальдостеронизмом.
С осторожностью применять при тяжелой хронической сердечной недостаточности (IV функционального класса по классификации NYHA); снижении ОЦК и/или избыточном выведении хлорида натрия из организма (в т.ч. в результате рвоты, диареи, приема диуретиков в высоких дозах); у пациентов, находящихся на гемодиализе или с КК менее 30 мл/мин; при стенозе аортального и митрального клапанов, а также при гипертрофической кардиомиопатии.
С особой осторожностью применять у пациентов с нарушением функции печени и ИБС, в связи с недостаточным клиническим опытом применения у данных категорий пациентов.
Не имеется данных о применении эпросартана у пациентов с терминальной стадией почечной недостаточности и недавно выполненной трансплантацией почек.
Беременность и лактация
Противопоказано применение при беременности и в период лактации (грудного вскармливания).
Применение в детском возрасте
Противопоказан в детском возрасте.
При нарушениях функции почек
У пациентов, функция почек которых зависит от активности ренин-ангиотензин-альдостероновой системы (например, при тяжелой сердечной недостаточности, двустороннем стенозе почечных артерий или стенозе почечной артерии единственной почки), во время лечения ингибиторами АПФ развивается олигурия и/или прогрессирующая азотемия, а в редких случаях — острая почечная недостаточность.
Описание препарата НАВИТЕН основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Предоставленная информация о ценах на препараты не является предложением о продаже или покупке товара. Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствии со статьей 55 ФЗ «Об обращении лекарственных средств».
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Активные вещества: этинилэстрадиол — 0,020 мг, дезогестрел — 0,150 мг;
Вспомогательные вещества: краситель хинолиновый жёлтый Е 104, ?-токоферол, магния стеарат, кремния диоксид коллоидный, стеариновая кислота, повидон, картофельный крахмал, лактозы моногидрат;
Пленочная оболочка: пропиленгликоль, макрогол 6000, гипромеллоза.
Круглые двояковыпуклые таблетки светло-жёлтого цвета с маркировкой «Р9» на одной стороне и «RG» на другой.
Фармакотерапевтическая группа:
контрацептивное средство (эстроген + прогестаген)
Код ATX
G03AA09
Фармакодинамика
Новинет® является комбинированным пероральным противозачаточным препаратом, основное контрацептивное действие которого заключается в ингибировании синтеза гонадотропинов и подавлении овуляции. Кроме того, за счет повышения вязкости цервикальной слизи замедляется движение сперматозоидов через цервикальный канал, а изменение состояния эндометрия препятствует имплантации оплодотворенной яйцеклетки. Этинилэстрадиол является синтетическим аналогом эндогенного эстрадиола, дезогестрел обладает выраженным гестагенным и антиэстрогенным действием, подобным эндогенному прогестерону, слабой андрогенной и анаболической активностью. Новинет® оказывает благоприятное воздействие на липидный обмен: повышает концентрацию липопротеинов высокой плотности (ЛПВП) в плазме крови, не влияя при этом на содержание липопротеинов низкой плотности (ЛПНП). На фоне применения препарата отмечается значительное уменьшение количества ежемесячно теряемой крови (при исходной меноррагии), нормализуется менструальный цикл, отмечается благоприятное воздействие на кожу (особенно при наличии вульгарных угрей).
Фармакокинетика
Дезогестрел
Всасывание
При пероральном приеме дезогестрел всасывается из желудочно-кишечного тракта (ЖКТ) быстро и практически полностью. Метаболизируется в 3-кето-дезогестрел, который является биологически активным метаболитом дезогестрела. Средняя максимальная концентрация в сыворотке крови (Cmax) 2 нг/мл, достигается через 1,5 часа (Тmax) после приема таблетки. Биодоступность препарата 62-81 %.
Распределение в организме
3-кето-дезогестрел связывается с белками плазмы крови, в основном с альбуминами и с глобулином, связывающим сексуальные гормоны (ГСПГ). Объем распределения составляет 1,5 л/кг.
Метаболизм
Кроме 3-кето-дезогестрела, который образуется в печени и в стенке кишечника, образуются другие метаболиты: З?-ОН-дезогестрел, З?-ОН-дезогестрел, З?-ОН-5?-Н-дезогестрел (метаболиты первой фазы). Они не обладают фармакологической активностью, и частично, путем конъюгации (вторая фаза метаболизации), превращаются в полярные метаболиты (сульфаты и глюкуронаты). Клиренс из плазмы крови около 2 мл/мин на 1 кг массы тела.
Выведение из организма
Среднее время полувыведения 3-кето-дезогестрела составляет 30 часов. Метаболиты выводятся почками и через кишечник (в соотношении 6:4).
Стабильная концентрация устанавливается к второй половине цикла. В это время уровень кетогестрела увеличивается в 2-3 раза.
Этинилэстрадиол
Всасывание
Этинилэстрадиол всасывается из ЖКТ быстро и полностью. Средняя максимальная концентрация в сыворотке крови (Cmax) 80 пг/мл — через 1-2 часа (Тmax) после приема таблетки. Биодоступность из-за пресистемной конъюгации и эффекта первого прохождения — около 60 %.
Распределение в организме
Этинилэстрадиол полностью связывается с белками плазмы крови, в основном с альбуминами. Объем распределения составляет 5 л/кг.
Метаболизм
Пресистемная конъюгация этинилэстрадиола значительна. Минуя стенку кишечника, (первая фаза метаболизма) он подвергается конъюгации в печени (вторая фаза метаболизма). Этинилэстрадиол и его конъюгаты первой фазы метаболизма (сульфаты и глюкурониды) выделяются в желчь и вступают в энтерогепатическую циркуляцию.
Клиренс из плазмы крови около 5 мл/мин на 1 кг массы тела.
Выделение из организма
Среднее время полувыведения этинилэстрадиола составляет около 24 часов. Около 40 % выводится почками и около 60 % через кишечник.
Стабильная концентрация устанавливается к 3-4 дню, при этом уровень этинилэстрадиола в сыворотке на 30-40 % выше, чем после однократной дозы
беременность или подозрение на нее;
лактация;
наличие тяжелых и/или множественных факторов риска венозного или артериального тромбоза (в т.ч. артериальная гипертензия средней или тяжелой степени с АД 160/100 мм.рт.ст и более);
предвестники тромбоза (в т.ч. транзиторная ишемическая атака, стенокардия), в том числе в анамнезе;
мигрень с очаговой неврологической симптоматикой, в том числе в анамнезе;
венозный или артериальный тромбоз/тромбоэмболия (в т.ч. тромбоз глубоких вен голени, эмболия легочной артерии, инфаркт миокарда, инсульт) в настоящее время или в анамнезе,
наличие венозной тромбоэмболии у родственников;
сахарный диабет (с наличием ангиопатии);
панкреатит (в т.ч. в анамнезе), сопровождающийся выраженной гипертриглицеридемией;
дислипидемия;
тяжелые заболевания печени, холестатическая желтуха (в т.ч. во время беременности), гепатит, в т.ч. в анамнезе (до нормализации функциональных и лабораторных параметров и в течение трех месяцев после возвращения этих показателей в норму);
желтуха вследствие приема ЛC, содержащих стероиды;
желчекаменная болезнь в настоящее время или в анамнезе;
синдром Жильбера, Дубина-Джонсона, Ротора;
опухоли печени (в т.ч. в анамнезе);
сильный зуд, отосклероз или прогрессирование отосклероза во время предыдущей беременности или при приеме глюкокортикостероидов;
гормонозависимые злокачественные новообразования половых органов и молочных желез (в т.ч. подозрение на них);
вагинальное кровотечение неясной этиологии;
курение в возрасте старше 35 лет (более 15 сигарет в день);
индивидуальная повышенная чувствительность к препарату или его компонентам.
С осторожностью
Состояния, повышающие риск развития венозного или артериального тромбоза/тромбоэмболии: возраст старше 35 лет, курение, семейный анамнез, ожирение (индекс массы тела более 30 кг/кв.м), дислипопротеинемия, артериальная гипертензия, мигрень, эпилепсия, клапанные пороки сердца, фибрилляция предсердий, длительная иммобилизация, обширное хирургическое вмешательство, хирургическое вмешательство на нижних конечностях, тяжелая травма, варикозное расширение вен и поверхностный тромбофлебит, послеродовый период, наличие тяжелой депрессии, в т.ч. в анамнезе, изменения биохимических показателей (резистентность активированного протеина С, гипергомоцистеинемия, дефицит антитромбина III, дефицит протеина С или S, антифосфолипидные антитела, в т.ч. антитела к кардиолипину, волчаночный антикоагулянт).
Сахарный диабет, не осложненный сосудистыми нарушениями, системная красная волчанка (СКВ), болезнь Крона, язвенный колит, серповидно-клеточная анемия; гипертриглицеридемия (в т.ч. в семейном анамнезе), острые и хронические заболевания печени.
Беременность и период лактации
Применение препарата во время беременности и в период кормления грудью противопоказано.
Способ применения и дозировка
Внутрь. Прием таблеток начинают с первого дня менструального цикла и принимают по 1 таблетке в сутки в течение 21 дня, по возможности в одно и то же время суток.
После приема последней таблетки из упаковки делают 7-дневный перерыв, во время которого происходит менструальноподобное кровотечение вследствие отмены препарата.
На следующий день после 7-дневного перерыва (через четыре недели после приема первой таблетки, в тот же день недели) возобновляют прием препарата из следующей упаковки, содержащей 21 таблетку, даже если кровотечение не прекратилось. Такой схемы приема таблеток придерживаются до тех пор, пока имеется необходимость в контрацепции. При соблюдении правил приема, контрацептивный эффект сохраняется и на время 7-дневного перерыва. Первый прием препарата
Прием первой таблетки следует начинать с первого дня менструального цикла. В этом случае не требуется использовать дополнительные методы контрацепции.
Прием таблеток можно начинать и с 2-5 дня менструации, но в этом случае в первом цикле использования препарата надо применять дополнительные методы контрацепции в первые 7 суток приема таблеток.
Если прошло более 5 дней после начала менструации, следует отложить начало приема до следующей менструации. Прием препарата после родов
Не кормящие грудью женщины могут начинать прием таблеток не ранее 21 дня после родов, предварительно проконсультировавшись с врачом. В этом случае нет необходимости в применении других методов контрацепции.
Если после родов уже имелся сексуальный контакт, тогда с приемом таблеток необходимо подождать до первой менструации.
Если принимается решение о приеме препарата позже, чем через 21 день после родов, тогда в первые 7 суток необходимо использовать дополнительные методы контрацепции. Прием препарата после аборта
После аборта, при отсутствии противопоказаний, начинать прием таблеток следует с первого дня, и в этом случае нет необходимости в применении дополнительных методов контрацепции. Переход с другого перорального контрацептива
Прием препарата Новинет® после использования другого гормонального перорального контрацептива содержащего 30 мкг этинилэстрадиола, по 21 дневной схеме:
Первую таблетку Новинет® рекомендуется принять на следующий день после завершения курса предыдущего препарата. Не требуется выдерживать 7-дневный перерыв или дожидаться начала менструации. Нет необходимости в применении дополнительных методов контрацепции.
При переходе на Новинет® с препарата, содержащего 28 таблеток, следует на следующий день после того, как закончились таблетки в упаковке, начать новую упаковку Новинет®. Переход к Новинет® после использования пероральных гормональных препаратов, содержащих только прогестаген ( так называемых «мини-пилей»):
Первую таблетку Новинет® надо принять в первый день цикла. Нет необходимости в применении дополнительных методов контрацепции.
Если при приеме мини-пили не возникает менструация, то после исключения беременности можно начинать прием Новинет® в любой день цикла, но в этом случае в первые 7 суток необходимо применять дополнительные методы контрацепции.
В вышеизложенных случаях в качестве дополнительных методов контрацепции рекомендуется применение следующих негормональных методов: использование шеечного колпачка со спермицидным гелем, презерватива, или воздержание от половых контактов. Применение календарного метода в этих случаях не рекомендуется. Отсрочка менструального цикла
Если имеется необходимость в отсрочке менструации, надо продолжать прием таблеток из новой упаковки, без 7-дневного перерыва, по обычной схеме. При отсрочке менструации могут появляться прорывные или мажущие кровотечения, но это не снижает противозачаточное действие препарата. Регулярный прием Новинет® можно восстановить после обычного 7-дневного перерыва. Пропущенные таблетки
Если женщина забыла принять таблетку своевременно, и после пропуска прошло не более 12 часов, нужно просто принять забытую таблетку, а далее продолжить прием в обычное время. Если между приемом таблеток прошло больше 12 часов — это считается пропуском таблетки, надежность контрацепции в этом цикле не гарантируется и рекомендуется применение дополнительных методов контрацепции.
При пропуске одной таблетки на первой или второй неделе цикла, необходимо принять 2 таблетки в следующий день и затем продолжить регулярный прием, используя дополнительные методы контрацепции до конца цикла.
При пропуске таблетки на третьей неделе цикла надо принять забытую таблетку, продолжить регулярный прием и не делать 7-дневный перерыв. Важно помнить, что в связи с минимальной дозой эстрогена повышается риск овуляции и/или кровянистых выделений при пропуске приема таблетки и поэтому рекомендуется применение дополнительных методов контрацепции. Что делать при рвоте или диарее?
Если после приема препарата появляется рвота или диарея, тогда всасывание препарата может быть неполноценным. Если симптомы прекратились в течение 12 часов, то надо принять еще одну таблетку дополнительно. После этого следует продолжать прием таблеток обычным образом. Если симптомы продолжаются больше 12 часов, то необходимо использовать дополнительные методы контрацепции во время рвоты или диареи и в последующие 7 суток.
Побочные эффекты, при появлении которых необходимо немедленное прекращение приема препарата:
— артериальная гипертензия;
— гемолитико-уремический синдром;
— порфирия;
— потеря слуха, обусловленная отосклерозом.
Редко встречающиеся: артериальные и венозные тромбоэмболии (в.т.ч. инфаркт миокарда, инсульт, тромбоз глубоких вен нижних конечностей, тромбоэмболия легочной артерии); обострение реактивной системной красной волчанки.
Очень редко встречающиеся: артериальная или венозная тромбоэмболия печеночных, мезентериальных, почечных, ретинальных артерий и вен; хорея Сиденхема (проходящая после отмены препарата). Другие побочные действия, менее тяжелые, но чаще встречающиеся. Целесообразность продолжения применения препарата решается индивидуально после консультации с врачом, исходя из соотношения польза/риск.
— Репродуктивная система: ациклические кровотечения/ кровянистые выделения из влагалища, аменорея после отмены препарата, изменение состояния влагалищной слизи, развитие воспалительных процессов влагалища (напр.: кандидоз).
— Молочные железы: напряжение, боль, увеличение молочных желез, галакторея.
— Желудочно-кишечный тракт и гепато-билиарная система: тошнота, рвота, болезнь Крона, язвенный колит, возникновение или обострение желтухи и/или зуда, связанного с холестазом, холелитиаз.
— Кожа: узловая/ экссудативная эритема, сыпь, хлоазма.
— Центральная нервная система: головная боль, мигрень, изменения настроения, депрессивные состояния.
— Метаболические изменения: задержка жидкости в организме, изменение (увеличение) массы тела, снижение толерантности к углеводам.
— Глаза: повышение чувствительности роговицы при ношении контактных линз.
— Прочие: аллергические реакции
Возможны тошнота, рвота, у девочек — кровянистые выделения из влагалища.
Препарат не имеет специфического антидота, лечение симптоматическое.
Если симптомы передозировки возникают в первые 2-3 часа после приема препарата, возможно промывание желудка.
Лекарственные средства, индуцирующие печеночные ферменты, такие как гидантоин, барбитураты, примидон, карбамазепин, рифампицин, окскарбазепин, топирамат, фелбамат, гризеофульвин, ЛС, содержащие зверобой обыкновенный снижают эффективность пероральных контрацептивов и повышают риск возникновения кровотечений «прорыва». Максимальный уровень индукции обычно достигается не ранее 2-3 нед, но может продолжаться до 4 нед. после отмены препарата.
Ампициллин, тетрациклин — снижают эффективность (механизм взаимодействия не установлен).
При необходимости совместного приема, рекомендуется использовать дополнительный барьерный метод контрацепции на протяжении всего курса лечения и в течение 7 дней (для рифампицина — в течение 28 дней) после отмены препарата.
Пероральные противозачаточные средства могут снижать толерантность к углеводам, повышать потребность в инсулине или пероральных антидиабетических средств.
Перед началом применения препарата и в последующем каждые 6 мес. Рекомендуется собрать подробный семейный или личный анамнез и пройти общемедицинское и гинекологическое обследование (осмотр гинекологом, взятие цитологического мазка, исследование молочных желез и функции печени, контроль артериального давления (АД), концентрации холестерина в крови, анализ мочи). Эти исследования необходимо периодически повторять, в связи с необходимостью своевременного выявления факторов риска или возникших противопоказаний.
Препарат является надежным контрацептивным лекарственным средством: индекс Перля (показатель числа беременностей, наступивших во время применения метода контрацепции у 100 женщин в течение 1 года) при правильном применении составляет около 0.05.
В каждом случае перед назначением гормональных контрацептивов индивидуально оцениваются преимущества или возможные отрицательные эффекты их приема. Этот вопрос необходимо обсудить с пациенткой, которая после получения нужной информации примет окончательное решение о предпочтении гормонального или какого-либо другого метода контрацепции. Состояние здоровья женщины необходимо тщательно контролировать. Если во время приема препарата появляется или ухудшается любое из ниже перечисленных состояний/заболеваний, необходимо прекратить прием препарата и перейти к другому, негормональному методу контрацепции:
— заболевания системы гемостаза.
— состояния/ заболевания, предрасполагающие к развитию сердечно-сосудистой, почечной недостаточности.
— эпилепсия
— мигрень
— риск развития эстроген-зависимой опухоли или эстроген-зависимых гинекологических заболеваний;
— сахарный диабет, не осложненный сосудистыми нарушениями;
— тяжелая депрессия (если депрессия связана с нарушением обмена триптофана, то с целью коррекции можно применять витамин В6);
— эпилепсия внезапно появившаяся или усугубившаяся,
— серповидноклеточная анемия, так как в отдельных случаях (например, инфекции, гипоксия) эстроген-содержащие препараты при этой патологии могут провоцировать явления тромбоэмболии.
— мигрень внезапно появившаяся или усугубившаяся,
— появление отклонений в лабораторных тестах оценки функции печени.
Тромбоэмболические заболевания
Эпидемиологические исследования доказали, что имеется связь между приемом пероральных гормональных противозачаточных средств и повышением риска артериальных и венозных тромбоэмболических заболеваний (в т.ч. инфаркт миокарда, инсульт, тромбоз глубоких вен нижних конечностей, тромбоэмболия легочной артерии). Доказан повышенный риск венозных тромбоэмболических заболеваний, но он значительно меньше, чем при беременности (60 случаев на 100 тысяч беременностей).
При применении пероральных противозачаточных препаратов очень редко наблюдается артериальная или венозная тромбоэмболия печеночных, мезентериальных, почечных сосудов или сосудов сетчатки.
Риск появления артериальных или венозных тромбоэмболических заболеваний повышается:
— с возрастом;
— при курении (интенсивное курение и возраст старше 35 относятся к факторам риска);
— при наличии в семейном анамнезе тромбоэмболических заболеваний (например, у родителей, брата или сестры). При подозрении на генетическую предрасположенность, необходимо перед применением препарата проконсультироваться со специалистом.
— при ожирении (индекс массы тела выше 30 кг/м2);
— при дислипопротеинемиях;
— при артериальной гипертензии;
— при заболеваниях клапанов сердца, осложненных гемодинамическими нарушениями,
— при фибрилляции предсердий;
— при сахарном диабете, осложненном сосудистыми поражениями;
— при длительной иммобилизации, после большого оперативного вмешательства, после оперативного вмешательства на нижних конечностях, после тяжелой травмы.
В этих случаях предполагается временное прекращение курса применения препарата: желательно прекратить не позже, чем за 4 недели до оперативного вмешательства, а возобновить – не ранее чем, через 2 недели после ремобилизации.
Повышается риск возникновения венозных тромбоэмболических заболеваний у женщин после родов.
Такие заболевания, как сахарный диабет, системная красная волчанка, гемолитико- уремический синдром, болезнь Крона, неспецифический язвенный колит, серповидноклеточная анемия, повышают риск развития венозных тромбоэмболических заболеваний.
Такие биохимические отклонения от нормы, как резистентность к активированному протеину С, гиперхромоцистеинемия, дефицит протеинов С, S, дефицит антитромбина III, наличие антифосфолипидных антител, повышают риск образования артериальных или венозных тромбоэмболических заболеваний.
При оценке соотношения польза/ риск приема препарата надо иметь в виду, что целенаправленное лечение данного состояния снижает риск образования тромбоэмболии. Признаками возникновения тромбоэмболии являются:
— внезапная боль в груди, которая иррадиирует в левую руку,
— внезапная одышка,
— любая непривычно сильная головная боль, продолжающаяся долгое время или появляющаяся впервые, особенно при сочетании с внезапной полной или частичной потерей зрения или диплопией, афазией, головокружением, коллапсом, фокальной эпилепсией), слабостью или выраженным онемением половины тела, двигательными нарушениями, сильной односторонней болью в икроножной мышце, острым животом).
Опухолевые заболевания
В некоторых исследованиях сообщали об учащении возникновения рака шейки матки у тех женщин, которые долгое время принимали гормональные противозачаточные средства, но результаты исследований достаточно противоречивы. В развитии рака шейки матки играет важную роль сексуальное поведение, инфицирование вирусом папилломы человека и другие факторы.
Метаанализ 54 эпидемиологических исследований показал, что имеется относительное повышение опасности рака молочных желез среди женщин, принимающих пероральные гормональные противозачаточные средства, однако более высокая выявляемость рака молочных желез могла быть связана с более регулярным медицинским обследованием. Рак молочных желез встречается редко среди женщин моложе 40 лет, независимо от того, принимают они гормональные противозачаточные средства или нет, и увеличивается с возрастом. Прием таблеток может расцениваться как один из многих факторов риска. Тем не менее, женщина должна быть поставлена в известность о возможности риска развития рака молочных желез, исходя из оценки соотношения пользы и риска (защита от рака яичника и эндометрия).
Имеются немногочисленные сообщения о развитии доброкачественной или злокачественной опухоли печени у женщин, длительно принимающих гормональные противозачаточные средства. Это следует иметь в виду при дифференциально- диагностической оценке болей в животе, которые могут быть связаны с увеличением размера печени или внутрибрюшным кровотечением.
Следует предупредить женщину, что препарат не предохраняет от ВИЧ-инфекции (СПИД) и других заболеваний, передающихся половым путем.
Эффективность препарата может снизиться при следующих случаях:
пропущенные таблетки, рвота и диарея, одновременное применение других препаратов, снижающих эффективность противозачаточных таблеток.
Если пациентка одновременно принимает другой препарат, который может снижать эффективность противозачаточных таблеток, следует применять дополнительные методы контрацепции.
Эффективность препарата может снижаться, если после нескольких месяцев их применения появляются нерегулярные, мажущие или прорывные кровотечения, в таких случаях целесообразно продолжить прием таблеток до их окончания в следующей упаковке. Если в конце второго цикла менструальноподобное кровотечение не начинается или ациклические кровянистые выделения не прекращаются, прекратить прием таблеток и возобновлять его только после исключения беременности.
Хлоазмы
Хлоазмы временами могут встречаться у тех женщин, у которых они имели место в анамнезе во время беременности. Тем женщинам, у которых имеется риск появления хлоазм, надо избегать контакта с солнечными лучами или ультрафиолетом во время приема таблеток.
Изменения лабораторных показателей
Под действием пероральных противозачаточных таблеток — в связи с эстрогенным компонентом — может изменяться уровень некоторых лабораторных параметров (функциональные показатели печени, почек, надпочечников, щитовидной железы, показатели гемостаза, уровни липопротеинов и транспортных протеинов).
После острого вирусного гепатита следует принимать после нормализации функции печени (не ранее чем через 6 мес). При диарее или кишечных расстройствах, рвоте контрацептивный эффект может снизиться (не прекращая приема препарата, необходимо использовать дополнительные негормональные методы контрацепции). Курящие женщины имеют повышенный риск развития сосудистых заболеваний с серьезными последствиями (инфаркт миокарда, инсульт). Риск зависит от возраста (особенно у женщин старше 35 лет) и от количества выкуриваемых сигарет. В период лактации может уменьшиться выделение молока, в незначительных количествах компоненты препарата выделяются с грудным молоком.
Влияние препарата на способность управлять автомобилем и рабочими механизмами
Исследований по изучению возможного влияния препарата на способность управлять автомобилем или другими механизмами не проводились.
Таблетки, покрытые пленочной оболочкой. 21 таблетка в блистере (Аl/ПВХ/ПВДХ). 1 или 3 блистера в картонной пачке с инструкцией по применению.
Хранить при температуре 15-30 °С.
Хранить в недоступном для детей месте.
3 года.
Не использовать по истечении срока годности.
Условия отпуска из аптек
По рецепту.
Название и адрес изготовителя
ОАО «Гедеон Рихтер», Венгрия
1103 Будапешт, ул. Дъемреи, 19-21, Венгрия
Претензии потребителей отправлять по адресу Московского Представительства
123242, Москва, ул. Красная Пресня, 1-7.
Мавенклад — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП-006137
Торговое наименование:
МАВЕНКЛАД®
Международное непатентованное наименование:
кладрибин
Лекарственная форма:
таблетки
Состав
1 таблетка содержит:
действующее вещество: кладрибин 10,00 мг;
вспомогательные вещества: гидроксипропилбетадекс 143,76 мг, сорбитол 64,04 мг, магния стеарат 2,20 мг.
Описание
Круглые двояковыпуклые таблетки белого цвета, с гравировкой «С» на одной стороне и «10» на другой стороне.
Фармакотерапевтическая группа:
иммунодепрессанты, селективные иммунодепрессанты.
Код ATX:
L04AA40
Фармакологические свойства
Механизм действия
Кладрибин (2-хлоро-2′-дезоксиаденозин) является нуклеозидным аналогом 2′-дезоксиаденозина. За счет наличия хлора в пуриновом кольце, кладрибин обладает резистентностью к действию аденозиндезаминазы, что увеличивает время нахождения пролекарства кладрибин в клетке.
Последующее фосфорилирование кладрибина в его активную трифосфатную форму, 2-хлордезоксиаденозинтрифосфат (Cd-ATP), преимущественно происходит в лимфоцитах, так как для них характерен постоянный высокий уровень дезоксицитидинкиназы (DCK) и относительно низкий уровень 5′-нуклеотидазы (5′-NTase). Высокое соотношение DCK и 5′-NTase способствует накоплению Cd-ATP в лимфоцитах, что приводит к гибели клеток.
В результате более низкого соотношения DCK и 5′-NTase другие клетки, развивающиеся из костною мозга, меньше подвержены воздействию кладрибина, чем лимфоциты.
DCK представляет собой фермент, ограничивающий скорость превращения пролекарства кладрибин в его активную трифосфатную форму, что приводит к селективному уменьшению делящихся и неделящихся Т и В клеток.
Первичный апоптоз-индуцирующий механизм действия Cd-ATP оказывает прямое и непрямое действие на синтез ДНК и функцию митохондрий. В делящихся клетках Cd-ATP препятствует синтезу ДНК путем ингибирования рибонуклеотидредуктазы и избирательной конкуренции с дезоксиаденозинтрифосфатом за включение в ДНК посредством ДНК-полимераз. В покоящихся клетках кладрибин вызывает одноцепочечные разрывы ДНК, быстрое потребление никотинамидадениндинуклеотида, истощение АТФ и гибель клеток. Имеются данные о том, что кладрибин также может вызывать прямой каспаз-зависимый и -независимый апоптоз посредством высвобождения цитохрома С и апоптоз-индуцирующего фактора в цитозоль неделящихся клеток.
Патогенез рассеянного склероза (PC) включает сложный каскад событий, в котором ключевую роль играют различные типы иммунных клеток, включая аутореактивные Т и В клетки. Механизм, с помощью которого кладрибин оказывает свои терапевтические эффекты при рассеянном склерозе, полностью не выяснен, однако считается, что его преимущественное воздействие на Т и В лимфоциты прерывает каскад событий в иммунной системе, имеющих центральное значение в развитии рассеянного склероза.
Различия в уровне экспрессии DCK и 5′-NTases между подтипами иммунных клеток могут объяснять различия в чувствительности иммунных клеток к кладрибину. Из-за этих различий клетки врожденной иммунной системы в меньшей степени подвержены воздействию кладрибина, чем клетки адаптивной иммунной системы.
Фармакодинамика
Кладрибин оказывает длительные эффекты, преимущественно направленные на лимфоциты и аутоиммунные процессы, участвующие в патогенезе рассеянного склероза.
В клинических исследованиях наибольшая частота лимфопении 3 или 4 степени тяжести (от 0,5×109/л до 0,2×109/л или менее 0,2×109/л) наблюдалась у пациентов через 2 месяца после приема первой дозы кладрибина в течение каждого года терапии, что указывало на разрыв во времени между концентрацией кладрибина в плазме крови и максимальным гематологическим эффектом.
Данные клинических исследований показывают, что при назначении препарата в рекомендуемой суммарной дозе 3,5 мг/кг массы тела постепенное возвращение показателей медианы числа лимфоцитов к нормальным значениям происходит на 84-й неделе после приема первой дозы кладрибина (примерно через 30 недель после приема последней дозы кладрибина). Более чем у 75 % пациентов число лимфоцитов возвратилось к норме к 144-й неделе после приема первой дозы кладрибина (примерно через 90 недель после приема последней дозы кладрибина).
Терапия кладрибином в таблетках приводит к быстрому сокращению числа циркулирующих CD4+ и CD8+ Т-клеток. CD8+ Т-клетки показывают менее выраженное снижение и более быстрое восстановление, чем CD4+ Т-клетки, что приводит к временному снижению соотношения CD4/CD8. Кладрибин уменьшает число CD19+ В-клеток и CD16+/CD56+ естественных клеток-киллеров, которые также восстанавливаются быстрее, чем CD4+ Т-клетки.
Эффективность у пациентов с высокой активностью заболевания
Был проведен апостериорный анализ эффективности в подгруппах пациентов с высокой активностью заболевания, получавших кладрибин перорально в рекомендуемой дозе 3,5 мг/кг. Подгруппа пациентов включала:
- пациенты с 1 обострением в течение предшествующего года и по крайней мере 1 TlGd+ очаг или 9 или более Т2 очагов на фоне проводимой терапии другими ПИТРС;
- пациенты с 2 или более обострениями в течение предшествующего года, независимо от того, проводилась терапия ПИТРС или нет.
Фармакокинетика
Кладрибин является пролекарством и для его активации требуется внутриклеточное фосфорилирование. Фармакокинетические показатели кладрибина изучались при внутривенном и пероральном введении пациентам с рассеянным склерозом и пациентам с онкологическими заболеваниями, а также в исследованиях in vitro.
Абсорбция
После перорального введения кладрибин быстро всасывается. После приема внутрь 10 мг кладрибина средняя максимальная концентрация (Сmax) в плазме крови находится в диапазоне от 22 нг/мл до 29 нг/мл, а соответствующая площадь под кривой «концентрация-время» (AUC) составляет от 80 до 101 нг ч/мл (среднее арифметическое из различных исследований). При приеме натощак среднее время достижения максимальной концентрации (Тmax) кладрибина в плазме крови составляет около 0,5 часа (в диапазоне от 0,5 ч до 1,5 ч). При одновременном приеме с высококалорийной пищей абсорбция кладрибина замедляется: среднее Тmax составляет 1,5 часа (в диапазоне от 1 ч до 3 ч), а Сmax снижается на 29 % (основываясь на среднем геометрическом значении), при этом AUC не изменяется. Биодоступность кладрибина после перорального введения в дозе 10 мг составляет около 40 %.
Распределение
Объем распределения препарата большой, что указывает на его экстенсивное распределение в тканях и на внутриклеточное поглощение. В среднем объем распределения кладрибина составляет от 480 л до 490 л. Связь кладрибина с белками плазмы крови составляет 20 % и не зависит от концентрации препарата.
Прохождению кладрибина через биологические мембраны способствуют различные транспортные белки, в том числе ENT1, CNT3 и BCRP.
В исследованиях in vitro кладрибин лишь минимально связан с P-gp (Р-гликопротеин). Клинически значимое взаимодействие с ингибиторами P-gp маловероятно. Возможные последствия влияния индукции P-gp на биодоступность кладрибина формально не изучались.
В исследованиях in vitro показано незначительное опосредованное транспортными белками поглощение кладрибина гепатоцитами.
Кладрибин обладает способностью проникать через гематоэнцефалический барьер. Небольшое исследование у онкологических пациентов показало, что отношение концентрации кладрибина в цереброспинальной жидкости к концентрации его в плазме составляет 0,25.
Кладрибин и/или его фосфорилированные метаболиты главным образом накапливаются и удерживаются в лимфоцитах. In vitro отношение внеклеточной концентрации к внутриклеточной концентрации через 1 час после воздействия кладрибина составляло примерно 30/40.
Биотрансформация
Метаболизм кладрибина изучали у пациентов с рассеянным склерозом после однократного перорального введения дозы 10 мг и однократного внутривенного введения дозы 3 мг. Основным компонентом, присутствующим в плазме и в моче, являлся неизмененный кладрибин как после перорального, так и после внутривенного введения. Метаболит 2-хлороаденин был также обнаружен в плазме и в моче, в количестве ≤3 % от неизмененного кладрибина после перорального введения. Другие метаболиты определялись в плазме и в моче в следовых количествах.
В клетках печени в условиях in vitro наблюдался незначительный метаболизм кладрибина (90 % кладрибина остается в неизмененном виде).
Кладрибин не является релевантным субстратом для ферментов цитохрома Р450 и потенциальным ингибитором CYP1A2, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4. Предполагается, что ингибирование этих ферментов или генетические полиморфизмы (например, CYP2D6, CYP2C9 или CYP2C19) не окажут клинически значимого влияния на фармакокинетику кладрибина или его воздействие. Кладрибин не оказывает клинически значимого индуктивного воздействия на ферменты CYP1A2, CYP2B6 и CYP3A4.
После проникновения в клетку при участии дезоксицитидинкиназы (DCK) происходит фосфорилирование кладрибина с образованием кладрибин-5′-монофосфата (Cd-AMP) (и также при участии дезоксигуанозинкиназы в митохондриях). В дальнейшем Cd-AMP фосфорилируется до дифосфата кладрибина (Cd-ADP) и трифосфата кладрибина (Cd-ATP). Дефосфорилирование и дезактивация Cd-AMP катализируются цитоплазматической 5′-нуклеотидазой (5′-Ntase). В исследовании внутриклеточной фармакокинетики Cd-AMP и Cd-ATP у пациентов с хроническим миелоидным лейкозом уровни Cd-ATP составляли примерно половину от уровня Cd-AMP. Внутриклеточный период полувыведения Cd-ATP составляет 10 ч, Cd-AMP – 15 ч.
Элиминация
Основываясь на объединенных популяционных фармакокинетических данных различных исследований, медианные значения элиминации составили 22,2 л/ч для почечного клиренса и 23,4 л/ч для метаболического (внепочечного) клиренса. Почечный клиренс превышал скорость клубочковой фильтрации, что указывает на активное выделение кладрибина почками. Метаболический клиренс кладрибина (примерно 50 %) включает в себя незначительный процесс метаболических изменений в печени и экстенсивное обширное внутриклеточное распределение, улавливание активного трифосфата кладрибина (Cd-ATP) во внутриклеточное пространство (т.е. в лимфоциты) и последующее выведение внутриклеточного Cd-ATP в соответствии с жизненным циклом этих клеток.
Период полувыведения кладрибина (Т1/2) – около 24 часов.
Дозо-временная зависимость
После перорального введения кладрибина в диапазоне доз от 3 мг до 20 мг Сmax и AUC увеличивались пропорционально дозе, следовательно, на абсорбцию препарата не влияют процессы с ограничением по скорости или накоплению для доз до 20 мг.
Не обнаружено значительного увеличения концентрации кладрибина в плазме крови после повторного введения. Нет данных, что фармакокинетика кладрибина после повторного введения может изменяться в зависимости от времени.
Фармакокинетика у особых групп пациентов
Не проводилось клинических исследований для оценки фармакокинетики кладрибина у пациентов с рассеянным склерозом пожилого возраста или педиатрического возраста, или у пациентов с почечной или печеночной недостаточностью.
На основе модели популяционной фармакокинетики статистически значимого влияния возраста (от 18 до 65 лет) или пола на фармакокинетику кладрибина не обнаружено.
Пациенты с почечной недостаточностью.
Почечный клиренс кладрибина зависит от клиренса креатинина (КК). Основываясь на популяционном фармакокинетическом анализе пациентов с нормальной функцией почек и с легкой почечной недостаточностью, ожидается, что общий клиренс у пациентов с легкой почечной недостаточностью (КК = 60 мл/мин) будет умеренно снижаться, приводя к увеличению экспозиции на 25 %. У пациентов со средней степенью почечной недостаточности (КК = 40 мл/мин) предполагаемое уменьшение клиренса кладрибина составляет 30 % и у пациентов с тяжелой степенью почечной недостаточности (КК = 20 мл/мин) – 40 %.
Пациенты с печеночной недостаточностью.
Роль печени в процессе выведения кладрибина незначительна.
Фармакокинетические взаимодействия.
Исследование взаимодействия лекарственных средств у пациентов с рассеянным склерозом показало, что биодоступность перорально введенного кладрибина в дозе 10 мг не изменялась при совместном применении с пантопразолом.
Показания к применению
Препарат МАВЕНКЛАД® показан для лечения взрослых пациентов с высокоактивным рецидивирующим рассеянным склерозом, подтвержденным данными клинических или радиологических исследований (см. раздел «Фармакодинамика»).
Противопоказания
- повышенная чувствительность к кладрибину или другим компонентам препарата;
- обострение хронической инфекции (туберкулез, гепатит);
- ВИЧ-инфекция;
- начало терапии кладрибином у иммунокомпрометированных пациентов, в том числе пациентов, получающих иммуносупрессивную или миелосупрессивную терапию (см. раздел «Взаимодействие с другими лекарственными средствами»);
- средняя и тяжелая степень почечной недостаточности (клиренс креатинина <60 мл/мин) (см. раздел «Особые указания»);
- средняя и тяжелая степень печеночной недостаточности;
- непереносимость фруктозы;
- совместное применение с интерфероном бета;
- вакцинация живыми, в том числе аттенуированными вакцинами;
- беременность, период грудного вскармливания;
- детский возраст до 18 лет (недостаточно клинических данных).
С осторожностью
У пациентов пожилого возраста, старше 65 лет, из-за недостаточности клинических данных и с учетом большей вероятности недостаточности почек или печени, сопутствующих заболеваний и других применяемых препаратов.
Следует соблюдать осторожность при комбинированной терапии с препаратами, обладающими гематотоксическими свойствами, индукторами транспортных белков BCRP и Р-гликопротеина.
Применение при беременности и в период грудного вскармливания
Контрацепция у мужчин и женщин
Перед началом терапии во время 1-го и 2-го года лечения препаратом МАВЕНКЛАД® пациенты мужского и женского пола, обладающие детородным потенциалом, должны быть предупреждены о возможном серьезном риске для плода и необходимости использовать эффективные методы контрацепции.
Женщинам с детородным потенциалом необходимо пройти тест на беременность до начала лечения препаратом МАВЕНКЛАД® на первом и втором году терапии и использовать эффективные методы контрацепции во время приема препарата и как минимум 6 месяцев после приема последней дозы.
Женщины, использующие системные гормональные противозачаточные средства, должны добавить барьерный метод контрацепции во время терапии препаратом МАВЕНКЛАД® и в течение как минимум 4 недель после последней дозы во время 1-го и 2-го года лечения.
Женщины, которые забеременели во время терапии, должны прекратить лечение препаратом МАВЕНКЛАД®.
Поскольку кладрибин угнетает синтез ДНК, можно ожидать неблагоприятные воздействия на гаметогенез человека. Поэтому пациенты мужского пола должны использовать эффективные методы контрацепции для предупреждения беременности у своих партнерш во время терапии препаратом МАВЕНКЛАД® и в течение как минимум 6 месяцев после приема последней дозы.
Беременность
Кладрибин ингибирует синтез ДНК, что может приводить к врожденным порокам развития при применении во время беременности.
Исследования на животных показали токсичность препарата МАВЕНКЛАД® в отношении репродуктивной системы.
МАВЕНКЛАД® противопоказан беременным женщинам (см. раздел «Противопоказания»), В случае наступления беременности в период лечения препарат должен быть отменен.
Период грудного вскармливания
Данные о проникновении кладрибина в грудное молоко человека отсутствуют. С учетом потенциальных нежелательных эффектов препарата рекомендуется прекращение грудного вскармливания во время терапии и в течение одной недели после приема последней дозы препарата МАВЕНКЛАД®.
Фертильность
Эффекты кладрибина на фертильность у пациентов мужского пола неизвестны.
В исследованиях на животных нарушения тестикулярной функции наблюдались у мышей и обезьян. Влияния кладрибина на фертильность или репродуктивную функцию у мышей не обнаружено.
Способ применения и дозы
Способ применения
Таблетки принимают внутрь, независимо от приема пищи, не разжевывая и запивая водой.
Поскольку таблетки не покрыты оболочкой, их необходимо проглатывать сразу же после освобождения из блистера, не оставлять на поверхности и не держать в руках дольше, чем это необходимо. В случае если таблетка была оставлена на поверхности или если она разломалась в процессе высвобождения из блистера, поверхность необходимо тщательно вымыть.
При обращении с препаратом руки должны быть сухими. После применения препарата необходимо тщательно вымыть руки.
Рекомендуемая доза
Рекомендуемая суммарная доза препарата МАВЕНКЛАД® составляет 3,5 мг/кг массы тела пациента в течение 2 лет: 1,75 мг/кг на 1 курс лечения в год. Годовой курс терапии состоит из 2 недель лечения: одна неделя в начале 1-го месяца и одна неделя в начале 2-го месяца соответствующего года лечения. Каждая неделя лечения состоит из 4 или 5 дней, в течение которых препарат принимают 1 раз в день в дозе 10 мг или 20 мг (одна или две таблетки) в зависимости от массы тела пациента.
Расчёт дозы и количества препарата в зависимости от массы тела пациента представлены ниже в таблицах 1 и 2.
После завершения 2 годовых курсов лечения дальнейший прием препарата в течение 3-го и 4-го года не требуется.
Возобновление лечения после 4-х лет не изучалось.
Критерии начета и продолжения лечения
Число лимфоцитов должно быть:
— в норме перед началом 1-го года лечения препаратом МАВЕНКЛАД®;
— ≥0,8×109/л перед началом 2-го года лечения препаратом МАВЕНКЛАД®.
При необходимости 2-й годовой курс лечения может быть отложен на срок до 6 месяцев до восстановления приемлемого числа лимфоцитов. В случае если период восстановления числа лимфоцитов занимает более 6 месяцев, прием препарата МАВЕНКЛАД® должен быть прекращен.
Расчет дозы
Расчет дозы в течение двух лет терапии проводится лечащим врачом на основании массы тела пациента в соответствии с Таблицей 1. Для некоторых диапазонов массы тела число таблеток может варьировать от одной недели лечения к другой. Пероральное применение кладрибина у пациентов массой тела менее 40 кг не исследовалось.
Таблица 1. Доза препарата МАВЕНКЛАД® на неделю лечения в зависимости от массы тела пациента для каждого года терапии.
| Масса тела пациента, кг | Доза в мг (число таблеток) на неделю лечения | |
| 1-я неделя лечения | 2-я неделя лечения | |
| более или равно 40, но менее 50 | 40 мг (4 таблетки) | 40 мг (4 таблетки) |
| более или равно 50, но менее 60 | 50 мг (5 таблеток) | 50 мг (5 таблеток) |
| более или равно 60, но менее 70 | 60 мг (6 таблеток) | 60 мг (6 таблеток) |
| более или равно 70, но менее 80 | 70 мг (7 таблеток) | 70 мг (7 таблеток) |
| более или равно 80, но менее 90 | 80 мг (8 таблеток) | 70 мг (7 таблеток) |
| более или равно 90, но менее 100 | 90 мг (9 таблеток) | 80 мг (8 таблеток) |
| более или равно 100, но менее 110 | 100 мг (10 таблеток) | 90 мг (9 таблеток) |
| более или равно 110 | 100 мг (10 таблеток) | 100 мг (10 таблеток) |
Таблица 2 показывает распределение общего числа таблеток по дням в течение недельного курса терапии. Интервал между приемом таблеток должен составлять 24 часа. Прием препарата должен осуществляться в одно и то же время суток в течение каждой недели терапии. Если суточная доза составляет 2 таблетки, таблетки принимают вместе как одну дозу.
Таблица 2. Распределение общего числа таблеток препарата МАВЕНКЛАД® в дозе 10 мг по дням в течение недельного курса терапии.
| Общее число таблеток в неделю | 1-й день | 2-й день | 3-й день | 4-й день | 5-й день |
| 4 | 1 | 1 | 1 | 1 | 0 |
| 5 | 1 | 1 | 1 | 1 | 1 |
| 6 | 2 | 1 | 1 | 1 | 1 |
| 7 | 2 | 2 | 1 | 1 | 1 |
| 8 | 2 | 2 | 2 | 1 | 1 |
| 9 | 2 | 2 | 2 | 2 | 1 |
| 10 | 2 | 2 | 2 | 2 | 2 |
Пропущенную дозу препарата (1 или 2 таблетки) следует принять, как только вы об этом вспомнили, в тот же день в соответствии с графиком лечения.
Пропущенная доза не должна приниматься вместе с последующей запланированной дозой на следующий день. В случае пропуска дозы пациент должен принять пропущенную дозу на следующий день, продлив, таким образом, курс приема препарата на сутки. Если пропущены две последовательные дозы, применяется то же правило, и число дней недельного курса лечения увеличивается на два дня.
Особые группы пациентов
Пациенты с почечной недостаточностью.
Клинические исследования по применению препарата МАВЕНКЛАД® у пациентов с почечной недостаточностью не проводились.
У пациентов с легкой степенью почечной недостаточности (клиренс креатинина от 60 до 89 мл/мин) коррекция дозы препарата не требуется.
Препарат МАВЕНКЛАД® противопоказан пациентам со средней и тяжелой степенью почечной недостаточности, так как безопасность и эффективность применения препарата у данной группы пациентов не установлены (см. раздел «Противопоказания»).
Пациенты с печеночной недостаточностью.
Клинических исследований по применению препарата у пациентов с печеночной недостаточностью не проводились.
Несмотря на то, что роль печени в процессе выведения кладрибина незначительна, применение препарата МАВЕНКЛАД® у пациентов со средней и тяжелой степенью печеночной недостаточности (индекс Чайлд-Пью >6) противопоказано, так как данные отсутствуют (см. раздел «Противопоказания»).
Пациенты пожилого возраста (старше 65 лет).
Клинические исследования по применению кладрибина в таблетках не включали пациентов старше 65 лет, поэтому неизвестно, есть ли у них отличие в ответе на терапию по сравнению с более молодыми пациентами (см. раздел «С осторожностью»).
Детский и подростковый возраст.
Безопасность и эффективность препарата МАВЕНКЛАД® у пациентов с рассеянным склерозом в возрасте до 18 лет не установлена, поэтому прием препарата в этой группе пациентов противопоказан (см. раздел «Противопоказания»).
Инструкция по использованию специальной упаковки препарата МАВЕНКЛАД®
- Вымойте и насухо вытрите руки, приготовьте стакан питьевой воды.
- Возьмите упаковку препарата в руку и поверните к себе той стороной, где напечатана инструкция по обращению со специальной упаковкой.
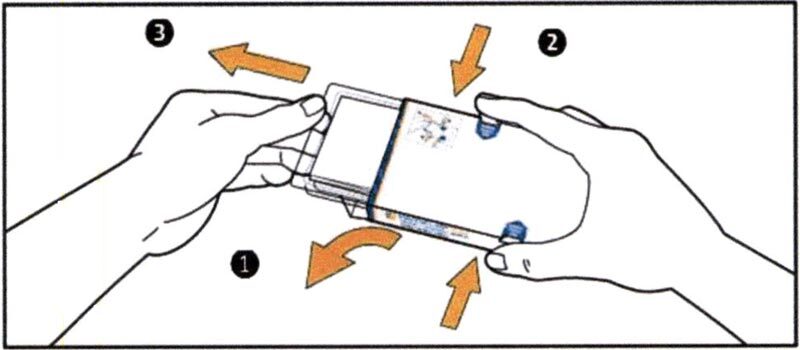
- (1) Откройте клапан картонной пачки с левой стороны.
(2) Одновременно нажмите и удерживайте в нажатом состоянии кнопки, расположенные на боковых поверхностях картонной пачки, указательным и большим пальцами правой руки.
(3) Потяните пластиковый контейнер до упора, но не извлекайте его из пачки. - Возьмите из пластикового контейнера инструкцию по применению. Убедитесь в том, что вы ознакомились со всей информацией, представленной в инструкции, включая инструкцию по обращению со специальной упаковкой. Храните инструкцию в безопасном месте.
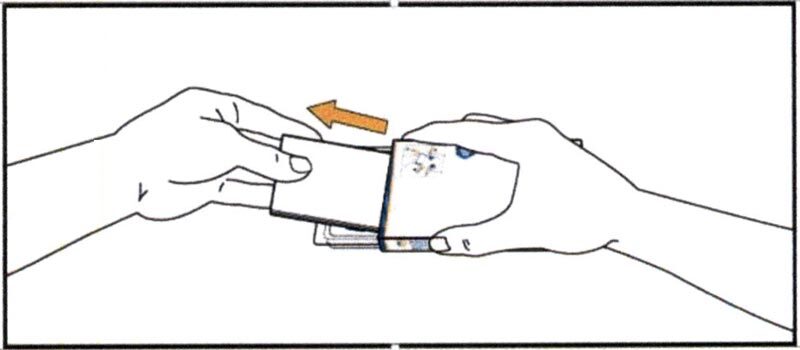
- Приподнимите блистер из пластикового контейнера и выдавите большим пальцем на ладонь 1 или 2 таблетки согласно прописанной схеме лечения.
- Положите таблетку в рот и запейте ее водой. Таблетку необходимо проглотить сразу, не разжевывая и не рассасывая. Необходимо избегать длительного контакта таблетки с кожей рук и касания руками носа, глаз и других частей тела.
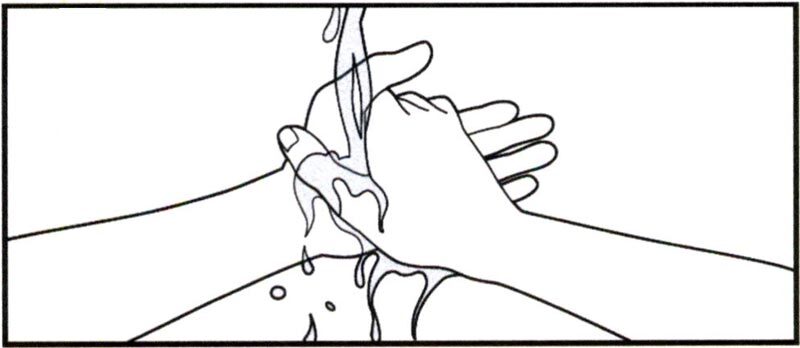
- Тщательно вымойте руки с мылом.
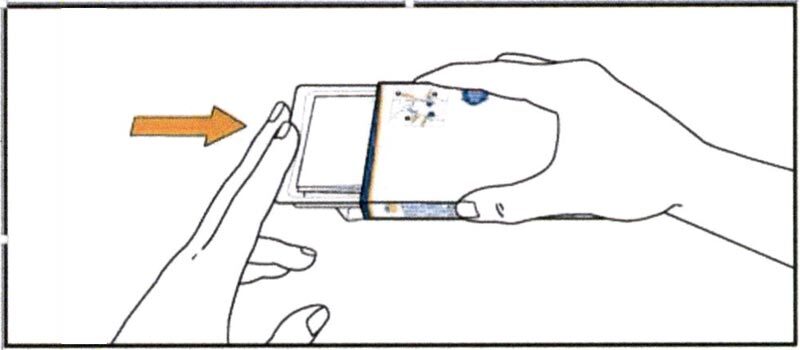
- Верните контейнер с блистером назад в упаковку. Храните препарат в оригинальной упаковке для защиты от влаги.
Храните таблетки МАВЕНКЛАД® в блистере до следующего приема. Не выдавливайте таблетки заранее. Не храните таблетки в другом контейнере.
Побочное действие
Для описания частоты возникновения нежелательных реакций (HP) используется следующая классификация: очень часто (≥1/10), часто (≥1/100 до <1/10), нечасто (≥1/1000 до <1/100), редко (≥1/10000 до <1/1000), очень редко (<1/10000), частота неизвестна (частота не может быть определена на основе имеющихся данных).
Инфекционные и паразитарные заболевания
Часто: опоясывающий лишай, герпес слизистой оболочки полости рта.
Очень редко: туберкулез.
Со стороны крови и лимфатической системы
Очень часто: лимфопения.
Часто: снижение числа нейтрофилов.
Со стороны кожи и подкожных тканей
Часто: кожная сыпь, алопеция.
Описание отдельных нежелательных реакций
Лимфопения
В клинических исследованиях у 20-25 % пациентов, получивших кумулятивную дозу кладрибина 3,5 мг/кг в течение 2 лет в качестве монотерапии, развивалась транзиторная лимфопения 3 или 4 степени тяжести, установленная по результатам лабораторных исследований. Лимфопения 4 степени тяжести наблюдалась у менее 1 % пациентов. Наиболее часто лимфопения 3 или 4 степени тяжести наблюдалась у пациентов через 2 месяца после приема первой дозы кладрибина в рамках 1-го и 2-го годовых курсов терапии (частота лимфопении 3-й степени составила на 1-м и 2-м годах 4,0 % и 11,3 %, соответственно, частота лимфопении 4-й степени на 1-м и 2-м годах составила 0 % и 0,4 %, соответственно). Ожидается, что у большинства пациентов восстановление числа лимфоцитов до нормальных значений или до значения лимфопении 1-й степени происходит в течение девяти месяцев.
Чтобы уменьшить риск развития тяжелой лимфопении, необходимо определять число лимфоцитов до начала терапии кладрибином, во время терапии и после ее окончания (см. раздел «Особые указания»), а также строго соблюдать критерии начала и продолжения лечения кладрибином (см. раздел «Способ применения и дозы»).
Передозировка
Симптомы: имеется ограниченный опыт случаев передозировки препаратом МАВЕНКЛАД®. Известно, что лимфопения вследствие приема препарата МАВЕНКЛАД® является дозозависимой.
Лечение: антидот при передозировке неизвестен. Рекомендуется назначение симптоматической терапии и тщательное наблюдение. Возможно потребуется рассмотреть вопрос о прекращении терапии. Из-за быстрого и экстенсивного внутриклеточного и тканевого распределения маловероятно, что гемодиализ при передозировке кладрибином будет эффективен.
Взаимодействие с другими лекарственными средствами
В состав препарата МАВЕНКЛАД® входит гидроксипропилбетадекс, который может увеличивать растворимость и системную биодоступность слаборастворимых лекарственных средств при совместном приеме. Прием других пероральных препаратов возможен не ранее, чем за 3 часа до или через 3 часа после приема препарата МАВЕНКЛАД®.
Иммунодепрессивные препараты.
Использование препарата у иммунокомпрометированных пациентов, включая пациентов, получающих иммуносупрессивную или миелосупрессивную терапию (например, метотрексат, циклофосфамид, циклоспорин или азатиоприн) или длительное лечение глюкокортикостероидами, противопоказано из-за риска дополнительного влияния на иммунную систему (см. раздел «Противопоказания»).
Проведение краткосрочной терапии глюкокортикостероидами допускается.
Препараты, модифицирующие течение болезни.
Совместное применение кладрибина с интерфероном бета может увеличить риск развития лимфопении. Безопасность и эффективность применения препарата МАВЕНКЛАД® в комбинации с другими препаратами, модифицирующими течение болезни, у пациентов с рассеянным склерозом не установлена. Совместное применение не рекомендовано.
Препараты, обладающие гематотоксическими свойствами.
При применении препарата МАВЕНКЛАД® до или совместно с препаратами, обладающими гематотоксическими свойствами (например, карбамазепин), можно ожидать дополнительные нежелательные эффекты со стороны крови. В таких случаях следует проводить тщательный мониторинг гематологических показателей.
Вакцинация живыми, в том числе аттенуированными вакцинами.
Лечение препаратом МАВЕНКЛАД® не следует начинать в течение 4-6 недель после вакцинации живыми, в том числе аттенуированными вакцинами из-за повышения риска активизации инфекции.
Вакцинация живыми, в том числе аттенуированными вакцинами не должна назначаться как во время лечения препаратом МАВЕНКЛАД®, так и после прекращения приема препарата до тех пор. пока число лейкоцитов в крови не вернется к норме.
Сильнодействующие ингибиторы транспортных белков ENT1, CNT3, BCRP.
На уровне абсорбции кладрибина единственное возможное клинически значимое взаимодействие вероятно с белками резистентности рака молочной железы (BCRP или ABCG2). Ингибирование белков BCRP в желудочно-кишечном тракте может увеличивать биодоступность кладрибина при пероральном приёме и его системное действие.
Известные BCRP ингибиторы (например, элтромбопаг) in vivo могут менять фармакокинетические параметры субстратов транспортных белков на 20 %.
Данные исследований in vitro свидетельствуют о том, что кладрибин является субстратом уравновешивающих переносчиков нуклеозидов (ENT1) и концентрирующих переносчиков нуклеозидов (CNT3) транспортных белков. Следовательно, биодоступность, внутриклеточное распределение и почечная элиминация кладрибина теоретически могут быть изменены под действием сильнодействующих ингибиторов транспортных белков ENT1 и CNT3, таких как дилазеп, нифедипин, нимодипин, цилостазол, сулиндак или резерпин.
Однако их непосредственное влияние на действие кладрибина трудно предсказать. Несмотря на то что клиническое значение таких взаимодействий неизвестно, рекомендуется избегать совместного назначения сильнодействующих ингибиторов транспортных белков (ENT1, CNT3 или BCRP) в течение 4-5 дней терапии кладрибином. В случае если это невозможно, следует рассмотреть выбор альтернативного лекарственного препарата с отсутствием или с минимальным ингибированием транспортных белков ENT1, CNT3 или BCRP. Если и это невозможно, рекомендуется снижение дозы этих лекарственных препаратов до минимальной поддерживающей, раздельный прием препаратов и тщательное наблюдение за пациентами.
Сильнодействующие индукторы транспортных белков BCRP и Р-гликопротеина.
Влияние сильнодействующих индукторов эффлюксных транспортных белков BCRP и Р-гликопротеина на биодоступность и распределение кладрибина не изучалось.
Снижение эффектов кладрибина возможно при совместном применении индукторов транспортных белков BCRP (например, кортикостероидов) или индукторов транспортных белков Р-гликопротеина (например, рифампицина, препаратов зверобоя).
Гормональные контрацептивные средства.
В настоящее время не установлено, влияет ли кладрибин на снижение эффективности системных гормональных контрацептивных средств. В связи с этим женщинам, которые применяют системные гормональные контрацептивные средства, необходимо дополнительно пользоваться барьерными методами контрацепции на фоне терапии кладрибином и в течение как минимум 4 недель после приема последней дозы препарата каждого года лечения кладрибином в таблетках.
Особые указания
Гематологический мониторинг.
Механизм действия кладрибина связан с уменьшением числа лимфоцитов. Снижение числа лимфоцитов является дозозависимым. Уменьшение числа нейтрофилов, эритроцитов, уровня гематокрита, уровня гемоглобина, а также тромбоцитов по сравнению с начальными значениями наблюдалось в ходе клинических исследований, однако данные параметры обычно остаются в норме.
Аддитивные нежелательные гематологические реакции возможны, если кладрибин назначается до или совместно с другими лекарственными средствами, которые влияют на показатели крови (см. раздел «Взаимодействие с другими лекарственными средствами»).
Число лимфоцитов должно определяться:
- перед началом лечения препаратом МАВЕНКЛАД® на первом году терапии;
- перед началом 2-ого года лечения препаратом МАВЕНКЛАД® на втором году терапии;
- через 2 и 6 месяцев после начала лечения на первом и втором годах терапии. Если число лимфоцитов составляет менее 0,5×109/л, то контроль должен проводиться до восстановления числа лимфоцитов.
Для принятия решения о лечении исходя из числа лимфоцитов, смотри раздел «Способ применения и дозы» и подраздел «Инфекционные заболевания».
Инфекционные заболевания.
При приеме кладрибина может ослабляться иммунная защита организма и повышаться вероятность развития или обострения инфекционных заболеваний. До начала терапии препаратом МАВЕНКЛАД® следует исключить ВИЧ-инфекцию, активный туберкулез, активный гепатит (см. раздел «Противопоказания»). Могут активироваться латентные инфекции, в том числе туберкулез и гепатит. Поэтому до начала терапии на первом и втором годах лечения необходимо провести скрининг на латентные инфекции, в особенности на туберкулез и гепатит В и С. Начало терапии препаратом МАВЕНКЛАД® следует отложить до полного выздоровления.
Начало терапии также следует отложить в случае острой инфекции до ее разрешения. Особое внимание следует уделять пациентам, не имеющим в анамнезе указание на перенесенную инфекцию, вызываемую вирусом ветряной оспы (varicella zoster). Таким серонегативным к вирусу ветряной оспы пациентам до начала терапии кладрибином рекомендуется проводить вакцинацию. Начало терапии препаратом МАВЕНКЛАД® следует отложить на 4-6 недель для обеспечения полного эффекта вакцинации.
Увеличение заболеваемости опоясывающим лишаем (Herpes zoster) было отмечено у пациентов, принимающих кладрибин. Если число лимфоцитов не превышает 0,2×109/л, следует назначить профилактическое антигерпетическое лечение на период пока сохраняется лимфопения 4 степени.
Пациентов с числом лимфоцитов ниже 0,5×109/л необходимо тщательно наблюдать на предмет признаков и симптомов инфекции, в особенности опоясывающего лишая. В случае обнаружения симптомов инфекции необходимо начать соответствующую терапию. Лечение препаратом МАВЕНКЛАД® может быть прервано или отложено до полного выздоровления.
Случаи прогрессирующей мультифокальной лейкоэнцефалопатии (ПМЛ) были зарегистрированы у пациентов, получавших кладрибин по поводу волосатоклеточного лейкоза с другим режимом дозирования.
В базе данных клинических исследований кладрибина при рассеянном склерозе (1976 пациентов, 8650 пациенто-лет) не отмечено ни одного случая ПМЛ. Тем не менее перед началом терапии препаратом МАВЕНКЛАД® (обычно в течение предшествующих 3 месяцев) необходимо выполнить магнитно-резонансную томографию (МРТ). Это особенно важно, если пациент уже получал препараты для лечения рассеянного склероза, которые имеют риск развития ПМЛ.
Злокачественные новообразования.
В клинических исследованиях и долгосрочных наблюдениях у пациентов, получавших кумулятивную дозу кладрибина в таблетках 3,5 мг/кг, частота злокачественных новообразований была выше (10 случаев на 3414 пациенто-лет или 0,29 случаев на 100 пациенто-лет), чем у пациентов, получавших плацебо (3 случая на 2022 пациенто-лет или 0,15 случаев на 100 пациенто-лет).
Препарат МАВЕНКЛАД® не рекомендован пациентам с рассеянным склерозом с активными злокачественными новообразованиями. Вопрос о назначении препарата МАВЕНКЛАД® пациентам с указанием на злокачественное образование в анамнезе должен решаться индивидуально с учетом соотношения возможного риска и пользы для пациента. Пациентам, получавшим терапию препаратом МАВЕНКЛАД®, рекомендовано проходить стандартные обследования на выявление злокачественных новообразований.
Контрацепция у мужчин и женщин.
Перед началом терапии во время первого и второго года лечения препаратом МАВЕНКЛАД® пациенты мужского и женского пола, обладающие детородным потенциалом, должны быть предупреждены о возможном серьезном риске для плода и необходимости использовать эффективные методы контрацепции.
У женщин с детородным потенциалом беременность должна быть исключена до начала терапии препаратом МАВЕНКЛАД® на первом и втором годах терапии. Женщинам детородного возраста необходимо использовать эффективные методы контрацепции во время лечения препаратом МАВЕНКЛАД® и как минимум 6 месяцев после приема последней дозы. Мужчины должны использовать эффективные методы контрацепции для предупреждения беременности у своих партнерш во время терапии препаратом МАВЕНКЛАД® и в течение как минимум 6 месяцев после приема последней дозы.
Переливание крови.
Пациентам, которым требуется переливание крови, рекомендуется до переливания крови провести облучение клеточных компонентов с целью предотвращения трансфузионно-обусловленной реакции «трансплантат против хозяина». Рекомендуется консультация специалиста-гематолога.
Смена терапии, переход с других препаратов на кладрибин и с кладрибина на другие препараты.
У пациентов, получавших ранее терапию иммуномодулирующими и иммуносупрессорными препаратами, механизм их действия и продолжительность терапевтического эффекта должны быть рассмотрены до начала терапии препаратом МАВЕНКЛАД®. Возможное аддитивное влияние на иммунную систему должно быть также принято во внимание при приеме таких препаратов пациентами, получавшими препарат МАВЕНКЛАД®.
Пациенты педиатрического возраста.
Безопасность и эффективность препарата МАВЕНКЛАД® у пациентов с рассеянным склерозом педиатрического возраста не установлена. Прием препарата пациентам до 18 лет противопоказан.
Пациенты пожилого возраста.
Клинические исследования по применению кладрибина в таблетках не включали пациентов старше 65 лет, поэтому неизвестно, есть ли у них отличие в ответе на терапию по сравнению с более молодыми пациентами.
Следует соблюдать осторожность при использовании препарата МАВЕНКЛАД® у пациентов пожилого возраста, принимая во внимание большую вероятность почечной или печеночной недостаточности, сопутствующих заболеваний и совместного применения лекарственных препаратов.
Пациенты с почечной недостаточностью.
Клинические исследования по применению препарата МАВЕНКЛАД® у пациентов с почечной недостаточностью не проводились.
У пациентов с легкой степенью почечной недостаточности (клиренс креатинина от 60 до 89 мл/мин) коррекция дозы препарата не требуется.
Препарат МАВЕНКЛАД® противопоказан пациентам со средней и тяжелой степенью почечной недостаточности, так как безопасность и эффективность применения препарата у данной группы пациентов не установлены (см. раздел «Противопоказания»).
Пациенты с печеночной недостаточностью.
Клинических исследований по применению препарата у пациентов с печеночной недостаточностью не проводилось.
Несмотря на то что роль печени в процессе выведения кладрибина незначительна, применение препарата МАВЕНКЛАД® у пациентов со средней и тяжелой степенью печеночной недостаточности (индекс Чайлд-Пью больше 6) противопоказано, так как данные отсутствуют (см. раздел «Противопоказания»).
Непереносимость фруктозы.
Препарат МАВЕНКЛАД® содержит сорбитол в своем составе, поэтому пациентам с непереносимостью фруктозы прием препарата не рекомендован.
Влияние на способность управлять транспортными средствами, механизмами
Препарат МАВЕНКЛАД® не оказывает влияния на способность управлять транспортными средствами и механизмами.
Форма выпуска
Таблетки, 10 мг.
По 1,4, 5, 6, 7 или 8 таблеток в блистере из алюминиевой фольги, 1 блистер в картонном конверте с 8 отверстиями для таблеток. 1 картонный конверт закреплен в пластиковом контейнере. Инструкция по медицинскому применению вложена в пластиковый контейнер. 1 пластиковый контейнер закреплен в картонной пачке с системой «защиты от детей» и контролем первого вскрытия.
Условия хранения
При температуре не выше 25 °С в оригинальной упаковке (пачке картонной).
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не использовать после истечения срока годности.
Условия отпуска
Отпускают по рецепту.
Производитель
Все стадии производства, включая выпускающий контроль качества:
НЕРФАРМА С.Р.Л., Виале Пастер, 10 (Нервиано), 20014 Милан, Италия.
Или в случае упаковки препарата Р-Фарм Джермани ГмбХ, Германия:
Производитель:
Производство готовой лекарственной формы и фасовка (первичная упаковка):
НЕРФАРМА С.Р.Л., Виале Пастер, 10 (Нервиано), 20014 Милан, Италия.
Вторичная (потребительская упаковка) и выпускающий контроль качества:
Р-Фарм Джермани ГмбХ, Хайнрих-Мак-Штрассе, 35, г. Иллертиссен, 89257, Германия.
Владелец регистрационного удостоверения
ООО «Мерк»
Юридический адрес: 1 15054, г. Москва, ул. Валовая, д. 35, Россия
Организация, принимающая претензии потребителей
ООО «Мерк»
115054, г. Москва, ул. Валовая, д. 35
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)