Описание биологически активной добавки Миофертал (порошок растворимый 2 г) основано на официальной инструкции, утверждено компанией-производителем в 2020 году
Дата согласования: 19.06.2020

19.06.2020
Содержание
- Группа
- Нозологическая классификация (МКБ-10)
- Состав
- Характеристика
- Фармакологическое действие
- Рекомендуется
- Противопоказания
- Способ применения и дозы
- Побочные действия
- Форма выпуска
- Производитель
- Условия хранения препарата
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Группа
Нозологическая классификация (МКБ-10)
Состав
| Порошок растворимый | 1 пакетик-стик |
| активные вещества: | |
| мио-инозитол | 1000 мг |
| фолиевая кислота | 200 мкг |
| Содержание мио-инозитола и фолиевой кислоты в пакетике-стике Миофертала не превышает верхний допустимый уровень потребления, разрешенный Российским законодательством1 | |
| 1Единые санитарно-эпидемиологические и гигиенические требования к продукции (товарам), подлежащей санитарно-эпидемиологическому надзору, контролю (с изменениями на 21 мая 2019 года), глава 2, приложение 5 |
Характеристика
БАД к пище.
Фармакологическое действие
Фармакологическое действие
— восполняющее дефицит биологически активных веществ.
Рекомендуется
В качестве дополнительного источника мио-инозитола (инозит, инозитол, витамин В8) и фолиевой кислоты (витамин В9) для пациентов обоего пола; в терапии состояний, обусловленных синдромом поликистозных яичников (для восстановления функции яичников, менструального цикла; для снижения синтеза тестостерона у женщин и устранения клинических проявлений андрогенных нарушений (гирсутизм, жирная кожа, акне, сальность и выпадение волос); для наступления желательной беременности; для повышения качества зрелых ооцитов при подготовке к экстракорпоральному оплодотворению; в комбинированной терапии состояний, обусловленных инсулинорезистентностью, в т.ч. андрогенного ожирения (совместно с коррекцией питания и физической активностью); для профилактики дефекта нервной трубки, других пороков развития плода и осложненного течения беременности в течение 3 месяцев при подготовке к беременности и I триместра беременности.
Противопоказания
Индивидуальная непереносимость компонентов.
Способ применения и дозы
Внутрь,во время или после приема пищи. Содержимое пакетика высыпать в рот и запить водой или содержимое пакетика высыпать в стакан воды комнатной температуры, размешать и выпить приготовленный раствор. Суточная доза может быть разделена на два приема.
Рекомендуется принимать по 1 пакетику-стик в день в любое время дня во время или после приема пищи. Продолжительность приема — 30 дней.
По рекомендации врача, кратность и длительность приема могут быть изменены. В терапии состояний, сопровождающихся повышенной потребностью в мио-инозитоле и фолиевой кислоте, суточная доза обычно не превышает 2–4 г мио-инозитола и 400–800 мкг фолиевой кислоты, что соответствует содержимому 2–4 пакетиков-стик. Продолжительность приема составляет 3–6 месяцев.
Побочные действия
В рекомендуемых дозах не сопровождается побочными эффектами. Редко при суточном приеме мио-инозитола в высоких дозах (содержимое более 12 пакетиков) отмечались незначительные и, как правило, быстро проходящие нежелательные явления со стороны желудочно-кишечного тракта (метеоризм, диарея), тяжесть которых не нарастала с увеличением дозы даже до 30–50 г/сут.
Форма выпуска
Порошок растворимый в пакетике-стик 2 г. В упаковке 30 пакетиков.
Производитель
Компания «СОКИМ Интернешнл С.п.А.», Виа Гизолфа, 86 – 20010 Корнаредо (МИ) Италия.
Тел.: +39/026-2020; факс: +39/026-202040.
По заказу и под контролем: АРГУМЕНТУМ ХОЛДИНГ АГ, зарегистрирована по адресу: Зумпфштрассе 15, 6312 Штайнхаузен, Швейцария.
Организация, уполномоченная принимать претензии от потребителей: ООО «Аргументум», 121471, Москва, Можайское ш., 29, эт. 1-й, пом. VI, комн. 39, оф. 62.
www.argumentum-ag.ru
Условия хранения препарата
В защищенном от прямых солнечных лучей месте, при температуре не выше 25 °C.
Хранить в недоступном для детей месте.
Срок годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Дата обновления: 08.08.2022
Заказ в аптеках Москвы
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в соответствие со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 N 61-ФЗ.
Отзывы
Прочитайте все отзывы и оставьте свой
Мериоферт — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛП-000120
Торговое наименование препарата
Мериоферт
Международное непатентованное наименование
Менотропины
Лекарственная форма
лиофилизат для приготовления раствора для внутримышечного и подкожного введения
Состав
1 флакон с лиофилизатом содержит:
Действующее вещество — высокоочищенный человеческий менопаузальный гонадотропин чМГ (менотропин) 75 ME ФСГ+75 ME ЛГ, 150 ME ФСГ+150 ME ЛГ.
Вспомогательный компонент — лактозы моногидрат 10,00 мг
1 ампула с растворителем содержит: натрия хлорид (апирогенный для инъекций) 9 мг, вода для инъекций до 1 мл.
Описание
Уплотненная масса от белого до светло-желтого цвета.
Растворитель — прозрачная бесцветная жидкость без запаха.
Фармакотерапевтическая группа
Фолликулостимулирующее средство
Код АТХ
G03GA02
Фармакодинамика:
Препарат Мериоферт является препаратом человеческого менопаузального гонадотропина (чМГ), высокой степени очистки. Относится к группе менотропинов. Соотношение биологической активности фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ) составляет 1:1. Препарат получают из мочи женщин в постменопаузе.
Специфические рецепторы к гонадотропинам присутствуют только в тканях половых органов. В яичниках ЛГ связывается с рецепторами на поверхности тека-клеток и желтого тела, а также с гранулезными клетками больших фолликулов.
ФСГ связывается с рецепторами на поверхности гранулезных клеток небольших фолликулов в яичниках и клеток Сертоли в яичках.
У женщин препарат Мериоферт стимулирует рост и созревание фолликулов яичников, повышает концентрацию эстрогенов, стимулирует пролиферацию эндометрия. У мужчин стимулирует сперматогенез при азооспермии и олигоастеноспермии.
Фармакокинетика:
Биологическая эффективность чМГ в основном обусловлена фолликулостимулирующим компонентом. Фармакокинетические свойства чМГ при внутримышечном и подкожном введении имеют высокую индивидуальную вариабельность.
Всасывание
По данным исследований, проведенных для препарата Мериоферт, после однократного подкожного и внутримышечного введения препарата в дозе 300 ME время достижения максимальной концентрации препарата в плазме (Тmax) составляет 22 и 19 часов, соответственно.
Биодоступность препарата при подкожном введении выше, чем при внутримышечном введении.
Выведение
Выводится преимущественно почками. Период полувыведения при однократном введении препарата Мериоферт (300 ME по ФСГ) составляет приблизительно 45 часов при внутримышечном введении и 40 часов при подкожном введении.
Показания:
У женщин:
— Ановуляция (включая синдром поликистозных яичников (СПКЯ) при неэффективности терапии кломифеном).
— Контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении вспомогательных репродуктивных технологий (ВРТ).
У мужчин:
— Стимуляция сперматогенеза при азооспермии и олигоастеноспермии, обусловленными врожденным или приобретенным гипогонадотропным гипогонадизмом (в комбинации с препаратом хорионического гонадотропина человеческого (ХГЧ)).
Противопоказания:
— Повышенная чувствительность к менотропину и другим компонентам препарата.
— Опухоли гипофиза или гипоталамуса.
— Декомпенсированные заболевания щитовидной железы, недостаточность коры надпочечников, гиперпролактинемия.
— Возраст до 18 лет.
У женщин:
Персистирующее увеличение яичников, кисты яичников (не обусловленные синдромом поликистозных яичников).
Аномалии развития половых органов, несовместимые с беременностью.
Фибромиома матки, несовместимая с беременностью.
Кровотечения из влагалища неясной этиологии.
Эстрогензависимые опухоли (рак яичников, рак матки или рак молочной железы).
Первичная яичниковая недостаточность.
Беременность и период грудного вскармливания.
У мужчин:
Рак предстательной железы, опухоль яичек, андрогензависимые опухоли.
Первичная тестикулярная недостаточность.
С осторожностью:
Наличие факторов риска тромбоэмболических осложнений, таких как индивидуальная или семейная предрасположенность, тяжелая степень ожирения (индекс массы тела >30 кг/м2) или тромбофилия, так как в этом случае существует повышенный риск развития венозного или артериального тромбоза и тромбоэмболии в процессе или после применения гонадотропинов. В этом случае польза от лечения гонадотропинами должна превосходить риск от их применения.
Беременность и лактация:
Препарат противопоказан при беременности и кормлении грудью.
Способ применения и дозы:
Препарат Мериоферт вводится внутримышечно или подкожно с периодической сменой места введения. Подкожный способ введения предпочтительнее, так как он обеспечивает наибольшее всасывание лекарственного вещества. Терапию препаратом Мериоферт следует проводить только под контролем врача, имеющего соответствующую специализацию и опыт лечения бесплодия.
Раствор готовится непосредственно перед инъекцией с использованием прилагаемого растворителя. Дозы препарата, описанные ниже, приводятся по ФСГ и являются одинаковыми как для подкожного, так и для внутримышечного способа введения.
У женщин дозу препарата устанавливают индивидуально в зависимости от реакции яичников. Для этого необходим мониторинг ответа яичников на проводимую терапию в виде ультразвукового исследования (УЗИ) в сочетании с определением концентрации эстрадиола в плазме крови.
Ановуляция (включая СПКЯ при неэффективности терапии кломифеном).
Препарат Мериоферт может вводиться ежедневно. Применение препарата следует начинать в течение первых 7 дней менструального цикла. Рекомендуемая начальная доза 75-150 МЕ/сут. При отсутствии достаточной реакции яичников доза постепенно увеличивается. Рекомендуемый интервал для повышения дозы должен составлять не менее 7 дней. Рекомендуемая повышающая доза 37,5 ME, но не более 75 ME. Максимальная суточная доза обычно не превышает 225 ME. Если терапевтический эффект не достигнут в течение 4 недель лечения, инъекции препарата Мериоферт прекращают, а затем начинают новый цикл с более высокой дозы препарата. Пациентке рекомендуется использовать барьерные методы контрацепции или воздержание от половых контактов до наступления менструации.
При достижении адекватного ответа яичников на следующий день после последней инъекции препарата Мериоферт однократно вводят 5000-10000 ME ХГЧ для индукции овуляции. Пациентке рекомендуется иметь половые контакты в день введения ХГЧ и на следующий день после введения. В качестве альтернативного метода возможно проведение внутриматочной инсеминации.
При чрезмерной реакции яичников введение препарата Мериоферт необходимо прекратить и отказаться от введения ХГЧ.
Лечение следует возобновить в следующем цикле в более низкой дозе, чем в предыдущем цикле.
Контролируемая гиперстимуляция яичников с целью индукции роста множественных фолликулов при проведении вспомогательных репродуктивных технологий (ВРТ).
Широко используемый протокол для гиперстимуляции предполагает введение 150-225 ME препарата Мериоферт ежедневно начиная с 2 или 3 дня менструального цикла и продолжающееся, до тех пор, пока не будет достигнуты достаточные размеры фолликулов. Коррекция суточной дозы осуществляется в соответствии с ответом пациента на терапию. Суточная доза препарата не должна превышать 450 ME ФСГ.
Через 24-48 часов после последней инъекции препарата Мериоферт, назначается одна инъекция ХГЧ в дозе 5000 ME-10000 ME для индукции окончательного созревания фолликулов.
Для предотвращения выброса эндогенного ЛГ в настоящее время широко используются агонисты гонадотропин рилизинг гормона (аГнРГ). В этом случае применение препарата
Мериоферт следует начинать приблизительно через две недели после начала лечения агонистами ГнРГ. В дальнейшем оба препарата продолжают применятся совместно до достижения адекватного уровня развития фолликулов. Доза препарата Мериоферт корректируется в соответствии с реакцией яичников пациентки.
При гипогонадотропном гипогонадизме у мужчин для стимуляции сперматогенеза препарат Мериоферт назначается, если предшествующая терапия препаратами ХГЧ вызвала лишь андрогенную реакцию без признаков усиления сперматогенеза. В этом случае лечение продолжается путем введения 2000 ME ХГЧ 2-3 раза в неделю вместе с инъекциями препарата Мериоферт по (75 ME или 150 ME) 2-3 раза в неделю. Лечение по этой схеме следует продолжать минимум в течение 3 месяцев.
При отсутствии положительного эффекта в течение этого времени лечение может быть продолжено до 18 месяцев.
Побочные эффекты:
Нежелательные побочные реакции, наблюдавшиеся при приеме препарата, были в большинстве случаев умеренными и транзиторными.
Наиболее частыми побочными реакциями были: образование кист яичников, реакции в месте инъекции и головная боль (с частотой до 10%). Наиболее серьезными побочными реакциями были СГЯ и осложнения, связанные с этим синдромом.
Основные побочные реакции приведены в таблице ниже:
Неблагоприятные побочные реакции классифицировали следующим образом: очень частые (≥1/10); частые — (от ≥ 1/100 до ≤ 1/10); нечастые — (от ≥ 1/1000 до ≤1/100); редкие — (от ≥ 1/10000 до ≤ 1/1000); очень редкие — (≤ 1/10000).
|
Органы и системы |
Частота |
Побочная реакция |
|
Со стороны желудочно-кишечного тракта |
Часто |
Гастроинтестинальный синдром, включая тошноту, рвоту, диарею, кишечную колику и вздутие живота, боль в животе |
|
Общие расстройства и нарушения в месте введения |
Очень часто |
Боль, покраснение, кровоподтеки, припухлость и/или раздражение в месте инъекции |
|
Со стороны нервной системы |
Очень часто |
Головная боль |
|
Нарушения со стороны половых органов и молочной железы |
Очень часто |
Увеличение яичников и образование кист яичника |
|
Часто |
Синдром гиперстимуляции яичников, гинекомастия (у мужчин) |
|
|
Редко |
Перекрут яичника |
|
|
Со стороны сердечнососудистой системы |
Очень редко |
Тромбоэмболия |
|
Со стороны иммунной системы |
Очень редко |
Системные аллергические реакции, такие как покраснение кожи и кожная сыпь, отек Квинке |
|
Со стороны кожи и подкожной клетчатки (у мужчин) |
Часто |
Акне |
Передозировка:
В случае передозировки возможно развитие СГЯ и тромбоэмболических осложнений. Симптомы СГЯ — увеличение яичников, боли внизу живота, тошнота, рвота, диарея, увеличение массы тела, олигурия, асцит, гидроторакс, гемоперитонеум, гемоконцентрация, одышка (подробная информация представлена в разделе «Особые указания»). Симптомы СГЯ легкой или умеренной степени тяжести обычно не требуют дополнительного лечения и проходят самостоятельно в течение 2-3 недель. При СГЯ тяжелой степени необходима госпитализация в отделения интенсивной терапии специализированных гинекологических стационаров для проведения комплексного лечения.
Взаимодействие:
Фармакодинамическое
Препарат Мериоферт может назначаться отдельно или в комбинации с агонистами или антагонистами гонадотропин рилизинг гормона (ГнРГ)
Совместное применение препарата Мериоферт с другими препаратами, используемыми для стимуляции овуляции (например, ХГЧ, кломифен) может усиливать реакцию фолликулов. При совместном применение с агонистами Г нРГ может потребоваться увеличение дозы менотропина.
Фармацевтическое
Препарат Мериоферт не следует смешивать с другими лекарственными препаратами в одном шприце.
Особые указания:
Лечение должно проводиться под наблюдением врача, имеющего опыт лечения бесплодия.
Перед началом применения препарата Мериоферт рекомендуется проведение обследования для выявления гипотиреоза, недостаточности коры надпочечников, гиперпролактинемии, опухолей гипофиза или гипоталамуса; а также соответствующего специфического лечения.
СГЯ
СГЯ — синдром, отличный от неосложненного увеличения яичников, проявления которого зависят от степени тяжести. Он включает в себя значительное увеличение яичников, высокую концентрацию эстрогенов в сыворотке крови, а также увеличение проницаемости сосудов, что может привести к накоплению жидкости в брюшной, плевральной и, реже, перикардиальной полостях (при СГЯ тяжелой степени). При СГЯ средней тяжести наблюдаются следующие симптомы: боль в животе, вздутие живота, значительное увеличение яичников, увеличение массы тела, одышка, олигурия и желудочно-кишечные симптомы, включая тошноту, рвоту и диарею. При СГЯ тяжелой степени развивается гиповолемия, гемоконцентрация, электролитные нарушения, асцит, гемоперитонеум, гидроторакс, острый респираторный дистресс синдром и тромбоэмболические осложнения.
Чрезмерная реакция яичников на введение гонадотропинов редко приводит к развитию СГЯ, если не вводится ХГЧ с целью стимуляции овуляции. Поэтому в случае гиперстимуляции яичников не следует вводить ХГЧ, а пациентку следует предупредить воздерживаться от половых актов или использовать барьерные методы контрацепции не менее 4 дней. СГЯ может быстро прогрессировать (в течение от 24 часов до нескольких дней), становясь серьезным медицинским осложнением, поэтому пациенты должны наблюдаться, по крайней мере, в течение 2-х недель после введения ХГЧ. Соблюдение рекомендованных доз препарата Мериоферт, режима введения и тщательный контроль терапии может свести к минимуму случаи гиперстимуляции яичников и многоплодной беременности. При проведении ВРТ аспирация содержимого всех фолликулов до наступления овуляции может снизить риск развития СГЯ.
СГЯ может быть более тяжелым и затяжным при развитии беременности. Чаще всего СГЯ развивается после прекращения лечения гонадотропинами и достигает максимума тяжести в течение 7-10 дней после окончания лечения. Обычно СГЯ проходит спонтанно после начала менструации.
При СГЯ средней тяжести и тяжелой степени пациентку госпитализируют и начинают специфическую терапию.
СПЯ встречается с высокой частотой у пациенток с синдромом поликистозных яичников.
Многоплодная беременность.
При многоплодной беременности отмечается повышенный риск неблагоприятных материнских и перинатальных исходов. При применении менотропинов многоплодная беременность развивается чаще, чем при естественном зачатии. В случае проведения экстракорпорального оплодотворения (ЭКО) вероятность возникновения многоплодной беременности зависит от числа введенных эмбрионов, их качества и возраста пациентки. Пациентка должна быть предупреждена о потенциальном риске многоплодной беременности до начала лечения.
Осложнения беременности.
Частота самопроизвольных абортов при беременности, наступившей после лечения препаратом Мериоферт, выше, чем у здоровых женщин.
Эктопическая беременность.
При заболеваниях маточных труб в анамнезе, как при естественном зачатии, так и при лечении бесплодия, у женщин имеется высокий риск возникновения эктопической беременности. Распространенность внематочной беременности после ЭКО от 2 до 5% по сравнению с 1 до 1,5% в общей популяции.
Новообразования органов репродуктивной системы.
Имеются сообщения о новообразованиях яичников и других органов репродуктивной системы, как доброкачественных, так и злокачественных, у женщин, которым проводилось лечение бесплодия с помощью нескольких методик ВРТ. Пока не установлено, увеличивает ли лечение гонадотропинами исходный риск этих опухолей у женщин с бесплодием.
Врожденные пороки
Распространенность врожденных пороков развития плода при использовании ВРТ несколько выше, чем при естественном зачатии. Считается, что это может быть связано с индивидуальными особенностями родителей (возрастом матери, характеристиками спермы) и многоплодной беременностью.
Тромбоэмболические осложнения
Женщины с известными факторами риска развития тромбоэмболических осложнений, таких как индивидуальная или семейная предрасположенность, ожирение (индекс массы тела > 30 кг/м2) или тромбофилия могут иметь повышенный риск венозных или артериальных тромбоэмболических осложнений во время или после лечения гонадотропинами. В таких случаях польза их применения должна превышать риск.
Следует учитывать, что сама беременность также повышает риск развития тромбоэмболических осложнений.
У мужчин с высокой концентрацией ФСГ в крови (что свидетельствует о первичном гипогонадизме) препарат Мериоферт обычно неэффективен.
Влияние на способность управлять транспортными средствами и механизмами:
Препарат Мериоферт не влияет на способность управлять транспортными средствами и механизмами.
Форма выпуска/дозировка:
Лиофилизат для приготовления раствора для внутримышечного и подкожного введения 75 ME ФСГ+75 ME ЛГ, 150 ME ФСГ+150 ME ЛГ в комплекте с растворителем: натрия хлорида раствор для инъекций 0,9%.
Упаковка:
Лиофилизат: по 75 ME ФСГ+75 ME ЛГ, 150 ME ФСГ+150 ME ЛГ во флаконе прозрачного силиконизированного стекла типа I для парентеральных препаратов (Евр.Ф.) с бромбутил-каучуковой пробкой и крышкой (тип флип оф).
Растворитель: по 1 мл в ампуле прозрачного стекла типа I.
Один флакон, содержащий лиофилизат, помещают в пачку картонную вместе с одной ампулой растворителя и инструкцией по применению. Либо 10 индивидуальных картонных пачек, каждая из которых содержит флакон с лиофилизатом, ампулу с растворителем и инструкцию по применению помещают в общую картонную пачку.
Условия хранения:
Хранить при температуре не выше 25 °С в защищенном от света месте.
Восстановленный раствор следует использовать немедленно.
Хранить в недоступном для детей месте.
Срок годности:
Лиофилизат — 2 года.
Растворитель — 5 лет.
Срок годности комплекта устанавливается по компоненту с наименьшим сроком годности.
Не применять по истечении срока годности.
Условия отпуска
По рецепту
Производитель
ИБСА Институт Биокимик С.А., Via al Molino, 6926 Montagnola, Switzerland, Швейцария
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
ИБСА Институт Биокимик С.А.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
В статье рассмотрено влияние микронутриента мио-инозитола на женскую репродуктивную функцию.
Введение
При гормональных формах бесплодия у пациенток отмечаются нарушения менструального цикла, ановуляция, синдром поликистоза яичников (СПКЯ), хроническое воспаление, избыточная масса тела и атерогенный профиль крови. Попытки преодоления бесплодия только на основе использования технологий гормональной стимуляции, без устранения вышеперечисленных фоновых патологий зачастую малорезультативны, а в случае зачатия могут приводить к формированию пороков развития плода. Одной из основополагающих причин коморбидности бесплодия и фоновых патологий является недостаточная обеспеченность микронутриентами (фолаты, мио-инозитол и др.) [1]. Поэтому индивидуально подобранная микронутриентная поддержка является основным инструментом для «тонкой настройки» репродуктивной функции, в т. ч. с целью формирования овуляторных циклов, зрелых ооцитов и профилактики пороков развития плода.
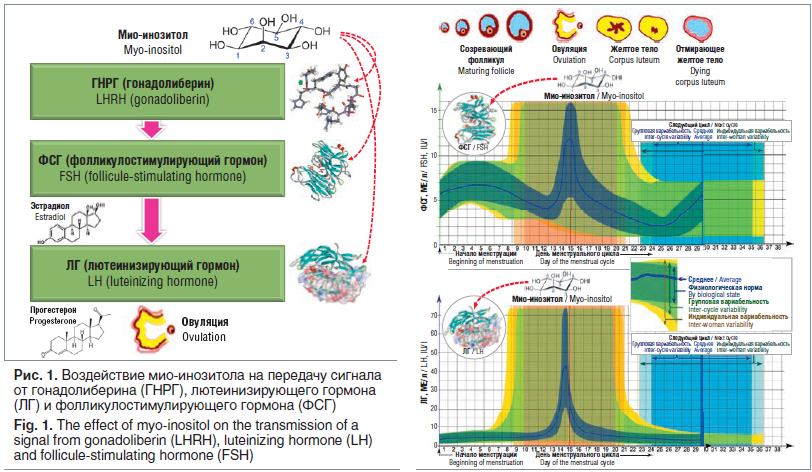
Мио-инозитол — эндогенный метаболит, необходимый для синтеза более 50 инозитолфосфатных производных, участвующих в передаче внутриклеточного сигнала от рецепторов гонадотропин-рилизинг гормона (ГНРГ), фолликулостимулирующего гормона (ФСГ), лютеинизирующего гормона (ЛГ), инсулина и др. [2]. Принципиальным условием синтеза достаточного количества мио-инозитола (2–3 г/сут) является совершенное здоровье почек. Их заболевания (пиелонефрит, гломерулонефрит, диабетическая нефропатия, почечная форма гипертензии и др.) и лекарственная нагрузка на этот орган резко снижают синтез мио-инозитола в почках. Соответственно, при любой патологии почек у пациентки возникает недостаточность мио-инозитола, для коррекции которой необходим прием данного микронутриента, в т. ч. с целью поддержки функционирования репродуктивной системы.
Для принятия врачом осознанного решения о необходимости назначения пациентке мио-инозитола необходимо понимание всего спектра его молекулярно-
физиологических воздействий на репродуктивную сферу. В настоящей работе представлен анализ результатов исследований, в которых изучались эффекты мио-инозитола, проведенный посредством компьютерного анализа массива из 44 тыс. статей в рецензируемых научных журналах, опубликованных к 2018 г., на основе современных методов интеллектуального анализа данных [3].
Анализ показал, что десятки разновидностей рецепторов (например, рецепторы ГНРГ, ФСГ, ЛГ, гистаминовые, ГАМК и т. д.), будучи активированными, задействуют специальные сигнальные белки фосфоинозитолкиназы (в т. ч. PI3K), приводящие к секреции кальция из эндоплазматического ретикулума клетки в цитозоль [2]. Кальций, диацилглицерол, циклический аденозинмонофосфат (цАМФ) и различные фосфат-производные мио-инозитола (фосфатидилинозитол и пр.) являются эссенциальными «вторичными сигналами» (англ. «secondary messenger»), участвующими в регуляции каскадных механизмов, выполняющих биологические роли соответствующих рецепторов.
В нашей предыдущей статье показано, что нарушения обмена мио-инозитола приводят к инсулинорезистентности, ГНРГ/ФСГ/ЛГ-резистентности клеток, нарушениям овуляции, торможению вызревания ооцитов (рис. 1) и ускоряют формирование поликистозных яичников [4]. В настоящей статье мы рассмотрим влияние мио-инозитола на репродукцию, иммунитет, лечение бесплодия, синергизм с фолатами и другими витаминами/минералами и профилактику врожденных пороков развития (ВПР).
Мио-инозитол и репродуктивная функция
Мио-инозитол и его производные необходимы для реализации эффектов гонадотропина, ЛГ и ФСГ — тем самым осуществляется значительное влияние на функционирование репродуктивной системы и фертильность (инвазия трофобласта при закреплении бластоцисты, функции яичников, ооцитов, плаценты). Следует также отметить, что мио-инозитол, воздействуя на соединительную ткань, не только влияет на состояние костей, кожи и ранозаживление, но и имеет принципиальное значение для физиологического развития эмбриона [5].
Как известно, СПКЯ является основной причиной бесплодия вследствие метаболических, гормональных дисфункций яичников. Поликистоз яичников сочетается с инсулинорезистентностью и компенсаторной гиперинсулинемией. Комбинированная терапия СПКЯ с включением мио-инозитола снижает риск нарушений обмена углеводов и жиров у пациенток с избыточной массой тела; положительно влияет на состояние гормональной регуляции и функции яичников [6].
Эффекты мио-инозитола в сочетании с фолиевой кислотой (ФК) были изучены в систематическом анализе 6 рандомизированных контролируемых исследований (РКИ) у женщин с СПКЯ (n=617). Результаты анализа позволяют рекомендовать использование комбинации мио-инозитол (2–4 г/сут) + ФК (200–400 мкг/сут) в течение 8–12 нед. для улучшения функции яичников, а также метаболических и гормональных показателей у пациенток с СПКЯ [7]. Кроме того, прием мио-инозитола способствует улучшению показателей уровней триглицеридов, липопротеинов высокой плотности, холестерина и диастолического артериального давления [8].
Проспективное РКИ показало, что мио-инозитол улучшает функциональное состояние ооцитов у пациенток с СПКЯ, которым проводились циклы интрацитоплазматических инъекций сперматозоидов (ИКСИ). В группе, состоявшей из 70 женщин 18–35 лет, 35 пациенток с ановуляторным циклом получали 200 мкг/сут ФК и 2 г/сут мио-инозитола в течение 24 нед., а другие 35 пациенток — плацебо. После 24 нед. только 5 из 35 получавших мио-инозитол пациенток имели ановуляторный цикл, в то время как в контрольной группе такой цикл отмечался у 14 из 35 пациенток, что соответствовало 4-кратному снижению риска возникновения ановуляторного цикла: отношение шансов (ОШ) 0,25; 95% доверительный интервал (ДИ) 0,08–0,80, р=0,016) [9].
Иммунитет и мио-инозитол
Мио-инозитол необходим для функционирования Т-клеток и В-клеток, NK-лейкоцитов, макрофагов, нейтрофилов, тучных клеток, гранулоцитов, системы комплемента, интерферонов. Например, секреция провоспалительных факторов простагландина Е2 (PGE2) и лейкотриена B4 (LTB4) мононуклеарными клетками периферической крови снижается при добавлении 600 мкмоль/л мио-инозитола в культуру [10]. Мио-инозитол ингибирует киназы Akt и ERK, вовлеченные в онкопролиферативные процессы, приводит к регрессии поражений бронхов при курении. Исследовались 206 биоптатов бронхов от курильщиков с большим стажем курения (n=21, возраст — 40–74 года, индекс курильщика >30 пачка/лет). В результате лечения мио-инозитолом отмечено снижение фосфорилирования Akt (р<0,01) и ERK (р<0,05) [11]. Таким образом, для поддержки укрепления противоопухолевого иммунитета необходим прием мио-инозитола.
Мио-инозитол и функционирование печени и почек
Состояние репродуктивной системы женщины напрямую зависит от эффективности функционирования печени и почек. Мио-инозитол оказывает значительное воздействие на функционирование печени, способствуя реализации биологических эффектов фактора роста гепатоцитов, стимулирует секрецию желчи, профилактирует развитие стеатогепатита и цирроза печени. Мио-инозитол поддерживает функции почечных канальцев, осуществляющих реабсорбцию необходимых организму макро- и микронутриентов из первичной мочи. При диабете отмечается ускоренная элиминация мио-инозитола: его средний уровень в моче у здоровых лиц составляет 5,6 мкг/мл, а у больных с почечной недостаточностью — 29 мкг/мл. Клиренс мио-инозитола у здоровых лиц составляет 2,8 мл/мин (при уровне реабсорбции 97%), а у пациентов с почечной недостаточностью может достигать 17 мл/мин, что свидетельствует о повышении его выведения с мочой [12]. Поэтому женщины с патологией печени и почек, в т. ч. в анамнезе, должны быть информированы о значении мио-инозитола для поддержки соматического и репродуктивного здоровья.
Мио-инозитол и профилактика пороков развития
В настоящее время отмечается рост числа случаев беременности в позднем возрасте, на фоне хронической патологии печени и почек, беременности в результате применения технологий ЭКО/ИКСИ; возрастает нагрузка токсикантами, антибиотиками, эстрогеновыми и другими «антивитаминными» препаратами. Как следствие, создается почва для формирования патологий беременности, ВПР и отклонений развития плода. Профилактика ВПР фолатами не всегда эффективна, т. к. фолаты — не единственный микронутриент, необходимый для физиологического развития плода. Например, нарушения нейруляции связаны с недостатком не только фолатов, но и витаминов А, В6, В12, цинка и мио-инозитола, причем только 70% дефектов нервной трубки (ДНТ) являются фолат-зависимыми [13]. В то же время повторные случаи формирования плодов с ДНТ, несмотря на дотации ФК беременным, указывают на существование фолат-резистентных ДНТ.
Важность применения мио-инозитола для профилактики ДНТ, в особенности фолат-резистентных, обусловлена тем, что производные мио-инозитола принимают комплексное участие в функционировании репродуктивной системы (формировании овуляторных циклов, зрелых ооцитов, эмбриогенезе и развитии плода [14]), применяются для профилактики экстрагенитальной патологии у беременной. Участие мио-инозитола и его производных в обеспечении функционирования рецепторов инсулина, гонадолиберина, ФСГ, ЛГ, факторов роста нервной ткани и др. обеспечивает не только нормальный ход эмбриогенеза и развития плода, но и функционирование сердечно-сосудистой, нервной систем, печени и почек [2]. Особым преимуществом профилактики ВПР мио-инозитолом является его высокий уровень безопасности — даже в дозе 12 г/сут он вызывает легкие побочные эффекты со стороны ЖКТ (тошнота, метеоризм, диарея) у отдельных пациенток [15]. В то же время в реальной клинической практике препараты мио-инозитола принимаются в дозах от 0,5 до 4,0 г/сут.
В экспериментальных и клинических работах показана эффективность приема мио-инозитола для профилактики пороков развития. Так, дотации мио-инозитола позволяют предупреждать ВПР, связанные с инсулинорезистентностью и гипергликемией, характерными для пациенток с избыточной массой тела и СПКЯ. Фосфат-производные мио-инозитола участвуют в процессах передачи сигнала от инсулинового рецептора [2], и поэтому его низкие концентрации в тканях эмбриона на этапе органогенеза могут индуцировать эмбриопатии, связанные с гипергликемией.
В эксперименте на моделях стрептозоцинового диабета у беременных крыс было показано, что содержание миоинозитола в эмбрионах было ниже на 36% по сравнению с таковым в контрольной группе без диабета (p=0,01), ассоциировалось с задержкой развития эмбриона (его длина в основной группе — 3,37±0,04 мм, в контрольной — 3,87±0,03 мм, р=0,01); пониженным числом сомитов (в основной группе — 27,5±0,2, в контрольной — 29,1±0,2, р=0,01) и повышенной частотой патологий нервной системы (в основной группе — 17,6%, в контрольной — 1,9%, р<0,001) [16]. Прием мио-инозитола при стрептозоциновом диабете приводил к значительному снижению частоты развития ДНТ (в основной группе — 9,5%, в контрольной — 20,4%, р<0,05) [17]. Достоверное снижение частоты встречаемости ДНТ наблюдалось при использовании миоинозитола в дозе 0,08 г/кг/сут, в то время как увеличение дозы до 0,16 г/кг/сут и даже до 0,5 г/кг/сут не приводило к существенному улучшению результата профилактики ДНТ [18].
Клинические наблюдения за группами пациенток с гестационным диабетом (ГД) подтверждают результаты экспериментальных исследований. Прием мио-инозитола снижает риск возникновения ГД даже у женщин с семейной историей диабета 2-го типа. Например, в проспективном рандомизированном плацебо-контролируемом исследовании группа пациенток получала 4 г/сут мио-инозитола и 400 мкг/сут ФК, разделенные на 2 приема в сутки (n=110), начиная с конца I триместра. Пациентки в группе плацебо (n=110) получали только 400 мкг/сут ФК. Заболеваемость ГД была значительно ниже при приеме мио-инозитола — 6%, в то время как в контрольной группе — 15,3% (ОШ=0,35, р=0,04). При приеме мио-инозитола также были отмечены статистически значимое снижение частоты макросомии (масса плода >4000 г) и уменьшение средней массы плода в сторону середины интервала нормы [19].
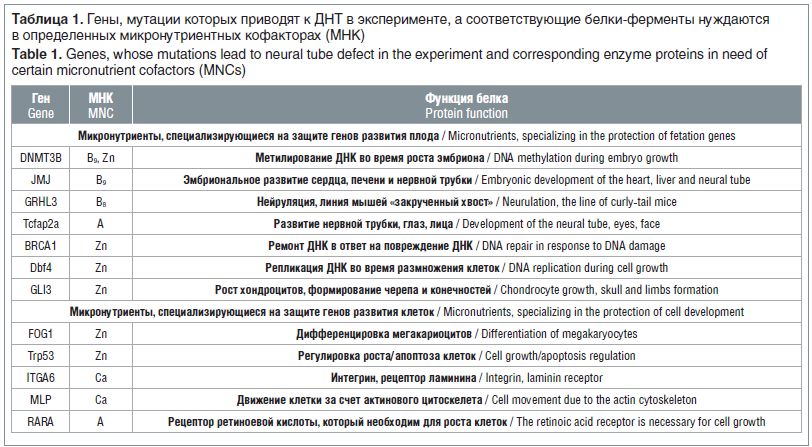
Кроме того, в экспериментальных исследованиях были определены гены, опосредующие взаимосвязь риска ДНТ, дефицитов мио-инозитола и других микронутриентов, а также существование фолат-чувствительных и фолат-резистентных моделей ДНТ [20]. В экспериментах по делеции генов было установлено более 60 генов, инактивация которых приводит к формированию линий мышей с ДНТ. Эти гены встречаются и у человека. Анализ экспериментального материала с использованием метода анализа функциональных взаимосвязей [21, 22] показал, что не менее 19 из 60 генов кодируют белки и ферменты, активность или уровни которых существенно зависят от наличия определенных микронутриентных кофакторов (табл. 1) [23].
К микронутриентам, необходимым для профилактики ДНТ, относятся цинк, мио-инозитол, фолаты, магний, кальций и витамин А. Дефицит каждого из этих микронутриентов имитирует делецию соответствующего гена (т. к. активность соответствующего белка резко снизится при отсутствии кофактора). Первичная профилактика ДНТ ФК, мио-инозитолом, цинком и витамином А была продемонстрирована и в экспериментальных и в клинических исследованиях [24].
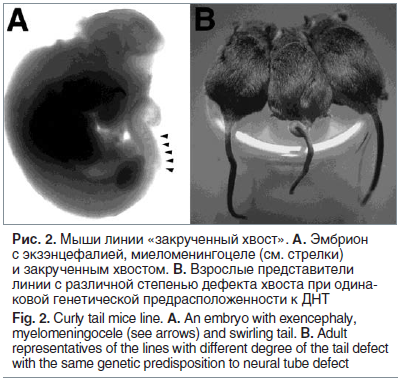
Нарушения нейруляции в линии мышей «закрученный хвост» (англ. curly tail, ген Ct/GRHL3) более, чем другие мутантные линии, напоминают ДНТ, наблюдаемые в акушерской практике. Данная линия (рис. 2) является фолат-резистентной, и эффективная профилактика ДНТ в этой линии может быть достигнута дотациями мио-инозитола [25]. Другими важными микронутриентами для профилактики ДНТ в линии «закрученный хвост» являются ретиноевая кислота, витамины В2, С и D. В то же время профилактика ДНТ посредством фолатов, пиридоксина, витамина В12 или цинка не имела эффекта [26].
В эксперименте было показано, что ФК в сочетании с мио-инозитолом эффективно снижает риск врожденных дефектов через эпигенетические эффекты (метилирование ДНК) и сигнальный путь Wnt/катенин. В частности, сочетание ФК с мио-инозитолом предотвращает нарушение активности каскада Wnt алкоголем и способствует нормальной активации генов во время кардиогенеза. Например, впрыскивание 25% этанола в перепелиные яйца приводило к формированию аномалий сердечных клапанов у 68% эмбрионов, и только у 32% наблюдалось нормальное развитие. Совместное впрыскивание этанола и ФК (10 мкг/мл) приводило к нормальному кардиогенезу у 51% эмбрионов, а совместное применение ФК и миоинозитола — у 62% эмбрионов, что близко к значению в 67% в контрольной группе [27].
Мио-инозитол существенно уменьшает частоту встречаемости ДНТ, даже при отсутствии дотаций фолатов. Эмбриопротекторные эффекты мио-инозитола проявляются в увеличении метаболизма липидов, стимулировании основного сигнального белка протеинкиназы С и повышении экспрессии рецепторов ретиноевой кислоты, таким образом, закрытие задней части нервной трубки происходит без задержки [28].
Молекулярно-биологические исследования позволили очертить круг мио-инозитол-зависимых белков,посредством которых и осуществляется эмбриопротекция мио-инозитолом (протеинкиназа С, рецепторы инозитол-1,4,5-трифосфата, ферменты инозитол-1,3,4-трифосфат-5/6-киназа, инозитол полифосфат-5-фосфатаза,
фосфатидилинозитол-4-фосфат-5-киназа и рецептор тромбоцитарного фактора роста альфа) [23]. Например, рецепторы инозитол-1,4,5-трифосфата обеспечивают эффекты производных мио-инозитола и необходимы для развития пула стволовых клеток сердца в висцеральной мезодерме. Аномальное развитие данного ростка приводит к целому спектру дефектов выносящих сосудов сердца. Делеции генов инозитол-1,4,5-трифосфат рецепторов в эксперименте приводили к выраженной гипоплазии выносящего тракта сердца, правого желудочка и избыточному апоптозу клеток мезодермы [29]. Мутации гена IP3R1, найденные в человеческих популяциях, снижают активность фермента и приводят к врожденной спиноцеребральной атаксии 15-го и 29-го типов (номер по ОМИМ 147265) [30].
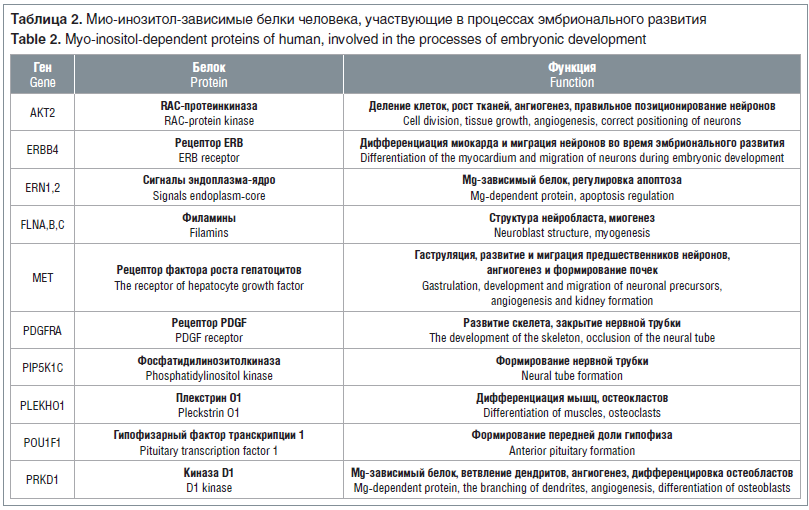
Систематический биоинформационный анализ миоинозитол-зависимых белков человека, участвующих в процессах эмбрионального развития (табл. 2), позволил получить результаты, сопоставимые с результатами систематизированных ранее экспериментальных и молекулярно-биологических исследований [2]. В частности, в результате анализа были установлены обсуждавшиеся ранее гены PIP5K1C (кодирующий фермент фосфатидилинозитол-4-фосфат-5-киназу, необходимый для синтеза внутриклеточной сигнальной молекулы фосфатидилинозитол дифосфата) и PDGFRA (рецептор тромбоцитарного фактора роста альфа, играющего важную роль в эмбриональном развитии, делении и миграции клеток сомита). Кроме того, в результате биоинформационного анализа были выявлены другие перспективные гены для дальнейших экспериментальных и клинических исследований пороков развития (см. табл. 2).
Оценка клинической эффективности мио-инозитола для поддержки репродуктивного здоровья
Наиболее ярко клиническая эффективность миоинозитола для решения проблем репродукции была продемонстрирована у пациенток с СПКЯ. Участие мио-
инозитола в передаче сигнала от рецептора инсулина и осуществлении эффектов основных репродуктивных гормонов обеспечивает более полное вызревание ооцитов [31]. Например, в РКИ при прохождении циклов ИКСИ пациентки со СПКЯ и хроническим ановуляторным бесплодием получали комплекс мио-инозитола 4 г/сут и ФК 400 мкг/сут либо только ФК 400 мкг/сут в течение 3 мес. По сравнению с приемом только ФК сочетанное применение мио-инозитола и ФК обеспечивало достоверное увеличение числа фолликулов диаметром более 15 мм, рост числа активных ооцитов на фоне существенного снижения среднего числа незрелых ооцитов и повышения среднего числа эмбрионов хорошего качества (по шкале S1) [32].
Важно отметить, что добавление мио-инозитола к ФК у пациенток без СПКЯ, проходящих циклы ИКСИ, позволяет уменьшить число используемых зрелых ооцитов и сократить дозировку рекомбинантного ФСГ (рФСГ) без уменьшения числа клинических беременностей. В группе женщин без СПКЯ и с базальным уровнем ФСГ <10 МЕ/мл (n=100, <40 лет) пациентки получали рФСГ (начальная доза — 150 МЕ) в течение 6 дней. За 3 мес. до начала процедур ЭКО группа была рандомизирована на получение 4 г/сут мио-инозитола и 400 мкг/сут ФК (n=50) или только ФК 400 мкг/сут (n=50). Совместное использование мио-инозитола и ФК позволило снизить общее количество гонадотропинов, необходимое для достижения вызревания ооцитов, в среднем на 400 МЕ (р=0,05) [33].
В сравнительном многоцентровом исследовании была оценена эффективность мио-инозитола и ФК для улучшения качества ооцитов/эмбрионов и результатов цикла ЭКО у пациенток без СПКЯ. Пациентки опытной группы (n=133) получали мио-инозитол 1000 мг/сут и ФК 0,1 мг/сут, а пациентки контрольной группы (n=137) — плацебо. Общее количество зрелых ооцитов было значительно выше в группе мио-инозитол + ФК (12; 95% ДИ: 1–37), чем в группе плацебо (всего 8; 95% ДИ: 0–24) (р<0,001) [34].
В другом проспективном РКИ с участием женщин с СПКЯ, проходящих ЭКО, было также показано, что дотации мио-инозитол + ФК приводят к улучшению показателей оплодотворения и улучшению качества эмбрионов. За 2 мес. до ЭКО группа участниц была рандомизирована на группу плацебо (n=15) и группу «мио-инозитол + ФК» (4000 мг/сут мио-инозитола, 400 мкг/сут ФК, n=14). Из 233 ооцитов, отобранных в группе «мио-инозитол + ФК», оплодотворялись 136 (58,4%), тогда как только 128 из 300 отобранных ооцитов (42,7%) оплодотворились в группе плацебо. Продолжительность стимуляции составила 9,7±3,3 дня в группе «мио-инозитол + ФК» и 11,2±1,8 дня — в группе плацебо (р<0,05). Количество используемых единиц гормона рФСГ было ниже в группе «мио-инозитол + ФК» (1750 ед., плацебо — 1850 ед.) [35].
Метаанализ 6 РКИ (n=935) подтвердил, что прием комбинации «мио-инозитол + ФК» за 3 мес. до проведения ИКСИ способствовал повышению частоты клинической беременности у бесплодных женщин, проходящих индукцию овуляции для ИКСИ или трансплантацию эмбриона in vitro. Пациентки контрольной группы принимали только ФК. Дотации комбинации мио-инозитол + ФК были ассоциированы со значительно повышенной частотой клинической беременности (р=0,03), более низкой частотой невынашивания (95% ДИ: 0,08–0,50, p=0,0006). Шансы получения эмбриона 1-й степени были выше (ОШ 1,8; 95% ДИ: 1,10–2,74, p=0,02), а риск формирования вырожденных ооцитов — ниже (ОШ 0,5; 95% ДИ: 0,11–0,86, p=0,02) на фоне дотаций мио-инозитол + ФК. Прием комбинации мио-инозитол + ФК также способствовал снижению суммарной дозы гормона рФСГ, необходимого для стимуляции овуляции (-334 ед., 95% ДИ: -591…-210 ед., p=0,001) [36].
Заключение
Анализ исследований свидетельствует о наличии важных резервов нормализации менструального цикла, восстановления чувствительности яичников к гормонам, поддержки противоопухолевого иммунитета, повышения качества ооцитов, вероятности наступления беременности. Очевидно, что в условиях выраженного полигиповитаминоза [37], повсеместного использования «антивитаминных» препаратов [38] и гипергликемического питания поддержка мио-инозитолом приобретает исключительную важность. Мио-инозитол позволяет не только преодолевать резистентность клеток к инсулину и глюкозе, но и поддерживать ряд сигнальных каскадов (рецепторов ГНРГ, ЛГ, ФСГ и др.), важных для овуляции, вызревания ооцитов, а также обеспечивать профилактику пороков развития (в т. ч. фолат-резистентных). Повысить обеспеченность мио-инозитолом можно, например, посредством приема препарата Миоферт (произведен по технологии GMP, содержит 1000 мг инозита (в виде мио-инозитола) и 200 мкг ФК в 1 пакетике-стике) в виде водного раствора. Для приготовления раствора для питья следует использовать только чистую питьевую воду комнатной температуры, растворение в молоке, соках, киселе недопустимо (т. к. это снизит биодоступность мио-инозитола из препарата).
Работа выполнена при участии гранта РФФИ 15-07-04143 в рамках диссертационного исследования А.Г. Калачёвой.
This work was supported by the Russian Foundation for Basic Research grant 15-07-04143 under thesis research by Alla G. Kalacheva.
Сведения об авторах: 1Торшин Иван Юрьевич — к.х.н., старший научный сотрудник лаборатории фармакоинформатики; 1Громова Ольга Алексеевна — д.м.н., профессор, ведущий научный сотрудник, научный руководитель института фармакоинформатики; 2Калачёва Алла Геннадьевна — к.м.н., доцент кафедры фармакологии; 3Тетруашвили Нана Картлосовна — д.м.н., профессор, заведующая отделением патологии беременных; 2Демидов Вадим Игоревич — к.м.н., доцент кафедры патологической анатомии. 1ФИЦ ИУ РАН. 119333, Россия, г. Москва, ул. Вавилова, д. 44, корп. 2. 2ФГБОУ ВО ИвГМА Минздрава России. 153000, Россия, г. Иваново, Шереметевский пр., д. 8. 3ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России. 117997, Россия, г. Москва, ул. Академика Опарина, д. 4. Контактная информация: Громова Ольга Алексеевна, e-mail: unesco.gromova@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 18.09.2018.
About the authors: 1Ivan Yu. Torshin — PhD in Chemistry, Senior Researcher of the Laboratory of Pharmacoinformatics; 1Olga A. Gromova — MD, PhD, Professor, Leading Researcher, Science Нead of the Institute of Pharmacoinformatics; 2Alla G. Kalacheva — MD, PhD, Associate Professor of the Department of Pharmacology; 3Nana K. Tetruashvili — MD, PhD, Professor, Head of the Department of Pathology of Pregnancy; 2Vadim I. Demidov — MD, PhD, Associate Professor of the Department of Pathological Anatomy. 1Federal Research Center “Computer Science and Control” of the Russian Academy of Sciences. 44, bld. 2, Vavilova str., Moscow, 119333, Russian Federation. 2Ivanovo State Medical Academy. 8, Sheremetevsky ave., Ivanovo, 153000, Russian Federation. 3V.I. Kulakov Research Center of Obstetrics, Gynecology and Perinatology. 4, Oparina str., Moscow, 117997, Russian Federation. Contact information: Olga A. Gromova, e-mail: unesco.gromova@gmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received: 18.09.2018.
Медикамент запрещен для реализации в аптеках.
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|
||
|

Информация о лекарственных препаратах, размещенная на AptekaMos.ru, не должна использоваться неспециалистами для самостоятельного принятия решения об их покупке и применении без консультации врача.
Свидетельство о регистрации средства массовой информации ЭЛ № ФС77-44705 выдано Федеральной службой по надзору в сфере связи, информационных технологий и массовых коммуникаций (Роскомнадзор) 21 апреля 2011 года.