Уменьшает воспаление, Облегчает симптомы ДГПЖ
узнать больше
ЧТО ТАКОЕ ПЕРМИКСОН?
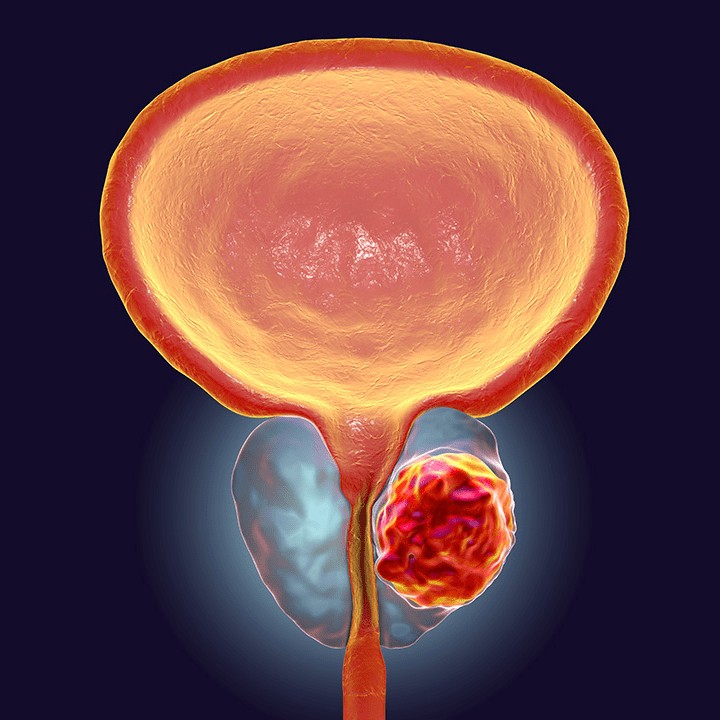
Пермиксон (Permixon) — это оригинальный препарат французской компании «Пьер Фабр», предназначенный для лечения умеренных нарушений мочеиспускания, связанных с доброкачественной гиперплазией предстательной железы (ДГПЖ) 1-й и 2-й стадии.1
Пермиксон содержит гексановый экстракт плодов пальмы ползучей (Serenoa repens), который обладает антиандрогенным, антипролиферативным и противовоспалительным действием1, а также обладает специфичностью и селективностью к тканям предстательной железы3.
ПОЧЕМУ ПЕРМИКСОН?
Применение препарата Пермиксон приводит к снижению выраженности основных симптомов нижних мочевых путей (СНМП), обусловленных ДГПЖ (уменьшение никтурии и поллакиурии, снижение баллов по шкале IPSS4, повышение скорости потока мочи (Qmax), сокращение количества остаточной мочи), уменьшению объема простаты и снижает риск прогрессирования ДГПЖ1.
РУ ЛП-№(000340)-(РГ-RU)-300821
КЛИНИЧЕСКИ
ДОКАЗАННОЕ ДЕЙСТВИЕ
Единственный гексановый экстракт плодов пальмы ползучей, обладающий доказанным противовоспалительным действием1.
Европейская ассоциация урологов рекомендует из растительных экстрактов только гексановый экстракт как «признанный препарат»2
БЕЗОПАСЕН ЛИ ПРИЕМ ПРЕПАРАТА ПЕРМИКСОН?
Важнейшей характеристикой любого лекарственного средства является его переносимость. Данные клинических испытаний препарата Пермиксон у пациентов с ДГПЖ свидетельствуют, что препарат хорошо переносится5.
Пермиксон практически не вызывает побочных эффектов, которые встречаются при использовании синтетических лекарственных средств6.
Не описано случаев его взаимодействия с другими лекарственными средствами1.
АРГУМЕНТЫ «ЗА» ПРИМЕНЕНИЕ
ПЕРМИКСОНА ПРИ ДГПЖ
Пермиксон показан с первых симптомов ДГПЖ, так как он быстро улучшает уродинамические параметры и облегчает симптомы ДГПЖ, повышая качество жизни пациента.
1
Пермиксон быстро действует
при симптомах ДГПЖ
Лечение ДГПЖ препаратом Пермиксон приводит к быстрому улучшению уродинамических параметров и симптомов ДГПЖ (по оценке баллов по шкале IPPS*)10
2
Пермиксон обладает комплексным
механизмом действия
Пермиксон обладает уникальным тройным механизмом действия: антиандрогенной, противовоспалительной и антипролиферативной активностью. Этот механизм отличается и дополняет действие α-блокаторов, которые действуют только на симптомы и не влияют на прогрессирование ДГПЖ1,10
3
Пермиксон хорошо переносится
Пермиксон значительно улучшает оценку MSF-4, что соответствует улучшению сексуальной жизни. При лечении Пермиксоном не было описано никаких специфических побочных эффектов.8
4
Пермиксон легко комбинировать
с другими препаратами
На сегодняшний день Пермиксон не имеет описанных лекарственных взаимодействий, что позволяет использовать его одновременно с другими лекарственными средствами.11
Где купить
Вы можете купить препарат Пермиксон в следующих аптечных сетях:


Состав
Экстракт плодов ползучей пальмы, диоксидтитана, полиэтиленгликоль, индигокармин, оксид железа, желатин.
Форма выпуска
Капсулы в ячейковой контурной упаковке по 15 штук, в картонной коробке по 2 упаковки.
Фармакологическое действие
Антиандрогенное, противоотечное, противовоспалительное и антипролиферативное действие, проявляющиеся местно, на уровне предстательной железы.
Фармакодинамика и фармакокинетика
Фармакодинамика
Антиандрогенное местное действие препарата обусловлено ингибированием процесса синтеза дигидротестостерона и воздействием на механизм его фиксации к цитозольным рецепторам. Это снижает синтез белка.
Местное антипролиферативное действие вызвано снижением активности фибробластического и эпидермального факторов роста и усилением процесса гибели клеток простаты, что способствует торможению роста предстательной железы и последующему уменьшению ее объема. Механизм противовоспалительного действия на местном уровне вызван способностью действующего вещества ингибировать активность фосфолипазы и арахидоновой кислоты, что способствует уменьшению синтезамедиаторов воспаления (лейкотриенов и простагландинов).
Пермиксон уменьшает воспалительный процесс и отечность в простате, уменьшает сосудистый стаз и проницаемость капилляров, устраняет компрессию мочевыводящего канала, улучшает уродинамику. На фоне применения Пермиксона замедляется рост предстательной железы и увеличение ее объема, уменьшаются проявления патологических процессов аденомы простаты — дизурии, чувства неполного опорожнения мочевого пузыря, никтурии, и болезненных ощущений во время мочеиспускания.
Фармакокинетика
Данные отсутствуют.
Показания к применению
Доброкачественная гиперплазия предстательной железы (аденома) I и II стадии.
Противопоказания
Индивидуальная гиперчувствительность.
Побочные действия
Аллергические реакции, гастралгия, тошнота.
Инструкция по применению Пермиксона (Способ и дозировка)
Суточная доза для взрослых 320 мг (по 1-ой капсуле 160 мг два раза в сутки) или однократно 320 мг (2 капсулы), не разжевывая.
Инструкция по применению Пермиксона рекомендует принимать препарат одновременно с приемом пищи. Длительность терапии — 1,5-2 месяца, по показаниям курс лечения можно повторить.
Передозировка
О случаях передозировки данные отсутствуют.
Взаимодействие
Антагонизма Пермиксона и препаратов, часто употребляемых в терапии доброкачественной гиперплазии простаты: антибиотиков, противовоспалительных средств и уросептиков не выявлено.
Условия продажи
Безрецептурный отпуск.
Условия хранения
При температуре до 30°C.
Срок годности
3 года.
Аналоги Пермиксона
Совпадения по коду АТХ 4-го уровня:
Капистан, Проста ургенин, Простамол, Серпенс, Строген С, Простаплант, Простесс, Простол, Простакур, Простагут.
Аналоги следует применять после консультации с врачом.
Отзывы о Пермиксоне
Многочисленные отзывы о Пермиксоне на форумах в большинстве случаев положительные. После курса лечения улучшается самочувствие — уменьшаются боли в промежности, уменьшается частота мочеиспусканий, улучшается качество жизни.
Цена Пермиксона, где купить
Цена Пермиксона в капсулах 160 мг, № 30 варьирует в пределах 797 —864 рублей за упаковку. Приобрести Пермиксон можно в большинстве аптек Москвы.
- Интернет-аптеки РоссииРоссия
Аптека Диалог
-
Пермиксон (капс. 160мг №30)Pierre Fabre Medicament
Ригла
-
Пермиксон капс. 160мг №30Pierr Fabre
показать еще
Пермиксон: место препарата в патогенетической терапии ДГПЖ

А.В. Сивков
К.м.н., заместитель директора по науке НИИ урологии и интервенционной
радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии»
Минздрава России (г. Москва)
Соавтор – д.м.н., профессор В.Н. Синюхин
Проблема лечения больных доброкачественной гиперплазией предстательной железы (ДГПЖ) до сих пор остается актуальной. Согласно литературным данным, 15–25% мужчин в возрасте 50-65 лет страдают этим заболеванием, которое приводит к выраженному снижению качества жизни за счет симптомов нарушения функции нижних мочевых путей (СНМП). В настоящее время считают, что в патогенезе ДГПЖ имеет значение как генетическая предрасположенность, так и дисрегуляция гормонального обмена, которая приводит к активации гиперпластических процессов в предстательной железе (ПЖ), торможению апоптоза, а также к выделению целого ряда медиаторов, вызывающих хроническое воспаление.
Современные представления о патогенезе ДГПЖ
Рост ПЖ, поддержка ее структуры и функции зависит от постоянного поступления в нее андрогенов. Тестостерон метаболизируется до дигидротестостерона (ДГТ) под воздействием изоэнзимов Δ,4,3-кетостероид-5-α-редуктазы (5α-R). Эти энзимы локализуются на мембране ядра клеток стромы и эпителия железы. ДГТ связывается со специфическим рецептором и вызывает экспрессию целого ряда гормон-зависимых генов, запускающих механизмы деления клетки. Этот процесс зависит не только от концентрации андрогенов, главным образом ДГТ, который образуется в ПЖ из тестостерона при воздействии 5α-R 1 и 2 типов и имеет большое сродство к андрогенному рецептору (АР), но и от состояния внутриклеточных стероидных сигнальных путей, передающих сигнал от АР через лиганд-активируемый ядерный транскрипционный фактор. Это приводит к стимуляции процесса транскрипции в андроген-зависимых генах, несущих ответственность за контроль клеточного цикла, течение пролиферативных процессов и выработку простатспецифического антигена (ПСА).
Постоянная стимуляция АР необходима прежде всего для роста и функции ПЖ. Этот процесс работает путем трансактивации домена, закодированного в первом экзоне гена АР (Xq 11-12), которому в норме свойственен полиморфизм CAG, GGN и GGC повторов, кодирующих тракты полиглутамина и полиглицина. При исследовании генетического полиморфизма некоторых генов, ответственных за метаболизм стероидов, показана их тесная связь с вероятностью возникновения ДГПЖ. Об этом свидетельствует тот факт, что у родственников мужчин, больных с ранним возникновением ДГПЖ, кумулятивный риск возникновения этого заболевания составляет 66%, тогда как в контрольной группе – лишь 17% (p = 0,01).
Кроме того, при исследовании полиморфизма генов, кодирующих 5α-R 2 типа (SRD 5A1 и SRD 5 A2), было установлено, что имеется тесная взаимосвязь между выраженностью полиморфизма генов, объемом ДГПЖ, эффективностью проводимой антиандрогенной терапии и концентрацией половых гормонов и их метаболитов
Интересна роль α1-адренорецепторов в патогенезе ДГПЖ. Предполагают, что в ПЖ они участвуют в процессе кооперативной регуляции работы внутриклеточных эффекторов, гормонов, факторов роста, которые влияют не только на тонус гладкомышечных элементов ПЖ, но и на их объем.
В последнее время появилось большое число исследований, показывающих, что ДГПЖ – это иммуновоспалительное заболевание. При этом в ткани ПЖ обнаруживают воспалительные инфильтраты, содержащие лимфоциты и макрофаги, количество которых коррелирует с объемом ДГПЖ. Они секретируют факторы роста, включая фактор роста фибробластов (FGF), цитокины: интерлейкин-1 (IL-1), интерлейкин-6 (IL-6), фактор некроза опухоли-α (TNF-α). Также наблюдают повышенную активность Т-клеток и аутоиммунные реакции, которые способствуют пролиферации стромальных и эпителиальных клеток. Было показано, что повышенное содержание в ткани при ДГПЖ провоспалительных цитокинов и цитокинов семейства IL-17 A, E, F и их рецепторов сопровождает повышение содержания клеток воспаления и сосудов с экспрессией CD 31+, а также провоспалительных хемокинов: MCP-1/CCL2 (фактор, хемотаксиса моноцитов), IP10/CXCL10 (индуцируемый гамма-интерфероном белок), MIF (фактор ингибирующий миграцию макрофагов). Провоспалительные цитокины повышают активность циклооксигеназы-2 (COX-2) и вызывают образование простагландинов и окиси азота, что стимулирует пролиферативные процессы в ПЖ и вызывает ее отечность. Ряд авторов считают, что активные формы кислорода приводят к повреждению ткани ПЖ, так как после завершения процесса трансляции вызывают модификацию структуры ДНК и ее клеток, что может привести к малигнизации процесса
Сахарный диабет и метаболический синдром являются факторами риска образования ДГПЖ. Отмечена взаимосвязь между резистентностью к инсулину, гиперинсулинемией и ДГПЖ. Гиперинсулинемия приводит к образованию в печени инсулиноподобных факторов роста (IGF), которые обладают митогенным и антиапоптическим эффектом. Эти факторы связываются в ПЖ со своими рецепторами и стимулирует увеличение ее объема. Концентрация IGF и белков, связывающих IGF в крови и ПЖ, коррелирует с выраженностью в ней пролиферативных процессов и участвует в регуляции образования андрогенов и гормона роста.
Гипергликемия и гиперинсулинемия также стимулируют образование в стромальных фибробластах ПЖ инсулиноподобного фактора роста-1 (IGF-1). Последний связывается со своим рецептором на эпителиальных клетках ПЖ и стимулирует их пролиферацию через целевой ген.
Общие подходы к лечению ДГПЖ
Современное лечение ДГПЖ / СНМП воздействует на различные звенья патогенеза этого заболевания. На первом месте стоят α1А-адреноблокаторы (доксазозин, теразозин, алфузозин, тамзулозин, силодозин): их считают препаратами выбора при ДГПЖ. Затем идут ингибиторы 5α-редуктазы (финастерид, дутастерид), которые при длительной терапии у пациентов с величиной ПЖ более 40 куб. см способны привести к уменьшению объема ДГПЖ. М-холинолитики (толтеродин, троспиума хлорид, солифенацин) и агонист β3-адренорецепторов – мирабегрон чаще используют в комбинации с α1А-адреноблокаторами для купирования проявлений гиперактивного мочевого пузыря при ДГПЖ. Тадалафил (ингибитор фосфодиэстеразы 5 типа) улучшает симптомы ДГПЖ у больных, страдающих эректильной дисфункцией. По показаниям применяют нестероидные противовоспалительные препараты. Обсуждают возможность применения антиоксидантов при ДГПЖ [16]. Однако все эти препараты обладают целым рядом побочных эффектов и воздействуют только на отдельные фазы патогенеза ДГПЖ.
Современное лечение ДГПЖ / СНМП воздействует на различные звенья патогенеза этого заболевания. На первом месте стоят α1А-адреноблокаторы (доксазозин, теразозин, алфузозин, тамзулозин, силодозин): их считают препаратами выбора при ДГПЖ. Затем идут ингибиторы 5α-редуктазы (финастерид, дутастерид), которые при длительной терапии у пациентов с величиной ПЖ более 40 куб. см способны привести к уменьшению объема ДГПЖ. М-холинолитики (толтеродин, троспиума хлорид, солифенацин) и агонист β3-адренорецепторов – мирабегрон чаще используют в комбинации с α1А-адреноблокаторами для купирования проявлений гиперактивного мочевого пузыря при ДГПЖ. Тадалафил (ингибитор фосфодиэстеразы 5 типа) улучшает симптомы ДГПЖ у больных, страдающих эректильной дисфункцией. По показаниям применяют нестероидные противовоспалительные препараты. Обсуждают возможность применения антиоксидантов при ДГПЖ [16]. Однако все эти препараты обладают целым рядом побочных эффектов и воздействуют только на отдельные фазы патогенеза ДГПЖ.
Механизмы действия Пермиксона
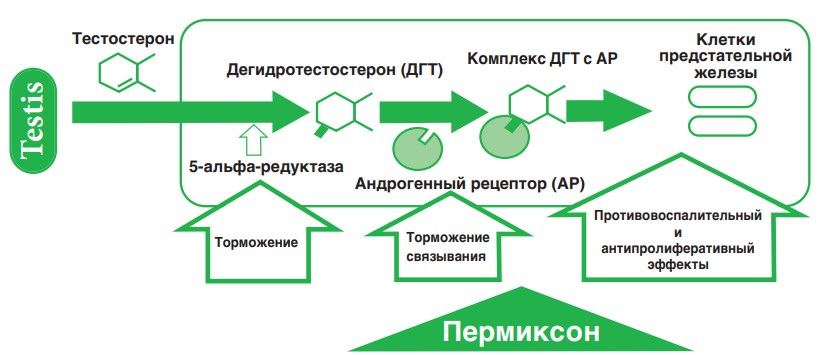
Пермиксон (Permixon) представляет собой комплексную смесь свободных и эстерифицированных жирных кислот, полипренов и фитостеролов, полученных из плодов пальмы ползучей (Serenoa repens или Sabal serrulata). Препарат содержат несколько ингредиентов и поэтому при его применении возможен комплексный фармакологический эффект, действующий на различные звенья патогенеза ДГПЖ (рис. 1). Другими словами, эффект этой смеси можно сравнить с комбинированной лекарственной терапией, каждый компонент которой может обладать по отношению к другому аддитивным или синергическим действием.
Рис.1. Патогенез ДГПЖ и механизм действия Пермиксона
Влияние Пермиксона на клеточные структуры ПЖ
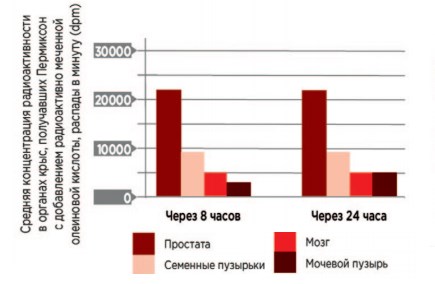
При исследовании любого препарата, как правило, проводят изучение специфичности и селективности его действия. Это касается и Пермиксона. C.W. Bayne и соавт. в культуры тканей из различных органов добавили нарастающие концентрации Пермиксона. При исследовании препаратов этих культур на электронном микроскопе оказалось, что только в клетках ПЖ были отмечены выраженные структурные изменения, которые заключались в накоплении липидных капель в цитоплазме, изменении мембраны ядра, его поляризации, разрушении органелл, конденсации хроматина. Это подтвердило специфичное действие Пермиксона именно на клетки ПЖ [20]. При присоединении радиоактивной метки к входящим в состав Пермиксона свободным жирным кислотам и введении его крысам оказалось, что в наибольших количествах метка накапливалась в ПЖ (рис. 2), что свидетельствует в пользу селективности действии лекарственного препарата на этот орган.
Таким образом, преимущественное накопление компонентов Пермиксона в ПЖ вызывает в ней морфологические изменения, которые могут отразиться на физико-химических характеристиках и повлиять на различные системы регуляции работы органа как на клеточном, так и молекулярном уровнях.
Влияние Пермиксона на гормональный статус ПЖ
В 1998 г. F. Di Silverio с соавт. сообщили, что трехмесячная терапия Пермиксоном приводит к выраженному уменьшению содержания ДГТ в ПЖ. Затем в опытах in vitro на культуре эпителиальных клеток и клеток рака ПЖ было показано, что Пермиксон тормозит активность 5α-R 1 и 2 типов и не вызывает повышения концентрации простатспецифического антигена (ПСА) в культуральной среде. Это, по-видимому, связано с тем, что препарат не влияет на опосредованный АР процесс транскрипции. Данный феномен был подтвержден и in vivo. Интересно отметить, что при культивировании клеток других органов не наблюдали торможения активности 5α-R. Тем не менее до сих пор не удалось объяснить, почему Пермиксон тормозит активность 5α-R и рост ПЖ, но не влияет на продукцию эпителиальными клетками ПСА. Возможно, это связано тем, что препарат воздействует на клеточную и внутриклеточные мембраны стромальных и эпителиальных клеток ПЖ, приводит к изменению микроокружения 5α-R и, как следствие, торможению ее активности. При этом Пермиксон не влияет на работу генов, от которых зависит действие андрогенов и выработка ПСА.
Пермиксон оказывает действие не только на активность 5α-R , но и на различные фазы метаболизма андрогенов и тормозит связывание ДГТ с АР. Он также обладает и антиэстрогенной активностью. В исследовании ткани ПЖ больных ДГПЖ при применении этого препарата было отмечено уменьшение количества ядерной фракции эстрогенных рецепторов. Известно, что рост ПЖ зависит не только от концентрации андрогенов, но и от других гормонов, например пролактина, который принимает участие в процессах формирования гиперплазии железы. В опытах на мышах с гиперпролактинемией, вызванной введением сульпирида, было отмечено торможение Пермиксоном гиперплазии ПЖ. Кроме того, удалось показать, что препарат модулирует пути трансдакции сигнала пролактина и блокирует его действие на процесс С-зависимого фосфорилирования калиевых каналов протеинкиназой.
Таким образом, Пермиксон обладает антиандрогенным действием, тормозит активность 5α-R, блокирует АР ПЖ, уменьшает в ней число эстрогенных рецепторов и снижает стимуляцию пролактином гиперпластических процессов. Кроме того, препарат имеет еще одно преимущество перед синтетическими ингибиторами 5α-R, так как не влияет на концентрацию ПСА.
Противовоспалительное действие Пермиксона
Противовоспалительное действие Пермиксона начали исследовать еще в 90-е годы прошлого столетия. В одной из первых работ было изучено его влияние на образование из арахидоновой кислоты полиморфоядерными лейкоцитами крови человека хемоаттрактанта нейтрофилов – лейкотриена (LTB 4) после их стимуляции ионофором А 23127. Было показано, что Пермиксон тормозит продукцию ее метаболитов: 5-HETE, 20-COOH LTB4, LTB4 и 20-OH LTB. Эти результаты были подтверждены дальнейшими иммуногистохимическими исследованиями удаленного гиперплазированного участка ПЖ, которые показали, что трехмесячный прием Пермиксона вызывает резкое снижение количества В-лимфоцитов (но не T-лимфоцитов и макрофагов), TNF-α и IL-1β. При оценке по международной шкале простатических симптомов (IPSS) эти изменения коррелировали с клинически значимым улучшением состояния пациентов, что свидетельствует о противовоспалительном действии препарата. Это затем нашло подтверждение в работах других авторов.
Еще одна исследовательская группа провела изучение противовоспалительной активности Пермиксона при ДГПЖ. В опытах in vitro было оценено влияние препарата на пролиферацию и жизнеспособность клеток ПЖ с использованием клеточных линий из тканей здоровой и гиперплазированной железы. В тканях при ДГПЖ были отмечены повышенные индексы пролиферативной активности. Добавление разных концентраций Пермиксона уменьшало клеточную пролиферацию во всех клеточных линиях. Наиболее выраженный эффект отметили в стромальных и эпителиальных клетках при гиперплазии ПЖ. Добавление провоспалительных медиаторов IL-6, IL-17 и FGF в клеточную культуру провоцировало выраженную пролиферацию всех трех типов клеток: стромальных, эпителиальных и здоровых. Последующее добавление Пермиксона уменьшило клеточную пролиферацию, индуцированную FGF-2 в стромальных и здоровых клетках, а IL-6 и IL-17 – в клеточной линии гиперплазированных тканей. Авторы выполнили микроматричный анализ для сравнения экспрессии генов в эпителиальных и стромальных клетках при ДГПЖ после добавления Пермиксона и без него. При добавлении препарата была выявлена недостаточная экспрессия генов, кодирующих провоспалительные медиаторы (IL-1β, IL-6 и хемокина C-X-C motif). Также отмечено уменьшение экспрессии гена, кодирующего человеческий рецептор эпидермального фактора роста 3 (ERBB3), что привело к избыточной экспрессии человеческого гена блокировки роста (GAS1).
В исследовании de la Taille A. на модели in vivo у самцов крыс линии Спрег-Доули вызвали ДГПЖ путем 14-дневного введения тестостерона пропионата. Животные были рандомизированы на три группы лечения: ЭППП ( Пермиксон), финастерид и контроль (без активного лечения). Проводили количественное определение в ПЖ мРНК для 90 генов. Оказалось, что Пермиксон обеспечил статистически значимое снижение (p < 0,05) экспрессии большинства транскриптов воспалительных генов. Были получены четкие доказательства того, что он оказывает влияние на каскад арахидоновой кислоты, особенно на сигнальный путь липоксигеназы и, таким образом, воздействует на воспалительный процесс при ДГПЖ.
Рис. 2. Простатспецифическое действие препарата Пермиксон [21]
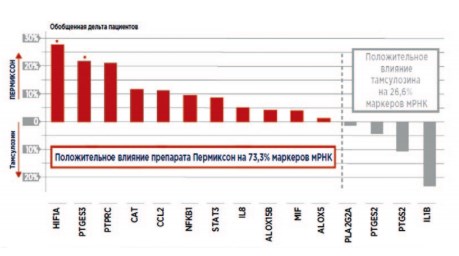
A. Latil и соавт. провели международное рандомизированное двойное слепое исследование влияния препарата Пермиксон на маркеры воспаления. Пациенты принимали этот препарат внутрь в дозе 320 мг/сут. или тамсулозин в дозе 0,4 мг/сут. в течение 3 месяцев. В десквамированных эпителиальных клетках ПЖ, выделенных из мочи после массажа ПЖ, проводили количественный анализ мРНК 29 наиболее значимых маркеров воспаления, а также исследовали белки мочи. Через 90 дней от начала терапии наблюдали снижение экспрессии генов, в среднем, для 65,4% маркеров, выявленных в группе, принимавшей Пермиксон, и для 46,2% – в группе тамсулозина. Для 15 генов, наиболее часто демонстрировавших экспрессию, разница была выше: 80 и 33% соответственно. Кроме того, для 11 из 15 маркеров (73,3%) повышение регуляции наблюдали у меньшего числа пациентов в группе Пермиксона, по сравнению с группой тамсулозина: 4 из 15 маркеров или 26,6% (рис. 3). Оказалось, что на 90 день приема препарата уменьшение числа пациентов с наличием экспрессии белков провоспалительных хемокинов МСР-1/CCL2 и IP-10 /CХCL наблюдали только в группе Пермиксона. Кроме того, Пермиксон, по сравнению с тамсулозином, в большей степени снижал экспрессию MIF (p = 0,007). Однако в отличие от получавших тамсулозин, в группе Пермиксона, где в начале терапии наблюдали большую экспрессию MIF, ответ на лечение по критерию IPSS оказался лучше, чем у пациентов с небольшим содержанием данного белка: среднее изменение оценки по шкале IPSS: -6,2 и -4,5 баллов, соответственно. Данные результаты впервые на клиническом уровне продемонстрировали противовоспалительные свойства Пермиксона при лечении СНМП, обусловленных ДГПЖ.
Рис. 3. Снижение уровня экспрессии генов маркеров воспаления ПЖ через 90 дней применения препарата Пермиксон [35]
Таким образом, на основании приведенных данных можно утверждать, что Пермиксон обладает противовоспалительным действием и способен предотвращать дальнейшее развитие ДГПЖ у пациентов с хроническим воспалением ПЖ.
Пермиксон – пролиферация и апоптоз
В литературе содержится информация о том, что с началом развития ДГПЖ в ее клетках наблюдают процесс торможения апоптоза. Лечение Пермиксоном сопровождается увеличением апоптического индекса в клетках ПЖ, тогда как в клетках других органов этот эффект не наблюдали.
F. Vacherot и соавт. изучали влияние Пермиксона на апоптоз и пролиферацию в клетках гиперплазированной ПЖ у больных, получавших этот препарат в течение 3 месяцев. Оказалось, что апоптоз / пролиферативный индекс увеличился в эпителиальных клетках в 5,5, а в стромальных клетках – в 8,8 раза, что говорит об антипролиферативных свойствах этого лекарственного средства.
В другом исследовании проведено изучение молекулярных маркеров, связанных с процессом апоптоза в ткани удаленной ДГПЖ после 3-месячного приема Пермиксона. Измеряли маркеры Bax и Bcl-2 (семейство Bcl-2), характеризующие, соответственно, проапоптические и антиапоптические изменения. Также определяли активность каспазы-3 – белкового эффектора апоптического каскада. Авторы показали, что по сравнению с контрольной группой, соотношение Bax/Bcl-2 и активность каспазы-3 были достоверно выше в ткани ПЖ больных, получавших препарат перед операцией.
Таким образом, Пермиксон обладает антипролиферативным и проапоптотическим действием.
Пермиксон: результаты клинического применения
В настоящее время в библиографической базе PubMed найдены ссылки на 430 работ, в которых изучено действие препаратов пальмы ползучей. Первые из них относятся в началу 80-х гг. прошлого века.
В 1991 г. G. Dathe и Н. Schmid в результате рандомизированного сравнительного исследования продолжительностью 6 месяцев одни из первых определили оптимальную терапевтическую дозу Пермиксона у больных с ДГПЖ. У 49 пациентов оценили эффективность двух доз препарата: 320 мг (группа I, n = 24) и 960 мг (группа II, n = 25) в сутки. Оказалось, что у всех больных средняя скорость мочеиспускания (Qave) и суммарный объем мочеиспускания (V) увеличивались с 16 по 24 неделю от начала приема препарата. При приеме препарата в дозе 160 мг или 480 мг два раза в сутки – нормальную скорость мочеиспускания (Qmax > 14 мл/сек) наблюдали у 33 и 48% больных соответственно. Объем остаточной мочи (Vres) снизился, начиная с 16 недели, на 27 и 32% у больных I и II групп, соответственно. При приеме препарата в дозе 320 мг/сут субъективная симптоматика исчезла у 46% больных, 960 мг в день – у 60%. В результате исследования было показано, что оптимальной терапевтической дозой Пермиксона является 320 мг/сут.
Подобные результаты были получены в 1999 г. в исследовании В.Н. Степанова и соавт. на 100 амбулаторных больных с ДГПЖ в рандомизированном 3-месячном исследовании в параллельных группах. Было показано, что к концу первого месяца приема препарата значительно улучшились показатели IPSS, Qmax, Qave, V. К концу третьего месяца лечения все они, за исключением V и Qave, продолжали улучшаться. Таким образом, прием Пермиксона в дозе 320 мг/сут. улучшает суммарный балл IPSS и все показатели мочеиспускания. Препарат оказывает тот же эффект в дозе 160 мг два раза в день.
Исследование D. Authie и J. Cauquil включало 500 пациентов с ДГПЖ (средний возраст 68,2 года). У большинства из них имели место симптомы расстройства мочеиспускания: ноктурия – у 97%; дневная поллакиурия – у 67%; дизурия – у 92% и императивные позывы – у 70%. Все пациенты получали Пермиксон (320 мг/сут.) в течение 3 месяцев. Авторами зарегистрирован выраженный симптоматический эффект препарата: к концу лечения средняя частота позывов в ночное время снизилась с 4,0 до 1,8, причем улучшение по данному показателю было отмечено у 82%, а полное исчезновение симптома – у 45% больных. Частота дневных мочеиспусканий сократилась с 6,3 до 4,6 у 2/3 мужчин, а уменьшение дизурии и императивности позывов достигнуто у 75 и 85% пациентов соответственно.
F. Foroutan изучал клиническую эффективность Пермиксона в дозе 320 мг/сут. в течение 3 месяцев у 592 пациентов с ДГПЖ. В результате лечения отмечено статистически значимое уменьшение симптомов заболевания и снижение показателя IPSS с 17 до 10 баллов, а также достоверная положительная динамика объективных параметров: Qmax, количества остаточной мочи и объема ПЖ, хотя последнее и было незначительным – 1,84 мл. Похожие результаты были получены рядом отечественных авторов в коротких несравнительных исследованиях Пермиксона.
В НИИ урологии в 1999 г. проанализированы результаты лечения 48 больных ДГПЖ, которые получали Пермиксон по 160 мг дважды в день в течение 12 месяцев. Было отмечено уменьшение выраженности симптомов по шкале I-PSS с 14,35 до 10,61 балла (-26,1%) через 6 месяцев и до 10,42 (- 27,4%) через 12 месяцев лечения. В те же периоды времени средний показатель Qmax увеличился с 10,62 до 12,60 мл/сек (+18,7%) и до 12,73 мл/сек (+19,9%) соответственно. Индекс качества жизни QOL через 6 месяцев наблюдения снизился с 3,49 до 2,60 баллов (-25,3%), достигнув к концу года 2,49 (-28,7%). Также было зарегистрировано небольшое уменьшение среднего объема предстательной железы: на 11,8% через 6 месяцев и 15,6% через 12 месяцев. Показатель ПСА не изменялся в течение всего периода лечения.
Изучение эффективности Пермиксона у больных с различными исходными значениями IPSS и Qmax дало нам возможность сделать заключение о том, что препарат наиболее результативен у пациентов с умеренной выраженностью симптомов ДГПЖ (IPSS < 18) и умеренными уродинамическими нарушениями (Qmax > 10 мл/сек).
Большое клиническое значение имеют данные уродинамических исследований, характеризующие влияние Пермиксона на состояние мочевого пузыря и степень инфравезикальной обструкции. На основании анализа данных комплексного уродинамического обследования больных ДГПЖ, получавших Пермиксон, был сделан вывод, что препарат оказывает позитивное влияние на функциональное состояние мочевого пузыря и уменьшает степень инфравезикальной обструкции. Вместе с тем ни в одном случае полностью устранить проявления обструкции не удалось.
Особый интерес представляют работы, в которых сравнивали эффективность и безопасность Пермиксона с плацебо и другими лекарственными средствами. Результаты 7 плацебо-контролируемых исследований, в которых приняло участие в общей сложности 559 человек, обобщены в 1996 г. G. Plosker и R. Brogden. В трех наиболее значимых из них, где участвовало 410 больных ДГПЖ, пациенты были разделены на две практически равные группы: принимавшие Пермиксон (320 мг/сут.) и плацебо. В этих исследованиях продолжительностью от 1 до 3 месяцев достоверно продемонстрирована клиническая эффективность препарата по сравнению с плацебо. При этом частота ночных мочеиспусканий уменьшилась на 33–46%, дневная поллакиурия – на 11–20%, a Qmax увеличилась на 29–50%, что было существенно выше, чем в группе плацебо, где аналогичные показатели составили 15–18, 1–3 и 5–9% соответственно.
В трех других опубликованных исследованиях продолжительностью 1–2 месяца с участием 79 больных на фоне приема Пермиксона было отмечено уменьшение ноктурии на 50–74%, снижение частоты дневных мочеиспусканий на 29–43% и рост Qmax на 26–43%, тогда как в группе плацебо эти же показатели были равны 13–39%, 8-29% и 2–19%. Лишь в одном из 7 опубликованных исследований авторы не выявили существенных различий между изучаемыми признаками.
В ряде наблюдений Пермиксон выступил в качестве эффективного средства устранения дизурии. В исследовании J. Descotes и соавт., проведенном на 176 больных ДГПЖ, показано, что в течение одного месяца дизурия уменьшилась у 31% у получавших Пермиксон (320 мг/сут.) по сравнению с 16% – в группе плацебо (р < 0,05). Подобные же результаты были получены в другом исследовании, охватившем 146 пациентов.
Предметом ряда исследований стало изучение влияния Пермиксона на объем остаточной мочи. При этом на фоне применения препарата уменьшение Vres относительно первоначальных значений составило 15–50% и было статистически значимым, по сравнению с группой плацебо, где наблюдали не только снижение, но и увеличение этого показателя.
Таким образом, большинство проведенных плацебо-контролируемых исследований Пермиксона достоверно продемонстрировали клиническую эффективность лечения, которая проявляется выраженным уменьшением симптомов заболевания и улучшением уродинамических показателей.
Описание клинических результатов применения Пермиксона было бы неполным без рассмотрения материалов его исследования в сравнении с другими лекарственными препаратами. Особенно интересны данные, касающиеся финастерида и α1-адреноблокаторов.
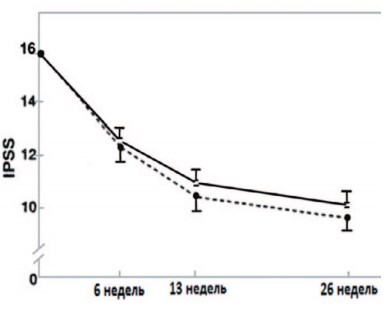
Показательно широкомасштабное исследование J.С. Carraro и соавт., в ходе которого в течение 6 месяцев двойным слепым методом сравнивали эффективность и безопасность Пермиксона и финастерида. Для участия в исследовании было рандомизировано 1098 мужчин с ДГПЖ, отобранных в 87 урологических центрах 9 европейских стран. Анализ клинических результатов проведен у 1069 пациентов, из которых 536 получали Пермиксон (320 мг/сут.) и 533 – финастерид (5 мг/сут.). Данная работа – одно из самых крупных сравнительных исследований этих двух препаратов у пациентов с ДГПЖ. Основными критериями сравнения в этом исследовании были: динамика симптомов по шкале IPSS, изменение Qmax, a также показателей качества жизни и сексуальной функции. Через 6 месяцев лечения отмечено уменьшение симптомов по шкале I-PSS с 15,7 ± 5,7 до 9,5 ± 5,5 баллов (-39%) в группе финастерида и с 15,7 ± 5,9 до 9,9 ± 5,4 баллов (-37%) среди пациентов, получавших Пермиксон (р < 0,001) (рис. 4). Симптоматическое улучшение уже через 6 недель превысило 20% в обеих группах. Кроме того, более 50% больных в каждой из групп к моменту окончания лечения отметили улучшение качества жизни (QOL), динамика показателя которого составила -38% у принимавших Пермиксон и 41% – у получавших финастерид. Различия итоговых значений IPSS и QOL в обеих группах, при сравнении их между собой оказались статистически недостоверными.
Половая функция по результатам анкетирования не претерпела существенных изменений на фоне терапии Пермиксоном, а у пациентов, лечившихся финастеридом, было выявлено ее некоторое ухудшение.
Рис. 4. Общая средняя оценка по шкале IPSS у мужчин с ДГПЖ, получающих препарат Пермиксон в дозе 320 мг (белые квадраты) или финастерид в дозе 5 мг (черные ромбы) (± 95% доверительный интервал)
В обеих группах отмечено улучшение уродинамических показателей. При этом Qmax увеличилась с 10,6 ± 2,8 до 13,3 ± 6,7 мл/с (+25%) через 6 месяцев лечения Пермиксоном и с 10,8 ± 3,1 до 14,0 ± 7,4 мл/с (+30%) в группе финастерида (р < 0,001): улучшение оказалось несколько более выраженным у пациентов, принимавших финастерид (р < 0,05). Наибольший эффект обоих препаратов наблюдали у больных с выраженной симптоматикой (IPSS > 18) и относительно сохранным мочеиспусканием (Qmax > 10 мл/с), число которых в результате лечения сократилось практически на 80% за счет перехода больных в группы с менее выраженными клиническими проявлениями. В результате применения как Пермиксона, так и финастерида произошло незначительное, но статистически достоверное (р < 0,001) уменьшение объема ПЖ. В первом случае оно составило 6%, а во втором – 18%, что свидетельствует об отсутствии четкой корреляции между ослаблением симптоматики и изменением объема железы.
В ходе описываемого сравнительного исследования была изучена зависимость результатов лечения Пермиксоном от объема ПЖ. Оказалось, что клиническая эффективность Пермиксона не зависит от исходного объема железы. Было также отмечено значительное (на 41%) снижение уровня ПСА в группе финастерида (р < 0,001), тогда как у принимавших Пермиксон этот показатель существенно не изменился (+3%). Указанное различие является статистически значимым.
Таким образом, описанное исследование продемонстрировало, что Пермиксон и финастерид одинаково эффективно воздействуют на симптомы ДГПЖ, качество жизни и уродинамические показатели при статистических различиях в динамике уровней ПСА и влиянии на половую функцию в пользу Пермиксона
Представляют интерес сравнительные исследования Пермиксона и α1-адреноблокаторов. Так, M. Grasso и соавт. изучили результаты применения Пермиксона (320 мг/сут.) у 31 больного и альфузозина (2,5 мг 3 раза в день) у 32 пациентов с ДГПЖ в течение 3 недель лечения. Эффективность препаратов оценивали с использованием шкалы Boyarsky и критерия Qmax. В результате лечения уменьшение симптомов составило 27% в первой группе и 39% – во второй (р < 0,01). Увеличение Qmax также было в целом достоверным, но более выраженным во второй группе (+51%) по сравнению с первой (+27%), хотя различия между ними и не были статистически столь значимыми.
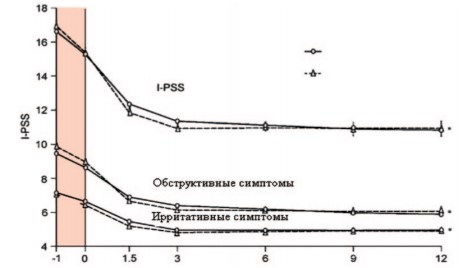
Рис. 5 Изменение среднего профиля оценки Пермиксона и Тамсулозина по шкале I-PSS с течением времени
В 2002 г. в 11 странах Европы было проведено 12-месячное двойное слепое рандомизированное сравнительное исследование Пермиксона и тамсулозина (PERMAL), которое включило 811 больных ДГПЖ с оценкой СНМП по шкале I-PSS ≥ 10 баллов. После 4-недельного вводного периода 704 пациента были случайным образом распределены в группы тамсулозина (0,4 мг/сут.; n = 354) и Пермиксона (320 мг/сут.; n = 350). В начале исследования и периодически в течение года у пациентов проводили оценку по шкале IPSS, шкале качества жизни – QOL и измеряли Qmax. Через 12 месяцев в каждой группе лечения показатели IPSS снизились на 4,4 балла, какиелибо различия в улучшении ирритативных или обструктивных симптомов отсутствовали (рис. 5). Повышение показателя Qmax было сопоставимо в обеих группах: 1,8 мл/сек. – для препарата Пермиксон, 1,9 мл/сек. – для тамсулозина. Уровень ПСА оставался неизменным на фоне небольшого снижения объема ПЖ у пациентов, принимавших Пермиксон. Оба препарата продемонстрировали хорошую переносимость, однако в группе тамсулозина чаще наблюдали нарушения эякуляции. Это исследование показало, что эффективность применения Пермиксона и тамсулозина при лечении СНМП у мужчин с ДГПЖ на протяжении 12 месяцев практически одинакова, с преимуществом безопасности растительного препарата.
В другой работе эта же группа авторов дополнительно проанализировала результаты лечения 124 больных с выраженными проявлениями СНМП (IPSS > 19), получавших тамсулозин (n = 59) и Пермиксон (n = 65). Через 12 месяцев общий показатель IPSS снизился в группе тамсулозина на 5,8, а в группе Пермиксона – на 7,8 баллов, что составило, соответственно, 25 и 35,2% от исходного уровня. Оказалось, что чем выше были исходные показатели IPSS в группе Пермиксона, тем больше они снижались в процессе терапии. В этой группе улучшение наступало через 3 месяца после начала лечения и оставалось на том же уровне весь период наблюдения. В группе тамсулозина Qmax увеличилась на 1,7 мл/сек., а в группе Пермиксона – на 1,2 мл/сек. Объем ПЖ снизился при приеме тамсулозина на 0,9 см3 , а при приеме Пермиксона – на 2,2 см3 . Таким образом, Пермиксон (320 мг/сут.) и тамзулосин (0,4 мг/сут.), принимаемые в течение 12 месяцев, вызывают сопоставимое улучшение симптомов и показателей мочеиспускания у пациентов с выраженными СНМП/ДГПЖ. Похожие результаты были получены и в ходе сравнения Пермиксона с празозином.
Принципиальные выводы о клинической эффективности Пермиксона были сделаны по итогам метаанализа, представленного P. Boyle и соавт. в 2004 г. В работе были обобщены материалы 12 основных плацебо-контролируемых и сравнительных исследований Пермиксона, включавших результаты лечения 2794 больных ДГПЖ. С высокой степенью статистической достоверности авторам удалось продемонстрировать: лечение Пермиксоном приводит к увеличению Qmax дополнительно на 1,87 ± 0,55 мл/сек. по сравнению с плацебо (р < 0,001); терапия Пермиксоном уменьшает частоту ночных мочеиспускании на 0,55 ± 0,10 по сравнению с плацебо (р < 0,001).
Таким образом, сегодня можно с уверенностью констатировать, что клиническая эффективность Пермиксона по отношению к плацебо статистически доказана.
Важнейшей характеристикой любого лекарственного средства является его переносимость. Данные клинических испытаний Пермиксона у пациентов с ДГПЖ, получавших его в дозе по 160 мг дважды в день (320 мг/сут.), свидетельствуют, что препарат легко переносится большинством (94,4%) пациентов. Только у 2–3% мужчин, принявших участие в двух широкомасштабных несравнительных исследованиях (1092 человека), наблюдали какие-либо побочные эффекты. В основном это были незначительные жалобы на нарушение функции желудочно-кишечного тракта (тошнота), которые исчезали самостоятельно при приеме препарата во время еды. Ни у одного из пациентов терапия не была прервана в связи с каким-либо осложнением.
В ходе описанного выше международного мультицентрового двойного слепого рандомизированного сравнительного исследования эффективности и безопасности Пермиксона и финастерида не отмечено значимых различий их переносимости. Жалобы на боль в животе, диарею, запор, тошноту были наиболее часты среди нежелательных явлений и характерны в равной мере как для Пермиксона, так и для финастерида. Отрицательного влияния Пермиксона на половую функцию не зарегистрировано, а снижение либидо и половой потенции чаще ассоциировали с финастеридом.
Более того, как показали G. D’Ottavio и соавт. при изучении влияния 3-месячного курса терапии Пермиксоном (320 мг/сут.) на фертильность у мужчин относительно молодого возраста (средний возраст 36 лет) с сохраненной эякуляцией, в течение 12 месяцев наблюдения ни по одному из параметров (объем эякулята, концентрация и подвижность сперматозоидов) не отмечено каких-либо значимых отклонений. У этих больных отсутствовали побочные эффекты и не было зарегистрировано по сравнению с исходными данными существенных изменений лабораторных параметров крови. Пермиксон не влиял на либидо, половую потенцию и не вызывал гинекомастии. Приведенные данные являются основанием для расширения показаний к применению препарата у лиц молодого возраста и у больных, страдающих хроническим простатитом.
Клинически важны исследования по лечению хронического простатита (ХП) ЭППП в сочетании с антибактериальными препаратами. Так, V. Magri и соавт. наблюдали в течение 6 недель 137 больных, которым для лечения ХП был назначен ципрофлоксацин, альфузозин и ЭППП. Ремиссию заболевания наблюдали у 94% больных, стойкий эффект сохранялся в течение 30 месяцев наблюдения.
В отдельном исследовании K. Stamatiou и N. Pierris разделили 56 больных ХП на 2 группы. Первая в течение 15 дней получала прулифлоксацин в дозе 600 мг, больные второй группы в течение 8 недель дополнительно принимали ЭППП. У больных, получавших ЭППП, по сравнению с пациентами первой группы, наблюдали полное исчезновение болевого синдрома, СНМП и статистически недостоверную эрадикацию всех возбудителей.
G. Busetto c cоавт. провели исследование на 210 больных с бактериальным простатитом, половина которых принимала только прулифлоксацин в дозе 600 мг в течение 21 дня, а другой группе пациентов дополнительно был назначен ЭППП в дозе 320 мг/сут., Lactobacillus Sporogenes (200 мг) и арбутин (100 мг). Оказалось, что через два месяца наблюдения у больных первой группы биологический рецидив заболевания составил 27,6%, а второй – 7,8%. У больных второй группы, согласно опроснику NIH-CPSI, через 6 месяцев после окончания терапии была меньшая выраженность СНМП. Этот показатель в первой группе был 13,25, а второй – лишь 3,67 балла. Таким образом, комбинация антибактериальной терапии с ЭППП, к которым относится и Пермиксон, улучшает течение и симптоматику ХП и снижает вероятность рецидива заболевания.
Особый интерес вызывает опубликованный в 2016 г. G. Novara и соавт. систематический обзор и метаанализ всех рандомизированных клинических исследований (РКИ) применения Пермиксона при ДГПЖ и СНМП с использованием баз данных Medline, Scopus и Web of Science. Авторами выполнен поиск по термину «Serenoa repens» во всех рубриках. Отбору подлежали только РКИ, в которых изучали эффективность и безопасность препарата Пермиксон при лечении СНМП/ДГПЖ. В рамках систематического поиска было выделено 12 РКИ: в 7 исследованиях сравнивали препарат Пермиксон и плацебо; в 2 исследованиях сравнивали Пермиксон и тамсулозин; в 2 исследованиях Пермиксон в комбинации с тамсулозином сравнивали, соответственно, с плацебо в комбинации с тамсулозином и с тамсулозином в виде монотерапии; еще в 1 исследовании провели сравнительную оценку препаратов Пермиксон и финастерида.
Оказалось, что в сравнении с плацебо Пермиксон значительно более эффективно сокращал частоту ночных мочеиспусканий (взвешенная разность средних значений – WMD – 0,31; p = 0,03) и увеличивал максимальную скорость потока мочи (Qmax; WMD 3,37; p < 0,0001). Для препарата Пермиксон и плацебо были получены сопоставимые показатели общей частоты нежелательных явлений (отношение шансов – ОШ 1,12; p = 0,92) и выбывания из исследования (ОШ 1,52; p = 0,60).
Пермиксон продемонстрировал аналогичную эффективность в сравнении с тамсулозином, применяемым в виде монотерапии и финастеридом, применяемым в виде краткосрочной терапии, с точки зрения улучшения балла по шкале IPSS (WMD 1,15; 95% доверительный интервал – ДИ 1,11–3,40; p = 0,32) и показателей Qmax (WMD 0,16; 95% ДИ 0,60–0,28; p = 0,48). В сравнении с монотерапией тамсулозином комбинация Пермиксона и тамсулозина показала более высокую эффективность с точки зрения улучшения СНМП (WMD 0,31; 95% ДИ 0,13–0,48; p < 0,01), но не показателей Qmax (WMD 0,10; 95% ДИ -0,02–0,21; p = 0,10). Препарат Пермиксон продемонстрировал благоприятный профиль безопасности, оказав крайне ограниченное влияние на нарушение эякуляции в сравнении с тамсулозином (0,5 и 4% соответственно, p = 0,007) и снижение либидо и потенции в сравнении с краткосрочной терапией финастеридом (2,2 и 1,5% в сравнении с 3 и 2,8% соответственно).
Был сделан вывод, что препарат Пермиксон сокращал частоту ночных мочеиспусканий и улучшал показатели Qmax в сравнении с плацебо, а также не уступал по эффективности тамсулозину и краткосрочной терапии финастеридом с точки зрения улучшения СНМП. Более того, он продемонстрировал благоприятный профиль безопасности, оказав весьма ограниченное влияние на сексуальную функцию, показатели которой в значительной степени зависят от всех лекарственных препаратов, используемых для лечения СНМП/ДГПЖ. Кроме того, авторы считают, что исследования, в которых выражают сомнение об эффективности экстрактов плодов пальмы ползучей при лечении СНМП/ДГПЖ, не распространяются на препарат Пермиксон.
Заключение
Пермиксон является эффективным и безопасным средством патогенетической терапии ДГПЖ, воздействующим на ряд факторов развития и прогрессирования этого заболевания. Он обладает тройным действием на ПЖ: антиандрогенным, противовоспалительным и антипролиферативным. Вместе с тем мы считаем, что о патогенетическом действии препарата можно говорить лишь с позиций его длительного применения, с учетом времени, необходимого для клинической реализации эффекта ингибирования 5α-редуктазы. При проведении коротких курсов терапии Пермиксоном на первый план, вероятно, выступает его противовоспалительное и противоотечное действие. В многочисленных исследованиях отмечено статистически достоверное воздействие препарата на симптомы и клинические проявления ДГПЖ в сравнении с плацебо и другими лекарственными средствами.
Способность влиять на патогенез ДГПЖ на нескольких уровнях определяет место препарата Пермиксон и позволяет выделить группы больных, предпочтительные для такого лечения:
- Больные с умеренной выраженностью симптомов заболевания (IPSS < 18) и уродинамических нарушений (Qmax > 10 мл/с). Им может быть рекомендована длительная (многомесячная) терапия препаратом Пермиксон с целью предотвращения дальнейшего прогрессирования симптомов ДГПЖ, с оценкой результатов лечения через 10–12 месяцев.
- Больные с манифестной симптоматикой (IPSS > 18) и умеренной выраженностью уродинамических нарушений (Qmax > 10 мл/с). Если через 3–6 месяцев лечения препаратом Пермиксон не наступило существенного симптоматического улучшения, необходимо рассмотреть вопрос об изменении проводимой медикаментозной терапии.
- Больные гиперплазией ПЖ в сочетании с хроническим простатитом. Терапия препаратом Пермиксон возможна в комплексе с антибактериальными и/или противоспалительными препаратами и физиотерапией. В этом случае Пермиксон назначают с учетом его противовоспалительного и противоотечного действия. После стихания явлений хронического простатита тактику дальнейшего лечения определяют так же, как в группах 1 и 2.
- Больные относительно молодого возраста с сохранной половой функцией и клиническими признаками хронического простатита. Использование препарата Пермиксон в качестве элемента комбинированной медикаментозной терапии, в первую очередь совместно с α1-адреноблокаторами и антибиотиками, позволяет улучшить результаты лечения.
Показано, что эффективность Пермиксона возрастает с продолжительностью лечения, которое должно быть рассчитано не менее 4–6 месяцев), а то и годы. С одной стороны, это необходимо учитывать специалистам, планирующим лечение препаратом Пермиксон, а с другой – на это надо ориентировать и пациентов при обсуждении с ними программы медикаментозной терапии ДГПЖ.
Препарат практически не имеет противопоказаний, не влияет на уровень ПСА и не затрудняет диагностику рака ПЖ. Не описано случаев его взаимодействия с другими лекарственными средствами, что расширяет возможности применения Пермиксона у лиц пожилого возраста с отягощенным соматическим статусом.
Тематики и теги
Действующее вещество : 1 таблетка содержит липидостеролового экстракта плодов Serenoa repens (с содержанием свободных и / или этерифицированных жирных кислот (97%) и фракции неомыляемые веществ (3%)) 80 мг
Вспомогательные вещества : магния карбонат, кремния диоксид коллоидный, каолин, крахмал пшеничный, казеин метилированный, повидон, магния стеарат, гипромеллоза, гидроксипропилцеллюлоза, полиэтиленгликоль 400, титана диоксид (Е 171), индиготин (Е 132), хинолин желтый (Е 104 ).
Таблетки, покрытые пленочной оболочкой.
Основные физико-химические свойства: таблетки зеленого цвета.
Средства, применяемые при доброкачественной гипертрофии предстательной железы.
Код АТХ G04C X02.
Фармакологические.
Липидостероловий экстракт плодов Serenoa repens обладает противовоспалительными, антиандрогенные и антипролиферативные свойства и используется для лечения доброкачественной гипертрофии предстательной железы.
Противовоспалительные свойства проявляются вследствие ингибирования:
- фосфолипазы А2 (что приводит к снижению синтеза арахидоновой кислоты)
- циклооксигеназы (что приводит к снижению синтеза простагландинов)
- липоксигеназы (что приводит к снижению синтеза лейкотриенов).
Это действие на каскад арахидоновой кислоты и некоторые воспалительные цитокины объясняет противовоспалительной активностью Serenoa repens , отмеченную как на экспериментальных моделях у животных, так и у больных доброкачественной гипертрофии предстательной железы.
Антиандрогенная активность проявляется преимущественно вследствие ингибирования 5α-редуктазы — фермента, который трансформирует тестостерон в его активный метаболит дигидротестостерон (ДГТ). Эта антиандрогенная активность также усиливается вследствие снижения пролактинзалежного проникновения тестостерона в клетки, ингибирование Эстрогензависимые формирования андрогенных рецепторов и, наконец, ингибирование связывания ДГТ с его рецепторами.
Антиандрогенная активность Serenoa repens была подтверждена на экспериментальных моделях доброкачественной гипертрофии предстательной железы у крыс.
Антипролиферативные свойства объясняются тем, что липидостероловий экстракт плодов Serenoa repens замедляет пролиферацию железистого эпителия (исходя из пролиферативного индекса, оцененного по включением тимидина, меченного изотопом трития), вызванной факторами роста в органотипичних культурах клеток предстательной железы человека.
Serenoa repens снижает синтез белков в культурах клеток предстательной железы, который стимулирует комбинация тестостерона и пролактина (последний принимает участие в регулировании объема предстательной железы).
Фармакокинетика.
Поскольку действующее вещество препарата является растительным экстрактом, который содержит смесь многих компонентов, проведение традиционных фармакокинетических исследований на людях невозможно.
Симптоматическое лечение умеренных расстройств мочеиспускания, вызванных доброкачественной гипертрофией предстательной железы.
Повышенная чувствительность к действующему веществу или к любым другим компонентам препарата.
Аллергические реакции на пшеничный крахмал (кроме непереносимости глютена).
Экспериментальные исследования не выявили клинически значимого взаимодействия Пермиксон с другими препаратами, которые применяются при лечении доброкачественной гипертрофии предстательной железы (такими, как антибиотики для лечения инфекций мочевого тракта, антисептики и противовоспалительные средства).
При приеме лекарственных средств с антикоагулянтной или антитромботической действием следует учесть, что Serenoa repens теоретически может продлить время кровотечения.
Исследования in vitro продемонстрировали отсутствие ингибиторных и индукционных свойств липидостеролового экстракта плодов Serenoa repens .
Фармакокинетические взаимодействия с другими лекарственными средствами не ожидается.
Перед применением препарата необходимо проконсультироваться с врачом.
Превышать рекомендуемую дозу.
Прием препарата натощак может вызвать тошноту.
Применение плодов Serenoa repens пациентам с печеночной и почечной недостаточностью не исследовался.
Препарат предназначен только для лечения медико подтвержденной доброкачественной гипертрофии предстательной железы. При ухудшении симптомов заболевания следует обратиться к врачу.
При появлении гематурии или повышении температуры тела следует немедленно обратиться к врачу.
Препарат Пермиксон могут принимать больные целиакией. Хотя пшеничный крахмал и может содержать глютен, но в таком незначительном количестве, что его прием считается безопасным для пациентов с непереносимостью глютена.
Применение в период беременности или кормления грудью.
Пермиксон не предназначен для лечения женщин.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами.
Не влияет на скорость психомоторных реакций.
Препарат принимают внутрь по 4 таблетки в сутки во время еды, запивая стаканом воды.
Продолжительность лечения определяет врач индивидуально.
Дети.
Препарат предназначен для лечения детей.
Отсутствуют данные о случаях передозировки у людей. Возможно усиление проявлений побочных реакций со стороны пищеварительного тракта.
Лечение симптоматическое.
Ниже приведена информация по нежелательных эффектов, возможно, вызванных Пермиксон, полученную во время 7 клинических исследований, в которые были включены 2127 пациентов, а также в течение постмаркетинговых наблюдений.
В зависимости от частоты побочных реакций разделены на следующие категории: очень часто (≥ 1/10), часто (≥ 1/100, <1/10), нечасто (≥ 1/1000, <1/100), редко (≥ 1 / 10000, <1/1000), единичные (<1/10000), частота неизвестна (имеющиеся данные не позволяют оценить частоту этих реакций).
Со стороны нервной системы
Распространены головная боль.
Со стороны пищеварительного тракта
Распространены : боль в животе.
Редко : тошнота.
Со стороны пищеварительной системы
Редко : повышение уровня гамма-глутамилтрансферазы (ГГТ), повышение уровня аланинаминотрансферазы (АЛТ) и аспартатаминотрансферазы (АСТ).
Со стороны кожи и подкожных тканей
Редко : кожные высыпания, возможны реакции гиперчувствительности.
Частота неизвестна : отеки.
Со стороны репродуктивной системы и молочных желез
Редко : гинекомастия (оборотная, исчезает после прекращения лечения).
Хранить в недоступном для детей месте при температуре не выше 25 ° C.
По 15 таблеток в блистере. По 4 блистера в картонной упаковке.