Релвар Эллипта (Relvar Ellipta) инструкция по применению
📜 Инструкция по применению Релвар Эллипта
💊 Состав препарата Релвар Эллипта
✅ Применение препарата Релвар Эллипта
📅 Условия хранения Релвар Эллипта
⏳ Срок годности Релвар Эллипта
Описание лекарственного препарата
Релвар Эллипта
(Relvar Ellipta)
Основано на официальной инструкции по применению препарата, утверждено компанией-производителем
и подготовлено для электронного издания справочника Видаль 2018
года, дата обновления: 2018.07.31
Код ATX:
R03AK10
(Вилантерол и флутиказона фуроат)
Лекарственные формы
| Релвар Эллипта |
Порошок д/ингаляций дозированный, 22 мкг+184 мкг/1 доза: ингалятор 30 доз рег. №: ЛП-002451 |
|
|
Порошок д/ингаляций дозированный, 22 мкг+92 мкг/1 доза: ингалятор 30 доз рег. №: ЛП-002451 |
Форма выпуска, упаковка и состав
препарата Релвар Эллипта
Порошок для ингаляций дозированный 22 мкг+92 мкг/доза белого цвета.
Стрип с вилантеролом (30 ячеек)
Вспомогательные вещества: магния стеарат — 125 мкг, лактозы моногидрат — до 12.5 мг.
Стрип с флутиказона фуроатом (30 ячеек)
Вспомогательные вещества: лактозы моногидрат — до 12.5 мг.
30 доз — ингаляторы пластиковые со счетчиком доз (1) с двумя стрипами алюминиевыми ламинированными (каждый по 30 ячеек) — контейнеры многослойные из фольги алюминиевой (1) с легко открывающейся крышкой — пачки картонные.
Порошок для ингаляций дозированный 22 мкг+184 мкг/доза белого цвета.
Стрип с вилантеролом (30 ячеек)
Вспомогательные вещества: магния стеарат — 125 мкг, лактозы моногидрат — до 12.5 мг.
Стрип с флутиказона фуроатом (30 ячеек)
Вспомогательные вещества: лактозы моногидрат — до 12.5 мг.
30 доз — ингаляторы пластиковые со счетчиком доз (1) с двумя стрипами алюминиевыми ламинированными (каждый по 30 ячеек) — контейнеры многослойные из фольги алюминиевой (1) с легко открывающейся крышкой — пачки картонные.
* при производстве готового препарата смеси действующих и вспомогательных веществ могут закладываться в конечный продукт с избытком до 8% для компенсации потерь при наполнении ячеек.
** указано номинальное количество действующего вещества, закладываемое в процессе производства.
Фармакологическое действие
Механизм действия
Вилантерол и флутиказона фуроат относятся к двум различным классам лекарственных препаратов — синтетический глюкокортикоид и селективный бета2-адреномиметик длительного действия.
Фармакодинамические эффекты
Вилантерола трифенатат относится к классу селективных бета2-адреномиметиков длительного действия (ДДБА).
Фармакологические эффекты агонистов β2-адренорецепторов, включая вилантерола трифенатат, по крайней мере, частично связаны со стимуляцией внутриклеточной аденилатциклазы — фермента, который катализирует превращение аденозинтрифосфата (АТФ) в циклический 3′,5′-аденозинмонофосфат (циклический АМФ). Повышение уровня циклического АМФ приводит к расслаблению гладкой мускулатуры бронхов и угнетению высвобождения из клеток (в первую очередь из тучных клеток) медиаторов реакций гиперчувствительности немедленного типа.
Флутиказона фуроат является синтетическим трехфтористым глюкокортикоидом с выраженным противовоспалительным действием. Точный механизм действия, позволяющий купировать симптомы бронхиальной астмы и хронической обструктивной болезни легких (ХОБЛ), неизвестен. Глюкокортикоиды продемонстрировали широкий спектр действия на различные типы клеток (например, эозинофилы, макрофаги, лимфоциты) и медиаторы (например, цитокины и хемокины, участвующие в процессе воспаления).
Между глюкокортикоидами и ДДБА происходят молекулярные взаимодействия, в результате которых стероидные гормоны активируют ген β2-адренорецептора, повышая число восприимчивых адренорецепторов. ДДБА связываются с глюкокортикоидным рецептором, обеспечивая его стероидозависимую активацию и стимулируя транслокацию в ядро клетки. Эти синергические взаимодействия приводят к усилению противовоспалительной активности, что было продемонстрировано в экспериментах in vitro и in vivo с различными клетками воспаления, участвующими в патофизиологических процессах развития бронхиальной астмы и ХОБЛ. Результаты клинических исследований с использованием биоптатов дыхательных путей также продемонстрировали синергию глюкокортикоидов и ДДБА, возникающую при назначении этих препаратов пациентам с ХОБЛ в терапевтических дозах.
Фармакокинетика
Всасывание
Абсолютная биодоступность вилантерола и флутиказона фуроата при ингаляционном введении комбинации вилантерола и флутиказона фуроата составила в среднем 27.3% и 15.2% соответственно. Пероральная биодоступность вилантерола и флутиказона фуроата была низкой, и в среднем составляла <2% и 1.26% соответственно. Принимая во внимание низкую пероральную биодоступность, системное действие вилантерола и флутиказона фуроата после ингаляционного приема в первую очередь обусловлено всасыванием части ингаляционной дозы, поступившей в легкие.
Распределение
После в/в введения вилантерол и флутиказона фуроат активно распределяются в организме, при этом средние Vd в равновесном состоянии составляют 165 л и 661 л соответственно.
Оба вещества — вилантерол и флутиказона фуроат — обладают низкой способностью связываться с эритроцитами. В исследованиях in vitro связывание вилантерола и флутиказона фуроата с белками плазмы человека было высоким и достигало в среднем 93.9% и >99.6% соответственно. Степень связывания с белками плазмы in vitro не уменьшалась у пациентов с нарушениями функции печени или почек.
Несмотря на то, что вилантерол и флутиказона фуроат являются субстратами Р-гликопротеина (P-gp), при одновременном введении комбинации вилантерола и флутиказона фуроата с ингибиторами P-gp изменение системной экспозиции вилантерола или флутиказона фуроата считается маловероятным, т.к. оба вещества обладают хорошей абсорбционной способностью.
Метаболизм
На основании данных in vitro экспериментов можно заключить, что основные пути метаболизма вилантерола и флутиказона фуроата в организме человека в первую очередь опосредованы изоферментом CYP3A4.
Вилантерол преимущественно метаболизируется путем О-деалкилирования с образованием ряда метаболитов, обладающих существенно более низкой бета1— и бета2-адреномиметической активностью.
Флутиказона фуроат преимущественно метаболизируется путем гидролиза S-фторметилкарботиоатной группы с образованием метаболитов, имеющих значительно более низкую глюкокортикоидную активность.
Было проведено клиническое исследование лекарственных взаимодействий препарата с изоферментом цитохрома CYP3A4 при непрерывном введении комбинации вилантерола и флутиказона фуроата (22 мкг+184 мкг/доза) и сильного ингибитора изофермента цитохрома CYP3A4 — кетоконазола (400 мг) на примере здоровых добровольцев. Введение комбинации вилантерола и флутиказона фуроата привело к увеличению средней AUC(0-24) и средней Cmax флутиказона фуроата на 36% и 33% соответственно. Увеличение экспозиции флутиказона фуроата было ассоциировано со снижением средней концентрации сывороточного кортизола на 27%, измеренного за период 0-24 ч.
Введение комбинации вилантерола и флутиказона фуроата и кетоконазола привело к увеличению средних значений AUC(0-t) и Cmax вилантерола на 65% и 22% соответственно. Увеличение экспозиции вилантерола не приводило к усилению характерных для бета-агонистов системных эффектов в отношении ЧСС, содержания калия в крови или корригированного интервала QT (QTcF).
Выведение
После перорального приема флутиказона фуроат в организме человека метаболизировался, главным образом с образованием метаболитов, которые преимущественно выводились через ЖКТ, за исключением дозы радиоактивного вещества <1%, выведенной с мочой. T1/2 из плазмы флутиказона фуроата после ингаляционного приема препарата составлял в среднем 24 ч.
После перорального приема вилантерол в организме человека главным образом метаболизировался с образованием метаболитов, которые экскретировались с мочой и фекалиями, в соотношении приблизительно 70% и 30% дозы радиоактивного вещества, соответственно. T1/2 из плазмы вилантерола после ингаляционного приема комбинации вилантерола и флутиказона фуроата составлял в среднем 2.5 ч.
Особые группы пациентов
В ходе третьей фазы клинических исследований проводился популяционный мета-анализ фармакокинетики вилантерола и флутиказона фуроата у пациентов с бронхиальной астмой и ХОБЛ. В рамках популяционного фармакокинетического анализа оценивалось влияние демографических ковариат (возраст, пол, вес, ИМТ, расовая и этническая принадлежность) на фармакокинетику вилантерола и флутиказона фуроата.
Раса
Пациенты с бронхиальной астмой и ХОБЛ восточноазиатского, японского и юго-восточноазиатского происхождения (12–14% пациентов) имели в среднем более высокие показатели AUC(0–24) (выше не более чем на 53%) в сравнении с пациентами европеоидной расы. Тем не менее, в этих популяциях не обнаружено признаков более высокой системной экспозиции, связанной с более выраженным влиянием на экскрецию кортизола с мочой за 24-часовой период. У пациентов, страдающих ХОБЛ, влияние расовой принадлежности на фармакокинетические параметры вилантерола не выявлено.
В среднем, по результатам оценки Cmax вилантерола была на 220-287% выше, a AUC(0-24) была сопоставима у пациентов азиатского происхождения по сравнению с показателями у других расовых групп. Тем не менее, более высокая Cmax вилантерола не имела клинически значимого влияния на ЧСС.
Дети
Для подростков (12 лет или старше) рекомендации но изменению режима дозирования отсутствуют.
Фармакокинетика комбинации вилантерола и флутиказона фуроата у пациентов младше 12 лет не изучалась. Безопасность и эффективность применения комбинации вилантерола и флутиказона фуроата у детей младше 12 лет пока не установлена.
Пациенты пожилого возраста
Влияние возраста на фармакокинетику вилантерола и флутиказона фуроата изучалось в третьей фазе клинических исследований, включавших пациентов с ХОБЛ и бронхиальной астмой.
У пациентов с бронхиальной астмой, не было обнаружено признаков влияния возраста (12-84 лет) на фармакокинетический профиль флутиказона фуроата и вилантерола.
Несмотря на увеличение (37%) AUC(0-24) вилантерола у пациентов с ХОБЛ на протяжении всего наблюдаемого возрастного диапазона от 41 до 84 лет, признаков влияния возраста пациентов на фармакокинетический профиль флутиказона фуроата не выявлено. У пожилого пациента (в возрасте 84 года) с низкой массой тела (35 кг) AUC(0-24) вилантерола ожидается на 35% выше результата, рассчитанного для популяции (в среднем, пациент с ХОБЛ в возрасте 60 лет и массой тела 70 кг), в то время как Cmax вилантерола останется неизмененной. Маловероятно, что эти различия являются клинически релевантными.
Пациенты с нарушением функции почек
По данным клинико-фармакологического исследования для вилантерола и флутиказона фуроата тяжелое нарушение функции почек (КК <30 мл/мин) не приводит к значительному увеличению системной экспозиции вилантерола или флутиказона фуроата или к развитию более выраженных системных эффектов глюкокортикостероидов или бета2-агонистов в сравнении со здоровыми добровольцами. Коррекции дозы для пациентов с нарушением функции почек не требуется.
Влияние гемодиализа не изучалось.
Пациенты с нарушением функции печени
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени (согласно классификации цирроза печени по Чайлд-Пью: стадии цирроза А, В или С) наблюдалось увеличение системной экспозиции флутиказона фуроата (по измеренной AUC(0–24) до трех раз) в сравнении со здоровыми добровольцами. Повышение системной экспозиции флутиказона фуроата (при назначении комбинации вилантерола и флутиказона фуроата в дозировке 22 мкг+184 мкг/доза) у пациентов с нарушением функции печени средней степени (стадия В по классификации Чайлд-Пью) было ассоциировано со снижением концентрации сывороточного кортизола в среднем на 34% в сравнении со здоровыми добровольцами. У пациентов с нарушением функции печени тяжелой степени (стадия С по классификации Чайлд-Пью), получавших более низкую дозу 11 мкг+92 мкг, не наблюдалось снижения концентрации сывороточного кортизола. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22 мкг+92 мкг.
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени легкой, средней или тяжелой степени (стадии А, В и С по классификации Чайлд-Пью) не отмечалось значительного увеличения системной экспозиции вилантерола (по Cmax и AUC).
В сравнении со здоровыми добровольцами пациентов с нарушением функции печени легкой или средней степени (принимавших вилантерол в дозе 22 мкг) или тяжелой степени (принимавших вилантерол в дозе 11 мкг) не наблюдалось клинически значимых бета-адренергических системных эффектов (изменение ЧСС или концентрации сывороточного калия), вызванных приемом комбинации вилантерола и флутиказона фуроата.
Пол, масса тела, ИМТ
Согласно результатам популяционного фармакокинетического анализа данных третьей фазы клинических исследований, включавшей 1213 пациентов с бронхиальной астмой (712 женщин) и 1225 пациентов с ХОБЛ (392 женщины), признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль флутиказона фуроата не обнаружено.
По данным популяционного анализа фармакокинетики с участием 856 пациентов с бронхиальной астмой (500 женщин) и 1091 пациента с ХОБЛ (340 женщин) признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль вилантерола не обнаружено.
Не требуется коррекции дозы на основании данных о половой принадлежности, массе тела или ИМТ.
Показания препарата
Релвар Эллипта
- бронхиальная астма (в качестве поддерживающей терапии);
- ХОБЛ (в качестве поддерживающей терапии обструкции дыхательных путей у пациентов с ХОБЛ, включая хронический бронхит и/или эмфизему легких). Применение препарата Релвар Эллипта позволяет сократить число обострений ХОБЛ у пациентов с повторными обострениями в анамнезе.
Режим дозирования
Препарат Релвар Эллипта предназначен только для ингаляционного применения.
Препарат Релвар Эллипта следует применять 1 раз/сут в одно и то же время, утром или вечером.
После ингаляции следует прополоскать рот водой, не проглатывая.
Бронхиальная астма
Пациент должен быть проинформирован о необходимости регулярного применения препарата Релвар Эллипта даже в случае бессимптомного течения заболевания.
При возникновении симптомов заболевания в период между приемами препарата в качестве неотложной терапии следует применять ингаляционные формы бета2-агонистов короткого действия.
Врач должен регулярно оценивать состояние пациента, чтобы обеспечить своевременное назначение оптимальной дозы препарата Релвар Эллипта. Доза может быть изменена только по рекомендации врача.
Взрослые и подростки 12 лет и старше
Рекомендуемая доза препарата Релвар Эллипта:
- 1 ингаляция 22 мкг+92 мкг 1 раз/сут
или
- 1 ингаляция 22 мкг+184 мкг 1 раз/сут.
Начальная доза препарата Релвар Эллипта 22 мкг+92 мкг назначается пациентам, которым требуются низкие или средние дозы ингаляционных глюкокортикоидов, применяемых в комбинации с бета2-агонистами длительного действия.
Препарат Релвар Эллипта в дозировке 22 мкг+184 мкг следует назначать пациентам, которым требуется более высокая доза ингаляционных ГКС, применяемых в комбинации с бета2-агонистами длительного действия.
Если препарат Релвар Эллипта в дозировке 22 мкг+92 мкг не обеспечивает адекватного контроля заболевания, рассматривается вопрос об увеличении дозы до 22 мкг+184 мкг, что может улучшить уровень контроля над течением бронхиальной астмы.
Дети
Безопасность и эффективность применения препарата Релвар Эллипта у детей младше 12 лет не установлена.
ХОБЛ
Взрослые
Рекомендуемая доза препарата Релвар Эллипта 1 ингаляция 22 мкг+92 мкг 1 раз/сут.
Препарат Релвар Эллипта в дозировке 22 мкг+184 мкг не показан для лечения пациентов с ХОБЛ.
Дети
Препарат по показанию ХОБЛ у детей не применяется.
Особые группы пациентов
Пациентам пожилого возраста (старше 65 лет) не требуется коррекция дозы препарата.
Пациентам с нарушением функции почек не требуется коррекция дозы препарата.
По данным клинико-фармакологического исследования у пациентов с нарушениями функции печени легкой, средней и тяжелой степени наблюдается трехкратное возрастание степени системной экспозиции флутиказона фуроата (AUC). Препарат следует назначать с осторожностью пациентам с нарушениями функции печени, у которых риск развития системных нежелательных реакций, вызванных приемом ГКС, более высок. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22 мкг+92 мкг.
Рекомендации по применению
При первом использовании ингалятора Эллипта нет необходимости в проверке правильности его работы или специальной подготовки ингалятора к эксплуатации. Просто необходимо последовательно соблюдать рекомендации но применению.
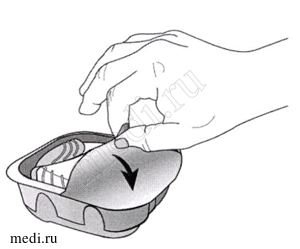
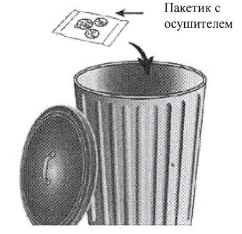
Ингалятор Эллипта упакован в контейнер. Не открывайте контейнер до тех пор, пока не будете готовы осуществить ингаляцию лекарственного препарата. Когда будете готовы использовать ингалятор, снимите крышку с контейнера. Контейнер содержит пакетик с осушителем для снижения влажности. Не вскрывайте пакетик, он не предназначен для еды или ингаляций, его следует выбросить.
Когда Вы достаете ингалятор из контейнера, его крышка находится в закрытом положении. Не открывайте ее до тех пор, пока Вы не будете готовы к приему препарата.
В специально отведенном поле «Использовать до» на этикетке ингалятора напишите дату, которая будетсоответствовать дате вскрытия плюс 6 недель. Не следует использовать ингалятор после этой даты.
Ниже приведены пошаговые инструкции использования ингалятора Эллипта:
I. Прочитайте следующую информацию перед использованием
При открытии и закрытии крышки ингалятора Эллипта без приема лекарственного препарата происходит потеря одной дозы. Эта доза остается закрытой внутри ингалятора, но она будет недоступна для приема. Невозможно случайно получить большую дозу или двойную дозу за одну ингаляцию.
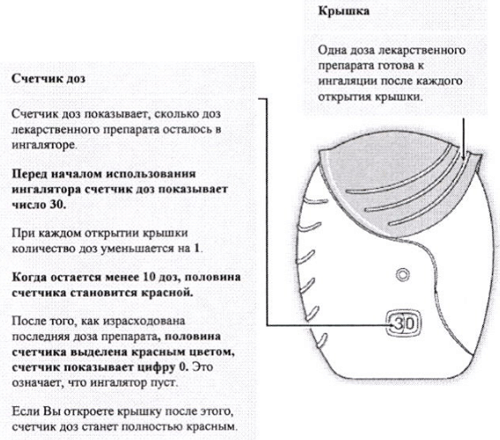
Одна доза лекарственного препарата готова к ингаляции после каждого открытия крышки.
Счетчик доз показывает, сколько доз лекарственного препарата осталось в ингаляторе.
Перед началом использования ингалятора счетчик доз показывает число 30.
При каждом открытии крышки количество доз уменьшается на 1.
Когда остается менее 10 доз, половина счетчика становится красной.
После того, как израсходована последняя доза препарата, половина счетчика выделена красным цветом, счетчик показывает цифру 0. Это означает, что ингалятор пуст.
Если Вы откроете крышку после этого, счетчик доз станет полностью красным.
II. Подготовка дозы
Не открывайте крышку, пока Вы не будете готовы к приему препарата. Не встряхивайте ингалятор.
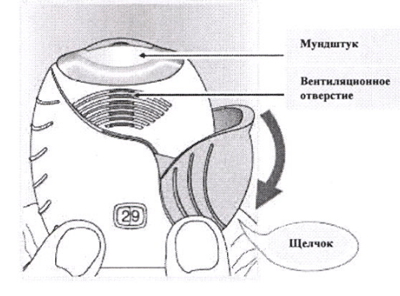
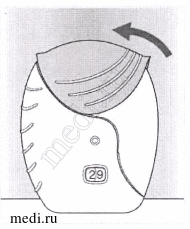
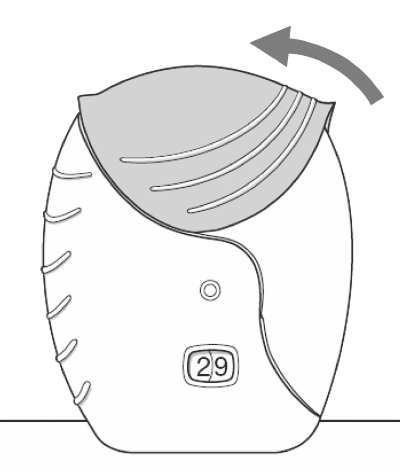
1. Опустите крышку вниз до щелчка.
2. Доза препарата готова к ингаляция, и в подтверждение этого счетчик доз уменьшает число доз на единицу.
3. Если счетчик доз не уменьшил число доз после того, как Вы услышали щелчок, то ингалятор не готов к подаче дозы лекарственного препарата. В этом случае следует обратиться по телефону или адресу, указанному в разделе «За дополнительной информацией обращаться».
4. Никогда не встряхивайте ингалятор.
III. Ингаляция лекарственного препарата
1. Удерживая ингалятор на некотором расстоянии ото рта. сделайте выдох максимальной глубины. Не выдыхайте в ингалятор.
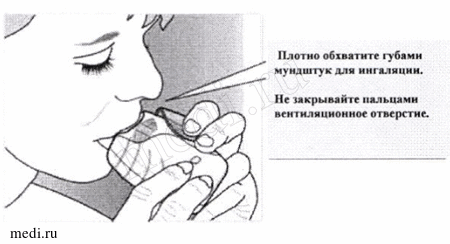
2. Поместите мундштук между губами и плотно обхватите его губами. Не закрывайте пальцами вентиляционное отверстие.
3. Сделайте один глубокий, долгий, равномерный вдох через рот. Задержите дыхание насколько возможно (по крайней мере, на 3—4 сек).
4. Уберите ингалятор изо рта.
5. Медленно и спокойно выдохните.
Вы можете не почувствовать вкус или не ощутить поступление лекарственного препарата даже при правильном использовании ингалятора.
IV. Закрытие ингалятора и полоскание ротовой полости
Если Вы хотите протереть мундштук, используйте сухую салфетку перед закрытием крышки.
1. Поднимите крышку до упора, добившись полного закрытия мундштука.
2. После ингаляции следует прополоскать рот водой. Это снизит вероятность развития таких побочных явлений, как боль в горле и полости рта.
При хранении в холодильнике ингалятор следует выдержать при комнатной температуре не менее часа перед использованием.
Побочное действие
Для определения частоты развития нежелательных реакций, связанных с приемом препарата Релвар Эллипта, использовались данные крупных клинических исследований среди пациентов с ХОБЛ и бронхиальной астмой. Программа клинической разработки препарата для лечения бронхиальной астмы включала 7034 пациента, у которых проводилась комплексная оценка нежелательных реакций. В программе клинической разработки препарата для лечения ХОБЛ принимали участие 6237 пациентов, у которых проводилась комплексная оценка нежелательных реакций.
Исключая пневмонию и переломы, профили безопасности препарата у пациентов с ХОБЛ и бронхиальной астмой были схожи. По данным клинических исследований пневмония и переломы более часто наблюдались у пациентов, страдающих ХОБЛ.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости, согласно классификации ВОЗ определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и <1/10), нечасто (≥1/1000 и <1/100), редко (≥1/10 000 и <1/1000), очень редко (<1/10 000, включая отдельные случаи).
Частота встречаемости нежелательных реакций
Инфекционные и паразитарные заболевания: часто — пневмония, инфекции верхних дыхательных путей, бронхит, грипп, кандидоз полости рта и глотки.
Со стороны нервной системы: очень часто — головная боль.
Со стороны сердечно-сосудистой системы: нечасто — экстрасистолия.
Со стороны дыхательной системы: очень часто — назофарингит; часто — орофарингеальная боль, синусит, фарингит, ринит, кашель, дисфония.
Со стороны пищеварительной системы: часто — боль в животе.
Со стороны костно-мышечной системы: часто — артралгия, боль в спине, переломы.
Общие расстройства и нарушения в месте введения: часто — лихорадка.
Данные пострегистрационного наблюдения
Со стороны иммунной системы: редко — реакции гиперчувствительности, в т.ч. анафилаксия, ангионевротический отек, сыпь, крапивница.
Нарушения психики: редко — тревожность.
Со стороны нервной системы: редко — тремор.
Со стороны сердечно-сосудистой системы: редко — учащенное сердцебиение, тахикардия.
Со стороны дыхательной системы: редко — парадоксальный бронхоспазм.
Со стороны костно-мышечной системы: часто — мышечный спазм.
Противопоказания к применению
- пациентам, имеющим в анамнезе тяжелые аллергические реакции на молочный белок или повышенную чувствительность к действующим веществам или любому другому компоненту, входящему в состав препарата;
- детям до 12 лет для лечения бронхиальной астмы;
- препарат Релвар Эллипта в дозе 22 мкг+184 мкг/доза не показан для лечения ХОБЛ.
С осторожностью: при приеме симпатомиметиков, включая препарат Релвар Эллипта, со стороны сердечно-сосудистой системы могут наблюдаться такие нежелательные явления, как аритмия (например, наджелудочковая тахикардия и экстрасистолия). В связи с этим пациентам, страдающим тяжелыми формами сердечно-сосудистых заболеваний, препарат Релвар Эллипта следует назначать с осторожностью.
Как и другие лекарственные средства, в состав которых входят ГКС, препарат Релвар Эллипта следует с осторожностью назначать пациентам с туберкулезом легких, а также пациентам с хроническими или невылеченными инфекциями.
Применение при беременности и кормлении грудью
Фертильность
Данные по влиянию на фертильность человека отсутствуют. В доклинических исследованиях воздействия вилантерола и флутиказона фуроата на фертильность не обнаружено.
Беременность
Данные о применении препарата во время беременности ограничены.
Применение препарата Релвар Эллипта у беременных женщин допустимо только в том случае, если потенциальная польза для матери превышает возможный риск для плода.
Период грудного вскармливания
Данных об экскреции вилантерола или флутиказона фуроата или их метаболитов в грудное молоко человека недостаточно. Однако другие глюкокортикоиды и бета2-агонисты определяются в грудном молоке. Риск проникновения препарата вместе с молоком в организм новорожденного или ребенка не может быть исключен.
Принимая во внимание соотношение пользы терапии для матери и грудного вскармливания для ребенка, необходимо решить вопрос либо об отмене препарата, либо о прекращении грудного вскармливания.
Применение при нарушениях функции печени
Препарат следует назначать с осторожностью пациентам с нарушениями функции печени, у которых риск развития системных нежелательных реакций, вызванных приемом глюкокортикостероидов, более высок.
Применение при нарушениях функции почек
Пациентам с нарушением функции почек не требуется индивидуальный подбор дозы препарата.
Применение у детей
Применение препарата детям в возрасте до 12 лет противопоказано.
Применение у пожилых пациентов
Пациентам старше 65 лет не требуется индивидуальный подбор дозы препарата.
Особые указания
Обострения
Препарат Релвар Эллипта не предназначен для купирования острых симптомов бронхиальной астмы или обострения ХОБЛ, в таких случаях требуется назначение бронходилататоров короткого действия. Увеличение частоты приема бронходилататоров короткого действия с целью купирования симптомов свидетельствует об ухудшении контроля над заболеванием и необходимости консультации врача.
Пациентам с бронхиальной астмой или ХОБЛ не следует прекращать лечение препаратом Релвар Эллипта без наблюдений врача, т.к. отмена терапии может привести к возобновлению симптомов.
На фоне лечения препаратом Релвар Эллипта могут развиваться нежелательные явления, связанные с течением бронхиальной астмы или обострением заболевания. Пациентам следует рекомендовать продолжить лечение. В случае отсутствия контроля над заболеванием или ухудшения состояния после начала терапии препаратом Релвар Эллипта необходима консультация врача.
Парадоксальный бронхоспазм
Как и при других видах ингаляционной терапии, после приема препарата может развиваться парадоксальный бронхоспазм, сопровождающийся быстрым нарастанием свистящих хрипов. В этом случае показаны неотложное назначение ингаляционного бронходилататора короткого действия и немедленная отмена препарата Релвар Эллипта. Пациент должен быть осмотрен врачом, и ему, при необходимости, может быть назначена альтернативная терапия.
Нарушение функции печени
Пациентам с нарушением функции печени средней и тяжелой степени следует назначать дозу 22 мкг+92 мкг, таким пациентам следует находиться под наблюдением врача для контроля над системными побочными реакциями, связанными с применением ГКС.
Системные эффекты ГКС
При применении ингаляционных ГКС (особенно при длительном приеме в высоких дозах) могут развиваться системные побочные реакции. Такие побочные реакции развиваются значительно реже, чем при пероральном приеме ГКС. К проявлениям возможного неблагоприятного системного действия относятся: подавление функции гипоталамо-гипофизарно-надпочечниковой системы, снижение минеральной плотности костей, замедление скорости роста у детей и подростков, катаракта и глаукома.
Пневмония
У пациентов с ХОБЛ, получающих препарат Релвар Эллипта, наблюдалось повышение частоты развития пневмонии, а также частоты возникновения тяжелых форм пневмонии, требующих госпитализации пациента. В некоторых случаях клинические эпизоды пневмонии имели летальный исход. Врачам следует помнить о возможности развития пневмонии у пациентов с ХОБЛ, не забывая о том, что клинические признаки такого инфекционного заболевания маскируются симптомами обострения ХОБЛ. Более высокий риск развития пневмонии на фоне приема препарата Релвар Эллипта имеют следующие группы пациентов с ХОБЛ: курящие пациенты, пациенты, ранее перенесшие пневмонию, пациенты с ИМТ <25 кг/м2 и пациенты с объемом форсированного выдоха (ОФВ1) <50% от должных величии. При назначении терапии препаратом Релвар Эллипта следует учитывать вышеуказанные факторы, в случае возникновения пневмонии лечение должно быть пересмотрено.
У пациентов с бронхиальной астмой случаи развития пневмонии наблюдались нечасто. Пациенты с бронхиальной астмой, получавшие препарат Релвар Эллипта в дозировке 22 мкг+184 мкг/доза, возможно, имели более высокий риск развития пневмонии в сравнении с пациентами, получавшими более низкую дозу препарата Релвар Эллипта (22 мкг+92 мкг/доза), или с группой плацебо. Факторы риска не установлены.
В ходе проведения клинических исследований у пациентов, страдающих ХОБЛ, была выявлена низкая частота возникновения переломов костей во всех лечебных группах, но при этом во всех группах, получавших комбинацию вилантерола и флутиказона фуроата, она была несколько выше (2%), чем в группе, получавших монотерапию вилантеролом 22 мкг (<1%).
Влияние на способность к управлению транспортными средствами и механизмами
Исследования по изучению влияния препарата Релвар Эллипта на способность к вождению автотранспорта и работе с механизмами не проводились. Исходя из данных фармакологии вилантерола или флутиказона фуроата, неблагоприятное влияние препарата на эти виды деятельности не предполагается.
Передозировка
Симптомы
При проведении клинических исследований не было получено данных о передозировке комбинацией вилантерола и флутиказона фуроата.
Передозировка препарата Релвар Эллипта может вызывать развитие симптомов и признаков, обусловленных действием отдельных компонентов препарата и характерных для передозировки бета2-агонистами и ингаляционными ГКС (см. раздел «Особые указания»).
Лечение
Специфическое лечение передозировки комбинацией вилантерола и флутиказона фуроата отсутствует. В случае развития передозировки назначается симптоматическая терапия и, при необходимости, обеспечивается соответствующее наблюдение за больным.
Применение кардиоселективных бета-адреноблокаторов следует рассматривать только в случаях сильно выраженных эффектов передозировки вилантеролом, которые клинически проявляются невосприимчивостью к поддерживающей терапии. Кардиоселективные бета-адреноблокаторы следует с осторожностью назначать пациентам, у которых наблюдались эпизоды бронхоспазма в анамнезе.
Лекарственное взаимодействие
При назначении препарата в терапевтических дозах клинически значимое лекарственное взаимодействие вилантерола пли флутиказона фуроата считается маловероятным вследствие низких плазматических концентраций последних при ингаляционном введении.
Бета-адреноблокаторы могут ослаблять или антагонизировать действие бета2-адреномиметиков. Следует избегать одновременного приема неселективных и селективных бета-блокаторов, исключая случаи, когда их назначение строго необходимо.
Вилантерол и флутиказона фуроат подвергаются быстрому первичному метаболизму в печени посредством изофермента системы цитохрома CYP3A4. При одновременном назначении препарата с сильными ингибиторами изофермента цитохрома CYP3A4 (например, кетоконазол, ритонавир) следует соблюдать осторожность, поскольку возможно повышение системного воздействия вилантерола и флутиказона фуроата, что в свою очередь может привести к повышению риска развития нежелательных реакций.
Вилантерол и флутиказона фуроат являются субстратами P-gp. По результатам клинико-фармакологического исследования с участием здоровых добровольцев, которым одновременно назначались вилантерол и сильный ингибитор P-gp и умеренный ингибитор изофермента цитохрома CYP3A4 верапамил, значимого влияния на фармакокинетику вилантерола не выявлено. Клинико-фармакологические исследования совместного назначения специфического ингибитора P-gp и флутиказона фуроата не проводились.
Условия хранения препарата Релвар Эллипта
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата Релвар Эллипта
Срок годности не вскрытого алюминиевого контейнера — 2 года; вскрытого алюминиевого контейнера — 6 недель.
Не применять после истечения срока годности, указанного на упаковке.
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ГЛАКСОСМИТКЛЯЙН ТРЕЙДИНГ АО
(Россия)

|
|
125167 Москва |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Релвар Эллипта — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП 002451 — 070217
Торговое наименование препарата:
Релвар Эллипта®.
Группировочиое наименование:
вилантерол + флутиказона фуроат / vilanterol fluticasone furoate.
Лекарственная форма:
порошок для ингаляций дозированный.
Состав на 1 дозу
|
Наименование компонентов |
Количество в одной ячейке , мкг |
|
|
22 мкг + 92 мкг/доза |
22 мкг + 184 мкг/доза |
|
|
Стрип с вилантеролом |
||
|
Действующее вещество: |
||
|
Вилантерола трифенатат микронизированный (в пересчете на вилантерол) |
40 (25)2 |
40 (25)2 |
|
Вспомогательные вещества: |
||
|
Магния стеарат |
125 |
125 |
|
Лактозы моногидрат |
до 12.5 мг |
до 12,5 мг |
|
Стрип с флутиказона фуроатом |
||
|
Действующее вещество: |
||
|
Флутиказона фуроат микронизированный |
1002 |
2002 |
|
Вспомогательное вещество: |
||
|
Лактозы моногидрат |
до 12.5 мг |
до 12.5 мг |
Примечание:
1. При производстве готового препарата смеси действующих и вспомогательных веществ могут закладываться в конечный продукт с избытком до 8 % для компенсации потерь при наполнении ячеек.
2. Указано номинальное количество действующего вещества, закладываемого в процессе производства, доставленное количество составляет 22 мкг вилантерола, 92 мкг и 184 мкг флутиказона фуроата, что соответствует указанным дозировкам.
Описание
Пластиковый ингалятор с корпусом светло серого цвета, бледно-голубой крышкой мундштука и счетчиком доз, упакованный в контейнер из фольги, содержащий пакетик с осушителем. Контейнер запечатан легко открывающейся фольгой. Ингалятор содержит два стрипа, каждый стрип состоит из 30 равномерно распределенных ячеек, каждая из которых содержит порошок белого цвета
Фармакотерапевтическая группа
Бронходилатирующее средство комбинированное (бета2-адреномиметик селективный + глюкокортикостероид местный).
Код АТХ: R03AK10
Фармакологические свойства
Фармакодинамика
Механизм действия
Вилантерол и флутиказона фуроат относятся к двум классам лекарственных средств — синтетический глюкокортикостероид и селективный бета2-адреномиметик .
Фармакодинамические эффекты
Вилантерола трифенатат относится к классу селективных бета2-адреномиметиков длительного действия (ДДБА). Фармакологические эффекты агонистов бета-адренорецепторов, включая вилантерола трифенатат, по крайней мере, частичносвязаны со стимуляцией внутриклеточной аденилатциклазы — фермента, который катализирует превращение аденозинтрифосфата (АТФ) в циклический 3′,5′-аденозинмонофосфат (циклический АМФ). Повышение уровня циклического АМФ приводит к расслаблению гладкой мускулатуры бронхов и угнетению высвобождения из клеток (в первую очередь из тучных клеток) медиаторов реакций гиперчувствительности немедленного типа.
Флутиказона фуроат является синтетическим трехфтористым глюкокортикостероидом с выраженным противовоспалительным действием. Точный механизм действия, позволяющий купировать симптомы бронхиальной астмы и хронической обструктивной болезни легких (ХОБЛ), неизвестен. Глюкокортикостероиды продемонстрировали широкий спектр действия на различные типы клеток (например, эозинофилы, макрофаги, лимфоциты) и медиаторы (например, цитокины и хемокины, участвующие в процессе воспаления).
Между глюкокортикостероидами и ДДБА происходят молекулярные взаимодействия, в результате которых стероидные гормоны активируют ген бета2-адренорецептора, повышая количество восприимчивых адренорецепторов. ДДБА связываются с глюкокортикостероидным рецептором, обеспечивая его стероидозависимую активацию и стимулируя транслокацию в ядро клетки. Эти синергические взаимодействия приводят к усилению противовоспалительной активности, что было продемонстрировано в экспериментах in vitro и in vivo с различными клетками воспаления, участвующими в патофизиологических процессах развития бронхиальной астмы и ХОБЛ. В мононуклеарных клетках периферической крови у пациентов с ХОБЛ наблюдалось более выраженное противовоспалительное действие в присутствии комбинации вилантерола с флутиказона фуроатом по сравнению с одним флутиказона фуроатом в концентрациях, достигаемых при применении в клинических дозах.
Фармакокинетика
Всасывание
Абсолютная биодоступность вилантерола и флутиказона фуроата при ингаляционном введении комбинации вилантерола и флутиказона фуроата составила в среднем 27,3 % и 15,2 %, соответственно. Пероральная биодоступность вилантерола и флутиказона фуроата была низкой и в среднем составляла < 2 % и 1,26 %, соответственно. Принимая во внимание низкую пероральную биодоступность, системное действие вилантерола и флутиказона фуроата после ингаляционного приема в первую очередь обусловлено всасыванием части ингаляционной дозы, поступившей в легкие.
Распределение
После внутривенного введения вилантерол и флутиказона фуроат активно распределяются в организме, при этом средние объемы распределения в равновесном состоянии составляют 165 л и 661 л, соответственно. Оба вещества— вилантерол и флутиказона фуроат— обладают низкой способностью связываться с эритроцитами. В исследованиях in vitro связывание вилантерола и флутиказона фуроата с белками плазмы крови человека было высоким и достигало в среднем 93,9 % и > 99,6 %, соответственно. Степень связывания с белками плазмы крови in vitro не уменьшалась у пациентов с нарушениями функции печени или почек.
Несмотря на то, что вилантерол и флутиказона фуроат являются субстратами Р-гликопротеина (P-gp), при одновременном введении комбинации вилантерола и флутиказона фуроата с ингибиторами P-gp
изменение системной экспозиции вилантерола или флутиказона фуроата считается маловероятным, так как оба вещества обладают хорошей абсорбционной способностью.
Метаболизм
На основании данных экспериментов in vitro можно заключить, что основные пути метаболизма вилантерола и флутиказона фуроата в организме человека в первую очередь опосредованы изоферментом CYP3A4.
Вилантерол преимущественно метаболизируется путем О-деалкилирования с образованием ряда метаболитов, обладающих существенно более низкой бета1 и бета2-адреномиметической активностью.
Флутиказона фуроат преимущественно метаболизируется путем гидролиза S-фторметилкарботиоатной группы с образованием метаболитов, имеющих значительно более низкую глюкокортикостероидную активность.
Было проведено клиническое исследование лекарственных взаимодействий препарата с изоферментом CYP3A4 при непрерывном введении комбинации вилантерола и флутиказона фуроата (22 мкг + 184 мкг/доза)
и сильного ингибитора изофермента CYP3A4 — кетоконазола (400 мг) здоровым добровольцам.
Введение комбинации вилантерола и флутиказона фуроата привело к увеличению средней площади под фармакокинетической кривой (AUQo—24) и средней максимальной концентрации (Сmах) флутиказона фуроата на 36 % и 33 %, соответственно. Увеличение экспозиции флутиказона фуроата сопровождалось снижением средней концентрации сывороточного кортизола на 27 %, измеренной за период 0-24 часа.
Введение комбинации вилантерола и флутиказона фуроата и кетоконазола привело к увеличению средних значений AUQ 0-24 и Сmах вилантерола на 65 % и 22 %, соответственно. Увеличение экспозиции вилантерола не приводило к усилению характерных для бета-агонистов системных эффектов в отношении частоты сердечных сокращений, содержания калия в крови или корригированного интервала QT (QTcF).
Выведение
После перорального приема флутиказона фуроат в организме человека метаболизировался главным образом с образованием метаболитов, которые преимущественно выводились через желудочно-кишечный тракт, за исключением дозы радиоактивного вещества < 1 %, выведенной с мочой. Период полувыведения из плазмы крови для флутиказона фуроата после ингаляционного приема препарата составлял в среднем 24 часа.После перорального приема вилантерол в организме человека главным образом метаболизировался с образованиемметаболитов, которые экскретировались с мочой и фекалиями в соотношении приблизительно 70 % и 30 % дозы радиоактивного вещества, соответственно. Период полувыведения из плазмы крови для вилантерола после ингаляционного приема комбинации вилантерола и флутиказона фуроата составлял в среднем 2,5 часа.
Особые группы пациентов
В ходе третьей фазы клинических исследований проводился популяционный мета-анализ фармакокинетики вилантерола ифлутиказона фуроата у пациентов с бронхиальной астмой и ХОБЛ. В рамках популяционного фармакокинетического анализа оценивалось влияние демографических ковариат (возраст, пол, вес, индекс массы тела (ИМТ), расовая и этническая принадлежность) на фармакокинетику вилантерола и флутиказона фуроата.
Раса
Пациенты с бронхиальной астмой и ХОБЛ восточноазиатской, японской и юго-восточноазиатской рас (12-14% пациентов) имели в среднем более высокие показатели
AUC(0-24) (выше не более чем на 53 %) в сравнении с пациентами европеоидной расы. Тем не менее, в этих популяциях не обнаружено признаков более высокой системной экспозиции, связанной с более выраженным влиянием на экскрециют кортизола с мочой за 24-часовой период. У пациентов, страдающих ХОБЛ, влияние
расовой принадлежности на фармакокинетические параметры вилантерола не выявлено.
В среднем, по результатам оценки Сmах вилантерола была на 220-287 % выше, а AUC(0-24) была сопоставима у пациентов азиатского происхождения по сравнению с показателями у других расовых групп. Тем не менее, более высокая Сmах вилантерола не оказывала клинически значимого влияния на частоту сердечных сокращений.
Дети
Для подростков (12 лет или старше) рекомендации по изменению режима дозирования отсутствуют. Фармакокинетика комбинации вилантерола и флутиказона фуроата у пациентов младше 12 лет не изучалась. Безопасность и эффективность применения комбинации вилантерола и флутиказона фуроата у детей младше 12 лет пока не установлена.
Пациенты пожилого возраста
Влияние возраста на фармакокинетику вилантерола и флутиказона фуроата изучалось в третьей фазе клинических исследований, включавших пациентов с ХОБЛ и бронхиальной астмой.
У пациентов с бронхиальной астмой не было обнаружено признаков влияния возраста (12-84 лет) на фармакокинетический профиль флутиказона фуроата и вилантерола.
Несмотря на увеличение (37 %) AUC(o_24) вилантерола у пациентов с ХОБЛ в возрастном диапазоне от 41 до 84 лет, признаков влияния возраста пациентов на фармакокинетический профиль флутиказона фуроата не выявлено. У пожилого пациента (в возрасте 84 лет) с низкой массой тела (35 кг) прогнозируется, что AUC(0-24) вилантерола будет на 35 % выше результата, рассчитанного для популяции (в среднем, пациент с ХОБЛ в возрасте 60 лет и массой тела 70 кг), в то время как Стах вилантерола останется неизмененной. Маловероятно, что эти различия являются клинически релевантными.
Пациенты с нарушением функции почек
По данным клинико-фармакологического исследования для вилантерола и флутиказона фуроата тяжелое нарушение функции почек (клиренс креатинина < 30 мл/мин) не приводит к значительному увеличению системной экспозиции вилантерола или флутиказона фуроата или к развитию более выраженных системных эффектов глюкокортикостероидов или бетаг-агонистов в сравнении со здоровыми добровольцами. Коррекции дозы для пациентов с нарушением функции почек не требуется.
Влияние гемодиализа не изучалось.
Пациенты с нарушением функции печени
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени (согласно классификации цирроза печени по Чайлд-Пью: стадии цирроза А, В или С) наблюдалось увеличение системной экспозиции флутиказона фуроата (по измеренной AUC(0-24) до трех раз) в сравнении со здоровыми добровольцами. Повышение системной экспозиции флутиказона фуроата (при назначении комбинации вилантерола и флутиказона фуроата в дозировке 22 мкг + 184 мкг/доза) у пациентов с нарушением функции печени средней степени тяжести (стадия В по классификации Чайлд-Пью) сопровождалось снижением концентрации сывороточного кортизола в среднем на 34 % в сравнении со здоровыми добровольцами. У пациентов с нарушением функции печени тяжелой степени (стадия С по классификации Чайлд Пью), получавших более низкую дозу 11 мкг + 92 мкг, не наблюдалось снижения концентрации сывороточного кортизола. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22 мкг + 92 мкг (см. раздел «Способ применения и дозы»).
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени легкой, средней или тяжелой степени (стадии А, В и С по классификации Чайлд-Пью) не отмечалось значительного увеличения системной экспозиции вилантерола (Смах и AUC). В сравнении со здоровыми добровольцами у пациентов с нарушением функции печени легкой или средней степени (принимавших вилантерол в дозе 22 мкг) или тяжелой степени (принимавших вилантерол в дозе 11 мкг) не наблюдалось клинически значимых бета-адренергических системных эффектов (изменение частоты сердечных сокращений или концентрации сывороточного калия), вызванных приемом комбинации вилантерола и флутиказона фуроата.
Пол, масса тела, индекс массы тела (ИМТ)
Согласно результатам популяционного фармакокинетического анализа данных третьей фазы клинических исследований, включавшей 1213 пациентов с бронхиальной астмой (712 женщин) и 1225 пациентов с ХОБЛ (392 женщины), признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль флутиказона фуроата не обнаружено.
По данным популяционного анализа фармакокинетики с участием 856 пациентов с бронхиальной астмой (500 женщин) и 1091 пациента с ХОБЛ (340 женщин)признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль вилантерола не обнаружено.
Не требуется коррекции дозы на основании данных о половой принадлежности, массе тела или ИМТ.
Показания к применению
Бронхиальная астма
Препарат Релвар Эллипта применяется в качестве поддерживающей терапии бронхиальной астмы.
ХОБЛ (хроническая обструктивная болезнь легких)
Препарат Релвар Эллипта* применяется в качестве поддерживающей терапии обструкции дыхательных путей у пациентов с ХОБЛ, включая хронический бронхит и/или эмфизему легких. Применение препарата Релвар Эллипта* позволяет сократить число обострений ХОБЛ у пациентов с повторными обострениями в анамнезе.
Противопоказания
Препарат Релвар Эллипта противопоказан:
- пациентам, имеющим в анамнезе тяжелые аллергические реакции на молочный белок или повышенную чувствительность к действующим веществам или любому другому компоненту; входящему в состав препарата;
- детям до 12 лет для лечения бронхиальной астмы.
- Препарат Релвар Эллипта в дозе 22 мкг + 184 мкг/доза не показан для лечения ХОБЛ.
С осторожностью
При приеме симпатомиметиков, включая препарат Релвар Эллипта , со стороны сердечно-сосудистой системы могут наблюдаться такие нежелательные явления, как аритмия (например, наджелудочковая тахикардия и экстрасистолия). В плацебо-контролируемомклиническом исследовании у пациентов с ХОБЛ и повышенным риском развития сердечно сосудистых заболеваний или с сердечно сосудистым заболеванием, принимающих препарат Релвар Эллипта , не отмечалось повышения риска развития сердечно сосудистых явлений, серьезных сердечно сосудистых явлений или летального исхода по причине сердечно-сосудистой патологии по сравнению с пациентами, принимающими плацебо. Однако пациентам, страдающим тяжелыми формами сердечно-сосудистых заболеваний, препарат Релвар Эллипта следует назначать с осторожностью.
Как и другие лекарственные средства, в состав которых входят глюкокортикостероиды, препарат Релвар Эллипта® следует с осторожностью назначать пациентам с туберкулезом легких, а также пациентам с хроническими или невылеченными инфекциями.
Применение при беременности и в период грудного вскармливания
Фертильность
Данные по влиянию на фертильность человека отсутствуют. В доклинических исследованиях воздействия вилантерола и флутиказона фуроата на фертильность не обнаружено.
Беременность
Данные о применении препарата во время беременности ограничены.
Применение препарата Релвар Эллипта* у беременных женщин допустимо только в том случае, если потенциальная польза для матери превышает возможный риск для плода.
Период грудного вскармливания
Данных об экскреции вилантерола или флутиказона фуроата или их метаболитов в грудное молоко человека недостаточно. Однако другие глюкокортикостероиды и бета2-агонисты определяются в грудном молоке. Риск проникновения препарата вместе с молоком в организм новорожденного или ребенка не может быть исключен.
Принимая во внимание соотношение пользы терапии для матери и грудного вскармливания для ребенка, необходимо решить вопрос либо об отмене препарата, либо о прекращении грудного вскармливания.
Способ применения и дозы
Препарат Релвар Эллипта предназначен только для ингаляционного применения.
Препарат Релвар Эллипта следует применять один раз в сутки в одно и то же время, утром или вечером.
После ингаляции следует прополоскать рот водой, не проглатывая.
Бронхиальная астма
Пациент должен быть проинформирован о необходимости регулярного применения препарата Релвар Эллипта даже в случае бессимптомного течения заболевания.
При возникновении симптомов заболевания в период между приемами препарата в качестве неотложной терапии следует применять ингаляционные формы бета2-агонистов короткого действия.
Врач должен регулярно оценивать состояние пациента, чтобы обеспечить своевременное назначение оптимальной дозировки препарата Релвар Эллипта.
Дозировка может быть изменена только но рекомендации врача.
Взрослые и подростки 12 лет и старше
Рекомендуемая доза препарата Релвар Эллипта: одна ингаляция 22 мкг + 92 мкг один раз в сутки или одна ингаляция 22 мкг+ 184 мкг один раз в сутки.
Начальная доза препарата Релвар Эллипта 22 мкг + 92 мкг назначается пациентам. которым требуются низкие или средние дозы ингаляционных глюкокортикостсроидов. применяемых в комбинации с бета2-агонистами длительного действия.
Препарат Релвар Эллипта в дозировке 22 мкг + 184 мкг следует назначать пациентам, которым требуется более высокая доза ингаляционных глюкокортикостероидов, применяемых в комбинации с бета2-агонистами длительного действия.
Если препарат Релвар Эллипта» в дозировке 22 мкг + 92 мкг не обеспечивает адекватного контроля заболевания, рассматривается вопрос об увеличении дозы до 22 мкг +184 мкг. что может улучшить уровень контроля над течением бронхиальной астмы.
Дети
Безопасность и эффективность применения препарата Релвар Эллипта* у детей младше 12 лет не установлена.
ХОБЛ
Взрослые
Рекомендуемая доза препарата Релвар Эллипта®: одна ингаляция 22 мкг + 92 мкг один раз в сутки.
Препарат Релвар Эллипта в дозировке 22 мкг+ 184 мкг не показан для лечения пациентов с ХОБЛ.
Дети
Препарат по показанию ХОБЛ у детей не применяется.
Особые группы пациентов
Пациенты пожилого возраста
Пациентам старше 65 лет не требуется коррекция дозы препарата (см. раздел «Фармакокинетика», подраздел «Особые
группы пациентов»).
Пациенты с нарушением функции почек
Пациентам с нарушением функции почек не требуется коррекция дозы препарата (см. раздел «Фармакокинетика»).
Пациенты с нарушением функции печени
По данным клинико-фармакологического исследования у пациентов с нарушениями функции печени легкой, средней и тяжелой степени наблюдается трехкратное возрастание степени системной экспозиции флутиказона фуроата (AUC) (см. раздел «Фармакокмнстика»).
Препарат следует назначать с осторожностью пациентам с нарушениями функции печени, у которых риск развития системных нежелательных реакций, вызванных приемом глюкокортикостеропдов, более высок. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22мкг + 92мкг (см. раздел «Фармакокинетика»).
Рекомендации по применению
При первом использовании ингалятора Эллипта нет необходимости в проверке правильности его работы или специальной подготовке ингалятора к эксплуатации. Просто последовательно соблюдайте рекомендации по применению, указанные ниже.
В пачке картонной ингалятора Эллипта содержатся:
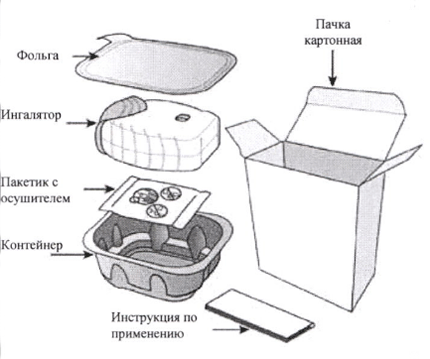
Ингалятор Эллипта упакован в контейнер. Не открывайте контейнер до тех пор, пока не будете готовы осуществить ингаляцию лекарственного препарата. Когда Вы будете готовы использовать ингалятор, снимите фольгу с контейнера. Контейнер содержит пакетик с осушителем для снижения влажности. Не вскрывайте данный пакетик, он не предназначен для еды или ингаляций, его следует выбросить.
Когда Вы достаете ингалятор из контейнера, его крышка находится в закрытом положении. Не открывайте ее до тех пор, пока Вы не будете готовы осуществить ингаляцию лекарственного препарата. В специально отведенноми поле «Использовать до» на этикетке ингалятора напишите дату, которая будет соответствовать дате вскрытия плюс 6 недель. Не следует использовать ингалятор после этой даты.
Ниже приведены пошаговые инструкции использования ингалятора Эллипта :
I.Прочитайте информацию использованием
При открытии и закрытии крышки ингалятора Эллипта без приема лекарственного препарата происходит потеря одной дозы. Эта доза остается закрытой внутри ингалятора, но она будет недоступна для приема. Невозможно случайно получить большую дозу или двойную дозу за одну ингаляцию.
II. Подготовка дозы
Не открывайте крышку, пока Вы не будете готовы к приему препарата.
Не встряхивайте ингалятор.
1. Опустите крышку вниз до щелчка.
2. Доза препарата готова к ингаляции, и в подтверждение этого счетчик доз уменьшает число доз на единицу.
3. Если счетчик доз не уменьшил число доз после того, как Вы услышали щелчок, то ингалятор не готов к подаче дозы лекарственного препарата. В этом случае следует обратиться по телефону или адресу, указанному в разделе «За дополнительной информацией обращаться».
4. Никогда не встряхивайте ингалятор.
III. Ингаляция препарата
1. Удерживая ингалятор на некотором расстоянии ото рта, сделайте выдох максимальной глубины. Не выдыхайте в ингалятор.
2. Поместите мундштук между губами и плотно обхватите его губами. Не закрывайте пальцами вентиляционное отверстие
3. Сделайте один долгий, равномерный, глубокий вдох через рот. Задержите дыхание насколько возможно (по крайней мере, на 3-4 секунды).
4. Уберите ингалятор изо рта.
5. Медленно и спокойно выдохните.
Вы можете не почувствовать вкус или не ощутить поступление лекарственного препарата даже при правильном использовании ингалятора.
Если Вы хотите протереть мундштук, сделайте это до закрытия крышки, используя сухую салфетку.
IV. Закрытие ингалятора и полоскание ротовой полости
1. Поднимите крышку до упора, добившись полного закрытия мундштука.
2. После ингаляции следует прополоскать рот водой. Это снизит вероятность развития таких побочных явлений, как боль в горле и полости рта
Побочное действие
Данные клинических исследований
Для определения частоты развития нежелательных реакций, связанных с приемом препарата Релвар Эллипта ,
использовались данные крупных клинических исследований среди пациентов с ХОБЛ и бронхиальной астмой. Программа клинической разработки препарата для лечения бронхиальной астмы включала 7 034 пациента, у которых проводилась комплексная оценка нежелательных реакций. В программе клинической разработки препарата для лечения ХОБЛ принимали участие 6 237 пациентов, у которых проводилась комплексная оценка нежелательных реакций. Исключая пневмонию и переломы, профили безопасности препарата у пациентов с ХОБЛ и бронхиальной астмой были схожи. По данным клинических исследований, пневмония и переломы более часто наблюдались у пациентов, страдающих ХОБЛ.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости определяется согласно классификации Всемирной организации здравоохранения следующим образом: очень часто (> 1/10), часто (> 1/100 и < 1/10), нечасто (> 1/1 000 и < 1/100), редко (> 1/10 000 и < 1/1 000), очень редко (< 1/10 000, включая отдельные случаи).
Частота встречаемости нежелательных реакций
Инфекционныеипаразитарные заболевания
Часто: пневмония, инфекции верхних дыхательных путей, бронхит, грипп, кандидоз полости рта и глотки.
Нарушения со стороны нервной системы
Очень часто: головная боль,
Нарушения со стороны сердца
Нечасто: экстрасистолия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто: назофарингит.
Часто: орофарингеальная боль, синусит, фарингит, ринит, кашель, дисфония.
Нарушения со стороны желудочно-кишечного тракта
Часто: боль в животе.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: артралгия, боль в спине, переломы.
Общие расстройства и нарушения в месте введения
Часто: лихорадка.
Данные пострегистрационного наблюдения
Нарушения со стороны иммунной системы
Редко: реакции гиперчувствительности, в том числе анафилаксия, ангионевротический отек, сыпь, крапивница.
Нарушения психики
Редко: тревога.
Нарушения со стороны нервной системы
Редко: тремор.
Нарушения со стороны сердца
Редко: учащенное сердцебиение, тахикардия.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: мышечный спазм.
Нарушения со стороны дыхательной системы, органов средостения
Редко: парадоксальный бронхоспазм.
Передозировка
Симптомы
При проведении клинических исследований не было получено данных о передозировке комбинацией вилантерола и флутиказона фуроата.
Передозировка препаратом Релвар Эллипта» может вызывать развитие симптомов и признаков, обусловленных действием отдельных компонентов препарата и характерных для передозировки бета2-агонистами и ингаляционными глюкокортикостероидами (см. раздел «Особые указания»).
Лечение
Специфическое лечение передозировки комбинацией вилантерола и флутиказона фуроата отсутствует. В случае развития передозировки назначается симптоматическая терапия и, при необходимости, обеспечивается соответствующее наблюдение за больным.
Применение кардиоселективных бета-адреноблокаторов следует рассматривать только в случаях сильно выраженных эффектов передозировки вилантеролом, которые клинически проявляются невосприимчивостью к поддерживающей терапии. Кардиоселективные бета-адреноблокаторы следует с осторожностью назначать пациентам, у которых наблюдались эпизоды бронхоспазма в анамнезе.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ
При назначении препарата в терапевтических дозах клинически значимые лекарственные взаимодействия вилантерола или флутиказона фуроата считаются маловероятными вследствие низких плазматических концентраций последних при ингаляционном введении.
Бета-адреноблокаторы могут ослаблять или антагонизировать действие бета2-адреномиметиков. Следует избегать одновременного приема неселективных и селективных бета-блокаторов. исключая случаи, когда их назначение строго необходимо.
Вилантерол и флутиказона фуроат подвергаются быстрому первичному метаболизму в печени посредством изофермента системы цитохрома CYP3A4.
При одновременном назначении препарата с сильными ингибиторами изофермента цитохрома CYP3A4 (например, кетоконазол, ритонавир) следует соблюдать осторожность, поскольку возможно повышение системного воздействия вилантерола и флутиказона фуроата, что в свою очередь может привести к повышению риска развития нежелательных реакций (см. раздел «Фармакокинетика»).
Вилантерол и флутиказона фуроат являются субстратами P-gp. По результатам клинико-фармакологического исследования с участием здоровых добровольцев, которым одновременно назначались вилантерол и сильный ингибитор P-gp и умеренный ингибитор изофермента цитохрома CYP3A4 верапамил, значимого влияния на фармакокинетику вилантерола не выявлено. Клинико-фармакологические исследования совместного назначения специфического ингибитора P-gr и флутиказона фуроата не проводились.
ОСОБЫЕ УКАЗАНИЯ
Обострения
Препарат Релвар Эллипта не предназначен для купирования острых симптомов бронхиальной астмы или обострения ХОБЛ, в таких случаях требуется назначение бронходилататоров короткого действия.
Увеличение частоты приема бронходилататоров короткого действия с целью купирования симптомов свидетельствует об ухудшении контроля над заболеванием и необходимости консультации врача.
Пациентам с бронхиальной астмой или ХОБЛ не следует прекращать лечение препаратом Релвар Эллипта без наблюдения врача, так как отмена терапии может привести к возобновлению симптомов.
На фоне лечения препаратом Релвар Эллипта могут развиваться нежелательные явления, связанные с течением бронхиальной астмы или обострением заболевания. Пациентам следует рекомендовать продолжить лечение. В случае отсутствия контроля над заболеванием или ухудшения состояния после начала терапии препаратом Релвар Эллипта необходима консультация врача.
Парадоксальный бронхоспазм
Как и при других видах ингаляционной терапии, после приема препарата может развиваться парадоксальный бронхоспазм, сопровождающийся быстрым нарастанием свистящих хрипов. В этом случае показаны неотложное назначение ингаляционного бронходилататора длительного действия и немедленная отмена препарата Релвар Эллипта. Пациент должен быть осмотрен врачом, и ему, при необходимости, может быть назначена альтернативная терапия.
Пациенты с нарушением функции печени
Пациентам с нарушением функции печени средней и тяжелой степени следует назначать дозу 22 мкг + 92 мкг, таким пациентам следует находиться под наблюдением врача для контроля над системными побочными реакциями, связанными с применением глюкокортикостероидов.
Системныеэффекты глюкокортикостероидов
При применении ингаляционных глюкокортикостероидов (особенно при длительном приеме в высоких дозах) могут развиваться системные побочные реакции. Такие побочные реакции развиваются значительно реже, чем при пероральном приеме глюкокортикостероидов. К проявлениям возможного неблагоприятного системного действия относятся: подавление функции гипоталамо-гипофизарно-надпочечниковой системы, снижение минеральной плотности костей, замедление скорости роста у детей и подростков, катаракта и глаукома.
Пневмония
У пациентов с ХОБЛ, получающих препарат Релвар Эллипта , наблюдалось повышение частоты развития пневмонии, а также частоты возникновения тяжелых форм пневмонии, требующих госпитализации пациента. В некоторых случаях клинические эпизоды пневмонии имели летальный исход. Врачам следует помнить о возможности развития пневмонии у пациентов с ХОБЛ, не забывая о том, что клинические признаки такого инфекционного заболевания маскируются симптомами обострения ХОБЛ. Более высокий риск развития пневмонии на фоне приема препарата Релвар Эллипта имеют следующие группы пациентов с ХОБЛ: курящие пациенты, пациенты, ранее перенесшие пневмонию, пациенты с индексом массы тела < 25 кг/м и пациенты с объемом форсированного выдоха (ОФВ0 < 50 % от должных величин. При назначении терапии препаратом Релвар Эллипта следует учитывать вышеуказанные факторы, в случае возникновения пневмонии лечение должно быть пересмотрено.
У пациентов с бронхиальной астмой случаи развития пневмонии наблюдались нечасто. Пациенты с бронхиальной астмой, получавшие препарат Релвар Эллипта в дозировке 22 мкг + 184 мкг/доза, возможно, имели более высокий риск развития пневмонии в сравнении с пациентами, получавшими более низкую дозу препарата Релвар Эллипта (22 мкг + 92 мкг/доза), или с группой плацебо. Факторы риска не установлены.
В ходе проведения клинических исследований у пациентов, страдающих ХОБЛ, была выявлена низкая частота возникновения переломов костей во всех лечебных группах, но при этом во всех группах, получавших комбинацию вилантерола и флутиказона фуроата, она была несколько выше (2 %), чем в группе, получавших монотерапию вилантеролом 22 мкг (< 1 %).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ, МЕХАНИЗМАМИ
Исследования по изучению влияния препарата Релвар Эллипта на способность к вождению автотранспорта и работе с механизмами не проводились. Исходя из данных фармакологии вилантерола или флутиказона фуроата, неблагоприятное влияние препарата на эти виды деятельности не предполагается.
Форма выпуска
Порошок для ингаляций дозированный, 22 мкг + 92 мкг/доза, 22 мкг + 184 мкг/доза.
По 30 доз в пластиковый ингалятор с корпусом светло-серого цвета, бледно-голубой крышкой мундштука и счетчиком доз. Ингалятор содержит два алюминиевых ламинированных стрипа, каждый из которых состоит из 30 ячеек, которые содержат порошок белого цвета. Ингалятор помещен в многослойный контейнер из алюминиевой фольги, содержащий пакетик с осушителем. Контейнер запечатан легко открывающейся фольгой. По 1 контейнеру вместе с инструкцией по применению в пачку картонную.
Срок годности
Не вскрытый алюминиевый контейнер: 2 года.
Вскрытый алюминиевый контейнер: 6 недель.
В специально отведенном поле «Использовать до» на этикетке ингалятора напишите дату. Дату следует указать сразу после того, как ингалятор был извлечен из контейнера.
Не применять после истечения срока годности, указанного на упаковке.
Условия хранения
Хранить при температуре не выше 25°С. Хранить в недоступном для детей месте.
Условия отпуска
По рецепту.
Производитель
«Глаксо Оперэйшенс Великобритания Лимитед» / Glaxo Operations UK Limited
SGI2 ODJ, Хертфордшир, Вэа, Прайори стрит, Великобритания / Priory Street, Ware, Hertfordshire, SGI2 ODJ. United Kingdom
НАИМЕНОВАНИЕ И АДРЕС ЮРИДИЧЕСКОГО ЛИЦА, НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
ЗАО «ГлаксоСмитКляйн Трейдинг» 119180, г. Москва, Якиманская наб., д. 2
За дополнительной информацией обращаться:
ЗАО «ГлаксоСмитКляйн Трейдинг»
121614, г. Москва, ул. Крылатская, д. 17, корп. 3, эт. 5
Бизнес-Парк «Крылатские холмы»
Купить Релвар Эллипта в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
МНН: Вилантерол, Флутиказона фуроат
Производитель: Глаксо Оперэйшенс Великобритания Лимитед (Глаксо Вэллком Оперэйшенс)
Анатомо-терапевтическо-химическая классификация: Вилантерол и флутиказона фуроат
Номер регистрации в РК:
№ РК-ЛС-5№021461
Информация о регистрации в РК:
07.09.2020 — бессрочно
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
10 450 KZT
- Скачать инструкцию медикамента
Торговое название
Релвар® Эллипта®
Международное непатентованное название
Нет
Лекарственная форма
Порошок для ингаляций дозированный, 92 мкг/22 мкг, 184 мкг/22 мкг, 30 доз
Состав
1 доза содержит
активные вещества: 100 мкг1 или 200 мкг1 флутиказона фуроата микронизированного, 40 мкг вилантерола трифенатат микронизированный (25 мкг1 в пересчете на вилантерол), вспомогательные вещества: магния стеарат, лактозы моногидрат.
1Указано номинальное количество действующего вещества, закладываемое в процессе производства; доставляемое количество составляет 184 мкг или 92 мкг флутиказона фуроата и 22 мкг вилантерола, что соответствует указанным дозировкам.
Описание
Пластиковый ингалятор Элиппта® с корпусом светло-серого цвета, бледно-голубой крышкой мундштука и счетчиком доз, упакованный в контейнер из фольги, содержащий влагопоглощающий пакетик. Контейнер запечатан легко открывающейся фольгой. Ингалятор содержит два стрипа, каждый стрип состоит из 30 равномерно распределенных ячеек, каждая из которых содержит порошок белого цвета.
Фармакотерапевтическая группа
Препараты для лечения обструктивных заболеваний дыхательных путей. Симпатомиметики ингаляционные. Симпатомиметики в комбинации с другими препаратами для лечения обструктивных заболеваний дыхательных путей. Вилантерол и флутиказона фуроат
Код АТХ R03AK10
Фармакологические свойства
Фармакокинетика
Всасывание
Абсолютная биодоступность вилантерола и флутиказона фуроата при ингаляционном введении комбинации вилантерола и флутиказона фуроата составила в среднем 15,2 % и 27,3 %, соответственно. Пероральная биодоступность обоих веществ была низкой, и в среднем составляла 1,26 % и < 2 %, соответственно. Принимая во внимание низкую пероральную биодоступность, системное действие вилантерола и флутиказона фуроата после ингаляционного приема в первую очередь обусловлено всасыванием части ингаляционной дозы, поступившей в легкие.
Распределение
После внутривенного введения вилантерол и флутиказона фуроат активно распределяются в организме, при этом средние объемы распределения в равновесном состоянии составляют 165 л и 661 л, соответственно.
Оба вещества обладают низкой способностью связываться с эритроцитами. В исследованиях in vitro связывание вилантерола и флутиказона фуроата с белками плазмы человека было высоким и достигало в среднем > 93,9 % и 99,6 %, соответственно. Степень связывания с белками плазмы in vitro не уменьшалась у пациентов с нарушениями функции печени и почек.
Несмотря на то, что вилантерол и флутиказона фуроат являются субстратами Р-гликопротеина (P-gp), при одновременном назначении комбинации вилантерола и флутиказона фуроата с ингибиторами P-gp изменение системной экспозиции вилантерола или флутиказона фуроата считается маловероятным, так как оба вещества обладают хорошей абсорбционной способностью.
Метаболизм
На основании in vitro экспериментов можно заключить, что ключевые пути метаболизма вилантерола и флутиказона фуроата в организме человека в первую очередь опосредуются через изофермент цитохрома CYP3A4.
Вилантерол преимущественно метаболизируется путем О-деалкилирования с образованием целого ряда метаболитов, обладающих существенно более низкой бета1- и бета2-адреномиметической активностью.
Флутиказона фуроат преимущественно метаболизируется путем гидролиза S-фторметилкарботиатной группы с образованием метаболитов, имеющих значительно более низкую глюкокортикостероидную активность.
Было проведено клиническое исследование лекарственных взаимодействий препарата с изоферментом цитохрома CYP3A4 при длительном введении комбинации флутиказона фуроата и вилантерола (184 мкг/доза + 22 мкг) и сильного ингибитора изофермента цитохрома CYP3A4 — кетоконазола (400 мг) на примере здоровых добровольцев. Совместное введение препаратов привело к повышению средней площади под фармакокинетической кривой (AUC(0–24)) и средней максимальной концентрации (Cmax) флутиказона фуроата на 36 % и 33 %, соответственно. Увеличение экспозиции флутиказона фуроата было ассоциировано со снижением средней концентрации сывороточного кортизола на 27 %, измеренного за период 0–24 часа.
Совместное введение комбинации вилантерола и флутиказона фуроата и кетоконазола привело к повышению средних AUC(0–t) и Cmax вилантерола на 65 и 22 %, соответственно. Увеличение экспозиции вилантерола не приводило к усилению характерных для бета-агонистов системных эффектов — влияние на частоту сердечных сокращений, содержание калия в крови или интервал QT.
Выведение
После перорального приема флутиказона фуроат в организме человека, главным образом, метаболизировался с образованием метаболитов, которые преимущественно выводились через желудочно-кишечный тракт, за исключением дозы радиоактивного вещества < 1 %, выведенной с мочой. Предполагаемый период полувыведения из плазмы флутиказона фуроата после ингаляционного приема препарата составлял в среднем 24 часа.
После перорального приема вилантерол в организме человека, главным образом, метаболизировался с образованием метаболитов, которые экскретировались с мочой и фекалиями, в соотношении приблизительно 70 % и 30 % дозы радиоактивного вещества, соответственно. Период полувыведения из плазмы вилатерола после ингаляционного приема препарата составлял в среднем 2,5 часа.
Особые группы пациентов
В ходе третьей фазы клинических исследований проводился популяционный мета-анализ фармакокинетики вилантерола и флутиказона фуроата у пациентов с бронхиальной астмой и хронической обструктивной болезнью легких (ХОБЛ). В рамках данного анализа оценивалось влияние демографических показателей (возраст, пол, вес, индекс массы тела, расовая и этническая принадлежность) на фармакокинетику вилантерола и флутиказона фуроата.
Раса
У пожилых пациентов с бронхиальной астмой или ХОБЛ оценивалась AUC(0–24) флутиказона фуроата. Согласно полученным данным, пациенты восточно-азиатской, японской и южно-азиатской расы (12–14 % пациентов) имели в среднем более высокие показатели AUC(0–24) (выше не более чем на 53 %) в сравнении с пациентами европеоидной расы. Тем не менее, в этих популяциях признаков более высокой системной экспозиции, проявляющейся более выраженным влиянием на экскрецию кортизола с мочой за 24-часовой период, не обнаружено. У пациентов, страдающих ХОБЛ, влияние расовой принадлежности на фармакокинетические параметры вилантерола не выявлено.
В среднем, по результатам оценки Сmax вилантерола была на 220–287 % выше, а AUC(0–24) была сопоставима у пациентов азиатского происхождения по сравнению с показателями у других расовых групп. Тем не менее, более высокая Сmax вилантерола не имела клинически значимого влияния на частоту сердечных сокращений.
Дети
Для подростков (12 лет или старше) рекомендации по изменению режима дозирования отсутствуют.
Фармакокинетика комбинации флутиказона фуроата и вилантерола у пациентов младше 12 лет не изучалась. Безопасность и эффективность применения комбинации вилантерола и флутиказона фуроата у детей младше 12 лет пока не установлена.
Пациенты пожилого возраста
Влияние возраста на фармакокинетику флутиказона фуроата и вилантерола изучалось в третьей фазе клинических исследований, включавших пациентов с ХОБЛ и бронхиальной астмой.
У пациентов с бронхиальной астмой, не было обнаружено признаков влияния возраста (12–84 лет) на фармакокинетический профиль флутиказона фуроата и вилантерола.
Несмотря на увеличение (37 %) AUC(0–24) вилантерола у пациентов с ХОБЛ на протяжении всего наблюдаемого возрастного диапазона от 41 до 84 лет, признаков влияния возраста пациентов на фармакокинетический профиль флутиказона фуроата не выявлено.
Пациенты с нарушением функции почек
По данным клинико-фармакологического исследования тяжелое нарушение функции почек (клиренс креатинина < 30 мл/мин) не приводит к значительному увеличению системной экспозиции вилантерола или флутиказона фуроата или к развитию более выраженных системных эффектов глюкокортикостероидов или бета2-агонистов в сравнении со здоровыми добровольцами. Индивидуальный подбор дозы для пациентов с нарушением функции почек не требуется.
Влияние гемодиализа не изучалось.
Пациенты с нарушением функции печени
После непрерывного приема комбинации флутиказона фуроата и вилантерола в течение 7 дней у пациентов с нарушением функции печени (согласно классификации цирроза печени по Чайлд-Пью: стадии цирроза А, В или С) наблюдалось увеличение системной экспозиции флутиказона фуроата (по измеренной AUC(0–24) до трех раз) в сравнении со здоровыми добровольцами. Повышение системной экспозиции флутиказона фуроата (при назначении комбинации флутиказона фуроата и вилантерола в дозировке 184 мкг + 22 мкг /доза) у пациентов с нарушением функции печени средней тяжести (стадия В по классификации Чайлд-Пью) было ассоциировано со снижением концентрации сывороточного кортизола в среднем на 34 % в сравнении со здоровыми добровольцами.
У пациентов с тяжелой степенью печеночной недостаточности (стадия С по классификации Чайлд-Пью), получавшим комбинации флутиказона фуроата и вилантерола в дозировке 92 мкг + 22 мкг /доза сывороточный уровень кортизола не уменьшался.
У пациентов со средней и тяжелой печеночной недостаточностью максимальная доза препарата составляет 92 мкг + 22 мкг /доза
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени легкой, средней или тяжелой степени (стадии А, В и С по классификации Чайлд-Пью) не отмечалось значительного увеличения системной экспозиции вилантерола (по Сmax и AUC(0–24)).
В сравнении со здоровыми добровольцами у пациентов с нарушением функции печени легкой или средней степени (принимавших вилантерол в дозе 22 мкг) или тяжелой степени (принимавших вилантерол в дозе 11 мкг) не наблюдалось клинически значимых бета-адренергических системных эффектов (изменение частоты сердечных сокращений или концентрации сывороточного калия), вызванных приемом комбинации вилантерола и флутиказона фуроата.
Пол, масса тела, индекс массы тела
По данным третьей фазы популяционного анализа данных фармакокинетики, включавшего 1213 пациентов с бронхиальной астмой (712 женщин) и 1225 пациентов с ХОБЛ (392 женщины), признаков влияния пола, массы тела или индекса массы тела на фармакокинетический профиль флутиказона фуроата не обнаружено.
По данным популяционного анализа с участием 856 пациентов с бронхиальной астмой (500 женщин) и 1091 пациентов с ХОБЛ (340 женщин) признаков влияния пола, массы тела или индекс массы тела на фармакокинетический профиль вилантерола не обнаружено.
Не требуется индивидуальный подбор дозы на основании данных о половой принадлежности, массы тела или индекса массы тела
Фармакодинамика
Механизм действия
Вилантерол и флутиказона фуроат относятся к двум различным классам лекарственных препаратов — селективный бета2-адреномиметик длительного действия и синтетический глюкокортикостероид соответственно.
Фармакодинамические эффекты
Вилантерол относится к классу селективных бета2-адреномиметиков длительного действия (ДДБА).
Фармакологические эффекты агонистов бета2-адренорецепторов, включая вилантерол, по крайней мере частично связаны со стимуляцией внутриклеточной аденилатциклазы — фермента, который катализирует превращение аденозинтрифосфата (АТФ) в циклический 3’,5’-аденозинмонофосфат (циклический АМФ). Повышение уровня циклического АМФ приводит к расслаблению гладкой мускулатуры бронхов и угнетению высвобождения из клеток (в первую очередь из тучных клеток) медиаторов реакций гиперчувствительности немедленного типа.
Флутиказона фуроат является синтетическим трехфтористым глюкокортикостероидом с выраженным противовоспалительным действием. Точный механизм действия, позволяющий купировать симптомы бронхиальной астмы и хронической обструктивной болезни легких (ХОБЛ), не известен. Глюкокортикостероиды продемонстрировали широкий спектр действия на различные типы клеток (например, эозинофилы, макрофаги, лимфоциты) и медиаторы (например, цитокины и химокины, участвующие в процессе воспаления).
Между глюкокортикостероидами и ДДБА происходят молекулярные взаимодействия, в результате которых стероидные гормоны активируют ген бета2-адренорецептора, повышая число восприимчивых адренорецепторов. ДДБА связываются с глюкокортикостероидным рецептором, обеспечивая его стероидо-зависимую активацию и стимулируя транслокацию в ядро клетки. Эти синергические взаимодействия приводят к усилению противовоспалительной активности, что выявляется в экспериментах in vitro и in vivo с различными клетками воспаления, участвующими в патофизиологических процессах развития бронхиальной астмы и ХОБЛ. Результаты клинических исследований с использованием биоптатов дыхательных путей также продемонстрировали синергию глюкокортикостероидов и ДДБА, возникающую при назначении этих препаратов пациентам с ХОБЛ в терапевтических дозах.
Показания к применению
Для дозировок 92мкг/22мкг и 184мкг/22мкг
— базисная терапия пациентов с бронхиальной астмой, у которых заболевание неадекватно контролируется ингаляционными глюкокортикостероидами или короткодействующими бета2-адреномиметиками «по требованию».
Для дозировки 92мкг/22мкг
— симптоматическая терапия при ХОБЛ (хроническая обструктивная болезнь легких) у взрослых пациентов с обострениями ХОБЛ в анамнезе, несмотря на длительную бронходилатирующую терапию
Способ применения и дозы
Препарат Релвар® Эллипта® предназначен только для ингаляционного применения.
Препарат Релвар® Эллипта® следует применять один раз в сутки в одно и то же время, утром или вечером.
После ингаляции следует прополоскать рот водой, не проглатывая использованную воду.
Бронхиальная астма
Пациент должен быть проинформирован о необходимости регулярного применения препарата Релвар® Эллипта® даже в случае бессимптомного течения заболевания.
При возникновении симптомов заболевания в период между приемами препарата в качестве неотложной терапии следует применять ингаляционные формы бета2-агонистов короткого действия.
Врач должен регулярно оценивать состояние пациента, чтобы обеспечить своевременное назначение оптимальной дозировки препарата Релвар® Эллипта®. Дозировка может быть изменена только по рекомендации врача.
Взрослые и подростки 12 лет и старше
Рекомендуемая доза препарата Релвар® Эллипта®:
— одна ингаляция 92 мкг флутиказона фуроата и 22 мкг вилантерола один раз в сутки
или
— одна ингаляция 184 мкг флутиказона фуроата и 22 мкг вилантерола один раз в сутки.
Начальная доза препарата Релвар® Эллипта® 92 мкг флутиказона фуроата и 22 мкг вилантерола назначается пациентам, которым требуются низкие или средние дозы ингаляционных глюкокортикостероидов, применяемых в комбинации с бета2-агонистами длительного действия.
Препарат Релвар® Эллипта® в дозировке 184 мкг флутиказона фуроата и 22 мкг вилантерола следует назначать пациентам, которым требуется более высокая доза ингаляционных глюкокортикостероидов, применяемых в комбинации с бета2-агонистами длительного действия.
Если препарат Релвар® Эллипта® в дозировке 92 мкг флутиказона фуроата и 22 мкг вилантерола не обеспечивает адекватного контроля заболевания, рассматривается вопрос об увеличении дозы до 184 мкг флутиказона фуроата и 22 мкг вилантерола , что может улучшить уровень контроля над течением бронхиальной астмы.
Дети
Безопасность и эффективность применения препарата Релвар® Эллипта® у детей младше 12 лет не установлена.
ХОБЛ
Взрослые
Рекомендуемая доза препарата Релвар® Эллипта® составляет одну ингаляцию 92 мкг флутиказона фуроата и 22 мкг вилантерола один раз в сутки.
Препарат Релвар® Эллипта® в дозировке 184 мкг флутиказона фуроата и 22 мкг вилантерола не показан для лечения пациентов с ХОБЛ.
Дети
Препарат по показанию ХОБЛ у детей не применяется.
Особые группы пациентов
Пациенты пожилого возраста
Пациентам старше 65 лет не требуется индивидуальный подбор дозы препарата (см. раздел «Фармакокинетика», подраздел «Особые группы пациентов»).
Пациенты с нарушением функции почек
Пациентам с нарушением функции почек не требуется индивидуальный подбор дозы препарата (см. раздел «Фармакокинетика»).
Пациенты с нарушением функции печени
По данным клинико-фармакологического исследования у пациентов с нарушениями функции печени легкой, средней и тяжелой степени наблюдается трехкратное возрастание степени системной экспозиции флутиказона фуроата (с увеличением таких показателей как Cmax и AUC) (см. раздел «Фармакокинетика»).
Пациентам с нарушениями функции печени следует назначать препарат с осторожностью, в связи с наличием более высокого риска развития системных нежелательных реакций, вызванных приемом глюкокортикостероидов. У пациентов со средней и тяжелой печеночной недостаточностью максимальная доза препарата составляет 92мкг/22мкг (см. раздел «Фармакокинетика»)
Рекомендации по применению
Ингалятор Эллипта® содержит предварительно отмеренные дозы и готов к использованию.
При первом использовании ингалятора Эллипта® нет необходимости в проверке правильности его работы или специальной подготовки ингалятора к эксплуатации. Просто последовательно соблюдайте рекомендации по применению.
Ингалятор Эллипта® упакован в контейнер, содержащий влагопоглощающий пакетик с силикагелем, который не предназначен для еды или ингаляций. Данный пакетик следует утилизировать.
Когда Вы достаете ингалятор из контейнера, его крышка находится в закрытом положении. Не открывайте ее до тех пор, пока Вы не будете готовы к приему препарата.
На этикетке ингалятора Эллипта®, в отведенном для этого месте «Использовать до», необходимо написать дату окончания использования препарата. Дата «Использовать до» составляет 6 недель с момента вскрытия контейнера. После этой даты ингалятор Эллипта® не должен быть использован, контейнер может быть утилизирован.
Ниже приведена пошаговая инструкция использования ингалятора Эллипта®:
-
Прочитайте следующую информацию перед использованием.
П ри открытии и закрытии крышки ингалятора Эллипта® без приема лекарственного препарата происходит потеря одной дозы. Эта доза остается закрытой внутри ингалятора, но она будет недоступна для приема. Невозможно случайно получить большую дозу или двойную дозу за одну ингаляцию.
Побочные действия
-
Подготовка дозы
Не открывайте крышку, пока Вы не будете готовы к приему препарата. Не встряхивайте ингалятор.
-
Опустите крышку вниз до щелчка.
-
Доза препарата готова к ингаляции, и в подтверждение этого счетчик доз уменьшает число доз на единицу.
-
Если счетчик доз не уменьшил число доз после того, как Вы услышали щелчок, то ингалятор не готов к подаче дозы лекарственного препарата. В этом случае следует обратиться к врачу или по телефону/адресу, указанному в разделе «Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)».
-
Никогда не встряхивайте ингалятор.
-
Ингаляция лекарственного препарата
-
Удерживая ингалятор на некотором расстоянии ото рта, сделайте выдох максимальной глубины. Не выдыхайте в ингалятор.
-
Поместите мундштук между губами и плотно обхватите его губами. Не закрывайте пальцами вентиляционное отверстие.
-
Сделайте один глубокий, долгий, равномерный вдох. Задержите дыхание насколько возможно (по крайней мере, на 3–4 секунды).
-
Уберите ингалятор изо рта.
-
Медленно и спокойно выдохните.
Губы должны точно повторять форму мундштука ингалятора
Вы можете не почувствовать вкус или не ощутить поступление лекарственного препарата даже при правильном использовании ингалятора.
-
Закрытие ингалятора и полоскание ротовой полости.
Если Вы хотите протереть мундштук, используйте сухую бумажную салфетку перед закрытием крышки.
-
Поднимите крышку до упора, добившись полного закрытия мундштука.
-
После ингаляции следует прополоскать рот водой. Это снизит вероятность развития таких побочных явлений, как боль в горле и полости рта.
Побочные действия
Для определения частоты развития нежелательных реакций, связанных с применением препарата Релвар® Эллипта®, использовались данные крупных клинических исследований среди пациентов с ХОБЛ и бронхиальной астмой. Программа клинической разработки препарата для лечения бронхиальной астмы включала 7 034 пациентов, у которых проводилась комплексная оценка нежелательных явлений. В программе клинической разработки препарата для лечения ХОБЛ принимали участие 6 237 пациентов, у которых также проводилась комплексная оценка нежелательных явлений.
Исключая такие нежелательные явления, как пневмония и переломы, профиль безопасности препарата у пациентов с ХОБЛ и бронхиальной астмой был схож. По данным клинических исследований пневмония и переломы более часто наблюдались у пациентов, страдающих ХОБЛ.
Нежелательные явления, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости определяется следующим образом: очень часто (≥ 1/10), часто (≥ 1/100 и < 1/10), нечасто (≥ 1/1 000 и < 1/100), редко (≥ 1/10 000 и < 1/1 000), очень редко (< 1/10 000, включая отдельные случаи).
|
Очень часто — головная боль — назофарингит Часто — пневмония*, инфекции верхних дыхательных путей, бронхит, грипп, кандидоз полости рта и глотки — орофарингеальная боль, синусит, фарингит, ринит, кашель, дисфония (осиплость голоса) — артралгия, боль в спине, переломы** — боль в животе — лихорадка Нечасто — экстрасистолия Редко — сыпь, крапивница — реакции гиперчувствительности, включая анафилаксию, — ангионевротический отек |
Описание отдельных нежелательных реакций
* Пневмония
В ходе проведения двух клинических исследований с повторяющимся дизайном продолжительностью 12 месяцев с участием 3 255 пациентов, страдающих ХОБЛ, количество случаев пневмонии на 1000 пациентов в год, получающих флутиказона фуроат /вилантерол (184мкг/22 мкг) составило 97.7, в группе флутиказона фуроат/вилантерол (92мкг/22 мкг) составило 85.7 и 42.3 в группе вилантерола (22 мкг).
В тяжелых случаях пневмонии, число случаев на 1000 пациентов в год составили 33.6, 35.5, 7.6 соответственно, для случаев, требующих госпитализации, на 1000 пациентов в год составили 35.1 для группы получающих флутиказона фуроат /вилантерол (184мкг/22 мкг), 42.9 в группе флутиказона фуроат/вилантерол (92 мкг/22 мкг) и 12.1 в группе вилантерола (22 мкг).
Случаи пневмонии с летальным исходом составили 8.8 для группы пациентов, получавших флутиказона фуроат/вилантерол (184 мкг/ 22 мкг) в сравнении с 1.5 для группы флутиказона фуроат /вилантерол (92 мкг/22 мкг) и 0 в группе вилантерола (22 мкг).
В полном анализе 11 исследований в области астмы (7.034), частота случаев пневмонии на 1000 пациентов в год составила 18.4 для группы пациентов, принимавших флутиказона фуроат/вилантерол (184 мкг/22 мкг) в сравнении с 9.6 для группы флутиказона фуроат /вилантерол (92 мкг/22 мкг) и 8.0 в группе плацебо.
** Переломы
В ходе проведения двух клинических исследований с повторяющимся дизайном продолжительностью 12 месяцев с участием 3 255 пациентов, страдающих ХОБЛ, частота возникновения переломов костей в целом была низкой во всех группах лечения, но при этом во всех группах флутиказона фуроата/вилантерола она была несколько выше (2 %), чем в группе, монотерапии вилантеролом в дозе 25 мкг (< 1 %). Несмотря на большее число переломов в группах лечения флутиказона фуроата/вилантерола по сравнению с группой вилантерола в дозе 22 мкг, типичные переломы, связанные с приемом глюкокортикостероидов (например, компрессионные переломы позвоночника/переломы грудных и поясничных позвонков, переломы бедра и вертлужной впадины), возникали в < 1 % случаев в группах лечения флутиказона фуроатом/вилантеролом и вилантеролом.
При комплексном анализе результатов 11 клинических исследований с участием пациентов, страдающих бронхиальной астмой (7 034 пациентов), частота возникновения переломов составила < 1 %, и, как правило, эти переломы были связаны с травмой.
Данные, полученные при пострегистрационном применении
Редко
— пальпитация (ощущение сердцебиения)
— тахикардия
— тремор
— тревожность (беспокойство)
Противопоказания
-наличие в анамнезе тяжелых аллергических реакций на молочный белок
-повышенная чувствительность к действующим веществам или любому компоненту, входящему в состав препарата.
С осторожностью: — период лактации
— лицам, страдающим тяжелыми формами сердечно-сосудистых
заболеваний, при одновременном приеме симпатомиметиков
— пациентам с туберкулезом легких
— пациентам с хроническими или невылеченными инфекциями.
Лекарственные взаимодействия
При назначении препарата в терапевтических дозах клинически значимые лекарственные взаимодействия вилантерола или флутиказона фуроата считаются маловероятными вследствие низких плазматических концентраций последних при ингаляционном введении.
Бета-адреноблокаторы могут ослаблять действие бета2-адреномиметиков. Следует избегать одновременного приема неселективных и селективных бета-блокаторов, исключая случаи, когда их назначение строго необходимо.
Вилантерол и флутиказона фуроат подвергаются быстрому первичному метаболизму в печени посредством изофермента системы цитохрома CYP3A4.
При одновременном назначении препарата с сильными ингибиторами изофермента цитохрома CYP3A4 (например, кетоконазол, ритонавир) следует соблюдать осторожность, поскольку возможно повышение системного воздействия вилантерола и флутиказона фуроата, что в свою очередь может привести к повышению риска развития нежелательных реакций (см. раздел «Фармакокинетика»).
Вилантерол и флутиказона фуроат являются субстратами P-gp. По результатам клинико-фармакологического исследования с участием здоровых добровольцев, которым одновременно назначались вилантерол и сильный ингибитор P-gp и умеренный ингибитор изофермента цитохрома CYP3A4 верапамил, значимого влияния на фармакокинетику вилантерола не выявлено. Клинико-фармакологические исследования совместного назначения специфического ингибитора P-gr и флутиказона фуроата не проводились.
Особые указания
Обострения заболевания
Препарат Релвар® Эллипта® не предназначен для купирования острых симптомов бронхиальной астмы или острых состояний при ХОБЛ, в таких случаях требуется назначение бронходилататоров короткого действия. Пациентам с бронхиальной астмой или ХОБЛ не следует прекращать лечение препаратом Релвар® Эллипта® без рекомендации врача, так как отмена терапии может привести к обострению заболевания.
На фоне лечения препаратом Релвар® Эллипта® могут развиваться нежелательные явления, связанные с течением бронхиальной астмы или обострением заболевания. Пациентам следует рекомендовать продолжить лечение. В случае отсутствия контроля над заболеванием или ухудшения состояния после начала терапии препаратом Релвар® Эллипта® необходима консультация врача.
Кардиоселективные бета-адреноблокаторы следует с осторожностью назначать пациентам, у которых наблюдались эпизоды бронхоспазма в анамнезе.
Парадоксальный бронхоспазм
Как и при других видах ингаляционной терапии, после приема препарата может развиваться парадоксальный бронхоспазм, сопровождающийся быстрым нарастанием свистящих хрипов. В этом случае показаны неотложное назначение ингаляционного бронходилататора короткого действия и немедленная отмена препарата Релвар® Эллипта®. Пациент должен быть осмотрен врачом, и ему, при необходимости, может быть назначена альтернативная терапия.
Кардиоваскулярные эффекты
Возможно развитие кардиоваскулярных эффектов, таких как сердечная аритмия (суправентрикулярная тахикардия и экстрасистолия), на фоне применения симпатомиметиков, включая препарат Релвар® Эллипта®, соответственно, препарат должен назначаться с осторожностью пациентам с кардиоваскулярными заболеваниями.
Печеночная недостаточность
У пациентов со средней и тяжелой печеночной недостаточностью максимальная доза препарата составляет 92мкг/22мкг и пациенты должны находиться под наблюдением на предмет развития побочных реакций на глюкокортикостероиды.
Системные эффекты кортикостероидов
При применении ингаляционных глюкокортикостероидов (особенно при длительном приеме в высоких дозах) могут развиваться системные побочные эффекты. Такие побочные эффекты развиваются значительно реже, чем при пероральном приеме глюкокортикостероидов. К проявлениям возможного неблагоприятного системного действия относятся: подавление функции гипоталамо-гипофизарно-надпочечниковой системы, снижение минеральной плотности костей, замедление скорости роста у детей и подростков, катаракта и глаукома.
Пневмония
У пациентов с ХОБЛ, получающих препарат Релвар® Эллипта®, наблюдалось повышение частоты развития пневмонии, а также частоты развития тяжелых форм пневмонии, требующих госпитализации пациента. В некоторых случаях клинические эпизоды пневмонии имели летальный исход. Врачам следует помнить о возможности развития пневмонии у пациентов с ХОБЛ, не забывая о том, что клинические признаки такого инфекционного заболевания маскируются симптомами обострения ХОБЛ. Наиболее высокий риск развития пневмонии на фоне приема препарата Релвар® Эллипта® имеют следующие группы пациентов с ХОБЛ: курящие пациенты, пациенты, ранее перенесшие пневмонию, пациенты с индексом массы тела < 25 кг/м2 и пациенты с объемом форсированного выдоха (ОФВ1) < 50 % от должных величин.
При назначении терапии препаратом Релвар® Эллипта® следует учитывать вышеуказанные факторы, в случае развития пневмонии необходима коррекция лечения.
У пациентов с бронхиальной астмой случаи развития пневмонии наблюдались не часто. Пациенты с бронхиальной астмой, получавшие препарат Релвар® Эллипта® в дозировке 184мкг+22мкг/доза, имели более высокий риск развития пневмонии в сравнении с пациентами, получавшими более низкую дозу препарата Релвар® Эллипта® (92мкг+22мкг/доза), или с группой плацебо. Факторы риска не установлены.
В ходе проведения клинических исследований у пациентов, страдающих ХОБЛ, была выявлена низкая частота возникновения переломов костей во всех лечебных группах, но при этом во всех группах, получавших комбинацию вилантерола и флутиказона фуроата, она была несколько выше (2 %), чем в группе, получавших монотерапию вилантеролом 22 мкг (< 1 %).
Гипергликемия
Отмечались сообщения о повышении уровня глюкозы крови у пациентов, страдающих сахарным диабетом, и это должно приниматься во внимание при назначении препарата Релвар® Эллипта® пациентам, страдающим сахарным диабетом.
Пациентам с редкими генетическими патологиями: непереносимостью галактозы или глюкозо-галактозной мальабсорбцией, не следует применять данный препарат.
Применение у детей
Препарат по показанию ХОБЛ у детей не применяется.
Безопасность и эффективность применения препарата Релвар® Эллипта® у детей младше 12 лет не установлена.
Детям от 12 до 18 лет при лечении бронхиальной астмы рекомендуется применение препарата Релвар® Эллипта® под контролем взрослых.
Фертильность
Данные по влиянию на фертильность человека отсутствуют. В доклинических исследованиях воздействия вилантерола и флутиказона фуроата на фертильность не обнаружено.
Беременность
Данные о применении препарата во время беременности ограничены.
Применение препарата Релвар® Эллипта® у беременных женщин допустимо только в том случае, если потенциальная польза для матери превышает возможный риск для плода.
Данных об экскреции вилантерола или флутиказона фуроата или их метаболитов в грудное молоко человека недостаточно. Однако другие глюкокортикостероиды и бета2-агонисты определяются в грудном молоке. Риск проникновения препарата вместе с молоком в организм новорожденного или ребенка не может быть исключен.
Принимая во внимание соотношение пользы терапии для матери и грудного вскармливания для ребенка, необходимо решить вопрос либо об отмене препарата, либо о прекращении грудного вскармливания.
Особенности влияния лекарственного средства на способность управлять транспортным средством или потенциально опасными механизмами
Исследования по изучению влияния препарата Релвар® Эллипта® на способность к вождению автотранспорта и работе с механизмами не проводились. Исходя из данных фармакологии вилантерола или флутиказона фуроата, неблагоприятное влияние препарата на эти виды деятельности не предполагается.
Передозировка
Симптомы: при проведении клинических исследований не было получено данных о передозировке комбинацией вилантерола и флутиказона фуроата.
Передозировка препаратом Релвар® Эллипта® может вызывать развитие симптомов и признаков, обусловленных действием отдельных компонентов препарата и характерных для передозировки бета2-агонистами и ингаляционными глюкокортикостероидами (см. раздел «Особые указания»).
Лечение: специфическое лечение отсутствует. В случае развития передозировки назначается симптоматическая терапия и, при необходимости, обеспечивается соответствующее наблюдение за больным.
Применение кардиоселективных бета-адреноблокаторов следует рассматривать только в случаях сильно выраженных эффектов передозировки вилантеролом.
Дальнейшее лечение рекомендовано согласно клиническим показаниям или в соответствии с рекомендациями национального токсикологического центра.
Форма выпуска и упаковка
Порошок для ингаляций дозированный, 92 мкг/22 мкг/доза, 184 мкг/22 мкг/доза.
По 30 доз помещают в пластиковый ингалятор с корпусом светло-серого цвета, бледно-голубой крышкой мундштука и счетчиком доз. Ингалятор содержит два алюминиевых ламинированных стрипа, каждый из которых состоит из 30 ячеек, которые содержат порошок белого цвета. Пластиковый ингалятор помещен в многослойный контейнер из алюминиевой фольги, содержащий влагопоглощающий пакетик с силикагелем. Контейнер запечатан легко открывающейся фольгой. По 1 контейнеру вместе с инструкцией по медицинскому применению на государственном и русском языках помещают в картонную пачку.
Условия хранения
Хранить при температуре не выше 25 ºС.
Хранить в недоступном для детей месте!
В случае, если препарат Релвар® Эллипта® хранился в холодильнике, необходимо перед использованием оставить ингалятор при комнатной температуре на один час.
Хранить ингалятор Эллипта® внутри герметичного контейнера для защиты от влаги. Вскрыть контейнер рекомендуется непосредственно перед первым применением.
На этикетке ингалятора Эллипта®, в отведенном для этого месте «Использовать до», необходимо написать дату окончания использования препарата.
Дата должна быть указана сразу после вскрытия герметичного контейнера.
Срок хранения
2 года.
Срок хранения после вскрытия контейнера: 6 недель.
Не применять по истечении срока годности.
Условия отпуска из аптек
По рецепту
Производитель
Глаксо Оперэйшенс Великобритания Лимитед (Глаксо Вэллком Оперэйшенс), Великобритания
(Priory Street, Ware, Hertfordshire, SG12 0DJ, United Kingdom)
Упаковщик
Глаксо Оперэйшенс Великобритания Лимитед (Глаксо Вэллком Оперэйшенс), Великобритания
(Priory Street, Ware, Hertfordshire, SG12 0DJ, United Kingdom)
Владелец регистрационного удостоверения
Глаксо Груп Лимитед, Великобритания
(980 Great West Road, Brentford, Middlesex TW8 9GS, United Kingdom)
Релвар и Эллипта являются зарегистрированными товарными знаками группы компаний «ГлаксоСмитКляйн»
Адрес организации, принимающей на территории Республики Казахстан претензии от потребителей по качеству продукции (товара)
Представительство ГлаксоСмитКляйн Экспорт Лтд в Казахстане
050059, г.Алматы, ул.Фурманова, 273
Номер телефона: +7 727 258 28 92, +7 727 259 09 96
Номер факса: + 7 727 258 28 90
Адрес электронной почты: kaz.med@gsk.com
Утвержденную инструкции по медицинскому применению смотрите также на сайте www.dari.kz
| 676500741477976396_ru.doc | 349 кб |
| 317428851477977647_kz.doc | 485 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Форма выпуска, состав и упаковка
порошок д/ингаляций дозированный (92 мкг+22 мкг)/доза: ингалятор 30 доз
Рег. №: 10352/15/15/19 от 31.12.2019 — Срок действия рег. уд. не ограничен
Порошок для ингаляций дозированный белого цвета.
| 1 доза | |
| вилантерол | 22 мкг |
| в виде вилантерола трифенатата микронизированного 40 мкг, в т.ч. номинальное количество вилантерола 25 мкг что соответствует доставленной дозе вилантерола 22 мкг |
Вспомогательные вещества: магния стеарат, лактозы моногидрат.
Порошок для ингаляций дозированный белого цвета.
| 1 доза | |
| флутиказона фуроат (микронизированный) | 92 мкг |
| флутиказона фуроат микронизированный 100 мкг, что соответствует доставленной дозе флутиказона фуроата 92 мкг |
Вспомогательные вещества: лактозы моногидрат.
30 доз — ингаляторы пластиковые (1) , корпус светло-серого цвета, бледно-голубой крышкой мундшрука и счетчиком доз; в комплекте с двумя алюм. ламинир. стрипами, в каждом по 30 ячеек — контейнеры из фольги алюминиевой многослойной (1) с влагопоглощ. пакетиком — пачки картонные.
порошок д/ингаляций дозированный (184 мкг+22 мкг)/доза: ингалятор 30 доз
Рег. №: 10352/15/15/19 от 31.12.2019 — Срок действия рег. уд. не ограничен
Порошок для ингаляций дозированный белого цвета.
| 1 доза | |
| вилантерол | 22 мкг |
| в виде вилантерола трифенатата микронизированного 40 мкг, в т.ч. номинальное количество вилантерола 25 мкг что соответствует доставленной дозе вилантерола 22 мкг |
Вспомогательные вещества: магния стеарат, лактозы моногидрат.
Порошок для ингаляций дозированный белого цвета.
| 1 доза | |
| флутиказона фуроат (микронизированный) | 184 мкг |
| флутиказона фуроат микронизированный 200 мкг*, что соответствует доставленной дозе флутиказона фуроата 184 мкг |
Вспомогательные вещества: лактозы моногидрат.
30 доз — ингаляторы пластиковые (1) , с корпусом свето-серого цвета, бледно-голубой крышкой мундштука и счетчиком доз; в комплекте с двумя алюм. ламинир. стрипами, каждый из 30 ячеек. — контейнеры из фольги алюминиевой многослойной (1) с влагопогл. пакетиком — пачки картонные.
Описание лекарственного препарата РЕЛВАР™ ЭЛЛИПТА™ основано на официально утвержденной инструкции по применению препарата и сделано в 2017 году. Дата обновления: 11.12.2017 г.
Фармакологическое действие
Механизм действия
Флутиказона фуроат и вилантерол представляют собой два класса лекарственных препаратов (синтетический кортикостероид и селективный агонист β2-рецепторов длительного действия).
Фармакодинамическое действие
Флутиказона фуроат
Флутиказона фуроат представляет собой синтетический трифторированный кортикостероид с выраженным противовоспалительным действием. Точный механизм воздействия флутиказона фуроата на симптомы астмы и хронической обструктивной болезни легких (ХОБЛ) неизвестен. Известно, что кортикостероиды широко воздействуют на многие типы клеток (например, эозинофилы, макрофаги, лимфоциты) и медиаторы (например, цитокины и хемокины, вовлеченные в воспалительный процесс).
Вилантерола трифенатат
Вилантерола трифенатат представляет собой селективный длительно действующий бета2-агонист (ДДБА).
Фармакологическое действие агонистов β2-адренорецепторов, включая вилантерола трифенатат, как минимум отчасти обусловлено стимуляцией внутриклеточной аденилциклазы – фермента, являющегося катализатором превращения аденозинтрифосфата (АТФ) в циклический-3’,5’-аденозинмонофосфат (циклический АМФ). Повышенные показатели уровня АМФ вызывают расслабление гладких мышц бронхов и ингибирование высвобождения медиаторов гиперчувствительности немедленного типа из клеток, в особенности из тучных клеток.
Между кортикостероидами и ДДБА происходит молекулярное взаимодействие, в результате чего стероиды активируют ген β2-рецепторов, тем самым повышая количество и чувствительность рецепторов. ДДБА подготавливают глюкокортикоидный рецептор к стероидозависимой активации и усиливают ядерную транслокацию в клетках. Данные синергидные взаимодействия находят отражение в повышенном противовоспалительном действии, наблюдавшемся in vitro и in vivo в ряде воспалительных клеток, имеющих отношение к патофизиологии как астмы, так и ХОБЛ. В ходе исследований биопсийного материала дыхательных путей в отношении флутиказона фуроата и вилантерола были также получены доказательства синергизма между кортикостероидами и ДДБА при применении клинических доз препаратов у пациентов с ХОБЛ.
Клиническая эффективность и безопасность
Астма
В ходе трех рандомизированных двойных слепых исследований III фазы (HZA106827, HZA106829 и HZA106837) различной продолжительности оценивались безопасность и эффективность комбинации флутиказона фуроат/вилантерол у взрослых пациентов и подростков с персистирующей астмой. Все пациенты принимали ИКС (ингаляционный кортикостероид) с или без ДДБА на протяжении минимум 12 недель до посещения 1. В исследовании HZA106837 у всех пациентов отмечалось как минимум одно обострение в течение года, предшествовавшего посещению 1, при котором требовалась терапия пероральными кортикостероидами. Продолжительность исследования HZA106827 составляла 12 недель. В ходе исследования оценивалась эффективность комбинации флутиказона фуроат/вилантерол 92/22 мкг [n=201] и флутиказона фуроата 92 мкг [n=205]) по сравнению с плацебо [n=203]. Все препараты принимались 1 раз/сут. Продолжительность исследования HZA106829 составляла 24 недели. В ходе исследования оценивалась эффективность комбинации флутиказона фуроат/вилантерол 184/22 мкг [n=197] и флутиказона фуроата 184 мкг [n=194]) при применении 1 раз/сут по сравнению с флутиказона пропионатом 500 мкг 2 раза/сут [n=195].
В исследованиях HZA106827/HZA106829 комбинированными первичными конечными точками оценки эффективности были изменение минимального показателя ОФВ1 в ходе клинического визита (до применения бронхолитического средства и до начала дозирования) в конце периода лечения у всех пациентов по сравнению с исходным уровнем и взвешенное среднее значение серийного ОФВ1 через 0-24 ч после приема дозы, вычисленное для подгруппы пациентов в конце периода терапии. Изменение процентного соотношения 24-часовых периодов без препаратов экстренной помощи по сравнению с исходным уровнем было вторичной конечной точкой. Результаты в отношении первичных и ключевых вторичных конечных точек данных исследований приведены в Таблице 1.
Таблица 1. Результаты в отношении первичных и ключевых вторичных конечных точек исследований HZA106827 и HZA106829
| № исследования | HZA106829 | HZA106827 | ||
| Доза ФФ/ВИ* (мкг) | ФФ/ВИ 184/22 1 раз/сут и ФФ 184 1 раз/сут | ФФ/ВИ 184/22 1 раз/сут и ФП 500 2 раза/сут | ФФ/ВИ 92/22 1 раз/сут и ФФ 92 1 раз/сут | ФФ/ВИ 92/22 1 раз/сут и плацебо 1 раз/сут |
| Изменение минимального показателя ОФВ1 с переносом вперед данных последнего наблюдения (ПВДПН) по сравнению с исходным уровнем | ||||
| Различия между препаратами Величина Р (95%-й ДИ) |
193 мл p<0.001 (108, 277) |
210 мл p<0.001 (127, 294) |
36 мл p=0.405 (-48, 120) |
172 мл p<0.001 (87, 258) |
| Взвешенное среднее значение серийного ОФВ1 через 0-24 ч после приема дозы | ||||
| Различия между препаратами Величина Р (95%-й ДИ) |
136 мл p=0.048 (1, 270) |
206 мл p=0.003 (73, 339) |
116 мл p=0.06 (-5, 236) |
302 мл p<0.001 (178, 426) |
| Изменение процентного соотношения 24-часовых периодов без препаратов экстренной помощи по сравнению с исходным уровнем | ||||
| Различия между препаратами Величина Р (95%-й ДИ) |
11.7% p<0.001 (4.9, 18.4) |
6.3% p=0.067 (-0.4, 13.1) |
10.6% p<0.001 (4.3, 16.8) |
19.3% p<0.001 (13.0, 25.6) |
| Изменение процентного соотношения 24-часовых периодов без проявления симптомов по сравнению с исходным уровнем | ||||
| Различия между препаратами | 8.4% | 4.9% | 12.1% | 18.0% |
| Величина Р (95%-й ДИ) |
p=0.010 (2.0, 14.8) |
p=0.137 (-1.6, 11.3) |
p<0.001 (6.2, 18.1) |
p<0.001 (12.0, 23.9) |
| Изменение утренней пиковой скорости выдоха по сравнению с исходным уровнем | ||||
| Различия между препаратами Величина Р (95%-й ДИ) |
33.5 л/мин p<0.001 (22.3, 41.7) |
32.9 л/мин p<0.001 (24.8, 41.1) |
14.6 л/мин p<0.001 (7.9, 21.3) |
33.3 л/мин p<0.001 (26.5, 40.0) |
| Изменение вечерней пиковой скорости выдоха по сравнению с исходным уровнем | ||||
| Различия между препаратами Величина Р (95%-й ДИ) |
30.7 л/мин p<0.001 (22.5, 38.9) |
26.2 л/мин p<0.001 (18.0, 34.3) |
12.3 л/мин p<0.001 (5.8, 18.8) |
28.2 л/мин p<0.001 (21.7, 34.8) |
*ФФ/ВИ = комбинация флутиказона фуроат/вилантерол
ФП = флутиказона пропионат
В исследовании HZA106837 применялась различная длительность терапии (минимальная продолжительность 24 недели, максимальная – 76 недель; у большинства пациентов продолжительность лечения составила минимум 52 недели). В исследовании HZA106837 пациенты были рандомизированы для получения комбинации флутиказона фуроат/вилантерол 92/22 мкг [n=1009] или ФФ 92 мкг [n=1010]. Оба препарата принимались 1 раз/сут. В исследовании HZA106837 первичной конечной точкой было время до первого тяжелого обострения астмы. Тяжелое обострение астмы определялось как ухудшение астмы, требующее применения системных кортикостероидов на протяжении не менее 3 дней, госпитализации в стационар или посещения отделения неотложной помощи вследствие астмы, требовавшей применения системных кортикостероидов. Скорректированное среднее изменение минимального ОФВ1 по сравнению с исходным уровнем также оценивалось как вторичная конечная точка.
В исследовании HZA106837 риск возникновения тяжелого обострения астмы у пациентов, получавших комбинацию флутиказона фуроат/вилантерол 92/22 мкг, снизился на 20% по сравнению с пациентами, получавшими только ФФ 92 мкг (отношение рисков 0.795, p=0.036 95%-й ДИ 0.642, 0.985). Коэффициент возникновения тяжелого обострения астмы у каждого пациента в год составил 0.19 в группе ФФ 92 мкг (приблизительно 1 в каждые 5 лет) и 0.14 в группе комбинации флутиказона фуроат/вилантерол 92/22 мкг (приблизительно 1 в каждые 7 лет). Соотношение частоты возникновения обострений при приеме комбинации флутиказона фуроат/вилантерол 92/22 мкг и ФФ 92 мкг составило 0.755 (95-й ДИ 0.603, 0.945). Отсюда следует, что снижение частоты возникновения тяжелых обострений астмы у пациентов, получавших комбинацию флутиказона фуроат/вилантерол 92/22 мкг, составило 25% по сравнению с пациентами, получавшими ФФ 92 мкг (p=0.014). 24-часовое бронхорасширяющее действие комбинации флутиказона фуроат/вилантерол сохранялось на протяжении периода терапии длительностью 1 год. Признаки потери эффективности не отмечались (тахифилаксия отсутствовала). При применении комбинации флутиказона фуроат/вилантерол 92/22 мкг наблюдалось устойчивое улучшение минимального показателя ОФВ1 от 83 мл до 95 мл на 12-й, 36-й и 52-й неделе, а также в конечной точке по сравнению с показателями при применении ФФ 92 мкг (p<0.001 95%-й ДИ 52, 126 мл в конечной точке). У 44% пациентов в группе флутиказона фуроат/вилантерол 92/22 мкг астма была хорошо контролируемой (ACQ7 ≤0.75) на момент окончания терапии. У пациентов в группе ФФ 92 мкг данный показатель составил 36% (p<0.001 95%-й ДИ 1.23, 1.82).
Исследования сравнения с комбинацией салметерол/флутиказона пропионат
В ходе исследования продолжительностью 24 недели (HZA113091) у взрослых пациентов и подростков с персистирующей астмой улучшение легочной функции по сравнению с исходным уровнем наблюдалось как при применении комбинации флутиказона фуроат/вилантерол 92/22 мкг 1 раз/сут вечером, так и при применении комбинации салметерол/ФП 50/250 мкг 2 раза/сут. Скорректированные средние показатели повышения взвешенного среднего значения ОФВ1 за период 0-24 ч на 341 мл на фоне терапии по сравнению с исходным уровнем (комбинация флутиказона фуроат/вилантерол) и на 377 мл (комбинация салметерол/ФП) свидетельствовали об общем улучшении легочной функции на протяжении 24 ч при применении обоих видов терапии. Скорректированное среднее значение разницы в зависимости от вида терапии между группами, составившее 37 мл, не являлось значимым со статистической точки зрения (p=0.162). В отношении минимального показателя ОФВ1 у пациентов в группе комбинации флутиказона фуроат/вилантерол наблюдалось изменение предела среднего значения по сравнению с исходным уровнем на 281 мл, а у пациентов в группе салметерол/ФП – на 300 мл; (разница в отношении скорректированного среднего значения 19 мл (95%-й ДИ:-0.073, 0.034) не являлась значимой со статистической точки зрения (p=0.485).
Сравнительные исследования с комбинациями салметерол/ФП или других ИКС/ДДБА, где бы надлежащим образом сравнивались эффекты на обострения астмы, не проводились.
Монотерапия флутиказона фуроатом
В ходе рандомизированного двойного слепого плацебо-контролируемого исследования продолжительностью 24 недели (FFA112059) оценивались безопасность и эффективность ФФ 92 мкг 1 раз/сут [n=114] и ФП 250 мкг 2 раза/сут [n=114] по сравнению с плацебо [n=115] у взрослых пациентов и подростков с персистирующей астмой. Все пациенты должны были получать стабильную дозу ИКС на протяжении не менее 4 недель до визита 1 (скрининговый визит). Применение ДДБА не разрешалось на протяжении 4 недель после визита 1. Первичной конечной точкой эффективности было изменение минимального показателя ОФВ1 во время клинического визита (до применения бронхолитического средства и до начала дозирования) в конце периода лечения по сравнению с исходным уровнем. Изменение процентного соотношения 24-часовых периодов без купирующей терапии по сравнению с исходным уровнем на протяжении периода лечения продолжительностью 24 недели было вторичной конечной точкой. Во временной точке 24 недели ФФ и ФП повысили минимальное значение ОФВ1 на 146 мл (95%-й ДИ 36, 257 мл, p=0.009) и 145 мл (95%-й ДИ 33, 257 мл, p=0.011), соответственно, по сравнению с плацебо. Оба препарата (ФФ и ФП) повысили процентное соотношение 24-часовых периодов без купирующей терапии на 14.8% (95%-й ДИ 6.9, 22.7, p<0.001) и 17.9% (95%-й ДИ 10.0, 25.7, p<0.001), соответственно, по сравнению с плацебо.
Исследование реакции на провокационный тест с аллергеном
Бронхопротекторное действие комбинации флутиказона фуроат/вилантерол 92/22 мкг на ранний и поздний астматический ответ на вдыхаемый аллерген оценивалось в ходе плацебо-контролируемого перекрестного исследования многократных доз с четырьмя периодами (HZA113126) у пациентов с легкой формой астмы. Пациенты были рандомизированы для получения комбинации флутиказона фуроат/вилантерол 92/22 мкг, ФФ 92 мкг, вилантерола 22 мкг или плацебо 1 раз/сут на протяжении 21 дня; через 1 ч после последней дозы осуществлялся ингаляционный тест с аллергеном. Использовались следующие аллергены: клещ домашней пыли, кошачья перхоть или пыльца березы. Отбор производился на основании скрининговых тестов. Результаты измерений серийного ОФВ1 сравнивались с показателями, полученными после ингаляции физиологического раствора до теста с аллергеном (исходный уровень). В целом, наибольшее влияние на ранний астматический ответ наблюдалось при применении комбинации флутиказона фуроат/вилантерол 92/22 мкг, по сравнению с ФФ 92 мкг или вилантеролом 22 мкг в виде монотерапии. Как комбинация флутиказона фуроат/вилантерол 92/22 мкг, так и ФФ 92 мкг фактически ликвидировали поздний астматический ответ по сравнению с вилантеролом в виде монотерапии. Применение комбинации флутиказона фуроат/вилантерол 92/22 мкг обеспечивало значительно большую защиту от гиперреактивности бронхов, вызванной аллергенами, чем монотерапия ФФ или вилантеролом. Оценка производилась в День 22 посредством провокационной пробы с метахолином.
Хроническая обструктивная болезнь легких
В программу клинических исследований ХОБЛ были включены следующие рандомизированные контролируемые исследования: одно продолжительностью 12 недель (HZC113107), два продолжительностью 6 месяцев (HZC112206, HZC112207) и два исследования продолжительностью 1 год (HZC102970, HZC102871) с участием пациентов с клиническим диагнозом ХОБЛ. В данных исследованиях изучались показатели функции легких, одышки, а также умеренных и тяжелых обострений заболевания.
Исследования продолжительностью 6 месяцев
HZC112206 и HZC112207 были рандомизированными двойными слепыми плацебо-контролируемыми исследованиями с параллельными группами продолжительностью 24 недели, в ходе которых проводилось сравнение действия комбинации с действием отдельно вилантерола и ФФ, а также плацебо. В исследовании HZC112206 оценивалась эффективность комбинации флутиказона фуроат/вилантерол 46/22 мкг [n=206] и комбинации флутиказона фуроат/вилантерол 92/22 мкг [n=206] в сравнении с эффективностью ФФ 92 мкг [n=206], вилантерола 22 мкг [n=205] и плацебо [n=207], все препараты принимались 1 раз/сут. В исследовании HZC112207 оценивалась эффективность комбинации флутиказона фуроат/вилантерол 92/22 мкг [n=204] и комбинации флутиказона фуроат/вилантерол 184/22 мкг [n=205] в сравнении с ФФ 92 мкг [n=204], ФФ 184 мкг [n=203] и вилантеролом 22 мкг [n=203] и плацебо [n=205], все препараты принимались 1 раз/сут.
Пациентам, участвовавшим в исследованиях, предъявлялись следующие требования: анамнез курения минимум 10 пачко-лет; соотношение ОФВ1/ФЖЕ после применения сальбутамола менее или равное 0.70; показатель ОФВ1 после применения сальбутамола менее или равный 70% от прогнозируемого значения, а также одышка ≥2 (шкала от 0 до 4) по модифицированной шкале опросника Британского медицинского исследовательского совета (mMRC) на этапе скрининга. Во время скрининга среднее значение ОФВ1 до применения бронхолитического средства составило 42.6% и 43.6% от прогнозируемого значения, средний показатель обратимости составил 15.9% и 12.0% в исследованиях HZC112206 и HZC112207, соответственно. Первичными конечными точками в обоих исследованиях были взвешенные средние значения ОФВ1 от 0 до 4 ч после получения дозы препарата в День 168 и изменение от исходного значения минимального показателя ОФВ1 до получения дозы препарата в День 169.
На основании полного анализа обоих исследований был сделан вывод, что применение комбинации флутиказона фуроат/вилантерол 92/22 мкг приводит к клинически значимому улучшению функции легких. В День 169 применение комбинации флутиказона фуроат/вилантерол 92/22 мкг и вилантерола привело к увеличению откорректированного среднего минимального показателя ОФВ1 на 129 мл (95%-й ДИ: 91, 167 мл, p <0.001) и 83 мл (95%-й ДИ: 46, 121 мл, p <0.001), соответственно, в сравнении с плацебо. Использование комбинации флутиказона фуроат/вилантерол 92/22 мкг привело к увеличению минимального показателя ОФВ1 на 46 мл в сравнении с вилантеролом (95%-й ДИ: 8, 83 мл, p=0.017). В День 168 применение комбинации флутиказона фуроат/вилантерол 92/22 мкг и вилантерола привело к увеличению откорректированного взвешенного среднего значения ОФВ1 на протяжении 0-4 ч на 193 мл (95%-й ДИ: 156, 230 мл, p <0.001) и 145 мл (95%-й ДИ: 108, 181 мл, p <0.001), соответственно, в сравнении с плацебо. Применение комбинации флутиказона фуроат/вилантерол 92/22 мкг привело к росту скорректированного среднего взвешенного среднего значения ОФВ1 на протяжении 0-4 ч на 148 мл в сравнении с применением отдельно ФФ (95%-й ДИ: 112, 184 мл, p <0.001).
Исследования продолжительностью 12 месяцев
Исследования HZC102970 и HZC102871 были рандомизированными двойными слепыми исследованиями с параллельными группами продолжительностью 52 недели, в ходе которых проводилось сравнение действия комбинации флутиказона фуроат/вилантерол 184/22 мкг, комбинации флутиказона фуроат/вилантерол 92/22 мкг, комбинации флутиказона фуроат/вилантерол 46/22 мкг и вилантерола 22 мкг (все препараты применялись 1 раз/сут) на годовой показатель развития умеренных/тяжелых обострений болезни у пациентов с ХОБЛ с анамнезом курения минимум 10 пачко-лет; соотношением ОФВ1/ФЖЕ после применения сальбутамола менее или равным 0.70; показателем ОФВ1 после применения сальбутамола менее или равным 70% от прогнозируемого значения и документально подтвержденной историей ≥1 обострения ХОБЛ, при котором потребовалась терапия антибиотиками и/или пероральными кортикостероидами или госпитализация за период в 12 месяцев до визита 1. Первичной конечной точкой был годовой показатель развития умеренных и тяжелых обострений болезни. Умеренные/тяжелые обострения определялись как усиление симптомов, которое потребовало терапии пероральными кортикостероидами и/или антибиотиками или госпитализации в стационар. В обоих исследованиях был 4-недельный вводный период, в течение которого все испытуемые получали немаскированную комбинацию салметерол/ФП 50/250 2 раза/сут с целью стандартизовать фармакотерапию ХОБЛ и стабилизировать заболевания до рандомизации для применения маскированного исследуемого лекарственного препарата в течение 52 недель. До начала вводного периода участники исследования прекращали прием ранее использованных лекарственных препаратов для терапии ХОБЛ за исключением бронхолитических средств короткого действия. Использование одновременно применяемых ингалируемых бронхолитических средств длительного действия (бета2-агонистов и антихолинергических средств), комбинированных препаратов, содержащих ипратропий/сальбутамол, пероральных бета2-агонистов и препаратов теофиллина не разрешалось в течение всего периода терапии. Допускалось использование пероральных кортикостероидов и антибиотиков для неотложного лечения обострений ХОБЛ в соответствии с особыми рекомендациями. В течение исследований участники по мере необходимости применяли сальбутамол.
Результаты обоих исследований свидетельствуют, что терапия комбинацией флутиказона фуроат/вилантерол 92/22 мкг 1 раз/сут приводит к снижению годового показателя развития умеренных/тяжелых обострений ХОБЛ в сравнении с терапией вилантеролом (Таблица 2).
Таблица 2: Анализ частоты возникновения обострений через 12 месяцев терапии
|
Конечная точка |
HZC102970 | HZC102871 | HZC102970 и HZC102871 (интегрированный анализ) | |||
| Вилантерол (n=409) | флутиказона фуроат/вилантерол 92/22 (n=403) | Вилантерол (n=409) | флутиказона фуроат/вилантерол 92/22 (n=403) | Вилантерол (n=818) | флутиказона фуроат/вилантерол 92/22 (n=806) | |
| Умеренные и тяжелые обострения | ||||||
| Скорректированный средний годовой уровень | 1.14 | 0.90 | 1.05 | 0.70 | 1.11 | 0.81 |
| Соотношение с ВИ 95%-й ДИ величина р % снижения (95%-й ДИ) |
0.79 (0.64, 0.97) 0.024 21 (3, 36) |
0.66 (0.54, 0.81) <0.001 34 (19, 46) |
0.73 (0.63, 0.84) <0.001 27 (16, 37) |
|||
| Абсолютная разница в количестве в год по сравнению с вилантеролом (95%-й ДИ) |
0.24 (0.03, 0.41) |
0.36 (0.20, 0.48) |
0.30 (0.18, 0.41) |
|||
| Время до первого обострения: Отношение рисков (95%-й ДИ) % снижения риска величина р |
0.80 |
0.72 |
0.76 |
По результатам интегрированного анализа исследований HZC102970 и HZC102871 на неделе 52, при применении комбинации флутиказона фуроат/вилантерол 92/22 мкг наблюдалось улучшение скорректированного среднего показателя минимального ОФВ1 по сравнению с вилантеролом 22 мкг (42 мл 95%-й ДИ: 19, 64 мл, p<0.001). 24-часовое бронхорасширяющее действие комбинации флутиказона фуроат/вилантерол сохранялось с момента приема первой дозы и на протяжении периода терапии длительностью 1 год. Признаки потери эффективности не отмечались (тахифилаксия отсутствовала).
В совокупности в двух исследованиях сердечно-сосудистые заболевания в анамнезе или факторы риска их возникновения были отмечены у 2009 (62%) пациентов в процессе отбора. Частота сердечно-сосудистых заболеваний/факторов риска была идентичной во всех группах терапии, при этом чаще всего отмечались следующие заболевания: гипертензия (46%), гиперхолестеринемия (29%) и сахарный диабет (12%). Сходное снижение частоты умеренных и тяжелых обострений наблюдалось в данной подгруппе по сравнению со всей популяцией. У пациентов с сердечно-сосудистыми заболеваниями и факторами риска в анамнезе применение комбинации флутиказона фуроат/вилантерол 92/22 мкг привело к значительному снижению ежегодной частоты возникновения среднетяжелых/тяжелых обострений ХОБЛ по сравнению с вилантеролом (скорректированные средние годовые показатели частоты возникновения 0.83 и 1.18, соответственно, 30%-е снижение (95%-й ДИ 16, 42%, p<0.001)). На неделе 52 при применении комбинации флутиказона фуроат/вилантерол 92/22 мкг также наблюдалось улучшение скорректированного среднего показателя минимального ОФВ1 по сравнению с вилантеролом 22 мкг (44 мл 95%-й ДИ: 15, 73 мл, (p=0.003)).
Исследования сравнения с комбинацией салметерол/флутиказона пропионат
В ходе исследования продолжительностью 12 недель (HZC113107) у пациентов с ХОБЛ улучшение легочной функции по сравнению с исходным уровнем наблюдалось как при применении комбинации флутиказона фуроат/вилантерол 92/22 мкг 1 раз/сут утром, так и при применении комбинации салметерол/ФП 50/500 мкг 2 раза/сут. Скорректированные средние показатели повышения взвешенного среднего значения ОФВ1 за период 0-24 ч на 130 мл на фоне терапии по сравнению с исходным уровнем (комбинация флутиказона фуроат/вилантерол) и на 108 мл (комбинация салметерол/ФП) свидетельствовали об общем улучшении легочной функции на протяжении 24 ч при применении обоих видов терапии. Скорректированное среднее значение разницы в зависимости от вида терапии между группами 22 мл (95%-й ДИ: -18, 63 мл) не являлось статистически значимым (p=0.282). Скорректированное среднее изменение минимального ОФВ1 по сравнению с исходным уровнем в момент времени День 85 составило 111 мл в группе комбинации флутиказона фуроат/вилантерол и 88 мл в группе комбинации салметерол/ФП; разница, составлявшая 23 мл (95%-й ДИ: -20, 66) между группами терапии, не была значимой с клинической или статистической точки зрения (p=0.294).
Сравнительные исследования с комбинациями салметерол/ФП или другими общепринятыми бронхолитическими средствами, где бы надлежащим образом сравнивалось действие на обострения ХОБЛ, не проводились.
Дети
Европейское агентство по оценке лекарственных средств отказалось от обязательного представления результатов исследований препарата Релвар™ Эллипта™ во всех подмножествах педиатрической популяции по ХОБЛ (информацию по применению у пациентов детского возраста смотрите в разделе «Режим дозирования»).
Европейское агентство по оценке лекарственных средств отложило обязательное представление результатов исследований препарата Релвар™ Эллипта™ во всех подмножествах педиатрической популяции в отношении астмы (информацию по применению у пациентов детского возраста смотрите в разделе «Режим дозирования»).
Фармакокинетика
Всасывание
Абсолютная биодоступность флутиказона фуроата и вилантерола при ингаляционном применении в виде комбинации флутиказона фуроат/вилантерол в среднем составила 15.2% и 27.3% соответственно. Биодоступность флутиказона фуроата и вилантерола при приеме внутрь была низкой и в среднем составляла 1.26% и <2% соответственно. С учетом низкой биодоступности при приеме внутрь системное воздействие флутиказона фуроата и вилантерола при ингаляционном введении в первую очередь обусловлено всасыванием части ингаляционной дозы, поступившей в легкие.
Распределение
После в/в введения флутиказона фуроат и вилантерол широко распределяются по организму. Средние показатели Vd в равновесном состоянии составляют 661 л и 165 л соответственно.
Оба препарата – флутиказона фуроат и вилантерол – имеют слабую связь с эритроцитами. In vitro связывание с белками плазмы крови человека флутиказона фуроата и вилантерола было высоким и в среднем составляло >99.6% и 93.9% соответственно. Снижение степени связывания с белками плазмы у пациентов с почечной или печеночной недостаточностью не наблюдалось.
Флутиказона фуроат и вилантерол являются субстратами Р-гликопротеина (Р-гп). Тем не менее, считается, что одновременное применение комбинации флутиказона фуроат/вилантерол с ингибиторами Р-гп не изменяет системное воздействие флутиказона фуроата или вилантерола, поскольку оба препарата представляют собой хорошо абсорбируемые молекулы.
Метаболизм
На основании данных исследований in vitro, основные пути метаболизма флутиказона фуроата и вилантерола у человека преимущественно опосредованы CYP3A4.
Флутиказона фуроат метаболизируется главным образом посредством гидролиза группы S-фторметилового эфира карботиокислоты в метаболиты со значительно сниженной активностью кортикостероидов. Вилантерол метаболизируется преимущественно посредством О-деалкилирования в ряд метаболитов со значительно сниженной активностью бета1— и бета2-агонистов.
Выведение
После приема внутрь у человека флутиказона фуроат выводится преимущественно в виде метаболитов, которые выделяются практически исключительно с калом. С мочой выводится <1% восстановленной радиоактивной дозы.
После приема внутрь у человека вилантерол выводится преимущественно посредством метаболизма. Метаболиты выделяются с мочой и калом (70% и 30% радиоактивной дозы соответственно). Т1/2 вилантерола из плазмы после однократного ингаляционного введения комбинации флутиказона фуроат/вилантерол составил в среднем 2.5 ч. Эффективный Т1/2 для накопления вилантерола составляет 16 ч у пациентов с астмой и 21.3 ч у пациентов с ХОБЛ, что было установлено в результате ингаляционного введения многократных доз вилантерола 25 мкг.
Фармакокинетика у особых групп пациентов
Дети
У подростков (12 лет или старше) изменение дозировки не рекомендуется.
Фармакокинетика комбинации флутиказона фуроат/вилантерол у пациентов в возрасте младше 12 лет не изучена. Безопасность и эффективность комбинации флутиказона фуроат/вилантерол у детей в возрасте младше 12 лет не установлены.
Пациенты пожилого возраста (>65 лет)
Влияние возраста на фармакокинетику флутиказона фуроата и вилантерола было установлено в исследованиях III фазы с участием пациентов с ХОБЛ и астмой. Нет доказательств того, что возраст (12-84) влияет на фармакокинетику флутиказона фуроата и вилантерола у пациентов с астмой.
Нет доказательств того, что возраст влияет на фармакокинетику флутиказона фуроата у пациентов с ХОБЛ, тогда как отмечалось повышение (37%) показателя AUC (0-24) вилантерола в возрастном диапазоне от 41 до 84 лет. У пациента пожилого возраста (84 года) с низкой массой тела (35 кг) предполагается, что показатель AUC (0-24) вилантерола будет на 35% выше предполагаемого значения по популяции (пациент с ХОБЛ в возрасте 60 лет и массой тела 70 кг), тогда как показатель Cmax оставался неизменным. Маловероятно, что данные различия являются значимыми с клинической точки зрения.
Рекомендации по изменению режима дозирования у пациентов с астмой и пациентов с ХОБЛ отсутствуют.
Почечная недостаточность
Исследование клинической фармакологии комбинации флутиказона фуроат/вилантерол показало, что тяжелая почечная недостаточность (КК <30 мл/мин) не приводила к значительно большей экспозиции флутиказона фуроата или вилантерола или более выраженному системному воздействию кортикостероидов или бета2-агонистов по сравнению с показателями у пациентов с нормальной функцией почек. Коррекции режима дозирования у пациентов с почечной недостаточностью не требуется.
Влияние гемодиализа не изучено.
Печеночная недостаточность
После применения многократных доз комбинации флутиказона фуроат/вилантерол на протяжении 7 дней наблюдалось усиление системного воздействия флутиказона фуроата (до трехкратного увеличения по измерению показателя AUC(0-24)) у пациентов с печеночной недостаточностью (А, В или С по классификации Чайлд-Пью) по сравнению со здоровыми субъектами. Усиление системного воздействия флутиказона фуроата у пациентов с умеренной печеночной недостаточностью (В по классификации Чайлд-Пью; комбинация флутиказона фуроат/вилантерол 184/22 мкг) ассоциировалось со средним снижением уровня кортизола в сыворотке на 34% по сравнению со здоровыми субъектами. Нормализованное по дозе системное воздействие флутиказона фуроата было идентичным у пациентов с умеренной и тяжелой печеночной недостаточностью (В или С по классификации Чайлд-Пью).
После применения многократных доз комбинации флутиказона фуроат/вилантерол на протяжении 7 дней не наблюдалось существенного усиления системного воздействия вилантерола (Cmax и AUC) у пациентов с легкой, умеренной или тяжелой печеночной недостаточностью (А, В или С по классификации Чайлд-Пью).
Комбинация флутиказона фуроат/вилантерол не оказывает значимое с клинической точки зрения воздействие на бета-адренергические системные эффекты (частота сердечных сокращений или концентрация калия в сыворотке) у пациентов с легкой или умеренной печеночной недостаточностью (вилантерол, 22 мкг) или с тяжелой печеночной недостаточностью (вилантерол, 12.5 мкг) по сравнению со здоровыми субъектами.
Другие особые группы пациентов
У пациентов из Восточной Азии, Японии или Юго-Восточной Азии с астмой (12-13% пациентов) предполагаемое значение AUC (0-24) флутиказона фуроата было в среднем на 33%-53% выше по сравнению с представителями других расовых групп. Тем не менее, не было получено доказательств того, что более высокое системное воздействие у пациентов данной популяции связано с более сильным влиянием на выделение кортизола с мочой за 24 ч. В среднем, предполагается, что показатель Cmax вилантерола будет на 220-287% выше, а показатель AUC (0-24) у пациентов азиатского происхождения будет сопоставим с аналогичным показателем у пациентов из других расовых групп. Тем не менее, не было получено доказательств того, что данный более высокий показатель Cmax вилантерола приводил к клинически значимому влиянию на ЧСС.
У пациентов из Восточной Азии, Японии или Юго-Восточной Азии с ХОБЛ (13-14% пациентов) предполагаемое значение AUC (0-24) флутиказона фуроата было в среднем на 23%-30% выше по сравнению с представителями европеоидной расы. Тем не менее, не было получено доказательств того, что более высокое системное воздействие у пациентов данной популяции связано с более сильным влиянием на выделение кортизола с мочой за 24 ч. У пациентов с ХОБЛ расовая принадлежность не оказывала влияния на расчетные фармакокинетические параметры вилантерола.
Пол, масса тела и ИМТ
В результате популяционного фармакокинетического анализа III фазы не были получены доказательства того, что пол, масса тела или ИМТ (индекс массы тела) влияют на фармакокинетику флутиказона фуроата. Анализ проводился на основании данных у 1213 пациентов с астмой (712 женщин) и 1225 пациентов с ХОБЛ (392 женщины).
В результате популяционного фармакокинетического анализа не были получены доказательства того, что пол, масса тела или ИМТ влияют на фармакокинетику вилантерола. Анализ проводился на основании данных у 856 пациентов с астмой (500 женщин) и 1091 пациентов с ХОБЛ (340 женщин).
Коррекции режима дозирования на основании пола, массы тела или ИМТ не требуется.
Показания к применению
Астма
Препарат Релвар™ Эллипта™ показан для регулярного лечения астмы у взрослых пациентов и подростков в возрасте 12 лет и старше в тех случаях, когда целесообразно применение комбинированного лекарственного препарата (бета2-агонист длительного действия и ингаляционный кортикостероид):
— у пациентов с недостаточным контролем заболевания на фоне терапии ингаляционными кортикостероидами и периодического использования ингаляционного бета2-адреномиметика короткого действия «по требованию».
ХОБЛ (хроническая обструктивная болезнь легких)
Препарат Релвар™ Эллипта™ показан для терапии симптомов ХОБЛ у взрослых пациентов с ОФВ1 <70% от прогнозируемого значения (после применения бронхолитического средства) с обострениями заболевания в анамнезе, несмотря на регулярную терапию бронхолитическими препаратами.
Реклама
Режим дозирования
Астма
Взрослые и подростки в возрасте 12 лет и старше
Одна ингаляция препарата Релвар™ Эллипта™ 92/22 мкг или 184/22 мкг 1 раз/сут.
У пациентов, как правило, улучшается функция легких в течение 15 мин после вдыхания препарата Релвар™ Эллипта™. Однако пациента следует проинформировать, что для поддержания контроля над симптомами астмы требуется регулярное ежедневное применение препарата, которое необходимо продолжать даже при отсутствии симптомов.
В случае если симптомы заболевания появляются между приемами препарата, для быстрого облегчения следует использовать бета2-агонисты короткого действия.
Необходимо рассмотреть возможность применения начальной дозы препарата Релвар™ Эллипта™ 92/22 мкг у взрослых пациентов и подростков в возрасте с 12 лет, которым требуются низкие или средние дозы ингаляционных кортикостероидов в комбинации с бета2-агонистом длительного действия. Если не удается обеспечить адекватный контроль при помощи препарата Релвар™ Эллипта™ 92/22 мкг, дозу можно увеличить до 184/22 мкг, что позволит дополнительно улучшить контроль астмы.
Работникам здравоохранения необходимо проводить регулярное обследование пациентов для того, чтобы убедиться, что дозировка получаемой комбинации флутиказона фуроат/вилантерол остается оптимальной, изменение дозировки допускается только по указанию врача. Дозу следует титровать до самой низкой дозы, при которой достигается эффективный контроль симптомов заболевания.
Необходимо рассмотреть возможность применения препарата Релвар™ Эллипта™ 184/22 мкг у взрослых пациентов и подростков в возрасте 12 лет и старше, которым требуется более высокая доза ингалируемого кортикостероида в комбинации с бета2-агонистом длительного действия.
Максимальная рекомендуемая доза Релвар™ Эллипта™ составляет 184/22 мкг 1 раз/сут.
Пациентам с астмой следует назначать такую дозу препарата Релвар™ Эллипта™, которая содержит флутиказона фуроат (ФФ) в количестве, соответствующем тяжести заболевания. Медицинские работники, назначающие рецептурные препараты, должны знать, что для пациентов страдающих астмой, 100 мкг флутиказона фуроата (ФФ) 1 раз/сут приблизительно эквивалентно 250 мкг флутиказона пропионата (ФП) 2 раза/сут, в то время как 200 мкг ФФ 1 раз/сут приблизительно эквивалентно 500 мкг ФП 2 раза/сут.
Дети в возрасте до 12 лет
Безопасность и эффективность применения препарата Релвар™ Эллипта™ для лечения астмы у детей в возрасте до 12 лет не установлены.
ХОБЛ
Взрослые (18 лет и старше)
Одна ингаляция препарата Релвар™ Эллипта™ 92/22 мкг 1 раз/сут.
Пациентам с ХОБЛ не показан препарат Релвар™ Эллипта™ 184/22 мкг. Применение дозировки 184/22 мкг в сравнении с дозировкой 92/22 мкг у пациентов с ХОБЛ не приносит дополнительной пользы, кроме того потенциально усиливается риск развития пневмонии и системных нежелательных реакций, вызванных кортикостероидами (см. разделы «Особые указания» и «Побочное действие»).
У пациентов, как правило, улучшается функция легких в течение 16-17 мин после вдыхания препарата Релвар™ Эллипта™.
Дети
Применение препарата Релвар™ Эллипта™ для лечения ХОБЛ у детей нецелесообразно.
Особые группы пациентов
Для пациентов пожилого возраста (>65 лет) коррекция дозы не требуется (см. раздел «Фармакокинетика»).
Для пациентов с почечной недостаточностью коррекция дозы не требуется (см. раздел «Фармакокинетика»).
В исследованиях с участием пациентов с печеночной недостаточностью легкой, средней и тяжелой степени было выявлено усиление системного воздействия флутиказона фуроата (в отношении как Cmax, так и AUC) (см. раздел «Фармакокинетика»). При подборе дозы пациентам с печеночной недостаточностью следует соблюдать осторожность, поскольку у них наблюдается повышенный риск развития системных нежелательных реакций, вызванных кортикостероидами. Для пациентов с печеночной недостаточностью средней или тяжелой степени максимальная доза составляет 92/22 мкг (см. раздел «Особые указания»).
Способ применения
Препарат Релвар™ Эллипта™ предназначен только для проведения ингаляций.
Препарат следует использовать в одно и то же время каждый день. Окончательное решение относительно времени применения (в дневное или вечернее время суток) остается за лечащим врачом.
Если прием препарата был пропущен, следующую дозу необходимо принять в обычное время на следующий день.
При хранении препарата в холодильнике необходимо перед использованием выдержать ингалятор минимум в течение часа при комнатной температуре.
После проведения ингаляции пациенту следует прополоскать рот водой, воду не глотать.
При первом применении ингалятора нет необходимости проверять его исправность и особым образом подготавливать его к использованию. Следует придерживаться подробной инструкции.
Ингалятор Эллипта™ находится в контейнере, в который также помещен пакетик с поглотителем влаги для понижения уровня влажности. После вскрытия контейнера пакетик необходимо удалить.
Пациентов стоит проинструктировать не открывать контейнер до тех пор, пока они не готовы вдохнуть дозу лекарственного средства.
Когда ингалятор извлекают из контейнера, он находится в «закрытом» состоянии. После открытия контейнера ингалятор следует использовать в течение 6 недель. Ингалятор не следует использовать после истечения данного периода. После вскрытия контейнер можно выкинуть. Не следует открывать ингалятор до тех пор, пока пациент не будет готов ингалировать дозу лекарственного препарата.
Подробная пошаговая инструкция к 30-дозовому ингалятору Эллипта™, приведенная ниже, подходит также для 14-дозового ингалятора Эллипта™.
Пациенту необходимо прочитать следующую информацию перед использованием.
При открытии и закрытии крышки ингалятора Эллипта™ без приема лекарственного препарата происходит потеря одной дозы. Эта доза остается закрытой внутри ингалятора, но она будет недоступна для приема. Невозможно случайно получить большую дозу или двойную дозу за одну ингаляцию.
Одна доза лекарственного препарата готова к ингаляции после каждого открытия крышки.
Счетчик доз показывает, сколько доз лекарственного препарата осталось в ингаляторе.
Перед началом использования ингалятора счетчик доз показывает число 30.
При каждом открытии крышки количество доз уменьшается на 1.
Когда остается менее 10 доз, половина счетчика становится красной.
После того, как израсходована последняя доза препарата, половина счетчика выделена красным цветом, счетчик показывает цифру 0. Это означает, что ингалятор пуст. Если открыть крышку после этого, счетчик доз станет полностью красным.
Подготовка дозы
Не следует открывать крышку, пока пациент не будет готов к приему препарата.
Не встряхивать ингалятор.
1. Опустить крышку вниз до щелчка.
2. Доза препарата готова к ингаляции, и в подтверждение этого счетчик доз уменьшает число доз на единицу.
3. Если счетчик доз не уменьшил число доз после того, как послышался щелчок, ингалятор не готов к подаче дозы лекарственного препарата. В этом случае следует обратиться в аптеку.
Ингаляция лекарственного препарата
1. Удерживая ингалятор на некотором расстоянии ото рта, сделать выдох максимальной глубины. Не выдыхать в ингалятор.
2. Поместить мундштук между губами и плотно обхватить его губами (губы должны точно повторять форму ингалятора). Не закрывать пальцами вентиляционное отверстие.
3. Сделать один глубокий, долгий, равномерный вдох. Задержать дыхание насколько возможно (по крайней мере, на 3-4 секунды).
4. Убрать ингалятор изо рта.
5. Медленно и спокойно выдохнуть.
Пациент может не почувствовать вкус или не ощутить поступление лекарственного препарата даже при правильном использовании ингалятора.
Закрытие ингалятора и полоскание ротовой полости
Если необходимо протереть мундштук, следует использовать сухую бумажную салфетку перед закрытием крышки.
1. Поднять крышку до упора, добившись полного закрытия мундштука.
2. После ингаляции следует прополоскать рот водой. Это снизит вероятность развития таких побочных явлений, как боль в горле и полости рта.
Побочные действия
Обзор профиля безопасности
Данные, полученные в результате масштабных клинических исследований астмы и ХОБЛ, были использованы для определения частоты развития неблагоприятных побочных реакций, вызванных применением комбинации флутиказона фуроат/вилантерол. В комплексную оценку побочных реакций в ходе программы клинических исследований астмы было включено в целом 7034 пациента. В комплексную оценку побочных реакций в ходе программы клинических исследований ХОБЛ было включено в целом 6237 пациентов.
Наиболее часто в связи с применением флутиказона фуроата и вилантерола сообщалось о таких неблагоприятных побочных реакциях как головная боль и назофарингит. За исключением пневмонии и переломов костей профиль безопасности был одинаковым для пациентов с астмой и ХОБЛ. В клинических исследованиях случаи пневмонии и переломов более часто отмечались у пациентов с ХОБЛ.
Перечень побочных реакций
Неблагоприятные побочные реакции внесены в список в соответствии с системно-органным классом и частотой возникновения. Частота возникновения определялась следующим образом: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); редко (от ≥1/10 000 до <1000); очень редко (<1/10 000).
В каждой частотной группе неблагоприятные побочные реакции расположены в порядке убывания степени серьезности.
Инфекции и инвазии: часто — пневмония*, инфекция верхних дыхательных путей, бронхит, грипп, кандидоз ротовой полости и горла.
Со стороны иммунной системы: редко — реакции гиперчувствительности, включая анафилаксию, ангионевротический отек, сыпь и крапивницу.
Со стороны нервной системы: очень часто — головная боль; редко — тремор.
Со стороны психики: редко — беспокойство.
Со стороны сердечно-сосудистой системы: нечасто — экстрасистолия; редко — учащенное сердцебиение, тахикардия.
Со стороны дыхательной системы: очень часто — назофарингит; часто — боль в орофарингеальной области, синусит, фарингит, ринит, кашель, дисфония.
Со стороны ЖКТ: часто — боль в области живота.
Со стороны костно-мышечной системы: часто — артралгия, боль в спине, переломы костей**, мышечные спазмы.
Общие расстройства и реакции в месте введения: часто — пирексия.
*, ** Смотрите ниже «Описание отдельных побочных реакций».
Описание отдельных побочных реакций
Пневмония
В результате объединенного анализа двух повторных годичных исследований у пациентов с ХОБЛ с обострением в предшествующем году (n=3255) количество случаев пневмонии на 1000 пациенто-лет составило 97.9 в группе ФФ/ВИ 184/22, 85.7 в группе ФФ/ВИ 92/22 и 42.3 в группе ВИ 22. Для тяжелой пневмонии соответствующее количество явлений на 1000 пациенто-лет составило 33.6, 35.5, и 7.6 соответственно, в то время как количество случаев серьезной пневмонии на 1000 пациенто-лет составило 35.1 в группе ФФ/ВИ 184/22, 42.9 в группе ФФ/ВИ 92/22, 12.1 в группе ВИ 22. Число случаев пневмонии с летальным исходом, скорректированное в зависимости от дозировки, составило 8.8 в группе ФФ/ВИ 184/22 в сравнении с 1.5 в группе ФФ/ВИ 92/22 и 0 в группе ВИ 22.
В объединенном анализе 11 исследований астмы (7034 пациента) частота возникновения пневмонии на 1000 пациенто-лет составила 18.4 в группе ФФ/ВИ 184/22 в сравнении с 9.6 в группе ФФ/ВИ 92/22 и 8.0 в группе плацебо.
Переломы костей
В двух повторных исследованиях продолжительностью 12 месяцев с участием 3255 пациентов с ХОБЛ общая частота возникновения переломов костей была низкой во всех группах терапии, с более высокими показателями в группах, получавших препарат Релвар™ Эллипта™ (2%) в сравнении с группой, получавшей вилантерол 22 мкг (<1%). Несмотря на то, что в группах, получавших Релвар™ Эллипта™, было отмечено большее количество переломов в сравнении с группой, получавшей вилантерол 22 мкг, переломы обычно связанные с применением кортикостероидов (например, компрессионный перелом позвоночника/перелом позвонка в пояснично-грудном отделе, переломы шейки бедра и вертлужной впадины) отмечались в <1% случаев в группах терапии препаратами Релвар™ Эллипта™ и вилантеролом.
В результате объединенного анализа 11 исследований астмы (7034 пациентов) частота возникновения переломов составила <1%, как правило, переломы являлись следствием травмы.
Применение при беременности и кормлении грудью
Беременность
В исследованиях на животных была выявлена репродуктивная токсичность при применении доз, не используемых в клинической практике. Данные о применении флутиказона фуроата и вилантерола трифенатата беременными женщинами отсутствуют или являются недостаточными.
Беременным женщинам следует назначать комбинацию флутиказона фуроат/вилантерол только в том случае, когда предполагаемая польза для матери превосходит возможный риск для плода.
Грудное вскармливание
Информация о выделении флутиказона фуроата или вилантерола трифенатата и/или их метаболитов в грудное молоко недостаточна. Однако другие кортикостероиды и бета2-агонисты обнаруживают в женском молоке. Нельзя исключить риск для новорожденных/младенцев, находящихся на грудном вскармливании.
Необходимо принять решение о прерывании грудного вскармливания или прекращении применения комбинации флутиказона фуроат/вилантерол, учитывая пользу грудного кормления для ребенка и благоприятное воздействие терапии на женщину.
Фертильность
Данные о влиянии на фертильность человека отсутствуют. Исследования на животных не выявили воздействия комбинации флутиказона фуроат/вилантерола трифенатат на фертильность.
Применение при нарушениях функции печени
При подборе дозы пациентам с печеночной недостаточностью следует соблюдать осторожность, поскольку у них наблюдается повышенный риск развития системных нежелательных реакций, вызванных кортикостероидами.
Применение у детей
Безопасность и эффективность применения препарата Релвар™ Эллипта™ для лечения астмы у детей в возрасте до 12 лет не установлены.
Применение препарата Релвар™ Эллипта™ для лечения ХОБЛ у детей нецелесообразно.
Особые указания
Обострение заболевания
Комбинацию флутиказона фуроат/вилантерол не следует использовать для терапии острых симптомов астмы или острого приступа ХОБЛ, для таких случаев требуются бронхолитические средства короткого действия. Более частое применение бронхолитических средств для устранения симптомов означает ослабление контроля, пациенту следует обратиться к врачу.
Пациентам не следует прекращать применение комбинации флутиказона фуроат/вилантерол для лечения астмы или ХОБЛ без наблюдения врача, поскольку симптомы заболевания могут возобновиться после приостановки лечения.
Нежелательные явления, обусловленные астмой, и обострения могут отмечаться во время терапии комбинацией флутиказона фуроат/вилантерол. Пациентов необходимо проинструктировать о необходимости продолжать терапию и обращаться за медицинской консультацией, если симптомы астмы не контролируются или усиливаются после начала применения препарата Релвар™ Эллипта™.
Парадоксальный бронхоспазм
После применения препарата возможно возникновение парадоксального бронхоспазма с усилением свистящего дыхания. В таком случае необходимо незамедлительно использовать ингаляционное бронхолитическое средство короткого действия. Применение препарата Релвар™ Эллипта™ следует сразу прекратить, провести осмотр пациента и при необходимости назначить альтернативное лечение.
Сердечно-сосудистое действие
При применении симпатомиметических лекарственных средств, в т.ч. препарата Релвар™ Эллипта™, могут наблюдаться нежелательные реакции со стороны сердечно-сосудистой системы, включая сердечную аритмию, например, суправентрикулярную тахикардию и экстрасистолию. Поэтому следует с осторожностью использовать комбинацию флутиказона фуроат/вилантерол у пациентов с тяжелым сердечно-сосудистым заболеванием либо с нарушением сердечного ритма, тиреотоксикозом, нескорректированной гипокалиемией или у пациентов с предрасположенностью к низким уровням калия в сыворотке.
Пациенты с печеночной недостаточностью
Пациентам с печеночной недостаточностью средней и тяжелой степени следует использовать дозировку 92/22 мкг, необходимо проводить мониторинг пациентов на предмет появления системных нежелательных реакций, вызванных кортикостероидами (смотрите раздел «Фармакокинетика»).
Системные эффекты, вызванные кортикостероидами
Системные эффекты могут наблюдаться при применении любых ингаляционных кортикостероидов, в особенности в высоких дозах в течение длительного времени. Возникновение подобных эффектов значительно менее вероятно, чем при использовании пероральных кортикостероидов. К возможным системным воздействиям относятся синдром Кушинга, кушингоидная внешность, угнетение функции надпочечников, снижение минеральной плотности костной ткани, задержка роста у детей и подростков, катаракта и глаукома, и, в более редких случаях, воздействие на психику и поведение, включая развитие психомоторной гиперактивности, нарушение сна, тревожность, депрессивный синдром и агрессивность (в особенности у детей).
Комбинацию флутиказона фуроат/вилантерол следует с осторожностью применять у пациентов с туберкулезом легких или у пациентов с хроническими или нелечеными инфекциями.
Гипергликемия
Поступали сообщения о повышении уровней глюкозы в крови у пациентов с диабетом, это следует учитывать при назначении препарата пациентам с сахарным диабетом в анамнезе.
Пневмония у пациентов с ХОБЛ
Было отмечено увеличение случаев заболевания пневмонией, включая случаи, приведшие к госпитализации, у пациентов с ХОБЛ, которые получали ингаляционные кортикостероиды. Имеются свидетельства повышения риска развития пневмонии при увеличении дозы стероида, однако это не было окончательно продемонстрировано во всех исследованиях.
Не получено окончательных клинических свидетельств влияния внутриклассовых различий ингаляционных кортикостероидов на величину риска развития пневмонии.
Врачам следует быть бдительными в отношении возможного развития пневмонии у пациентов с ХОБЛ, поскольку клинические признаки таких инфекций частично совпадают с симптомами обострений ХОБЛ. Факторы риска развития пневмонии у пациентов с ХОБЛ включают курение, старший возраст, низкий ИМТ и тяжелую степень ХОБЛ.
Пациентам с ХОБЛ не назначается препарат Релвар™ Эллипта™ 184/22 мкг. Применение дозировки 184/22 мкг в сравнении с дозировкой 92/22 мкг не приносит дополнительной пользы, кроме того потенциально усиливается риск развития системных нежелательных реакций, вызванных кортикостероидами (см. раздел «Побочное действие»).
Пневмония у пациентов с астмой
Частота заболевания пневмонией у пациентов с астмой при применении более высокой дозы была в пределах среднестатистических показателей. Частота заболевания пневмонией у пациентов с астмой, принимавших комбинацию флутиказона фуроат/вилантерол 184/22 мкг, была в числовом отношении выше в сравнении с пациентами, принимавшими комбинацию флутиказона фуроат/вилантерол 92/22 мкг или плацебо (см. раздел «Побочное действие»). Факторы риска не были выявлены.
Вспомогательные вещества
Данный лекарственный препарат не следует применять пациентам с такими редкими врожденными заболеваниями, как непереносимость галактозы, дефицит лактазы lapp или нарушение всасывания глюкозы-галактозы.
Влияние на способность к вождению автотранспорта и управлению механизмами
Флутиказона фуроат или вилантерол не оказывает либо оказывает крайне незначительное влияние на способность управлять автомобилем и работу с техникой.
Передозировка
Симптомы
Передозировка комбинации флутиказона фуроат/вилантерол может вызывать признаки и симптомы, обусловленные действием отдельных компонентов, в т.ч. сходные с симптомами передозировки других бета2-агонистов и соответствующие известным эффектам ингаляционных кортикостероидов (см. раздел «Особые указания»).
Лечение
При передозировке комбинации флутиказона фуроат/вилантерол не требуется специфической терапии. При передозировке пациенту следует проводить поддерживающее лечение с обеспечением при необходимости соответствующего мониторинга.
Возможность проведения кардиоселективной бета-блокады следует рассмотреть только в случае выраженных эффектов передозировки вилантерола, имеющих клиническое значение и невосприимчивых к поддерживающему лечению. Лекарственные препараты для кардиоселективной бета-блокады следует применять с осторожностью у пациентов с бронхоспазмом в анамнезе.
Дальнейшую терапию следует проводить по клиническим показаниям.
Лекарственное взаимодействие
Клинически значимое лекарственное взаимодействие, вызванное применением комбинации флутиказона фуроат/вилантерол в клинических дозах, расценивается как маловероятное вследствие низких концентраций в плазме после вдыхания дозы препарата.
Взаимодействие с бета-адреноблокаторами
Бета2-адреноблокаторы могут ослаблять или противодействовать эффекту бета2-адренергических агонистов. Следует избегать одновременного применения неселективных и селективных бета2-адреноблокаторов, за исключением случаев, когда существуют убедительные причины для их использования.
Взаимодействие с ингибиторами CYP3A4
Как флутиказона фуроат, так и вилантерол быстро выводятся путем экстенсивного пресистемного метаболизма при участии фермента печени CYP3A4.
Следует соблюдать осторожность при совместном использовании с сильными ингибиторами CYP3A4 (такими как кетоконазол, ритонавир), поскольку существует возможность усиления системного воздействия флутиказона фуроата и вилантерола, таким образом, необходимо избегать их одновременного применения. В исследовании CYP3A4 обусловленного лекарственного взаимодействия с повторными дозами с участием здоровых добровольцев, принимавших комбинацию флутиказона фуроат/вилантерол (184/22 мкг) и сильный ингибитор CYP3A4 кетоконазол (400 мг), отмечено увеличение среднего значения AUC(0-24) и Cmax флутиказона фуроата на 36% и 33% соответственно. Усиление воздействия флутиказона фуроата было связано со снижением на 27% взвешенного среднего значения содержания кортизола в сыворотке крови за 0-24 ч. При одновременном применении увеличились средние показатели AUC(0-t) и Cmax вилантерола на 65% и 22% соответственно. Увеличение экспозиции вилантерола не было связано с усилением системного воздействия бета2-агониста на ЧСС, уровень калия в крови или корректированный интервал QT.
Взаимодействие с ингибиторами Р-гликопротеина
Флутиказона фуроат и вилантерол являются субстратами Р-гликопротеина (P-гп). В ходе исследования клинической фармакологии с участием здоровых добровольцев, одновременно принимавших вилантерол и сильнодействующий P-гп и умеренный ингибитор CYP3A4 верапамил, не было выявлено заметного воздействия на фармакокинетику вилантерола. Исследования клинической фармакологии специфического ингибитора P-гп и флутиказона фуроата не проводились.
Симпатомиметические лекарственные препараты
Одновременное применение других симпатомиметических лекарственных препаратов (отдельно или в составе комбинированной терапии) может усиливать нежелательные реакции, вызванные флутиказона фуроатом/вилантеролом. Не следует применять препарат Релвар™ Эллипта™ в сочетании с другими бета2-адренергическими агонистами длительного действия или лекарственными средствами, содержащими бета2-адренергические агонисты длительного действия.
Дети
Исследования взаимодействия проводились только с участием взрослых пациентов.
Условия хранения препарата
Препарат следует хранить в оригинальной упаковке с целью защиты от влаги, в недоступном для детей месте при температуре не выше 25°С.
Срок годности препарата
Срок годности невскрытого алюминиевого контейнера — 2 года, вскрытого алюминиевого контейнера — 6 недель. Не применять после истечения срока годности, указанного на упаковке.
BY/FFT/0008/17.12.15
Контакты для обращений
ГлаксоСмитКляйн, представительство, (Великобритания)
Представительство
ООО «GlaxoSmithKline Export Ltd»
в Республике Беларусь
220039 Минск, Воронянского ул. 7А, оф. 400
Тел.: (375-17) 213-20-16
Факс: (375-17) 213-18-66
Бронходилатирующее средство комбинированное (бета2-адреномиметик селективный + глюкокортикостероид местный).
Код АТХ
R03AK10
Фармакологические свойства
Фармакодинамика
Механизм действия
Вилантерол и флутиказона фуроат относятся к двум классам лекарственных средств — синтетический глюкокортикостероид и
селективный бета2-адреномиметик обусловлено всасыванием части ингаляционной дозы, поступившей в
Фармакодинамические эффекты
Вилантерола трифенатат относится к классу селективных бета2-адреномиметиков длительного действия (ДДБА). Фармакологические эффекты агонистов бета-адренорецепторов, включая вилантерола трифенатат, по крайней мере, частичносвязаны со стимуляцией внутриклеточной аденилатциклазы — фермента, который катализирует превращение аденозинтрифосфата (АТФ) в циклический 3′,5′-аденозинмонофосфат (циклический АМФ). Повышение уровня циклического АМФ приводит к расслаблению гладкой мускулатуры бронхов и угнетению высвобождения из клеток (в первую очередь из тучных клеток) медиаторов реакций гиперчувствительности немедленного типа.
Флутиказона фуроат является синтетическим трехфтористым глюкокортикостероидом с выраженным противовоспалительным действием. Точный механизм действия, позволяющий купировать симптомы бронхиальной астмы и хронической обструктивной болезни легких (ХОБЛ), неизвестен. Глюкокортикостероиды продемонстрировали широкий спектр действия на различные типы клеток (например, эозинофилы, макрофаги, лимфоциты) и медиаторы (например, цитокины и хемокины, участвующие в процессе воспаления).
Между глюкокортикостероидами и ДДБА происходят молекулярные взаимодействия, в результате которых стероидные гормоны активируют ген бета2-адренорецептора, повышая количество восприимчивых адренорецепторов. ДДБА связываются с глюкокортикостероидным рецептором, обеспечивая его стероидозависимую активацию и стимулируя транслокацию в ядро клетки. Эти синергические взаимодействия приводят к усилению противовоспалительной активности, что было продемонстрировано в экспериментах invitro и invivoс различными клетками воспаления, участвующими в патофизиологических процессах развития бронхиальной астмы и ХОБЛ.
В мононуклеарных клетках
периферической крови у пациентов с
ХОБЛ наблюдалось более выраженное
противовоспалительное
действие
в
присутствии комбинации вилантерола с
флутиказона фуроатом по сравнению с
одним
флутиказона
фуроатом
в
концентрациях,
достигаемых
при
применении в клинических дозах
Фармакокинетика
Всасывание
Абсолютная биодоступность вилантерола и флутиказона фуроата при ингаляционном введении комбинации вилантерола и флутиказона фуроата составила в среднем 27,3 % и
15,2 %, соответственно. Пероральная биодоступность вилантерола и флутиказона фуроата была низкой и в среднем составляла < 2 % и 1,26 %, соответственно. Принимая во внимание низкую пероральную биодоступность, системное действие вилантерола и флутиказона фуроата после ингаляционного приема в первую очередь обусловлено всасыванием части ингаляционной дозы, поступившей в легкие.
Распределение
После внутривенного введения вилантерол и флутиказона фуроат активно распределяются в организме, при этом средние объемы распределения в равновесном состоянии составляют 165 л и 661 л, соответственно. Оба вещества— вилантерол и флутиказона фуроат— обладают низкой способностью связываться с эритроцитами. В исследованиях invitroсвязывание вилантерола и флутиказона фуроата с белками плазмы крови человека было высоким и достигало в среднем 93,9 % и > 99,6 %, соответственно. Степень связывания с белками плазмы крови invitroне уменьшалась у пациентов с нарушениями функции печени или почек.
Несмотря на то, что вилантерол и флутиказона фуроат являются субстратами Р-гликопротеина (P-gp), при одновременном введении комбинации вилантерола и флутиказона фуроата с ингибиторами P-gp
изменение системной экспозиции вилантерола или флутиказона фуроата считается маловероятным, так как оба вещества обладают хорошей абсорбционной способностью.
Метаболизм
На основании данных экспериментов invitro можно заключить, что основные пути метаболизма вилантерола и флутиказона фуроата в организме человека в первую очередь опосредованы изоферментом CYP3A4.
Вилантерол преимущественно метаболизируется путем О-деалкилирования с образованием ряда метаболитов, обладающих существенно более низкой бета1 и бета2-адреномиметической активностью.
Флутиказона фуроат преимущественно метаболизируется путем гидролиза S-фторметилкарботиоатной группы с образованием метаболитов, имеющих значительно более низкую глюкокортикостероидную активность.
Было проведено клиническое исследование лекарственных взаимодействий препарата с изоферментом CYP3A4 при непрерывном введении комбинации вилантерола и флутиказона фуроата (22 мкг + 184 мкг/доза)
и сильного ингибитора изофермента CYP3A4 — кетоконазола (400 мг) здоровым добровольцам.
Введение комбинации вилантерола и флутиказона фуроата привело к увеличению средней площади под фармакокинетической кривой (AUQo—24) и средней максимальной концентрации (Сmах) флутиказона фуроата на 36 % и 33 %, соответственно. Увеличение экспозиции флутиказона фуроата сопровождалось снижением средней концентрации сывороточного кортизола на 27 %, измеренной за период 0-24 часа.
Введение комбинации вилантерола и флутиказона фуроата и кетоконазола привело к увеличению средних значений AUQ 0-24 и Сmах вилантерола на 65 % и 22 %, соответственно. Увеличение экспозиции вилантерола не приводило к усилению характерных для бета-агонистов системных эффектов в отношении частоты сердечных сокращений, содержания калия в крови или корригированного интервала QT (QTcF).
Выведение
После перорального приема флутиказона фуроат в организме человека метаболизировался главным образом с образованием метаболитов, которые преимущественно выводились через желудочно-кишечный тракт, за исключением дозы радиоактивного вещества < 1 %, выведенной с мочой. Период полувыведения из плазмы крови для флутиказона фуроата после ингаляционного приема препарата составлял в среднем 24 часа.После перорального приема вилантерол в организме человека главным образом метаболизировался с образованиемметаболитов, которые экскретировались с мочой и фекалиями в соотношении приблизительно 70 % и 30 % дозы радиоактивного вещества, соответственно. Период полувыведения из плазмы крови для вилантерола после ингаляционного приема комбинации вилантерола и флутиказона фуроата составлял в среднем 2,5 часа.
Особые группы пациентов
В ходе третьей фазы клинических исследований проводился популяционный мета-анализ фармакокинетики вилантерола ифлутиказона фуроата у пациентов с бронхиальной астмой и ХОБЛ. В рамках популяционного фармакокинетического анализа оценивалось влияние демографических ковариат (возраст, пол, вес, индекс массы тела (ИМТ), расовая и этническая принадлежность) на фармакокинетику вилантерола и флутиказона фуроата.
Раса
Пациенты с бронхиальной астмой и ХОБЛ восточноазиатской, японской и юго-восточноазиатской рас (12-14% пациентов) имели в среднем более высокие показатели
AUC(0-24) (выше не более чем на 53 %) в сравнении с пациентами европеоидной расы. Тем не менее, в этих популяциях не обнаружено признаков более высокой системной экспозиции, связанной с более выраженным влиянием на экскрециют кортизола с мочой за 24-часовой период. У пациентов, страдающих ХОБЛ, влияние
расовой принадлежности на фармакокинетические параметры вилантерола не выявлено.
В среднем, по результатам оценки Сmах вилантерола была на 220-287 % выше, а AUC(0-24) была сопоставима у пациентов азиатского происхождения по сравнению с показателями у других расовых групп. Тем не менее, более высокая Сmах вилантерола не оказывала клинически значимого влияния на частоту сердечных сокращений.
Дети
Для подростков (12 лет или старше) рекомендации по изменению режима дозирования отсутствуют. Фармакокинетика комбинации вилантерола и флутиказона фуроата у пациентов младше 12 лет не изучалась. Безопасность и эффективность применения комбинации вилантерола и флутиказона фуроата у детей младше 12 лет пока не установлена.
Пациенты пожилого возраста
Влияние возраста на фармакокинетику вилантерола и флутиказона фуроата изучалось в третьей фазе клинических исследований, включавших пациентов с ХОБЛ и бронхиальной астмой.
У пациентов с бронхиальной астмой не было обнаружено признаков влияния возраста (12-84 лет) на фармакокинетический профиль флутиказона фуроата и вилантерола.
Несмотря на увеличение (37 %) AUC(o_24) вилантерола у пациентов с ХОБЛ в возрастном диапазоне от 41 до 84 лет, признаков влияния возраста пациентов на фармакокинетический профиль флутиказона фуроата не выявлено. У пожилого пациента (в возрасте 84 лет) с низкой массой тела (35 кг) прогнозируется, что AUC(0-24) вилантерола будет на 35 % выше результата, рассчитанного для популяции (в среднем, пациент с ХОБЛ в возрасте 60 лет и массой тела 70 кг), в то время как Стах вилантерола останется неизмененной. Маловероятно, что эти различия являются клинически релевантными.
Пациенты с нарушением функции почек
По данным клинико-фармакологического исследования для вилантерола и флутиказона фуроата тяжелое нарушение функции почек (клиренс креатинина < 30 мл/мин) не приводит к значительному увеличению системной экспозиции вилантерола или флутиказона фуроата или к развитию более выраженных системных эффектов глюкокортикостероидов или бетаг-агонистов в сравнении со здоровыми добровольцами. Коррекции дозы для пациентов с нарушением функции почек не требуется.
Влияние гемодиализа не изучалось.
Пациенты с нарушением функции печени
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени (согласно классификации цирроза печени по Чайлд-Пью: стадии цирроза А, В или С) наблюдалось увеличение системной экспозиции флутиказона фуроата (по измеренной AUC(0-24) до трех раз) в сравнении со здоровыми добровольцами. Повышение системной экспозиции флутиказона фуроата (при назначении комбинации вилантерола и флутиказона фуроата в дозировке 22 мкг + 184 мкг/доза) у пациентов с нарушением функции печени средней степени тяжести (стадия В по классификации Чайлд-Пью) сопровождалось снижением концентрации сывороточного кортизола в среднем на 34 % в сравнении со здоровыми добровольцами. У пациентов с нарушением функции печени тяжелой степени (стадия С по классификации Чайлд Пью), получавших более низкую дозу 11 мкг + 92 мкг, не наблюдалось снижения концентрации сывороточного кортизола. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22 мкг + 92 мкг (см. раздел «Способ применения и дозировка»).
После непрерывного приема комбинации вилантерола и флутиказона фуроата в течение 7 дней у пациентов с нарушением функции печени легкой, средней или тяжелой степени (стадии А, В и С по классификации Чайлд-Пью) не отмечалось значительного увеличения системной экспозиции вилантерола (Смах и AUC). В сравнении со здоровыми добровольцами у пациентов с нарушением функции печени легкой или средней степени (принимавших вилантерол в дозе 22 мкг) или тяжелой степени (принимавших вилантерол в дозе 11 мкг) не наблюдалось клинически значимых бета-адренергических системных эффектов (изменение частоты сердечных сокращений или концентрации сывороточного калия), вызванных приемом комбинации вилантерола и флутиказона фуроата.
Пол, масса тела, индекс массы тела (ИМТ)
Согласно результатам популяционного фармакокинетического анализа данных третьей фазы клинических исследований, включавшей 1213 пациентов с бронхиальной астмой (712 женщин) и 1225 пациентов с ХОБЛ (392 женщины), признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль флутиказона фуроата не обнаружено.
По данным популяционного анализа фармакокинетики с участием 856 пациентов с бронхиальной астмой (500 женщин) и 1091 пациента с ХОБЛ (340 женщин)признаков влияния пола, массы тела или ИМТ на фармакокинетический профиль вилантерола не обнаружено.
Не требуется коррекции дозы на основании данных о половой принадлежности, массе тела или ИМТ.
Бронхиальная астма
Препарат Релвар Эллипта применяется в качестве поддерживающей терапии бронхиальной астмы.
ХОБЛ (хроническая обструктивная болезнь легких)
Препарат Релвар Эллипта* применяется в качестве поддерживающей терапии обструкции дыхательных путей у пациентов с ХОБЛ, включая хронический бронхит и/или эмфизему легких. Применение препарата Релвар Эллипта* позволяет сократить число обострений ХОБЛ у пациентов с повторными обострениями в анамнезе.
Препарат Релвар Эллипта противопоказан:
- пациентам, имеющим в анамнезе тяжелые аллергические реакции на молочный белок или повышенную чувствительность к действующим веществам или любому другому компоненту; входящему в состав препарата;
- детям до 12 лет для лечения бронхиальной астмы.
- Препарат Релвар Эллипта в дозе 22 мкг + 184 мкг/доза не показан для лечения ХОБЛ.
С осторожностью
При приеме симпатомиметиков, включая препарат Релвар Эллипта , со стороны сердечно-сосудистой системы могут наблюдаться такие нежелательные явления, как аритмия (например, наджелудочковая тахикардия и экстрасистолия).
В плацебо-
контролируемом
клиническом
исследовании у пациентов с ХОБЛ и
повышенным риском развития сердечно
сосудистых заболеваний или с сердечно
сосудистым заболеванием, принимающих
препарат Релвар Эллипта , не отмечалось
повышения риска развития сердечно
сосудистых явлений, серьезных сердечно
сосудистых явлений или летального исхода
по причине сердечно-сосудистой патологии по сравнению
с
пациентами,
принимающими
плацебо
Однако пациентам, страдающим тяжелыми формами сердечно-сосудистых заболеваний, препарат Релвар Эллипта следует назначать с осторожностью.
Как и другие лекарственные средства, в состав которых входят глюкокортикостероиды, препарат Релвар Эллипта® следует с осторожностью назначать пациентам с туберкулезом легких, а также пациентам с хроническими или невылеченными инфекциями.
Применение при беременности и в период грудного вскармливания
Фертильность
Данные по влиянию на фертильность человека отсутствуют. В доклинических исследованиях воздействия вилантерола и флутиказона фуроата на фертильность не обнаружено.
Беременность
Данные о применении препарата во время беременности ограничены.
Применение препарата Релвар Эллипта* у беременных женщин допустимо только в том случае, если потенциальная польза для матери превышает возможный риск для плода.
Период грудного вскармливания
Данных об экскреции вилантерола или флутиказона фуроата или их метаболитов в грудное молоко человека недостаточно. Однако другие глюкокортикостероиды и бета2-агонисты определяются в грудном молоке. Риск проникновения препарата вместе с молоком в организм новорожденного или ребенка не может быть исключен.
Принимая во внимание соотношение пользы терапии для матери и грудного вскармливания для ребенка, необходимо решить вопрос либо об отмене препарата, либо о прекращении грудного вскармливания.
Способ применения и дозировка
Препарат Релвар Эллипта предназначен только для ингаляционного применения.
Препарат Релвар Эллипта следует применять один раз в сутки в одно и то же время, утром или вечером.
После ингаляции следует прополоскать рот водой, не проглатывая.
Бронхиальная астма
Пациент должен быть проинформирован о необходимости регулярного применения препарата Релвар Эллипта даже в случае бессимптомного течения заболевания.
При возникновении симптомов заболевания в период между приемами препарата в качестве неотложной терапии следует применять ингаляционные формы бета2-агонистов короткого действия.
Врач должен регулярно оценивать состояние пациента, чтобы обеспечить своевременное назначение оптимальной дозировки препарата Релвар Эллипта.
Дозировка может быть изменена только но рекомендации врача.
Взрослые и подростки 12 лет и старше
Рекомендуемая доза препарата Релвар Эллипта: одна ингаляция 22 мкг + 92 мкг один раз в сутки или одна ингаляция 22 мкг+ 184 мкг один раз в сутки.
Начальная доза препарата Релвар Эллипта 22 мкг + 92 мкг назначается пациентам. которым требуются низкие или средние дозы ингаляционных глюкокортикостсроидов. применяемых в комбинации с бета2-агонистами длительного действия.
Препарат Релвар Эллипта в дозировке 22 мкг + 184 мкг следует назначать пациентам, которым требуется более высокая доза ингаляционных глюкокортикостероидов, применяемых в комбинации с бета2-агонистами длительного действия.
Если препарат Релвар Эллипта» в дозировке 22 мкг + 92 мкг не обеспечивает адекватного контроля заболевания, рассматривается вопрос об увеличении дозы до 22 мкг +184 мкг. что может улучшить уровень контроля над течением бронхиальной астмы.
Дети
Безопасность и эффективность применения препарата Релвар Эллипта*
у
детей младше 12 лет не установлена.
ХОБЛ
Взрослые
Рекомендуемая доза препарата Релвар Эллипта®: одна ингаляция 22 мкг + 92 мкг один раз в сутки.
Препарат Релвар Эллипта в дозировке 22 мкг+ 184 мкг не показан для лечения пациентов с ХОБЛ.
Дети
Препарат по показанию ХОБЛ у детей не применяется.
Особые группы пациентов
Пациенты пожилого возраста
Пациентам старше 65 лет не требуется коррекция дозы препарата (см. раздел «Фармакокинетика», подраздел «Особые
группы пациентов»).
Пациенты с нарушением функции почек
Пациентам с нарушением функции почек не требуется коррекция дозы препарата (см. раздел «Фармакокинетика»).
Пациенты с нарушением функции печени
По данным клинико-фармакологического исследования у пациентов с нарушениями функции печени легкой, средней и тяжелой степени наблюдается трехкратное возрастание степени системной экспозиции флутиказона фуроата (AUC) (см. раздел «Фармакокмнстика»).
Препарат следует назначать с осторожностью пациентам с нарушениями функции печени, у которых риск развития системных нежелательных реакций, вызванных приемом глюкокортикостеропдов, более высок. Для пациентов с нарушением функции печени средней и тяжелой степени максимальная доза составляет 22мкг + 92мкг (см. раздел «Фармакокинетика»).
Рекомендации по применению
При первом использовании ингалятора Эллипта нет необходимости в проверке правильности его работы или специальной подготовке ингалятора к эксплуатации. Просто последовательно соблюдайте рекомендации по применению,
указанные ниже
В пачке картонной ингалятора Эллипта содержатся
Ингалятор Эллипта упакован в контейнер.
Не открывайте контейнер до тех пор, пока не будете готовы осуществить ингаляцию лекарственного препарата. Когда Вы будете готовы использовать ингалятор, снимите фольгу с контейнера. Контейнер
содержит пакетик с
осушителем для снижения влажности. Не вскрывайте данный пакетик, он не предназначен для еды или ингаляций, его следует выбросить
Когда Вы достаете ингалятор из контейнера, его
крышка находится в закрытом положении. Не открывайте ее до тех пор, пока Вы не будете готовы
осуществить ингаляцию лекарственного препарата. В специально
отведенноми
поле
«Использовать до» на этикетке ингалятора
напишите
дату,
которая
будет
соответствовать дате вскрытия плюс 6 недель. Не следует использовать ингалятор после этой даты
Ниже приведены пошаговые инструкции использования ингалятора Эллипта :
I
Прочитайте
информацию
использованием
При открытии и закрытии крышки ингалятора Эллипта без приема лекарственного препарата происходит потеря одной дозы. Эта доза остается закрытой внутри ингалятора, но она будет недоступна для приема. Невозможно случайно получить большую дозу или двойную дозу за одну ингаляцию.
II. Подготовка дозы
Не открывайте крышку, пока Вы не будете готовы к приему препарата.
Не встряхивайте ингалятор.
1. Опустите крышку вниз до щелчка.
2. Доза препарата готова к ингаляции, и
в подтверждение этого счетчик доз уменьшает число доз на единицу.
3. Если счетчик доз не уменьшил число доз после того, как Вы услышали щелчок, то ингалятор не готов к подаче дозы лекарственного препарата. В этом случае следует обратиться по телефону или адресу, указанному в разделе «За дополнительной информацией обращаться».
4. Никогда не встряхивайте ингалятор.
III. Ингаляция
препарата
1. Удерживая ингалятор на некотором расстоянии ото рта, сделайте выдох максимальной глубины. Не выдыхайте в ингалятор.
2. Поместите мундштук между губами и плотно обхватите его губами. Не закрывайте пальцами вентиляционное отверстие
3. Сделайте один долгий, равномерный, глубокий вдох через рот. Задержите дыхание насколько возможно (по крайней мере, на 3-4 секунды).
4. Уберите ингалятор изо рта.
5. Медленно и спокойно выдохните.
Вы можете не
почувствовать вкус или не ощутить поступление лекарственного препарата даже при правильном использовании ингалятора.
Если Вы хотите протереть мундштук,
сделайте это до закрытия крышки,
используя сухую салфетку.
IV
Закрытие
ингалятора
и
полоскание ротовой полости
1
Поднимите крышку до
упора, добившись полного закрытия мундштука.
2. После ингаляции следует прополоскать рот водой. Это снизит вероятность развития таких побочных явлений, как боль в горле и полости рта
Данные клинических исследований
Для определения частоты развития нежелательных реакций, связанных с приемом препарата Релвар Эллипта ,
использовались данные крупных клинических исследований среди пациентов с ХОБЛ и бронхиальной астмой. Программа клинической разработки препарата для лечения бронхиальной астмы включала 7 034 пациента, у которых проводилась комплексная оценка нежелательных реакций. В программе клинической разработки препарата для лечения ХОБЛ принимали участие 6 237 пациентов, у которых проводилась комплексная оценка нежелательных реакций. Исключая пневмонию и переломы, профили безопасности препарата у пациентов с ХОБЛ и бронхиальной астмой были схожи. По данным клинических исследований, пневмония и переломы более часто наблюдались у пациентов, страдающих ХОБЛ.
Нежелательные реакции, представленные ниже, перечислены в соответствии с поражением органов и систем органов и частотой встречаемости. Частота встречаемости определяется согласно классификации Всемирной организации здравоохранения следующим образом: очень часто (> 1/10), часто (> 1/100 и < 1/10), нечасто (> 1/1 000 и < 1/100), редко (> 1/10 000 и < 1/1 000), очень редко (< 1/10 000, включая отдельные случаи).
Частота встречаемости нежелательных
реакций
Инфекционныеипаразитарныезаболевания
Часто: пневмония, инфекции верхних дыхательных путей, бронхит, грипп, кандидоз полости рта и глотки.
Нарушения со стороны нервной системы
Очень часто: головная боль,
Нарушения со стороны сердца
Нечасто: экстрасистолия.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения
Очень часто: назофарингит.
Часто: орофарингеальная боль, синусит, фарингит, ринит, кашель, дисфония.
Нарушения со стороны желудочно-кишечного тракта
Часто: боль в животе.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: артралгия, боль в спине, переломы.
Общие расстройства и нарушения в месте введения
Часто: лихорадка.
Данные
пострегистрационного
наблюдения
Нарушения со стороны иммунной системы
Редко: реакции гиперчувствительности, в том числе анафилаксия, ангионевротический отек, сыпь, крапивница.
Нарушения психики
Редко: тревога.
Нарушения со стороны нервной системы
Редко: тремор.
Нарушения со стороны сердца
Редко: учащенное сердцебиение, тахикардия.
Нарушения со стороны скелетно-мышечной и соединительной ткани
Часто: мышечный спазм.
Нарушения со стороны дыхательной системы, органов
средостения
Редко: парадоксальный бронхоспазм.
Симптомы
При проведении клинических исследований не было получено данных о передозировке комбинацией вилантерола и флутиказона фуроата.
Передозировка препаратом Релвар Эллипта» может вызывать развитие симптомов и признаков, обусловленных действием отдельных компонентов препарата и характерных для передозировки бета2-агонистами и ингаляционными глюкокортикостероидами (см. раздел «Особые указания»).
Лечение
Специфическое лечение передозировки комбинацией вилантерола и флутиказона фуроата отсутствует. В случае развития передозировки назначается симптоматическая терапия и, при необходимости, обеспечивается соответствующее наблюдение за больным.
Применение кардиоселективных бета-адреноблокаторов следует рассматривать только в случаях сильно выраженных эффектов передозировки вилантеролом, которые клинически проявляются невосприимчивостью к поддерживающей терапии. Кардиоселективные бета-адреноблокаторы следует с осторожностью назначать пациентам, у которых наблюдались эпизоды бронхоспазма в анамнезе.
При назначении препарата в терапевтических дозах клинически значимые лекарственные взаимодействия вилантерола или флутиказона фуроата считаются маловероятными вследствие низких плазматических концентраций последних при ингаляционном введении.
Бета-адреноблокаторы могут ослаблять или антагонизировать действие бета2-адреномиметиков. Следует избегать одновременного приема неселективных и селективных бета-блокаторов. исключая случаи, когда их назначение строго необходимо.
Вилантерол и флутиказона фуроат подвергаются быстрому первичному метаболизму в печени посредством изофермента системы цитохрома CYP3A4.
При одновременном назначении препарата с сильными ингибиторами изофермента цитохрома CYP3A4 (например, кетоконазол, ритонавир) следует соблюдать осторожность, поскольку возможно повышение системного воздействия вилантерола и флутиказона фуроата, что в свою очередь может привести к повышению риска развития нежелательных реакций (см. раздел «Фармакокинетика»).
Вилантерол и флутиказона фуроат являются субстратами P-gp. По результатам клинико-фармакологического исследования с участием здоровых добровольцев, которым одновременно назначались вилантерол и сильный ингибитор P-gp и умеренный ингибитор изофермента цитохрома CYP3A4 верапамил, значимого влияния на фармакокинетику вилантерола не выявлено. Клинико-фармакологические исследования совместного назначения специфического ингибитора P-gr и флутиказона фуроата не проводились.
Обострения
Препарат Релвар Эллипта не предназначен для купирования острых симптомов бронхиальной астмы или обострения ХОБЛ, в таких случаях требуется назначение бронходилататоров короткого действия.
Увеличение частоты приема бронходилататоров короткого действия с целью купирования симптомов свидетельствует об ухудшении контроля над заболеванием и необходимости консультации врача.
Пациентам с бронхиальной астмой или ХОБЛ не следует прекращать лечение препаратом Релвар Эллипта без наблюдения врача, так как отмена терапии может привести к возобновлению симптомов.
На фоне лечения препаратом Релвар Эллипта могут развиваться нежелательные явления, связанные с течением бронхиальной астмы или обострением заболевания. Пациентам следует рекомендовать продолжить лечение. В случае отсутствия контроля над заболеванием или ухудшения состояния после начала терапии препаратом Релвар Эллипта необходима консультация врача.
Парадоксальный бронхоспазм
Как и при других видах ингаляционной терапии, после приема препарата может развиваться парадоксальный бронхоспазм, сопровождающийся быстрым нарастанием свистящих хрипов. В этом случае показаны неотложное назначение ингаляционного бронходилататора длительного действия и немедленная отмена препарата Релвар Эллипта. Пациент должен быть осмотрен врачом, и ему, при необходимости, может быть назначена альтернативная терапия.
Пациенты
с
нарушением функции печени
Пациентам с нарушением функции печени средней и тяжелой степени следует назначать дозу 22 мкг + 92 мкг, таким пациентам следует находиться под наблюдением врача для контроля над системными побочными реакциями, связанными с применением глюкокортикостероидов.
Системные
эффекты
глюкокортикостероидов
При применении ингаляционных глюкокортикостероидов (особенно при длительном приеме в высоких дозах) могут развиваться системные побочные реакции. Такие побочные реакции развиваются значительно реже, чем при пероральном приеме глюкокортикостероидов. К проявлениям возможного неблагоприятного системного действия относятся: подавление функции гипоталамо-гипофизарно-надпочечниковой системы, снижение минеральной плотности костей, замедление скорости роста у детей и подростков, катаракта и глаукома.
Пневмония
У пациентов с ХОБЛ, получающих препарат Релвар Эллипта , наблюдалось повышение частоты развития пневмонии, а также частоты возникновения тяжелых форм пневмонии, требующих госпитализации пациента. В некоторых случаях клинические эпизоды пневмонии имели летальный исход. Врачам следует помнить о возможности развития пневмонии у пациентов с ХОБЛ, не забывая о том, что клинические признаки такого инфекционного заболевания маскируются симптомами обострения ХОБЛ. Более высокий риск развития пневмонии на фоне приема препарата Релвар Эллипта имеют следующие группы пациентов с ХОБЛ: курящие пациенты, пациенты, ранее перенесшие пневмонию, пациенты с индексом массы тела < 25 кг/м и пациенты с объемом форсированного выдоха (ОФВ0 < 50 % от должных величин. При назначении терапии препаратом Релвар Эллипта следует учитывать вышеуказанные факторы, в случае возникновения пневмонии лечение должно быть пересмотрено.
У пациентов с бронхиальной астмой случаи развития пневмонии наблюдались нечасто. Пациенты с бронхиальной астмой, получавшие препарат Релвар Эллипта в дозировке 22 мкг + 184 мкг/доза, возможно, имели более высокий риск развития пневмонии в сравнении с пациентами, получавшими более низкую дозу препарата Релвар Эллипта (22 мкг + 92 мкг/доза), или с группой плацебо. Факторы риска не установлены.
В ходе проведения клинических исследований у пациентов, страдающих ХОБЛ, была выявлена низкая частота возникновения переломов костей во всех лечебных группах, но при этом во всех группах, получавших комбинацию вилантерола и флутиказона фуроата, она была несколько выше (2 %), чем в группе, получавших монотерапию вилантеролом 22 мкг (< 1 %).
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ,
МЕХАНИЗМАМИ
Исследования по изучению влияния препарата Релвар Эллипта на способность к вождению автотранспорта и работе с механизмами не проводились. Исходя из данных фармакологии вилантерола или флутиказона фуроата, неблагоприятное влияние препарата на эти виды деятельности не предполагается.
Порошок для ингаляций дозированный, 22 мкг + 92 мкг/доза, 22 мкг + 184 мкг/доза.
По 30 доз в пластиковый ингалятор с корпусом светло-серого цвета, бледно-голубой крышкой мундштука и счетчиком доз. Ингалятор содержит два алюминиевых ламинированных стрипа, каждый из которых состоит из 30 ячеек, которые содержат порошок белого цвета. Ингалятор помещен в многослойный контейнер из алюминиевой фольги, содержащий пакетик с осушителем. Контейнер запечатан легко открывающейся фольгой. По 1 контейнеру вместе с инструкцией по применению в пачку картонную.
Не вскрытый алюминиевый контейнер: 2 года.
Вскрытый алюминиевый контейнер: 6 недель.
В специально отведенном поле «Использовать до» на этикетке ингалятора напишите дату. Дату следует указать сразу после того, как ингалятор был извлечен из контейнера.
Не применять после истечения срока годности, указанного на упаковке.
Хранить при температуре не выше 25°С. Хранить в недоступном для детей месте.
По рецепту.
Производитель
«Глаксо Оперэйшенс Великобритания Лимитед» / Glaxo Operations UK Limited
SGI2 ODJ, Хертфордшир, Вэа, Прайори стрит, Великобритания / Priory Street, Ware, Hertfordshire, SGI2 ODJ. United Kingdom
НАИМЕНОВАНИЕ И АДРЕС ЮРИДИЧЕСКОГО ЛИЦА, НА ИМЯ КОТОРОГО
ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
ЗАО «ГлаксоСмитКляйн Трейдинг» 119180, г. Москва, Якиманская наб., д. 2
За дополнительной информацией обращаться
ЗАО «ГлаксоСмитКляйн Трейдинг»
121614, г. Москва, ул. Крылатская, д. 17, корп. 3, эт. 5
Бизнес-Парк «Крылатские холмы»