Химические свойства
Ритуксимаб – синтетические, химерные моноклональные, выведенные с помощью генной инженерии антитела мыши/человека. Вещество по своему структурному строению относится к иммуноглобулину IgG1 каппа. Основа молекулы – постоянный человеческий сегмент, на который нарастили вариабельные фрагменты тяжелых и легких цепей мышиных антител.
Средство состоит из 2 тяжелых (451 аминокислота) и 2 легких (213 аминокислот) цепей, его молекулярная масса = 145 кД.
Фармакологическое действие
Противоопухолевое.
Фармакодинамика и фармакокинетика
Вещество специфически связывается с антигеном CD20, который расположен на поверхности зрелых и пре-В-лимфоцитов. Такого рода антиген отсутствует на про-В-клетках, здоровых клетках различных тканей, стволовых гемопоэтических и нормальных плазматических клетках. DC20 активно участвует во всех стадиях созревания В-лимфоцитов, является регулятором тока ионов кальция через полунепроницаемую клеточную мембрану. После того, как молекула антигена связалась с действующим веществом, образовавшееся соединение не сбрасывается во внеклеточное пространство, не существует в крови в свободном виде и не интернелизуется.
Антинеопластическое действие соединения основано на его способности связываться с антигеном CD-20 на поверхности лимфоцитов и индуцировать иммунологические реакции, которые приводят к лизису В-клеток. Клеточный лизис происходит по двум механизмам: АЗЦТ и КЗЦТ. Дополнительно Ритуксимаб приводит к апоптозу клеток человеческой В-клеточной лимфомы на линии DHL-4.
Вещество оказывает влияние на лимфоидные клетки тимуса, периферической крови, селезенки (белая пульпа), лимфатические узлы.
Медиана числа В-клеток восстанавливается до первоначального уровня через год, после отмены лекарственного средства. Антихимерные антитела человека обнаружили у 1% пациентов, проходивших лечение Ритуксимабом. У 3 из 356 человек можно было пронаблюдать объективный клинический ответ на терапию.
После внутривенной инфузии лекарственного средства наблюдается пропорциональный рост максимальной концентрации и периода полувыведения от дозировки. Отмечается отрицательная корреляция сывороточных уровней соединения с величиной опухоли. Ритуксимаб накапливается в организме, его можно обнаружить в организме в течение 3-6 месяцев после того, как была введена последняя доза.
Были проведены клинические исследования, в которых участвовали пациенты с различной степенью тяжести неходжкинской лимфомы и использовались разные схемы лечения.
При проведении начальной терапии, по 4 инъекции в неделю у 42 % пациентов наступила частичная ремиссия, у 6% — полная. Организм начинал отвечать на лечение в среднем на 50 день, после начала использования препарата. Заболевание начинало прогрессировать через 11,2 месяца. У 23% больных в начале эксперимента присутствовали признаки и симптомы заболевания, и у 64% их них они исчезали.
При начальной терапии и использовании схемы лечения на 8 уколов каждую неделю, наблюдались следующие показатели: частичная ремиссия – 43%, полная ремиссия – 14%, прогрессирование болезни – через 13,4 месяца. Однако, если опухолевая масса была размером более 10 см или проводилось повторное лечение, то данные показатели были несколько ниже.
У пациентов, находящихся в преклонном возрасте не наблюдалось каких либо изменений в частоте и тяжести проявления побочных эффектов, частоте возникновения ремиссии и рецидива.
Показания к применению
Применение Ритуксимаба:
- для лечения фолликулярных или низкой степени злокачественности В-клеточных неходжиновских лимфом;
- при рецидивирующей или химиоустойчивой В-клеточной лимфоме;
- для лечения прочих видов лимфомы в составе комплексной терапии;
- в активной форме ревматоидного артрита, если другие методы лечения оказались недостаточно эффективными.
Противопоказания
Лекарственное средство не рекомендуется использовать у пациентов с аллергией на Ритуксимаб или белок мыши.
Побочные действия
В промежутке времени от 12 часов до суток после первой инфузии препарата могут развиться симптомы, характерные для синдрома лизиса опухоли: гиперкалиемия, гиперурикемия, сбои в работе почек, гипокальциемия, гиперфосфатемия.
Также во время лечения веществом наблюдались тяжелые реакции со стороны слизистых оболочек и кожи: перанеопластическая пузырчатка, дерматиты, синдром Стивенса-Джонсона, токсический эпидермальный некролиз.
Есть сообщения о развитии фатальных инфузионных реакций во время введения первой инъекции. Летальный исход был инициирован гипоксией, инфильтрацией легких, острым респираторным дистресс-синдромом, кардиогенным шоком и инфарктом миокарда. Большинство фатальных реакций происходили после первой инфузии.
Также сообщалось о случаях развития острой почечной недостаточности, которая требовала проведения диализа, нередко побочные реакции такого рода приводили к смерти пациента.
Ритуксимаб не рекомендуется сочетать с цисплатином. При такой комбинации лекарств значительно повышается риск развития тяжелой почечной недостаточности.
Могут проявиться следующие побочные реакции (наблюдались во время проведения монотерапии препаратом):
- лихорадка, развитие вторичных инфекций, головная боль, боли в спине, озноб, астения;
- приливы крови, повышение или понижение АД;
- рвота, запор, диарея, тошнота;
- анемия, лейкопения, тромбоцитопения;
- нейтропения, лимфопения, гипергликемия;
- отеки по периферии, артралгия, миалгия;
- тревожность, головокружение, ринит и кашель;
- диспноэ, потливость, крапивница, зуд на коже;
- ангиодэма, бронхоспазм, повышение активности ферментов печени.
Доказано, что введение 8 доз лекарства в неделю повышает вероятность возникновения побочных реакций.
Во время первой инъекции чаще всего возникают:
- лихорадка, озноб, дрожь по телу;
- зуд, тошнота, астения, головная боль, снижение АД;
- першение в горле, насморк, рвота, гипертензия, крапивница.
Перечисленные выше симптомы наблюдаются уже через 30 минут – 2 часа после внутривенного введения и проходят после прерывания инфузии. В тяжелых случаях показано проведение симптоматической терапии, внутривенное введение физ. раствора, парацетамола и дифенгидрамина.
Во время проведения монотерапии могут также возникнуть гематологические нежелательные явления: гипоплазия костного мозга, поздняя нейтропения, пролонгированная панцитопения.
Лекарственное средство приводит к снижению иммунитета, истощению В-клеток, уменьшению уровня иммуноглобулина, лимфопении. У 31% пациентов лечение препаратом вызвало развитие бактериальных инфекций, грибковых и вирусных заболеваний.
У лиц, склонных к возникновению аритмий или со стенокардией во время введения препарата следует внимательно следить за работой сердечной мышцы.
Зарегистрированы случаи реактивации гепатита В, после окончания лечения средством. Заболевание обнаруживалось в течение 4 месяцев после первой инфузии или 1 месяца после введения последней дозы Ритуксимаба.
Сообщалось в развитии увеита, зрительного нефрита, системного васкулита, плеврита, сывороточной болезни, артрита.
Во время постмаркетингового исследования был зарегистрирован случай возникновения прогрессирующей мультифокальной лейкоэнцефалопатии.
Ритуксимаб, инструкция по применению (Способ и дозировка)
Схему лечения назначает лечащий врач в зависимости от стадии заболевания и вида опухоли.
Лечение Ритуксимабом
Препарат вводят внутривенно, капельно.
Перед использованием вещества его необходимо развести в инфузионном пакете или флаконе р-ом хлорида натрия 9% или водным 5% р-ом глюкозы до концентрации от 1 до 4 мг на один мл.
Вводят лекарственное средство капельно из расчета 375 мг на квадратный метр поверхности тела. Раствор можно вводить от 1 до 8 раз в неделю. При проведении одной инфузии в 7 дней курс лечения составляет один месяц.
Скорость инфузии – 50 мг в час при первом введении. Затем скорость можно постепенно увеличивать на 50 мг в час, каждые 30 минут. Максимальная скорость – 400 мг в час. При после дующих инфузиях начальная скорость введения = 100 мг в час.
Передозировка
В клинических условиях передозировка средством не наблюдалась. Максимальное количество вещества, которое вводили пациенту за один раз, не превышало 500 мг на квадратный метр поверхности тела.
Взаимодействие
Препарат Ритуксимаб нельзя сочетать с другими моноклональными антителами, это может вызвать тяжелые аллергические реакции.
Лекарства, угнетающие функцию кроветворения костного мозга, увеличивают риск развития миелосупрессии.
Средство можно сочетать с доксорубицином, преднизолоном, циклофосфамидом, винкристином.
Условия продажи
Нужен рецепт.
Условия хранения
Вещество хранят в защищенном от доступа прямых солнечных лучей месте, с температурным режимом от 2 до 8 градусов Цельсия. Нельзя допускать замораживания препарата.
Срок годности
30 месяцев.
Особые указания
Эффективность и последствия проведения иммунизации во время проведения терапии Ритуксимабом не изучались.
Инфузии следует производить в условиях стационара под наблюдением гематологов или онкологов, которые ранее имели опыт обращения с данным средством. Во время проведения терапии, особенно при первом введении, необходимо держать оборудования для реанимации. За 12 часов до начала проведения терапии следует прекратить прием антигипертензивных препаратов.
За пол часа перед инъекцией показана премедикация: обезболивающие, жаропонижающие, антигистаминные средства, кортикостероиды по показаниям.
Лекарство нельзя вводить внутривенно струйно или болюсно.
Если во время введения вещества наблюдаются легкие или умеренные побочные реакции, то скорость введения необходимо снизить.
Если размер опухоли превышает 10 см или число циркулирующих злокачественных клеток более 25000 на мм3, то во время лечения следует соблюдать особую осторожность, может возникнуть синдром лизиса опухоли. Синдром может привести к летальному исходу. В качестве мер осторожности рекомендуется тщательно наблюдать за состоянием больного, проводить лабораторный мониторинг, контроль функции почек и уровня электролитов в крови.
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня:
Лекарства, активным действующим веществом которых является Ритуксимаб: Мабтера, Ацеллбия, Ритуксимаб.
Отзывы о Ритуксимабе
Лечение данным веществом чаще всего плохо переносится пациентами, неизбежно проявления побочных реакций, особенно со стороны кроветворения и сердечно-сосудистой системы. Говорить об эффективности лекарственного средства сложно, все зависит от степени тяжести заболевания, схемы лечения и сопутствующих болезней. Нередко после прохождения курса препарата у пациента развивается устойчивая ремиссия.
Цена Ритуксимаба, где купить
Купить Ритуксимаб в составе препарата Мабтера можно за 12000-20000 рублей, 2 флакона, дозировкой по 100 мг на 10 мл.
Со стороны пищеварительной системы: тошнота, рвота, диарея, диспепсия, анорексия, боли в животе, повышение активности ЛДГ, нарушение вкусовых ощущений; в единичных случаях — небольшое транзиторное повышение показателей функциональных печеночных проб.
Со стороны нервной системы: слабость, головная боль, головокружение, тревога, депрессия, парестезии, гиперестезии, возбуждение, бессонница, нервозность, сонливость, неврит, нарушения слезоотделения, боли в ушах.
Со стороны сердечно-сосудистой системы: транзиторная артериальная гипотензия, артериальная гипертензия, брадикардия, тахикардия, ортостатическая гипотензия, вазодилатация, приливы, аритмия, обострение имевшихся раньше заболеваний сердца (в т.ч. стенокардии, хронической сердечной недостаточности), периферические отеки, отеки лица.
Со стороны системы кроветворения: тяжелая тромбоцитопения, тяжелая нейтропения, тяжелая анемия, лейкопения, лимфаденопатия.
Со стороны обмена веществ: гипергликемия, снижение массы тела, гипокальциемия, гиперкальциемия.
Со стороны костно-мышечной системы: артралгии, миалгии, боли в костях, боли в пояснице, боли в грудной клетке, боли в области шеи, мышечный гипертонус; редко — повышение активности КФК, спонтанные переломы.
Со стороны мочевыделительной системы: дизурия, гематурия, гиперурикемия.
Дерматологические реакции: повышенное потоотделение (в т.ч. ночью), сухость кожи.
Аллергические реакции: крапивница, зуд, бронхоспазм, одышка, отек языка или глотки, (ангионевротический отек), ринит, усиление кашля, бронхиальная астма, псевдоларингит; в единичных случаях — облитерирующий бронхиолит.
Прочие: возможны лихорадка и озноб (развиваются преимущественно при первой инфузии обычно в первые 2 ч), боли в месте локализации опухоли, общее недомогание, увеличение живота, боли в месте инфузии; редко — нарушения свертывания крови, увеличение частоты развития инфекционных заболеваний, рецидивы имевшихся ранее опухолей кожи.
Связь развития указанных побочных реакций с применением ритуксимаба точно не установлена.
Перспективы применения ритуксимаба при аутоиммунных заболеваниях человека
Статьи
Опубликовано в журнале:
« Русский Медицинский Журнал», 2007, Том 15, № 26, С. 1-6
Академик РАМН, профессор Е.Л. Насонов
ГУ Институт ревматологии РАМН, Москва
Аутоиммунные заболевания включают более 80 нозологических форм и относятся к числу наиболее распространенных и тяжелых болезней человека, частота которых в популяции составляет 5–8%. Для лечения аутоиммунных заболеваний используется широкий спектр препаратов, обладающих противовоспалительной (глюкокортикоиды – ГК), цитотоксической или иммуносупрессивной (в низких дозах) активностью, большая часть из которых создавалась для лечения злокачественных новообразований или подавления отторжения трансплантата. Рациональное применение этих препаратов на ранних этапах болезни, в сочетании с экстракорпоральными методами очищения крови в период обострения, позволило существенно улучшить непосредственный и отдаленный прогноз, однако во многих случаях не позволяет контролировать прогрессирование заболевания, развитие угрожающих для жизни осложнений или ассоциируется с тяжелыми побочными эффектами.
Среди разнообразных иммунных нарушений, лежащих в основе развития аутоиммунных заболеваний, изучение дефектов В–клеточной регуляции вызывает особый интерес, в том числе и с точки зрения разработки новых патогенетически обоснованных подходов к лечению [1]. Напомним, что В–лимфоциты – клетки иммунной системы, участвующие в развитии и поддержании адаптивного иммунитета, образуются из гемопоэтических предшественников в костном мозге в течение всей жизни человека, участвуют в поддержании иммунологической толерантности к собственным антигенам (ауто-антигенам). Дефект В–клеточной толерантности приводит к синтезу аутоантител, которые, активируя эффекторные звенья иммунного ответа, индуцируют развитие воспаления и деструкции тканей организма человека. Однако значение В–клеток в развитии аутоиммунных заболеваний не исчерпывается только синтезом «патогенных» аутоантител. Установлено, что нарушение В–клеточной ко-стимуляции Т–лимфоцитов играет фундаментальную роль в развитии аутоиммунных реакций и может развиваться на самых ранних стадиях патологического процесса до клинической манифестации и заболевания [2]. Кроме того, по данным клинических и эпидемиологических исследований, у пациентов с аутоиммунными ревматическими заболеваниями наблюдается увеличение риска развития В–клеточных неходжскинских лимфом [3]. Все это вместе взятое делает В–клетки перспективными терапевтическими «мишенями» при аутоиммунных заболеваниях [4–7].
Первым и пока единственным анти–В–клеточным препаратом, разрешенным к применению в клинической практике, является ритуксимаб (Rituximab, МабТера «Ф. Хоффман–Ля Рош Лтд.») – химерные моноклональные антитела к CD20 антигену В–лимфоцитов [8]. Препарат применяется в медицине с 1997 года для лечения В–клеточных неходжскинских лимфом, а в последние годы – широкого круга аутоиммунных заболеваний [9].
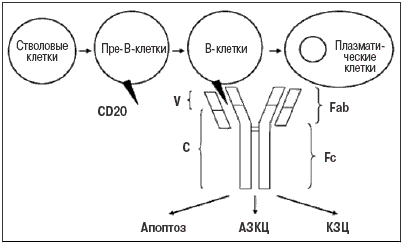
Выбор CD20 молекулы в качестве мишени для моноклональных антител связан с особенностями дифференцировки В–клеток, которые в процессе созревания от стволовых клеток в плазматические клетки проходят несколько последовательных стадий, для каждой из которых характерна экспрессия определенных мембранных молекул (рис. 1). Экспрессия CD20 наблюдается на мембране «ранних» и зрелых В–лимфоцитов, но не стволовых, «ранних» пре–В, дендритных и плазматических клеток. Поэтому их истощение не отменяет регенерацию пула В–лимфоцитов и не влияет на синтез иммуноглобулинов плазматическими клетками. Кроме того, CD20 не высвобождается с мембраны В–лимфоцитов в кровяное русло и поэтому не блокирует взаимодействие ритуксимаба с В–клетками, что увеличивает эффективность терапии. Полагают, что способность ритуксимаба элиминировать В–клетки реализуется за счет нескольких механизмов, в том числе комплемент–зависимой и антитело–зависимой клеточной цитотоксичности, а также индукции апоптоза [10]. В свою очередь истощение В–клеток может оказывать существенное влияние на основные механизмы развития аутоиммунных заболеваний человека и имеет серьезное патогенетическое обоснование:
- ослабление антиген–презентирующей функции В–клеток в отношении индукции пролиферации и синтеза цитокинов CD4+ Т–клетками;
- деструкция аберрантных ростковых центров, что приводит к снижению образования аутоантиген–специфичных В–клеток памяти, плазматических клеток и синтеза антител;
- истощение предшественников плазматических клеток, что приводит к подавлению синтеза антител и образования иммунных комплексов;
- модуляция активности других аутореактивных кле ток за счет нарушения функции Т–клеток;
- активация Т–регуляторных клеток (CD4+ CD25+).
Рис.1 Механизмы действия ритуксимаба
В настоящее время возможность эффективного контроля аутоиммунных патологических состояний путем истощения (и/или модуляции функции) В–клеток доказана в клинических исследованиях. Об этом свидетельствует высокая эффективность ритуксимаба при наиболее распространенном и тяжелом аутоиммунном ревматическом заболевании – ревматоидном артрите (РА), что послужило основанием для регистрации препарата для лечения этого заболевания. Детальный анализ результатов клинических исследований ритуксимаба при РА представлен в предыдущих публикациях [7,11,12].
В последние годы очень быстро накапливается клинический опыт применения ритуксимаба для лечения других аутоиммунных заболеваний человека [13–15].
Следует особо подчеркнуть, что в большинстве случаев ритуксимаб назначали пациентам с очень тяжелым течением болезней, которые были резистентны к стандартной глюкокортикоидной и цитотоксической терапии, внутривенному иммуноглобулину, экстракорпоральным методам очищения крови, нередко по жизненным показаниям.
Системная красная волчанка
Системная красная волчанка (СКВ) – аутоиммунное ревматическое заболевание, в основе патогенеза которого лежат дефекты иммунорегуляции, приводящие к неконтролируемой гиперпродукции аутоантител к компонентам собственных тканей и развитию хронического воспаления, затрагивающего многие органы и системы. При этом В–лимфоциты играют ключевую роль в развитии иммунопатологических процессов при этом заболевании [16].
В настоящее время имеются данные о применении ритуксимаба более чем у 100 пациентов с СКВ, как взрослых, так и детей, результаты которых суммированы в обзоре [17]. Результаты проведенных исследований позволяют сделать следующие основные выводы:
- В целом лечение ритуксимабом ассоциировалось с достоверным снижением активности заболевания более чем у 80% пациентов.
- Назначение ритуксимаба высокоэффективно у больных СКВ с активными внепочечными проявлениями болезни (серозит, полиартрит, поражение кожи, стоматит, лихорадка, анемия), с прогрессирующим волчаночным нефритом (III–IV морфологический тип по классификации ВОЗ).
- Ритуксимаб может быть препаратом выбора у больных с «критическим» течением СКВ, обусловленным тяжелым поражением ЦНС (коматозное состояние, судороги, психоз), а также мультиорганным тромбозом, связанным с катастрофическим антифосфолипидным синдромом.
- Предварительные результаты свидетельствуют о высокой эффективности повторных курсов терапии ритуксимабом в случае развития обострения.
Синдром Шегрена
Синдром Шегрена (СШ) – системное аутоиммунное заболевание, поражающее экзокринные железы и проявляющееся персистирующей сухостью рта и глаз, связанное с нарушением функции слюнных и слезных желез [18]. СШ весьма распространен в популяции, встречается с частотой 0,6%–3,3% или 4 новых случая на 100 000 населения в год. СШ чаще развивается у женщин среднего возраста, соотношение женщин к мужчинам колеблется от 14:1 до 24:1. Выделяют первичный синдром (болезнь) Шегрена и вторичный СШ, развивающийся у больных РА и другими аутоиммунными ревматическими и неревматическими заболеваниями.
СШ – потенциально тяжелое заболевание, характеризующееся развитием широкого спектра экстрагландулярных (системных) проявлений и высоким риском лимфом, что отражает фундаментальную роль В–клеточной гиперреактивности в иммунопатогенезе болезни [3]. Полагают, что первичный СШ представляет собой уникальную модель для изучения процессов, лежащих в основе трансформации поликлональной В–клеточной активации в олиго– (моно–) клональную пролиферацию В–клеток, приводящую, в конечном счете, к развитию злокачественных В–клеточных лимфопролиферативных заболеваний. В настоящее время патогенетически обоснованная терапия СШ практически не разработана и сводится к симптоматическому лечению сухого кератоконъюнктивита и ксеростомии и применению ГК и цитостатиков у пациентов с тяжелыми системными проявлениями болезни. Попытки назначения ингибиторов ФНО–α дали противоречивые результаты и патогенетически недостаточно обоснованы. Данные, касающиеся эффективности ритуксимаба при СШ, суммированы в таблице 1.
Таблица 1. Результаты применения ритуксимаба при первичном синдроме Шегрена
| Авторы | Число и характеристика больных | Тип исследования | Результаты |
| J.E. Gottenberg et al. [20] | n=6; лимфома (2); системные проявления (4) | Ретроспективное | Эффективен |
| J. Pijpe et al. [21] | n=15; активное заболевание длительность (< 4 лет), MALT–лимфома (7) | Открытое (фаза III) | Эффективен |
| R. Seror et al. [22] | n=16; лимфома (5); системные проявления (11), в том числе криоглобулинемия (5), поражение легких (2), артрит (4), тромбоцитопения (1), множественный мононеврит (1) |
Ретроспективное | Эффективен |
| V. Davauchelle– Pensek et al. [23] | n=16; активное заболевание | Открытое | Эффективен |
Влияние лечения ритуксимабом на проявления сухого кератоконъюнктивита и ксеростомии анализировалось в 3–х исследованиях. По данным J.E. Gottenberg и соавт. [20], у 3 пациентов наблюдалось существенное улучшение, а у 2 – стабилизация клинической симптоматики. Сходные результаты получены J. Pijpe и соавт. [21]. В то же время R. Seror и соавт. [22] не выявили существенного влияния лечения на проявления сухого синдрома. В исследовании V. Davauchelle–Pensec и соавт. [23] установлена эффективность ритуксимаба в отношении таких проявлений заболевания, как слабость, сухость во рту, поражение суставов, общее состояние (SF–36), функционального состояния легких (1 пациент).
Особенно выраженный эффект отмечен в отношении системных проявлений заболевания. По данным J.E. Gottenberg и соавт. [20], существенная положительная динамика обнаружена у 5 из 6 пациентов, что позволило существенно снизить дозу ГК. R. Seror и соавт. [22] продемонстрировали высокую эффективность ритукси-маба в отношении системных проявлений у 9 из 11 больных.
Несомненный интерес представляют материалы, касающиеся эффективности ритуксимаба у пациентов с СШ и лимфомами. В исследовании J.E. Gottenberg и соавт. [209] полная ремиссия отмечена у 1 пациента, а по данным J. Pijpe и соавт. [21], полная ремиссия достигнута у 3, а частичная – у 2–х пациентов. Прогрессирование болезни имело место только у 1 больного. По данным R. Seror и соавт. [22], развитие ремиссии имело место у 4 из 5 пациентов с лимфомой. Кроме того, имеются данные о высокой эффективности ритуксимаба в качестве адъювантной терапии при агрессивных В–клеточных лимфомах. M. Vougarelis и соавт. [24] представили результаты о длительной ремиссии агрессивной диффузной В–клеточной лимфомы у 6 пациентов с пер вичным СШ, получавших комбинированную терапию циклофосфамидом, доксорубицином, винкристином, преднизолоном (CHOP) и ритуксимабом. В целом эффективность терапии была выше, чем в группе сравнений, у пациентов, получавших только цитотоксическую терапию без ритуксимаба.
Идиопатические воспалительные миопатии (ИВМ)
Идиопатические воспалительные миопатии (ИВМ) – группа аутоиммунных ревматических заболеваний, которые могут встречаться как в виде самостоятельных нозологических форм, так и в качестве синдрома при различных ревматических заболеваниях [25]. Наиболее частыми формами ИВМ являются полимиозит (ПМ) и дерматомиозит (ДМ). В основе патогенеза ИВМ лежит аутоиммунное поражение мышц, которое имеет свои особенности при ПМ и ДМ. При ПМ в клеточном инфильтрате преобладают CD 8+ Т–лимфоциты и макрофаги, а при ДМ – CD 4+ Т–лимфоциты. Развитие ИВМ может сопровождаться синтезом широкого спектра аутоантител, которые получили название миозит–специфических. Лечение ПМ/ДМ в значительной степени остается эмпирическим и обычно состоит из сочетания ГК и иммуносупрессивной терапии, однако у многих пациентов лечение недостаточно эффективно. Поэтому опыт применения ритуксимаба при ИВМ представляет несомненный интерес (табл. 2).
Таблица 2. Эффективность ритуксимаба при идиопатических воспалительных миопатиях
| Авторы | Диагноз/ число больных | Предшествующая терапия | Эффективность |
| T.D. Levine [26] | ДМ–7 | ГК, ЦсА, МТ, ВИГ | Увеличение мышечной силы (36%–113%); снижение КФК; купирование кожных проявлений, улучшение функции легких |
| E. Noss et al. [27] | ДМ–1 ПМ–2 | ГК, МТ, МФМ | Увеличение мышечной силы (нормализация – у 2–х), нормализация КФК, снижение дозы ГК |
| O. Lambotte et al. [28] | Антисинтетазный синдром – 1 | ГК, МТ, азатиоприн, ВИГ | Увеличение мышечной силы, нормализация КФК, улучшение функции легких |
| L. Brulhart [29] | Антисинтетазный синдром – 1 | ГК, МТ | Увеличение мышечной силы, нормализация КФК, купирование альвеолита |
| M.A. Cooper et al. [30] | Ювенильный ДМ – 4 | ГК, МТ, ВИГ | Увеличение мышечной силы, нормализация КФК, купирование кожных проявлений |
| C.C. Mok et al. [31] | ПМ – 4 | ГК (4), пульс МП (2), аза (4), МТ (1), МФМ (4), ЦсА (3), такролимус (1), ВИГ (1) | Нормализация мышечной силы и КФК – 2 Нормализация КФК, умеренное увеличение мышечной силы – 2 |
Примечание: МТ – метотрексат, ЦсА – циклоспорин А, ВИГ – внутривенный иммуноглобулин, АЗА – азатиоприн; МФМ – микофенолата мофетил; МП – метилпреднизолон
Как видно из таблицы, лечение ритуксимабом было эффективным у большинства больных, что проявлялось в нормализации (или существенном увеличении) мышечной силы и снижении концентрации КФК. У больных с ДМ во всех случаях отмечено купирование кожных проявлений. У пациентов с антисистетазным синдромом отмечена нормализация функции легких.
Cистемные васкулиты
Системные васкулиты, ассоциирующиеся с синтезом антинейтрофильных цитоплазматических антител (АНЦА), – группа системных аутоиммунных заболеваний, характеризующихся преимущественно васкулитом мелких сосудов и синтезом АНЦА [32]. Выделяют 2 основные формы этих васкулитов: гранулематоз Вегенера (ГВ), для которого характерно образование гранулем и деструктивное поражение верхних дыхательных путей, и микроскопический полиангиит (МПА), при котором эти проявления, как правило, не наблюдаются.
Применение ритуксимаба при АНЦА–ассоциированных системных васкулитах теоретически оправдано и определяется важной патогенетической ролью АНЦА (антитела к протеиназе 3 и антитела к миелопероксидазе) в развитии системного поражения сосудов. Кроме того, В–клетки участвуют в образовании гранулем при ГВ, а увеличение их уровня в периферической крови ассоциируется с активностью заболевания.
В настоящее время проведено очень большое число клинических исследований, свидетельствующих об эффективности ритуксимаба при ГВ и МПА (табл. 3).
Таблица 3. Эффективность ритуксимаба при АНЦА–ассоциированных системных васкулитах
| Авторы | Характеристика | Эффективность | Обострение |
| O. Flossman et al. [33] | Проспективное n=11 (5 ГВ, 5 МПА, 1 синдром Чарга–Стросса) | Полная ремиссия – 9 Частичная ремиссия – 1 Отсутствие эффекта – 1 |
У 6 (в среднем через 16,5 мес.) |
| K.A. Keogh et al. [34] | Проспективное n=10 (ГВ) | Полная ремиссия – 10 | 1 (9 мес.) |
| P.M. Aries et al. [35] | Проспективное n=7 | Полная ремиссия – 1 Частичная ремиссия – 1 Отсутствие эффекта – 5 |
Нет данных |
| K.A. Keogh et al. [36] | Ретроспективное n=11 (10 ГВ, МПА – 1) | Полная ремиссия – 11 | 2 (7 и 12 мес.) |
| P. Eriksson et al. [37] | Ретроспективное n=9 (2 ГВ, 5 МПА) | Полная ремиссия – 1 Частичная ремиссия – 2 |
2 (2 и 13 мес.) |
| R. Omdal et al. [38] | Ретроспективное n=3 (ГВ) | Полная ремиссия – 3 | 3 (8, 12 и 27 мес.) |
| J–E Gottenberg [20] | Ретроспективное n=2 (ГВ) | Полная ремиссия – 1 Частичная ремиссия – 1 |
Нет данных |
Примечание: ГВ – гранулематоз Вегенера; МПА – микроскопический полиангиит
В целом выраженный клинически эффект в отношении основных клинических проявлений болезни отмечен более чем у 90% пациентов. При этом более чем у 80% пациентов была достигнута полная ремиссия, а обострение заболевание хорошо контролировалось повторными курсами терапии (в среднем через 9–12 мес.). Примечательно, что обострение ассоциировалось с нормализацией уровня В–клеток и увеличением титров АНЦА. Однако у многих больных ремиссия сохранялась в отсутствии лечения или на фоне приема небольших доз ГК, несмотря на нормализацию уровня В–клеток и увеличение титров АНЦА. Следует обратить внимание на то, что некоторые проявления ГВ, в частности ретроорбитальная гранулема, менее «чувствительна» к ритуксимабу, чем гранулематозное поражение легких. У некоторых пациентов ритуксимаб назначали в комбинации с другими иммуносупрессивными препаратами, включая циклофосфамид, метотрексат, азатиоприн и микофенолата мофетил, в то время как у других – в виде монотерапии в сочетании только с ГК. Следует обратить внимание на то, что полный клинический эффект на фоне лечения ритуксимабом развивается к концу третьего месяца, что диктует необходимость дальнейшего изучения оптимальных схем комбинированной терапии.
Криоглобулинемический васкулит
Смешанная криоглобулинемия (СК) – системный васкулит, связанный с пролиферацией клонов В–клеток, синтезирующих «патогенный» IgM, обладающий активностью ревматоидного фактора (РФ) [32]. СК ведет к развитию широкого спектра клинических проявлений, выраженность которых варьирует от умеренно выраженного кожного васкулита по типу пурпуры, артралгий и астении (синдром СК) до тяжелых неврологических нарушений и поражения почек. В настоящее время убедительно доказана роль вируса гепатита С (ВГС) в развитии СК, который выявляется у 60–90% пациентов, а у 36–55% пациентов, инфицированных ВГС, развивается криоглобулинемия. При этом у 15–20% пациентов с СК, ассоциированной с ВГС, развивается тяжелых васкулит, который в отсутствие эффективного лечения может привести к летальному исходу у 15–20% с КВ, связанным с ВГС, и у 50% с ЕСК.
Лечение СК практически не разработано. У пациентов с инфекцией ВГС монотерапия интерфероном (ИФН)–α недостаточно эффективна и часто сопровождается развитием обострений. Более эффективна комбинированная терапия ИФН–α и рибавирином, на фоне которой почти у 80% пациентов развивается ремиссия, однако у некоторых пациентов имеют место тяжелые побочные эффекты. Применение ГК, циклофосфамида и плазмафереза у пациентов, резистентных к противовирусной терапии, также имеет ограниченную эффективность и сопровождается тяжелыми побочными эффектами.
В настоящее время проведена серия исследований (всего 57 пациентов), которые суммированы в обзоре P. Cocoub и соавт. [39], свидетельствующих о высокой эффективности ритуксимаба при КВ (табл. 4).
Таблица 4. Эффективность ритуксимаба при криоглобулинемическом васкулите [39]
| ВГС (+) n=43 | ВГС (-) n=14 | |||
| n | % | n | % | |
| Поражение кожи • Полная/частичная ремиссия |
33 27 |
81,8 | 5 3 |
60 |
| Артралгии • Полная/частичная ремиссия |
30 24 |
80 | 4 3 |
75 |
| Нейропатия • Полная/частичная ремиссия |
25 23 |
92 | 4 4 |
100 |
| Криоглобулинемия • Полная/частичная ремиссия |
15 13 |
86,6 | 7 5 |
71,4 |
У двух третей больных был КВ, связанный с инфекцией ВГБ, а у остальных – ессенциальная смешанная криоглобулинемия (ЕСК). Основными клиническими проявлениями КВ были поражение кожи (84%), артралгии (61,4%), периферическая нейропатия (54,4%), гломерулонефрит (31,6%), которые были рефрактерны у противовирусной (более чем у половины больных) и иммуносупрессивной терапии у остальных. Как видно из таблицы 4, ритуксимаб был эффективен в отношении основных клинических проявлений КВ, причем у 80–93% пациентов развилась полная (или частичная) ремиссия. Однако у 39% больных развилось обострение в среднем через 6,7 мес. после последней инфузии. При этом у 8 из 14 удалось достигнуть ремиссии на фоне повторного курса терапии. Примечательно, что ритуксимаб был одинаково эффективен как у пациентов с ЕСК, так и с КВ, связанным с ВГС.
Идиопатическая тромбоцитопеническая пурпура
Идиопатическая тромбоцитопеническая пурпура (ИТП) – частое гематологическое аутоиммунное заболевание, связанное с синтезом антитромбоцитарных антител, характеризующееся тромбоцитопенией и риском кровотечений. В настоящее время проведено 19 исследований (всего 313 пациентов), в которых изучалась эффективность ритуксимаба, и 29 исследований (306 пациентов), посвященных безопасности терапии, результаты которых обобщены в недавно опубликованном систематическом обзоре [40]. Проведенный анализ продемонстрировал очень высокую эффективность ритуксимаба (62,5%) в отношении нормализации концентрации тромбоцитов (табл. 5).
Таблица 5. Эффективность ритуксимаба при ИТП [41]
| Число тромбоцитов х109 | Эффективность, % |
| Всего (>50) | 62,5 |
| Полный ответ (>150) | 46,3 |
| Частичный ответ (50–150) | 24,0 |
Длительность эффекта в среднем составила 10,5 мес. У большинства пациентов применялась стандартная схема лечения, состоящая из 4 еженедельных инфузий препарата в дозе 375 мг/м2. Примерно у половины пациентов до назначения ритуксимаба была проведена спленэктомия, которая была неэффективна.
Пузырчатка
Пузырчатка – потенциально смертельное аутоиммунное заболевание, проявляющееся тяжелым поражением кожи и слизистых оболочек [41]. В основе развития заболевания лежит синтез аутоантител, реагирующих с десмоглеином 1 и 3 и молекулами адгезии эпидермиса, обеспечивающими сцепление между кератиноцитами соответственно в коже и слизистых [42]. Недавно появились сообщения об успешном применении ритуксимаба у пациентов с тяжелой пузырчаткой, рефрактерной к стандартной терапии, включающей высокие дозы ГК, цитостатиков, плазмаферез и внутривенный иммуноглобулин [43]. В исследовании P. Joly и соавт. [44], в которое вошел 21 пациент, лечение ритуксимабом (375 мг/кг в течение 4 недель) привело к полной ремиссии у 18 (86%) пациентов. Длительность ремиссии составила в среднем 35 месяцев, причем у 8 пациентов удалось полностью отменить ГК, а у остальных – существенно снизить поддерживающую дозу препарата. Сходные данные ранее получены другими авторами, которые сообщают о полной ремиссии у 9 из 11 больных с фатальным течением заболевания, однако состояние ремиссии поддерживалось инфузиями внутривенного иммуноглобулина [45].
Заболевания почек
Как уже отмечалось, ритуксимаб зарекомендовал себя как эффективный препарат для лечения волчаночного нефрита. Поэтому представляют особый интерес результаты применения ритуксимаба при других формах почечной патологии.
Мембранозная нефропатия (МН) – наиболее частая причина (20%) идиопатического нефротического синдрома (ИНС) [46]. Несмотря на то что у трети пациентов могут развиваться спонтанные ремиссии, почти в 40% случаев процесс прогрессирует, приводя к развитию хронической почечной недостаточности в течение 10 лет после начала болезни, даже несмотря на проводимую иммуносупрессивную терапию [47,48].
Характерной особенностью поражения почек при МН является накопление иммунных депозитов на внешней стороне базальной мембраны клубочков почек. Иммунные депозиты состоят из IgG (часто IgG4), мембрано–атакующего комплекса комплемента (C5b–C9), а также плохо охарактеризованных белковых молекул, которые, как предполагают, могут выступать в роли аутоантигенов. Таким образом, МН может быть своеобразной формой аутоиммунного заболевания, развитие которого связано с синтезом «нефритогенных» аутоантител. В процессе изучения экспериментальной модели МН, Хеймановского нефрита, было показано, что одним из вероятных аутоантигенов является мембранный белок подоцитов почки, который получил название мегалин. Его аналогом при МН у человека может быть нейтральная эндопептидаза – фермент, присутствующий на мембране подоцитов и других компонентов почечной ткани [49].
По данным P. Ruggenenti и соавт. [50], лечение ритуксимабом ассоциируется с достоверным снижением протеинурии, увеличением концентрации сывороточного альбумина у пациентов с ИНС, резистентным к длительной терапии ингибиторами ангиотензинпревращающего фермента (АПФ). Отмечена связь между эффективностью терапии ритуксимабом и тяжестью интерстициального фиброза и атрофии канальцев, по данным морфологического исследования в динамике [51].
Кроме того, предварительные результаты свидетельствуют о высокой эффективности ритуксимаба у детей с стероидрезистентным нефротическим синдромом [52] и очаговым сегментарным гломерулосклерозом, нередко развивающимся после пересадки почки [53]. Эти данные свидетельствуют о перспективах применения ритуксимаба в нефрологии и трансплантологии [54].
Таким образом, ритуксимаб является чрезвычайно эффективным и относительно безопасным препаратом для лечения РА и других тяжелых аутоиммунных заболеваний. Его внедрение в клиническую практику по праву можно считать крупным достижением медицины начала XXI века, которое имеет не только важное клиническое, но и теоретическое значение, поскольку способствует расшифровке фундаментальных звеньев патогенеза аутоиммунных заболеваний человека.
Фактически ритуксимаб является родоначальником нового направления в лечении аутоиммунных заболеваний человека, в основе которого лежит модуляция В–клеточного звена иммунитета.
Однако изучение места ритуксимаба в клинической медицине только начинается. Поскольку, как уже отмечалось, в большинстве случаев препарат назначали пациентам с очень тяжелым течением болезней, нередко по жизненным показаниям, неудивительно, что контролируемых исследований его эффективности и безопасности при большинстве аутоиммунных заболеваний (за исключением РА) до сих пор не проводилось. Тем не менее, хотя представленные выше оптимистические результаты основываются главным образом на материалах открытых «пилотных» исследований или ретро спективном анализе исходов терапии в небольших группах больных, они создают хорошие предпосылки для более широкого внедрения ритуксимаба в клинической практике и должны стимулировать организацию широкомасштабных контролируемых испытаний, необходимых для расширения официальных показаний к его применению.
ЛИТЕРАТУРА
1. Browning JL. B cell move to centre stage: novel opportunities for autoimmune disease treatment. Nature Rev. 2006; 5: 564–576
2. Bizzaro N, Tozzoli R, Shoenfeld Y. Are we at stage to predict autoimmune rheumatic diseases? Arthritis Rheum 2007; 56: 1736–1744
3. Hansen A, Lipsky PE, Dorner T. B cell lymphoproliferation in chronic inflammatory rheumatic diseases. Nature Clin Pracr Rheumatol 2007; 3: 561–
4. Edwards JCW, Cambridge G. Rheumatoid arthritis: the predictable effect of small immune complexes in which antibody is also antigen. Br J Rheumatol. 1998; 37:126–130.
5. Youinou P, Jamin C, Saraux A. B–cell: a logical target for treatment of rheumatoid arthritis. Clin Exp Rheumatol 2007; 25: 318–328
6. Driver CB, Ishimori M, Weisman WH. The B cell in systemic lupus erythematosus: a rational target for more effective therapy. Ann Rheum Dis 2007; August 24 on line
7. Edwards JCW, Cambridge G, Leandro MJ. B cell depletion therapy in rheumatic disease Best Pract Res Clin Rheumatol 2006; 20: 915–928
8. Reff ME, Carner K, Chambers KS, et al. Depletion of B cells in vivo by a chimeric mouse human antibody to CD20. Blood. 1994; 83:435–445.
9. Boye J, Elter T, Engert A. An overview of the current clinical use of the anti–CD20 monoclonal antibody rituximab. Ann Oncol 2003; 14: 520–535
10. Johnson P, Glennie M. The mechanism of action of rituximab in the elimination of tumor cells. Semin Oncol 2003 (Supp 2); 30:3–8.
11. Насонов ЕЛ. Перспективы применения моноклональных антител к В–лимфоцитам (ритук-симаб) при ревматоидном артрите. Клин. Фармакол. терапия 2006; 1–5:55–58
12. Насонов Е.Л. Новые направления терапии ревматоидного артрита: перспективы применения моноклональных антител к В–лимфоцитам (ритуксимаб). РМЖ 2006; 25: 1778–1782
13. Соловьев С.К., Котовская М.А., Насонов Е.Л. Ритуксимаб в лечении системной красной волчанки. РМЖ 2005; 13: 1731–1735
14. Nielsen CH, Fassi DE, Hasselbalch HC, et al. B cell depletion with rituximab in the treatment of autoimmune disrases. Expert Opin Biol Ther 2007; 7: 1061–1078
15. Schmidt E, Hunzelman N, Zillikens D, et al. Rituximab in refractory autoimmune diseases Clin Exp Dermatol 2006; 31: 503–508
16. Lipsky PE. Systemic lupus erythematosus: an autoimmune disease of B cell hyperactivity. Nat Immunol. 2001; 2:764–766.
17. Соловьев СК, Торгашина А, Асеева Е, Насонов Е.Л. Ритуксимаб. Анти–В–клеточная терапия системной красной волчанки. ГУ Институт ревматологии РАМН, Москва, 2007, 20 стр.
18. Moutsopoulos HM, Chused TM, Mann DL, et al. Sjogrens`s syndrome (sicca syndrome): current issues. Ann Intern Med 1980; 92: 212–226
19. Ramos–Casals M, Brito–Zeron P. Emerging biological therapy in primary Sjogren`s syndrome. Rheumatology 2007, June 22, on line.
20. Gottenberg J–E, Guillevin L, Lambotte O, et al. Tolerance and short term efficacy of rituximab in 43 patients with systemic autoimmune disease. Ann Rheum Dis 2005;64: 913–920.
21. Pijpe J, van Imhoff GW, Spijkervet FK, et al. Rituximab treatment in patients with primary Sjogren`s syndrome: an open–label phase II study. Arthritis Rheum 2005; 64: 913–920
22. Seror R, Sorbet C, Guilleven L, et al. Tolerance and efficacy of rituximab and changed in serum biomarkers in patients with systemic complications of primary Sjogren`s syndrome. Ann Rheum Dis 2006; Sept 1 on lime
23. Davauchelle–Pensec V, Pennec Y, Morvan J, et al. Improvement of Sjogren`s syndrome after two infusions of rituximab (Anti–CD20). Arthritis Care Res 2007; 57: 310–317
24. Voulgarelis M, Giannouli S, Anagnostou D, Tzioufas AG, Combined therapy with rituximab plus cyclophosphamide/doxorubicin/vincristin/prednisolon (CHOP) for Sjogren`s syndrome associated B–cell aggressive B cell aggressive non–Hodgkin`s lymphoma. Rheumatology (Oxford) 2004; 43: 1050–1053
25. Dalakas MC, Hohlfeld R. Polymyositis and dermatomyositis. Lancet 2003; 362: 971–982.
26. Levin T.D. Rituximab in the treatment of dermatomyositis. Arthritis Rheum 2005; 52: 601–607.
27. Noss EH, Hausner–Sypek DL, Weinblatt ME. Rituximab as the therapy for refractory polymyosi-tis and dermatomyositis. J Rheumatol 2006; 33: 1021–1026.
28. Lambotte O, R Kotb, G Maigne et al. Efficacy of Rituximab in refractory polymyositis.J Rheumatology 2005;32:1369–70.
29. Brulhart L, Waldburger J–M, Gabay C. Rituximab in the treatment of antisynthetase syndrom. Ann Rheum Dis 2006; 65: 974–975
30. Cooper MA, Willingham DL, Brown DE, et al. Rituximab for the treatment of juvenile dermato-myositis. Arthritis Rheum 2007; 56: 3107–3111
31. Mok CC, Ho LY, To CH. Rituximab for refractory polymyositis: an open–label prospective study. J Rheumatol 2007; 34: 1864–1868
32. Насонов Е.Л., Баранов А.А., Шилкина Н.П. Васкулиты и васкулопатии. Ярославль. Издательство «Волга», 1999., 612 стр.
33. Flossman O, Jones RB, Jayne DRW, Luqmani RA. Should rituximab be used to treat antineu-trophil cytoplasmic antibody associated vasculitis? Ann Rheum Dis 2006;15 June on line.
34. Keogh KA, Ytterberg SR, Fervenza FC, Carlson KA, Schroeder DR, Specks U. Rituximab for refractory Wegener’s granulomatosis: report of a prospective, open–label pilot trial. Am J Respir Crit Care Med 2006;173:180–7
35. Aries PM, Hellmich B, Voswinkel J, Both M, N lle B, Holl–Ulrich K, et al. Lack of efficacy of ritu-ximab in Wegener’s granulomatosis with refractory granulomatous manifestations. Ann Rheum Dis 2006;65:853–8.
36. Keogh KA, Wylam ME, Stone JH, Specks U. Induction of remission by B lymphocyte depletion in eleven patients with refractory antineutrophil cytoplasmic antibody–associated vasculitis. Arthritis Rheum 2005;52:262–8
37. Eriksson P. Nine patients with anti–neutrophil cytoplasmic antibody–positive vasculitis successfully treated with rituximab. J Intern Med 2005;257:540–8.
38. Omdal R, Wildhagen K, Hansen T, Gunnarsson R, Kristoffersen G. Anti–CD20 therapy of treatment–resistant Wegener’s granulomatosis: favourable but temporary response. Scand J Rheumatol 2005;34:229–32
39. Cocoub P, Delluc A, Saadoun D, et al. Anti–CD20 monoclonal antibody (rituximab) treatment for cryoglobulinemia vasculitis? Where do we stand? Ann Rheum Dis 2007; 20 June on line.
40. Arnold DA, Dentali F, Crowther MA, et al. Systemic review: efficacy and safety of rituximab for adults with idiopathic thrombocytopenic purpura. Ann Intern Med 2007; 146: 25–33
41. Anhalt GJ, Diaz LA. Research advances in pemphigus. JAMA 2001; 285:652–654
42. Kottke MD, Delva E, Kowalczyk. The desmosome; cell science lessons from human diseases. J Cell Sci 2006; 119: 797–806
43. Schmidt E, Hunzelman N, Zillikens D, et al. Rituximab in refractory autoimmune bullous diseases. Clin Exp Dermatol 2006; 31: 503–508
44. Joly P, Mouquet H, Roujeau J–C, et al. A single cycle of rituximab for the treatment of severe pemphigus. New Engl J Med 2007; 357: 545–552
45. Ahmed AR, Spigelman Z, Cavacini LA, Posner MR. Treatment of pemphigus vulgaris with rituxi-mab and intravenous immune globulin. New Engl J Med 2006; 355: 1772–1779
46. Glassoks RJ. Diagnosis and natural course of membranous nephropathy. Semin Nephrol 2003; 23: 324–332.
47. Glassock RJ. The treatment of idiopathic membranous nephropathy; a dilemma or a conundrum? Am J Kidney Dis 2004; 44: 562–566
48. Perna A, Schieppati A, Zamora J, et al. Immunosupressive treatment for idiopathic membranous nephropathy: a systemic review. Am J Kidney Dis 2004; 44: 385–401
49. Ronco P, Debiec H. Molecular dissection of target antigens and nephritogenic antibodies in membranous nephropathy; towards epitope–driven therapies. J Am Soc Nephrol 2006; 17: 1772–1774
50. Ruggenenti P, Chiurchiu C, Brusegan V, et al. Rituximab in idiopathic membranous nephropat-hy; a one–year prospective study. J Amer Soc Nephrol 2003;14:1851–1857
51. Ruggenenti P, Chiurchiu C, Abbate M, et al. Rituximab for idiopathic membranous nephropathy; who can benefit? Clin J Am Soc Nephrol 2006; 1: 738–748
52. Bagga A, Sinha A, Moudgil A. Rituximab in patients with steroid–resistant nephrotic syndrome. New Engl J Med 2007; 356: 2751–2752
53. Pescovitz MD, Book BK, Sidner RA. Resolution of recurrent focal segmental glomerulosclerosis proteinuria after rituximab treatment. N Engl J Med 2006; 35: 1961–1963
54. Salama AD, Pusey CD. Rituximab in renal disease and transplantation Nature Clin Pract Nephrol 2005; 2: 221–230.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Ритуксимаб — революционер в химиотерапии некоторых злокачественных лимфом, к тому же произведенный с помощью генной инженерии.
- Химические свойства и состав
- Фармакологическое действие
- Фармакодинамика и фармакокинетика
- Показания к применению
- Противопоказания
- Побочные действия
- Особые указания
- Передозировка
- Взаимодействие
- Фертильность, беременность и лактация
- Срок годности
- Аналоги
Химические свойства и состав
Ритуксимаб относится к биологическим лекарственным препаратам, а конкретно — к моноклональным антителам или коротко МАБ.
Это иммуноглобулин, то есть синтезируемый иммунными клетками крупный белок.
По функционалу – антитело, которому в организме человека надлежит связаться с определенного вида антигеном – чужеродным белком, бактериальным продуктом или определенного рода клеточным субстратом. Ритуксимабу необходимо связаться с рецептором на поверхности нездоровой клетки крови.
Это моноклональное антитело, поскольку производится не всеми подряд клетками крови, а определенной группой или клоном.
Белок состоит из трёх разной длины цепочек аминокислот, синтезированных клетками мышей и человеческими, поэтому антитело называется химерным, то есть смешанным из животных и человеческих белков – для уменьшения токсичности лекарства.
Фармакологическое действие
В организме человека ритуксимаб ищет специальный антиген CD20, который существует на поверхности большинства злокачественных клеток, составляющих В-лимфомы, и на обычных В-лимфоцитах. На других клетках крови подобного антигена быть не должно и в плазме крови он не плавает.
Связавшись с антигеном, ритуксимаб обрывает жизненно необходимую цепочку клеточных биохимических реакций, и как результат – клетка включает программу самоубийства или апоптоза. Кроме того, препарат усиливает повреждающее действие других цитостатиков, поэтому его включают в схемы химиотерапии при лимфомах и лимфолейкозе.
Поскольку МАБ убивает и нормальные В-лимфоциты, обладающие CD20, то они тоже погибают. Как видим, избирательность действия лекарственного препарата заключается не в способности найти и уничтожить опухолевую клетку, а в убийстве обладающих антигеном клеток. У одного из сотни больных лимфомой организм вырабатывает антитела, нейтрализующие химерные белки, что делает использование препарата бесполезным.
Фармакодинамика и фармакокинетика
Практически весь введенный ритуксимаб с кровью доходит до места приложения силы, что обозначается как 100% биодоступность. Концентрация препарата в крови возрастает с каждым введением, к четвёртой капельнице количество активного вещества вдвое больше начального, а к восьмой капельнице достигается максимум. На этом процессе не отражается ни возраст пациента, ни его пол, ни национальность.
На выведение из организма половины дозы лекарственного средства потребуется более трёх недель, но следы находят и через полгода после завершения лечения. Выведение ритуксимаба возложено на макрофаги, также заглатывающие бактерии, вирусы и всё чужеродное для человека, но это только предположение. Почки и печень, по-видимому, в процессе удаления препарата не участвуют, во всяком случае у пациентов с недостаточностью их функции нет необходимости изменять дозировку.
Показания к применению
К ритуксимабу чувствительны только клеточные колонии, содержащие на поверхности рецепторы СD20, и сегодня такие лимфопролиферативные процессы специально выявляются анализами. Как правило, хорошо реагируют на терапию неходжкинские В-крупноклеточные лимфомы и низкой агрессивности фолликулярные лимфомы. Препарат используется как в самом начале и для поддерживающего лечения, так и при прогрессировании заболевания на других схемах, и при появлении рецидивов.
Второе показание – хронический лимфолейкоз, используется в первой линии, при неэффективности предшествующей химиотерапии или рецидиве, как правило, в комплексе с другими цитостатиками.
Противопоказания
Исключено применение ритуксимаба при аллергии на него.
Нельзя использовать у пациентов с иммунным дефицитом, поскольку препарат уничтожает и без того недостаточные В-лимфоциты.
При острых воспалительных и инфекционных процессах на лечение накладывается временное табу, так как подавление иммунитета может привести к генерализации инфекции.
Очень осторожно используется лекарство при сниженных показателях лейкоцитов – нейтрофилов и тромбоцитов, что обычно для последствий химиотерапии.
Введение препарата часто осложняется одышкой и отеком легочной ткани, поэтому у пациентов с легочными метастазами или дыхательной недостаточностью могут быть очень неприятные для здоровья последствия. Тем не менее, это не считается абсолютным противопоказанием, просто надо проводить лечение с известной долей предусмотрительности.
Клинические исследования у несовершеннолетних не проводятся, поэтому неизвестны «подводные камни» терапии, оттого препарат не лицензирован для этой возрастной категории. Исключено применение у беременных и кормящих мам.
Побочные действия
Любое противоопухолевое лечение чревато осложнениями и ритуксимаб не исключение, спектр осложнений достаточно широк, некоторые побочные реакции встречаются часто, некоторые не минует большинство пациентов. При комбинированной химиотерапии на токсичность ритуксимаба накладываются побочные реакции от других препаратов схемы.
Очень часто на фоне лечения ритуксимабом развивается:
- локальная отечность кожи – ангионевротический отек, когда участок «подушкой» поднимается рядом с совершенно неизменными тканями;
- развитие инфекции сопряжено с механизмом действия и главной силой препарата – уничтожением лимфоцитов;
- разнообразные сыпи с зудом;
- головные боли и нередко с повышением температуры;
- тошнота.
После курса в анализе крови снижаются показатели и G-иммуноглобулин, но 4 степень падения уровня отмечается едва ли у 1-2%. Уменьшение численности В-лимфоцитов не фатально, но очень продолжительно — до года.
При очень высокой чувствительности к ритуксимабу и массированным распадом опухолевых узлов возможно развитие синдрома опухолевого лизиса, который необходимо заблаговременно спрогнозировать и провести профилактические мероприятия.
Особые указания
У каждого второго во время капельницы, особенно при первых введениях, развивается неприятное состояние – инфузионная реакция, когда пациент ощущает резко нахлынувшую слабость до «трясучки», с тошнотой и головной болью, в некоторых местах начинает зудеть кожа и может быстро появиться сыпь, из-за спастического сокращения дыхательных путей трудно дышать.
Если, несмотря на предварительное введение лекарственных средств – премедикацию, развилась тяжелая инфузионная реакция, то на время прекращается введение ритуксимаба, дополнительно внутривенно вводятся вспомогательные препараты, и при нормализации состояния продолжают капельное введение ритуксимаба, но скорость падения капель уменьшаю вдвое.
Как правило, к следующей капельнице интенсивность реакции снижается, а последнюю 8-ую капельницу 99% пациентов переносят без реакции. Тем не менее, всегда перед введением ритуксимаба профилактически вводятся препараты, предотвращающие аллергические проявления, болевой синдром и повышение температуры.
Передозировка
В инструкции к препарату производители указывают отсутствие сведений о передозировке – превышению разрешенной для использования дозы. Передозировка при химиотерапии невозможна, поскольку лекарство вводится в стандартной дозе, рассчитываемой на поверхность тела больного. Плохая переносимость не имеет отношения к передозировке, так как побочные реакции обусловлены механизмом действия лекарственного средства и индивидуальной чувствительностью тканей пациента.
Взаимодействие
Ритуксимаб входит в множество лекарственных комбинаций, которые изучаются в клинических исследованиях не только на эффективность, но и безопасность для пациентов. Для лечения онкогематологических процессов рекомендуются определенные – стандартные комбинации, в которых минимально совпадает токсичность при максимальной результативности каждого препарата в отдельности.
Для капельного введения ритуксимаба используются специальные системы, поскольку молекулы лекарства соединяются с материалом обычных капельниц.
Фертильность, беременность и лактация
На беременных и кормящих, как и на детях, противоопухолевые лекарства не изучаются. В доклинических исследованиях, конечно, могут проводиться эксперименты с беременными животными, но совпадение реакций у животных и человека абсолютно не гарантируется.
Иммуноглобулины G способны проходить в грудное молоко и плод, у случайно забеременевших на фоне лечения МАБ анализы крови новорожденных демонстрировали снижение числа В-лимфоцитов.
Женщинам репродуктивного возраста настоятельно рекомендуется предохранение во время терапии и не менее года после её завершения.
Срок годности
После выпуска препарат разрешается использовать два с половиной года.
Аналоги
Ритуксимаб – биологический препарат, состоящий из 1200 аминокислот, часть которых довольно постоянна. Точное копирование его структуры совершенно невозможно, поскольку производство базируется на генной инженерии. Все производители ритуксимаба стараются сделать идентичный оригиналу препарат, но отличаются лабораторные мыши, белковые структуры которых идут на изготовление лекарства.
Клинические исследования, как правило, проводятся только с первым — оригинальным средством, остальные — только копии с неизвестной долей отличий, поэтому эффективность с токсичностью препаратов от разных производителей могут отличаться.
Ритуксимаб – это международное наименование, каждый производитель дает лекарству свое имя — торговое, первым была Мабтера. После окончания патентной защиты появилась ацеллбия, реддитукс и другие.
Вам не надо думать, какое лекарственное средство для вас лучше и где его купить – это наша забота, вы просто должны быть уверенными, что получите только оригинальный препарат, имеющий достоверные доказательства клинической эффективности и безопасности.
Список литературы
- Ardeshna K., Qian W., Smith P. et al. /An Intergroup Randomised Trial of Rituximab Versus a Watch and Wait Strategy In Patients with Stage II, III, IV, Asymptomatic, Non-Bulky Follicular Lymphoma (Grades 1, 2 and 3a). A Preliminary Analysis// Blood (ASH Annual Meeting Abstracts). 2010;116
- Kahl B.S., Hong F., Williams M. et al./ Results of Eastern Cooperative Oncology Group Protocol E4402 (RESORT): A Randomized Phase III Study Comparing Two Different Rituximab Dosing Strategies for Low Tumor Burden Follicular Lymphoma// Blood (ASH Annual Meeting Abstracts). 118(21):LBA-6.
- Hallek M, Fischer K, Fingerle-Rowson G. et al./ Addition of rituximab to fludarabine and cyclophosphamide in patients with chronic lymphocytic leukaemia: a randomised, open-label, phase 3 trial// Lancet. 2010; 376(9747).
- Fischer K, Cramer P, Busch R, et al. / Bendamustine in combination with rituximab for previously untreated patients with chronic lymphocytic leukemia: A multicenter Phase II study of the German Chronic Lymphocytic Leukemia Study Group //J Clin Oncol 2012: 30.
МНН: Ритуксимаб
Производитель: Карагандинский фармацевтический комплекс
Анатомо-терапевтическо-химическая классификация: Rituximab
Номер регистрации в РК:
РК-ЛС-5№023141
Информация о регистрации в РК:
04.10.2021 — 04.10.2031
Информация о реестрах и регистрах
Информация по ценам и ограничения
Предельная цена закупа в РК:
292 716.6 KZT
- Скачать инструкцию медикамента
Торговое название
Ритуксимаб
Международное непатентованное название
Ритуксимаб
Лекарственная форма
Концентрат
для приготовления раствора для инфузий,10
мг/мл
Состав
1
мл препарата
содержит
активное
вещество
— ритуксимаб – 10.0
мг,
вспомогательные
вещества: натрия цитрата дигидрат –
7.35
мг, полисорбат—80
– 0.70
мг, натрия хлорид – 9.00
мг, кислота хлороводородная – до рН 6.5,
вода для инъекций – до 1.0 мл.
Описание
Прозрачная,
от бесцветного до светло-желтого цвета жидкость
Фармакотерапевтическая группа
Антинеопластические
и иммуномодулирующие препараты. Антинеопластические препараты.
Антинеопластические препараты другие. Моноклональные
антитела. Ритуксимаб.
Код
АТХ L01XC02
Фармакологические свойства
Фармакокинетика
Неходжкинская
лимфома
По
данным популяционного фармакокинетического анализа у пациентов с
неходжкинской лимфомой при однократном или многократном введении
ритуксимаба в виде монотерапии или в комбинации с химиотерапией по
схеме CHOP (циклофосфамид, доксорубицин, винкристин, преднизолон)
неспецифический клиренс (CL1),
специфический клиренс (CL2)
(вероятно, связанные с В-клетками или опухолевой нагрузкой) и объем
распределения в плазме (V1)
составляют 0,14 л/день, 0,59 л/день и 2,7 л, соответственно. Медиана
терминального периода полувыведения (Т1/2)
составляет 22 дня. Исходный уровень CD19-положительных клеток и
размер опухолевого очага влияет на CL2
ритуксимаба, вводимого внутривенно в дозе 375 мг/м2
1 раз в неделю, в течение 4 недель. Показатель CL2
выше у пациентов с более высоким уровнем CD19-положительных клеток
или большим размером опухолевого очага. Индивидуальная вариабельность
CL2 сохраняется и
после коррекции размера опухолевого очага и уровня CD19-положительных
клеток. Относительно небольшие изменения показателя V1
зависят от величины площади поверхности тела (1,53-2,32 м2)
и от химиотерапии по схеме CHOP и составляют 27,1% и 19,0%,
соответственно. Возраст, пол, расовая принадлежность, общее состояние
по шкале ВОЗ (Всемирной Организации Здравоохранения) не влияют на
фармакокинетику ритуксимаба. Таким образом, коррекция дозы
ритуксимаба в зависимости от вышеперечисленных факторов значимо не
влияет на фармакокинетическую вариабельность.
Средняя
максимальная концентрация (Cmax)
возрастает после каждой инфузии: после первой инфузии составляет 243
мкг/мл, после четвертой инфузии — 486 мкг/мл, а после восьмой — 550
мкг/мл. Минимальная и максимальная концентрации препарата обратно
пропорционально коррелируют с исходным числом CD19-положительных
В-клеток и величиной опухолевой нагрузки. При эффективном лечении
медиана равновесной концентрации препарата выше. Медиана равновесной
концентрации препарата выше у пациентов с гистологическими подтипами
опухоли В, С и D (классификация IWF), чем с подтипом А. Следы
ритуксимаба можно обнаружить в организме в течение 3-6 месяцев после
последней инфузии.
Фармакокинетический
профиль ритуксимаба (6 инфузий по 375 мг/м2)
в комбинации с 6 циклами химиотерапии CHOP был практически таким же,
как и при монотерапии.
Хронический
лимфолейкоз
Средняя
максимальная концентрация (Cmax)
после пятой инфузии ритуксимаба в дозе
500 мг/м2
составляет 408 мкг/мл.
Гранулематоз
с полиангиитом (гранулематоз Вегенера) и микроскопический полиангиит
По
данным популяционного фармакокинетического анализа после четырех
инфузий ритуксимаба в дозе 375 мг/м2
1 раз в неделю медиана Т1/2
– 23 дня, средний клиренс – 0.313 л/сутки и объем
распределения – 4.5 л.
Фармакокинетика
у отдельных групп пациентов
Пол:
объем распределения и клиренс ритуксимаба с поправкой на площадь
поверхности тела у мужчин несколько больше, чем у женщин, коррекции
дозы ритуксимаба не требуется.
Пациенты
с почечной и печеночной недостаточностью:
фармакокинетические данные у больных с почечной и печеночной
недостаточностью отсутствуют.
Фармакодинамика
Активным
компонентом препарата Ритуксимаб является ритуксимаб — химерное
моноклональное антитело мыши/человека, которое специфически
связывается с трансмембранным антигеном CD20. Этот антиген расположен
на пре-В-лимфоцитах и зрелых В-лимфоцитах, но отсутствует на
стволовых гемопоэтических клетках, про-В-клетках, нормальных
плазматических клетках, клетках других тканей и экспрессируется более
чем в 95% случаев при В-клеточных неходжкинских лимфомах.
Экспрессированный на клетке СD20 после связывания с антителом не
интернализуется и перестает поступать с клеточной мембраны во
внеклеточное пространство. CD20 не циркулирует в плазме в виде
свободного антигена и поэтому не конкурирует за связывание с
антителом.
Ритуксимаб
связывается с антигеном CD20 на В-лимфоцитах и инициирует
иммунологические реакции, опосредующие лизис В-клеток. Возможные
механизмы клеточного лизиса включают комплемент-зависимую
цитотоксичность, антитело-зависимую клеточную цитотоксичность и
индукцию апоптоза. Ритуксимаб повышает чувствительность линий
В-клеточной лимфомы человека к цитотоксическому действию некоторых
химиотерапевтических препаратов in vitro.
Число
В-клеток в периферической крови после первого введения препарата
снижается ниже нормы и начинает восстанавливаться у пациентов с
гематологическими злокачественными заболеваниями через 6 месяцев,
достигая нормальных значений через 12 месяцев после завершения
терапии, однако продолжительность периода восстановления количества
В-клеток может быть больше.
У
пациентов с гранулематозом с полиангиитом и микроскопическим
полиангиитом снижение числа CD19-положительных
B-клеток
до уровня менее 10 клеток/мкл происходит после двух первых инфузий
ритуксимаба, и у большинства пациентов сохраняется на данном уровне в
течение 6 месяцев.
Антихимерные
антитела выявлены у 1,1% обследованных больных с неходжкинской
лимфомой. Антимышиные антитела у обследованных больных не выявлены.
Показания к применению
Применение
препарата Ритуксимаб
показано пациентам со
следующими заболеваниями:
Неходжкинская
лимфома
Препарат
Ритуксимаб
показан к применению для
лечения фолликулярной лимфомы III-IV стадии в комбинации с
химиотерапией у ранее нелеченых пациентов.
Препарат
Ритуксимаб
показан к применению для
лечения фолликулярной лимфомы в качестве поддерживающей терапии после
ответа на индукционную терапию.
Препарат
Ритуксимаб показан к применению в качестве монотерапии при лечении
фолликулярной лимфомы III-IV стадии в случае выявлении
химиоустойчивости или при втором и последующих рецидивах после
химиотерапии.
Препарат
Ритуксимаб
показан к применению при
лечении CD20-положительной диффузной В-крупноклеточной неходжкинской
лимфомы в комбинации с химиотерапией по схеме СНОР (циклофосфамид,
доксорубицин, винкристин, преднизолон).
Хронический
лимфолейкоз (ХЛЛ)
Препарат
Ритуксимаб
показан к применению в
комбинации с химиотерапией при лечении
рецидивирующего/химиоустойчивого хронического лимфолейкоза и у ранее
нелеченых пациентов. Имеются только ограниченные данные об
эффективности и безопасности применения препарата при лечении
пациентов, ранее получавших моноклональные антитела, включая
ритуксимаб, или у пациентов с невосприимчивостью к предшествующей
химиотерапии в сочетании с ритуксимабом.
Ревматоидный
артрит
Препарат
Ритуксимаб
показан к применению в
сочетании с метотрексатом для лечения пациентов с тяжелым активным
ревматоидным артритом. При непереносимости или недостаточном ответе
на другие базисные противоревматические препараты, включая один или
несколько ингибиторов фактора некроза опухоли.
Было
показано, что применение ритуксимаба в сочетании с метотрексатом
приводит к уменьшению скорости прогрессирования повреждения суставов
по данным рентгенологического исследования, а также улучшению
физических функций.
Гранулематоз
с полиангиитом и микроскопический полиангиит
Препарат
Ритуксимаб
показан к применению в
сочетании с глюкокортикоидами для индукции ремиссии у взрослых
пациентов с тяжелой активной формой гранулематоза с полиангиитом
(Вегенера) и микроскопическим полиангиитом.
Способ применения и дозы
Введение
препарата Ритуксимаб должно осуществляться под тщательным наблюдением
опытного медицинского работника при наличии необходимых условий для
проведения реанимационных мероприятий.
Перед
каждой инфузией препарата Ритуксимаб необходимо проводить
премедикацию (жаропонижающий препарат, например, парацетамол, и
антигистаминный препарат, например, дифенгидрамин).
Пациентам
с неходжкинской лимфомой и хроническим
лимфолейкозом в состав премедикации
необходимо включить глюкокортикостероиды, если они не применяются в
составе схемы химиотерапии в сочетании с препаратом Ритуксимаб.
Пациентам
с ревматоидным артритом в качестве
премедикации следует ввести 100 мг метилпреднизолона внутривенно за
30 мин до применения препарата Ритуксимаб, чтобы избежать или
уменьшить частоту и тяжесть инфузионных реакций.
Пациентам
с гранулематозом с полиангиитом или
микроскопическим полиангиитом рекомендуется
вводить внутривенно по 1000 мг метилпреднизолона ежедневно в течение
от 1 до 3 дней до первого применения препарата Ритуксимаб (последняя
доза метилпреднизолона может быть введена в день первой инфузии
препарата Ритуксимаб). После этого следует назначить преднизолон в
дозе 1мг/кг/день перорально (не более 80 мг/день; с постепенным
снижением дозы преднизолона до полной отмены, темпы снижения дозы
определяются конкретной клинической ситуацией) во время и после
применения Ритуксимаба.
Необходимо
проверить маркировку препарата, чтобы убедиться, что пациенту будет
введен препарат, соответствующий сделанному назначению.
Неходжкинская
лимфома
Фолликулярная неходжкинская
лимфома
Комбинированная
терапия
Рекомендуемая
доза препарата Ритуксимаб в сочетании с химиотерапией для
индукционной терапии ранее не леченых пациентов или пациентов с
рецидивирующей/рефрактерной фолликулярной лимфомой составляет 375
мг/м2 площади
поверхности тела на один цикл, до 8 циклов.
В
случае химиотерапии с использованием глюкокортикоидных гормонов
препарат Ритуксимаб следует применять в первый день каждого цикла
химиотерапии после внутривенного введения глюкокортикоидного
компонента химиотерапии.
Поддерживающая
терапия
-
Ранее
не леченые пациенты с фолликулярной лимфомой.
Рекомендуемая
доза препарата Ритуксимаб для применения в поддерживающей терапии у
ранее не леченых пациентов с фолликулярной лимфомой, ответивших на
индукционную терапию, составляет 375 мг/м2
площади поверхности тела 1 раз в 2 месяца (начинать поддерживающую
терапию следует через 2 месяца после последней дозы индукционной
терапии) до появления признаков прогрессирования заболевания или не
дольше двух лет.
-
Пациенты
с рецидивирующей/рефрактерной фолликулярной лимфомой.
Рекомендуемая
доза препарата Ритуксимаб для применения в поддерживающей терапии у
пациентов с рецидивирующей/рефрактерной фолликулярной лимфомой,
ответивших на индукционную терапию, составляет 375 мг/м2
площади поверхности тела 1 раз в 3 месяца (начинать поддерживающую
терапию следует через 3 месяца после последней дозы индукционной
терапии) до появления признаков прогрессирования заболевания или не
дольше двух лет.
Монотерапия
-
Пациенты
с рецидивирующей/рефрактерной фолликулярной лимфомой.
Рекомендуемая
доза препарата Ритуксимаб при применении в качестве монотерапии для
индукционного лечения у взрослых пациентов с химиоустойчивой
фолликулярной лимфомой III-IV стадий или для лечения после второго и
последующих рецидивов после проведенной химиотерапии составляет 375
мг/м2 площади
поверхности тела, внутривенно один раз в неделю в течение четырех
недель.
Рекомендуемая
доза препарата Ритуксимаб для применения в качестве монотерапии для
лечения пациентов с рецидивирующей/рефрактерной фолликулярной
лимфомой, ответивших на предшествующую монотерапию ритуксимабом,
составляет 375 мг/м2
площади поверхности тела, внутривенно раз в неделю в течение четырех
недель.
Диффузная
В-крупноклеточная неходжкинская лимфома
Препарат
Ритуксимаб следует применять в комбинации с химиотерапией по схеме
СНОР. Рекомендуемая доза составляет 375 мг/м2 в
первый день каждого цикла химиотерапии после внутривенного введения
глюкокортикостероидного компонента химиотерапии по схеме CHOP, 8
циклов. Безопасность и эффективность применения ритуксимаба в
комбинации с другими химиотерапевтическими схемами для лечения
диффузной В-крупноклеточной неходжкинской лимфомы
не установлены.
Коррекция
дозы препарата во время лечения.
Не
рекомендуется снижать дозу препарата Ритуксимаб. При комбинированном
применении химиотерапии с препаратом Ритуксимаб допустимо снижение
доз компонентов химиотерапии по стандартным схемам.
Хронический
лимфолейкоз
Для
снижения риска возникновения синдрома лизиса опухоли у пациентов с
хроническим лимфолейкозом (ХЛЛ) рекомендуется профилактическое
обеспечение достаточной гидратации и введение урикостатиков за 48
часов до начала терапии. У пациентов с ХЛЛ и уровнем лимфоцитов >
25 × 109/л
рекомендуется внутривенное введение преднизона/преднизолона в дозе
100 мг за короткое время до инфузии препарата Ритуксимаб для снижения
частоты и тяжести острых инфузионных реакций и/или синдрома
высвобождения цитокинов.
Рекомендуемая
доза препарата Ритуксимаб в комбинации с химиотерапией (у пациентов,
ранее не получавших лечение, и при рецидивирующем/рефрактерном
лимфолейкозе) составляет 375 мг/м2 в
0 день первого цикла, затем 500 мг/м2 в
1 день каждого последующего цикла, 6 циклов. Химиотерапию проводят
после введения препарата Ритуксимаб.
Ревматоидный
артрит
Курс
лечения препаратом Ритуксимаб состоит из двух внутривенных инфузий в
дозе 1000 мг каждая. Рекомендуемый режим введения препарата
Ритуксимаб: первая инфузия внутривенно в дозе 1000 мг; повторная
внутривенная инфузия в дозе 1000 мг должна выполняться через 2
недели.
Необходимость
в проведении дальнейших курсов должна быть оценена через 24 недели
после предыдущего курса.
Повторное
лечение в эти сроки следует проводить только при сохранении
остаточной активности болезни, в противном случае повторное лечение
следует отложить до возобновления активности болезни.
Имеющиеся
данные об эффективности ритуксимаба показывают, что клинический
ответ, как правило, достигается в течение 16-24 недель начального
курса лечения. Необходимость продолжения терапии для пациентов, не
имеющих признаков благоприятного терапевтического эффекта в течение
этого периода времени, должна быть тщательно пересмотрена.
Гранулематоз
с полиангиитом и микроскопический полиангиит
Рекомендуемая
доза препарата Ритуксимаб для лечения, направленного на индукцию
ремиссии гранулематоза с полиангиитом или микроскопического
полиангиита: 375 мг/м2
площади поверхности тела, внутривенно 1 раз в неделю в течение
четырех недель (всего 4 инфузии).
При
необходимости рекомендуется проводить профилактические меры против
развития пневмоцистной пневмонии (пневмонии, вызванной P.jirovecii)
пациентам с гранулематозом с полиангиитом и микроскопическим
полиангиитом во время и после лечения препаратом Ритуксимаб.
Особые
группы пациентов
Дети
Эффективность
и безопасность применения ритуксимаба у детей до 18 лет не
установлена. Данные отсутствуют.
Пожилые
пациенты
При
лечении пожилых пациентов (старше 65 лет) коррекция дозы препарата не
требуется.
Правила
приготовления и хранения раствора
Необходимое
количество препарата Ритуксимаб набирают в асептических условиях и
разводят до расчетной концентрации (1-4 мг/мл) в инфузионном флаконе
(пакете) с 0,9% раствором натрия хлорида для инфузий или 5% раствором
декстрозы (растворы должны быть стерильными и апирогенными). Для
перемешивания аккуратно переворачивают флакон (пакет) во избежание
пенообразования. Перед введением необходимо осмотреть раствор на
предмет отсутствия посторонних примесей или изменения окраски.
Врач
отвечает за приготовление, условия и время хранения готового раствора
до его использования.
Так
как препарат Ритуксимаб не содержит консервантов, приготовленный
раствор необходимо использовать немедленно.
Приготовленный
инфузионный раствор физически и химически стабилен в течение 12 часов
при комнатной температуре или в течение не более 24 часов при
температуре от 2 до 8° С.
Способ
применения
Приготовленный
раствор препарата Ритуксимаб вводят внутривенно капельно, через
отдельный катетер. Вводить препарат внутривенно струйно или болюсно
нельзя.
Для
выявления возможного возникновения синдрома высвобождения цитокинов
пациенты должны находиться под наблюдением.
При
возникновении у пациентов тяжелых реакций (затрудненное дыхание,
бронхоспазм, гипоксия) инфузию следует немедленно прекратить.
Пациенты с неходжкинской лимфомой должны быть
обследованы для выявления признаков синдрома лизиса опухоли, включая
выполнение соответствующих лабораторных анализов, а также проведение
рентгенографии грудной клетки для выявления инфильтративных изменений
в легких. Лечение не должно возобновляться до полного разрешения всех
симптомов, нормализации результатов лабораторных анализов и
изменений, выявленных при рентгенографии грудной клетки. При
соблюдении этих условий лечение может быть возобновлено, но скорость
инфузии первой дозы препарата должна быть уменьшена, по крайней мере,
в 2 раза. В случае повторного возникновения тяжелых нежелательных
реакций необходимо рассмотреть вопрос о целесообразности продолжении
лечения, учитывая все особенности конкретного случая.
При
возникновении легких и умеренных инфузионных реакций в большинстве
случаев достаточно уменьшить скорость введения препарата. При
улучшении состояния пациента скорость введения препарата может быть
увеличена.
Первая
инфузия
Рекомендуемая
скорость первой инфузии препарата: 50 мг/ч; по прошествии первых 30
минут, скорость можно повышать на 50 мг/ч каждые 30 минут до
максимального значения 400 мг/ч.
Последующие
инфузии
Для
всех показаний к применению
Скорость
инфузии Ритуксимаба для последующих доз может начинаться со 100 мг/ч,
и увеличиваться на 100мг/ч каждые 30 минут до максимального значения
400 мг/ч.
Только
при ревматоидном артрите
Альтернативный
ускоренный режим последующих инфузий
Если
у пациентов не наблюдалось проявления тяжелых инфузионных реакций при
первой инфузии Ритуксимаба в дозе 1000 мг (стандартный режим
коррекции скорости инфузии), скорость инфузии препарата может быть
увеличена при второй и последующих инфузиях при той же концентрации
препарата (4 мг/мл в объеме 250 мл). Начальная скорость инфузии
должна составлять 250 мг/ч первые 30 минут, затем скорость может быть
увеличена до 600 мг/ч в течение следующих 90 минут. Если ускоренная
инфузия переносится хорошо, то этот режим введения может быть
использован при последующих инфузиях.
Пациентам,
имеющим клинически значимые сердечно-сосудистые заболевания, в том
числе аритмию, или при наличии серьезных инфузионных реакций в ходе
любого предыдущего лечения биопрепаратами, в т. ч. ритуксимабом,
увеличивать скорость инфузий не рекомендуется.
Побочные действия
Применение
при неходжкинской лимфоме и хроническом лимфолейкозе
Краткий
обзор профиля безопасности препарата
Профиль
безопасности ритуксимаба при лечении неходжкинской лимфомы и
хронического лимфолейкоза определен на основе данных клинических
испытаний и пострегистрационного наблюдения. Пациенты получали
монотерапию ритуксимабом (индукционную терапию или поддерживающую
терапию после индукционной) или терапию ритуксимабом в комбинации с
химиотерапией.
Наиболее
часто наблюдаемыми нежелательными лекарственными реакциями (НЛР) у
пациентов, получавших ритуксимаб, были инфузионные реакции,
возникавшие у большинства пациентов во время первой инфузии. Частота
связанных с инфузией симптомов существенно уменьшается с последующими
инфузиями и составляет менее 1% после восьмой инфузии ритуксимаба.
Развитие
инфекционных осложнений (преимущественно бактериальной и вирусной
природы) наблюдалось приблизительно у 30-55% пациентов во время
клинических исследований у пациентов с НХЛ и у 30-50% пациентов во
время клинических исследований у пациентов с ХЛЛ.
Наиболее
распространенные серьезные нежелательные лекарственные реакции:
-
Инфузионные
реакции (в т. ч. синдром высвобождения цитокинов и синдром лизиса
опухоли).
-
Инфекции.
-
Сердечно-сосудистые
нарушения.
Также
среди серьезных НЛР были зафиксированы реактивация гепатита В и
прогрессирующая многоочаговая лейкоэнцефалопатия.
Список
побочных реакций
Частота
возникновения побочных реакций при использовании ритуксимаба в
качестве монотерапии или в комбинации с химиотерапией приведена ниже.
В каждой частотной группе нежелательные эффекты представлены в
порядке уменьшения серьезности. Для оценки частоты реакций
используются следующие критерии: очень часто (≥ 1/10), часто
(≥ 1/100 до < 1/10), нечасто (≥ 1/1 000
до< 1/100), редко (≥ 1/10 000 до< 1/1 000),
очень редко (< 1/10 000) и неизвестно (не могут быть
оценены на основе имеющихся данных).
НЛР,
выявленные только во время пострегистрационного наблюдения, и для
которых частота не может быть оценена, перечислены как «неизвестно».
НЛР
в клинических исследованиях или во время пострегистрационного
наблюдения у пациентов с НХЛ и ХЛЛ, получавших ритуксимаб в качестве
монотерапии и (или) поддерживающей терапии или в комбинации с
химиотерапией
Инфекции
и инвазии:
Очень
часто: бактериальные
инфекции, вирусные инфекции, + бронхит.
Часто:
сепсис, + пневмония, + инфекции, сопровождающиеся повышением
температуры тела, + опоясывающий герпес, + инфекция дыхательных
путей, грибковые инфекции, инфекции неизвестной этиологии, +острый
бронхит, + синусит, гепатит В1.
Редко:
серьезные вирусные инфекции2,
пневмоцистная пневмония.
Очень
редко: прогрессирующая многоочаговая
лейкоэнцефалопатия.
Нарушения
со стороны кроветворной и лимфатической системы:
Очень
часто: нейтропения,
лейкопения, + фебрильная нейтропения, + тромбоцитопения.
Часто:
анемия, + панцитопения, + гранулоцитопения.
Нечасто:
нарушения свертываемости крови, апластическая
анемия, гемолитическая анемия, лимфаденопатия.
Очень
редко: транзиторное повышение уровня IgM в
сыворотке крови3.
Неизвестно:
поздняя нейтропения3.
Нарушения
со стороны иммунной системы:
Очень
часто: инфузионные реакции4,
ангионевротический отек.
Часто:
гиперчувствительность.
Редко:
анафилаксия.
Очень
редко: синдром лизиса опухоли, синдром
высвобождение цитокинов4,
сывороточная болезнь.
Неизвестно:
острая обратимая тромбоцитопения, ассоциированная с инфузионными
реакциями4.
Нарушения
обмена веществ и питания:
Часто:
гипергликемия, снижение веса, периферические
отеки, отек лица, повышение ЛДГ, гипокальциемия.
Психические
расстройства:
Нечасто:
депрессия, нервозность.
Расстройства
нервной системы:
Часто:
парестезии, гипестезия, возбуждение,
бессонница, вазодилатация, головокружение, тревожность.
Нечасто:
дисгевзия.
Очень
редко: периферическая невропатия, паралич
лицевого нерва5.
Неизвестно:
невропатия черепных нервов, потеря чувствительности5.
Заболевания
глаз:
Часто:
нарушение слезоотделения, конъюнктивит.
Очень
редко: тяжелая потеря зрения.
Нарушения
со стороны органов слуха и равновесия:
Часто:
звон в ушах, боль в ушах.
Неизвестно:
потеря слуха5.
Нарушения
со стороны сердца:
Часто:
+инфаркт миокарда4,6,
аритмия, +фибрилляция предсердий, тахикардия, +заболевание сердца.
Нечасто:
+левожелудочковая недостаточность, +наджелудочковая тахикардия,
+желудочковая тахикардия, + стенокардия, + ишемия миокарда,
брадикардия.
Редко:
тяжелые сердечные заболевания4,6.
Очень
редко: сердечная недостаточность4,6.
Нарушения
со стороны сосудов:
Часто:
гипертензия, ортостатическая гипотензия, гипотензия.
Очень
редко: васкулит (преимущественно кожный),
лейкоцитокластический васкулит.
Нарушения
со стороны дыхательной системы, органов грудной клетки и средостения:
Часто:
бронхоспазм4,
заболевания органов дыхания, боль в груди, одышка, усиление кашля,
ринит.
Нечасто:
астма, облитерирующий бронхиолит, болезни легких, гипоксия.
Редко:
интерстициальная болезнь легких7.
Очень
редко: дыхательная недостаточность4.
Неизвестно:
инфильтрация легких.
Желудочно-кишечные
расстройства:
Очень
часто: тошнота.
Часто:
рвота, диарея, боль в животе, дисфагия, стоматит,
запор, диспепсия, анорексия, раздражение в горле.
Нечасто:
увеличение живота.
Очень
редко: перфорация желудка и/или кишечника7.
Заболевания
кожи и подкожной клетчатки:
Очень
часто: зуд, сыпь,
+ алопеция.
Часто:
крапивница, потливость, ночная потливость,
+заболевание кожи.
Очень
редко: тяжелые буллезные кожные реакции,
синдром Стивенса-Джонсона токсический эпидермальный некролиз (синдром
Лайелла)7.
Нарушения
со стороны скелетной мускулатуры, соединительной ткани и костей:
Часто:
гипертонус, мышечная
боль, боль в суставах, боль в спине, боль в шее, боль.
Нарушения
со стороны почек и мочевыводящих путей:
Очень
редко: почечная недостаточность 4.
Общие
нарушения и нарушения в месте введения:
Очень
часто: лихорадка, озноб, астения, головная
боль.
Часто:
боль в области опухоли, приливы, недомогание, гриппоподобный синдром,
+утомляемость, + озноб, + полиорганная недостаточность 4.
Нечасто:
боль в месте инфузии.
Лабораторные
и инструментальные данные:
Очень
часто: уменьшение уровня IgG.
Для
каждого термина подсчет частоты проводился на основе любой степени
проявления реакции (от легкой до тяжелой), за исключением терминов,
отмеченных «+», для которых подсчет частоты основан только
на тяжелых проявлениях (≥ 3 баллов по шкале Общих критериев
токсичности Национального института рака (NCI CTC)) реакций.
Учитывались только самые частые случаи проявления реакций в
клинических исследованиях
1
включает в себя реактивацию и первичные инфекции; частота основана на
данных при терапии рецидивирующего/рефрактерного ХЛЛ по схеме R-FC
2
см. также раздел инфекции ниже
3
см. также раздел гематологических нежелательных реакций ниже
4
см. также раздел инфузионных реакций ниже. Были зафиксированы редкие
смертельные случаи
5
признаки и симптомы нейропатии черепных нервов. Происходили в разное
время вплоть до нескольких месяцев после завершения терапии
ритуксимабом
6
наблюдались в основном у пациентов с сердечными заболеваниями и/или
предшествующей кардиотоксической химиотерапией и чаще всего
сопровождались инфузионными реакциями
7
включая смертельные случаи
Нежелательные
явления, обозначенные приведенными ниже терминами, были зафиксированы
во время клинических исследований, однако встречались с той же или
меньшей частотой у групп пациентов, проходящих лечение ритуксимабом,
по сравнению с контрольными группами: гематотоксичность,
нейтропеническая инфекция, инфекции мочевыводящих путей, сенсорное
расстройство, гипертермия.
Признаки
и симптомы, указывающие на инфузионные реакции, были зафиксированы
более чем у 50% пациентов, участвовавших в клинических исследованиях,
и преимущественно проявлялись во время первой инфузии в течение
первого часа или двух. В основном они проявлялись в виде лихорадки,
озноба и дрожи. Также наблюдали гиперемию, ангионевротический отек,
бронхоспазм, рвоту, тошноту, крапивницу / сыпь, утомляемость,
головную боль, раздражение горла, насморк, зуд, боль, тахикардию,
артериальную гипертензию, гипотензию, одышку, диспепсию, астению и
признаки синдрома лизиса опухоли. Тяжелые инфузионные реакции (такие
как бронхоспазм, гипотензия) проявлялись не более чем в 12% случаев.
Кроме того, в ряде случаев были зарегистрированы инфаркт миокарда,
фибрилляция предсердий, отек легких и острая обратимая
тромбоцитопения. Ухудшение течения уже существующих сердечных
заболеваний, таких как стенокардия или застойная сердечная
недостаточность, или тяжелые расстройства со стороны сердца
(сердечная недостаточность, инфаркт миокарда, фибрилляция
предсердий), отек легких, полиорганная недостаточность, синдром
лизиса опухоли, синдром высвобождения цитокинов, почечная
недостаточность, и дыхательная недостаточность выявлялись с более
низкой или неизвестной частотой. Частота возникновения симптомов
инфузионных реакций существенно снижалась с последующими инфузиями.
На восьмом цикле лечения, включающего ритуксимаб, они встречались у
<1% пациентов.
Описание
отдельных нежелательных реакций
Инфекции
Ритуксимаб
вызывает истощение пула В-лимфоцитов у 70-80% пациентов, при этом
снижение концентрации иммуноглобулинов в сыворотке наблюдается только
у небольшого числа пациентов.
В
рандомизированных исследованиях случаи проявления локального
кандидоза и опоясывающего герпеса были зафиксированы намного чаще у
групп, получавших лечение ритуксимабом. Тяжелые инфекции были
зарегистрированы примерно у 4% пациентов, получавших монотерапию
ритуксимабом. При проведении поддерживающей терапии ритуксимабом
продолжительностью до 2 лет наблюдалось увеличение общей частоты
инфекций, в том числе инфекций 3-4 степени тяжести, по сравнению с
группой наблюдения. За 2-летний период лечения не получено каких-либо
данных о кумулятивной токсичности в отношении риска развития
инфекций.
Кроме
того, в ходе лечения ритуксимабом были зафиксированы случаи
проявления других тяжелых вирусных инфекции, в т. ч. новых случаев,
реактивации или обострений ранее существовавших инфекций, в том числе
с летальным исходом. Большинство пациентов получали ритуксимаб в
комбинации с химиотерапией или как часть курса при трансплантации
гемопоэтических стволовых клеток.
Примерами
таких серьезных вирусных инфекций являются инфекции, вызванные
герпесвирусами (цитомегаловирус, вирус ветряной оспы и вирус простого
герпеса), JC вирус (прогрессирующая многоочаговая лейкоэнцефалопатия
(ПМЛ)) и вирус гепатита С.
Случаи
ПМЛ со смертельным исходом, произошедшие после прогрессирования
заболевания и повторного лечения, также были зафиксированы в
клинических исследованиях.
Были
зафиксированы случаи реактивации гепатита В, большинство из которых
были отмечены у больных, получающих ритуксимаб в сочетании с
цитотоксической химиотерапией. У пациентов с рецидивирующим /
химиоустойчивым ХЛЛ частота возникновения гепатита В 3-4 степени
тяжести (реактивация и первичная инфекция) составляла 2% при лечении
по схеме R-FC против 0% у пациентов, получающих терапию по схеме FC.
Прогрессирование
саркомы Капоши наблюдалось у пациентов с ранее существовавшей
саркомой Капоши, получающих терапию ритуксимабом. В большинстве
случаев эти реакции наблюдались у ВИЧ-положительных пациентов и
происходили при лечении препаратом по неутвержденным показаниям к
применению.
Гематологические
нежелательные реакции
Гематологические
нарушения наблюдались у меньшинства пациентов и чаще всего были
легкими и обратимыми. Тяжелая (3-4 степень тяжести) нейтропения
наблюдалась у 4,2% пациентов, анемия у 1,1% пациентов,
тромбоцитопения – у 1,7 % пациентов. В ходе поддерживающей
терапии ритуксимабом продолжительностью до 2 лет лейкопения (5% по
сравнению с 2%, 3-4 степени тяжести, соответственно) и нейтропения
(10% и 4 %, 3-4 степени тяжести, соответственно) наблюдалась с
большей частотой по сравнению с группами наблюдения. Тромбоцитопения
развивалась редко (<1%, 3-4 степени тяжести), частота её не
отличалась между группами. В ходе лечения ритуксимабом в комбинации с
химиотерапией зафиксированы более частые случаи развития лейкопении
3-4 степени тяжести (R-CHOP 88% по сравнению с CHOP 79%, R-FC 23% по
сравнению с FC 12%), нейтропении (R-CVP 24% по сравнению с CVP 14%;
R-CHOP 97% по сравнению с CHOP 88%, R-FC 30% по сравнению с FC 19% у
ранее нелеченых пациентов с ХЛЛ), панцитопении (R-FC 3% по сравнению
с FC 1% у ранее не леченых пациентов с ХЛЛ), по сравнению с их
частотой при применении только химиотерапии. Тем не менее, более
высокая частота развития нейтропении у пациентов, получавших
ритуксимаб в комбинации с химиотерапией, по сравнению с пациентами,
получавшими только химиотерапию, не была связана с более высокой
частотой инфекционных осложнений.
Исследования
у неполучавших ранее лечения пациентов и у пациентов с рецидивирующим
или химиоустойчивым ХЛЛ показали, что у вплоть до 25% пациентов,
получающих терапию по схеме R-FC, нейтропения была затяжной
(количество нейтрофилов ниже 1×109/л
в период между 24 и 42 днем после последнего введения препарата), или
проявлялась поздно (количество нейтрофилов ниже 1×109/л
после 42 дня после последнего введения препарата у пациентов не
имевших затяжной нейтропении и восстановившихся до 42 дня) после
лечения ритуксимабом в комбинации с FC.
Различий
в частоте развития анемии выявлено не было. Зафиксированы случаи
проявления поздней нейтропении, начавшейся позднее чем через 4 недели
после последней инфузии ритуксимаба.
В
исследовании терапии первой линии при ХЛЛ у пациентов со стадией С по
классификации Binet
наблюдалось больше нежелательных явлений у пациентов, получавших
R-FC, по сравнению с группой FC (R-FC 83% и FC 71%).
В
исследовании при рецидивирующем/рефрактерном ХЛЛ тромбоцитопения 3-4
степени тяжести была зафиксирована у 11% пациентов из группы R-FC по
сравнению с 9% пациентов из группы FC.
В
исследованиях применения ритуксимаба при лечении пациентов с
макроглобулинемией Вальденстрёма кратковременное повышение
сывороточных уровней IgM было зафиксировано после начала лечения, что
может сопровождаться развитием синдрома повышенной вязкости и
сопутствующими ему проявлениями. Временно повышенный уровень IgM
обычно возвращался к изначальным значениям в течение 4 месяцев.
Нежелательные
реакции со стороны сердечно-сосудистой системы
Реакции
со стороны сердечно-сосудистой системы при монотерапии ритуксимабом в
клинических исследованиях отмечены у 18,8%
пациентов. Наиболее часто встречались понижение и повышение
артериального давления. Во время инфузии наблюдалось нарушение
сердечного ритма 3 и 4 степени тяжести (включая желудочковую и
наджелудочковую тахикардию) и стенокардия.
Частота
сердечно-сосудистых нарушений 3 и 4 степени тяжести при
поддерживающей терапии была сходной у больных, получавших ритуксимаб
и не получавших его. Серьезные нежелательные явления со стороны
сердечно-сосудистой системы (в том числе, фибрилляция предсердий,
инфаркт миокарда, левожелудочковая недостаточность, ишемия миокарда)
возникали у менее 1% больных, не получавших ритуксимаб, и у 3%
больных, получавших ритуксимаб.
В
исследованиях, оценивающих эффективность ритуксимаба в комбинации с
химиотерапией частота нарушений сердечного ритма 3 и 4 степени
тяжести, главным образом наджелудочковых аритмий (тахикардия,
трепетание и мерцание предсердий), в группе R-СНОР была выше (14
пациентов, 6,9%), чем в группе СНОР (3 пациента,
1,5%). Все аритмии развивались либо в связи с
инфузией ритуксимаба, либо были связаны с такими предрасполагающими
состояниями, как лихорадка, инфекция, острый инфаркт миокарда или на
фоне сопутствующих заболеваний дыхательной и сердечно-сосудистой
систем. Группы R-СНОР и СНОР не различались между собой по частоте
других нежелательных явлений со стороны сердца 3 и 4 степени тяжести,
включая сердечную недостаточность, заболевания миокарда и
манифестацию ишемической болезни сердца.
В
исследованиях при ХЛЛ общая частота сердечно-сосудистых нарушений 3 и
4 степени тяжести была низкой, как при терапии первой линии (4% в
группе R-FC, 3% FC), так и
при терапии рецидивирующего/рефрактерного хронического лимфолейкоза
(4% R-FC, 4% FC).
Дыхательная
система
Были
зафиксированы случаи развития
интерстициального заболевания легких, в том
числе некоторые – с летальным исходом.
Неврологические
расстройства
У
4 больных (2%) из группы R-CHOP (индукционная фаза лечения,
включающая режим R-CHOP, не более 8 циклов) с сердечно-сосудистыми
факторами риска развилось нарушение мозгового кровообращения,
вызванное тромбоэмболией, в ходе первого цикла терапии. Разница между
группами в частоте других тромбоэмболий отсутствовала. В группе CHOP
цереброваскулярные явления были отмечены у 3 пациентов (1,5%), все
они проявились в период последующего наблюдения.
Общая
частота неврологических нарушений 3 и 4 степени тяжести в клинических
исследованиях оказалась низкой как в исследованиях первой линии
терапии хронического лимфолейкоза (4% в группе R-FC, 4% FC), так и
при терапии рецидивирующего/рефрактерного хронического лимфолейкоза
(3% в группе R-FC, 3% FC).
Зафиксированы
случаи развития синдрома обратимой задней энцефалопатии / обратимого
заднего лейкоэнцефалопатического синдрома. Эти состояния проявлялись
нарушением зрения, головной болью, судорогами и изменением
психического состояния, сопровождавшимися или не сопровождавшимися
гипертензией. Для подтверждения данных диагнозов необходимо выполнить
визуализацию головного мозга. В выявленных случаях имелись известные
факторы риска развития синдрома обратимой задней энцефалопатии /
обратимого заднего лейкоэнцефалопатического синдрома, в том числе,
основное заболевание пациента, гипертензия, иммуносупрессивная
терапия и / или химиотерапия.
Желудочно-кишечные
расстройства
Перфорации
стенки желудочно-кишечного тракта, в некоторых случаях приводящие к
смерти, были зафиксированы у пациентов, получавших ритуксимаб для
лечения неходжкинской лимфомы. В большинстве из этих случаев
ритуксимаб применялся в комплексе с химиотерапией.
Концентрация
IgG
В
клинических исследованиях поддерживающей терапии у пациентов с
рецидивирующей / рефрактерной фолликулярной лимфомой, после
индукционного курса медиана концентрация IgG была ниже нижней границы
нормы (<7 г/л) и в группе, получавшей ритуксимаб, и в группе, не
получавшей препарат. В группе, не получавшей ритуксимаб, медиана
уровня IgG постепенно увеличилась и превысила нижнюю границу нормы, в
то время как в группе, получавшей ритуксимаб, медиана уровня IgG не
изменилась. У 60% пациентов, получавших ритуксимаб в течение 2 лет,
уровень IgG оставался ниже нижней границы нормы, в то время как в
группе, не получавшей терапии ритуксимабом, через 2 года доля таких
пациентов снизилась до 36%.
Зафиксировано
небольшое число спонтанных сообщений и публикаций о случаях развития
гипогаммаглобулинемии у детей, получавших ритуксимаб. Некоторые из
этих эпизодов были тяжелыми и требовали долговременной поддерживающей
терапии иммуноглобулином.
О
последствиях долгосрочного истощения пула В-клеток у пациентов
детского возраста неизвестно.
Нарушения
со стороны кожи и подкожной клетчатки
Токсический
эпидермальный некролиз (синдром Лайелла) и синдром Стивенса-Джонсона,
в некоторых случаях приводившие к смерти, регистрировались очень
редко.
Особые
категории больных — монотерапия
ритуксимабом
Старшая
возрастная группа (≥ 65 лет):
Частота
и степень тяжести всех нежелательных лекарственных реакций и
нежелательных реакций 3 и 4 степени тяжести не отличается от таковой
у более молодых пациентов (< 65 лет).
Массивное
опухолевое поражение
Зафиксирована
более высокая частота развития НЛР 3-4 степени тяжести у пациентов с
массивным опухолевым поражением, чем без него (25,6 % и 15,4 %
соответственно). Частота проявления НЛР любой степени у этих групп
одинакова.
Повторная
терапия
Доля
пациентов с НЛР при повторной терапии не отличается от таковой при
проведении первоначальной терапии (любая степень и степени 3-4 НЛР).
Особые
категории больных – комбинированное
лечение ритуксимабом
Пожилые
пациенты (≥ 65 лет)
При
применении ритуксимаба в первой линии терапии, а также при терапии
рецидивирующего/рефрактерного хронического лимфолейкоза частота
нежелательных явлений 3 и 4 степени тяжести со стороны системы крови
и лимфатической системы была выше по сравнению с более молодыми
пациентами (< 65 лет).
Опыт
применения препарата при ревматоидном артрите
Краткий
обзор профиля безопасности препарата
Общий
профиль безопасности ритуксимаба при лечении ревматоидного артрита
определен на основании данных клинических исследований и
пострегистрационного наблюдения.
Профиль
безопасности применения ритуксимаба при лечении пациентов со
среднетяжелым и тяжелым ревматоидным артритом представлен в следующих
разделах. Информация о безопасности, собранная в ходе
пострегистрационных наблюдений отражает ожидаемый профиль
нежелательных реакций, установленный из материалов клинических
исследований ритуксимаба.
Список
нежелательных реакций
Для
оценки частоты реакций используются следующие критерии: очень часто
(≥ 1/10), часто (≥ 1/100 до < 1/10), нечасто
(≥ 1/1 000 до < 1/100), редко (≥ 1/10 000
до< 1/1 000), очень редко (< 1/10 000) и
неизвестно (не могут быть оценены на основе имеющихся данных). В
каждой частотной группе нежелательные эффекты представлены в порядке
уменьшения серьезности.
Среди
нежелательных реакций, связанных с применением ритуксимаба, чаще
всего были зафиксированы инфузионные реакции. С первой инфузией
инфузионные реакции проявились у 23% пациентов, частота реакций
уменьшалась с последующими инфузиями. Серьезные инфузионные реакции
наблюдались редко (0,5% пациентов) и преимущественно во время
начального курса.
В
периоде пострегистрационного наблюдения помимо реакций, обнаруженных
в клинических исследованиях применения при ревматоидном артрите, были
зафиксированы случаи проявления ПМЛ и реакции по типу сывороточной
болезни.
Обзор
нежелательных лекарственных реакций, зафиксированных в ходе
клинических и постмаркетинговых исследований лечения ритуксимабом
пациентов с ревматоидным артритом.
Инфекции
и инвазии:
Очень
часто: инфекции верхних дыхательных путей,
инфекции мочевыводящих путей.
Часто:
бронхит, синусит, гастроэнтерит, микоз стоп.
Очень
редко: ПМЛ, реактивация
гепатита B.
Нарушения
со стороны системы крови и лимфы:
Часто:
нейтропения1.
Редко:
поздняя нейтропения
2.
Очень
редко: реакции по типу сывороточной болезни.
Нарушения
со стороны сердца:
Редко:
стенокардия, фибрилляции предсердий, сердечная
недостаточность, инфаркт миокарда.
Очень
редко: трепетание предсердий.
Нарушения
со стороны иммунной системы/ Общие
нарушения и нарушения в месте введения:
Очень
часто:3Инфузионные
реакции (гипертензия, тошнота, сыпь, лихорадка, зуд, крапивница,
раздражение горла, приливы, гипотензия, ринит, дрожь, тахикардия,
утомляемость, боль в ротоглотке, периферические отеки, эритема).
Нечасто:
3Инфузионные
реакции (анасарка, бронхоспазм, свистящее дыхание, отек гортани,
ангионевротический отек, генерализованный зуд, анафилаксия,
анафилактоидные реакции).
Нарушения
обмена веществ и питания:
Часто:
гиперхолестеринемия.
Расстройства
нервной системы:
Очень
часто: головная боль.
Часто:
парестезии, мигрень, головокружение, воспаление седалищного нерва.
Заболевания
кожи и подкожной клетчатки:
Часто:
алопеция.
Очень
редко: токсический эпидермальный некролиз
(синдром Лайелла), синдром Стивенса-Джонсона5.
Психические
расстройства:
Часто:
депрессия, тревожность.
Желудочно-кишечные
расстройства:
Часто:
Диспепсия, диарея, гастроэзофагеальный рефлюкс,
язвенный стоматит, боль в верхней части живота.
Нарушения
со стороны опорно-двигательного аппарата:
Часто:
артралгия / костно-мышечные боли, остеоартроз,
бурсит.
Лабораторные
и инструментальные данные:
Очень
часто: уменьшение уровня IgM4.
Часто:
уменьшение уровня IgG4.
1
Частота получена в рамках рутинного
лабораторного мониторинга в ходе клинических исследований
2
Частота получена на основе пострегистрационных данных
3
Реакции, происходящие во время или в
течение 24 часов после инфузии. См. также инфузионные реакции ниже.
Инфузионные реакции могут возникнуть в результате
гиперчувствительности и / или механизма действия препарата.
4
Включая результаты наблюдений, собранные в рамках рутинного
лабораторного мониторинга.
5
Включая случаи с летальным исходом.
Многократная
терапия
Профиль
НЛР, возникших в ходе множественных курсов терапии ритуксимабом,
сходен с профилем НЛР, возникших после первого применения. Частота
всех нежелательных реакций после первого применения ритуксимаба была
наибольшей в течение первых 6 месяцев и затем снижалась. Эта
динамика, в основном, определяется большим числом инфузионных реакций
(наиболее часто возникавших в течение первого курса лечения),
обострением РА и инфекций; все названные реакции были наиболее
частыми в первые 6 месяцев лечения.
Инфузионные
реакции
Инфузионные
реакции оказались наиболее часто встречающейся нежелательной реакцией
при введении ритуксимаба.
В
пострегистрационном периоде были зафиксированы случаи проявления
тяжелых инфузионных реакций со смертельным исходом.
В
исследовании, направленном на оценку безопасности ускоренных инфузий
ритуксимаба для лечения больных с РА, пациентам со среднетяжелым и
тяжелым РА, без признаков серьезных инфузионных реакций в течение 24
часов после первой инфузии, ритуксимаб вводился в виде двухчасовой
инфузии внутривенно. Из исследования были исключены пациенты с ранее
выявлявшимися серьезными инфузионными реакциями на введение
биопрепаратов для терапии РА. Частота, характер и тяжесть инфузионных
реакций оказались сопоставимыми с наблюдаемыми ранее значениями.
Серьезных инфузионных реакций зафиксировано не было.
Описание
некоторых нежелательных реакций
Инфекции
Общая
частота инфекций среди пациентов, получавших ритуксимаб, составила
примерно 94 на 100 пациенто-лет. Инфекции были представлены в
основном инфекциями верхних дыхательных путей и инфекциями
мочевыводящих путей легкой и средней степени тяжести. Частота тяжелых
инфекций и инфекций, требующих внутривенного введения антибиотиков,
составила 4 на 100 пациенто-лет. Заметного роста частоты серьезных
инфекций в ходе многократных курсов лечения ритуксимабом не
наблюдалось. Инфекции нижних дыхательных путей (включая пневмонию)
были зарегистрированы во время клинических испытаний со схожей
частотой возникновения в группах, получавших ритуксимаб, по сравнению
с контрольными группами.
Были
зарегистрированы случаи развития прогрессирующей многоочаговой
лейкоэнцефалопатии с летальным исходом у пациентов, проходивших
лечение ритуксимабом по поводу ревматоидного артрита и аутоиммунных
заболеваний, не предусмотренных показаниями к применению, в том
числе, по поводу системной красной волчанки (СКВ) и васкулита.
У
пациентов с неходжкинской лимфомой, получавших ритуксимаб в сочетании
с цитотоксической химиотерапией, были зарегистрированы случаи
реактивации гепатита B. У пациентов с РА, получавших ритуксимаб,
случаи реактивации гепатита В фиксировались крайне редко.
Нежелательные
реакции со стороны сердечно-сосудистой системы
Частота
серьезных нежелательных реакций со стороны сердечно-сосудистой
системы составила 1,3 на 100 пациенто-лет у пациентов, получавших
ритуксимаб и 1,3 на 100 пациенто-лет у пациентов, получавших плацебо.
В ходе многократных курсов терапии ритуксимабом не было зафиксировано
увеличения частоты как всех, так и только серьезных нежелательных
реакций со стороны сердца.
Неврологические
нарушения
Зафиксированы
случаи развития синдрома обратимой задней энцефалопатии/ обратимого
заднего лейкоэнцефалопатического синдрома. Эти состояния проявлялись
нарушением зрения, головной болью, судорогами и изменением
психического состояния, с или без сопутствующей гипертензии. Для
подтверждения данных диагнозов необходимо провести визуализацию
головного мозга. В выявленных случаях имелись известные факторы риска
развития синдрома обратимой задней энцефалопатии / обратимого заднего
лейкоэнцефалопатического синдрома, в том числе, основное заболевание
пациента, гипертензия, иммуносупрессивная терапия и / или
химиотерапия.
Нейтропения
Зафиксированы
случаи развития нейтропении при лечении ритуксимабом, большинство из
которых были временными, имели легкую или умеренную степени тяжести.
Нейтропения может проявиться в течение нескольких месяцев после
введения ритуксимаба. У 0,94% (13/1382) пациентов, получавших
ритуксимаб, и у 0,27% (2/731) пациентов, получавших плацебо,
развилась тяжелая нейтропения.
Случаи
нейтропении, в том числе тяжелой поздней и устойчивой нейтропении, в
ходе пострегистрационного наблюдения встречались редко, иногда они
сопровождались развитием инфекций со смертельным исходом.
Нарушения
со стороны кожи и подкожной клетчатки
Токсический
эпидермальный некролиз (синдром Лайелла) и синдром Стивенса-Джонсона,
некоторые со смертельным исходом, регистрировались очень редко.
Отклонения
лабораторных показателей
У
пациентов с РА, получавших ритуксимаб, возникала
гипогаммаглобулинемия (уровень IgG или IgM ниже нижней границы
нормы). Снижение уровня IgG или IgM не сопровождалось увеличением
частоты случаев инфекционных заболеваний у пациентов.
Зафиксировано
небольшое число спонтанных сообщений и публикаций о случаях развития
гипогаммаглобулинемии у детей, получавших ритуксимаб. Некоторые из
этих эпизодов были тяжелыми и требовали долговременной поддерживающей
терапии иммуноглобулином.
О
последствиях долгосрочного истощения пула В-клеток у пациентов
детского возраста информации нет.
Опыт
при лечении гранулематоза с полиангиитом и микроскопического
полиангиита
Сводная
таблица нежелательных явлений
Нежелательные
лекарственные реакции, приведенные в таблице 1, проявлялись у ≥ 5%
пациентов, получавших ритуксимаб.
Таблица
1. Нежелательные лекарственные реакции, наблюдавшиеся в течение 6
месяцев у ≥ 5% пациентов, получавших ритуксимаб, и с большей
частотой, чем у пациентов группы сравнения в регистрационном
клиническом исследовании
|
Система Нежелательное |
Ритуксимаб |
|
Нарушения |
|
|
тромбоцитопения |
7% |
|
Нарушения |
|
|
диарея |
18% |
|
диспепсия |
6% |
|
запор |
5% |
|
Общие |
|
|
периферические |
16% |
|
Нарушения |
|
|
синдром |
5% |
|
Инфекции |
|
|
инфекции |
7% |
|
бронхит |
5% |
|
опоясывающий |
5% |
|
назофарингит |
5% |
|
Лабораторные |
|
|
снижение |
6% |
|
Нарушения |
|
|
гиперкалиемия |
5% |
|
Нарушения |
|
|
мышечные |
18% |
|
артралгия |
15% |
|
боль |
10% |
|
мышечная |
5% |
|
скелетно-мышечные |
5% |
|
боль |
5% |
|
Нарушения |
|
|
головокружение |
10% |
|
тремор |
10% |
|
Психические |
|
|
бессонница |
14% |
|
Нарушения |
|
|
кашель |
12% |
|
одышка |
11% |
|
носовое |
11% |
|
заложенность |
6% |
|
Заболевания |
|
|
акне |
7% |
|
Нарушения |
|
|
гипертензия |
12% |
|
приливы |
5% |
Описание
некоторых нежелательных реакций
Инфузионные
реакции
Инфузионная
реакция при гранулематозе с полиангиитом и микроскопическом
полиангиите определялась как любое нежелательное явление, возникшее в
популяции оценки безопасности в течение 24 часов после инфузии и
сочтенное исследователями как связанным с инфузией. Среди пациентов,
получавших ритуксимаб, как минимум у 12% проявились инфузионные
реакции. Все
инфузионные реакции имели 1-2 степень по классификации СТС. Наиболее
распространенными проявлениями инфузионных реакций были синдром
высвобождения цитокинов, гиперемия, раздражение горла и тремор.
Ритуксимаб применялся в комбинации с внутривенным введением
глюкокортикоидов, что могло уменьшить частоту и тяжесть этих явлений.
Инфекции
У
пациентов, получавших ритуксимаб, общая частота инфекций составляла
примерно 237 на 100 пациенто-лет (95% ДИ 197-285) в 6-месячной
первичной конечной точке. Инфекции были представлены в основном
инфекциями верхних дыхательных путей, опоясывающим герпесом и
инфекциями мочевыводящих путей от легкой до умеренной степени
тяжести. Частота серьезных инфекций составляла примерно 25 на 100
пациенто-лет. Самой часто сообщаемой серьезной инфекцией в группе
ритуксимаба была пневмония с частотой 4%.
Злокачественные
новообразования
Частота
развития злокачественных новообразований у пациентов с гранулематозом
с полиангиитом и микроскопическим полиангиитом, получавших ритуксимаб
, составила 2,00 на 100 пациенто-лет на дату общего закрытия
исследования (завершение периода наблюдения последним пациентом). На
основании стандартизированных коэффициентов заболеваемости,
заболеваемость злокачественными новообразованиями оказалась сходной с
ранее зафиксированной частотой заболеваемости у пациентов с
ANCA-ассоциированным васкулитом.
Сердечно-сосудистые
нежелательные реакции
Сердечно-сосудистые
события наблюдались с частотой примерно 273 на 100 пациенто-лет (95%
ДИ 149-470) в 6-месячной первичной конечной точке. Частота серьезных
кардиологических явлений составляла 2,1 на 100 пациенто-лет (95% ДИ
3-15). Наиболее частыми явлениями оказались тахикардия (4%) и
фибрилляция предсердий (3%).
Неврологические
нарушения
При
аутоиммунных процессах были зафиксированы случаи развития синдрома
обратимой задней энцефалопатии/ обратимого заднего
лейкоэнцефалопатического синдрома. Эти состояния проявлялись
нарушением зрения, головной болью, судорогами и изменением
психического состояния, с или без сопутствующей гипертензии. Для
подтверждения данных диагнозов необходимо провести визуализацию
головного мозга. В выявленных случаях имелись известные факторы риска
развития синдрома обратимой задней энцефалопатии / обратимого заднего
лейкоэнцефалопатического синдрома, в том числе, основное заболевание
пациента, гипертензия, иммуносупрессивная терапия и / или
химиотерапия.
Реактивация
гепатита В
В
ходе пострегистрационного наблюдения было зафиксировано небольшое
число случаев реактивации гепатита В у пациентов с гранулематозом с
полиангиитом и микроскопическим полиангиитом, получавших ритуксимаб.
Некоторые из этих случаев окончились летальным исходом.
Гипогаммаглобулинемия
Гипогаммаглобулинемия
(уровень IgA, IgG или IgM ниже нижней границы нормы) была
зафиксирована у пациентов с гранулематозом с полиангиитом и
микроскопическим полиангиитом, получавших ритуксимаб. В группе
ритуксимаба 27%, 58% и 51% пациентов с нормальными уровнями
иммуноглобулинов на исходный момент, имели низкие уровни IgA, IgG и
IgM, соответственно. В группе циклофосфамида таких пациентов
оказалось 25%, 50% и 46%, соответственно.
У
пациентов с низким уровнем IgA, IgG или IgM не наблюдалось увеличения
частоты случаев инфекционных заболеваний или числа серьезных
инфекций.
Нейтропения
У
24% пациентов в группе ритуксимаба (один курс) и у 23% пациентов в
группе циклофосфамида зафиксированы случаи развития нейтропении
степени 3 или выше по классификации СТС. Развитие нейтропении не было
связано с увеличением заболеваемости серьезными инфекциями у
пациентов, получавших ритуксимаб. Влияние многократных курсов
ритуксимаба на развитие нейтропении у пациентов с гранулематозом с
полиангиитом и микроскопическим полиангиитом в ходе клинических
исследований не изучалось.
Заболевания
кожи и подкожной клетчатки
Токсический
эпидермальный некролиз (синдром Лайелла) и синдром Стивенса-Джонсона,
регистрировались очень редко. В отдельных случаях был отмечен
летальный исход.
Представление
данных о потенциальных нежелательных реакциях
Сообщение
о потенциальных нежелательных реакциях после регистрации
лекарственного средства является важным действием. Оно позволяет
продолжать мониторинг соотношения риска и пользы лекарственного
средства.
Контактные
данные для направления информации о потенциальных нежелательных
реакциях:
ТОО
«Карагандинский фармацевтический комплекс»
Республика
Казахстан
100009,
г. Караганда, ул. Газалиева, стр. 16
Тел
(7212)90-80-43, e-mail medinfo@kphk.kz
, сайт:
www.kphk.kz
Противопоказания
Противопоказания
к применению пациентами с неходжкинской лимфомой и хроническим
лимфолейкозом
—
гиперчувствительность к действующему веществу, к белкам мыши или к
любому из вспомогательных веществ
—
острые, тяжелые инфекционные заболевания
—
пациенты с выраженным иммунодефицитом.
Противопоказания
к применению пациентами с ревматоидным артритом, гранулематозом с
полиангиитом и микроскопическим полиангиитом
—
гиперчувствительность к действующему веществу, к белкам мыши или к
любому из вспомогательных веществ
—
острые, тяжелые инфекционные заболевания.
Пациенты
с выраженным иммунодефицитом
—
тяжелая сердечная недостаточность (класс IV по классификации
Нью-Йоркской кардиологической ассоциации) или тяжелые,
неконтролируемые заболевания сердца.
Лекарственные взаимодействия
Данные
о лекарственных взаимодействиях ритуксимаба ограничены.
У
пациентов с хроническим лимфолейкозом совместное применение с
ритуксимабом не влияло на фармакокинетические показатели флударабина
и циклофосфамида. Кроме того, не наблюдалось влияния флударабина и
циклофосфамида на фармакокинетические показатели ритуксимаба.
Совместное
применение с метотрексатом не влияло на фармакокинетические
показатели ритуксимаба при применении у пациентов с ревматоидным
артритом.
У
пациентов с выявленными титрами антител к белкам мыши или
антихимерных антител могут наблюдаться аллергические реакции или
реакции гиперчувствительности при назначении других препаратов
моноклональных антител с диагностическими или лечебными целями.
Среди
пациентов с ревматоидным артритом частота клинически значимых
инфекций в ходе лечения ритуксимабом составила 6,01 на 100
пациенто-лет, а в ходе последующего лечения – 4,97 на 100
пациенто-лет.
Особые указания
Для
улучшения отслеживаемости применения биологических лекарственных
средств, торговое наименование введенного продукта следует четко
указать в карте пациента.
Прогрессирующая
многоочаговая лейкоэнцефалопатия (ПМЛ)
Зафиксированы
очень редкие случаи развития ПМЛ с летальным исходом после лечения
ритуксимабом. Пациентов следует регулярно обследовать для выявления
случаев возникновения/обострения неврологических симптомов или
признаков, указывающих на развитие ПМЛ. В случае подозрения на
развитие ПМЛ лечение должно быть приостановлено до исключения этого
диагноза. Врач должен провести обследование пациента и установить,
связаны ли симптомы с дисфункцией нервной системы и если да, то
оценить, могут ли наблюдаемые симптомы быть вызваны ПМЛ. При наличии
клинической необходимости следует проконсультироваться с неврологом.
При
возникновении сомнений следует провести МРТ-исследование,
предпочтительно с контрастным усилением, выполнить анализ
спинномозговой жидкости для выявления ДНК JC-вируса и повторить
неврологическое обследование.
Врач
должен быть особенно внимателен к симптомам, указывающим на ПМЛ,
которые пациент может не заметить (например, когнитивные,
неврологические или психиатрические проявления). Пациентам
рекомендуется информировать своего партнера или лицо, осуществляющее
уход, о получаемом лечении, поскольку они могут заметить
возникновение симптомов, которые пациент не в состоянии выявить
самостоятельно.
В
случае развития у пациента ПМЛ, лечение препаратом Ритуксимаб
необходимо прекратить и не возобновлять в дальнейшем.
У
пациентов с иммунодефицитом и ПМЛ при восстановлении функции иммунной
системы наблюдались случаи стабилизации или улучшения состояния.
Остается неизвестным, может ли раннее выявление ПМЛ и приостановление
лечения препаратом Ритуксимаб привести к аналогичной стабилизации или
улучшению результата.
Неходжкинская
лимфома и хронический лимфолейкоз
Инфузионные
реакции
При
введении ритуксимаба наблюдались инфузионные реакции. Развитие
инфузионных реакций при введении препарата Ритуксимаб может быть
обусловлено высвобождением цитокинов и/или других медиаторов. Синдром
высвобождения цитокинов может оказаться клинически неотличим от
острых реакций гиперчувствительности.
Эта
группа реакций, включающая синдром высвобождения цитокинов, синдром
лизиса опухоли, анафилактические реакции и реакции
гиперчувствительности, описана ниже.
Имеются
сообщения о тяжелых инфузионных реакциях с летальным исходом,
описанных в период пострегистрационного применения препарата
ритуксимаба для внутривенного введения. Реакции развивались в
пределах 30 мин – 2 ч после начала первой внутривенной инфузии
ритуксимаба. Для них были характерны проявления со стороны легких, в
некоторых случаях наблюдался быстрый лизис опухоли и проявления
синдрома лизиса опухоли, а также понижение артериального давления,
лихорадка, озноб, дрожь, крапивница, ангионевротический отек и другие
симптомы.
Тяжелая
степень выраженности синдрома высвобождения цитокинов характеризуется
тяжелой одышкой, часто сопровождающейся бронхоспазмом и гипоксией, а
также лихорадкой, ознобом, дрожью, крапивницей, ангионевротическим
отеком. Этот синдром может сопровождаться некоторыми проявлениями
синдрома лизиса опухоли, такими как гиперурикемия, гиперкалиемия,
гипокальциемия, гиперфосфатемия, острая почечная недостаточность,
повышенная активность лактатдегидрогеназы (ЛДГ), кроме того, его
проявления могут приводить к острой дыхательной недостаточности и
смерти. Острая дыхательная недостаточность может сопровождаться
интерстициальной инфильтрацией или отеком легких, видимым на
рентгенограмме грудной клетки. Синдром часто проявляется в течение
одного или двух часов после начала первой инфузии. Пациенты с
легочной недостаточностью в анамнезе или с опухолевой инфильтрацией
легких находятся в группе риска и должны продолжать лечение с
повышенной осторожностью.
При
развитии тяжелого синдрома высвобождения цитокинов, инфузия препарата
должна быть немедленно прекращена, пациентам должно быть оказано
активное симптоматическое лечение. Первоначальное улучшение
симптоматики может сменяться резким ухудшением, поэтому пациенты
должны находиться под внимательным наблюдением до полного разрешения
синдрома лизиса опухоли и легочной инфильтрации или до снятия этих
диагнозов. Последующее лечение пациентов после полного исчезновения
признаков и симптомов в редких случаях приводило к повторному
возникновению тяжелого синдрома высвобождения цитокинов.
Больным
с высокой опухолевой нагрузкой или с большим числом циркулирующих
злокачественных клеток (≥25
× 109/л)
(например, при хроническом
лимфолейкозе), у которых риск крайне тяжелого синдрома высвобождения
цитокинов может быть особенно высок, препарат Ритуксимаб следует
назначать с крайней осторожностью, под тщательным наблюдением. Первую
инфузию препарата таким больным следует вводить с меньшей скоростью
или разделить дозу препарата на два дня во время первого цикла
терапии и в каждый из последующих циклов, если перед введением
препарата Ритуксимаб число циркулирующих злокачественных клеток
сохраняется на уровне >25 × 109/л.
Побочные
инфузионные реакции всех видов наблюдалось у 77% пациентов,
получавших ритуксимаб (включая синдром высвобождения цитокинов,
сопровождающийся гипотензией и бронхоспазмом у 10% пациентов). Эти
симптомы, как правило, разрешались при прекращении инфузий
ритуксимаба и терапии жаропонижающими и антигистаминными препаратами,
а также, в отдельных случаях, кислородом, физиологическим раствором
внутривенно, бронходилататорами и глюкокортикоидами.
После
внутривенного введения белковых препаратов пациентам регистрировались
анафилактические и другие реакции гиперчувствительности. В отличие от
синдрома высвобождения цитокинов, истинные реакции
гиперчувствительности, как правило, возникают в течение нескольких
минут после начала инфузии. В связи с потенциальной возможностью
развития анафилактических реакций и других реакций
гиперчувствительности, при внутривенном введении препарата Ритуксимаб
необходимо иметь средства для их купирования: эпинефрин (адреналин),
антигистаминные и глюкокортикостероидные препараты. Клинические
проявления анафилаксии могут быть подобны клиническим проявлениям
синдрома высвобождения цитокинов (описано выше).
Сообщения
о проявлении реакций, связанных с гиперчувствительностью, встречаются
реже, чем сообщения о проявлении реакций, связанных с высвобождением
цитокинов.
Зафиксированы
случаи развития инфаркта миокарда, фибрилляции предсердий, отека
легких и острой обратимой тромбоцитопении.
Из-за
возможности развития гипотензии при введении препарата Ритуксимаб, не
менее чем за 12 ч до инфузии препарата Ритуксимаб следует избегать
приема антигипертензивных лекарственных средств.
Нарушения
со стороны сердца
Наблюдались
случаи возникновения стенокардии, аритмии, включая мерцание и
трепетание предсердий, сердечной недостаточности и инфаркта миокарда
у пациентов, получавших ритуксимаб. Пациенты с заболеваниями сердца в
анамнезе и/или получающие кардиотоксичную химиотерапию, должны
находиться под тщательным наблюдением.
Гематологическая
токсичность
Хотя
монотерапия препаратом Ритуксимаб не оказывает миелосупрессивного
действия, необходимо с осторожностью подходить к назначению препарата
при нейтропении менее 1,5 × 109/л
и/или тромбоцитопении менее 75 × 109/л,
поскольку опыт его клинического применения у таких пациентов
ограничен. Ритуксимаб применялся для лечения 21 пациента после
аутологичной трансплантации костного мозга и у пациентов других групп
риска с возможным нарушением функции костного мозга, без
возникновения явлений миелотоксичности. В ходе лечения препаратом
Ритуксимаб необходимо регулярно проводить развернутый анализ
периферической крови, включая подсчет количеств нейтрофилов и
тромбоцитов.
Инфекции
Серьезные
инфекционные заболевания, в том числе со смертельным исходом, могут
развиться у пациентов во время терапии препаратом Ритуксимаб.
Препарат Ритуксимаб не следует назначать пациентам с тяжелой активной
инфекцией (например, туберкулез, сепсис и оппортунистические
инфекции).
Врачи
должны проявлять осторожность при использовании препарата Ритуксимаб
для лечения пациентов с рецидивирующими или хроническими
инфекционными заболеваниями, а также с иными сопутствующими
заболеваниями, предрасполагающими к развитию серьезных инфекций.
У
пациентов, получавших ритуксимаб, были зафиксированы случаи
реактивации гепатита В, в том числе фульминантный гепатит с летальным
исходом. Большинство из этих пациентов также получали цитотоксическую
химиотерапию. Имеющаяся ограниченная информация, полученная из одного
исследования в популяции пациентов с рецидивирующим/рефрактерным
хроническим лимфолейкозом, позволяет предположить, что лечение
ритуксимабом может также ухудшить исход инфекции первичного гепатита
B.
Перед назначением препарата Ритуксимаб все пациенты должны пройти
скрининг на гепатит В. Минимальный набор тестов должен включать
определение HbsAg и HbcAb; в соответствии с местными рекомендациями
перечень тестов может быть дополнен. Препарат Ритуксимаб не следует
применять для лечения пациентов с активным гепатитом В. Пациентам с
любыми положительными серологическими маркерами гепатита B
следует проконсультироваться с врачом-гепатологом перед применением
ритуксимаба; в отношении таких пациентов необходимо проводить
соответствующий мониторинг и принимать меры по профилактике
реактивации вируса гепатита B
в соответствии с местными стандартами.
При
применении ритуксимаба у пациентов с неходжкинской лимфомой и
хроническим лимфолейкозом в очень редких случаях наблюдались случаи
ПМЛ. Большинство пациентов получали ритуксимаб в сочетании с
химиотерапией или в сочетании с трансплантацией гемопоэтических
стволовых клеток.
Иммунизация
Безопасность
иммунизации живыми вирусными вакцинами после лечения препаратом
Ритуксимаб пациентов с неходжкинской лимфомой и хроническим
лимфолейкозом не изучалась, вакцинация живыми вирусными вакцинами не
рекомендуется. Возможна вакцинация таких пациентов инактивированными
вакцинами, однако поствакцинальный ответ может быть ослаблен. В
нерандомизированном исследовании у пациентов с рецидивирующей
неходжкинской лимфомой низкой степени злокачественности наблюдалось
снижение частоты ответа на введение столбнячного анатоксина и
KHL-неоантигена
(КНL — гемоцианин моллюска фиссурелии) по сравнению с пациентами, не
получавшими ритуксимаб (16% против 81% и 4% против 76% (критерий
оценки – более чем 2–кратное повышение титра антител),
соответственно). Предполагается, что те же данные могут быть получены
для пациентов с хроническим лимфолейкозом, учитывая схожесть
заболеваний, но клинических исследований в этом направлении не
проводилось.
Средняя
величина титра антител к набору антигенов (Streptococcus pneumoniae,
Influenza A, паротит, краснуха, ветряная оспа) по сравнению с уровнем
до лечения не изменялась как минимум в течение 6 месяцев после
терапии ритуксимабом.
Кожные
реакции
При
лечении ритуксимабом зарегистрированы случаи развития таких тяжелых
кожных реакций как токсический эпидермальный некролиз (синдром
Лайелла) и синдром Стивенса-Джонсона, в ряде случаев с летальным
исходом. При выявлении данных реакций и подозрении на их связь с
Ритуксимабом применение препарата следует прекратить и в дальнейшем
не возобновлять.
Ревматоидный
артрит, гранулематоз с полиангиитом и микроскопический полиангиит
Пациенты
с ревматоидным артритом, не получавшие терапию метотрексатом
Использование
ритуксимаба для лечения пациентов с ревматоидным артритом, не
получавших терапию метотрексатом, не рекомендовано, т.к. нет
достоверных данных о благоприятности отношения польза-риск для этой
группы больных.
Инфузионные
реакции
При
введении препарата Ритуксимаб наблюдались инфузионные реакции.
Развитие инфузионных реакций при введении препарата Ритуксимаб может
быть обусловлено высвобождением цитокинов и/или других медиаторов.
Перед каждой инфузией препарата Ритуксимаб необходимо проводить
премедикацию жаропонижающим/болеутоляющим и антигистаминным
препаратами. Кроме того, перед каждой инфузией препарата Ритуксимаб
больные с ревматоидным артритом должны получать премедикацию
глюкокортикостероидами для уменьшения частоты и тяжести инфузионных
реакций.
При
пострегистрационном наблюдении у больных с ревматоидным артритом были
зарегистрированы тяжелые инфузионные реакции с летальным исходом. В
условиях клинических исследований с участием пациентов с ревматоидным
артритом большинство случаев инфузионных реакций были легкой или
средней степени тяжести. Наиболее часто наблюдались аллергические
реакции: головная боль, зуд, ощущение першения в горле, приливы,
сыпь, крапивница, повышение артериального давления и лихорадка.
Инфузионные реакции чаще наблюдались после первой инфузии любого
курса лечения, чем после второй инфузии; с увеличением числа
выполненных курсов частота реакций снижалась. Инфузионные реакции
обычно разрешались после замедления или прерывания введения
ритуксимаба и назначения медикаментозной терапии (жаропонижающие,
антигистаминные средства и, при необходимости, кислород, внутривенное
введение солевых растворов, бронходилататоров,
глюкокортикостероидов). Необходимо тщательно наблюдать за пациентами
с заболеваниями сердечно-сосудистой системы, а также за теми, у кого
ранее отмечались нежелательные реакции со стороны сердца и легких.
При развитии инфузионных реакций, в зависимости от их тяжести и
необходимого лечения, введение ритуксимаба следует временно
приостановить или отменить. В большинстве случаев после полного
исчезновения симптоматики инфузию можно возобновить со скоростью,
составляющей 50% от предшествовавшей (например, 50 мг/ч вместо 100
мг/ч).
В
связи с возможностью развития реакций гиперчувствительности при
введении препарата Ритуксимаб, необходимо иметь средства для их
купирования: эпинефрин (адреналин), антигистаминные и
глюкокортикостероидные препараты.
Отсутствуют
данные о безопасности применения ритуксимаба для лечения пациентов с
умеренно выраженной сердечной недостаточностью (класс III по
классификации NYHA) или тяжелыми неконтролируемыми
сердечно-сосудистыми заболеваниями. У пациентов с исходным наличием
ишемии сердца, получавших ритуксимаб, наблюдалось проявление
симптомов соответствующих состояний, например, стенокардия, а также
трепетание и мерцание предсердий. Пациенты с заболеванием сердца или
предшествующими сердечно-легочными побочными реакциями требуют
особого внимания в период лечения препаратом Ритуксимаб, и риск
развития сердечно-сосудистых осложнений у них должен быть учтен при
рассмотрении возможности лечения. Во время введения препарата за ними
следует внимательно наблюдать.
Из-за
возможности развития гипотензии, не менее чем за 12 ч до инфузии
препарата Ритуксимаб следует отказаться от приема антигипертензивных
лекарственных средств.
Инфузионные
реакции у пациентов с гранулематозом с полиангиитом и
микроскопическим полиангиитом были схожи с наблюдавшимися в рамках
клинических исследований у пациентов с ревматоидным артритом.
Нарушения
со стороны сердца
В
связи с возможностью развития стенокардии или аритмии (трепетание и
фибрилляция предсердий), сердечной недостаточности или инфаркта
миокарда, на фоне лечения ритуксимабом требуется тщательное
наблюдение за пациентами с заболеваниями сердца в анамнезе.
Инфекции
С
учетом механизма действия препарата Ритуксимаб и важной роли
B-лимфоцитов
в поддержании нормальной иммунного ответа можно предположить, что
пациенты имеют повышенный риск инфекций вследствие терапии препаратом
Ритуксимаб.
У
пациентов в ходе лечения ритуксимабом могут возникать серьезные
инфекционные заболевания, в том числе с летальным исходом. Препарат
Ритуксимаб не следует назначать пациентам с активной тяжелой
инфекцией или выраженным иммунодефицитом (очень низкий уровень СD4+,
CD8+ клеток). Следует соблюдать осторожность при решении вопроса о
назначении препарата Ритуксимаб пациентам с рецидивирующей или
хронической инфекцией в анамнезе или при наличии условий,
предрасполагающих к развитию серьезных инфекций, например,
гипогаммаглобулинемии. Рекомендуется определить уровень
иммуноглобулинов перед началом лечения препаратом Ритуксимаб.
Пациентов
с признаками инфекции, возникшими после терапии препаратом
Ритуксимаб, следует своевременно обследовать и лечить соответствующим
образом. Перед последующим курсом препарата Ритуксимаб пациенты
должны быть обследованы повторно, должен быть оценен риск
возникновения инфекционных заболеваний.
Очень
редкие случаи прогрессирующей многоочаговой лейкоэнцефалопатии (ПМЛ)
со смертельным исходом были зарегистрированы после использования
ритуксимаба для лечения больных с ревматоидным артритом и
аутоиммунными заболеваниями, в том числе системной красной волчанкой
(СКВ) и васкулитом.
Гепатит
В
При
применении ритуксимаба у пациентов с ревматоидным артритом,
гранулематозом с полиангиитом и микроскопическим полиангиитом
наблюдались случаи реактивации гепатита В (в том числе с летальным
исходом). Перед назначением препарата Ритуксимаб всем пациентам
следует пройти скрининг на выявление вируса гепатита B. Минимальный
набор тестов должен включать определение HBsAg и HBсAb, в
соответствии с местными рекомендациями перечень тестов может быть
дополнен. Препарат Ритуксимаб не следует применять для лечения
пациентов с активным гепатитом В. Пациентам с положительными
серологическими маркерами гепатита В следует проконсультироваться с
врачом-гепатологом перед применением препарата Ритуксимаб; в
отношении таких пациентов необходимо проводить соответствующий
мониторинг и принимать меры по профилактике реактивации гепатита В в
соответствии с местными стандартами.
Поздняя
нейтропения
Перед
каждым курсом препарата Ритуксимаб, регулярно вплоть до истечения 6
месяцев после прекращения лечения, а также в случае возникновения
признаков инфекции, рекомендуется измерять количество нейтрофилов.
Кожные
реакции
При
лечении ритуксимабом были зарегистрированы случаи развития таких
тяжелых кожных реакций, как токсический эпидермальный некролиз
(синдром Лайелла) и синдром Стивенса-Джонсона, в ряде случаев с
летальным исходом. При выявлении данных реакций и подозрении на их
связь с препаратом Ритуксимаб лечение следует прекратить и не
возобновлять.
Иммунизация
Перед
применением препарата Ритуксимаб следует изучить вакцинальный статус
пациента и действовать согласно соответствующим рекомендациям по
иммунизации. Вакцинацию следует завершить не менее чем за 4 недели до
первого введения препарата Ритуксимаб.
Безопасность
иммунизации живыми вирусными вакцинами после лечения препаратом
Ритуксимаб не изучалась. Вакцинация живыми вирусными вакцинами не
рекомендуется во время лечения препаратом Ритуксимаб, или когда пул
периферических В-клеток истощен. Возможна вакцинация
инактивированными вакцинами, однако частота ответа на такие вакцины
может снижаться.
Через
6 месяцев терапии ритуксимабом и метотрексатом в рандомизированном
клиническом исследовании у пациентов с ревматоидным артритом
наблюдалась сходная частота ответа на введение столбнячного
анатоксина (39% и 42%, соответственно) по сравнению с терапией
метотрексатом, также наблюдалось снижение частоты ответа на введение
полисахаридной пневмококковой вакцины (43% и 82%, соответственно, как
минимум 2 серотипа антител к пневмококку), КНL-неоантигена (47% и
93%, соответственно). В случае необходимости вакцинации
инактивированными вакцинами во время лечения препаратом Ритуксимаб
она должна быть завершена не менее чем за 4 недели до повторного
курса терапии.
Количество
пациентов с ревматоидным артритом, получавших лечение ритуксимабом и
имеющих положительный титр антител к Streptococcus
pneumonia, Influenza, паротиту, краснухе,
ветряной оспе и столбнячному анатоксину до и через 1 год после начала
терапии ритуксимабом не изменялось.
Сопутствующая
и (или) последующая терапия с использованием других
противоревматических препаратов при ревматоидном артрите
Совместное
использование препарата Ритуксимаб с противоревматическими
препаратами, отличающимися от указанных в разделе показаний и
дозировки «Ревматоидный артрит», не рекомендуется.
Объем
данных клинических исследований, необходимых для полной оценки
безопасности последовательного применения других противоревматических
препаратов (в том числе ингибиторов ФНО и других биопрепаратов) после
лечения ритуксимабом, ограничен. Имеющиеся сведения позволяют
заключить, что частота развития клинически значимых инфекций у
больных, ранее получавших ритуксимаб, а впоследствии получавших
терапию, изменяющую течение заболевания, остается неизменной. Однако
следует внимательно наблюдать за пациентами для выявления признаков
инфекции, если биологические агенты и (или) базисные препараты
используются вскоре после терапии препаратом Ритуксимаб.
Злокачественные
новообразования
Применение
иммуномодулирующих препаратов может увеличить риск возникновения
злокачественных новообразований. Данные, основанные на ограниченном
опыте применения ритуксимаба для лечения больных с ревматоидным
артритом, не позволяют утверждать о возможном повышении риска
развития злокачественных новообразований. Тем не менее, на данный
момент возможный риск развития солидных опухолей не может быть
исключен.
Фертильность,
беременность и лактация
Контрацепция
у мужчин и женщин
В
связи с длительным периодом выведения ритуксимаба из организма
пациентов с истощенным пулом В-клеток, женщины с сохраненным
детородным потенциалом должны использовать эффективные методы
контрацепции в период лечения и в течение 12 месяцев после окончания
лечения препаратом Ритуксимаб.
Беременность
Иммуноглобулины
G (IgG) способны проникать через плацентарный барьер.
Уровень
В-клеток у новорожденных при назначении ритуксимаба женщинам во время
беременности в клинических исследованиях не изучался. У некоторых
новорожденных, матери которых получали ритуксимаб во время
беременности, наблюдались временное истощение пула В-клеток и
лимфоцитопения. Эффективность и безопасность препарата у беременных
женщин не доказана. По этим причинам не рекомендуется назначать
препарат Ритуксимаб беременным женщинам, кроме случаев, когда
предполагаемая польза превышает риск.
Грудное
вскармливание
Неизвестно,
выделяется ли ритуксимаб с грудным молоком. Учитывая, что
иммуноглобулины класса IgG, циркулирующие в крови матери, выделяются
с грудным молоком, грудное вскармливание не следует производить во
время и в течение 12 месяцев после лечения препаратом Ритуксимаб.
Фертильность
Исследования
не выявили неблагоприятных воздействий ритуксимаба на репродуктивные
органы.
Особенности
влияния лекарственного средства на способность управлять транспортным
средством или потенциально опасными механизмами
Неизвестно
влияет ли препарат Ритуксимаб на способность к управлению и работе с
машинами и механизмами, хотя фармакологическая активность и описанные
нежелательные явления не дают оснований предполагать такое влияние.
Передозировка
Существует
ограниченный опыт применения ритуксимаба в дозах, превышающих
рекомендованные, в рамках клинических исследований у человека.
Максимальная доза 5000 мг (2250 мг/м2)
назначалась пациентам с хроническим лимфолейкозом в рамках
клинического исследования в нарастающих дозах, дополнительных данных
по безопасности не получено.
В
случае выявления передозировки следует немедленно прекратить инфузию
препарата и тщательно наблюдать за состоянием пациента.
При
пострегистрационном наблюдении сообщалось о пяти случаях
передозировки ритуксимабом. В трех случаях не сообщалось о
нежелательных явлениях. Среди осложнений передозировки наблюдались
гриппоподобные симптомы (доза ритуксимаба 1,8 г) и дыхательная
недостаточность с летальным исходом (доза ритуксимаба 2,0 г).
Форма выпуска и упаковка
Концентрат для приготовления
раствора для инфузий, 10 мг/мл.
По
10 мл или 50 мл препарата во флаконы бесцветного
нейтрального стекла I гидролитического класса, укупоренные резиновыми
пробками, с обкаткой алюминиевыми колпачками с пластиковой крышкой
типа «flip—off».
На каждый флакон наклеивают самоклеящуюся этикетку.
По 2 флакона (по 10
мл препарата) в контурную ячейковую упаковку из пленки ПВХ. По 1
контурной ячейковой упаковке вместе с инструкцией по применению на
государственном и русском языках помещают в пачку из картона.
По 1
флакону (по 50 мл препарата) вместе с инструкцией по применению
на государственном и русском языках помещают в пачку из картона.
Условия хранения
Хранить
в защищенном от света месте при
температуре от 2 до 8°С.
Не
замораживать.
Хранить
в недоступном для детей месте.
Срок хранения
30 месяцев.
Не
применять по истечении срока годности, указанного на упаковке.
Условия отпуска из аптек
По
рецепту
Производитель
ТОО
«Карагандинский
фармацевтический комплекс»
Республика
Казахстан
100009,
г.
Караганда, ул. Газалиева, 16
Тел/факс
(7212)908051, e-mail: kphk@kphk.kz,
сайт: www.kphk.kz
Упаковщик
ТОО
«Карагандинский
фармацевтический комплекс»
Республика
Казахстан
Владелец регистрационного удостоверения
ТОО
«Карагандинский
фармацевтический комплекс»
Республика
Казахстан
Наименование,
адрес и контактные данные организации на территории Республики
Казахстан, принимающей претензии (предложения) по качеству
лекарственных средств от потребителей:
ТОО
«Карагандинский фармацевтический комплекс»
Республика
Казахстан
100009,
г. Караганда, ул. Газалиева, 16
Тел./факс:
(7212) 908051, e-mail: kphk@kphk.kz, сайт: www.kphk.kz.
Наименование,
адрес и контактные данные организации на территории Республики
Казахстан, ответственной за пострегистрационное наблюдение за
безопасностью лекарственного средства:
ТОО
«Карагандинский фармацевтический комплекс»
Республика
Казахстан
100009,
г. Караганда, ул. Газалиева, стр. 16
Тел
(7212)90-80-43, e-mail medinfo@kphk.kz,
сайт:
www.kphk.kz
40
| Ритуксимаб_каз.doc | 0.32 кб |
| Ритуксимаб_рус.doc | 0.29 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники