Ротарикс® (моновалентная человеческая живая аттенуированная вакцина жидкая для профилактики ротавирусной инфекции)
Производитель: GlaxoSmithKline Biologicals s.a.
Анатомо-терапевтическо-химическая классификация: Вирус, возбудитель ротавирусной диареи, живой ослабленный
Номер регистрации в РК:
№ РК-ЛС-5№017557
Информация о регистрации в РК:
13.01.2016 — 13.01.2021
- Скачать инструкцию медикамента
Торговое название
Ротарикс®
(Моновалентная человеческая живая аттенуированная вакцина жидкая для профилактики ротавирусной инфекции)
Международное непатентованное название
Нет
Лекарственная форма
Суспензия для приема внутрь, 1.5 мл/1 доза в оральном аппликаторе (шприце) или в полиэтиленовой тубе
Состав
1.5 мл (1 доза) содержат
активное вещество — живой аттенуированный человеческий штамм ротавируса RIX4414 не менее 106 ЦПД 50 (цитопатогенное действие – 50%),
вспомогательные вещества: сахароза, динатрия адипат, среда Игла модифицированная Дульбекко (DMEM)1, вода для инъекций.
1состав среды Игла, модифицированной Дульбекко (DMEM):
натрия хлорид, калия хлорид, магния сульфата гептагидрат, железа нитрата нонагидрат, натрия фосфата дигидрат, натрия пируват, D-глюкоза, концентрированный раствор витаминов (фолиевая кислота, кальция пантотенат, холина хлорид, инозитол, никотинамид, пиридоксина хлоргидрат, тиамина хлоргидрат, рибофлавин), L-цистин, L-тирозин, раствор аминокислот (L-аргинин, глицин, L-изолейцин, L-лейцин, L-лизин, L-метионин, L-фенилаланин, L-треонин, L-триптофан, L-серин, L-валин), L-глутамин кальция хлорида дигидрат, натрия гидрокарбонат, феноловый красный, вода для инъекций.
Описание
Прозрачная, бесцветная жидкая суспензия без видимых включений.
Фармакотерапевтическая группа
Вакцины против ротавирусной диареи. Вирус, возбудитель ротавирусной диареи, живой ослабленный.
Код АТX J07BH01
Фармакологические свойства
Фармакокинетика
Проведение фармакокинетических исследований для вакцин не требуется.
Фармакодинамика
Ротарикс® – жидкая живая моновалентная вакцина аттенуированного штамма человеческого ротавируса RIX4414, культивируемого на клетках Веро. Ротарикс® проявляет эффективность в профилактике гастроэнтеритов, вызываемых следующими серотипами ротавируса: G1Р, G2Р, G3Р, G4Р, G9Р. Кроме того, клинически доказана эффективность против штаммов ротавируса G8Р (тяжелые гастроэнтериты) и G12P (прочие гастроэнтериты). Данные штаммы распространены по всему миру.
Ротарикс® предназначен для профилактики ротавирусной инфекции.
Иммунологические свойства
В клинических исследованиях, проведённых в 23 странах Европы, Латинской Америке и Азии, 1957 младенцев получили вакцину Ротарикс®, а 1006 младенцев получили плацебо в соответствии с разными графиками вакцинации (2 мес.–3 мес.; 2 мес.–4 мес., 3 мес.–4 мес.). Процентное соотношение детей с титрами антител ≥ 20 единиц/мл (по данным иммуноферментного анализа) после введения второй дозы вакцины колеблется в пределах от 77,9% до 100%, после применения плацебо уровни антител составили от 0% до 17,1%.
В исследовании у детей с ВИЧ-инфекцией вакцина Ротарикс® была иммуногенна с уровнем сероконверсии 57.1% (доверительный интервал [ДИ] 95%).
Выделение вакцины
Пик выделения вакцинного вируса со стулом приходится приблизительно на 7-й день после вакцинации и длится в целом 10 дней. Частички вирусного антигена, определяемого с помощью ИФА, обнаруживаются приблизительно в 50% стула после введения первой дозы и в 4% после введения второй дозы. При анализе стула на наличие живого вакцинного штамма, 17% исследуемых образцов показали положительный результат.
Защитная эффективность
Проведенные в Европе, Латинской Америке и Африке клинические исследования имели цель показать защитную эффективность Ротарикс® против гастроэнтеритов, вызванных ротавирусом, в том числе тяжелых.
Несмотря на то, что вакцина Ротарикс® вводится в режиме 2-х доз, в Европе были проведены исследования эффективности после введения первой дозы. Эффективность вакцины против гастроэнтерита разной степени тяжести в интервале между введением первой и второй доз составила 89.8% (доверительный интервал — 95%). Также анализ исследований, проведенных в Латинской Америке, показал, что эффективность вакцины против гастроэнтерита тяжелой степени в интервале между введением первой и второй доз составила 64.4% (доверительный интервал [ДИ] — 95%). После введения двух доз Ротарикса® защитная эффективность вакцины, наблюдаемая в течение первого и второго года жизни детей, представлена в таблицах 1, 2 и 3.
Таблица 1. Исследование, проведенное в Европе: дети в возрасте от 1 года до 2-х лет
Оценивали эффективность вакцины у 4000 детей в соответствии с различными графиками вакцинации (2, 3 месяца; 2, 4 месяца; 3, 4 месяца; 3, 5 месяцев).
|
Дети первого года жизни, получившие Ротарикс® =2572; получившие плацебо =1302 |
Дети второго года жизни, получившие Ротарикс® =2554; получившие плацебо =1294 |
|||
|
Эффективность вакцины (%) против ротавирусного гастроэнтерита разных степеней тяжести [95% ДИ] |
||||
|
Тип |
Разная степень тяжести |
Тяжёлая степень † |
Разная степень тяжести |
Тяжёлая степень † |
|
G1P[8] |
95.6 |
96.4 |
82.7 |
96.5 |
|
G2P[4] |
62.6* |
74.7* |
57.1 |
89.9 |
|
G3P[8] |
89.9 |
100 |
79.7 |
83.1* |
|
G4P[8] |
88.3 |
100 |
69.6* |
87.3 |
|
G9P[8] |
75.6 |
94.7 |
70.5 |
76.8 |
|
Штаммы с генотипом P[8] |
88.2 |
96.5 |
75.7 |
87.5 |
|
Циркулирующие ротавирусные штаммы |
87.1 |
95.8 |
71.9 |
85.6 |
|
Эффективность вакцины (%) против ротавирусного гастроэнтерита, требующего обращения к врачу |
||||
|
Циркулирующие ротавирусные штаммы |
91.8 |
76.2 |
||
|
Эффективность вакцины (%) против ротавирусного гастроэнтерита, требующего госпитализации |
||||
|
Циркулирующие ротавирусные штаммы |
100 |
92.2 |
†Тяжёлый гастроэнтерит, определённый баллом ≥11 по шкале Весикари
*Статистически недостаточно значимый показатель. Данные должны интерпретироваться с осторожностью.
Таблица 2. Исследование, проведённое в Латинской Америке
В исследованиях оценивали эффективность вакцины у более чем 20000 детей.
|
Тип |
Эффективность вакцины (%) против ротавирусного гастроэнтерита тяжелой степени† Дети первого года жизни, получившие Ротарикс =9,009; получившие плацебо =8,858 |
Эффективность вакцины (%) против ротавирусного гастроэнтерита тяжелой степени† Дети второго года жизни, получившие Ротарикс =7,175; получившие плацебо =7,062 |
|
Все ротавирусные штаммы |
84.7 |
79.0 |
|
G1P[8] |
91.8 |
72.4 |
|
G3P[8] |
87.7 |
71.9* |
|
G4P[8] |
50.8*# |
63.1 |
|
G9P[8] |
90.6 |
87.7 |
|
Штаммы с генотипом P |
90.9 |
79.5 |
†Тяжесть ротавирусного гастроэнтерита определялась как эпизоды диареи с рвотой или без, требующие госпитализации и/или мероприятий по регидратации.
*Статистически недостаточно значимый показатель. Данные должны интерпретироваться с осторожностью.
#Количество случаев, на которых основывались предположения об эффективности вакцины против G4P, были незначительны (1 случай в группе Ротарикса и 2 – в группе плацебо)
Обобщённый анализ пяти исследований эффективности вакцины показал 71,4% эффективности против тяжёлого гастроэнтерита (балл Весикари ≥11), вызванного типом ротавируса G2P.
Таблица 3. Исследование, проведённое в Африке
|
Тип |
Эффективность вакцины (%) против ротавирусного гастроэнтерита любой степени тяжести Ротарикс =2974; получившие плацебо =1443 |
Эффективность вакцины (%) против ротавирусного гастроэнтерита тяжелой степени† Ротарикс =2974; получившие плацебо =1443 |
|
G1P[8] |
68.3 |
56.6 |
|
G2P[4] |
49.3 |
83.8 |
|
G3P[8] |
43.4* |
51.5* |
|
G8P[4] |
38.7* |
63.6 |
|
G9P[8] |
41.8* |
56.9* |
|
G12P[6] |
48.0 |
55.5* |
|
Штаммы с генотипом P[4] |
39.3 |
70.9 |
|
Штаммы с генотипом P[6] |
46.6 |
55.2* |
|
Штаммы с генотипом P[8] |
61.0 |
59.1 |
†Тяжесть ротавирусного гастроэнтерита определялась по шкале Весикари с показателем тяжести ≥11.
*Статистически недостаточно значимый показатель. Данные должны интерпретироваться с осторожностью.
Эффективность и безопасность у недоношенных детей
В ходе клинических исследований 1009 недоношенным младенцам, 198 из которых были рождены в сроке от 27 до 30 недель и 801 младенец – в сроке 31-36 недель, назначались вакцина Ротарикс® или плацебо. Первая доза вводилась в возрасте 6 недель. Серьезные побочные эффекты были зафиксированы у 5.1% детей, получавших Ротарикс® по сравнению с 6.8% детей, получавших плацебо. Похожая частота других побочных эффектов наблюдалась у детей, получавших Ротарикс® или плацебо. Не наблюдалось ни одного случая возникновения кишечной непроходимости.
В клинических исследованиях с участием недоношенных детей, рожденных на 27-36 неделе, по изучению иммуногенности вакцины Ротарикс®, установлена иммуногенность вакцины в режиме двухдозного введения у 85.7% детей (доверительный интервал 95%): уровень титра анти-ротавирусных антител IgA в сыворотке был ³ 20Ед/мл (метод ИФА) через 1 месяц после введения второй дозы вакцины.
Эффективность и безопасность применения вакцины Ротарикс® у детей с ВИЧ
В клинических исследованиях 100 младенцам, инфицированным ВИЧ, назначали Ротарикс® или плацебо. Профиль безопасности был одинаков у детей, получавших вакцину или плацебо.
В исследовании у детей с ВИЧ-инфекцией вакцина Ротарикс® была иммуногенна с уровнем сероконверсии 57.1% (ДИ 95%).
Совместное применение с другими вакцинами
В результате 17 клинических исследований, проведенных в Европе, Северной и Латинской Америке, Азии и Африке, результаты, полученные на 31-й день после введения второй дозы, продемонстрировали, что совместное назначение нескольких детских вакцин не влияет на профиль безопасности и иммунный ответ на каждую из назначаемых вакцин (см. раздел «Лекарственные взаимодействия»).
Показания к применению
— профилактика ротавирусного гастроэнтерита или ротавирусной инфекции у детей с 6 до 24 недель жизни
Способ применения и дозы
Вакцина Ротарикс® предназначена только для приема внутрь!
Препарат ни при каких обстоятельствах нельзя вводить парентерально!
Курс вакцинации состоит из 2-х прививочных доз согласно национальному графику вакцинации, с соблюдением интервала между двумя прививками не менее 4-х недель: 6-10 недель или 2-4 месяца.
Для создания полноценного иммунитета необходимо получить 2 дозы вакцины. Первая доза вводится детям, начиная с 6-недельного возраста. Курс вакцинации должен быть завершен к 24-й неделе жизни ребенка.
Ротарикс® может применяться у недоношенных новорожденных с таким же режимом введения.
В клинических исследованиях изредка наблюдалось сплевывание и срыгивание ребенком вакцины. Дополнительная доза вакцины при этом не применялась. Тем не менее, если ребенок сплюнул или срыгнул большую часть вакцинной дозы, можно сразу же дать ребенку еще одну разовую дозу вакцины.
Настоятельно рекомендуется, чтобы дети, получившие первую дозу Ротарикса®, окончили курс вакцинации приемом второй дозой вакцины.
Не предусмотрено ограничений, связанных с приемом пищи или жидкости ребенком, включая грудное молоко, ни до, ни после вакцинации.
На основании данных, полученных в клинических испытаниях, грудное вскармливание не снижает защиту от ротавирусного гастроэнтерита, предоставляемую Ротариксом®. Следовательно, грудное вскармливание можно продолжить на протяжении всей программы вакцинации.
Инструкции по использованию
Вакцина представлена в виде прозрачной, бесцветной жидкости, без видимых частиц, для перорального приёма. В случае обнаружения любых инородных твёрдых частиц и/или аномального физического вида, откажитесь от применения вакцины.
Вакцина готова к использованию (не требуется восстановления или разведения). Вакцина не должна смешиваться с какими-либо другими вакцинами или растворами.
Неиспользованная вакцина и/или использованные туба и колпачок должны утилизироваться в соответствии с местными требованиями к биологическим материалам.
Инструкция по введению вакцины из перорального аппликатора:
| 843115161477976330_ru.doc | 229.5 кб |
| 616202181477977580_kz.doc | 336 кб |
Отправить прикрепленные файлы на почту
Национальный центр экспертизы лекарственных средств, изделий медицинского назначения и медицинской техники
Форма выпуска, состав и упаковка
лиофилизат д/пригот. сусп. д/приема внутрь 1 доза: фл. 1, 5, 10 или 25 шт. в компл. с растворителем и адаптером
Рег. №: 8673/08/13 от 24.05.2013 — Истекло
Лиофилизат для приготовления суспензии для приема внутрь в виде плотной массы или порошка беловатого цвета; при разведении образуется прозрачная, бесцветная суспензия; приложенный растворитель — мутная жидкость с медленно оседающим осадком белого цвета и бесцветной надосадочной жидкостью.
| 1 доза | |
| аттенуированный вакцинный штамм человеческого ротавируса RIX4414, культивируемого на клетках Веро | не менее 106.0 ТЦД50 |
Вспомогательные вещества: сахароза, декстран, сорбитол, аминокислоты; среда Игла, модифицированная Дулбеко (ДМЕМ).
Растворитель: кальция карбонат, ксантан, вода д/и.
1 доза (1 мл) — флаконы стеклянные (1) в комплекте с растворителем (шприц 1 шт.) и адаптером — пачки картонные.
1 доза (1 мл) — флаконы стеклянные (5) в комплекте с растворителем (шприц 5 шт.) и адаптером — пачки картонные.
1 доза (1 мл) — флаконы стеклянные (10) в комплекте с растворителем (шприц 10 шт.) и адаптером — пачки картонные.
1 доза (1 мл) — флаконы стеклянные (25) в комплекте с растворителем (шприц 25 шт.) и адаптером — пачки картонные.
Описание лекарственного препарата РОТАРИКС создано в 2015 году на основании инструкции, размещенной на официальном сайте Минздрава РБ. Дата обновления: 09.06.2015 г.
Фармакологическое действие
Защитная эффективность
В клинических исследованиях была продемонстрирована эффективность вакцины в отношении гастроэнтеритов, вызванных ротавирусами наиболее часто встречающихся генотипов G1P[8], G2P[4], G3P[8], G4P[8] и G9P[8]. Кроме того, была продемонстрирована эффективность в отношении нетипичных ротавирусных генотипов G8P[4] (тяжелый гастроэнтерит) и G12P[6] (гастроэнтерит любой степени тяжести). Данные штаммы циркулируют во всем мире.
Клинические исследования по защитной эффективности вакцины Ротарикс против ротавирусных гастроэнтеритов, в том числе тяжелых, проведены в Европе, Южной Америке и Африке.
Защитная эффективность в Европе
В европейском исследовании с участием 4000 человек оценивалось применение вакцины Ротарикс согласно различным утвержденным в Европе схемам вакцинации (2,3 месяца; 2,4 месяца; 3,4 месяца; 3,5 месяцев).
Тяжесть гастроэнтеритов определялась на основе 20-ти балльной шкалы Vesikari, которая оценивает полную клиническую картину ротавирусного гастроэнтерита, с учетом тяжести и длительности диареи и рвоты, тяжести лихорадки и обезвоживания, а также необходимости лечения.
Защитная эффективность после введения двух доз вшсцины Ротарикс, наблюдаемая на первом и на втором году жизни, приведена в таблице:
| 1 год жизни Ротарикс N=2572 Плацебо N=1302 (§) |
2 год жизни Ротарикс N=2554 Плацебо N=1294 (§) |
|||
| Эффективность вакцины (%) в отношении любых и тяжелых ротавирусных гастроэнтеритов [95% доверительный интервал] | ||||
| Генотип | Любой степени тяжести | Тяжелый1 | Любой степени тяжести | Тяжелый1 |
| G1P[8] | 95.6 [87.9;98.8] |
96.4 [85.7;99.6] |
82.7 [67.8;91.3] |
96.5 [86.2;99.6] |
| G2P[4] | 62.0* [<0.0;94.4] |
74.7* [<0.0;99.6] |
57.1 [<0.0;82.6] |
89.9 [9.4;99.8] |
| G3P[8] | 89.9 [9.5;99.8] |
100 [44.8;100] |
79.7 [<0.0;98.1] |
83.1* [<0.0;99.7] |
| G4P[8] | 88.3 [57.5;97.9] |
100 [64.9;100] |
69.6* [<0.0;95.3] |
87.3 [<0.0;99.7] |
| G9P[8] | 75.6 [51.1;88.5] |
94.7 [77.9;99.4] |
70.5 [50.7;82.8] |
76.8 [50.8;89.7] |
| Штаммысгенотипом Р[8] | 88.2 [80.8;93.0] |
96.5 [90.6;99.1] |
75.7 [65.0;83.4] |
87.5 [77.8;93.4] |
| Циркулирующие штаммы ротавируса | 87.1 [79.6;92.1] |
95.8 [89.6;98.7] |
71.9 [61.2;79.8] |
85.6 [75.8;91.9] |
| Эффективность вакцины (%) в отношении ротавирусных гастроэнтеритов, требующих медицинского наблюдения [95% доверительный «интервал] | ||||
| Циркулирующие штаммыротавируса | 91.8 [84;96.3] |
76.2 [63.0;85.0] |
||
| Эффективность вакцины (%) в отношении ротавирусных гастроэнтеритов, требующих госпитализации [95% доверительный интервал] | ||||
| Циркулирующие штаммы ротавируса | 100 [81.8;100] |
92.2 [65.6;99.1] |
1тяжелые гастроэнтериты определяются как показатель ≥11 по шкале Vesikari
(§) оценка эффективности у лиц, завершивших протокол исследования
* не является статистически значимым (р≥0.05). Полученные данные следует интерпретировать с осторожностью.
Эффективность вакцины на первом году жизни увеличивалась пропорционально увеличению степени тяжести заболевания, достигая 100% (95% доверительный интервал: 84.7; 100) для степени тяжести по шкале Vesikari≥17.
Защитная эффективность в Южной Америке
В клиническом исследовании, проведенном в Южной Америке, вакцина Ротарикс применялась у более чем 20000 детей. Степень тяжести гастроэнтерита определялась в соответствии с критериями ВОЗ. Защитная эффективность вакцины против тяжелых ротавирусных гастроэнтеритов, требующих госпитализации и/или регидратационной терапии в стационаре, а также эффективность двух доз вакцины Ротарикс против ротавирусных гастроэнтеритов, вызываемых различными генотипами ротавируса,представлена в нижеследующей таблице:
| Генотип | Тяжелые ротавирусные гастроэнтериты (на первом году жизни) Ротарикс N=9009 Плацебо N=8858 (§) |
Тяжелые ротавирусные гастроэнтериты (на втором году жизни) Ротарикс N=7175 Плацебо N=7062 (§) |
| Эффективность (%) [95% доверительный интервал] |
Эффективность (%) [95% доверительный интервал] |
|
| Все ротавирусные генотипы | 84.7 [71.7;92.4] |
79.0 [66.4;87.4] |
| G1P[8] | 91.8 [74.1;98.4] |
72.4 [34.5;89.9] |
| G3P[8] | 87.7 [8.3;99.7] |
71.9* [<0.0;97.1] |
| G4P[8] | 50.8#* [<0.0;99.2] |
63.1 [0.7;88.2] |
| G9P[8] | 90.6 [61.7;98.9] |
87.7 [72.9;95.3] |
| Штаммы с генотипом Р[8] | 90.9 [79.2;96.8] |
79.5 [67.0;87.9] |
(§) оценка эффективности у лиц, завершивших протокол исследования
* не является статистически значимым (р≥0.05). Полученные данные следует интерпретировать с осторожностью.
# Эффективность в отношении G4P[8] была оценена на основании очень маленького количества случаев (1 случай в группе Ротарикс и 2 случая в группе плацебо). В объединенном анализе пяти исследований эффективности* была продемонстрирована эффективность 71.4% (95% доверительный интервал: 20.1; 91.1) в отношении тяжелого ротавирусного гастроэнтеритата (балл по шкале Vesikari≥11), вызванного генотипом ротавируса G2P[4], на первом году жизни.
* В данных клинических исследованиях оценка конечных точек и доверительные интервалы составили: 100% (95% доверительный интервал: -1858.0; 100), 100% (95% доверительный интервал: 21.1; 100), 45.4% (95% доверительный интервал: -81.5; 86.6), 74.7 (95% доверительный интервал: -386.2; 99.6). Оценок для остальных исследований не получено.
Защитная эффективность в Африке
В клиническом исследовании, проведенном в Африке (Ротарикс: N=2974; плацебо: N=1443), оценивалась эффективность вакцины Ротарикс, применяемой в возрасте 10 и 14 недель (2 дозы) или в возрасте 6, 10 и 14 недель (3 дозы). Эффективность вакцины в отношении тяжелых ротавирусных гастроэнтеритов на первом году жизни составила 61.2% (95% доверительный интервал: 44.0; 73.2). Защитная эффективность вакцины (объединенные дозы)в отношении любого и тяжелого ротавирусного гастроэнтерита представлена в нижеследующей таблице:
| Генотип | Любой ротавирусный гастроэнтерит Ротарикс N=2974 Плацебо N=1443 |
Тяжелые ротавирусные гастроэнтериты Ротарикс N=2974 Плацебо N=1443 |
| Эффективность (%) [95%доверительный интервал] |
Эффективность (%) [95% доверительный интервал] |
|
| G1P[8] | 68.3 [53.6;78.5] |
56.6 [1.8;78.8] |
| G2P[4] | 49.3 [4.6;73.0] |
83.8 [9.6;98.4] |
| G3P[8] | 43.4* [<0;83.7] |
51.5* [<0;96.5] |
| G8P[4] | 38.7* [<0;67.8] |
63.6 [5.9;86.5] |
| G9P[8] | 41.8* [<0;72.3] |
56.9* [<0;85.5] |
| G12P[6] | 48.0 [9.7;70.0] |
55.5* [<0;82.2] |
| Штаммы с генотипом P[4] | 39.3 [7.7;59.9] |
70.9 [37.5;87.0] |
| Штаммы с генотипом Р[6] | 46.6 [9.4;68.4] |
55.2* [<0;81.3] |
| Штаммы сгенотипом Р[8] | 61.0 [47.3;71.2] |
59.1 [32.8;75.3] |
* не является статистически значимым (р≥0.05). Полученные данные следует интерпретировать с осторожностью.
Иммунный ответ
Иммунологическиймеханизм, лежащий в основе защиты Ротарикс против ротавирусных гастроэнтеритов, до конца не ясен. Взаимосвязь между ответом антител на вакцинацию против ротавируса и формированием защиты в отношении ротавирусных гастроэнтеритов не установлена.
Ниже представлен процент лиц, изначально серонегативных к ротавирусу (IgA титр антител <20 ЕД/мл (методом иммуноферментного анализа (ИФА)), с сывороточной концентрацией антиротавирусных антител IgA≥20 ЕД/мл через 1-2 месяца после получения второй дозы вакцины или плацебо в различных клинических исследованиях.
| Схема | Страны и регионы, в которых проводились исследования | Вакцина | Плацебо | ||
| N | %≥20 ЕД/мл [95% ДИ*] |
N | %≥20 ЕД/мл [95% ДИ*] |
||
| 2, 3 месяца | Франция, Германия | 239 | 82.8 [77.5;87.4] |
127 | 8.7 [4.4;15.0] |
| 2, 4 месяца | Испания | 186 | 85.5 [79.6;90.2] |
89 | 12.4 [6.3;21.0] |
| 3, 5 месяца | Финляндия, Италия | 180 | 94.4 [90.0;97.3] |
114 | 3.5 [1.0;8.7] |
| 3, 4 месяца | Чешская Республика | 182 | 84.6 [78.5;89.5] |
90 | 2.2 [0.3;7.8] |
| 2, 3-4 месяца | Южная Америка; 11 стран | 393 | 77.9 [73.8;81.6] |
341 | 15.1 [11.7;19.0] |
| 10, 14 недель и 6, 10, 14 недель (объединенная) | Южная Африка, Малави | 221 | 58.4 [51.6;64.9] |
111 | 22.5 [15.1;31.4] |
*ДИ — доверительный интервал
Иммунный ответ у недоношенных детей
В клиническом исследовании у недоношенных детей, рожденных в гестационном возрасте не менее 27 недель, иммуногенность вакцины Ротарикс оценивалась на подгруппе из 147 детей. Исследование продемонстрировало иммуногенность вакцины в данной группе населения: у 85.7% детей (95% доверительный интервал: 79.0; 90.9) достигался титр антиротавирусньгх антител IgA≥20 ЕД/мл (ИФА) через месяц после введения второй дозы вакцины.
Показания к применению
Ротарикс показан для проведения активной иммунизации детей в возрасте с 6 до 24-х недель для профилактики гастроэнтеритов, вызванных ротавирусной инфекцией.
Вакцина Ротарикс должна применяться в соответствии с официальными рекомендациями.
Реклама
Режим дозирования
Схема вакцинации
Курс вакцинации состоит из двух доз. Первую дозу следует давать ребенку в возрасте от 6-ти недель. Интервал между приемами должен составлять не менее 4-х недель. Курс вакцинации предпочтительно завершить к возрасту 16-ти недель, но он должен быть обязательно завершен к возрасту 24-х недель.
Вакцину Ротарикс можно в той же дозе назначать недоношенным детям, рожденным в гестационном возрасте не менее 27недель. В клинических исследованиях в редких случаях наблюдалось оплевывание и срыгивание ребенком вакцины. Дополнительная доза вакцины при этом не применялась. Темне менее в тех редких ситуациях, когда произошла регургитация большей части дозы вакцины, можно сразу же дать ребенку еще одну разовую дозу.
Настоятельно рекомендуется, чтобы дети, получившие первую дозу вакцины Ротарикс, закончили двухдозовый курс вакцинации Ротарикс. Нет данных о безопасности, иммуногенности и эффективности применения вакцины Ротарикс в качестве первой дозы курса вакцинации и применения другой ротавирусной вакцины в качестве второй дозы, или наоборот.
Вакцину Ротарикс нельзя использовать у детей старше 24-х недель.
Способ введения
Вакцина Ротарикс предназначена только для приема внутрь.
Вакцину ни при каких обстоятельствах не следует вводить парентерально!
Инструкции по использованию
Недопустимо механическое смешивание вакцины с другими лекарственными препаратами.
При хранении шприца с растворителем возможно образование белого осадка с прозрачной надосадочной жидкостью. Перед применением содержимое шприца следует внимательно осмотреть на предмет инородных частиц или несоответствия описанию, как до, так и после встряхивания.
Восстановленную вакцину перед применением также следует осмотреть, чтобы исключить попадание инородных твердых частиц и/или нарушения внешнего вида. Если в восстановленной вакцине наблюдаются посторонние включения или внешний вид не соответствует описанию, то вакцину не используют.
Восстановление вакцины:
1. Удалите пластиковую крышку с флакона, содержащего лиофилизат.
2. Поместите адаптер на флакон, нажимая на адаптер по направлению вниз, чтобы он плотно сел на флакон.
3. Энергично встряхните шприц с растворителем. После встряхивания полученная суспензия выглядит как мутная жидкость с медленно оседающим осадком белого цвета.
4. Снимите защитный колпачок с кончика шприца.
5. Соедините кончик шприца с адаптером, плотно прижимая его.
6. Введите содержимое шприца во флакон, содержащий лиофилизат вакцины.
7. Не разъединяя шприц с адаптером, встряхните флакон и осмотрите содержимое на полноту растворения. Восстановленная вакцина выглядит более мутной, чем растворитель. Такой внешний вид является нормальным.
8. Поместите смесь обратно в шприц.
9. Отсоедините шприц отадаптера.
10. Вакцина Ротарикс предназначена исключительно для приема внутрь. Ребенок должен находиться в положении полулежа. Введите содержимое шприца полностью в ротовую полостьребенка, прижав шприц к внутренней поверхности щеки.
11. Ни при каких обстоятельствах не вводите восстановленную вакцину парентерально!
Если вакцина не введена сразу после восстановления, на шприц, содержащий восстановленную вакцину, вновь надевают защитный колпачок. Шприц следует снова осторожно встряхнуть перед пероральным введением. Ни при каких обстоятельствах не вводите восстановленную вакцину парентерально!
Побочные действия
Клинические исследования
Профиль безопасности вакцины, представленный ниже, основывается на данных клинических исследовании, проведенных с применением жидкой (суспензия для приема внутрь) или лиофилизированной (лиофилизат для приготовления суспензии для приема внутрь) формы вакцины Ротарикс.
В четырех клинических исследованиях, включавших около 1900 детей, было применено около 3800 доз жидкой формы вакцины Ротарикс. Исследования показали, что профиль безопасности жидкой формы вакцины сравним с профилем лиофизилированной вакцины. В 23 плацебо-контролируемых клинических исследованиях было применено около 106000 доз вакцины Ротарикс в двух лекарственных формах (лиофилизат для приготовления суспензии для приема внутрь и суспензия для приема внутрь) у порядка 51000 детей.
В трех плацебо-контролируемых клинических исследованиях (Финляндия, Индия и Бангладеш), где вакцина Ротарикс применялась без сочетания с другими вакцинами (введение педиатрических вакцин было отложено), частота возникновения и тяжесть активно выявляемых нежелательных явлений (собранных через 8 дней после вакцинации), таких как диарея, рвота, потеря аппетита, лихорадка, раздражительность и кашель/ринорея в группе, получившей Ротарикс, были сопоставимы с плацебо. Также не было отмечено увеличения тяжести этих нежелательных реакций с применением второй дозы вакцины.
В результате объединенного анализа данных семнадцати плацебо-контролируемых клинических исследований (Европа, Северная Америка, Южная Америка, Азия и Африка), включая исследования, в которых вакцина Ротарикс применялась в сочетании с педиатрическими вакцинами, были зафиксированы следующие нежелательные реакции (собранные через 31 день после вакцинации) как возможно связанные с вакцинацией. Нежелательные реакции, приведенные ниже, перечислены в зависимости от анатомо-физиологической классификации и частоты встречаемости. В рамках каждой группы частоты встречаемости побочные реакции перечислены в порядке снижения степени серьезности.
Частота встречаемости определяется следующим образом: очень часто (≥1/10), часто (≥1/100 и <1/10), нечасто (≥1/1000 и 1/100), редко (≥1/10000 и <1/1000), очень редко (<1/10000, включая отдельные случаи).
Со стороны ЖКТ: часто – диарея; нечасто — боль в животе, метеоризм.
Со стороны кожи и подкожно-жировой клетчатки: нечасто – дерматит.
Общие реакции и реакции в месте введения: часто — раздражительность
Риск возникновения кишечной непроходимости изучался в крупномасштабном клиническом исследовании безопасности, проведенном в Южной Америке и Финляндии при участии 63225 детей. Это исследование продемонстрировало отсутствие повышенного риска возникновения кишечной непроходимости в группах, принимавших Ротарикс, по сравнению с группами плацебо (см. таблицу).
| Ротарикс | Плацебо | Относительный риск (95% ДИ*) | |
| Кишечная инвагинация, возникшая в течение 31 дня после: | Общее число детей — 31 673 | Общее число детей — 31552 | |
| Первой дозы | 1 | 2 | 0.50 (0.07;3.80) |
| Второй дозы | 5 | 5 | 0.99 (0.31;3.21) |
*ДИ: доверительный интервал
Безопасность у недоношенных детей
В клиническом исследовании 670 недоношенных детей, родившихся на 27-36 неделе гестации, получали вакцину Ротарикс и 339 получали плацебо. Первая доза вакцины вводилась, начиная с 6-й недели после рождения. Серьезные нежелательные реакции наблюдались у 5.1% детей, получивших Ротарикс, и у 6.8% детей, получивших плацебо. Частота побочных реакций в обеих группах была одинаковой. Случаев кишечной непроходимости отмечено не было.
Безопасность у детей с ВИЧ-инфекцией
В клиническом исследовании 100 детей с ВИЧ-инфекцией получили Ротарикс или плацебо. Профиль безопасности был схож в группах Ротарикс и плацебо.
Пострегистрационное наблюдение
В связи с тем, что информация о данных побочных реакциях поступала в спонтанных отчетах, не представляется возможным надежно оценить их частоту.
Со стороны дыхательной системы, органов грудной клетки и средостения: апноэ у глубоко недоношенных детей (≤28 недель гестации).
Со стороны ЖКТ: кишечная непроходимость, гематохезия, гастроэнтерит с выделением вакцинного вируса у детей с тяжелым комбинированным иммунодефицитом.
Противопоказания к применению
— гиперчувствительность к активному веществу или любому вспомогательному компоненту;
— гиперчувствительность, возникшая после предшествующего назначения вакцины для профилактики ротавирусной инфекции;
— кишечная непроходимость в анамнезе;
— вакцина противопоказана лицам с нескорректированным врожденным пороком развития ЖКТ, который может предрасполагать к развитию кишечной непроходимости;
— тяжелый комбинированный иммунодефицит;
— вакцинацию следует отложить в острый период заболевания, сопровождающийся тяжелым лихорадочным состоянием. Наличие незначительной инфекции не является противопоказанием для иммунизации;
— применение Ротарикса следует отложить в случае диареи или рвоты.
Применение при беременности и кормлении грудью
Вакцина Ротарикс не предназначена для применения у взрослых. Данные о применении вакцины у беременных и кормящих женщин отсутствуют.
Результаты клинических исследований указывают на то, что кормление грудью не приводит к ослаблению иммунной защиты против ротавирусных гастроэнтеритов, индуцированной вакциной Ротарикс. Таким образом, во время курса вакцинации грудное вскармливание возможно.
Особые указания
В соответствии со стандартами надлежащей клинической практики перед вакцинацией следует изучить анамнез ребенка, особенно в отношении наличия противопоказаний, и провести осмотр.
Данных по безопасности и эффективности применения вакцины Ротарикс у детей с заболеваниями ЖКТ или замедленным ростом нет. Решение о применении вакцины Ротарикс у таких детей должно приниматься с осторожностью, если, по мнению врача, отказ от вакцинации сопряжен с большим риском для ребенка.
В клинических исследованиях было продемонстрировано отсутствие повышенного риска возникновения кишечной непроходимости в группах, принимавших Ротарикс, по сравнению с группами плацебо.
Однако данные пострегистрационного наблюдения за безопасностью свидетельствуют о небольшом увеличении частоты возникновения кишечной непроходимости в 31-дневный период (преимущественно в течение 7 дней) после введения первой дозы вакцины.
В качестве меры предосторожности необходимо отслеживать симптомы, свидетельствующие о кишечной непроходимости (сильная боль в животе, непрекращающаяся рвота, кровянистый стул, вздутие живота и/или сильная лихорадка). Родителей необходимо просить сообщать о данных симптомах незамедлительно.
Нет оснований полагать, что ВИЧ-инфекции без симптомов или с симптомами легкой степени тяжести оказывают влияние на безопасность и эффективность вакцины Ротарикс. Клиническое исследование с участием ВИЧ-положительных детей с бессимптомным течением ВИЧ или с симптомами легкой степени тяжести не выявило явных проблем безопасности.
Назначение вакцины Ротарикс у детей с установленной или подозреваемой иммуносупрессией должно осуществляться с осторожностью после тщательной оценки соотношения пользы и риска. Выделение вакцинного вируса после вакцинации происходит с каловыми массами и достигает максимальных значений приблизительно на 7-й день после вакцинации. Вирусные частицы антигена, выявленные с помощью иммуноферментного анализа, обнаруживались в каловых массах 50% лиц, которые получили первую дозу вакцины и у 4% — после второй дозы вакцины. Анализ каловых масс показал, что живой вакцинный вирус присутствовал только в 17% случаев. В клинических исследованиях наблюдались случаи передачи вируса вакцины с каловыми массами серонегативным лицам, но эти случаи не приводили к возникновению клинических симптомов.
Ротарикс следует с осторожностью вводить лицам, находящимся в тесном контакте с пациентами с иммуносупрессией вследствие злокачественных новообразований, или других причин, или получающими иммуносупрессивную терапию.
При контактах с недавно вакцинированными против ротавирусной инфекции следует соблюдать личную гигиену (включая мытье рук после замены детских подгузников). Необходимо учитывать потенциальный риск апноэ и необходимость мониторинга дыхательной функции в течение 48-72 ч при проведении курса первичной вакцинации детей, родившихся преждевременно (≤28 недель гестации) и, особенно, детей с указаниями на незрелость респираторной системы. Ввиду высокой пользы вакцинации у детей данной группы, вакцинацию нельзя откладывать или отказывать в ее проведении. Защитный иммунный ответ может формироваться не у всех вакцинированных.
Возможность защитного действия вакцины Ротарикс в отношении штаммов ротавируса, не циркулировавших при проведении клинических исследований, в настоящее время неизвестна. Клинические исследования, в ходе которых были получены данные по эффективности, проводились в Европе, Центральной и Южной Америке и в Африке. Вакцина Ротарикс не защищает от гастроэнтерита, вызванного возбудителями, отличными от ротавируса.
Данных об использовании вакцины Ротарикс для постконтактной профилактики не получено.
Вакцину Ротарикс ни при каких обстоятельствах нельзя вводить парентерально!
Вакцина содержит сахарозу и сорбитол в качестве вспомогательных компонентов, поэтому вакцину не следует принимать пациентам с редкими наследственными заболеваниями непереносимости фруктозы, мальабсорбции глюкозы и галактозы, а также недостаточностью сахаразы-изомальтазы.
Влияние на способность управлять автомобилем или движущимися механизмами
Не применимо.
Лекарственное взаимодействие
Ротарикс можно принимать в сочетании с любой из следующих моно- или поливалентных вакцин [включая комбинированные вакцины (АаКДС-ГепВ-ИПВ/Хиб)]: дифтериино-столбнячная цельноклеточная коклюшная вакцина (АцКДС), дифтерийно-столбнячная бесклеточная коклюшная вакцина (АаКДС), вакцина для профилактики инфекции, вызываемой Haemophilus influenzae тип b (Хиб), вакцина для профилактики полиомиелита инактивированная (ИПВ), вакцина для профилактики гепатита В, пневмококковая конъюгированная вакцина и вакцина менингококковая серогруппы С конъюгированная. Клинические исследования показали, что иммунный ответ и профиль безопасности введенных вакцин не изменялись при одновременном введении.
Одновременное применение вакцины Ротарикс и оральной вакцины для профилактики полиомиелита (ОПВ) не влияет на иммунный ответ на антигены вируса полиомиелита. Хотя одновременное применение с ОПВ может незначительно снизить иммунный ответ на ротавирусную вакцину, в клиническом исследовании, включавшем более 4200 лиц, получивших Ротарикс одновременно с ОПВ, было продемонстрировано, что клиническая зашита против тяжелых ротавирусных гастроэнтеритов поддерживается на должном уровне.
Не предусмотрено ограничений, связанных с приемом пищи или жидкости ребенком ни до, ни после вакцинации.
Условия хранения препарата
Восстановленную вакцину применять сразу после приготовления, допускается хранить при температуре от 2°С до 8°С в течение не более 24 ч. Не замораживать. Хранить вакцину в оригинальной упаковке во избежание воздействия света.
Вакцина в комплекте с растворителем — 36 месяцев при температуре от 2°С до 8°С. Не замораживать.
Срок годности препарата
Восстановленную вакцину применять сразу после приготовления, допускается хранить при температуре от 2°С до 8°С в течение не более 24 ч. Не замораживать. Хранить вакцину в оригинальной упаковке во избежание воздействия света.
Вакцина в комплекте с растворителем — 36 месяцев при температуре от 2°С до 8°С. Не замораживать.
РОТАРИКС ™ — это моновалентная вакцина для профилактики ротавирусного гастроэнтерита, которая содержит живой ослабленный вирус, полученный из штамма ротавируса человека.
РОТАРИКС ™ соответствует требованиям Всемирной организации здравоохранения для биологических веществ и для вакцин против ротавирусной инфекции.
1 доза (1,5 мл) содержит
Действующее вещество : ротавирус человека, живой атенуйованих штамм RIX4414 * не менее
10 6,0 ТЦД 50.
* — выращенный на культуре клеток Vero.
Вспомогательные вещества: сахароза (1,073 г), натрия адипат (132,74 мг), модифицированное среду Игла-Дюльбекко (DMEM) (2,26 мг), вода для инъекций (до 1,5 мл).
В вакцине РОТАРИКС ™ могут присутствовать в остаточной количества следы свиного цирковирус, тип 1 (PCV-1). Данные о возможности PCV-1 вызывать болезнь у животных и инфицировать или вызывать болезни у человека отсутствуют. Свидетельств того, что наличие PCV-1 представляет риск по безопасности применения, нет.
Противовирусные вакцины. Вакцина для профилактики ротавирусной инфекции, живая атенуйованих
Фармакологические
Защитная эффективность
Были проведены клинические исследования в Европе и Латинской Америке, Африке и Азии для оценки защитной эффективности вакцины РОТАРИКС ™ против всех, в том числе тяжких вирусных гастроэнтеритов.
Тяжесть гастроэнтерита была определена согласно двум разным критериям:
- по 20-балльной шкале Весикари, которая оценивает полную клиническую картину ротавирусного гастроэнтерита, учитывая тяжесть и продолжительность диареи и рвоты, тяжесть лихорадки и обезвоживания, а также необходимость лечения
или
- определение клинических случаев базировалось на условиях Всемирной организации здравоохранения (ВОЗ).
Защитная эффективность вакцины по результатам исследований, проведенных в Европе и Латинской Америке
По результатам исследований, проведенных в Европе и Латинской Америке, после применения двух доз РОТАРИКС ™ защитная эффективность вакцины сохранялась в течение первого и второго года жизни ребенка, как показано в таблицах 1 и 2.
Таблица 1. Исследование, проведенное в Европе: 1-й и 2-й годы жизни вместе ( РОТАРИКС ™ N = 2572; плацебо N = 1302 *
| генотип | Эффективность вакцины (%) против любых и тяжелых вирусных гастроэнтеритов [95% ДИ] | |
| Ротавирусный гастроэнтерит любой тяжести | Тяжелый Ротавирусный гастроэнтерит ** | |
| G1P [8] |
89,5 [82,5; 94,1] |
96,4 [90,4; 99,1] |
| G2P [4] |
58,3 [10,1; 81,0] |
85,5 [24,0; 98,5] |
| G3P [8] |
84,8 [41,0; 97,3] |
93,7 [52,8; 99,9] |
| G4P [8] |
83,1 [55,6; 94,5] |
95,4 [68,3; 99,9] |
| G9P [8] |
72,5 [58,6; 82,0] |
84,7 [71,0; 92,4] |
| Штаммы генотипа P [8] |
81,8 [75,8; 86,5] |
91,9 [86,8; 95,3] |
| Циркулирующие штаммы ротавируса |
78,9 [72,7; 83,8] |
90,4 [85,1; 94,1] |
|
Эффективность вакцины (%) по отношению к вирусных гастроэнтеритов, нуждающихся в медицинской помощи [95% ДИ] |
||
| Циркулирующие штаммы ротавируса |
83,8 [76,8; 88,9] |
|
|
Эффективность вакцины (%) по частоте госпитализаций при вирусных гастроэнтеритах [95% ДИ] |
||
| Циркулирующие штаммы ротавируса |
96,0 [83,8; 99,5] |
Примечания:
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
ДИ — доверительный интервал.
Таблица 2. Исследование, проведенное в Латинской Америке: 1-й и 2-й годы жизни вместе
( РОТАРИКС ™ N = 7205; плацебо N = 7081 *
| генотип | Эффективность вакцины (%) против тяжелого ротавирусниого гастроэнтерита ** [95% ДИ] |
| Все ротавирусная гастроэнтериты |
80,5 [71,3; 87,1] |
| G1P [8] |
82,1 [64,6; 91,9] |
| G3P [8] |
78,9 [24,5; 96,1] |
| G4P [8] |
61,8 [4,1; 86,5] |
| G9P [8] |
86,6 [73,0; 94,1] |
| Штаммы генотипа P [8] |
82,2 [73,0; 88,6] |
Примечания:
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
ДИ — доверительный интервал.
Эффективность вакцины против тяжелых вирусных гастроэнтеритов составила 38,6% (95% ДИ: <0,0; 84,2) для штамма G2P [4]. Количество случаев, на основе которых оценивалась эффективность вакцины по отношению к G2P [4], была очень низкой.
В совокупном анализе данных 4 исследований по изучению эффективности вакцины было показано, что эффективность вакцины против тяжелых гастроэнтеритов (≥ 11 баллов по шкале Весикари), вызванных ротавирусом штамма G2P [4], составляет 71,4% (95% ДИ: 20,1 ; 91,1).
Защитная эффективность вакцины по результатам исследования, проведенного в Африке
В Африке было проведено клиническое исследование с участием более 4900 пациентов, в котором оценивалась вакцина РОТАРИКС ™ , которая предназначена примерно на 10 и 14-й неделе жизни (2 дозы) или на 6, 10 и 14-й неделе жизни (3 дозы). Эффективность вакцины против тяжелых вирусных гастроэнтеритов в течение первого года жизни ребенка составляла 61,2% (95% ДИ: 44,0; 73,2). Исследование было недостаточно, чтобы можно было оценить разницу между эффективностью двух схем применения вакцины — двух и трех доз.
Данные, которые показывают защитную эффективность вакцины против любых и тяжелых вирусных гастроэнтеритов, приведены в таблице 3.
Таблица 3. Исследование, проведенное в Африке: 1-й год жизни — обобщенные данные ( РОТАРИКС ™ N = 2974; плацебо N = 1443 *
| генотип | Эффективность вакцины (%) против всех вирусных гастроэнтеритов [95% ДИ] | |
| Ротавирусный гастроэнтерит любой тяжести | Тяжелый Ротавирусный гастроэнтерит ** | |
| G1P [8] |
68,3 (53,6; 78,5) |
56,6 (11,8; 78,8) |
| G2P [4] |
49,3 (4,6; 73,0) |
83,8 (9,6; 98,4) |
| G3P [8] |
43,4 * (<0; 83,7) |
51,5 *** (<0; 96,5) |
| G8P [4] |
38,7 * (<0; 67,8) |
63,6 (5,9; 86,5) |
| G9P [8] |
41,8 * (<0; 72,3) |
56,9 *** (<0; 85,5) |
| G12P [6] |
48,0 (9,7; 70,0) |
55,5 *** (<0; 82,2) |
| Штаммы генотипа P [4] |
39,3 (7,7; 59,9) |
70,9 (37,5; 87,0) |
| Штаммы генотипа P [6] |
46,6 (9,4; 68,4) |
55,2 *** (<0; 81,3) |
| Штаммы генотипа P [8] |
61,0 (47,3; 71,2) |
59,1 (32,8; 75,3) |
Примечание:
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
*** Не являются статистически достоверным (р ≥ 0,05). Эти значения должны быть интерпретированы с осторожностью.
ДИ — доверительный интервал.
Продолжительность защитной эффективности вакцины у детей до 3 лет, по результатам исследования, проведенного в Азии
Клиническое исследование, проведенное в Азии (Гонконг, Сингапур и Тайвань) с участием более 10000 пациентов, получавших вакцину РОТАРИКС ™ по различным графику (2, 4 месяца жизни, 3, 4 месяца жизни). После двух доз РОТАРИКС ™ защитная эффективность вакцины наблюдалась до 3 лет жизни (см. Табл. 4).
Таблица 4. Исследование, проведенное в Азии: эффективность до двух и трех лет ( РОТАРИКС ™ N = 5263; плацебо N = 5256 *)
| генотип |
эффективность вакцины до 2 лет |
эффективность вакцины до 3 лет |
| Эффективность вакцины (%) против всех вирусных гастроэнтеритов [95% ДИ] | ||
| Тяжелые ротавирусная гастроэнтериты ** | Тяжелый Ротавирусный гастроэнтерит ** | |
| G1P [8] |
100,0 (80,8; 100,0) |
100,0 (84,8; 100,0) |
| G2P [4] |
100,0 * (<; 100,0) |
100,0 *** (<; 100,0) |
| G3P [8] |
94,5 (64,9; 99,9) |
95,2 (70,4; 99,9) |
| G9P [8] |
91,7 (43,8; 99,8) |
91,7 (43,8; 99,8) |
| Штаммы генотипа P [8] |
95,8 (83,8; 99,5) |
96,6 (87,0; 99,6) |
| Циркулирующие штаммы ротавируса |
96,1 (85,1; 99,5) |
96,9 (88,3; 99,6) |
|
Эффективность вакцины (%) по вирусных гастроэнтеритов по отношению к частоте госпитализаций и / или регидратационной терапии в медицинских учреждениях [95% ДИ] |
||
| Циркулирующие штаммы ротавируса |
94,2 (82,2; 98,8) |
95,5 (86,4; 99,1) |
Примечание:
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
*** Не являются статистически достоверным (р ≥ 0,05). Эти значения должны быть интерпретированы с осторожностью.
ДИ — доверительный интервал.
иммунный ответ
В клинических исследованиях, проводившихся в Европе, Латинской Америке и Азии, 1957 младенцев получили по разным графикам прививки лиофилизированную вакцину РОТАРИКС ™ и 1006 младенцев — плацебо. Доля пациентов, которые до прививки были серонегативными к ротавируса (титры антител IgA <20 Ед / мл (ELISA)), с титром антиротавирусних IgA в сыворотке ³ 20 Ед / мл через 1 или 2 месяца после введения второй дозы вакцины или плацебо составляла от 77 9% до 100% и от 0% до 17,1% соответственно.
Иммунный ответ на введение вакцины РОТАРИКС ™ в форме суспензии по данным 3-х сравнительных исследований аналогична иммунного ответа на введение вакцины в форме лиофилизированного порошка.
В клиническом исследовании, проведенном в Африке, иммунный ответ оценивалась в 332 младенцев, получивших вакцину РОТАРИКС ™ (N = 221) или плацебо (N = 111) по графику прививки в 10 и 14 недель (2 дозы) или в 6, 10 и 14 недель (3 дозы). Доля пациентов, которые до прививки были серонегативными к ротавируса (титры антител IgA <20 Ед / мл (ELISA)), с сывороточными титрами антиротавирусних антител IgA ³ 20 Ед / мл через 1 месяц после введения последней дозы вакцины или плацебо составила 58,4% (объединенные данные для обоих режимов прививки) и 22,5%, соответственно.
Иммунный ответ у недоношенных младенцев
По данным клинических исследований после иммунизации недоношенных младенцев вакциной РОТАРИКС ™ в лиофилизированной форме в 85,7% вакцинированных достигался титр антиротавирусного IgA в сыворотке ≥ 20 Ед / мл (ELISA) через 1 месяц после введения второй дозы вакцины.
Безопасность вакцины у младенцев, инфицированных вирусом иммунодефицита человека (ВИЧ)
В клиническом исследовании 100 младенцев с ВИЧ-инфекцией получили лиофилизированную вакцину РОТАРИКС ™ или плацебо. Профиль безопасности для вакцины РОТАРИКС ™ и плацебо был подобным.
Выделение вакцинного вируса
После прививки встречается выделение вакцинного вируса с фекалиями, которое длится в среднем в течение 10 дней с максимальной экскреции вируса примерно на 7-й день после вакцинации. Наличие вирусных антигенов, обнаруженная по результатам ELISA, определялась в 50% образцов фекалий после введения первой дозы вакцины и в 4% образцов — после введения второй дозы. При тестировании этих образцов фекалий на наличие живого вакцинного вируса 17% из них были положительными.
В двух сравнительных контрольных исследованиях выделение вакцинного вируса после применения жидкой вакцины РОТАРИКС ™ было подобным тому, которое наблюдалось после применения лиофилизированной вакцины РОТАРИКС ™ .
эффективность
В таблице 5 продемонстрированы результаты нескольких исследований, проведенных по методу случай-контроль для оценки эффективности препарата РОТАРИКС ™ против тяжелого гастроэнтерита, вызванного ротавирусом, что привело к госпитализации.
Таблица 5. Эффективность против тяжелого гастроэнтерита, вызванного ротавирусом, что привело к госпитализации
| страны | Возраст (лет) |
Количество привитых двумя дозами (N) (Случаи / контроль) |
штамм |
Эффективность, рассчитанная по госпитализированными ротавирус-негативными пациентами, (%) [95% ДИ] |
Продолжительность периода наблюдения |
| Исследование, спонсором которых была компания «ГСК» | |||||
| Бельгия | <4 | 215/276 |
все G1P [8] G2P [4] |
90 [81; 95] 95 [78; 99] 85 [64; 94] |
2,4 года |
| Бразилия | <3 | 249/249 |
все G2P [4] |
76 [58; 86] 75 [57; 86] |
1 год |
| Сингапур | <5 | 136/272 |
все G1P [8] |
84 [32; 96] 91 [30; 99] |
2 года |
| другие исследования | |||||
| Эль-Сальвадор | <2 | 152/617 | все | 76 [64; 84] * | 2,5 года |
| Австралия | <1 | 21/84 | G2P [4] | 85 [16; 97] ** | 10 месяцев |
Примечание:
* У пациентов. не прошедшие полный курс вакцинации, эффективность после одной дозы составляла 51% (95% ДИ: 26; 67).
** Статистически значимая эффективность может быть продемонстрирована только для детей <1 года с гастроэнтеритом, вызванным ротавирусом и осложненным ацидозом.
ДИ — доверительный интервал.
Влияние на смертность 1
Исследование влияния препарата РОТАРИКС ™ , проведенные в Панаме, Бразилии и Мексике, продемонстрировали снижение смертности из-за диареи по всем причинам с диапазоном 22% -56% у детей в возрасте до 5 лет, в течение 2-3 лет после введения вакцины.
Влияние на госпитализацию 1
В ретроспективном исследовании базы данных в Бельгии, проведенном среди детей 5 лет и младше, прямое и косвенное влияние вакцинации препаратом РОТАРИКС ™ на связанную с ротавирусом госпитализацию имел диапазон от 64% (95% ДИ: 49; 76) до 80% ( 95% ДИ: 77; 83) через два года после введения вакцины. Подобные исследования в Бразилии, Австралии и Эль-Сальвадоре продемонстрировали снижение соответственно на 59%, 75% и 81%. Кроме того, три исследования влияния на госпитализацию из-за диареи из всех причин, проведенные в Латинской Америке, продемонстрировали снижение на 29% -37% через два года после введения вакцины.
Примечание :
1 — исследование влияния означают установление временного взаимосвязи, а не причинно-следственной связи между болезнью и вакцинацией.
Фармакокинетика
Оценка фармакокинетических свойств не является обязательной для вакцин.
Вакцина РОТАРИКС ™ показана для профилактики гастроэнтерита, вызывается ротавирусом (см. Разделы Особенности применения и Иммунобиологические и биологические свойства).
Прививка детей на территории Украины осуществляется согласно требованиям действующих приказов МЗ Украины.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ:
дозировка
Курс вакцинации состоит из двух доз. Первая доза может быть назначена ребенку, начиная с возраста 6 недель. Интервал между применением первой и второй дозы должен быть не менее 4 недель. Курс вакцинации следует закончить до достижения ребенком возраста 24 недели.
РОТАРИКС ™ может быть назначен по тем же показаниям и недоношенным детям, соблюдая такого же дозировки (см. Разделы « Иммунобиологические и биологические свойства» и «Побочные реакции» ).
По данным клинических исследований срыгивания или сплевывания при применении вакцины наблюдалось очень редко, и в таких случаях повторная доза не вводилась. Однако, в случае, если ребенок извергла или плюнула почти всю дозу, можно однократно заменить эту дозу во время этого же вакцинации.
Настоятельно рекомендуется, чтобы младенцы, которые получили первую дозу вакцины РОТАРИКС ™ , завершили 2-режим дозирования вакцинации препаратом РОТАРИКС ™ .
Вакцина РОТАРИКС ™ предназначена только для перорального применения.
Вакцину РОТАРИКС ™ ни в коем случае нельзя вводить в виде инъекции!
Отсутствуют ограничения на потребление младенцем пищи или жидкости, включая грудное молоко, как до, так и после вакцинации.
По данным, полученным в клинических исследованиях, грудное вскармливание не может уменьшить эффективность вакцины РОТАРИКС ™ . Поэтому в период проведения вакцинации можно продолжать кормить ребенка грудным молоком.
Информация о инструкции приготовления или восстановления следует смотреть в разделе «Техника применения / обращения с препаратом» .
дети
Вакцина РОТАРИКС ™ не должна использоваться у детей старше 24-недельного возраста.
Данные клинических исследований
Для определения частоты возникновения побочных действий применяется следующая классификация.
Очень часто (≥ 1/10)
Часто (≥ 1/100 — <1/10)
Нечасто (≥ 1/1000 — <1/100)
Редко (≥ 1/10000 — <1/1000)
Очень редко (<1/10000)
Профиль безопасности вакцины, приведенный ниже, основывается на данных клинических испытаний, проведенных как с лиофилизированной форме вакцины РОТАРИКС ™ , так и в форме уже готовой оральной суспензии.
Всего в 4 клинических исследованиях вакцины РОТАРИКС ™ в форме суспензии было иммунизированы 1900 младенцев, которым было введено около 3800 доз вакцины. По данным этих исследований было показано, что профиль безопасности вакцины в форме суспензии является сопоставимым с профилем безопасности вакцины в форме лиофилизированного порошка.
Всего в 23 клинических исследованиях были использованы 106000 доз вакцины РОТАРИКС ™ (в форме лиофилизированного порошка или суспензии) примерно 51000 младенцам
В трех плацебо-контролируемых клинических исследованиях, где РОТАРИКС ™ применялся самостоятельно (назначение других обычных педиатрических вакцин происходило по графику), частота и тяжесть таких ожидаемых симптомов (зарегистрированных в течение 8 дней после вакцинации), как диарея, рвота, потеря аппетита, лихорадка, раздражительность и кашель / насморк существенно не отличались в группе, вакцинировался РОТАРИКС ™ , по сравнению с группой, получавшей плацебо. Не было отмечено увеличение частоты и тяжести этих реакций и после применения второй дозы.
По данным обобщенного анализа 17 плацебо-контролируемых клинических исследований, где РОТАРИКС ™ применялся вместе с другими педиатрическими вакцинами (см. «Взаимодействие с другими медикаментами и другие виды взаимодействий» ), такие побочные действия (зарегистрированы в течение 31 дня после вакцинации), были оценены как быть связано с вакцинацией.
Со стороны желудочно-кишечного тракта
Часто : диарея
Нечасто : метеоризм, боли в животе
Со стороны кожи и подкожных тканей
Нечасто : дерматит
Общие нарушения и нарушения в месте введения
Часто раздражительность
Риск возникновения инвагинации был оценен в большом клиническом исследовании по безопасности применения этой вакцины в Латинской Америке и Финляндии с привлечением 63225 пациентов. По данным этого исследования не было выявлено увеличения риска возникновения инвагинации в группе пациентов, иммунизированных вакциной РОТАРИКС ™ по сравнению с группой плацебо, как показано в таблице ниже.
| Сроки проявления инвагинации |
РОТАРИКС ™ (количество человек) |
плацебо (количество человек) |
Относительный риск (95% ДИ) |
|
инвагинация течение 31 дня после: |
N = 31673 | N = 31552 | |
|
1 | 2 | 0,50 (0,07; 3,80) |
|
5 | 5 | 0.99 (0,31; 3,21) |
|
инвагинация течение первого года жизни: |
N = 10159 | N = 10010 | |
до 1 года |
4 | 14 | 0,28 (0,10; 0,81) |
Примечания:
N — общее количество человек.
ДИ — доверительный интервал.
Безопасность применения вакцины у недоношенных младенцев
В клиническом исследовании 1009 недоношенным младенцам было применено РОТАРИКС ™ в форме лиофилизированного порошка или плацебо (198 младенцев имели 27-30 недель гестации и 801 младенец — 31-36 недель гестации). Первая доза была применена в возрасте 6 недель. Серьезные побочные эффекты наблюдались в 5,1% младенцев, получавших РОТАРИКС ™, по сравнению с 6,8% младенцев, получавших плацебо. Аналогичная частота других побочных эффектов наблюдалась в группе младенцев, получавших РОТАРИКС ™, и в группе, получавшей плацебо. Сообщений о случаях инвагинации не было.
Данные постмаркетингового наблюдения
Со стороны желудочно-кишечного тракта
Редко : инвагинация * (см. «Особенности применения» ), кровянистые испражнения, гастроэнтериты с выделением вакцинного вируса у младенцев с тяжелым комбинированным иммунодефицитом (SCID).
вакцина РОТАРИКС ™ не должна применяться у лиц с повышенной чувствительностью после предыдущего применения вакцины РОТАРИКС ™ или к любому из компонентов вакцины (см. «Качественный и количественный состав» и «Перечень вспомогательных веществ» ).
Вакцина противопоказана лицам с наличием в анамнезе инвагинации.
Вакцина РОТАРИКС ™ не должна применяться у лиц с устраненных врожденным пороком развития желудочно-кишечного тракта (такой, как дивертикул Меккеля), что может быть причиной развития кишечной инвагинации.
Вакцина РОТАРИКС ™ не должна применяться у лиц с SCID (см. «Побочное действие» ).
Вакцина содержит сахарозу. Вакцина противопоказана пациентам с редкими наследственными проблемами непереносимости фруктозы, глюкозо-галактозы мальабсорбцией или сахароза-изомальтозною недостаточностью.
При проведении иммунизации на территории Украины относительно противопоказаний также следует руководствоваться действующими приказами МЗ Украины.
Особенности применения: согласно требованиям медицинской практики вакцинации должно предшествовать рассмотрение анамнеза (особенно того, что касается предыдущей вакцинации и возможных случаев побочного действия) и медицинское обследование.
Как и при применении других вакцин, введение вакцины РОТАРИКС ™ должно быть отложено у лиц с острыми заболеваниями, сопровождающимися лихорадкой. Однако, наличие незначительных инфекций, таких как простуда, не является противопоказанием для проведения иммунизации.
Применение вакцины РОТАРИКС ™ должно быть отложено у лиц, страдающих диареей или рвотой.
Данные о безопасности и эффективности применения вакцины РОТАРИКС ™ у младенцев с заболеваниями желудочно-кишечного тракта отсутствуют. Поэтому применять вакцину РОТАРИКС ™таким младенцам следует с осторожностью, сравнивать риск и пользу от вакцинации.
Риск инвагинации был изучен в большом клиническом исследовании (63225 младенцев), проведенном в Финляндии, Индии и Бангладеш. Увеличение риска возникновения инвагинации после применения вакцины РОТАРИКС ™ по сравнению с плацебо выявлено не было.
Однако, по данным постмаркетиногового исследования по безопасности было выявлено кратковременное увеличение риска инвагинации после вакцинации, главным образом в течение 7 дней после первой дозы вакцины и в меньшей степени, после второй дозиЗагальне снижение количества случаев инвагинации остается по частоте: редко. Влияние применения РОТАРИКС ™ на общий риск возникновения инвагинации не установлен.
Я мера, медицинский персонал в послевакцинальный период должен наблюдать за любым симптомом, указывающим на инвагинацию (тяжелая боль в животе, постоянное рвота, кровянистые испражнения, вздутие живота и / или высокая температура). Родителям или опекунам следует посоветовать быстро сообщать о появлении таких симптомов.
Применение вакцины РОТАРИКС ™ в имуноскомпрометованих младенцев, включая тех, которые находятся на иммуносупрессивной терапии, должно базироваться на тщательном сопоставлении возможной пользы и риска применения вакцины РОТАРИКС ™ .
Как известно, выделение вакцинного вируса с испражнениями появляется после вакцинации и длится в среднем до 10 дней с пиком выделения на 7-й день. По данным клинических исследований наблюдались случаи передачи вакцинного вируса серонегативным контактными лицам, но без появления каких-либо клинических симптомов. РОТАРИКС ™ следует с осторожностью применять лицам, тесно контактируют с пациентами с иммунодефицитом, в частности со злокачественными новообразованиями, или теми, кто получает иммуносупрессивную терапию.
Лица, контактирующие с недавно вакцинированными детьми, должны быть проинформированы о необходимости соблюдения тщательной гигиены (включая мытье рук) после смены подгузников у ребенка.
При проведении первичной иммунизации у недоношенных детей (рожденных ≤ 28 недель беременности) необходим мониторинг дыхания в течение 48-72 часов после прививки через потенциальный риск апноэ.
Как и при применении других вакцин, защитная иммунный ответ может быть получена не у всех вакцинированных детей.
Пока неизвестно, насколько вакцина РОТАРИКС ™ может обеспечивать защиту против штаммов ротавируса, не циркулировали в рамках проводимых клинических исследований.
Вакцина РОТАРИКС ™ не защищает от гастроэнтеритом НЕ ротавирусной этиологии.
Специальные предостережения относительно применения и использования препарата
Вакцина представляет собой прозрачную бесцветную жидкость, свободной от любых посторонних частиц; в оральном аппликаторе или пластиковой тубе, закрытых защитным колпачком. Препарат готов для использования (не требуется его растворения или разведения). Перед применением вакцину необходимо визуально проверить на наличие каких-либо посторонних частиц и / или изменение внешнего вида. В случае, если наблюдается что-либо из вышеперечисленного, вакцину не использовать.
Применение вакцины в оральном аппликаторе и тубе:
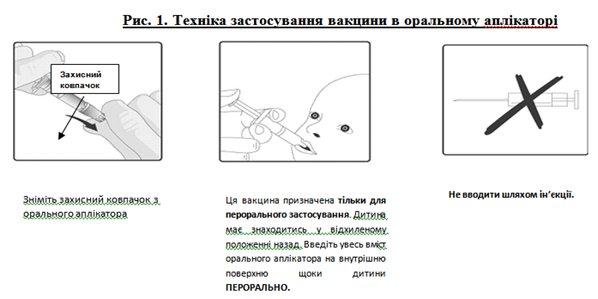
1. Техника применения вакцины в оральном аппликаторе приведена на рис. 1.
2. Техника применения вакцины в тубе приведена на рис. 2.
3. Эта вакцина предназначена только для перорального применения. Ребенка следует держать с отклоненной головой. Введите все содержимое орального аппликатора или тубы пероральный (на внутреннюю поверхность щеки).
4. Не вводить путем инъекции.
несовместимость
Эту вакцину нельзя смешивать с другими лекарственными средствами.
Рис. 1. Техника применения вакцины в оральном аппликаторе
Рис. 2. Техника применения вакцины в тубе
|
A Что вы должны сделать, прежде чем вводить РОТАРИКС ™
Если вы заметили что-нибудь необычное, не используйте вакцину.
|
|
|
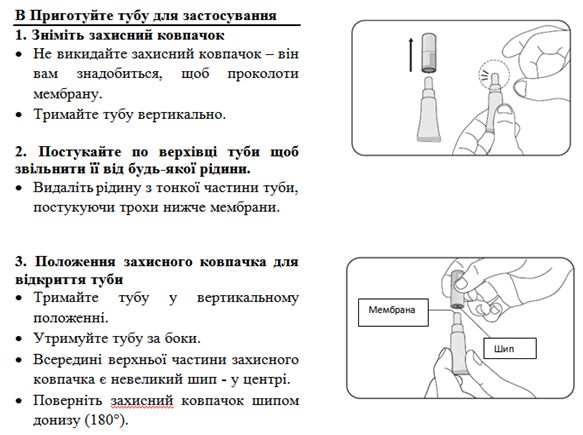
B Приготовьте тубу для применения 1. Снимите защитный колпачок
2. Постучите по верхушке тубы до тех пор, пока она будет свободной от любой жидкости.
|

|
3. Положения защитного колпачка, чтобы открыть тубу
|
|
|
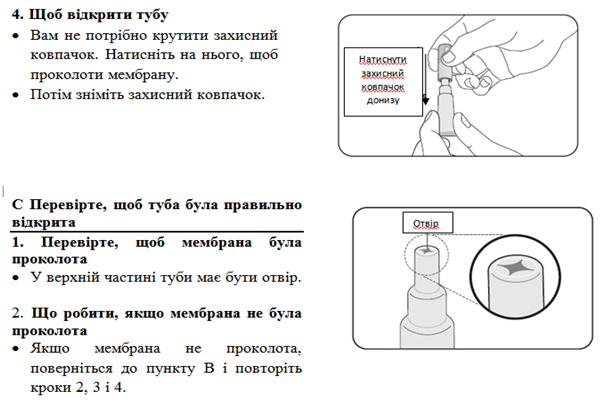
C Проверьте, чтобы туба была правильно открыта 1. Проверьте, чтобы мембрана была проколота
2. Что делать, если мембрана ни была проколота
|
|
D Введите вакцину
Если вы заметили что-нибудь необычное, не используйте вакцину.
1. Правильно посадите ребенка, чтобы ввести вакцину
2. Введите вакцину
|
Только для перорального применения
|
ВЗАИМОДЕЙСТВИЕ с другими медикаментами и другие виды взаимодействий: Вакцину РОТАРИКС ™ можно применять в сочетании с любым из следующих как моновалентных, так и комбинированных вакцин, включая гексавалентный вакцину DTPa-HBV-IPV / Hib — вакцину для профилактики дифтерии, столбняка, коклюша ( бесклеточную), гепатита В, полиомиелита и заболеваний, вызываемых Haemophilus influenzae типа b (Hib) вакцину для профилактики дифтерии, столбняка и коклюша (цельноклеточным) (DTPw), вакцину для профилактики дифтерии, столбняка и коклюша (бесклеточную) (DTPa), вакцину для профилактики заболеваний, вызываемых Hib, инактивированную вакцину для профилактики полиомиелита (IPV), вакцину для профилактики гепатита В (HBV), конъюгированные вакцины для профилактики пневмококковой инфекции и кон`юговану вакцину для профилактики заболеваний, вызываемых менингококками серогруппы С. Результаты исследований показали, что одновременное введение этих вакцин не влияло на их иммун огеннисть и безопасность.
Одновременное применение РОТАРИКС ™ и пероральной вакцины для профилактики полиомиелита (OPV) не оказало влияния на иммунный ответ к полиовирусов. Хотя совместное применение OPV вакцины может в небольшой степени уменьшать иммунный ответ ротавирусной вакцине, клинический защиту против тяжелых гастроэнтеритов, вызванных ротавирусами, сохраняется.
Применение в период беременности или кормления грудью.
Вакцина РОТАРИКС ™ не предназначена для применения у взрослых. Поэтому данные по применению вакцины у женщин во время беременности или кормления грудью отсутствуют, а исследования по изучению влияния на репродуктивную функцию у животных не проводились.
Вакцина РОТАРИКС ™ не предназначена для применения у взрослых.
вакцину следует хранить при температуре от 2 до 8 ° C (в холодильнике). Не замораживать. Хранить в оригинальной упаковке, чтобы защитить от света. Хранить в недоступном для детей месте.
При применении вакцины РОТАРИКС ™ не следует смешивать с другими лекарственными средствами.
3 года. Дата окончания срока годности вакцины указана на этикетке и на упаковке.
По 1 дозе (1,5 мл) вакцины в предварительно заполненном оральном аппликаторе из стекла типа I (Евр.Ф.) с защитным колпачком или пластиковой тубе с колпачком.
Оральный аппликатор или тубу вместе с инструкцией по применению вкладывают в картонную коробку. Размер упаковки: по 1; 5 предварительно заполненных оральных аппликаторов или туб.
Вакцина Ротарикс создана для профилактики ротавирусной инфекции — опасного заболевания, которое передаётся бытовым путём, через руки и быстро распространяется. У пациента начинаются приступы рвоты, поднимается температура, наблюдается диарея в течение нескольких суток. Кроме того, у заболевших людей проявляются симптомы похожие на простуду: ринит, краснеет горло, затруднено глотание.

Ротавирусная инфекция
Это инфекционное заболевание, которое нарушает работу желудочно-кишечного тракта. В группу риска входят дети. Проникающий в организме вирус снижает иммунную защиту, провоцирует рвоту и тошноту, диарею. Во время болезни температура тела пациента повышается до 39 градусов. Врачами не разработана универсальная схема лечения, оно направлено на подавление наиболее агрессивных признаков болезни.
Заражение происходит фекально-оральным путём, через предметы обихода, грязные руки. Во время лечения пациенту необходимо соблюдать постельный режим, принимать прописанные врачами лекарства. При своевременном лечении прогноз благоприятный и человек выздоравливает за 7–10 дней.
Для грудничков характерна тяжёлая и среднетяжелая форма болезни с быстрым обезвоживанием и потерей массы тела:
- При лёгкой форме патологии ребёнок плохо ест, вял, раздражён. У него повышается температура до 37,5 градусов. После еды грудничка рвёт, появляется диарея;
- При средней тяжести болезни температура может подниматься до 38 градусов, начинается срыгивание, рвота. Дефекация происходит до семи раз в сутки. Расстройство стула до трех суток;
- Для тяжёлой формы ротавирусной инфекции характерна рвота до 15 раз в сутки. Это провоцирует серьёзное обезвоживание, которое угрожает жизни и здоровью ребёнка. Слизистые оболочки становятся сухими. Средняя продолжительность выздоровления при соответствующем лечении достигает 10 дней.

Лечение грудничка ведётся по нескольким направлениям:
- Восполнение потерянной влаги. Для этого ребёнку дают много пить, используют Регидрон и другие балансирующие растворы, которые останавливают потерю влаги;
- Восстановление микрофлоры с помощью пробиотиков, содержащих лакто- и бифидобактерии в своём составе;
- Понижение температуры. Для этого используют ректальные свечи. Дозировка и препарат подбирается врачом.
Но самым адекватным средством от ротавирусной инфекции это его профилактика с помощью вакцин. Такая процедура позволяет уменьшить риск заражения инфекцией. Если заболеет, то форма ее будет лёгкой, в сравнении с детьми, которые не прошли эту процедуру.
Подробнее о Ротариксе
Ротарикс вакцина является продуктом английских фармакологов. Она выпускается в форме прозрачной суспензии. Своевременное вакцинирование лекарством помогает уменьшить негативные последствия ротавируса на организм и формирует стойкую иммунную защиту внутри кишечника.
Вакцинированный пациент в дальнейшем минимизирует риск заражения не только ротавирусом, но и другими кишечными инфекциями. Эту вакцину используют в профилактических целях больше, чем в 100 странах мира. Врачи отмечают её хорошую переносимость, минимальное количество побочных эффектов и возможность одновременного приёма с другими препаратами.
В состав Ротарикса входят несколько разновидностей возбудителя, вода, сахароза и другие компоненты. Ротарикс фасуется в тубу или аппликатор, в которых содержится разовая дозировка препарата. В коробку препарата укладывают от 5 до 100 единиц вакцины.
Показания
Ротарикс применяется в профилактике для уменьшения риска гастроэнтеритов. Оно предназначено для грудничков от полутора месяцев до полугода. В этот период заражение ротавирусом наиболее опасно, так как у грудничков организм быстро теряет воду, что может привести к смерти младенца.

Rotarix вакцина предназначена для приёма внутрь и не используется для прививок. Во время вакцинации схема питание ребёнка не меняется. Грудное вскармливание материнским молоком не снижает эффективность формирования иммунной защиты, поэтому при приёме ротарикса кормление не отменяют.
Противопоказания
Вакцину Ротарикс не рекомендуется применять для прививания грудничков, которые склонны к аллергиям, чувствительны к составляющим лекарства или имеют недоразвитый желудочно-кишечный тракт из-за врождённой аномалии.
Пояснения к использованию лекарства
Если вам непонятно, как подготовить содержимое флакона ротарикс, то инструкции по применению не рекомендует смешивать Ротарикс с другими медикаментами в одном шприце.
Иногда можно заметить осадок в шприце, если хранить его с растворителем. Лекарство встряхивают, смотрят, чтобы в жидкости не было инородных частиц. Если лекарство содержит хлопья, то его не следует использовать. ПопулярноПрофилактические меры с вакциной от гриппа Ультрикс
Как подготовить лекарство
Крышка из пластика снимается с флакона с лиофилизатом, потом на него крепится адаптер так, чтобы произошло чёткое сцепление с емкостью.
После этого шприц с содержимым интенсивно встряхивается до тех пор, пока жидкость не превратится в однородную массу. После этого колпачок снимается со шприца и кончик его соединяется с адаптером. Жидкость из шприца переливается во флакон с лиофилизатом. Флакон повторно встряхивается и переливается в шприц, потом адаптер отсоединяют.
Как применять вакцину
Для вакцинации Ротариксом голова ребёнка немного наклоняется, содержимое ёмкости заливается в рот. При этом врач должен целиться на слизистую оболочку щеки. Препарат не применяется в виде инъекций. Курс лекарства — это две дозы препарата.
Первый раз вакцинация проводится грудничкам с полутора месяцев, потом делается перерыв и вводится 2-я доза. Закончить вакцинацию нужно не позднее, чем ребёнку исполнится 6 месяцев.
Нельзя вводить сразу двойную дозировку лекарства. В случае, если младенец срыгнул и всё лекарственное средство вышло наружу, тогда вакцинация производится повторно. Это делается только при полной уверенности того, что лекарство вышло наружу.

Дети в возрасте от полутора до шести месяцев наиболее склонны к заражению ротавирусом. При возникновении заболевания у них могут наблюдаться конъюнктивит, ринит, увеличение температуры. Такие груднички становятся вялыми, плохо едят, возникает диарея, частые срыгивания, болит живот.
Особую опасность для маленького ребёнка представляет обезвоживание от потери воды из-за срыгивания, диареи. Нарушение водно-солевого баланса губительно влияет на мозг и может даже приводить к гибели грудничка.
Ротарикс не применяют детям в возрасте 12 месяцев, потому что у них начинают формироваться кишечная микрофлора, что снижает риск возникновения инфекции.
Как подготовиться к вакцинации
Применение Ротарикс не предусматривает специальных мероприятий по подготовке к вакцинации, но необходимо посетить врача и получить его заключение о состоянии ребёнка. Это делают перед любой прививкой или вакцинировании. Родители должны предупредить врача, если у ребёнка есть непереносимость каких-либо лекарственных средств или заболевания.
Приём лекарства запрещён, если у ребёнка повышена температура, есть заболевания дыхательной системы (ОРВИ, ОРЗ), нарушение стула. Не рекомендуется вводить лекарство, если у ребенка рвота. Необходим полный отказ от вакцинации. Проведение процедуры просто откладывается до полного выздоровления. Во время применения ротарикс не следует переводить ребёнка на искусственное питание, если мать кормит его грудью.

Как происходит взаимодействие с другими препаратами? Ротарикс можно использовать одновременно с прививками от гепатита, коклюша, полиомиелита и т. д. При этом лекарства нельзя смешивать. Одновременное проведение процедур по вакцинации от полиомиелита пероральное лекарство и против ротавирусной инфекции может ухудшать в формировании иммунитета от вируса.
Побочные эффекты
После проведения вакцинации возможен метеоризм, колики в животе, кожная сыпь. Перед проведением вакцинации необходимо убедиться в том, что ребёнок не болеет, у него не повышена температура. Врач проводит осмотр ребенка и выносит вердикт о его состоянии.
Дети с нарушениями работы пищеварительного тракта вакцинируют с особой осторожностью, потому что производителем не проводились специальные исследования о безопасности препарата в этом случае.
Существует вероятность сохранение в каловых массах вакцинированного ребенка составляющих вакцины, поэтому есть риск заражения людей, контактирующим с младенцем. Поэтому людям, имеющим проблемы с иммунитетом, онкологию, аутоиммунные заболевания следует проявлять особую осторожность и бдительность при уходе за такими детьми.
Родителям и лицам, осуществляющим уход за ребёнком, которому введён Ротарикс, следует тщательно мыть руки после контакта с каловыми массами, при смене подгузника.
Перед тем как применять Ротарикс необходимо посмотреть упаковку на повреждение. Раствор должен быть полностью прозрачным и не содержать хлопьев, осадка, примеси. Препарат не предназначен для вакцинирования взрослых пациентов используется только для детей в возрасте до полугода. ПопулярноМенингококковая инфекция у детей побеждена Менактрой
Совместимость с другими лекарственными средствами
По данным медицинских исследований, выявлено, что Ротарикс можно сочетать с лекарствами, подавляющими менингококки, дифтерию, гепатит, полиемиелит, коклюш и другие заболевания. При одновременном использовании иммунный ответ не ухудшается, он формируется в полной мере.

При одновременном применении этого препарата вместе с OPV-вакциной врачи отмечают снижение иммунной защиты на лекарство, но защита сохраняется. При приёме Ротарикса врачи рекомендуют временно отказаться от других лекарств, потому что вакцина с ними несовместима.
Аналоги лекарства
Единственным лекарством, которое полностью идентично по воздействию и составу является голландская вакцина Ротатек. Она состоит из компонентов вирусов, которые получены из бычьего и человеческого штаммов.
Это лекарство используется во многих странах в профилактических целях для защиты детей от ротавируса с 2006 года. Её можно применять для детей в возрасте от полутора месяцев. Ротатек хорошо комбинируется с другими вакцинами.
За 10 лет врачи отметили уменьшение заболеваемости детей ротавирусной инфекцией в два раза. Ряд врачей уверены, что применение этого лекарство способно усугубить течение болезни в некоторых случаях.
Его используют в качестве профилактики для детей в возрасте от 1,5 месяцев до полугода. Для формирования полноценной иммунной защиты пациенту следует вводить 3 дозы лекарственного средства. Метод введения такой же, как и Ротарикса. Эффективность лекарства аналогична.
Отзывы
Ротарикс предназначен для профилактики ротавируса у детей и включено в календарь прививок для обязательного вакцинирования этой группы больных. Но родитель может поставить её самостоятельно. В среднем, цена лекарства в аптечных сетях колеблется от 900 до 1100 рублей за одну дозу.
Многие родители, которые проводили вакцинирование самостоятельно, положительно отзываются о препарате. Они отмечают, что хотя такое вакцинирование не обязательно, но они не пожалели о своём решении провести профилактику ротавируса.

Большинство родителей говорят, что у их детей не было побочных эффектов после приёма вакцины. Некоторые отмечают, что после неё, даже, когда ротавирусной инфекцией заболели взрослые, у ребёнка не было замечено ни одного симптома грозной болезни. У него не поднялась температура, не было диареи и рвоты, не появилась ломота в мышцах.
Реже дети болеют им в лёгкой форме. Тяжёлая форма вируса у них не развивается. Лишь некоторые родители отметили после приёма лекарственного средства побочные эффекты в виде вздутия живота и кожной сыпи.
Как себя вести после вакцинирования
После того, как процедура проведена, стоит отметить, что rotarix вакцина начинает «работать» не сразу. В течение нескольких дней педиатры рекомендуют тщательно соблюдать гигиену:
- Родители должны следить, чтобы ребёнок после улицы или посещения общественных мест тщательно мыл руки;
- Во время смены подгузника и при общении с ребёнком, после вакцинирования родители тоже должны часто мыть руки;
- Уборка детской проводится несколько раз в день;
- Через несколько дней после приёма Ротарикса у ребёнка формируется иммунитет и потенциальная угроза заболеть у ребенка значительно уменьшается.
Применение во время лактации и беременности
Ротарикс не предназначен для проведения профилактики у беременных женщин, поэтому в инструкции по применению нет данных относительно вредного воздействия.
Кормление грудью во время проведения вакцинации младенца не прекращают. Ребёнка не следует переводить на искусственное питание. Влияние на управление автомобилем и другим транспортом и механизмами не установлено.
Хранение
Вакцину Ротарикс хранят не более суток при температурном режиме 2–8 градусов. Ротарикс не следует замораживать. Её хранят в тёмном прохладном месте. Нераспечатанное лекарство можно хранить в течение 3 лет при температурном режиме 2–8 градусов. Ротарикс не следует подвергать замораживанию.
Это перевод официальной инструкции лекарственного средства «Ротарикс вакцина для профилактики ротавирусной инфекции». Информация
предназначена только для медицинских специалистов.
- Состав
- Лекарственная форма
- Фармакологическая группа
- Фармакологические свойства
- Клинические характеристики
- Показания
- Противопоказания
- Взаимодействие
- Особенности применения
- Период беременности
- Управление автомобилем
- Способ применения и дозы
- Дети
- Передозировка
- Побочные эффекты
- Срок годности
- Условия хранения
- Упаковка
- Категория отпуска
- Производитель
- Местонахождение производителя
Еще
Ротарикс вакцина для профилактики ротавирусной инфекции инструкция по применению
Официальная инструкция лекарственного препарата Ротарикс вакцина для профилактики ротавирусной инфекции суспензия 1,5 мл/дозу. Описание и применение Rotariks vaktsina dlja profilaktiki rotavirusnoj infektsii, аналоги и отзывы. Инструкция Ротарикс вакцина для профилактики ротавирусной инфекции суспензия утвержденная компанией производителем.
Состав
действующее вещество : 1 доза (1,5 мл) содержит не менее 106,0 ТЦД50 ротавируса человека, живой атенуйованый штамм RIX4414 *;
Вспомогательные вещества: сахароза (1,073 г), натрия адипат (132,74 мг), модифицированное среду Игла-Дюльбекко (DMEM) (2,26 мг), вода для инъекций (до 1,5 мл).
* Выращенный на культуре клеток Vero.
В вакцине РОТАРИКС ™ могут присутствовать в остаточной количества следы свиного цирковирус, тип 1 (PCV-1). Данные о возможности PCV-1 вызывать болезнь у животных и инфицировать или вызывать болезни у человека отсутствуют. Свидетельств того, что наличие PCV-1 представляет риск безопасности применения, нет.
Лекарственная форма
Суспензия оральная.
Основные физико-химические свойства : вакцина представляет собой прозрачную бесцветную жидкость.
РОТАРИКС ™ — это моновалентная вакцина для профилактики ротавирусного гастроэнтерита, которая содержит живой ослабленный вирус, полученный из штамма ротавируса человека.
РОТАРИКС ™ соответствует требованиям Всемирной организации здравоохранения для биологических веществ и для вакцин против ротавирусной инфекции.
Фармакологическая группа
Вакцины. Противовирусные вакцины. Вакцина для профилактики ротавирусной инфекции, живая атенуйованих.
Код АТХ J07B Н01.
Фармакологические свойства
Фармакологические
Защитная эффективность
В ходе клинических испытаний была продемонстрирована эффективность против случаев гастроэнтерита, вызванного ротавирусом наиболее распространенных генотипов G1P [8], G2P [4], G3P [8], G4P [8] и G9P [8], и против ротавируса нераспространенными генотипов G8P [4] (тяжелый гастроэнтерит) и G12P [6] (любой гастроэнтерит). Все эти штаммы циркулируют по всему миру.
Были проведены клинические исследования в Европе и Латинской Америке, Африке и Азии для оценки защитной эффективности вакцины РОТАРИКС ™ против всех, в том числе тяжких, вирусных гастроэнтеритов.
Тяжесть гастроэнтерита были определены согласно двум разным критериям:
— по 20-балльной шкале Весикари, которая оценивает полную клиническую картину ротавирусного гастроэнтерита, учитывая тяжесть и продолжительность диареи и рвоты, тяжесть лихорадки и обезвоживания, а также необходимость лечения
или
— по критериям Всемирной организации здравоохранения (ВОЗ).
Защитная эффективность вакцины по результатам исследований, проведенных в Европе и Латинской Америке
По результатам исследований, проведенных в Европе и Латинской Америке, после применения двух доз вакцины РОТАРИКС ™ защитная эффективность сохранялась в течение первого и второго года жизни ребенка, как показано в таблицах 1 и 2.
Таблица 1. Исследование, проведенное в Европе: 1-й и 2-й годы жизни вместе ( РОТАРИКС ™ N = 2572; плацебо N = 1302 *)
|
Генотип |
Эффективность вакцины (%) против любых и тяжелых вирусных гастроэнтеритов [ 95% ДИ ] |
|
|
Ротавирусный гастроэнтерит любой тяжести |
Тяжелый Ротавирусный гастроэнтерит ** |
|
|
G1P [8] |
89,5 [82,5; 94,1] |
96,4 [90,4; 99,1] |
|
G2P [4] |
58,3 [10,1; 81,0] |
85,5 [24,0; 98,5] |
|
G3P [8] |
84,8 [41,0; 97,3] |
93,7 [52,8; 99,9] |
|
G4P [8] |
83,1 [55,6; 94,5] |
95,4 [68,3; 99,9] |
|
G9P [8] |
72,5 [58,6; 82,0] |
84,7 [71,0; 92,4] |
|
Штаммы генотипа P [8] |
81,8 [75,8; 86,5] |
91,9 [86,8; 95,3] |
|
Циркулирующие штаммы ротавируса |
78,9 [72,7; 83,8] |
90,4 [85,1; 94,1] |
|
Эффективность вакцины (%) против вирусных гастроэнтеритов, нуждающихся в медицинской помощи [ 95% ДИ ] |
||
|
Циркулирующие штаммы ротавируса |
83,8 [76,8; 88,9] |
|
|
Эффективность вакцины (%) по частоте госпитализаций при вирусных гастроэнтеритах [ 95% ДИ ] |
||
|
Циркулирующие штаммы ротавируса |
96,0 [83,8; 99,5] |
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
ДИ — доверительный интервал.
Таблица 2. Исследование, проведенное в Латинской Америке: 1-й и 2-й годы жизни вместе ( РОТАРИКС ™ N = 7205; плацебо N = 7081 *)
|
Генотип |
Эффективность вакцины (%) против тяжелого ротавирусниого гастроэнтерита ** [ 95% ДИ ] |
|
Все ротавирусная гастроэнтериты |
80,5 [71,3; 87,1] |
|
G1P [8] |
82,1 [64,6; 91,9] |
|
G3P [8] |
78,9 [24,5; 96,1] |
|
G4P [8] |
61,8 [4,1; 86,5] |
|
G9P [8] |
86,6 [73,0; 94,1] |
|
Штаммы генотипа P [8] |
82,2 [73,0; 88,6] |
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
ДИ — доверительный интервал.
Эффективность вакцины против тяжелых вирусных гастроэнтеритов составила 38,6% (95% ДИ: <0,0; 84,2) для штамма G2P [4]. Количество случаев, на основе которых оценивалась эффективность вакцины по отношению к G2P [4], была небольшой.
В совокупном анализе данных 4 исследований по изучению эффективности вакцины было показано, что эффективность вакцины против тяжелых гастроэнтеритов (≥ 11 баллов по шкале Весикари), вызванных ротавирусом штамма G2P [4], составляет 71,4% (95% ДИ: 20,1; 91,1).
Защитная эффективность вакцины по результатам исследования, проведенного в Африке
В Африке было проведено клиническое исследование с участием более 4900 пациентов, в котором оценивали вакцину РОТАРИКС ™ , которая предназначена примерно на 10 и 14 неделях жизни (2 дозы) или на 6, 10 и 14 неделях жизни (3 дозы). Эффективность вакцины против тяжелых вирусных гастроэнтеритов в течение первого года жизни ребенка составляла 61,2% (95% ДИ: 44,0; 73,2). Исследование является недостаточным для оценки разницы между эффективностью двух схем применения вакцины — дводозовои и тридозовои.
Данные, которые показывают защитную эффективность вакцины против любых и тяжелых вирусных гастроэнтеритов, приведены в таблице 3.
Таблица 3. Исследование, проведенное в Африке: 1-й год жизни — обобщенные данные ( РОТАРИКС ™ N = 2974; плацебо N = 1443 *)
|
Генотип |
Эффективность вакцины (%) против всех вирусных гастроэнтеритов [ 95% ДИ ] |
|
|
Ротавирусный гастроэнтерит любой тяжести |
Тяжелый Ротавирусный гастроэнтерит ** |
|
|
G1P [8] |
68,3 (53,6; 78,5) |
56,6 (11,8; 78,8) |
|
G2P [4] |
49,3 (4,6; 73,0) |
83,8 (9,6; 98,4) |
|
G3P [8] |
43,4* (<0; 83,7) |
51,5*** (<0; 96,5) |
|
G8P [4] |
38,7* (<0; 67,8) |
63,6 (5,9; 86,5) |
|
G9P [8] |
41,8* (<0; 72,3) |
56,9*** (<0; 85,5) |
|
G12P [6] |
48,0 (9,7; 70,0) |
55,5*** (<0; 82,2) |
|
Штаммы генотипа P [4] |
39,3 (7,7; 59,9) |
70,9 (37,5; 87,0) |
|
Штаммы генотипа P [6] |
46,6 (9,4; 68,4) |
55,2*** (<0; 81,3) |
|
Штаммы генотипа P [8] |
61,0 (47,3; 71,2) |
59,1 (32,8; 75,3) |
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
*** Не являются статистически достоверным (р ≥ 0,05). Эти значения должны быть интерпретированы с осторожностью.
ДИ — доверительный интервал.
Продолжительность защитной эффективности вакцины у детей в возрасте до 3 лет, по результатам исследования, проведенного в Азии
Клиническое исследование, проведенное в Азии (Гонконг, Сингапур и Тайвань) с участием более 10000 пациентов, получавших вакцину РОТАРИКС ™ по различным графику (2, 4 месяца жизни, 3, 4 месяца жизни). После двух доз вакцины РОТАРИКС ™ защитная эффективность наблюдалась до 3 лет жизни (см. Табл. 4).
Таблица 4. Исследование, проведенное в Азии: эффективность до двух и трех лет ( РОТАРИКС ™ N = 5263; плацебо N = 5256 *)
|
Генотип |
эффективность вакцины до 2 лет |
эффективность вакцины до 3 лет |
|
Эффективность вакцины (%) против всех вирусных гастроэнтеритов [ 95% ДИ ] |
||
|
Тяжелый Ротавирусный гастроэнтерит ** |
Тяжелый Ротавирусный гастроэнтерит ** |
|
|
G1P [8] |
100,0 (80,8; 100,0) |
100,0 (84,8; 100,0) |
|
G2P [4] |
100,0* (<; 100,0) |
100,0*** (<; 100,0) |
|
G3P [8] |
94,5 (64,9; 99,9) |
95,2 (70,4; 99,9) |
|
G9P [8] |
91,7 (43,8; 99,8) |
91,7 (43,8; 99,8) |
|
Штаммы генотипа P [8] |
95,8 (83,8; 99,5) |
96,6 (87,0; 99,6) |
|
Циркулирующие штаммы ротавируса |
96,1 (85,1; 99,5) |
96,9 (88,3; 99,6) |
|
Эффективность вакцины (%) против вирусных гастроэнтеритов по частоте госпитализаций и / или регидратационной терапии в медицинских учреждениях [ 95% ДИ ] |
||
|
Циркулирующие штаммы ротавируса |
94,2 (82,2; 98,8) |
95,5 (86,4; 99,1) |
* Когорта «согласно протоколу исследования» для оценки эффективности. Она включает всех субъектов когорты «согласно протоколу исследования» для оценки безопасности, которые были включены в исследование на период наблюдения по оценке эффективности.
** Тяжелым считался случай гастроэнтерита ³ 11 баллов по шкале Весикари.
*** Не являются статистически достоверным (р ≥ 0,05). Эти значения должны быть интерпретированы с осторожностью.
ДИ — доверительный интервал.
иммунный ответ
В клинических исследованиях, проводившихся в Европе, Латинской Америке и Азии, 1957 младенцев получили по разным графикам прививки лиофилизированную вакцину РОТАРИКС ™ и 1006 младенцев — плацебо. Доля пациентов, которые до прививки были серонегативными к ротавируса (титры антител IgA <20 Ед / мл (ELISA)), с титром антиротавирусних IgA в сыворотке ³ 20 Ед / мл через 1 или 2 месяца после введения второй дозы вакцины или плацебо составляла от 77 9% до 100% и от 0% до 17,1% соответственно.
Иммунный ответ на введение вакцины РОТАРИКС ™ в форме суспензии по данным 3-х сравнительных исследований аналогична иммунного ответа на введение вакцины в форме лиофилизированного порошка.
В клиническом исследовании, проведенном в Африке, иммунный ответ оценивали в 332 младенцев, получивших вакцину РОТАРИКС ™ (N = 221) или плацебо (N = 111) по графику прививки на 10 и 14 неделях (2 дозы) или на 6, 10 и 14 неделях (3 дозы). Доля пациентов, которые до прививки были серонегативными к ротавируса (титры антител IgA <20 Ед / мл (ELISA)), с сывороточными титрами антиротавирусних антител IgA ³ 20 Ед / мл через 1 месяц после введения последней дозы вакцины или плацебо составила 58,4% (объединенные данные для обоих режимов прививки) и 22,5% соответственно.
Иммунный ответ у недоношенных младенцев
По данным клинических исследований после иммунизации недоношенных младенцев вакциной РОТАРИКС ™ в лиофилизированной форме в 85,7% вакцинированных достигался титр антиротавирусного IgA в сыворотке ≥ 20 Ед / мл (ELISA) через 1 месяц после введения второй дозы вакцины.
Безопасность вакцины для младенцев, инфицированных вирусом иммунодефицита человека (ВИЧ)
В клиническом исследовании 100 младенцев с ВИЧ-инфекцией получили лиофилизированную вакцину РОТАРИКС ™ или плацебо. Профиль безопасности вакцины РОТАРИКС ™ и плацебо был подобным.
Выделение вакцинного вируса
После прививки встречается выделение вакцинного вируса с фекалиями, которое длится в среднем в течение 10 дней с максимальной экскреции вируса примерно на 7-й день после вакцинации. Наличие вирусных антигенов, обнаруженная по результатам ELISA, определялась в 50% образцов фекалий после введения первого дозы вакцины и в 4% образцов — после введения второй дозы. При тестировании этих образцов фекалий на наличие живого вакцинного вируса 17% из них были положительными.
В двух сравнительных контрольных исследованиях выделение вакцинного вируса после применения жидкой вакцины РОТАРИКС ™ было подобным тому, которое наблюдалось после применения лиофилизированной вакцины РОТАРИКС ™ .
эффективность
В обсервационных исследованиях эффективность вакцины была продемонстрирована против тяжелого гастроэнтерита, вызванного ротавирусом наиболее распространенных генотипов G1P [8], G2P [4], G3P [8] и G9P [8], а также менее распространенных генотипов G9P [4] и G9P [6] , что привело к госпитализации. Все эти штаммы циркулируют по всему миру.
В таблице 5 продемонстрированы результаты нескольких исследований, проведенных по методу случай-контроль для оценки эффективности препарата РОТАРИКС ™ против тяжелого гастроэнтерита, вызванного ротавирусом, что привело к госпитализации.
Таблица 5. Эффективность против тяжелого гастроэнтерита, вызванного ротавирусом, что привело к госпитализации
|
Страна |
возраст |
Количество привитых двумя дозами ( N ) (Случаи / контроль) |
штамм |
Эффективность, рассчитанная по госпитализированными ротавирус-негативными пациентами, (%) [ 95% ДИ ] |
|
|
Страны с высоким уровнем дохода |
|||||
|
Бельгия |
<4 лет |
160/198 |
все G1P [8] G2P [4] |
90 [81; 95] 95 [78; 99] 85 [64; 94] |
|
|
3-11 месяцев |
все G2P [4] |
91 [75;97] 83 [11;96] |
|||
|
Сингапур |
<5 лет |
136/272 |
все G1P [8] |
84 [32; 96] 91 [30; 99] |
|
|
Тайвань |
<3 лет |
275/1623 |
все G1P [8] |
92 [75;98] 95 [69;100] |
|
|
США |
<2 лет |
85/1062 |
все G1P [8] G2P [4] |
85 [73;92] 88 [68;95] 88 [68;95] |
|
|
8-11 месяцев |
все |
89 [48;98] |
|||
|
США |
<5 лет |
74/255 |
G3P [8] |
68 [34;85] |
|
|
Страны со средним уровнем дохода |
|||||
|
Боливия |
<3 лет |
300/974 |
все G9P [8] G3P [8] G2P [4] G9P [6] |
77 [65;84] 85 [69;93] 93 [70;98] 69 [14;89] 87 [19;98] |
|
|
6-11 месяцев |
все G9P [8] |
77 [51;89] 90 [65;97] |
|||
|
Бразилия |
<2 лет |
115/1481 |
все G1P [8] G2P [4] |
72 [44;85] 89 [78;95] 76 [64;84] |
|
|
Бразилия |
<3 лет |
249/249 |
все G2P [4] |
76 [58;86] 75 [57;86] |
|
|
3-11 месяцев |
G2P [4] |
96 [68;99] 95 [66;99] |
|||
|
Эль-Сальвадор |
<2 лет |
251/770 |
все |
76 [64; 84]* |
|
|
6-11 месяцев |
83 [68;91] |
||||
|
Мексика |
<2 лет |
9/17 |
G9P [4] |
94 [16;100] |
|
|
Страны с низким уровнем дохода |
|||||
|
Малави |
<2 лет |
81/234 |
все |
63 [23;83] |
* У пациентов, не прошедших полный курс вакцинации, эффективность после одной дозы составляла от 51% (95% ДИ: 26; 67, Эль-Сальвадор) до 60% (95% ДИ: 37; 75, Бразилия).
ДИ — доверительный интервал.
Влияние на смертность 1
Исследование влияния препарата РОТАРИКС ™ , проведенные в Панаме, Бразилии и Мексике, продемонстрировали снижение смертности из-за диареи по всем причинам с диапазоном 22 — 56% в возрасте до 5 лет, в течение 2 — 3 лет после введения вакцины.
Влияние на госпитализацию 1
В ретроспективном исследовании базы данных в Бельгии, проведенном с участием детей 5 лет и младше, прямое и косвенное влияние вакцинации препаратом РОТАРИКС ™ на связанную с ротавирусом госпитализации составил от 64% (95% ДИ: 49; 76) до 80% ( 95% ДИ: 77; 83) через два года после введения вакцины. Подобные исследования в Бразилии, Австралии и Эль-Сальвадоре продемонстрировали снижение уровня госпитализации на 45 — 88%. Кроме того, два исследования влияния на госпитализацию из-за диареи из всех причин, проведенные в Латинской Америке, продемонстрировали снижение на 38 — 40% через четыре года после введения вакцины.
1 исследование влияния означают установление временного взаимосвязи, а не причинно-следственной связи между болезнью и вакцинацией.
Фармакокинетика
Оценка фармакокинетических свойств не применяется для вакцин.
Клинические характеристики
Ротарикс вакцина для профилактики ротавирусной инфекции Показания
Вакцина РОТАРИКС ™ показана для профилактики гастроэнтерита, вызванного ротавирусом (см. Разделы «Способ применения и дозы», «Особенности применения», «Иммунобиологические и биологические свойства»).
Прививка детей на территории Украины осуществляется согласно требованиям действующих приказов МЗ Украины.
Противопоказания
Повышенная чувствительность после предыдущего применения вакцины РОТАРИКС ™ или к любому из компонентов вакцины (см. Раздел «Состав»).
Наличие в анамнезе инвагинации.
Устраненных врожденный порок развития желудочно-кишечного тракта (например дивертикул Меккеля), что может быть причиной развития кишечной инвагинации.
Тяжелый комбинированный иммунодефицит (SCID) (см. Раздел «Побочные реакции»).
Редкая наследственная форма непереносимости фруктозы, глюкозо-галактозы мальабсорбцией или сахароза-изомальтозною недостаточностью. Вакцина содержит сахарозу.
При проведении иммунизации на территории Украины относительно противопоказаний также следует руководствоваться действующими приказами МЗ Украины.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Вакцину РОТАРИКС ™ можно применять в сочетании с любым из следующих как моновалентных, так и комбинированных вакцин, включая гексавалентный вакцину DTPa-HBV-IPV / Hib — вакцину для профилактики дифтерии, столбняка, коклюша (бесклеточную), гепатита В, полиомиелита и заболеваний , вызываемых Haemophilus influenzaeтипа b (Hib) вакцину для профилактики дифтерии, столбняка и коклюша (цельноклеточным) (DTPw), вакцину для профилактики дифтерии, столбняка и коклюша (бесклеточную) (DTPa), вакцину для профилактики заболеваний, вызываемых Hib, инактивированную вакцину для профилактики полиомиелита (IPV), вакцину для профилактики гепатита В (HBV), конъюгированные вакцины для профилактики пневмококковой инфекции и конъюгированной вакцины для профилактики заболеваний, вызванных менингококками серогруппы С. Результаты исследований показали, что одновременное введение этих вакцин не влияло на их иммуногенность и безопасность.
Одновременное применение вакцины РОТАРИКС ™ и пероральной вакцины для профилактики полиомиелита (OPV) не оказало влияния на иммунный ответ к полиовирусов. Хотя совместное применение OPV вакцины может в небольшой степени уменьшать иммунный ответ ротавирусной вакцине, клинический защиту против тяжелых гастроэнтеритов, вызванных ротавирусами, сохраняется.
Особенности применения
Согласно требованиям медицинской практики, вакцинации должно предшествовать изучение анамнеза (особенно по предварительной вакцинации и возможных случаев побочных реакций) и медицинское обследование.
Как и при применении других вакцин, введение вакцины РОТАРИКС ™ должно быть отложено у лиц с острыми заболеваниями, сопровождающимися лихорадкой. Однако наличие незначительных инфекций, таких как простуда, не является противопоказанием для проведения иммунизации.
Применение вакцины РОТАРИКС ™ должно быть отложено у лиц, страдающих диареей или рвотой.
Данные о безопасности и эффективности применения вакцины РОТАРИКС ™ у младенцев с заболеваниями желудочно-кишечного тракта отсутствуют. Поэтому применять вакцину РОТАРИКС ™ таким младенцам следует с осторожностью, взвешивая риск и пользу от вакцинации.
Риск инвагинации был изучен в большом клиническом исследовании (63225 младенцев), проведенном в Финляндии, Индии и Бангладеш. Увеличение риска возникновения инвагинации после применения вакцины РОТАРИКС ™ по сравнению с плацебо выявлено не было.
Однако, по данным постмаркетингового исследования по безопасности, было обнаружено кратковременное увеличение риска инвагинации после вакцинации, главным образом в течение 7 дней после первой дозы вакцины и в меньшей степени — после второй дозы . Общее количество возникновения случаев инвагинации остается по частоте: редко. Влияние применения вакцины РОТАРИКС ™ на общий риск возникновения инвагинации не установлен.
В качестве меры предосторожности, медицинский персонал в послевакцинальный период должен наблюдать за любым симптомом, указывающим на инвагинацию (тяжелая боль в животе, постоянное рвота, кровянистые испражнения, вздутие живота и / или высокая температура). Родителям или опекунам следует посоветовать быстро сообщать о появлении таких симптомов.
Применение вакцины РОТАРИКС ™ имуноскомпрометованим младенцам, включая тех, кто получает иммуносупрессивную терапию, должно базироваться на тщательном сопоставлении возможной пользы и риска применения вакцины РОТАРИКС ™ .
Как известно, выделение вакцинного вируса с испражнениями появляется после вакцинации и длится в среднем до 10 дней с пиком выделения на 7-й день. По данным клинических исследований наблюдались случаи передачи вакцинного вируса серонегативным контактным лицам, но без появления каких-либо клинических симптомов. РОТАРИКС ™ следует с осторожностью применять лицам, тесно контактируют с пациентами с иммунодефицитом, в частности со злокачественными новообразованиями, или теми, кто получает иммуносупрессивную терапию.
Лица, контактирующие с недавно вакцинированными детьми, должны быть проинформированы о необходимости соблюдения тщательной гигиены (включая мытье рук) после смены подгузников у ребенка.
При проведении первичной иммунизации у недоношенных детей (рожденных ≤ 28 недель беременности) необходим мониторинг дыхания в течение 48 — 72 часов после прививки через потенциальный риск апноэ.
Как и при применении других вакцин, защитная иммунный ответ может быть получена не у всех вакцинированных детей.
Пока неизвестно, насколько вакцина РОТАРИКС ™ может обеспечивать защиту против штаммов ротавируса, не циркулировали в рамках проводимых клинических исследований.
Вакцина РОТАРИКС ™ не защищает от гастроэнтеритом неротавируснои этиологии.
Применение в период беременности или кормления грудью
Вакцина РОТАРИКС ™ не предназначена для применения у взрослых. Поэтому данные по применению вакцины женщинами во время беременности или кормления грудью отсутствуют.
Основываясь на доказательствах, полученных в результате клинических исследований, грудное вскармливание не уменьшает защиту от ротавирусного гастроэнтерита, полученного после (вследствие) применение вакцины РОТАРИКС ™. Таким образом, грудное вскармливание можно продолжать во время вакцинации.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Способ применения Ротарикс вакцина для профилактики ротавирусной инфекции и дозы
дозировка
Курс вакцинации состоит из двух доз. Первая доза может быть назначена ребенку, начиная с возраста 6 недель. Интервал между применением первой и второй дозы должен быть не менее 4 недель. Курс вакцинации следует закончить до достижения ребенком возраста 24 недели.
РОТАРИКС ™ может быть назначен по тем же показаниям и недоношенным детям, соблюдая такого же дозировки (см. Разделы « Иммунобиологические и биологические свойства» и «Побочные реакции» ).
По данным клинических исследований, срыгивание или сплевывания при применении вакцины наблюдалось очень редко и в таких случаях повторная доза не вводилась. Однако, если ребенок извергла или плюнула почти всю дозу, можно однократно заменить эту дозу во время этого же вакцинации.
Настоятельно рекомендуется, чтобы младенцы, которые получили первую дозу вакцины РОТАРИКС ™ , завершили 2-дозирования курс вакцинации препаратом РОТАРИКС ™ .
способ применения
Вакцина РОТАРИКС ™ предназначена только для перорального применения.
Вакцину РОТАРИКС ™ ни в коем случае нельзя вводить в виде инъекции!
Отсутствуют ограничения на потребление младенцем пищи или жидкости, включая грудное молоко, как до, так и после вакцинации.
По данным, полученным в клинических исследованиях, грудное вскармливание не может уменьшить эффективность вакцины РОТАРИКС ™. Поэтому в период проведения вакцинации можно продолжать кормить ребенка грудным молоком.
Инструкции по приготовлению или восстановления вакцины приведены ниже.
Техника применения / обращения с препаратом .
Специальные предостережения относительно применения и использования препарата
Вакцина представляет собой прозрачную бесцветную жидкость, свободной от любых посторонних частиц; в оральном аппликаторе или пластиковой тубе, закрытых защитным колпачком. Препарат готов для использования (не требуется его растворения или разведения). Перед применением вакцину необходимо визуально проверить на наличие каких-либо посторонних частиц и / или изменение внешнего вида. В случае, если наблюдается что-либо из вышеперечисленного, вакцину не использовать.
Применение вакцины в оральном аппликаторе и тубе:
- Техника применения вакцины в оральном аппликаторе приведена на рис. 1.
- Техника применения вакцины в тубе приведена на рис. 2.
- Эта вакцина предназначена только для перорального применения. Ребенка следует держать с отклоненной головой. Введите все содержимое орального аппликатора или тубы пероральный (на внутреннюю поверхность щеки).
- Не вводить путем инъекции.
Рис. 2. Техника применения вакцины в тубе
Дети
Вакцина РОТАРИКС ™ не должна использоваться у детей старше 24-недельного возраста.
Передозировка
Было получено некоторые сообщения о случаях передозировки. В общем сообщении побочные реакции были аналогичными тем, которые наблюдаются после применения рекомендуемой дозы вакцины РОТАРИКС ™.
Побочные эффекты
Данные клинических исследований
Для определения частоты возникновения побочных действий применяется следующая классификация.
Очень часто (≥ 1/10)
Часто (≥ 1/100 — < 1/10)
Нечасто (≥ 1/1000 — < 1/100)
Редко (≥ 1/10000 — <1/1000)
Очень редко (<1/10000)
Профиль безопасности вакцины, приведенный ниже, основывается на данных клинических испытаний, проведенных как с лиофилизированной форме вакцины РОТАРИКС ™ , так и с уже готовой оральной суспензией.
Всего в 4 клинических исследованиях вакцины РОТАРИКС ™ в форме суспензии было иммунизированы 1900 младенцев, которым было введено около 3800 доз вакцины. По данным этих исследований было показано, что профиль безопасности вакцины в форме суспензии является сопоставимым с профилем безопасности вакцины в форме лиофилизированного порошка.
Всего в 23 клинических исследованиях были использованы 106000 доз вакцины РОТАРИКС ™ (в форме лиофилизированного порошка или суспензии) примерно 51000 младенцам.
В трех плацебо-контролируемых клинических исследованиях, где РОТАРИКС ™ применялся самостоятельно (назначение других обычных педиатрических вакцин происходило по графику), частота и тяжесть таких ожидаемых симптомов (зарегистрированных в течение 8 дней после вакцинации), как диарея, рвота, потеря аппетита, лихорадка, раздражительность и кашель / насморк существенно не отличались в группе, вакцинировался РОТАРИКС ™ , по сравнению с группой, получавшей плацебо. Не было отмечено увеличение частоты и тяжести этих реакций и после применения второй дозы.
По данным обобщенного анализа 17 плацебо-контролируемых клинических исследований, где РОТАРИКС ™ применялся вместе с другими педиатрическими вакцинами (см. Раздел «Взаимодействие с другими медикаментами и другие виды взаимодействий»), такие побочные реакции (зарегистрированы в течение 31 дня после вакцинации) были оценены как быть связано с вакцинацией.
|
Системы органов |
Частота |
побочные реакции |
|
Желудочно-кишечная система |
Часто |
диарея |
|
Нечасто |
Метеоризм, боли в животе |
|
|
Очень редко |
инвагинация |
|
|
неизвестно * |
кровянистые испражнения |
|
|
неизвестно * |
Гастроэнтериты с выделением вакцинного вируса у младенцев с тяжелым комбинированным иммунодефицитом (SCID) |
|
|
Кожа и подкожные ткани |
Нечасто |
Дерматит |
|
Общие расстройства и нарушения в месте введения |
Часто |
раздражительность |
|
Нарушение дыхания, функции органов грудной полости и средостения |
неизвестно * |
Апноэ у недоношенных новорожденных (рожденных ≤ 28 недель беременности) (см. Раздел «Особенности применения») |
* Поскольку об этих событиях было сообщено спонтанно, невозможно достоверно оценить их частоту.
Риск возникновения инвагинации был оценен в большом клиническом исследовании по безопасности применения этой вакцины в Латинской Америке и Финляндии с привлечением 63225 пациентов. По данным этого исследования не было выявлено увеличения риска возникновения инвагинации в группе пациентов, иммунизированных вакциной РОТАРИКС ™ по сравнению с группой плацебо, как показано в таблице ниже.
|
Сроки проявления инвагинации |
РОТАРИЙ ™ (количество человек) |
Плацебо (количество человек) |
Относительный риск (95% ДИ) |
|
инвагинация течение 31 дня после: |
N = 31 673 |
N = 31 552 |
|
|
1 |
2 |
0,50 (0,07; 3,80) |
|
5 |
5 |
0,99 (0,31; 3,21) |
|
инвагинация течение первого года жизни: |
N = 10159 |
N = 10 010 |
|
до 1 года |
4 |
14 |
0,28 (0,10; 0,81) |
N — общее количество человек.
ДИ — доверительный интервал.
Безопасность применения вакцины недоношенным младенцам
В клиническом исследовании 1009 недоношенным младенцам было применено РОТАРИКС ™ в форме лиофилизированного порошка или плацебо (198 младенцев имели 27 — 30 недель гестации и 801 ребенок — 31 — 36 недель гестации). Первая доза была применена в возрасте 6 недель. Серьезные побочные эффекты наблюдались в 5,1% младенцев, получавших РОТАРИКС ™, по сравнению с 6,8% младенцев, получавших плацебо. Аналогичная частота других побочных эффектов наблюдалась в группе младенцев, получавших РОТАРИКС ™, и в группе, получавшей плацебо. Сообщений о случаях инвагинации не было.
Данные постмаркетингового наблюдения
Со стороны желудочно-кишечного тракта
Редко : кровянистые испражнения, гастроэнтериты с выделением вакцинного вируса у младенцев с тяжелым комбинированным иммунодефицитом (SCID).
Очень редко инвагинация (см. «Особенности применения» )
Срок годности Ротарикс вакцина для профилактики ротавирусной инфекции
3 года. Дата окончания срока годности вакцины указана на этикетке и на упаковке.
Условия хранения Ротарикс вакцина для профилактики ротавирусной инфекции
Вакцину следует хранить при температуре от 2 до 8 ° C (в холодильнике). Не замораживать. Хранить в оригинальной упаковке, чтобы защитить от света. Хранить в недоступном для детей месте.
Несовместимость.
При применении вакцины РОТАРИКС ™ не следует смешивать с другими лекарственными средствами.
Упаковка
По 1 дозе (1,5 мл) вакцины в предварительно заполненном оральном аппликаторе из стекла типа I (Евр.Ф.) с защитным колпачком или пластиковой тубе с колпачком.
Оральный аппликатор или туба вместе с инструкцией по применению вложены в картонную коробку. По 1 или по 5 предварительно заполненных оральных аппликаторов или туб в картонной коробке.
Категория отпуска
По рецепту.
Производитель
ГлаксоСмитКляйн Биолоджикалз С.А., Бельгия / GlaxoSmithKline Biologicals SA, Belgium.
Местонахождение производителя
Рю де льИнститю, 89 1330 м. Риксенсарт, Бельгия / Rue de l’Institut, 89 1330 Rixensart, Belgium.
Дальнейшая информация
Помните, храните эти и все другие лекарства в недоступном для детей месте,
никогда не передавайте свои лекарства другим и используйте Ротарикс вакцина для профилактики ротавирусной инфекции только по назначению
врача.
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация,
которая отображается на этой странице, может быть применена к вашим личным обстоятельствам.
Внимание: Перевод на русский язык, выполнен редакторской командой Tabletki.info.
Авторское право:
- ГлаксоСмитКляйн Биолоджикалз С.А.
- http://www.drlz.com.ua — Государственный реестр ЛС Украины
| Тип данных | Сведения из реестра |
| Торговое наименование: | Ротарикс вакцина для профилактики ротавирусной инфекции |
| Производитель: | ГлаксоСмитКляйн Биолоджикалз С.А. |
| Форма выпуска: | суспензия оральная (1,5 мл / доза) по 1 или по 5 предварительно заполненных оральных аппликаторов или туб в картонной коробке |
| Регистрационное удостоверение: | UA/13060/01/01 |
| Дата начала: | 18.12.2018 |
| Дата окончания: | неограниченный |
| МНН: | Rota virus, live attenuated |
| Условия отпуска: | по рецепту |
| Состав: | 1 доза (1,5 мл) содержит не менее 106,0 ТЦД50 ротавируса человека, живой атенуйованих штамм RIX4414 * |
| Фармакологическая группа: | Вакцины. Противовирусные вакцины. Вакцина для профилактики ротавирусной инфекции, живая атенуйованих. |
| Код АТХ: | J07BH01 |
| Заявитель: | ГлаксоСмитКляйн Экспорт Лимитед |
| Страна заявителя: | Великобритания |
| Адрес заявителя: | 980 Грейт Уэст Роуд, Брентфорд, Миддлсекс, TW8 9GS, Большая Британия |
| Тип ЛС: | Иммунобиологический |
| ЛС биологического происхождения: | Да |
| ЛС растительного происхождения: | Нет |
| Гомеопатическое ЛС: | Нет |
| Тип МНН: | Моно |
| Досрочное прекращение | Нет |
| Код ATХ | Название группы |
| J | Противомикробные средства для системного применения |
| J07 | Вакцины |
| J07B | Вирусные вакцины |
| J07BH | Вакцины против роту — вирусной диареи |
| J07BH01 | Вирус, возбудитель роту — вирусной диареи — живой ослабленный |