Описание препарата Сертикан® (таблетки, 0.25 мг) основано на официальной инструкции, утверждено компанией-производителем в 2012 году
Дата согласования: 28.09.2012
Содержание
- Действующее вещество
- ATX
- Фармакологическая группа
- Нозологическая классификация (МКБ-10)
- Состав
- Описание лекарственной формы
- Фармакологическое действие
- Фармакодинамика
- Фармакокинетика
- Показания
- Противопоказания
- Применение при беременности и кормлении грудью
- Способ применения и дозы
- Побочные действия
- Взаимодействие
- Передозировка
- Особые указания
- Форма выпуска
- Производитель
- Условия отпуска из аптек
- Условия хранения
- Срок годности
- Заказ в аптеках Москвы
- Отзывы
Действующее вещество
ATX
Фармакологическая группа
Состав
| Таблетки диспергируемые | 1 табл. |
| активное вещество: | |
| эверолимус | 0,1 мг |
| 0,25 мг | |
| вспомогательные вещества: бутилгидрокситолуол; лактозы моногидрат; гипромеллоза, магния стеарат; кремния диоксид коллоидный безводный; кросповидон; лактоза безводная |
| Таблетки | 1 табл. |
| активное вещество: | |
| эверолимус | 0,25 мг |
| 0,5 мг | |
| 0,75 мг | |
| 1 мг | |
| вспомогательные вещества: бутилгидрокситолуол (соответственно дозировке активного вещества) — 0,025/0,05/0,0725/0,1 мг; лактозы моногидрат — 2,225/4,45/6,675/8,9 мг; гипромеллоза — 10/20/30/40 мг; магния стеарат — 0,4/0,625/0,938/1,25 мг; кросповидон — 16/25/37,5/50 мг; лактоза безводная — 51,1/74,375/111,562/148,75 мг |
Описание лекарственной формы
Таблетки 0,25 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «C», на другой — «NVR».
Таблетки 0,5 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «CН», на другой — «NVR».
Таблетки 0,75 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «CL», на другой — «NVR».
Таблетки 1 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «CU», на другой — «NVR».
Таблетки диспергируемые 0,1 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «I», на другой — «NVR».
Таблетки диспергируемые 0,25 мг: круглые, плоские, от белого до желтоватого цвета, со скошенными краями, допускается мраморность, на одной стороны маркировка «JO», на другой — «NVR».
Фармакологическое действие
Фармакологическое действие
—
иммунодепрессивное.
Фармакодинамика
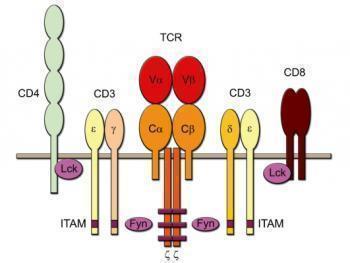
Активное вещество препарата Сертикан® — эверолимус — является ингибитором пролиферативного сигнала. Эверолимус оказывает иммуносупрессивный эффект за счет ингибирования антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими ИЛ Т-клеток, (например ИЛ-2 и ИЛ-15). Эверолимус ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием этих факторов роста Т-клеток с соответствующими рецепторами. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
На молекулярном уровне эверолимус образует комплекс с цитоплазматическим белком FKBP-12. В присутствии эверолимуса происходит ингибирование фосфорилирования р70 S6 киназы, стимулируемой фактором роста. Поскольку фосфорилирование р70 S6 киназы находится под контролем FRAP (так называемого m-TOR), эти данные позволяют предположить, что комплекс эверолимус-FКВР-12 связывается с FRAP. FRAP — это ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией; нарушение функции FRAP, таким образом, объясняет остановку клеточного цикла, вызываемую эверолимусом. Эверолимус имеет, следовательно, отличный от циклоспорина механизм действия. В доклинических моделях аллотрансплантации была показана более высокая эффективность комбинации эверолимуса с циклоспорином, по сравнению с изолированным использованием каждого из них.
Эффект эверолимуса не ограничивается влиянием на Т-клетки. Он ингибирует стимулируемую факторами роста пролиферацию как гемопоэтических, так и негемопоэтических клеток (например гладкомышечных клеток). Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, которая запускается при повреждении эндотелиальных клеток и приводит к образованию неоинтимы, играет ключевую роль в патогенезе хронического отторжения.
В экспериментальных исследованиях показано ингибирование образования неоинтимы у крыс с аллотрансплантатом аорты.
Фармакокинетика
Всасывание. После приема внутрь Cmax достигается через 1–2 ч. У пациентов после пересадки концентрация эверолимуса в крови пропорциональна дозе в диапазоне доз от 0,25 до 15 мг. На основании показателя AUC относительная биодоступность диспергируемых таблеток по сравнению с таблетками составляет 90%.
Влияние пищи: Cmax и AUC эверолимуса уменьшались на 60 и 16% соответственно при приеме таблеток с очень жирной пищей. Чтобы свести вариабельность к минимуму, препарат Сертикан® следует принимать или одновременно с пищей, или без нее.
Распределение. Соотношение концентрации эверолимуса в крови и его концентрации в плазме находится в пределах от 17 до 73% и зависит от значений концентрации в диапазоне от 5 до 5000 нг/мл. У здоровых добровольцев и пациентов с умеренными нарушениями функции печени связывание с белками плазмы составляет приблизительно 74%. VSS в конечной фазе у пациентов после трансплантации почки, находящихся на поддерживающей терапии, составляет (342±107) л.
Метаболизм. Эверолимус является субстратом CYP3A4 и Р-гликопротеина. Основными путями метаболизма, выявленными у человека, были моногидроксилирование и О-деалкилирование. Два основных метаболита образуются путем гидролиза циклического лактона. Ни один из них не имеет существенной иммуносупрессивной активности. В системном кровотоке находится в основном эверолимус.
Выведение. После введения однократной дозы меченого радиоактивной меткой эверолимуса пациентам после трансплантации, получающим циклоспорин, бoльшая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось с мочой. Неизмененное вещество не определялось ни в моче, ни в кале.
Фармакокинетика в равновесном состоянии
Фармакокинетика у пациентов с почечным и сердечным трансплантатом, получавших эверолимус 2 раза в сутки одновременно с циклоспорином в форме микроэмульсии, была сопоставима. Равновесное состояние достигалось на 4-й день с кумуляцией в крови в концентрациях, которые в 2–3 раза превышали концентрации в крови после применения первой дозы. После приема препарата Тmax составляет 1–2 ч. При приеме препарата в дозах 0,75 и 1,5 мг 2 раза в сутки средние значения Cmax составляют (11,1±4,6) нг/мл и (20,3±8,0) нг/мл, средние значения AUC — (75±31) нг?ч/мл и (131±59) нг?ч/мл соответственно. При приеме препарата в дозах 0,75 и 1,5 мг 2 раза в сутки С0 эверолимуса в крови составляют, в среднем, (4,1±2,1) нг/м или (7,1±4,6) нг/мл, соответственно (С0 — базальная концентрация, определяемая утром до приема очередной дозы). Экспозиция эверолимуса остается стабильной все время в течение первого года после трансплантации. С0 в высокой степени коррелировала с AUC с коэффициентом корреляции, колеблющимся между 0,86 и 0,94. На основании анализа фармакокинетики у пациентов после трансплантации общий клиренс составляет 8,8 л/ч (разброс — 27%), центральный кажущийся VSS составляет 110 л (разброс — 36%). T1/2 составляет (28±7) ч.
Фармакокинетика в особых клинических случаях
Нарушения функции печени. У 8 пациентов с умеренно выраженными нарушениями функции печени (класс В по шкале Child-Pough) AUC эверолимуса увеличивалась приблизительно в 2 раза по сравнению с таковой у 8 здоровых добровольцев. Показатель AUC положительно коррелировал с концентрацией сывороточного билирубина и увеличением ПВ и отрицательно коррелировал с концентрацией сывороточного альбумина. Если концентрация билирубина составляла >34 мкмоль/л, ПВ было >1,3 МНО (пролонгация >4 сек) и/или концентрация альбумина составляла <35 г/л, то наблюдалась тенденция к увеличению показателя AUC у пациентов с умеренно выраженной печеночной недостаточностью. Воздействие тяжелой печеночной недостаточности (класс С Child-Pugh) на AUC не изучено, но, вероятно, оно такое же или более выраженное, чем воздействие умеренной печеночной недостаточности.
Нарушения функции почек. Посттрансплантационная почечная недостаточность (Cl креатинина — 11–107 мл/мин) не влияла на фармакокинетические параметры эверолимуса.
Педиатрия. Cl эверолимуса повышался в линейной зависимости от возраста пациента (от 1 до 16 лет), площади поверхности тела (0,49–1,92 м2) и массы тела (11–77 кг). В равновесном состоянии Cl составлял (10,2±3,0) л/ч/м2, T1/2 — (30±11) ч.
Девятнадцать de novo пациентов после пересадки почки в возрасте от 1 года до 16 лет получали препарат Сертикан® в форме таблеток диспергируемых в дозе 0,8 мг/м2 (максимально — 1,5 мг) 2 разав сутки с циклоспорином в форме микроэмульсии. У этих пациентов AUC эверолимуса составляла (87±27) нг?ч/мл, и соответствовала таковой у взрослых, получающих 0,75 мг 2 раза/сут. В равновесном состоянии базальная концентрация составляла (4,4±1,7) нг/мл.
Взрослые пациенты. У взрослых пациентов в возрасте от 16 до 70 лет наблюдалось снижение клиренса эверолимуса на 0,33% в год (коррекции дозы не требуется).
На основании популяционного анализа фармакокинетики общий Cl был выше у пациентов негроидной расы, в среднем, на 20%.
Влияние на эффективность. У реципиентов почки и сердца в течение 6 мес после трансплантации была выявлена связь между базальной концентрацией эверолимуса и частотой подтвержденного биопсией острого отторжения и тромбоцитопении.
Таблица
|
Трансплантация почки |
|||||
| С0, нг/мл | ?3,4 | 3,5–4,5 | 4,6–5,7 | 5,8–7,7 | 7,8–15 |
| Отсутствие отторжения | 68% | 81% | 86% | 81% | 91% |
| Тромбоцитопения (<100·109/л) | 10% | 9% | 7% | 14% | 17% |
| Трансплантация сердца | |||||
| С0, нг/мл | ?3,5 | 3,6–5,3 | 5,4–7,3 | 7,4–10,2 | 10,3–21,8 |
| Отсутствие отторжения | 65% | 69% | 80% | 85% | 85% |
| Тромбоцитопения (<75·109/л) | 5% | 5% | 6% | 8% | 9% |
Показания
Профилактика отторжения трансплантата почки и сердца у взрослых реципиентов с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию циклоспорином в форме микроэмульсии и ГКС.
Данных по применению препарата Сертикан® у детей и подростков недостаточно для того, чтобы рекомендовать использование препарата у данной категории пациентов. Однако, имеются ограниченные данные о применении препарата в педиатрии при трансплантации почки.
Противопоказания
Повышенная чувствительность к эверолимусу, сиролимусу или другим компонентам препарата.
С осторожностью:
тяжелая печеночная недостаточность (т.к. безопасность и эффективность эверолимуса у пациентов с нарушениями функции печени не изучалась — рекомендуется тщательно мониторировать его концентрацию в плазме крови);
редкие наследственные нарушения, связанные с непереносимостью галактозы, тяжелой лактазной недостаточностью или глюкозо-галактозной мальабсорбцией;
дети и подростки (данных по применению препарата Сертикан® недостаточно для того, чтобы рекомендовать использование препарата у данной категории пациентов). Однако, имеются ограниченные данные о применении препарата в педиатрии при трансплантации почки;
одновременное применение других ЛС, оказывающих отрицательное влияние на функцию почек.
Всем пациентам рекомендуется регулярный контроль функции почек. При повышении концентрации креатинина в сыворотке следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина.
Применение при беременности и кормлении грудью
Данные по применению препарата Сертикан® при беременности отсутствуют.
В экспериментальных исследованиях показано наличие токсического влияния на репродуктивность, включая эмбриотоксичность и фетотоксичность. Неизвестно, существует ли потенциальный риск для человека. Не следует применять препарат Сертикан® у беременных женщин за исключением тех случаев, когда ожидаемая польза от терапии превышает потенциальный риск для плода.
Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения препаратом Сертикан® и в течение 8 нед после окончания терапии.
Неизвестно, выделяется ли эверолимус с грудным молоком человека.
В экспериментальных исследованиях было показано, что эверолимус и/или его метаболиты быстро проникали в молоко лактирующих крыс. Поэтому женщинам, получающим препарат Сертикан®, не следует кормить грудью.
Способ применения и дозы
Внутрь — или всегда вместе с пищей, или всегда без нее.
Взрослые. Рекомендуемая начальная доза препарата для пациентов с почечными и сердечными трансплантатами составляет по 0,75 мг 2 раза/сут. Препарат следует начать применять как можно скорее после трансплантации. Суточную дозу препарата Сертикан® всегда разделяют на 2 приема. Препарат Сертикан® принимают в одно и то же время с циклоспорином в форме микроэмульсии. Может потребоваться коррекция режима дозирования препарата Сертикан® с учетом достигнутых концентраций в плазме крови, переносимости, индивидуального ответа на лечение, изменений сопутствующей медикаментозной терапии и клинической ситуации. Коррекцию режима дозирования можно проводить с интервалами 4–5 дней.
Представители негроидной расы. Частота случаев развития острого отторжения, подтвержденного биопсией, была выше у представителей негроидной расы по сравнению с остальными. Согласно имеющейся ограниченной информации, представителям негроидной расы может потребоваться более высокая доза препарата Сертикан® для достижения такого же эффекта, как у остальных пациентов, получающих препарат в рекомендуемых для взрослых дозах. Имеющихся в настоящее время данных по эффективности и безопасности недостаточно для предоставления специфических рекомендаций по использованию эверолимуса у представителей негроидной расы.
Пациенты пожилого возраста (≥65 лет). Клинический опыт применения препарата Сертикан® у пациентов в возрасте ≥65 лет ограничен. Тем не менее, явных различий фармакокинетики эверолимуса у пациентов в возрасте ≥65–70 лет по сравнению с более молодыми взрослыми пациентами не отмечалось.
Пациенты с нарушениями функции почек. У пациентов с нарушениями функции почек коррекция дозы не требуется.
Применение при нарушениях функции печени. У пациентов с печеночной недостаточностью следует тщательно мониторировать базальную концентрацию эверолимуса в цельной крови. У пациентов с легкой и умеренной печеночной недостаточностью (класс А или В по шкале Child-Pough) дозу препарата Сертикан® следует уменьшить приблизительно в 2 раза по сравнению со средней дозой в тех случаях, когда имеется сочетание 2 показателей из перечисленных ниже: билирубин >34 мкмоль/л (> 2 мг/дл), альбумин <35 г/л (<3,5 г/дл), MHO (INR, International Normalized Ratio) >1,3 (пролонгация ПВ >4 с). Дальнейшее титрование дозы проводят, основываясь на данных терапевтического мониторинга. У пациентов с тяжелой печеночной недостаточностью (класс С по шкале Child-Pough) эверолимус не изучался.
Терапевтический мониторинг. Рекомендуется регулярный мониторинг терапевтической концентрации эверолимуса в цельной крови. На основании анализа экспозиция-эффективность и экспозиция-безопасность было выяснено, что у пациентов с С0 >3 нг/мл частота подтвержденного биопсией острого отторжения как почки, так и сердца, была ниже, чем у пациентов с С0 <3 нг/мл. Рекомендуемый верхний предел диапазона терапевтической концентрации эверолимуса составляет 8 нг/мл. Концентрации выше 12 нг/мл не изучались. Концентрации эверолимуса определяли методом хроматографии.
Особенно важно контролировать концентрации эверолимуса в крови у пациентов с печеночной недостаточностью в период одновременного применения сильных индукторов и ингибиторов CYP3А4, при переходе на другую лекарственную форму и/или если доза циклоспорина значительно снижена. Концентрации эверолимуса в крови при применении таблеток диспергируемых могут быть несколько ниже, чем при применении обычных таблеток. Предпочтительно проводить коррекцию режима дозирования препарата Сертикан®, основываясь на значениях С0 эверолимуса, определяемых более чем через 4–5 дней после предыдущего изменения дозы. Поскольку циклоспорин взаимодействует с эверолимусом, возможно снижение концентрации последнего, если концентрация циклоспорина существенно снижается (С0 <50 нг/мл).
Рекомендации по режиму дозирования циклоспорина при комбинированной терапии с препаратом Сертикан® у пациентов после трансплантации почки
Препарат Сертикан® не следует применять длительно с циклоспорином в полной дозе. Снижение дозы циклоспорина у пациентов после трансплантации почки, получавших препарат Сертикан®, приводило к улучшению функции почек. Снижение дозы циклоспорина следует начинать сразу после трансплантации. При этом рекомендуемые значения остаточной концентрации циклоспорина в плазме крови через 12 ч после приема препарата (С0 мониторинг) составляют: в период до 1 мес — 100–200 нг/мл; 2–3 мес — 75–150 нг/мл; 4–5 мес — 50–100 нг/мл; 6–12 мес — 25–50 нг/мл. Перед снижением дозы циклоспорина необходимо удостовериться, что равновесная концентрация эверолимуса в крови (С0) ≥3 нг/мл.
Рекомендации по режиму дозирования циклоспорина при комбинированной терапии с препаратом Сертикан® у пациентов после трансплантации сердца
Для пациентов после трансплантации сердца в поддерживающей фазе следует снижать дозу циклоспорина спустя месяц после трансплантации с целью улучшения функции почек. При прогрессировании нарушения функции почек или в том случае, если расчетное значение Cl креатинина составляет <60 мл/мин, необходима коррекция режима терапии. На основании данных, полученных в клинических исследованиях .установлено, что при назначении эверолимуса у данной категории больных целевые концентрации циклоспорина в плазме по данным С0 мониторинга должны быть следующими: 200–300 нг/мл к 1-му мес после трансплантации, 150–250 нг/мл — через 2 мес, 100–200 нг/мл — через 3–4 мес, 75–150 нг/мл через 5–6 мес, 50–100 нг/мл — через 7–12 мес.
Перед снижением дозы циклоспорина необходимо удостовериться, что равновесная концентрация эверолимуса в крови (С0) равна или выше 3 нг/мл.
При пересадке сердца имеются ограниченные данные относительно дозирования препарата Сертикан® при С0 циклоспорина 50–100 нг/мг через 12 мес после трансплантации.
Инструкции по применению препарата в форме таблеток. Таблетки следует принимать целиком, не дробить перед использованием; запивать стаканом воды.
Инструкции по применению препарата в форме таблеток диспергируемых. Пациентам, которые не могут глотать таблетки, назначают препарат Сертикан® в форме таблеток диспергируемых, из которых готовят дисперсию (взвесь мелких твердых частиц в воде).
Прием с помощью перорального шприца объемом 10 мл. При приеме диспергируемых таблеток можно использовать пероральный шприц. Для этого следует поместить диспергируемые таблетки в шприц. Максимальное количество препарата Сертикан®, из которого можно приготовить дисперсию с объемом воды 10 мл (шприц 10 мл), составляет 1,25 мг. Далее следует добавить воды до отметки 5 мл, подождать 90 с, при этом слегка встряхивая шприц. После образования дисперсии вводят содержимое шприца прямо в рот. Затем следует ополоснуть шприц, набрав 5 мл воды, и ввести содержимое в рот. После этого следует выпить 10–100 мл воды.
Прием из пластмассовой чашки. При приеме диспергируемых таблеток можно использовать пластмассовую чашку. Для этого следует поместить диспергируемые таблетки препарата Сертикан® в пластмассовую чашку, в которой находится приблизительно 25 мл воды. Максимальное количество препарата Сертикан®, из которого можно приготовить дисперсию с объемом воды 25 мл, составляет 1,5 мг. Далее следует оставить чашку примерно на 2 мин, чтобы образовалась дисперсия; перед употреблением взболтать содержимое чашки, чтобы позволить таблеткам раствориться. Затем следует сразу ополоснуть чашку, добавив 25 мл воды, и полностью выпить содержимое.
Введение через назогастральный зонд. При приеме диспергируемых таблеток можно использовать назогастральный зонд. Для этого следует поместить диспергируемые таблетки препарата Сертикан® в небольшой пластмассовый медицинский стакан, содержащий 10 мл воды. Подождать 90 с, слегка вращая стакан. Затем следует набрать дисперсию в шприц и медленно (в течение 40 с) ввести через назогастральный зонд. Затем ополоснуть стакан и шприц 3 раза, набирая по 5 мл воды, и ввести через зонд. После этого следует промыть зонд 10 мл воды. После введения препарата Сертикан® назогастральный зонд следует зажать минимум на 30 мин.
Если циклоспорин в форме микроэмульсии также вводят через назогастральный зонд, это необходимо производить до введения препарата Сертикан®. Не следует смешивать эти 2 препарата.
Побочные действия
Данные о частоте нежелательных реакций были получены в ходе 3 клинических исследований (объединенные данные от 1199 пациентов). В этих 3 рандомизированных, двойных слепых, контролируемых, мультицентровых клинических исследованиях (2 исследования — у пациентов с трансплантацией почки de novo и 1 исследование — у пациентов с трансплантацией сердца de novo), в которых препарат Сертикан® применяли в дозе 1,5 или 3 мг/сут в течение, по крайней мере, 12 мес в комбинации с циклоспорином в форме микроэмульсии и ГКС.
Также данные о частоте возникновения нежелательных реакций получены в 2 открытых исследованиях, в которых изучали эффективность и безопасность применения препарата Сертикан® в дозе 1,5 и 3 мг/сут в комбинации с циклоспорином в сниженной дозе у пациентов с пересадкой почки de novo.
Для определения частоты нежелательных реакций использованы следующие критерии: очень часто (≥1/10); часто (≥1/100, <1/10); иногда (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000).
Ниже перечислены нежелательные реакции, возможно или вероятно имеющие связь с применением препарата Сертикан®, которые были зарегистрированы в клинических исследованиях III фазы (трансплантация почки или сердца).
Инфекционные заболевания: часто — вирусные, бактериальные и грибковые инфекции, сепсис; иногда — раневая инфекция.
Со стороны системы кроветворения и лимфатической системы: очень часто — лейкопения1; часто — тромбоцитопения1, анемия1, коагулопатия, тромботическая тромбоцитопеническая пурпура/гемолитический уремический синдром; иногда — гемолиз.
Со стороны эндокринной системы: иногда — гипогонадизм у мужчин (снижение уровня тестостерона, повышение уровня ЛГ).
Нарушения метаболизма: очень часто — гиперхолестеринемия, гиперлипидемия; часто — гипертриглицеридемия.
Со стороны сосудистой системы: часто — повышение АД, лимфоцеле3, венозный тромбоз.
Со стороны дыхательной системы: часто — пневмония; иногда — интерстициальная болезнь легких, легочный альвеолярный протеиноз.
Со стороны пищеварительной системы: часто — боли в животе, диарея, тошнота, панкреатит, рвота.
Со стороны гепатобилиарной системы: иногда — гепатит, нарушения функции печени, желтуха, повышение уровней АЛТ, ACT , ГГТ.
Со стороны кожи и подкожной клетчатки: часто — ангионевротический отек4, акне, осложнения со стороны хирургической раны; иногда — сыпь.
Со стороны костно-мышечной системы: иногда — миалгия.
Со стороны мочевыделительной системы: часто — инфекции мочевых путей; иногда — некроз почечных канальцев, пиелонефрит.
Прочие: часто — отек, боль.
Примечание:
1 был установлен дозозависимый эффект или данное явление наблюдалось значительно чаще у пациентов, получавших препарат в дозе 3 мг/сут.
2 при трансплантации сердца.
3 при трансплантации почки.
4 преимущественно у пациентов, принимающих одновременно ингибиторы АПФ.
В контролируемых клинических исследованиях, в которых пациентов наблюдали не менее 1 года, лимфома или лимфопролиферативное заболевание развивались у 1,4% пациентов, получающих препарат Сертикан® (1,5 или 3 мг/сут) в комбинации с другими иммунодепрессантами. Злокачественные новообразования кожи были зарегистрированы у 1,3% пациентов, другие типы малигнизации — у 1,2% пациентов.
Возникновение этих нежелательных явлений может зависеть от степени и продолжительности иммуносупрессивной терапии. В основных исследованиях повышение концентрации креатинина в сыворотке наблюдалось более часто у пациентов, получающих препарат Сертикан® в комбинации с полной дозой циклоспорина в форме микроэмульсии, чем у пациентов контрольной группы. Общая частота нежелательных явлений была ниже при назначении уменьшенной дозы циклоспорина в форме микроэмульсии.
Профиль безопасности препарата Сертикан® в исследованиях при применении препарата вместе со сниженной дозой циклоспорина был таким же, как в 3 основных исследованиях, где назначалась стандартная доза циклоспорина. Однако при применении препарата Сертикан® вместе со сниженной дозой циклоспорина реже отмечалось повышение концентрации креатинина в плазме крови и наблюдались более низкое среднее значение и медиана концентрации креатинина в плазме, чем в других исследованиях III фазы.
При применении m-TOR-ингибиторов, включая препарат Сертикан®, редко отмечалось поражение паренхимы легких, например воспаление паренхимы легких (пневмониты) и/или фиброз легких неинфекционной этиологии, в единичных случаях с летальным исходом. В большинстве случаев после отмены терапии препаратом Сертикан® и/или назначения ГКС отмечалось исчезновение данных нежелательных реакций.
Взаимодействие
Эверолимус метаболизируется, главным образом, в печени и в некоторой степени в кишечной стенке при участии изофермента CYP3A4. Также эверолимус является субстратом для белка-переносчика P-гликопротеина. Следовательно, на абсорбцию и последующую элиминацию системно абсорбировавшегося эверолимуса могут оказывать влияние препараты, взаимодействующие с CYP3A4 и/или P-гликопротеином. Сочетанное применение препарата Сертикан® с сильными ингибиторами или индукторами CYP3A4 не рекомендуется. Ингибиторы P-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить концентрацию эверолимуса в сыворотке. In vitro эверолимус являлся конкурентным ингибитором CYP3A4 и CYP2D6, потенциально увеличивающим концентрации в плазме препаратов, выводящихся при участии этих ферментов. Поэтому следует соблюдать осторожность при одновременном применении Сертикана с субстратами CYP3A4 и CYP2D6, имеющими узкий терапевтический индекс. Все исследования взаимодействия in vivo проводились без одновременного применения циклоспорина.
Циклоспорин (ингибитор CYP3A4/P-гликопротеина). Биодоступность эверолимуса значительно увеличивалась при одновременном применении циклоспорина. В исследовании однократной дозы у здоровых добровольцев циклоспорин в виде микроэмульсии (Сандиммун Неорал) увеличивал AUC эверолимуса на 168% (от 46 до 365%) и Сmах — на 82% (от 25 до 158%) по сравнению с применением только одного эверолимуса. При изменении дозы циклоспорина может потребоваться коррекция режима дозирования эверолимуса.
Клиническая значимость влияния препарата Сертикан® на фармакокинетику циклоспорина минимальна у пациентов с пересадкой почки и сердца, получающих циклоспорин в форме микроэмульсии.
Рифампицин (индуктор CYP3A4). У здоровых добровольцев, получавших предшествующую терапию многократными дозами рифампицина, при последующем применении препарата Сертикан® в однократной дозе наблюдалось почти 3-кратное повышение Cl эверолимуса и уменьшение Сmах на 58% и AUC — на 63%. Комбинированное применение Сертикана с рифампицином не рекомендуется.
Аторвастатин (субстрат CYP3A4) или правастатин (субстрат P-гликопротеина). При приеме однократной дозы препарата Сертикан® с аторвастатином или правастатином здоровыми добровольцами клинически значимого влияния на фармакокинетику аторвастатина, правастатина и эверолимуса, а также на общую биореактивность ГМГ-КоА-редуктазы в плазме не обнаружено. Однако эти результаты не могут быть экстраполированы на другие ингибиторы ГМГ-КоА-редуктазы.
Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы, следует мониторировать на предмет развития рабдомиолиза и других нежелательных явлений в соответствии с инструкциями по применению вышеуказанных средств.
Другое возможное взаимодействие. Умеренные ингибиторы CYP3А4 и P-гликопротеина могут повышать концентрацию эверолимуса в крови (например противогрибковые средства: флуконазол; антибиотики группы макролидов — эритромицин; БКК — верапамил, никардипин, дилтиазем; ингибиторы протеазы — нелфинавир, индинавир, ампренавир).
Индукторы CYP3А4 могут повышать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови (например зверобой продырявленный, противосудорожные средства — карбамазепин, фенобарбитал, фенитоин; препараты для лечения ВИЧ — эфавиренз, невирапин.)
Грейпфрут и грейпфрутовый сок влияют на активность цитохрома Р450 и P-гликопротеина, поэтому следует избегать их употребления на фоне применения препарата Сертикан®.
Вакцинация. Иммунодепрессанты могут оказывать влияние на ответ при вакцинации; на фоне лечения препаратом Сертикан® вакцинация может быть менее эффективной. Следует избегать использования живых вакцин.
Передозировка
В экспериментальных исследованиях было показано, что эверолимус обладает низким потенциалом острой токсичности. После приема внутрь препарата в дозе 2000 мг/кг однократно не наблюдалось летальных исходов или тяжелой токсичности у мышей и крыс (контроль по диапазону значений).
Сообщения о случаях передозировки у человека очень ограничены. Имеется единственный факт случайного проглатывания 1,5 мг эверолимуса ребенком в возрасте 2 лет, при этом нежелательных явлений не наблюдалось. При однократном приеме внутрь в дозах до 25 мг у пациентов после трансплантации отмечалась приемлемая переносимость препарата.
Лечение: во всех случаях передозировки следует начать проведение общих поддерживающих мероприятий.
Особые указания
Лечение препаратом Сертикан® должны начинать и проводить только врачи, имеющие опыт проведения иммуносупрессивной терапии после трансплантации органов, и у которых имеется возможность мониторинга концентрации эверолимуса в цельной крови.
В клинических исследованиях препарат Сертикан® применяли одновременно с циклоспорином в форме микроэмульсии, базиликсимабом и ГКС. Применение препарата Сертикан® в комбинации с другими иммуносупрессивными средствами недостаточно изучено.
Применение препарата у пациентов с высоким иммунологическим риском недостаточно изучено.
Не рекомендуется совместное применение препарата Сертикан® с сильными ингибиторами CYP3A4 (например кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (например рифампицин, рифабутин), за исключением тех случаев, когда ожидаемая польза такой терапии превышает потенциальный риск.
Рекомендуется контролировать концентрации эверолимуса в цельной крови при одновременном применении с индукторами или ингибиторами CYP3A4 и после их отмены.
У пациентов, получающих терапию иммуносупрессивными средствами, включая препарат Сертикан®, повышается риск развития лимфом и других злокачественных заболеваний, особенно кожи. Абсолютный риск связан скорее с длительностью и интенсивностью иммуносупрессии, чем с использованием конкретного препарата. Следует регулярно контролировать состояние пациентов для выявления кожных новообразований, рекомендовать сведение к минимуму воздействие УФ излучения, солнечного света и использовать соответствующие солнцезащитные средства.
Гипериммуносупрессия, в т.ч. и при использовании схем терапии на основе препарата Сертикан® предрасполагает к развитию инфекций, особенно вызываемых оппортунистическими патогенами.
Имеются сообщения о развитии фатальных инфекций и сепсиса при применении препарата Сертикан®. В клинических исследованиях препарат Сертикан® проводили профилактику развития пневмонии, вызванной Pneumocystis jiroveci (carini), на протяжении 12 мес после трансплантации.
У больных с постоянно сохраняющейся клинической картиной пневмонии при неэффективности терапии антибиотиками и исключении инфекционных, неопластических и других, не связанных с применением ЛС процессов, следует заподозрить интерстициальное поражение легких.
Профилактику развития цитомегаловирусной инфекции рекомендовали в течение 3 мес после трансплантации, особенно у пациентов с повышенным риском развития этой инфекции.
Совместное применение препарата Сертикан® с циклоспорином в форме микроэмульсии у пациентов после трансплантации связывали с повышением содержания в сыворотке холестерина и триглицеридов, что может потребовать соответствующего лечения. Пациентов, получающих препарат Сертикан®, следует мониторировать с целью выявления гиперлипидемии и при необходимости проводить лечение гиполипидемическими средствами и назначать соответствующую корригирующую диету. Необходимо оценить соотношение риск/польза для пациентов, у которых выявлена гиперлипидемия до начала терапии иммуносупрессивными средствами, включая препарат Сертикан®. Также следует оценить соотношение риск/польза продолжения терапии препаратом Сертикан® у пациентов с тяжелой рефрактерной гиперлипидемией.
Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития нежелательных явлений, вызванных вышеуказанными ЛС.
Влияние на способность управлять автотранспортом и работать с механизмами. Исследования влияния препарата Сертикан® на способность к вождению и работе с механизмами не проводились.
Форма выпуска
Таблетки 0,25 мг. 10 табл. в блистере ПА/Алюм./ПВХ. По 5, б, 10 и 25 блистеров помещены в картонную пачку.
Таблетки 0,5 мг. 10 табл. в блистере ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров помещены в картонную пачку.
Таблетки 0,75мг. 10 табл. в блистере ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров помещены в картонную пачку.
Таблетки 1 мг. 10 табл. в блистере ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров помещены в картонную пачку.
Таблетки диспергируемые, 0,25 мг; 0,5 мг; 0,75мг; 1 мг. 10 табл. в блистере ПА/Алюм./ПВХ. По 5, б, 10 и 25 блистеров помещены в картонную пачку.
Производитель
Новартис Фарма АГ, Швейцария..
Произведено
Новартис Фарма Штейн АГ, Швейцария.
Лихтштрассе, 35, 4056, Базель, Швейцария.
Novartis Pharma AG, Switzerland.
Manufactured by Novartis Pharma Stein AG, Switzerland.
Lichtstrasse 35, 4056 Basel, Switzerland.
Дополнительную информацию о препарате можно получить по адресу
115035, Москва, Садовническая ул., 82/2.
Тел.: (495) 967-12-70; факс: (495) 967-12-68.
Условия отпуска из аптек
По рецепту.
Условия хранения
таблетки 0.25 мг блистер, 1 мг блистер, 0.75 мг блистер, 0.5 мг блистер —
При температуре не выше 30 °C, в оригинальной упаковке.
таблетки диспергируемые 0.1 мг блистер —
В сухом, защищенном от света месте, при температуре не выше 30 °C.
Хранить в недоступном для детей месте.
Срок годности
3 года.
Не применять по истечении срока годности, указанного на упаковке.
Представленная информация о ценах на препараты не является предложением о продаже или покупке товара.
Информация предназначена исключительно для сравнения цен в стационарных аптеках, осуществляющих деятельность в
соответствии со статьей 55 Федерального закона «Об обращении лекарственных средств» от 12.04.2010 № 61-ФЗ.
Сертикан — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер
ЛС-002282
Торговое наименование препарата
Сертикан
Международное непатентованное наименование
Эверолимус
Лекарственная форма
таблетки
Состав
1 таблетка содержит:
активное вещество — эверолимус 0,25 мг, 0,5 мг, 0,75 мг или 1 мг; вспомогательные вещества: бутилгидрокситолуол — (соответственно дозировке активного вещества) 0,025 мг, 0,050 мг, 0,0725 мг, 0,1 мг; лактозы моногидрат — 2,225 мг, 4,450 мг, б,675 мг, 8,90 мг; гипромеллоза — 10,00 мг, 20,00 мг, 30,00 мг, 40,00 мг; магния стеарат — 0,40 мг, 0,625 мг, 0,938 мг, 1,250 мг; кросповидон — 16,00 мг, 25,00 мг, 37,50 мг, 50,00 мг; лактоза безводная — 51,10 мг, 74,375 мг, 111,562 мг, 148,75 мг.
Описание
Таблетки 0,25 мг: круглые плоско цилиндрические от белого до желтоватого цвета таблетки со скошенными краями; допускается мраморность; на одной стороне нанесена гравировка «С», на другой — «NVR».
Таблетки 0,5 мг: круглые плоскоцилиндрические от белого до желтоватого цвета таблетки со скошенными краями; допускается мраморность; на одной стороне нанесена гравировка «СН», на другой-«NVR»
Таблетки 0,75 мг: круглые плоскоцилиндрические от белого до желтоватого цвета таблетки со скошенными краями; допускается мраморность; на одной стороне нанесена гравировка «СL», на другой — «NVR».
Фармакотерапевтическая группа
иммунодепрессивное средство
Код АТХ
L04AA18
Фармакодинамика:
Активное вещество препарата Сертикан® — эверолимус — является ингибитором пролиферативного сигнала. Эверолимус оказывает иммуносупрессивный эффект путем ингибирования антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими интерлейкинами Т-клеток, например, интерлейкином-2 и интерлейкином-15. Эверолимус ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием этих факторов роста Т-клеток с соответствующими рецепторами. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
На молекулярном уровне эверолимус образует комплекс с цитоплазматическим белком FKBP-12. В присутствии эверолимуса происходит ингибирование фосфорилирования р70 S6 киназы, стимулируемой фактором роста. Поскольку фосфорилирование р70 S6 киназы находится под контролем FRAP (так называемого m-TOR), эти данные позволяют предположить, что комплекс эверолимус-РКВР-12 связывается с FRAP. FRAP — это ключевой регуляторный белок, который управляет клеточным метаболизмом, ростом и пролиферацией; нарушение функции FRAP, таким образом, объясняет остановку клеточного цикла, вызываемую эверолимусом. Эверолимус имеет, таким образом, отличный от циклоспорина механизм действия. В доклинических моделях аллотрансплантации была показана более высокая эффективность комбинации эверолимуса с циклоспорином, чем при изолированном применении каждого из них. Эффект эверолимуса не ограничивается влиянием на Т-клетки. Он ингибирует стимулируемую факторами роста пролиферацию как гемопоэтических, так и негемопоэтических клеток (например, клеток гладкой мускулатуры сосудов).
Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, которая запускается при повреждении эндотелиальных клеток и приводит к образованию неоинтимы, играет ключевую роль в патогенезе хронического отторжения. В экспериментальных исследованиях показано ингибирование образования неоинтимы у крыс с аллотрансплантатом аорты.
Фармакокинетика:
Всасывание
После приема внутрь максимальная концентрация (Сmах ) достигается через 1-2 часа. У пациентов после трансплантации концентрация эверолимуса в крови пропорциональна принятой дозе в диапазоне доз от 0.25 мг до 15 мг. На основании показателя AUC относительная биодоступность диспергируемых таблеток по сравнению с обычной таблеткой составляет 0.90 (90% CI 0,76-1,07).
Влияние пищи: Сmах и AUC эверолимуса уменьшались на 60% и на 16%, соответственно, при приеме таблетированной лекарственной формы с очень жирной пищей. Чтобы свести к минимуму вариабельность, препарат Сертикан® следует принимать или только с пищей или только без нее.
Распределение
Соотношение концентрации эверолимуса в крови и его концентрации в плазме находится в пределах от 17% до 73% и зависит от значений концентрации в диапазоне от 5 до 5000 нг/мл. У здоровых добровольцев и пациентов с нарушениями функции печени легкой и средней степени тяжести связывание с белками плазмы крови составляет приблизительно 74%.
Объем распределения в конечной фазе (Vz/F) у пациентов после трансплантации почки, находящихся на поддерживающей терапии, составляет 342 ± 107 л.
Метаболизм
Эверолимус является субстратом изофермента CYP3A4 и Р-гликопротеина.
После приема внутрь в системном кровотоке определяются эверолимус и его шесть основных метаболитов, в т. ч. три моногидроксилированных метаболита, два продукта гидролиза с разорванным кольцом и фосфодиэтилхолиновый конъюгат эверолимуса. Эти метаболиты также определялись при изучении токсичности в исследованиях у животных, где их активность была приблизительно в сто раз ниже исходного вещества, что позволяет предположить, что именно эверолимус обладает фармакологической активностью.
Выведение
После введения однократной дозы меченого радиоактивной меткой эверолимуса пациентам после трансплантации, получающим циклоспорин, большая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось с мочой. Неизмененное вещество не определялось ни в моче, ни в кале.
Фармакокинетика в равновесном состоянии
Фармакокинетика у пациентов с трансплантатами почек и сердца, получающих эверолимус 2 раза в сутки одновременно с циклоспорином в форме микроэмульсии, была сопоставима. Равновесное состояние достигалось на 4 день с кумуляцией в крови в концентрациях, которые в 2-3 раза превышали концентрации в крови после применения первой дозы. После приема препарата Tmax составляет 1-2 часа. При дозах 0,75 мг и 1,5 мг 2 раза в сутки средние значения Сmах составляют 11,1 ± 4,6 и 20,3 ± 8,0 нг/мл, средние значения AUC — 75 ± 31 и 131 ± 59 нг*ч/мл, соответственно. При дозах 0,75 мг и 1,5 мг 2 раза в сутки C0 эверолимуса в крови составляют в среднем 4,1 ± 2,1 и 7,1 ± 4,6 нг/мл, соответственно (C0 — базальная концентрация, определяемая утром до приема очередной дозы). Экспозиция эверолимуса остается стабильной все время в течение первого года после трансплантации. C0 в высокой степени коррелировала с AUC с коэффициентом корреляции, колеблющимся между 0,86 и 0,94. На основании анализа фармакокинетики у пациентов после трансплантации общий клиренс (CL/F) составляет 8,8 л/ч (разброс составляет 27%), центральный объем распределения (Vc/F) составляет 110 л (разброс составляет 36 %). Период полувыведения составляет 28 ±7 ч.
Фармакокинетика у отдельных групп пациентов
Нарушения функции печени
По сравнению с фармакокинетикой эверолимуса у здоровых добровольцев, при применении препарата пациентами с легкими нарушениями функции печени (класс А Чайлд-Пыо) AUC эверолимуса увеличивается примерно в 1,6 раз, пациентами с нарушениями функции печени средней степени тяжести (класс В
Чайлд-Пью) — в 2,1 — 3,3 раз, пациентами с тяжелыми нарушениями функции печени (класс С Чайлд-Пью) — в 3,6 раз. У пациентов с печеночной недостаточностью легкой, средней и тяжелой степени тяжести период полувыведения эверолимуса составлял соответственно 52, 59 и 78 часов.
Увеличение периода полувыведения эверолимуса способствует отсроченному достижению равновесного состояния.
У пациентов с печеночной недостаточностью легкой степени (Чайлд-Пью класс А) дозу препарата Сертикан® следует уменьшить приблизительно до 2/3 по сравнению с обычной дозой. У пациентов с печеночной недостаточностью средней степени тяжести (Чайлд-Пью класс В) доза эверолимуса должна быть уменьшена приблизительно в 2 раза по сравнению с обычной. У пациентов с печеночной недостаточностью тяжелой степени (Чайлд-Пью класс С) доза эверолимуса должна быть уменьшена приблизительно до 1/3 от обычной.
Дальнейшее титрование дозы проводят, основываясь на данных терапевтического мониторинга.
Нарушения функции почек
Посттрансплантационная почечная недостаточность (клиренс креатинина 11-107 мл/мин) не влияла на фармакокинетические параметры эверолимуса.
Педиатрия
Клиренс эверолимуса (CL/F) повышался в линейной зависимости от возраста пациента (от 1 до 16 лет), площади поверхности тела (0,49-1,92 м2) и массы тела (11-77 кг). В равновесном состоянии клиренс составлял 10,2 ± 3,0 л/ч/м2 , период полувыведения — 30 ± 11 ч.
Девятнадцать de novo пациентов после трансплантации почки в возрасте от 1 года до 16 лет получали препарат Сертикан® в форме таблеток, диспергируемых в дозе 0,8 мг/м2 (максимально -1,5 мг) 2 раза в сутки с циклоспорином в форме микроэмульсии. У этих пациентов AUC эверолимуса составляла 87 ± 27 нг*ч/мл, что соответствовало таковой у взрослых, получающих 0,75 мг 2 раза в сутки. В равновесном состоянии базальная концентрация (C0) эверолимуса составляла 4,4 ±1,7 нг/мл.
Взрослые пациенты
У взрослых пациентов в возрасте от 16 до 70 лет наблюдалось снижение клиренса эверолимуса на 0,33 % в год.
Корректировки дозы не требуется.
Пациенты негроидной расы
На основании анализа фармакокинетики эверолимуса в популяции, общий клиренс был выше у пациентов негроидной расы в среднем на 20 %.
Влияние экспозиции на эффективность
У реципиентов почки и сердца в течение 6 месяцев после трансплантации была выявлена связь между базальной концентрацией эверолимуса (C0) и частотой подтвержденного биопсией острого отторжения и тромбоцитопении.
У реципиентов печени связь между концентрацией эверолимуса в крови и клиническими проявлениями менее определенная, однако, более высокая концентрация эверолимуса не коррелирует с повышением частоты нежелательных явлений.
Таблица 1. Влияние экспозиции на эффективность препарата Сертикан® у пациентов после трансплантации
|
Трансплантация почки |
|||||
|
С0 (нг/мл) |
≤3,4 |
3,5-4,5 |
4,6-5,7 |
5,8-7,7 |
7,8-15,0 |
|
Отсутствие отторжения |
68% |
81% |
86% |
81% |
91% |
|
Тромбоцитопения (<100 х 109/л) |
10% |
9% |
7% |
14% |
17% |
|
Трансплантация сердца |
|||||
|
С0 (нг/мл) |
≤3,5 |
3,6-5,3 |
5,4-7,3 |
7,4-10,2 |
10,3-21,8 |
|
Отсутствие отторжения |
65% |
69% |
80% |
85% |
85% |
|
Тромбоцитепения (< 75 х 109/л) |
5% |
5% |
6% |
8% |
9% |
|
Трансплантация печени |
|||||
|
С0 (нг/мл) |
≤3 |
3-8 |
≥8 |
||
|
Отсутствие отторжения |
88% |
98% |
92% |
||
|
Тромбоцитопения |
35% |
13% |
18% |
||
|
Нейтропения |
70% |
31% |
44% |
Показания:
-Трансплантация почки и сердца
Профилактика отторжения трансплантата у взрослых реципиентов почки и сердца с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию циклоспорином в форме микроэмульсии и глюкокортикостероидами.
-Трансплантация печени
Профилактика отторжения трансплантата у реципиентов печени с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию такролимусом и глюкокортикостероидами.
Противопоказания:
— Повышенная чувствительность к эверолимусу, сиролимусу или другим компонентам препарата.
— Редкие наследственные нарушения, связанные с непереносимостью галактозы, тяжелой лактазной недостаточностью или глюкозо-галактозной мальабсорбцией.
— Дети и подростки до 18 лет.
С осторожностью:
— Препарат следует с осторожностью применять у пациентов с нарушениями функции печени.
Рекомендуется тщательно титровать и мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
— Применение препарата Сертикан® с полной дозой циклоспорина у пациентов после трансплантации сердца и почек повышает риск развития дисфункции почек.
Чтобы избежать развития такой дисфункции, необходимо применять препарат со сниженными дозами циклоспорина. Всем пациентам рекомендуется регулярный контроль функции почек. При повышении концентрации креатинина в сыворотке следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина.
— Следует соблюдать осторожность при одновременном применении других лекарственных средств, оказывающих отрицательное влияние на функцию почек.
Данные о применении препарата Сертикан® без ингибиторов кальциневрина (ИКН) ограничены. У пациентов, которым было отменено лечение ИКН, отмечалось увеличение риска острого отторжения по сравнению с теми, кто продолжил лечение данными препаратами.
В клинических испытаниях препарат Сертикан® применялся в сочетании с микроэмульсией циклоспорина или с такролимусом, базиликсимабом и глюкокортикостероидами. Отсутствуют адекватные исследования комбинации препарата Сертикан® с другими, чем указано выше, препаратами.
— Следует соблюдать осторожность при применении индукционной терапии тимоглобулином (кроличий анти-тимоцитарный глобулин) и схемы иммуносупрессии, включающей препарат Сертикан® /циклоспорин/глюкокортикостероиды. По данным клинических исследований у реципиентов сердца, одновременное применение индукционной терапии тимоглобулином и схемы препарат Сертикан® /циклоспорин/глюкокортикостероиды (при концентрациях, рекомендуемых при трансплантации сердца), приводило к повышению числа случаев серьезных инфекционных заболеваний в течение первых трех месяцев после трансплантации. Данные эпизоды ассоциировались с более высокой смертностью среди пациентов, требующих госпитализации и относящихся к группе риска развития гипериммуносупрессии.
— Следует соблюдать осторожность при одновременном применении препарата Сертикан® с субстратами изофермента CYP3A4 с узким терапевтическим индексом (например, пимозид, терфенадин, астемизол, цизаприд, хинидин или производные алколоидов спорыньи).
Одновременное применение препарата Сертикан® с сильными ингибиторами или индукторами изофермента CYP3A4 не рекомендуется (например, кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир и/или рифампицин, рифабутин).
Беременность и лактация:
Данные по применению препарата Сертикан® у беременных женщин отсутствуют. В экспериментальных исследованиях показано наличие токсического влияния на репродуктивность, включая эмбриотоксичность и фетотоксичность. Неизвестно, существует ли потенциальный риск для человека. Не следует применять препарат у беременных женщин, за исключением тех случаев, когда ожидаемая польза от терапии превышает потенциальный риск для плода. Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения препаратом Сертикан® и в течение 8 недель после окончания терапии.
Неизвестно, выделяется ли эверолимус с грудным молоком у человека. В экспериментальных исследованиях было показано, что эверолимус и/или его метаболиты быстро проникали в молоко лактирующих крыс. Поэтому женщинам, получающим препарат Сертикан®, не следует кормить грудью.
Способ применения и дозы:
Препарат принимает внутрь. Таблетки следует принимать целиком, не дробить перед использованием; запивать стаканом воды.
Взрослые
Рекомендуемая начальная доза препарата для пациентов с трансплантатами почек и сердца составляет 0,75 мг 2 раза в сутки; следует начать применение препарата как можно скорее после трансплантации. Рекомендуемая начальная доза препарата для пациентов с трансплантатом печени составляет 1,0 мг 2 раза в сутки, терапию начинают примерно через 4 недели после трансплантации.
Суточную дозу препарата Сертикан® всегда разделяют на 2 приема; препарат принимают или всегда вместе с пищей, или всегда без нее. Препарат Сертикан® принимают в одно и то же время с циклоспорином в форме микроэмульсии или такролимусом. Может потребоваться коррекция режима дозирования препарата Сертикан® с учетом достигнутых концентраций в плазме крови, переносимости, индивидуального ответа на лечение, изменений сопутствующей медикаментозной терапии и клинической ситуации. Коррекцию режима дозирования можно проводить с интервалами 4-5 дней.
Представители негроидной расы
Частота случаев развития острого отторжения трансплантата почки, подтвержденного биопсией, была выше у представителей негроидной расы по сравнению с остальными. Согласно имеющейся ограниченной информации представителям негроидной расы может потребоваться более высокая доза препарата Сертикан® для достижения такого же эффекта, как у остальных пациентов, получающих препарат в рекомендуемых для взрослых дозах.
Имеющихся в настоящее время данных по эффективности и безопасности недостаточно для предоставления специфических рекомендаций по применении эверолимуса у представителей негроидной расы.
Пациенты пожилого возраста (≥ 65 лет)
Клинический опыт применения препарата Сертикан® у пациентов в возрасте ≥ 65 лет ограничен. Тем не менее, явных различий фармакокинетики эверолимуса у пациентов в возрасте ≥65-70 лет по сравнению с более молодыми взрослыми пациентами не отмечалось.
Пациенты с нарушениями функции почек
У пациентов с нарушениями функции почек коррекция дозы не требуется.
Пациенты с нарушениями функции печени
У пациентов с печеночной недостаточностью следует тщательно мониторировать базальную (С0 ) концентрацию эверолимуса в цельной крови. У пациентов с печеночной недостаточностью легкой степени (Чайлд-Пью класс А) дозу препарата Сертикан® следует уменьшить приблизительно до 2/3 по сравнению с обычной дозой. У пациентов с печеночной недостаточностью средней степени тяжести (Чайлд-Пью класс В) доза эверолимуса должна быть уменьшена приблизительно в 2 раза по сравнению с обычной дозой. У пациентов с печеночной недостаточностью тяжелой степени (Чайлд-Пью класс С) доза эверолимуса должна быть уменьшена приблизительно до 1/3 по сравнению с обычной дозой. Дальнейшее титрование дозы проводят, основываясь на данных терапевтического мониторинга.
В таблице 2 представлены сниженные дозы, округленные до наиболее близкой по эффективности дозировки таблеток:
Таблица 2. Уменьшение дозы препарата Сертикан® у пациентов с нарушениями функции печени
|
Нормльная функция печени |
Печеночная недостаточность легкой степени (Чайлд -Пыо А) |
Печеночная недостаточность средней степени (Чайлд -Пыо B) |
Печеночная недостаточность тяжелой степени (Чайлд -Пыо C) |
|
|
Трансплантация почки и сердца |
0,75 мг 2 раза в сутки |
0,5 мг 2 раза в сутки |
0,5 мг 2 раза в сутки |
0,25 мг 2 раза в сутки |
|
Трансплантация печени |
1 мг 2 раза в сутки |
0,75 мг 2 раза в сутки |
0,5 мг 2 раза в сутки |
0,5 мг 2 раза в сутки |
Терапевтический мониторинг
Рекомендуется регулярный мониторинг терапевтической концентрации эверолимуса в цельной крови. На основании анализа экспозиция- эффективность и экспозиция-безопасность было установлено, что у пациентов с С0 ≥ 3,0 нг/мл частота подтвержденного биопсией острого отторжения трансплантатов почек, сердца и печени была ниже, чем у пациентов с С0 < 3,0 нг/мл. Рекомендуемый верхний предел диапазона терапевтической концентрации эверолимуса составляет 8 нг/мл. Концентрации выше 12 нг/мл не изучались. Рекомендуемые терапевтические уровни эверолимуса основаны на применении метода хроматографии.
Особенно важно контролировать концентрации эверолимуса в крови у пациентов с печеночной недостаточностью в период одновременного применения мощных индукторов и ингибиторов изофермента CYP3A4, при переходе на другую лекарственную форму и/или если доза циклоспорина значительно снижена. Концентрации эверолимуса в крови при применении таблеток диспергируемых могут быть несколько ниже, чем при применении обычных таблеток. Предпочтительно проводить коррекцию режима дозирования препарата Сертикан®, основываясь на значениях С0 эверолимуса, определяемых более чем через 4-5 дней после предыдущего изменения дозы. Поскольку циклоспорин взаимодействует с эверолимусом, возможно снижение концентрации последнего, если концентрация циклоспорина существенно снижается (С0<50 нг/мл). Рекомендации по режиму дозирования циклоспорина при комбинированной терапии с препаратом Сертикан® у пациентов после трансплантации почки.
Препарат Сертикан® не следует применять длительно с циклоспорином в полной дозе. Снижение дозы циклоспорина у пациентов после трансплантации почки, получавших препарат Сертикан®, приводило к улучшению функции почек. Снижение дозы циклоспорина следует начинать сразу после трансплантации. При этом рекомендуемые значения остаточной концентрации циклоспорина в плазме крови через 12 часов после приемапрепарата ( С0 мониторинг) составляют: в период до 1 месяца — 100-200 нг/мл; 2-3 месяцев — 75-150 нг/мл; 4-5 месяцев -50-100 нг/мл; 6-12 месяцев — 25-50 нг/мл. Перед снижением дозы циклоспорина необходимо удостовериться, что равновесная концентрация эверолимуса в крови (С0) равна или выше 3 нг/мл.
Рекомендации по режиму дозирования циклоспорина при комбинированной терапии с препаратом Сертикан® у пациентов после трансплантации сердца.
Для пациентов после трансплантации сердца в поддерживающей фазе следует снижать дозу циклоспорина спустя месяц после трансплантации с целью улучшения функции почек. При прогрессировании нарушения функции почек или в том случае, если расчетное значение клиренса креатинина составляет <60 мл/мин, необходима коррекция режима терапии.
На основании данных, полученных в клинических исследованиях, установлено, что при применении эверолимуса у данной категории пациентов целевые концентрации циклоспорина в плазме по данным С0мониторинга должны быть следующими: 200-350 нг/мл к 1 месяцу после трансплантации, 150-250 нг/мл через 2 месяца, 100-200 нг/мл через 3-4 месяца, 75-150 нг/мл через 5-6 месяцев, 50-100 нг/мл через 7-12 месяцев.
Перед снижением дозы циклоспорина необходимо удостовериться, что равновесная концентрация эверолимуса в крови (С0) равна или выше 3 нг/мл.
Рекомендации по режиму дозирования такролимуса при комбинированной терапии с препаратом Сертикан® у пациентов после трансплантации печени.
У пациентов после трансплантации печени следует снижать дозу такролимуса с целью минимизировать токсическое влияние ингибиторов кальциневрина на почки. Снижение дозы такролимуса следует начинать примерно через 3 недели после начала комбинированной терапии с препаратом Сертикан®. Дозу такролимуса следует снижать до достижения в крови концентрации такролимуса — 3-5 нг/мл. При применении препарата Сертикан® у пациентов после трансплантации печени в комбинации со сниженной дозой такролимуса не было выявлено ухудшения функции почек по сравнению со стандартной дозой такролимуса. В клинических исследованиях не проводилось изучение одновременного применения препарата Сертикан® с полной дозой такролимуса. Пациентам, получающим препарат Сертикан® одновременно с такролимусом, рекомендуется регулярный контроль функции почек.
В клиническом испытании у реципиентов печени отмена терапии такролимусом ассоциировалась с повышением риска острого отторжения трансплантата.
Побочные эффекты:
Данные о частоте нежелательных реакций были получены в ходе пяти клинических испытаний препарата Сертикан® в сочетании с циклоспорином у 2497 реципиентов почки и трех клинических испытаниях у 1538 реципиентов сердца. У 719 реципиентов печени в одном клиническом испытании препарат Сертикан® применяли в сочетании с такролимусом.
Для определения частоты нежелательных реакций использованы следующие критерии: очень часто (≥ 1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100); редко (≥1/10 000, <1/1000); очень редко (<1/10 000); частота неизвестна8.
Ниже перечислены нежелательные реакции, возможно или вероятно имеющие связь с применением препарата Сертикан®, которые были зарегистрированы в клинических исследованиях фазы III. Тип выявляемых нежелательных реакций был примерно одинаков у пациентов с пересадкой почки, сердца и печени.
Инфекционные и паразитарные заболевания: очень часто — вирусные, бактериальные и грибковые инфекции, инфекции верхних дыхательных путей и нижних дыхательных путей (в т. ч. пневмония)1, инфекции мочевыводящих путей2; часто — сепсис, раневая инфекция.
Нарушения со стороны системы крови и лимфатической системы:очень часто — анемия/эритроцитопения, лейкопения, тромбоцитопения; часто — панцитопения, тромботическая тромбоцитопеническая пурпура/гемолитический уремический синдром.
Нарушения со стороны эндокринной системы: нечасто — гипогонадизм у мужчин (снижение концентрации тестостерона, повышение концентрации фолликулостимулирующего гормона (ФСГ) и лютеинизирующего гормона (ЛГ) в плазме крови).
Нарушения со стороны обмена веществ: очень часто — гиперлипидемия (холестерин, триглицериды), впервые выявленный сахарный диабет, гипокалиемия.
Нарушения со стороны сердца: — выпот в полость перикарда3, часто -тахикардия.
Нарушения со стороны сосудов: очень часто — повышение артериального давления, венозный тромбоз; часто -лимфоцеле4, носовые кровотечения, тромбоз сосудов трансплантированной почки; частота неизвестна -лейкоцитокластический васкулит. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: очень часто — плевральный выпот1, кашель1, одышка1; нечасто — интерстициальная болезнь легких5, частота неизвестна — легочный альвеолярный протеиноз.
Нарушения со стороны пищеварительной системы: очень часто — боли в животе, диарея, тошнота, рвота; часто панкреатит, стоматит/изъязвление слизистой оболочки полости рта, боль в области ротоглотки.
Нарушения со стороны печени и желчевыводящих путей: нечасто — гепатит неинфекционной этиологии, желтуха.
Нарушения со стороны кожи и подкожных тканей: часто ангионевротический отек6, акне, сыпь, частота неизвестна — эритродермия.
Нарушения со стороны скелетно-мышечной и соединительной ткани: часто — миалгия, артралгия.
Нарушения со стороны почек и мочевыводящих путей: часто протеинурия2, некроз почечных канальцев7.
Нарушения со стороны половых органов и молочной железы: часто — эректильная дисфункция.
Нарушения со стороны нервной системы: очень часто — головная боль.
Нарушения психики: очень часто -бессонница, тревожность. Доброкачественные, злокачественные и неуточненные заболевания: часто — злокачественные и неуточненные новообразования, злокачественные н неуточненные неоплазии кожи; нечасто: лимфомы/посттрансплантацнонный лимфопролиферативный синдром.
Общие расстройства и нарушения в месте введения: очень часто — боль, лихорадка, периферические отеки, замедление репаративных процессов, часто — послеоперационные грыжи.
Лабораторные и инструментальные данные: часто — повышение активности ферментов печени (аланинаминотрасферазы (АЛТ), аспартатаминотрасферазы (ACT), гамма-глутамилтранферазы (ГГТ)).
Ссылки:
1-встречается часто при трансплантации почек и печени
2-встречается часто при трансплантации сердца и печени
3-встречается часто при трансплантации сердца
4-встречается часто при трансплантации почек и сердца
5-от 0,4 до 2,5% по данным клинических исследований в зависимости от показания и режима дозирования (по результатам поиска в базе данных безопасности по стандартному MedDRA запросу по термину «интерстициальная болезнь легких»)
6-в основном у пациентов, получающих лечение ингибиторами АПФ
7-встречается часто при трансплантации почек
8-исходя из доступных данных, выявленных в ходе постмаркетингово наблюдения и при применении препарата в клинической практике, оценка частоты невозможна
В контролируемых клинических исследованиях с участием 3256 пациентов, получающих препарат Сертикан® в комбинации с другими иммунодепрессантами и находящихся под наблюдением не менее одного года, случаи малигнизации отмечались у 3,1%, у 1,0% — злокачественные новообразования кожи, лимфома или лимфопролиферативные заболевания развивались у 0,60% пациентов.
Возникновение этих нежелательных явлений может зависеть от степени и продолжительности иммуносупрессивной терапии. В исследованиях повышение концентрации креатинина в сыворотке наблюдалось более часто у пациентов, получающих препарат Сертикан® в комбинации с полной дозой циклоспорина в форме микроэмульсии, чем у пациентов контрольной группы.
За исключением повышения креатинина в сыворотке крови, профиль безопасности препарата в исследованиях применения препарата Сертикан® со сниженной дозой циклоспорина был таким же, как в 3-ех основных исследованиях, где применялась стандартная доза циклоспорина, однако при этом общая частота возникновения нежелательных явлений была ниже.
При применении m-TOR -ингибиторов, включая эверолимус, редко отмечалось поражение паренхимы легких, например воспаление паренхимы легких (пневмониты) и/или фиброз легких неинфекционной этиологии, в единичных случаях с летальным исходом. В большинстве случаев после отмены терапии препаратом Сертикан® и/или применения глюкокортикостероидов отмечалось исчезновение данных нежелательных реакций.
Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты, не указанные в инструкции, сообщите об этом врачу.
Передозировка:
В экспериментальных исследованиях было показано, что эверолимус обладает низким потенциалом острой токсичности. После однократных доз 2000 мг/кг перорально не наблюдалось летальных исходов или тяжелой токсичности у мышей и крыс (контроль по диапазону значений). Сообщения о случаях передозировки у человека очень ограничены. Имеется единственный факт случайного проглатывания 1,5 мг эверолимуса ребенком в возрасте 2 лет, при этом нежелательных явлений не наблюдалось. При однократном приеме внутрь в дозах вплоть до 25 мг у пациентов после трансплантации отмечалась приемлемая переносимость препарата. Во всех случаях передозировки следует начать проведение общих поддерживающих мероприятий.
Взаимодействие:
Эверолимус метаболизируется главным образом в печени и в некоторой степени в кишечной стенке при участии изофермента CYP3A4. Также эверолимус является субстратом для белка-переносчика Р-гликопротеина.
Следовательно, на абсорбцию и последующую элиминацию системно абсорбировавшегося эверолимуса могут оказывать влияние препараты, взаимодействующие с изоферментом CYP3A4 и/или Р-гликопротеином.
В случае если пациент принимает препарат Сертикан® одновременно с пероральными субстратами изофермента CYP3A4, необходимо отслеживать нежелательные явления, которые описаны в информации о лекарственном препарате соответствующего субстрата изофермента CYP3A4 для перорального применения. Все исследования взаимодействия in vivo проводились без одновременного применения циклоспорина.
Одновременное применение с ингибиторами АПФ увеличивает риск развития ангионевротического отека.
Выявленные нежелательные взаимодействия (одновременное применение не рекомендуется)
Рифампицин (индуктор изофермента CYP3A4)
У здоровых добровольцев, получавших предшествующую терапию многократными дозами рифампицина, при последующем применении препарата в однократной дозе наблюдалось почти 3-кратное повышение клиренса эверолимуса и уменьшение Сmах на 58% и AUC — на 63%. Комбинированное применение препарата Сертикан® с рифампицином не рекомендуется.
Кетоконазол (ингибитор изофермента CYP3A4)
Предварительное лечение здоровых добровольцев многократными дозами кетоконазола с последующей однократной дозой препарата Сертикан® приводило к увеличению Сmах эверолимуса почти в 4 раза, a AUC — в 15 раз.
Ожидаемые нежелательные взаимодействия (одновременное применение не рекомендуется)
Одновременное применение препарата Сертикан® с мощными ингибиторами или индукторами изофермента CYP3A4 не рекомендуется (например, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир, рифабутин).
Лекарственные взаимодействия, которые следует учитывать при одновременном применении
Препараты, влияющие на активность препарата Сертикан®
Циклоспорин (ингибитор изофермента CYP3A4/ Р-гликопротеина)
Биодоступность эверолимуса значительно увеличивалась при одновременном применении циклоспорина. В исследовании однократной дозы у здоровых добровольцев циклоспорин в виде микроэмульсии (Сандиммун Неорал) увеличивал AUC эверолимуса на 168% (от 46% до 365%) и Сmах — на 82% (от 25% до 158%) по сравнению с применением только одного эверолимуса. При изменении дозы циклоспорина может потребоваться коррекция режима дозирования эверолимуса.
Эритромицин (ингибитор изофермента CYP3A4)
Предварительное лечение здоровых добровольцев многократными дозами эритромицина с последующей однократной дозой препарата Сертикан® приводило к увеличению Cmax эверолимуса в 2 раза, a AUC — в 4,5 раз.
Верапамил (ингибитор изофермента CYP3A4)
При предварительном лечении здоровых добровольцев многократными дозами верапамила с последующей однократной дозой препарата Сертикан®, Сmах эверолимуса возрастала в 2,3 раза, a AUC -в 3,5 раз.
Влияние препарата Сертикан® на активность одновременно применяемых препаратов
Клиническая значимость влияния препарата Сертикан® на фармакокинетику циклоспорина минимальна у пациентов с трансплантатом почки и сердца, получающих циклоспорин в форме микроэмульсии.
Октреотид
При одновременном применении эверолимуса и октреотида Cmin последнего увеличивалась со средним геометрическим отношением (эверолимус к плацебо) в 1,47 раз.
Аторвастатин (субстрат изофермента CYP3A4) и правастатын (субстрат Р-гликопротеина)
Прием однократной дозы препарата с аторвастатином или правастатином здоровыми добровольцами клинически значимо не влиял на фармакокинетику аторвастатина, правастатина и эверолимуса, так же как и на общую биореактивность ГМГ-КоА-редуктазы в плазме. Однако, эти результаты не могут быть экстраполированы на другие ингибиторы ГМГ-КоА-редуктазы.
Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы, следует наблюдать на предмет развития рабдомиолиза и других нежелательных явлений в соответствии с инструкциями по применению вышеуказанных средств.
Мидазолам (субстрат изофермента CYP3A4A)
В исследованиях эверолимус показывает слабую ингибиторную активность в отношении изофермента CYP3A4A. У здоровых добровольцев, получавших предшествующую терапию многократными дозами эверолимуса, при последующем применении мидазолама в однократной дозе наблюдалось повышение Сmах мидазолама в 1,25 раз и повышение АиС(терминальной) мидазолама в 1,3 раза. Период полувыведения мидазолама не изменился.
Ожидаемые лекарственные взаимодействия, которые следует учитывать при одновременном применении
Препараты, влияющие на активность препарата Сертикан®
Умеренные индукторы изофермента CYP3A4 могут повышать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови (например, Зверобой продырявленный; противосудорожные средства: карбамазепин, фенобарбитал, фенитоин; противовирусные средства, в том числе для лечения ВИЧ-инфекции: эфавиренц, невирапин).
Умеренные ингибиторы изофермента CYP3A4 и Р-гликопротеина могут повышать концентрацию эверолимуса в крови (например, противогрибковые средства — флуконазол; блокаторы «медленных» кальциевых каналов никардипин, дилтиазем; противовирусные средства, в том числе для лечения ВИЧ-инфекции: нелфинавир, индинавир, ампренавир).
Ингибиторы Р-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить концентрацию эверолимуса в сыворотке.
In vitro эверолимус являлся конкурентным ингибитором изоферментов CYP3A4 и CYP2D6, потенциально увеличивающим концентрации в плазме препаратов, выводящихся при участии этих ферментов. Поэтому следует соблюдать осторожность при одновременном применении препарата Сертикан® с субстратами изоферментов CYP3A4 и CYP2D6, имеющими узкий терапевтический индекс (например, пимозид, терфенадин, астемизол, цизаприд, хинидин или производные алколоидов спорыньи).
Такролимус (ингибитор изофермента CYP3A4)
Такролимус ингибирует только CYP3A4, не влияя на активность Р-гликопротеина, и, таким образом, не оказывает клинически значимого влияния на фармакокинетику эверолимуса.
Другое возможное взаимодействие
Грейпфрут и грейпфрутовый сок влияют на активность цитохрома Р450 и Р-гликопротеина, поэтому следует избегать их употребления на фоне применения препарата Сертикан®.
Вакцинация
Иммунодепрессанты могут оказывать влияние на ответ при вакцинации; на фоне лечения препаратом вакцинация может быть менее эффективной. Следует избегать использования живых вакцин.
Особые указания:
Применение у детей
Данных по применению препарата Сертикан® у детей и подростков недостаточно для того, чтобы рекомендовать использование препарата у данной категории пациентов. Однако, имеются ограниченные исследования применения препарата Сертикан® в педиатрии при трансплантации почки.
Лечение препаратом Сертикан® должны начинать и проводить только врачи, имеющие опыт проведения иммуносупрессивной терапии после трансплантации органов. Необходимо регулярно определять концентрацию эверолимуса в цельной крови. Применение препарата Сертикан® у пациентов с высоким иммунологическим риском недостаточно изучено.
Не рекомендуется одновременное применение препарата с мощными ингибиторами изофермента CYP3A4 (например, кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (например, рифампицин, рифабутин), за исключением тех случаев, когда ожидаемая польза такой терапии превышает потенциальный риск. Рекомендуется контролировать концентрации эверолимуса в цельной крови при одновременном применении с индукторами или ингибиторами изофермента CYP3A4 и после их отмены.
У пациентов, получающих терапию иммуносупрессивными средствами, включая препарат Сертикан®, повышается риск развития лимфом и других злокачественных заболеваний, особенно кожи. Абсолютный риск связан скорее с длительностью и интенсивностью иммуносупрессии, чем с применением конкретного препарата. Следует регулярно контролировать состояние пациентов для выявления кожных новообразований. Пациентам следует рекомендовать сведение к минимуму воздействие ультрафиолетового излучения, солнечного света и использование соответствующих солнцезащитных средств.
Применение препарата Сертикан® ассоциировалось с развитием ангионевротического отека. В подавляющем большинстве таких случаев пациенты одновременно получали ингибиторы АПФ в качестве сопутствующей терапии.
При применении препарата Сертикан® одновременно с ИКН у пациентов после трансплантации возможно развитие протеинурии. Риск развития протеинурии пропорционален концентрации эверолимуса в сыворотке крови. У реципиентов почки, уже имеющих умеренную протеинурию и получающих поддерживающую иммуносупрессию на основе ИКН, отмечалось увеличение протеинурии при полной замене ИКН на препарат Сертикан®. Это ухудшение носило обратимый характер при условии прекращения терапии препаратом Сертикан® и возвращения к терапии, основанной на ИКН. Безопасность и эффективность перехода с ИКН на Сертикан® у данного контингента пациентов не установлена. У пациентов, получающих препарат Сертикан®, должен проводиться мониторинг протеинурии.
Одновременное применение препарата Сертикан® и препаратов ИКН может повышать риск возникновения ИКН-индуцированного гемолитического уремического синдрома, тромбоцитопенической пурпуры, тромботической микроангиопатии.
На фоне применения препарата в течение первых 30 дней после трансплантации отмечено увеличение риска развития тромбоза почечной артерии или вены, приводящего к отторжению трансплантата.
Препарат Сертикан®, как и другие ингибиторы m-TOR, может ухудшать процесс заживления ран, приводить к возникновению пост-трансплантационных осложнений, требующих хирургического вмешательства: расхождение краев раны, скопление экссудата, инфицирование раны. К развитию лимфоцеле склонны реципиенты почки с избыточной массой тела. У пациентов после трансплантации сердца возможно развитие перикардиального и плеврального выпота. У пациентов после трансплантации печени повышена частота развития послеоперационных грыж.
На фоне применения препарата Сертикан® повышается риск возникновения впервые диагностированного сахарного диабета, поэтому необходим тщательный мониторинг концентрации глюкозы в сыворотке крови. Имеются сообщения о возникновении обратимой азооспермии и олигоспермии у пациентов, получающих лечение m-TOR ингибиторами. Доклинические токсикологические исследования показали, что эверолимус может снижать сперматогенез. Риск развития мужского бесплодия может являться потенциальным нежелательным явлением длительной терапии препаратом Сертикан®.
Пациенты, получающие иммуносупрессивные препараты, в том числе препарат Сертикан®, являются группой риска развития инфекций, в особенности вызываемых оппортунистическими патогенами (бактериями, грибами, вирусами, простейшими). Имеются сообщения о развитии фатальных инфекций и сепсиса при применении препарата. Из оппортунистических инфекций, встречающихся у пациентов, получающих иммуносупрессивную терапию, возможно развитие ВК вирус-ассоциированной нефропатии, приводящей к отторжению трансплантата почки, и потенциально фатальной JC вирус-ассоциированной прогрессирующей множественной лейкоэнцефалопатии (ПМЛ). Эти инфекции обусловлены общим комплексом иммуносупрессии и должны рассматриваться при дифференциальной диагностике в случае снижения функции пересаженной почки и при развитии неврологической симптоматики. В клинических исследованиях препарата проводили профилактику развития пневмонии, вызванной Pneumocystis jiroveci (carini) и цитомегаловирусной инфекции после трансплантации, особенно у пациентов с повышенным риском развития этой инфекции.
Существуют данные о развитии интерстициальной болезни лёгких (интрапаренхиматозного воспаления (пневмонита), а также фиброза неинфекционной этиологии, сопровождавшегося в некоторых случаях летальным исходом) среди пациентов, получающих лечение препаратами рапамицина и его производных, в т. ч. препаратом Сертикан®.
У пациентов с постоянно сохраняющейся клинической картиной пневмонии при неэффективности терапии антибиотиками и исключении инфекционных, неопластических и других, не связанных с применением лекарственных средств процессов, следует заподозрить интерстициальное поражение легких. Как правило, состояние разрешается самостоятельно после прекращения приема препарата Сертикан® и/или добавление к терапии глюкокортикостероидов.
Одновременное применение препарата Сертикан® с циклоспорином в форме микроэмульсии или такролимусом у пациентов после трансплантации может быть связано с повышением содержания в сыворотке холестерина и триглицеридов, что может потребовать соответствующего лечения. Пациентов, получающих препарат Сертикан®, следует наблюдать с целью выявления гиперлипидемии; при необходимости проводить лечение гиполипидемическими средствами и назначать соответствующую корригирующую диету. Необходимо оценить соотношение риск/польза для пациентов, у которых выявлена гиперлипидемия до начала терапии иммуносупрессивными средствами, включая препарат Сертикан®. Также следует оценить соотношение риск/польза продолжения терапии препаратом Сертикан® у пациентов с тяжелой рефрактерной гиперлипидемией.
Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития рабдомиолиза и других нежелательных явлений, вызванных вышеуказанными лекарственными средствами.
Влияние на способность управлять транспортными средствами и механизмами:
Исследования влияния препарата Сертикан® на способность к управлению транспортными средствами и работе с механизмами не проводились.
Форма выпуска/дозировка:
Таблетки 0,25 мг.
Таблетки 0,5 мг.
Таблетки 0,75 мг.
Таблетки 1,0 мг.
Упаковка:
Таблетки 0,25 мг: 10 таблеток в блистер ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров вместе с инструкцией по применению в картонной пачке.
Таблетки 0,5 мг: 10 таблеток в блистер ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров вместе с инструкцией по применению в картонной пачке.
Таблетки 0,75 мг: 10 таблеток в блистер ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров вместе с инструкцией по применению в картонной пачке.
Таблетки 1,0 мг: 10 таблеток в блистер ПА/Алюм./ПВХ. По 5, 6, 10 и 25 блистеров вместе с инструкцией по применению в картонной пачке.
Условия хранения:
В сухом защищенном от света месте при температуре не выше 25 °С.
Препарат следует хранить в недоступном для детей месте.
Срок годности:
3 года.
Не применять препарат после истечения срока годности, указанного на упаковке.
Условия отпуска
По рецепту
Производитель
Новартис Фарма Штейн АГ, Schaffhauserstrasse, 4332 Stein, Switzerland, Швейцария
Владелец регистрационного удостоверения/организация, принимающая претензии потребителей:
Новартис Фарма АГ
Купить Сертикан в planetazdorovo.ru
*Цена в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Сертикан® (Certican®)
💊 Состав препарата Сертикан®
✅ Применение препарата Сертикан®
Описание активных компонентов препарата
Сертикан®
(Certican®)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2023.04.14
Владелец регистрационного удостоверения:
Код ATX:
L04AA18
(Эверолимус)
Лекарственная форма
| Сертикан® |
Таб. 1 мг: 50, 60, 100 или 250 шт. рег. №: ЛС-002282 |
Форма выпуска, упаковка и состав
препарата Сертикан®
Таблетки от белого до желтоватого цвета, круглые, плоскоцилиндрические, со скошенными краями; допускается мраморность; на одной стороне нанесена гравировка «CU», на другой — «NVR».
Вспомогательные вещества: бутилгидрокситолуол — 100 мкг, лактозы моногидрат — 8.9 мг, гипромеллоза — 40 мг, магния стеарат — 1.25 мг, кросповидон — 50 мг, лактоза безводная — 148.75 мг.
10 шт. — блистеры (6) — пачки картонные.
10 шт. — блистеры (5) — пачки картонные.
10 шт. — блистеры (10) — пачки картонные.
10 шт. — блистеры (25) — пачки картонные.
Фармакологическое действие
Иммунодепрессант, ингибитор передачи пролиферативного сигнала. Эверолимус является избирательным ингибитором серин-треониновой киназы mTOR (мишень рапамицина млекопитающих), специфически воздействующим на комплекс mTORC1, сигнал-преобразующей mTOR-киназы и регуляторного raptor-протеина (regulatory associated protein of mTOR). Эверолимус проявляет свою активность за счет высоко аффинного взаимодействия с внутриклеточным рецепторным белком FKPB12. Комплекс FKPB12-эверолимус связывается с mTORC1, ингибируя его способность к передаче сигналов. mTOR является ключевой серин-треониновой киназой, играющей центральную роль в регуляции клеточного роста, пролиферации и выживаемости. Регуляция сигнального пути mTORC1 является сложным процессом, зависящим от митогенов, факторов роста, энергетической составляющей и питательных веществ.
Иммуносупрессивное действие обусловлено ингибированием антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими интерлейкинами Т-клеток, например, интерлейкином-2 и интерлейкином-15. Эверолимус ингибирует внутриклеточный сигнальный путь, который в норме приводит к клеточной пролиферации, запускаемой связыванием этих факторов роста Т-клеток с соответствующими рецепторами. Блокада этого сигнала эверолимусом приводит к остановке деления клеток на стадии G1 клеточного цикла.
Помимо влияния на Т-клетки, эверолимус ингибирует стимулируемую факторами роста пролиферацию как гемопоэтических, так и негемопоэтических клеток (например, гладкомышечных клеток). Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, которая запускается при повреждении эндотелиальных клеток и приводит к образованию неоинтимы, играет ключевую роль в патогенезе хронического отторжения.
Комплекс mTORC1 является важнейшим регулятором синтеза белка в дистальной части PI3K/АКТ-зависимого каскада, регуляция которого нарушена в большинстве злокачественных опухолей человека, а также при генетических заболеваниях, таких как туберозный склероз (ТС).
Эверолимус является активным ингибитором роста и пролиферации опухолевых клеток, эндотелиальных клеток, фибробластов и гладкомышечных клеток кровеносных сосудов.
Соответственно центральному регуляторному действию комплекса mTORC1, эверолимус уменьшает пролиферацию клеток, гликолиз и ангиогенез в солидных опухолях in vivo, таким образом, реализуя два независимых пути подавления роста опухоли: прямая противоопухолевая активность и ингибирование стромальной составляющей опухоли.
Фармакокинетика
После приема внутрь Cmax достигается через 1-2 ч. У пациентов после пересадки концентрация эверолимуса в крови пропорциональна дозе в диапазоне доз от 0.25 мг до 15 мг.
Соотношение концентрации эверолимуса в крови и его концентрации в плазме находится в пределах от 17% до 73% и зависит от значений концентрации в диапазоне от 5 до 5000 нг/мл. У здоровых добровольцев и пациентов с умеренными нарушениями функции печени связывание с белками плазмы составляет приблизительно 74%. Vd в конечной фазе у пациентов после трансплантации почки, находящихся на поддерживающей терапии, составляет 342±107 л.
Эверолимус является субстратом CYP3A4 и Р-гликопротеина. Основными путями метаболизма, выявленными у человека, были моногидроксилирование и O-деалкилирование. Два основных метаболита образуются путем гидролиза циклического лактона. Ни один из них не имеет существенной иммуносупрессивной активности. В системном кровотоке находится в основном эверолимус.
После введения однократной дозы меченого радиоактивной меткой эверолимуса пациентам после трансплантации, получающим циклоспорин, большая часть (80%) радиоактивности определялась в кале, небольшое количество (5%) выделялось с мочой. Неизмененное вещество не определялось ни в моче, ни в кале.
Показания активных веществ препарата
Сертикан®
Профилактика отторжения трансплантата почки и сердца у взрослых реципиентов с низким и средним иммунологическим риском, получающих базовую иммуносупрессивную терапию циклоспорином и ГКС. Профилактика отторжения трансплантата печени у реципиентов с низким и средним иммунологическим риском базовую иммуносупрессивную терапию такролимусом и ГКС.
Распространенный и/или метастатический почечно-клеточный рак при неэффективности антиангиогенной терапии.
Гормонозависимый распространенный рак молочной железы у пациенток в постменопаузе в комбинации с ингибитором ароматазы после предшествующей эндокринной терапии.
Субэпендимальные гигантоклеточные астроцитомы (СЭГА), ассоциированные с туберозным склерозом у пациентов в возрасте старше 3 лет при невозможности выполнения хирургической резекции опухоли.
Ангиомиолипома почки, ассоциированная с туберозным склерозом, не требующая немедленного хирургического вмешательства.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Принимают внутрь.
Дозу устанавливают индивидуально, в зависимости от показаний, применяемой схемы лечения, лекарственной формы и возраста пациента.
Побочное действие
Со стороны системы кроветворения и лимфатической системы: очень часто — лейкопения; часто — тромбоцитопения, анемия, коагулопатия, тромботическая тромбоцитопеническая пурпура/гемолитический уремический синдром; иногда — гемолиз.
Со стороны эндокринной системы: иногда — гипогонадизм у мужчин (снижение уровня тестостерона, повышение уровня ЛГ).
Со стороны обмена веществ: очень часто — гиперхолестеринемия, гиперлипидемия; часто — гипертриглицеридемия.
Со стороны сердечно-сосудистой системы: часто — повышение АД, лимфоцеле, венозный тромбоз.
Со стороны дыхательной системы: часто — пневмония; иногда — пневмонит.
Со стороны пищеварительной системы: часто — боли в животе, диарея, тошнота, рвота; иногда — гепатит, нарушения функции печени, желтуха, повышение АЛТ, ACT , ГГТ.
Со стороны кожи и подкожной клетчатки: часто — ангионевротический отек, акне, осложнения со стороны хирургической раны; иногда — сыпь.
Со стороны костно-мышечной системы: иногда — миалгия.
Со стороны мочевыделительной системы: часто — инфекции мочевых путей; иногда — некроз почечных канальцев, пиелонефрит.
Прочие: часто — отек, боль, вирусные, бактериальные и грибковые инфекции, сепсис; иногда — раневая инфекция.
Противопоказания к применению
Повышенная чувствительность к эверолимусу, другим производным рапамицина; дети и подростки до 18 лет, за исключением пациентов в возрасте до 3 лет с СЭГА; нарушение функции печени (класс А, В, С по классификации Чайлд- Пью) у пациентов от 3 до 18 лет с СЭГА; беременность, период грудного вскармливания; одновременное применение эверолимуса с мощными ингибиторами изофермента CYP3A4 и/или P-гликопротеина; одновременное применение эверолимуса с мощными индукторами изофермента CYP3A4 и/или индукторами P-гликопротеина.
С осторожностью
При одновременном применении эверолимуса с умеренными ингибиторами CYP3A4 или ингибиторами P-гликопротеина; у пациентов старше 18 лет с нарушением функции печени тяжелой степени (класс С по классификации Чайлд-Пью) в случае, когда польза от применении данного средства превышает возможный риск; у пациентов до и после хирургических вмешательств; у пациентов во время или вскоре после проведения лучевой терапии.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания. Женщинам детородного возраста следует рекомендовать использовать эффективные методы контрацепции в период лечения и в течение 8 недель после окончания терапии.
Применение при нарушениях функции печени
У пациентов с нарушениями функции печени умеренной степени (класс В по классификации Чайлд-Пью) дозу требуется коррекция дозы.
Применение при нарушениях функции почек
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Особые указания
В период лечения рекомендуется регулярный контроль функции почек. При повышении содержания сывороточного креатинина следует рассмотреть вопрос о коррекции режима иммуносупрессивной терапии, в частности об уменьшении дозы циклоспорина. Следует с осторожностью применять одновременно другие лекарственные средства, которые могут нарушать функцию почек.
Не рекомендуется одновременное применение с сильными ингибиторами CYP3A4 (например, кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами (например, рифампицин, рифабутин), за исключением случаев, когда ожидаемая польза такой терапии превышает потенциальный риск. Рекомендуется контролировать концентрации эверолимуса в цельной крови при одновременном применении с индукторами или ингибиторами CYP3A4 и после их отмены.
Эверолимус не изучен у пациентов с тяжелой печеночной недостаточностью. Рекомендуется тщательно мониторировать концентрацию эверолимуса в плазме крови у пациентов с нарушениями функции печени.
В период лечения следует контролировать состояние пациентов для выявления кожных новообразований. Следует регулярно контролировать состояние пациентов для выявления кожных новообразований, рекомендовать сведение к минимуму воздействие ультрафиолетового излучения, солнечного света и использовать соответствующие солнцезащитные средства.
С осторожностью применять у пациентов с гиперлипидемией. В период лечения следует контролировать содержание в крови холестерина и триглицеридов. Следует оценивать соотношение риск/польза продолжения терапии эверолимусом у пациентов с тяжелой рефрактерной гиперлипидемией. Пациентов, получающих ингибиторы ГМГ-КоА-редуктазы и/или фибраты, следует наблюдать на предмет развития нежелательных реакций, вызванных применением указанных лекарственных средств.
Чрезмерная иммуносупрессия предрасполагает к развитию инфекций (в т.ч. оппортунистических). Имеются сообщения о развитии фатальных инфекций и сепсиса.
В течение 3 мес после трансплантации рекомендуется профилактика развития цитомегаловирусной инфекции, особенно у пациентов с повышенным риском ее развития.
Пациентам, получающим ингибиторы ГМГ-КоА-редуктазы, требуется клинический контроль с целью своевременного выявления рабдомиолиза.
В период лечения эверолимусом не следует применять живые вакцины.
Лекарственное взаимодействие
На абсорбцию и последующую элиминацию эверолимуса могут оказывать влияние препараты, взаимодействующие с CYP3A4 и/или Р-гликопротеином. Сочетанное применение эверолимуса с сильными ингибиторами или индукторами CYP3A4 не рекомендуется. Ингибиторы Р-гликопротеина могут снизить высвобождение эверолимуса из кишечных клеток и повысить концентрацию эверолимуса в сыворотке. In vitro эверолимус являлся конкурентным ингибитором CYP3A4 и CYP2D6, потенциально увеличивающим концентрации в плазме препаратов, выводящихся при участии этих ферментов.
Биодоступность эверолимуса значительно увеличивалась при одновременном применении циклоспорина (ингибитор CYP3A4/Р-гликопротеина).
При изучении лекарственного взаимодействия у здоровых добровольцев, получавших предшествующую терапию многократными дозами рифампицина (индуктор CYP3A4), при последующем применении эверолимуса в однократной дозе наблюдалось почти 3-кратное повышение клиренса эверолимуса и уменьшение Сmax на 58% и AUC — на 63% (данная комбинация не рекомендуется).
Умеренные ингибиторы CYP3A4 и Р-гликопротеина могут повышать концентрацию эверолимуса в крови, в т.ч. противогрибковые средства: флуконазол; антибиотики группы макролидов (эритромицин); блокаторы кальциевых каналов (верапамил, никардипин, дилтиазем); ингибиторы протеазы (нелфинавир, индинавир, ампренавир).
Индукторы CYP3A4 могут повышать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови, в т.ч. зверобой продырявленный, противосудорожные средства (карбамазепин, фенобарбитал, фенитоин); препараты для лечения ВИЧ (эфавиренз, невирапин).
Грейпфрут и грейпфрутовый сок влияют на активность изоферментов CYP и Р-гликопротеина, поэтому следует избегать употребления этих соков на фоне применения эверолимуса.
Поскольку иммунодепрессанты могут оказывать влияние на ответ при вакцинации, на фоне лечения эверолимусом вакцинация может быть менее эффективной.
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Аналоги Сертикан
Товары из категории — Лекарства для иммунитета
Инструкция по применению
Цена в интернет-аптеке WER.RU: от 4 169
Фармакологические свойства
Сертикан считается иммунодепрессивным медикаментом. В структуру продукта входит замедлитель сигнала пролиферативного типа – эверолимус. Средство характеризуется иммуносопрессивными качествами, которые происходят за счет замедления процесса пролиферации в Т-клеточных структурах. Как показывают медицинские исследования, вещество воздействует не только на этот вид структур. Замечено, что фармвещество колоссально влияет на организации гемопоэтического и негемопоэтического вида.
Состав и упаковка выпуска
В инструкции по применению указываются точные объемы соединений, которые внедрены в изделие. Основным веществом, входящим в химпрепарат, считается эверолимус. Для усиления его результативности в состав медикамента вводят дополнительные элементы – гипромеллозу, кросповидон, магния стеарат и другие материалы.
Продается средство в теблетированной форме. Окрас продукта – белый.
Показания к применению Сертикана
Препарат предупреждает отторжение нового материала почечной и сердечной структуры у совершеннолетних лиц, которые подвержены потенциальному риску иммунологического характера. При этом больному целесообразно лечиться циклоспорином в виде микроэмульсии или глюкокортикостероидов.
Международная классификация болезней (МКБ-10)
T86.1 Отмирание и отторжение трансплантата почки;
T86.2 Отмирание и отторжение трансплантата сердца;
Z94.0 Наличие трансплантированной почки;
Z94.1 Наличие трансплантированного сердца.
Побочные эффекты
О побочных реакциях стало известно по результатам 3 исследований. У людей, принимавших Сертикан, проявлялись такие вторичные признаки: пневмония, желтуха, дисфункция печеночной организации; понос, тошнота, гепатит, гемолиз, анемия; накожные высыпания, миалгия, акне; пиелонефрит, отечность, болевой синдром в области живота; лейкопения, инфицирование вирусного; бактериального и грибкового типа. Также иногда регистрируется тромбоцитопения, сепсис, некоторые гормональные расстройства у мужчин, лимфома. Зарегистрированы случаи формирования опухолей злокачественного характера.
Как показывает практика, проявление вторичных показаний зависит от интенсивности и продолжительности терапевтического воздействия. Чтобы предупредить развитие осложнений, целесообразно проконсультироваться с доктором. Только грамотный врачебный персонал способен установить точный диагноз и назначить результативную терапию.
Противопоказания
Запреты, которые налагаются на прием таблеток Сертикан, касаются только повышенной сенсетивности к соединению эверолимуса и других вспомогательных химкомпонентов, которые входят в структуру изделия.
Применение при беременности
Как реагирует организм беременной женщины на вещество, входящее в Сертикан, неизвестно. Так как адекватные исследования в этой области не проводились. Есть сведения о том, что препарат способен оказывать токсическое воздействие на половую сферу. Поэтому врачи не рекомендуют выписывать средство пациентке, вынашивающей плод. Исключения возможны только в редких случаях.
Также нет никакой информации о выделении основного химкомпонента медикамента в материнское молоко. Эксперименты показали, что материал и его метаболические материалы очень быстро внедряются в структуру молока у лактирующих крыс. Сотрудники медицинских учреждений настоятельно не советуют назначать таблетки во время грудного вскармливания.
Способ и особенности применения
Сертикан предназначен для введения внутрь. В основном химпрепарат употребляют в количестве по 0,75 мг несколько раз в 24 часа (дозировка касается совершеннолетних пациентов, у которых в организме содержатся искусственные структуры почек и сердца). Особенностью использования средства считается то, что таблетки необходимо начать принимать как можно быстрее после проведения хирургического вмешательства по внедрению трансплантата. Пациент должен помнить о том, что продукт целесообразно вводить вместе с едой или без нее.
При проведении терапии врач должен систематически наблюдать за состоянием больного, и особенно за некоторыми показателями биосистем. Если в кровяной субстанции обнаружено достаточное количество медикамента Сертикан, то норму средства возможно скорректировать. Об изменение дозировки стоит говорить и при проявлении индивидуальных особенностей организма, на основании информации клинической картины. Корректировку разрешается производить каждые 4-5 суток.
Врач обязательно будет учитывать вид расы человека. Так, чернокожим людям требуется повышение нормы. Однако, других специфических советов таким пациентам эксперты еще дать не могут. Это связано с малоизученностью особенностей воздействия препарата на организм человека. По данным клинических показаний прием Сертикана больными, которым больше 65 лет, не желателен. Но никаких отклонений в фармококинетике вещества не было обнаружено.
При назначении лечения людям, у которых установлена дисфункция почечной структуры, коррекция объема препарата не требуется. Особое внимание рекомендуется уделить патологии печени. Как указывает инструкция по применению, при недостаточной работе органа необходимо контролировать базальное количество эверолимуса в цельной кровяной субстанции. Если речь идет о незначительной или умеренной недостаточности печеночной структуры, то норму средства целесообразно сократить в несколько раз. Как реагируют биосистемы на продукт при развитии недостаточности в тяжелой форме, неизвестно. Официальных медицинских сведений по этому вопросу нет.
При применении продукта объем вещества медикамента может понижаться, если человек будет принимать деспергируемые средства. При необходимости использования изделия Сертикан вместе с циклоспорином первый уменьшает свою концентрацию в кровяной плазме. Препарат не желательно принимать в сочетании с соединением циклоспорина длительный период. Состояние пациентов, которые перенесли пересадку искусственного материала почечной организации, чувствуют себя на много лучше, когда дозировка циклоспорина понижалась. Уменьшать норму последнего рекомендуется через 30 дней после проведения хирургического вмешательства.
Известны случаи, когда больной не переносил уменьшение количества циклоспорина. Тогда медицинский персонал вынужден был пересмотреть схему приема средства Сертикан, или даже отменить его. С внимательностью выписывают продукт человеку, который перенес пересадку сердца. В процессе поддерживающего периода при определении нормы циклоспорина при введении его вместе с эверолимусом следует учитывать ограничения, которые указаны в инструкции по применению.
Специалистами разработаны правила введения таблеток в организм. Их необходимо употреблять целыми, не разжевывать. Обязательно запивать 200 мл воды. Если больной не может самостоятельно проглотить пилюлю, ее разбивают на мелкие частицы и растворяют в воде. Также возможно использования специального приспособления – шприца для перорального применения. Раздробленные таблетки разрешается засыпать в чашечку из пластмассы. После туда заливают 25 мл воды. Из такого количества жидкости можно получить наибольшую дозировку препарата Сертикан – 1,5 мг. Важным моментом в создании раствора является одно правило – приготовленное лекарство оставляют на несколько минут для того, чтобы возникла дисперсия. Перед непосредственным введением средства таблетки следует взболтать. В некоторых случаях используют зонд назо-гастрального типа. Пилюли засыпают в специальный стакан, в котором находится 10 мл воды. Чтобы образовался необходимый раствор, нужно подождать 90 секунд, взбалтывая материал. После содержимое набирают в шприц и с небольшой скоростью вводят через зонд. Рекомендуют ополаскивать емкость три раза, набирая туда по 5 мл воды, остатки Сертикана вводить в зонд. Не разрешается смешивать вещество вместе с циклоспорином.
Сведений о назначении продукта в детском возрасте очень мало. Поэтому выписывать таблетки настоятельно не рекомендуется.
Взаимодействие с другими лекарствами
Метаболические процессы, происходящие после введения средства Сертикан, в основном наблюдаются в печени и кишечном отделе. Поэтому перед употреблением медикамента следует тщательно обследоваться. Запрещено использовать препарат вместе с другими фармакологическими изделиями. Активное участие в расщеплении вещества принимает изофермент CYP3A4. Таким образом, на абсорбцию материала могут влиять химкомпоненты, которые связаны с CYP3A4 и/или Р-гликопротеином. Не желательно вводить таблетки вместе с сильными замедлителями или индукторами CYP3A4.
Доктор должен учитывать особенности взаимодействия препаратов, в том числе, циклоспорина и эверолимуса. Исследовалась биодоступность последнего. Она значительно повышалась, если вышеуказанные химические компоненты принимались вместе. Таким образом, иногда требуется изменение количества лекарств с целью их эффективного воздействия на организм. Как утверждают специалисты, Сертикан практически не влияет на фаромакокинетику вещества циклоспорина у больных с искусственными органами почек и сердца, которые употребляют последний как эмульсию. Известно, что медикамент в комбинации с соединением аторвастатина и правастатина не воздействовал на фармакокинетические качества изделий. Перед использованием продукта врач должен обратить внимание не только на научные исследования, полученные в ходе экспериментов при участие здоровых добровольцев и пациентов, но и индивидуальные особенности человека. Это поможет определиться с дозировкой средства. Применению любых медицинских изделий должно предшествовать тщательное обследование.
Таблетки не рекомендуют принимать вместе с таким фруктом, как грейпфрут (в том числе, и сок из него). Вещества растения способны воздействовать на активизацию некоторых составных материала. При введении вакцинации и использовании лекарства возможно понижение эффективности первой. Поэтому перед введением вакцин необходимо посоветоваться с доктором. В период терапии, согласно инструкции, вводить в организм живые вакцины не желательно.
Передозировка
Исследования показали, что продукт эверолимуса практически не токсичен в больших дозировках. Ученые проводили эксперименты на крысах. При получении средства в количестве 2000 мг/кг за один раз они не погибали. Также в это время у животных не проявлялись тяжелые отравления. Сведения о принятии сверхдоз медикамента Сертикан человеком минимальные. Известен случай случайного употребления таблетки (1,5 мг) 2-летним ребенком. Негативные реакции не наблюдались. Лекарство вводилось внутрь взрослыми, которые перенесли пересадку органов, в объеме до 25 мг. Результат был положительным – пациенты приемлемо перенесли химический продукт в таком количестве. Если после принятия овердозы у больного возникают симптомы отравления, необходимо срочно обратиться в больницу.
Аналоги
Существует средство, которое по своим характеристикам относится к альтернативным продуктам таблеток, — Афинитор. Однако, выписывать лекарство вправе только специалист.
Условия продажи
Препарат продается в аптеке по рецепту.
Условия хранения
В инструкции оговариваются правила содержания таблеток. Средство необходимо сберегать подальше от солнечного света, в месте, где нет доступа несовершеннолетним лицам. Температурный режим — 30°С. Показатели влажности в помещении должны быть нормальными. Срок годности – не больше 3 лет с момента выпуска. При обнаружении на упаковке повреждений или дефектов таблетки следует немедленно утилизировать.
Цены на Сертикан в Москве
Заберите заказ в в аптеке
WER (г. Москва)
Цена: от 4 169 руб.
Сертификаты и лицензии
Данные по применению Сертикана без ингибиторов кальциневрина (ИКН) (циклоспорина или такролимуса) ограничены. У пациентов, прекративших прием ИКН, отмечался повышенный риск острого отторжения по сравнению с пациентами, продолжавшими прием ИКН.
В клинических испытаниях Сертикан применялся одновременно с микроэмульсией циклоспорина или такролимусом, базиликсимабом и кортикостероидами. Адекватных исследований применения Сертикана в комбинации с другими иммуносупрессантами, кроме указанных, не проводилось. Следует соблюдать осторожность при одновременном применении тимоглобулиновой индукции (кроличий антитимоцитарный глобулин) и Сертикана/циклоспорина/стероидных препаратов. В клинических испытаниях у пациентов, перенесших трансплантацию сердца, в течение трех месяцев после трансплантации повышалась частота возникновения серьезных инфекций в подгруппе пациентов, которые получали индукцию кроличьим антитимоцитарным глобулином одновременно с приемом Сертикана, стероидов и циклоспорина в концентрациях, рекомендованных при пересадке сердца (выше, чем при пересадке почки). Это было связано с более высокой смертностью среди пациентов, которые были госпитализированы и, которым требовался желудочковый аппарат вспомогательного кровообращения перед трансплантацией, поскольку они могли быть особенно уязвимы к увеличению иммуносупрессии.
Рекомендуется тщательный мониторинг уровней эверолимуса в цельной крови (С0) и корректировка дозы эверолимуса у пациентов с нарушением функции печени.
Совместное применение Сертикана с сильными ингибиторами CYP3A4 (например, с такими как кетоконазол, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир) и индукторами CYP3A4 (например, с рифампицином, рифабутином) не рекомендуется, если польза не превышает риск. Мониторинг минимальных концентраций эверолимуса в цельной крови (С0) рекомендуется во время одновременного применения индукторов или ингибиторов CYP3A4, а также после отмены их приема.
У пациентов, применяющих иммуносупрессанты, включая Сертикан, может быть повышен риск развития лимфом или других злокачественных новообразований, особенно кожи. Предполагается, что абсолютный риск скорее связан с продолжительностью и интенсивностью иммуносупрессии, чем с применением определенного лекарственного средства. Пациентам необходимо регулярно обследоваться на наличие новообразований кожи; рекомендуется ограничивать воздействие солнечного света и ультрафиолетового излучения; следует использовать соответствующие солнцезащитные средства.
Чрезмерное подавление функции иммунной системы повергает пациентов к развитию инфекций, особенно вызываемых условно-патогенными микроорганизмами. Сообщалось также о летальных инфекциях и сепсисе. К оппортунистическим инфекциям, по отношению к которым могут быть уязвимы пациенты на иммуносупрессивной терапии, относятся: полиомавирусные инфекции, включая нефропатию, вызванную ВК вирусом, которая может приводить к потере почечного трансплантата, и потенциально фатальная прогрессивная мультифокальная лейкоэнцефалопатия, вызываемая JC вирусом. Данные инфекции, часто связанные с общей иммуносупрессивной нагрузкой, должны приниматься во внимание при дифференциальной диагностике иммуносупрессивных пациентов с ослабленной функцией почечного трансплантата или неврологическими симптомами.
В клинических испытаниях Сертикана была рекомендована противомикробная профилактика пневмонии, вызванной Pneumocystis jiroveci (carinii), и профилактика цитомегаловирусной инфекции (ЦМВ) после трансплантации, особенно у пациентов с повышенным риском развития оппортунистических инфекций.
Совместное применение Сертикана и микроэмульсии циклоспорина у пациентов, перенесших трансплантацию, было связано с увеличением уровня холестерина и триглицеридов в сыворотке крови, что может потребовать соответствующего лечения. У пациентов, которым назначен Сертикан, нужно контролировать уровень липидов и в случае необходимости провести терапию, включающую препараты, которые снижают уровень липидов, и назначить соответствующую диету. В отношении пациентов с имеющейся гиперлипидемией, перед началом иммуносупрессивной терапии, включая Сертикан, следует взвесить потенциальную пользу от лечения препаратом и возможный риск. Также необходимо еще раз взвесить пользу и риск продолжения терапии Сертиканом у больных с тяжелой устойчивой гиперлипидемией.
У пациентов, применяющих Сертикан в сочетании с ингибитором ГМК-КоА-редуктазы и/или фибратами, следует контролировать возможное развитие побочных эффектов, как описано в соответствующей информации о назначении этих лекарственных средств.
Применение препарата с высокими дозами циклоспорина повышает риск возникновения нарушений функции почек, поэтому необходимо снижение дозы циклоспорина в комбинации с Сертиканом для профилактики нарушений функции почек. Следует иметь в виду, что у пациентов с повышенным уровнем креатинина в сыворотке крови потребуется соответствующая модификация режима иммуносупрессии.
У пациентов после трансплантации печени применение Сертикана со снижением дозы такролимуса не приводило к ухудшению функции почек по сравнению со стандартной дозировкой такролимуса.
Регулярный мониторинг функции почек рекомендуется всем пациентам. Необходимо соблюдать осторожность при одновременном назначении с другими препаратами, оказывающими повреждающее действие на функцию почек.
Применение Сертикана с ингибиторами кальциневрина у пациентов после трансплантации может сопровождаться усилением протеинурии. Риск увеличивается при повышении концентрации эверолимуса в крови.
У пациентов с почечным трансплантатом при слабо выраженной протеинурии при проведении поддерживающей терапии иммунодепрессантами, включая ингибитор кальциневрина (ИКН), были сообщения об увеличении уровня протеинурии, когда вместо ИКН назначали Сертикан. При прекращении применения Сертикана и возвращении к применению ИКН отмечалась обратная реакция. Безопасность и эффективность перехода от ИКН на Сертикан у таких пациентов не была установлена. У пациентов, которые получают Сертикан, необходимо контролировать уровень протеинурии.
Имели место сообщения об увеличении риска возникновения тромбоза артерий и вен почки, что приводило к отторжению трансплантата. Это явление чаще наблюдалось в течение первых 30 дней после трансплантации.
Сертикан может ослаблять процесс заживления ран и приводить к таким осложнениям после трансплантации, как расхождение краев раны, накопление жидкости, раневая инфекция, при которых может понадобиться дополнительное хирургическое вмешательство. Лимфоцеле является наиболее часто встречаемым побочным эффектом у пациентов, перенесших трансплантацию почек, и более часто встречается у пациентов с более высоким индексом массы тела. Частота перикардиального и плеврального выпота увеличивается у пациентов, перенесших трансплантацию сердца, и частота возникновения инцизионной грыжи больше у пациентов, перенесших трансплантацию печени.
При применении Сертикана наблюдалось увеличение риска возникновения сахарного диабета после трансплантации. Поэтому следует контролировать концентрацию глюкозы в крови пациентов, принимающих препарат.
В литературе имеются сообщения об обратимой азооспермии и олигоспермии у пациентов, получавших лечение ингибиторами mTOR. Поскольку в доклинических токсикологических исследованиях продемонстрировано, что эверолимус может снижать сперматогенез, мужское бесплодие следует рассматривать как потенциальный риск при длительной терапии Сертиканом.
При одновременном применении Сертикана и ингибитора кальциневрина (ИКН) может повышаться риск возникновения ИКН-индуцированного гемолитико-уремического синдрома, тромботической тромбоцитопенической пурпуры и тромботической микроангиопатии.
Пациентам с редкими наследственными формами непереносимости галактозы, дефицитом лактазы или с синдромом глюкозо-галактозной мальабсорбции не следует применять этот препарат.
Совместное применение Сертикана и ингибиторов АПФ часто приводило к возникновению ангиоэдемы.
У пациентов, получавших рапамицины и их производные, включая Сертикан, наблюдались случаи интерстициальной болезни легких (ИБЛ), включая интрапаренхимальное воспаление легких (пневмонит) и/или фиброз неинфекционной этиологии, иногда фатальные. Диагноз ИБЛ необходимо дифференцировать у пациентов с симптомами инфекционной пневмонии, не поддающейся лечению антибиотиками, когда инфекционные, неопластические и другие немедикаментозные причины были исключены при соответствующем обследовании. Обычно состояние разрешается после отмены Сертикана и/или назначения глюкокортикоидов. Однако наблюдались также летальные исходы.
Способность влиять на скорость реакции при управлении автотранспортом или другими механизмами
Исследование влияния препарата на способность управлять автотранспортом и работать с механизмами не проводились.
Взаимодействие с другими лекарственными средствами и другие виды взаимодействий
Эверолимус метаболизируется, главным образом, в печени и, в некоторой степени, в стенке кишечника при участии СYР3А4-изофермента. Он также является субстратом для системы выведения многих лекарственных препаратов, Р-гликопротеина (PgP). Поэтому лекарственные препараты, влияющие на CYP3A4 и/или PgP, могут влиять на всасывание эверолимуса и его последующее выведение.
Установленные взаимодействия, из-за которых одновременное применение не рекомендуется
Рифампицин (индуктор CYP3A4). У здоровых добровольцев, получавших предварительно многократные дозы рифампицина, при последующем применении однократной дозы Сертикана наблюдалось увеличение клиренса эверолимуса почти в 3 раза, снижение Сmах на 58% и AUC на 63%. Комбинация с рифампицином не рекомендуется (см. раздел Меры предосторожности).
Кетоконазол (ингибитор CYP3A4). У здоровых добровольцев, получавших предварительно многократные дозы кетоконазола, при последующем применении однократной дозы Сертикана Сmах и AUC эверолимуса увеличивались в 3,9 и 15,0 раз, соответственно (см. раздел Меры предосторожности).
Предполагаемые взаимодействия, из-за которых одновременное применение не рекомендуется
Сильные ингибиторы и индукторы CYP3A4. Не рекомендуется сопутствующая терапия сильными ингибиторами и/или индукторами CYP3A4 (например, итраконазол, вориконазол, кларитромицин, телитромицин, ритонавир и/или рифампицин, рифабутин) (см. раздел Меры предосторожности).
Установленные взаимодействия, которые следует учитывать
Взаимодействия, влияющие на применение Сертикана
Циклоспорин (ингибитор CYP3A4/PgP). Биодоступность эверолимуса существенно повышалась при одновременном применении с циклоспорином. В исследовании однократной дозы препарата у здоровых добровольцев циклоспорин в форме микроэмульсии увеличивал AUC эверолимуса на 168% (диапазон 46-365%) и Сmах на 82% (диапазон 25-158%) по сравнению с таковыми при применении только эверолимуса. В случае изменения дозы циклоспорина может потребоваться коррекция дозы эверолимуса (см. раздел Способ применения и дозы).
Эритромицин (ингибитор CYP3A4). У здоровых добровольцев, получавших предварительно многократные дозы эритромицина, при последующем применении однократной дозы Сертикана Сmах и AUC эверолимуса увеличивались в 2,0 и 4,4 раза, соответственно.
Верапамил (ингибитор CYP3A4). У здоровых добровольцев, получавших предварительно многократные дозы верапамила, при последующем применении однократной дозы Сертикана Сmах и AUC эверолимуса увеличивались в 2,3 и 3,5 раза, соответственно.
Взаимодействия, влияющие на другие препараты
Циклоспорин (ингибитор CYP3A4/PgP). У пациентов после трансплантации почки или сердца, получавших циклоспорин в форме микроэмульсии, клиническая значимость влияния Сертикана на фармакокинетику циклоспорина была минимальной.
Октреотид. Сопутствующее применение эверолимуса с депо-октреотидом вызывало повышение Cmin октреотида со средним геометрическим соотношением (эверолимус/плацебо) в 1,47 раз.
Аторвастатин (субстрат CYP3A4) и правастатин (субстрат PgP). Однократное применение Сертикана у здоровых добровольцев одновременно с аторвастатином или правастатином не оказывало клинически значимого влияния на фармакокинетику аторвастатина, правастатина и эверолимуса, а также на общую биореактивность ГМГ-КоА-редуктазы в плазме крови. Однако эти результаты не могут экстраполироваться на другие ингибиторы ГМГ-КоА-редуктазы.
Пациентов необходимо контролировать на возможное развитие рабдомиолиза и других нежелательных явлений, как описано в соответствующих инструкциях по медицинскому применению ингибиторов ГМГ-КоА-редуктазы.
Мидазолам (субстрат CYP3A4A). В клиническом исследовании по изучению взаимодействия препаратов 25 здоровых добровольцев получали на первом этапе однократную дозу 4 мг мидозалама. На втором этапе они получали 10 мг эверолимуса один раз в день в течение 5 дней и однократно 4 мг мидозалама с последней дозой эверолимуса. Смакс мидозалама увеличилась в 1,25 раз (90% ДИ, 1,14-1,37) и AUCinf увеличилась в 1,30 раз (1,22-1,39). Период полувыведения мидозалама не изменился. Данное исследование показало, что эверолимус является слабым ингибитором CYP3A4.
Предполагаемые взаимодействия, которые следует учитывать
Взаимодействия, влияющие на применение Сертикана
Умеренные индукторы CYP3A4. Индукторы CYP3A4 могут усиливать метаболизм эверолимуса и уменьшать концентрации эверолимуса в крови (например, зверобой (Hypericum perforatum), противосудорожные средства (например, карбамазепин), фенобарбитал, фенитоин, анти-ВИЧ препараты (эфавиренц, невирапин)).
Умеренные ингибиторы CYP3A4. Умеренные ингибиторы CYP3A4 и PgP могут повышать уровни эверолимуса в крови (например, противогрибковые средства: флуконазол; блокаторы кальциевых каналов: никардипин, дилтиазем; ингибиторы протеазы: нелфинавир, индинавир, ампренавир).
Ингибиторы PgP. Ингибиторы PgP могут снижать выведение эверолимуса из клеток кишечника и повышать концентрацию эверолимуса в крови.
Ингибиторы АПФ. Одновременное применение Сертикана и ингибиторов АПФ может привести к развитию отека Квинке.
Вакцинация
Иммуносупрессанты могут влиять на ответ при вакцинации, поэтому вакцинация во время лечения Сертиканом может оказаться менее эффективной. Следует избегать применения живых вакцин.
Лекарственные взаимодействия с продуктами питания/напитками
Грейпфрут и грейпфрутовый сок снижают активность цитохрома Р450 и PgP, поэтому его употребления следует избегать.
Фармакологические свойства
Фармакодинамика
Эверолимус, ингибитор активации Т-клеток, предотвращает отторжение аллогенного трансплантата на моделях аллотрансплантации у грызунов и обезьян-приматов. Он оказывает иммуносупрессивное действие путем ингибирования антиген-активированной пролиферации Т-клеток и, соответственно, клональной экспансии, вызываемой специфическими интерлейкинами Т-клеток, например, интерлейкином-2 и интерлейкином-15. Эверолимус ингибирует внутриклеточную передачу сигнала, что обычно приводит к пролиферации клеток, запускаемой связыванием этих факторов роста Т-клеток с их рецепторами. Блокада этого сигнала эверолимусом вызывает угнетение деления клеток на стадии G1-клеточного цикла.
На молекулярном уровне эверолимус образует комплекс с цитоплазматическим белком FKBP-12. В присутствии эверолимуса подавляется фосфорилирование р70 S6-киназы, стимулируемое фактором роста. Поскольку фосфорилирование р70 S6-киназы находится под контролем FRAP (так называемого mTOR), эти данные предполагают, что комплекс эверолимус-РКВР-12 связывается с FRAP и, таким образом, подавляет функцию последнего. FRAP — основной регуляторный белок, управляющий метаболизмом клеток, ростом и пролиферацией; таким образом, нарушение функции FRAP приводит к угнетению клеточного цикла, вызванного эверолимусом.
Таким образом, эверолимус отличается от циклоспорина по механизму действия. На доклинических моделях аллотрансплантации комбинация эверолимуса и циклоспорина была более эффективной, чем каждого соединения в отдельности.
Действие эверолимуса не ограничивается Т-клетками. В целом, эверолимус подавляет стимулируемую фактором роста пролиферацию кроветворных клеток и некроветворных клеток, таких как гладкомышечные клетки сосудов. Стимулируемая фактором роста пролиферация гладкомышечных клеток сосудов, вызываемая повреждением эндотелиальных клеток и приводящая к образованию неоинтимы, играет главную роль в патогенезе хронического отторжения. Доклинические исследования эверолимуса продемонстрировали подавление образования неоинтимы на модели аллотрансплантата аорты крысы.
Фармакокинетика
Всасывание. Пиковые концентрации эверолимуса достигались через 1 -2 часа после приема внутрь. Концентрации эверолимуса в крови пациентов после трансплантации дозопропорциональны в диапазоне доз 0,25 мг-15 мг. На основании показателя AUC относительная биодоступность диспергируемой таблетки по сравнению с обычной таблеткой составляет 0,90 (90%, CI 0,76-1,07).
Влияние пиши. Сmах и AUC эверолимуса снижались на 60% и 16%, соответственно, при приеме препарата с очень жирной пищей. Чтобы минимизировать вариабельность, Сертикан следует принимать или только во время еды, или только между приемами пищи.
Распределение. Соотношение концентраций эверолимуса в крови и в плазме составляет от 17% до 73% и зависит от концентрации в диапазоне 5 нг/мл до 5000 нг/мл. Связывание с белками плазмы крови составляет приблизительно 74% у здоровых добровольцев и у пациентов с умеренной печеночной недостаточностью. Объем распределения в конечной фазе (Vz/F) у пациентов, перенесших трансплантацию почки и находящихся на поддерживающей терапии, составляет 342 ± 107 л.
Метаболизм.
Эверолимус является субстратом для CYP3A4 и Р-гликопротеина. После приема внутрь эверолимус является основным компонентом, циркулирующим в крови у человека. Шесть основных метаболитов эверолимуса обнаружены в крови у человека, в том числе три моногидроксилированных метаболита, два метаболита с гидролитически открытыми кольцами и конъюгат эверолимуса с фосфатидилхолином. Эти метаболиты также определялись у животных в исследованиях токсичности, они показали примерно в 100 раз меньшую активность, чем сам эверолимус. Таким образом, исходное вещество считается ответственным за большую часть общей фармакологической активности эверолимуса. Выведение. После однократной дозы меченого радиоизотопом эверолимуса у пациентов после трансплантации, получавших циклоспорин, основная часть радиоактивности (80%) была обнаружена в кале, и лишь незначительная часть (5%) выводилась с мочой. Неизмененное лекарственное средство не было обнаружено ни в моче, ни в кале.
Фармакокинетика в равновесном состоянии. Фармакокинетические параметры были сравнимы у пациентов, перенесших трансплантацию почки, и у пациентов, перенесших трансплантацию сердца, получавших эверолимус 2 раза в день и циклоспорин в виде микроэмульсии. Равновесное состояние было достигнуто на 4-й день, с кумуляцией в крови в концентрациях, которые в 2-3 раза превышали концентрации в крови после первой дозы. Значение Тmах достигалось через 1-2 часа после применения дозы. При приеме дозы 0,75 мг и 1,5 мг 2 раза в день Сmах составлял в среднем 11,1 ± 4,6 нг/мл и 20,3 ± 8,0 нг/мл, соответственно, a AUC составлял в среднем 75 ± 31 нг час/мл и 131 ± 59 нг час/мл, соответственно. При дозе 0,75 мг и 1,5 мг 2 раза в день минимальные уровни в крови (Cmin) составляли в среднем 4,1 ± 2,1 нг/мл и 7,1 ± 4,6 нг/мл, соответственно (утром до применения очередной дозы). Действие эверолимуса оставалось стабильным в течение 1-го года после трансплантации. Значение Cmin существенно коррелировало с AUC, создавая коэффициент корреляции между 0,86 и 0,94. Исходя из анализа фармакокинетических параметров популяции после перорального применения, клиренс (CL/F) составлял — 8,8 л/ч (разброс между пациентами — 27%), а центральный объем распределения (Vc/F) составлял 110 л (разброс между пациентами — 36%). Остаточная вариабельность в концентрациях препарата в крови составляла 31%. Период полувыведения — 28 ± 7 часов.
Нарушение функции печени. Среднее значение AUC эверолимуса у 7 пациентов с нарушением функции печени легкой степени тяжести (класс А по классификации Чайлд-Пью) было в 1,6 раз выше, чем у пациентов без нарушения функции печени. В двух независимых группах из 8 пациентов с нарушением функции печени умеренной степени тяжести (класс В по классификации Чайлд-Пью) среднее значение AUC эверолимуса было в 2,1 и 3,3 раза выше. У 6 пациентов с тяжелыми нарушениями функции печени (класс С по классификации Чайлд-Пью) среднее значение AUC эверолимуса было в 3,6 раза выше. Средний период полувыведения при легкой, умеренной и тяжелой степени нарушения функции печени составлял, соответственно, 52, 59 и 78 ч. Удлиненный период полувыведения замедляет достижение равновесного состояния уровня эверолимуса в крови (см. раздел «Способ применения и дозы»).
Нарушение функции почек. Нарушение функции почек у пациентов после трансплантации (диапазон клиренса креатинина 11-107 мл/мин) не влияло на фармакокинетические параметры эверолимуса.
Применение в педиатрии. Клиренс эверолимуса линейно повышался в зависимости от возраста пациента (от 1 до 16 лет), площади поверхности тела (0,49-1,92 м2) и массы тела (11-77 кг). В равновесном состоянии клиренс составлял 10,2 ± 3,0 л/час/м2, а период полувыведения — 30 ± 11 часов. 19 пациентов детского возраста (от 1 до 16 лет) с почечным трансплантатом de novo применяли диспергируемые таблетки Сертикана в дозе 0,8 мг/м2 (максимум 1,5 мг) 2 раза в день, одновременно с циклоспорином в виде микроэмульсии. У этой категории пациентов значение AUC эверолимуса составляло 87 ± 27 нг час/мл и было таким же у взрослых, которые применяли 0,75 мг препарата 2 раза в день. В равновесном состоянии минимальная концентрация (С0) составляла 4,4 ± 1,7 нг/мл.
Пожилые пациенты. Предельное снижение CL перорально применяемого эверолимуса до 0,33% на один год было оценено у взрослых (исследуемый возрастной диапазон составлял 16-70 лет). Коррекция дозы не требуется.
Этническая принадлежность. Согласно анализу фармакокинетических параметров популяции, клиренс препарата после перорального применения (CL/F) был, в среднем, на 20% выше у чернокожих пациентов, перенесших трансплантацию.
Зависимость ответа на препарат от экспозиции. В течение первых 6 месяцев после трансплантации почки и сердца наблюдается связь между средней минимальной концентрацией эверолимуса (С0) и частотой случаев подтвержденного биопсией острого отторжения и тромбоцитопении. У пациентов после трансплантации печени взаимосвязь между минимальной концентрацией эверолимуса и клиническими явлениями менее очевидна, однако более высокая экспозиция не коррелирует с увеличением частоты побочных явлений (см. Таблицу 1).
Таблица 1
| Трансплантация почки | |||||
| Мин. уровень (С0) (нг/мл) | ≤ 3,4 | 3,5-4,5 | 4,6-5,7 | 5,8-7,7 | 7,8-15,0 |
| Отсутствие отторжения | 68% | 81 % | 86% | 81 % | 91 % |
| Тромбоцитопения(< 100 × 109/л) | 10% | 9% | 7% | 14% | 17% |
| Трансплантация сердца | |||||
| Мин. уровень (С0) (нг/мл) | ≤ 3,5 | 3,6-5,3 | 5,4-7,3 | 7,4-10,2 | 10,3-21,8 |
| Отсутствие отторжения | 65 % | 69% | 80% | 85 % | 85 % |
| Тромбоцитопения (< 75 × 109/л) | 5% | 5% | 6% | 8% | 9% |
| Трансплантация печени | |||||
| Мин. уровень (С0) (нг/мл) | ≤ 3 | 3-8 | ≥ 8 | ||
| Отсутствие терапии BPAR | 88% | 98% | 92% | ||
| Тромбоцитопения (< 75 × 109/л) | 35% | 13% | 18% | ||
| Нейтропения (< 1.75 × 109/л) | 70% | 31% | 44% |
Фармацевтические характеристики
Основные физико-химические свойства
Таблетки от белого до желтоватого цвета с вкраплениями, круглые, плоские, со скошенными краями; гравировка «JO» с одной стороны и «NVR» — с другой.